文档内容
班级 姓名 学号 分数
第三章 水溶液中的离子反应与平衡(B 卷·能力提升练)
(时间:90分钟,满分:100分)
一、选择题(本题共16小题,每小题3分,共48分。)
1.在相同温度下,100mL 0.1mol·L-1的醋酸与10mL 1mol·L-1的醋酸相比较,下列说法正确的是
A.溶液中H+的物质的量前者大于后者
B.前者的电离程度小于后者
C.发生中和反应时所需NaOH的量前者大于后者
D.溶液中CHCOOH的物质的量前者大于后者
3
2.室温下,往0.1 mol·L-1的氨水中滴入酚酞溶液时,溶液将呈现粉红色。现采取下列措施,滴有酚酞的氨
水溶液颜色不会变浅的是
A.往溶液中滴入稀硫酸 B.往溶液中加入NH Cl晶体
4
C.把溶液加热至沸腾 D.往溶液中加入NaOH固体
3.下列应用与盐类水解无主要关系的是( )
A.用铝盐和铁盐作净水剂
SOCl AlCl 6H O AlCl
B.将 2(遇水剧烈水解)和 3 2 混合加热制取无水 3
FeSO FeSO 7H O
C. 4溶液制备 4 2 晶体时,不能直接蒸干结晶获取
D.草木灰与铵态氮肥不能混合施用
4.下表是几种弱酸在常温下的电离平街常数:
CHCOOH HCO HS HPO
3 2 3 2 3 4
K =7.5×10-3
a1
K =4.3×10-7 K =9.1×10-8
a1 a1
1.8×10-5 K =6.2×10-8
a2
K =5.6×10-11 K =1.1×10-12
a2 a2
K =2.2×10-13
a3
则下列说法中不正确的是
A.碳酸的酸性强于氢硫酸
B.多元弱酸的酸性主要由第一步电离决定
c
H
C.常温下,加水稀释醋酸, 增大
cCH COOH
3
D.向弱酸溶液中加少量NaOH溶液,电离平衡常数不变
1 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
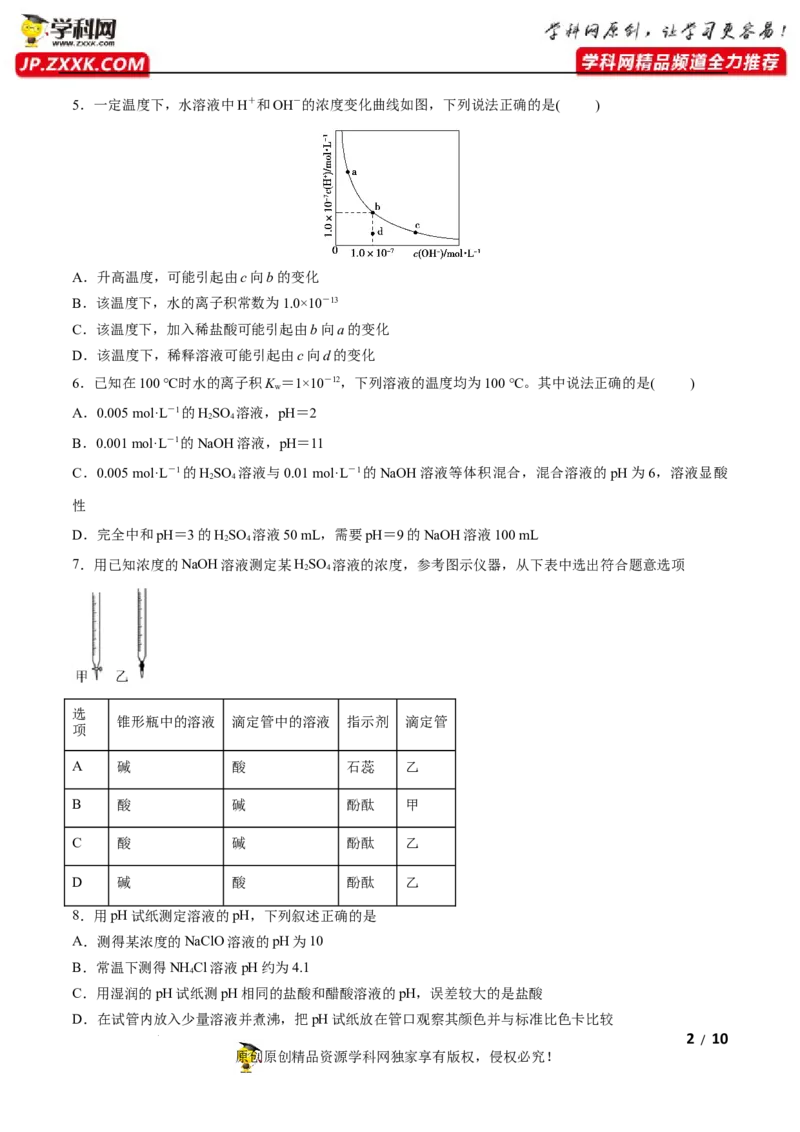
学科网(北京)股份有限公司5.一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入稀盐酸可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
6.已知在100 ℃时水的离子积K =1×10-12,下列溶液的温度均为100 ℃。其中说法正确的是( )
w
A.0.005 mol·L-1的HSO 溶液,pH=2
2 4
B.0.001 mol·L-1的NaOH溶液,pH=11
C.0.005 mol·L-1的HSO 溶液与0.01 mol·L-1的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸
2 4
性
D.完全中和pH=3的HSO 溶液50 mL,需要pH=9的NaOH溶液100 mL
2 4
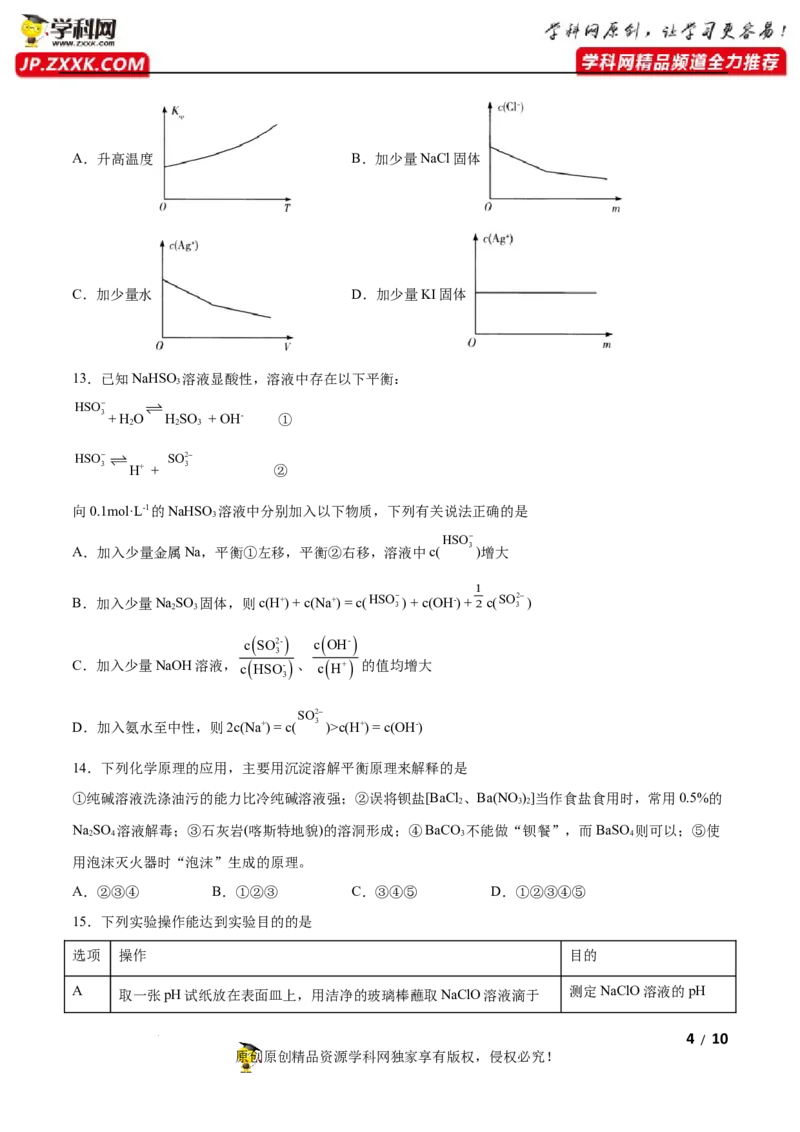
7.用已知浓度的NaOH溶液测定某HSO 溶液的浓度,参考图示仪器,从下表中选出符合题意选项
2 4
选
锥形瓶中的溶液 滴定管中的溶液 指示剂 滴定管
项
A 碱 酸 石蕊 乙
B 酸 碱 酚酞 甲
C 酸 碱 酚酞 乙
D 碱 酸 酚酞 乙
8.用pH试纸测定溶液的pH,下列叙述正确的是
A.测得某浓度的NaClO溶液的pH为10
B.常温下测得NH Cl溶液pH约为4.1
4
C.用湿润的pH试纸测pH相同的盐酸和醋酸溶液的pH,误差较大的是盐酸
D.在试管内放入少量溶液并煮沸,把pH试纸放在管口观察其颜色并与标准比色卡比较
2 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司9.根据下表信息,判断0.10 mol/L的下列各溶液pH最大的是( )
酸 电离常数(常温下)
CHCOOH K=1.8×10-5
3 a
HCO K =4.3×10-7,K =5.6×10-11
2 3 a1 a2
HS K =9.1×10-8,K =1.1×10-12
2 a1 a2
A.CHCOONa B.NaCO C.NaHCO D.NaS
3 2 3 3 2
FeCl
10.下列关于 3水解的说法错误的是
FeCl
A.在稀溶液中,水解达到平衡时,无论加 3饱和溶液还是加水稀释,平衡均向右移动
5 mol/L 0.5 mol/L FeCl Fe3+
B.浓度为 和 的两种 3溶液,其他条件相同时, 的水解程度前者小于后者
FeCl Fe3+
C.其他条件相同时,同浓度的 3溶液在50 ℃和20 ℃时发生水解,50 ℃时 的水解程度比20 ℃
时的小
Fe3+ FeCl
D.为抑制 的水解,更好地保存 3溶液,应加少量盐酸
11.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
0.1 molL-1 CH COONa c(Na+)=c(Cl-)>c(CH COO-)>c(H+)
A. 3 溶液和0.1mol/L盐酸等体积混合: 3
0.1 molL-1 NH Cl c(NH H O)>c(NH)>c(Cl-)>c(OH-)
B. 4 溶液和0.1mol/L氨水等体积混合(pH>7): 3 2 4
2
C.0.1 molL-1 Na CO 溶液和0.1 molL-1 NaHCO 溶液等体积混合: 3 c(Na+)=c(CO 3 2-)+c(HCO 3 -)+c(H 2 CO 3 )
2 3 3
0.1 molL-1 Na C O H C O
D. 2 2 4溶液和0.1mol/L盐酸等体积混合( 2 2 4为二元弱酸):
2c(C O2-)+c(HC O-)+c(OH-)=c(Na+)+c(H+)
2 4 2 4
12.已知:AgCls
Ag+aq+Cl-aq ΔH>0。室温下,在含大量AgCl的浊液中,仅改变横坐标轴对应
的一个条件,纵坐标轴代表的物理量的变化趋势符合实际的是
3 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A.升高温度 B.加少量NaCl固体
C.加少量水 D.加少量KI固体
13.已知NaHSO 溶液显酸性,溶液中存在以下平衡:
3
HSO
3+ H O HSO + OH- ①
2 2 3
HSO SO2
3 H+ + 3 ②
向0.1mol·L-1的NaHSO 溶液中分别加入以下物质,下列有关说法正确的是
3
HSO
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c( 3)增大
1
B.加入少量Na
2
SO
3
固体,则c(H+) + c(Na+) = c(HSO
3
) + c(OH-) +2c(SO
3
2 )
c SO2- c OH-
3
C.加入少量NaOH溶液,c HSO-、 c H+ 的值均增大
3
SO2
D.加入氨水至中性,则2c(Na+) = c( 3 )>c(H+) = c(OH-)
14.下列化学原理的应用,主要用沉淀溶解平衡原理来解释的是
①纯碱溶液洗涤油污的能力比冷纯碱溶液强;②误将钡盐[BaCl 、Ba(NO )]当作食盐食用时,常用0.5%的
2 3 2
NaSO 溶液解毒;③石灰岩(喀斯特地貌)的溶洞形成;④BaCO 不能做“钡餐”,而BaSO 则可以;⑤使
2 4 3 4
用泡沫灭火器时“泡沫”生成的原理。
A.②③④ B.①②③ C.③④⑤ D.①②③④⑤
15.下列实验操作能达到实验目的的是
选项 操作 目的
A 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取NaClO溶液滴于 测定NaClO溶液的pH
4 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司试纸的中部,与标准比色卡对比
证明Na CO 溶液中存在
B 向含有酚酞的Na CO 溶液中滴入BaCl 溶液,观察溶液颜色的变化 2 3
2 3 2
水解平衡
取2mL0.1molL1AgNO
3
溶液,先后滴加3滴0.1molL1NaCl溶液和5 比较K
sp
AgCl 、
C
滴0.1molL1KI溶液,观察沉淀情况 K AgI 的大小
sp
D 将FeNO 样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红
检验FeNO
3
2 样品是否
3 2
变质
16.用含铁废铜制备胆矾的流程如图所示,下列说法错误的是
A.“溶解”中加HO 只是将Fe2+氧化为Fe3+
2 2
B.流程中Cu (OH) CO 可用CuO代替
2 2 3
C.pH=3时,c(Cu2+)·c2(OH-)<K [Cu(OH) ]
sp 2
D.“系列操作”前加入HSO 的目的是抑制Cu2+的水解
2 4
二、非选择题(本题共5小题,共52分。)
17.(10分)结合下表回答下列问题(均为常温下的数据):请回答下列问题:
酸 电离常数(Ka)
CH COOH 1.810-5
3
HClO 310-8
H CO K =4.410-7 K =4.710-11
2 3 1 2
H C O K =5.410-2 K =5.410-5
2 2 4 1 2
H S K =1.310-7 K =7.110-15
2 1 2
(1)同浓度的
CH
3
COO-、HCO
3
-、CO
3
2-
、
HC
2
O-
4
、ClO-、S2-
中结合
H+
的能力最强的___________。
5 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司CH COOH
3
(2)常温下0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是_____(填字
母)。
c(H+) c(H+)
A.c
H+
B.c(CHCOOH) C.c(OH-) D.c
OH-
3
CH COOH
3
(3)取等体积物质的量浓度相等的 、HClO两溶液,分别用等浓度的NaOH稀溶液中和,则消
VCH COOH
V(HClO)
耗的NaOH溶液的体积大小关系为: 3 ___________ (填“>”、“<”或“=”)
(4)在新制氯水中加入少量的NaCl固体,水的电离平衡___________移动(填“向右”、“向左”、或“不”)。
c H+ =210-7mol/L c H+ =510-6mol/L
(5)某温度下,纯水中的 。若温度不变,滴入稀硫酸使 ,则由水
c
H+
电离出的 为___________ mol/L。
t℃ K =110-13
18.(10分)(1) 时,水的 w ,则该温度____(填“>”“<”或“=”)25℃,其理由是_____。
c H 1107molL1
(2)在(1)中所述温度下, 的溶液呈____(填“酸性”“碱性”或“中性”);若该溶液中只存
c
OH
molL1
在NaOH溶质,则由水电离出的 _______ 。
H
2
(3)实验室用Zn和稀硫酸制取 ,反应时溶液中水的电离平衡_______(填“向左”“向右”或“不”,下同)移动。
在新制氯水中加入少量NaCl固体,水的电离平衡_______移动。
BaOH
(4)25℃时,pH=4的盐酸中水的电离程度_______(填“大于”“小于”或“等于”)pH=10的 2溶液中水的电
离程度。
0.1molL1 K =1.7510-5 0.1molL1 K =1.410-3
(5) 乙酸(甲, a )和 氯乙酸(乙, a )的水溶液,下列可以表示两溶
c
H
液中由水电离出的 与加入水的体积V之间关系的是_______(填字母)。
6 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司a. b. c. d.
19.(11分)某学生用0.1000mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)___________A→F;
(2)若无上述B步骤操作,则测定结果会___________;
(3)上述A步骤之前,若先用待测液润洗锥形瓶,则对滴定结果的影响是___________;
(4)判断到达滴定终点的现象是___________;
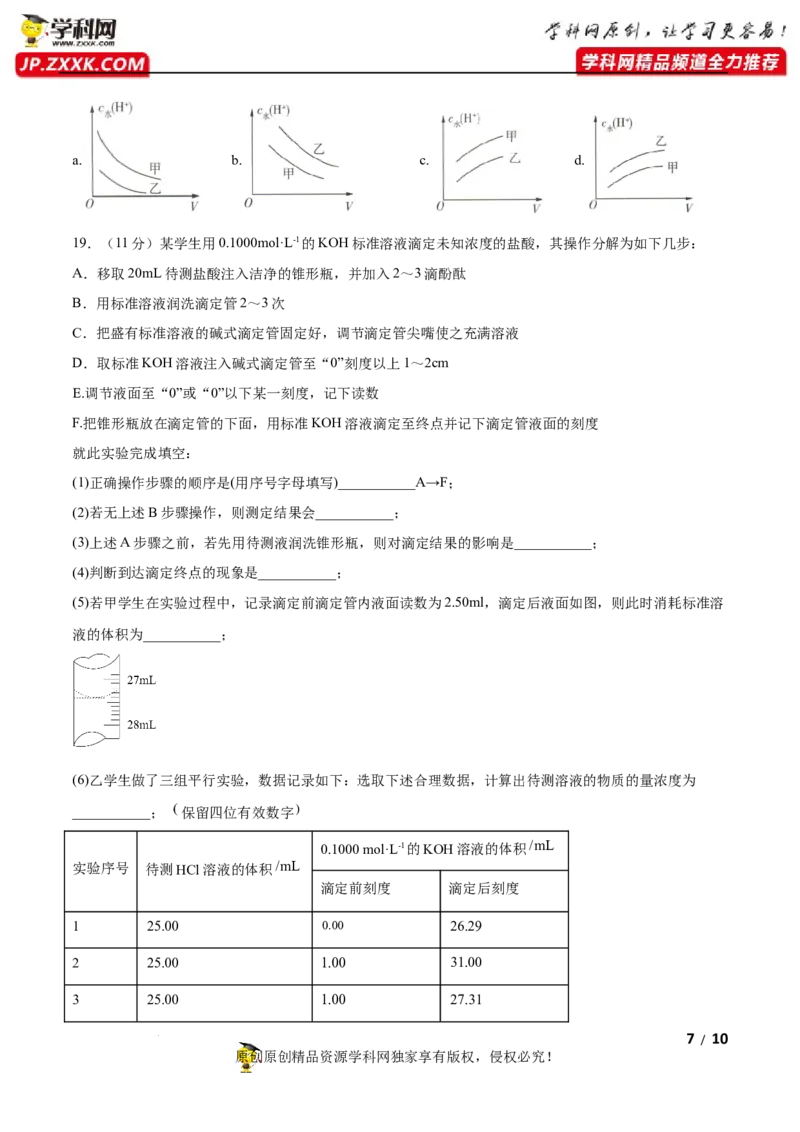
(5)若甲学生在实验过程中,记录滴定前滴定管内液面读数为2.50ml,滴定后液面如图,则此时消耗标准溶
液的体积为___________;
(6)乙学生做了三组平行实验,数据记录如下:选取下述合理数据,计算出待测溶液的物质的量浓度为
___________; (保留四位有效数字)
0.1000
mol·L-1的KOH溶液的体积/mL
实验序号 待测HCl溶液的体积/mL
滴定前刻度 滴定后刻度
1 25.00 0.00 26.29
2 25.00 1.00 31.00
3 25.00 1.00 27.31
7 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司20.(13分)按要求完成各题。
CO NaOH Na CO NaHCO
(1) 2是温室气体,可用 溶液吸收得到 2 3或 3。
Na CO CO2- CO2-
① 2 3俗称纯碱,因 3 水解而使其水溶液呈碱性,试写出 3 水解的离子方程式(忽略第二步水解):
K =
_______,其水解反应平衡常数(即水解常数)的表达式为 b _______。
K =210-4 c(HCO-):c(CO2-)=2:1 pH=
②已知25℃时, b ,则当溶液中 3 3 时,溶液的 _______。
0.1 molL1 Na CO c(OH-)-c(H+)= c(HCO-) c(H CO )
(2) 2 3溶液中 _______[用含 3 、 2 3 的关系式表示]。
Na CO
④向 2 3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:_______。
NaOH NO 2NO +2NaOH=NaNO +NaNO +H O 0.2 mol NaOH
(3)实验室可用 溶液吸收 2,反应为 2 3 2 2 。含 的
水溶液与 0.2 mol NO 2恰好完全反应得1L溶液A,溶液B为 0.1 molL1 的 CH 3 COONa 溶液,则两溶液中
c(NO) c(NO) c(CH COO-) HNO K =7.110-4
3 、 2 和 3 由大到小的顺序为_______(已知 2的电离常数 a ,
CH COOH K =1.810-5 pH
3 的电离常数 a )。可使溶液A和溶液B的 相等的方法是_______(填序号)。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH固体
c.向溶液B中加适量水 d.向溶液B中加适量NaOH固体
SO SO
(4)直接排放含 2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 2。吸收液(
NaOH SO n(SO2-):n(HSO)
溶液)吸收 2的过程中,pH随 3 3 的变化关系如下表:
n(SO2-):n(HSO) 91∶9 1∶1 9∶91
3 3
pH 8.2 7.2 6.2
NaHSO
3
①由上表判断 溶液显_______性,理由:_______。
②当吸收液呈中性时,溶液中离子浓度关系正确的是_______(填序号)。
8 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司c(Na+)=2c(CO2-)+c(HCO)
a. 3 3
c(Na+)>c(HSO)>c(SO2-)>c(H+)=c(OH-)
b. 3 3
c(Na+)+c(H+)=c(SO2-)+c(HSO)+c(OH-)
c. 3 3
21.(8分)T、T 两种温度下BaSO 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
1 2 4
(1)T ________(填“”“”或“”)T 温度时K (BaSO)=________。
1 2 sp 4
(2)根据T 温度时BaSO 的沉淀溶解平衡曲线,判断下列说法正确的是________(填序号)。
1 4
A.加入NaSO 固体可由a点变为b点
2 4
B.T 温度下,在T 曲线上方区域(不含曲线)的任意一点时,均有BaSO 沉淀生成
1 1 4
C.蒸发溶剂可能由d点变为T 曲线上a、b之间(不含a、b)的某一点
1
D.升温可由b点变为d点
(3)T 时,现有0.2mol的BaSO 沉淀,每次用1L饱和NaCO 溶液(浓度为1.7mol/L)处理。若使BaSO 中的
2 4 2 3 4
SO2 全部转化到溶液中,需要反复处理________次。[提示:BaSO(s)+CO2
(aq)
SO2
(aq)+BaCO (s)
4 4 3 4 3
K BaSO ⇌
K= sp 4 ;
K BaCO
sp 3
9 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司10 / 10
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司