文档内容
安徽省智学大联考·皖中名校联盟、合肥八中 2023-2024 学年
高二下学期年级期末检测化学试题
全卷满分 100分,考试时间 75分钟。
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息。
2.请将答案正确填写在答题卡上。
可能用到的相对原子质量:H1 Li7 C12 Mg24 Ni59
一、单选题(本题共 14小题,每小题只有一个选项正确,每题 3分,共 42分)
1. 化学与生产生活密切相关,以下说法正确的是
A. 蒽、萘属于苯的同系物,二者均为重要的化工原料
B. 可利用乙炔在氧气中燃烧时,形成的氧炔焰来焊接或切割金属
( )
C. 神舟十六号载人飞船燃料偏二甲肼 CH N-NH 属于烃类
3 2 2
D. 纳米四氧化三铁可用于制备隐身材料,它属于胶体
2. 下列说法不正确的是
A. 甲醛中π键的电子云轮廓图:
B. 苯的球棍模型:
C. Mn2+的价层电子排布式:3d5
D. 葡萄糖的一种环状结构简式:
3. 下列关于烷烃的叙述正确的是
A. 丙烷的三个碳原子可能在同一条直线上
B. 和 互为同分异构体
C. 含不对称碳原子的烷烃至少有7个碳原子
D. 碳原子数小于20,一氯代物不存在同分异构体的烷烃有7种
第1页/共10页
学科网(北京)股份有限公司4. 物质的结构决定物质的性质,下列性质差异与结构因素匹配错误的是
性质差异 结构因素
A 热稳定性:HF大于HCl HF分子间存在氢键,HCl分子间不存在氢键
B 酸性:CH COOH>CH CH OH 羟基的极性
3 3 2
C 水中的溶解性:O >O 分子极性
3 2
D 熔点:金刚石>碳化硅>晶体硅 共价键键能
A. A B. B C. C D. D
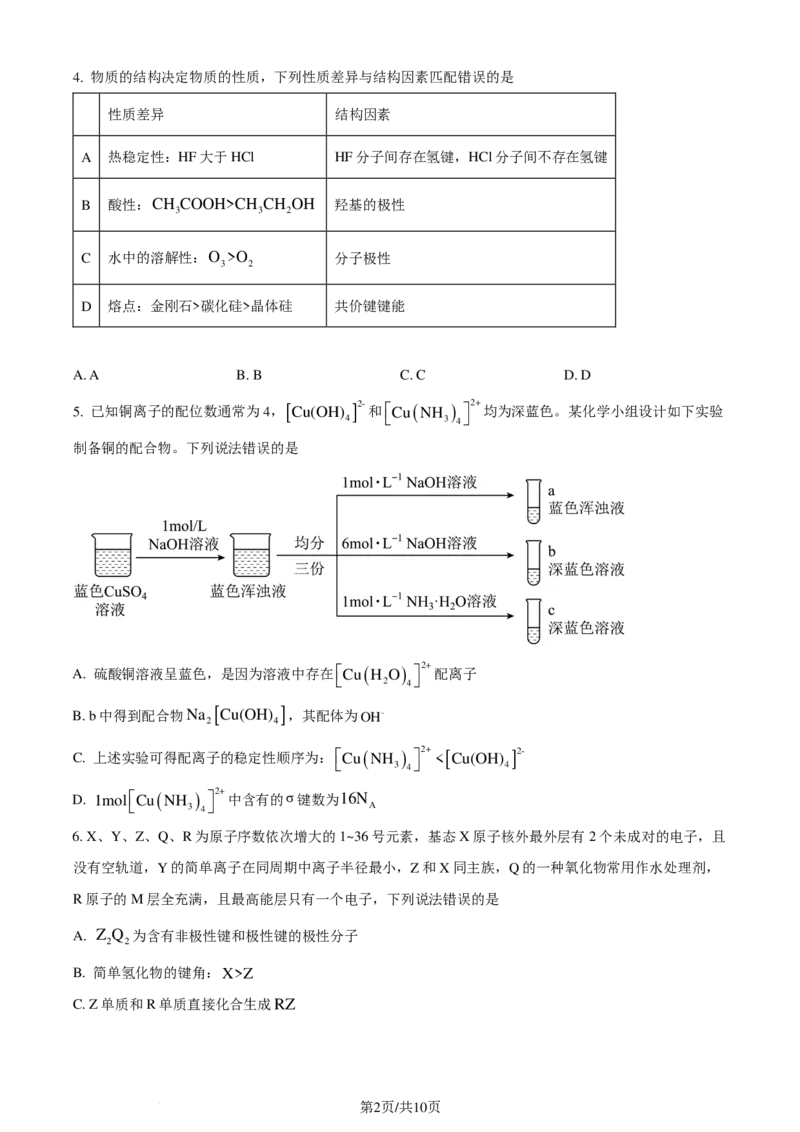
5. 已知铜离子的配位数通常为4,[ Cu(OH) ]2-和Cu ( NH ) 2+ 均为深蓝色。某化学小组设计如下实验
4 3 4
制备铜的配合物。下列说法错误的是
A. 硫酸铜溶液呈蓝色,是因为溶液中存在Cu ( H O ) 2+ 配离子
2 4
[ ]
B. b中得到配合物Na Cu(OH) ,其配体为OH-
2 4
C. 上述实验可得配离子的稳定性顺序为:Cu ( NH ) 2+ < [ Cu(OH) ]2-
3 4 4
D. 1molCu ( NH ) 2+ 中含有的σ键数为16N
3 4 A
6. X、Y、Z、Q、R为原子序数依次增大的1~36号元素,基态X原子核外最外层有2个未成对的电子,且
没有空轨道,Y的简单离子在同周期中离子半径最小,Z和X同主族,Q的一种氧化物常用作水处理剂,
R原子的M层全充满,且最高能层只有一个电子,下列说法错误的是
A. Z Q 为含有非极性键和极性键的极性分子
2 2
B. 简单氢化物的键角:X>Z
C. Z单质和R单质直接化合生成RZ
第2页/共10页
学科网(北京)股份有限公司D. YQ 分子中存在配位键
2 6
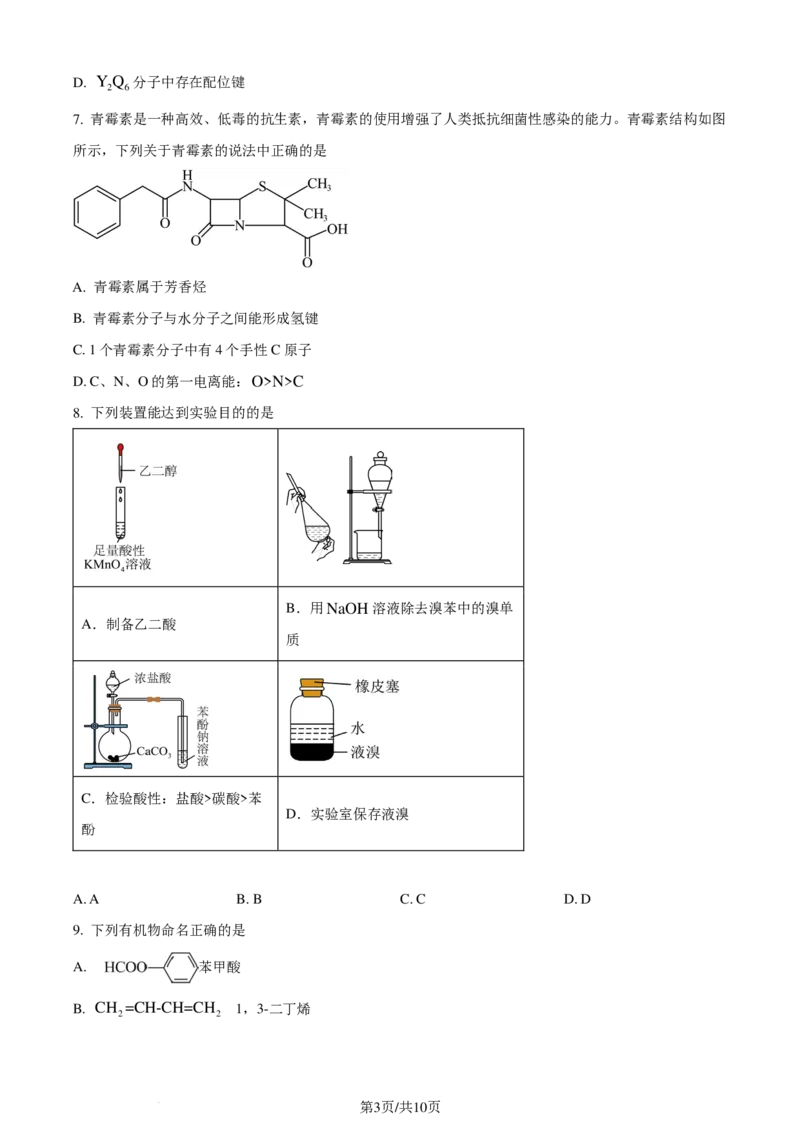
7. 青霉素是一种高效、低毒的抗生素,青霉素的使用增强了人类抵抗细菌性感染的能力。青霉素结构如图
所示,下列关于青霉素的说法中正确的是
A. 青霉素属于芳香烃
B. 青霉素分子与水分子之间能形成氢键
C. 1个青霉素分子中有4个手性C原子
D. C、N、O的第一电离能:O>N>C
8. 下列装置能达到实验目的的是
B.用NaOH溶液除去溴苯中的溴单
A.制备乙二酸
质
C.检验酸性:盐酸>碳酸>苯
D.实验室保存液溴
酚
A. A B. B C. C D. D
9. 下列有机物命名正确的是
A. 苯甲酸
B. CH =CH-CH=CH 1,3-二丁烯
2 2
第3页/共10页
学科网(北京)股份有限公司C. 二乙酸乙二酯
( ) ( )
D. CH C=CHCH CH 2,4-二甲基-2-戊烯
3 2 3 2
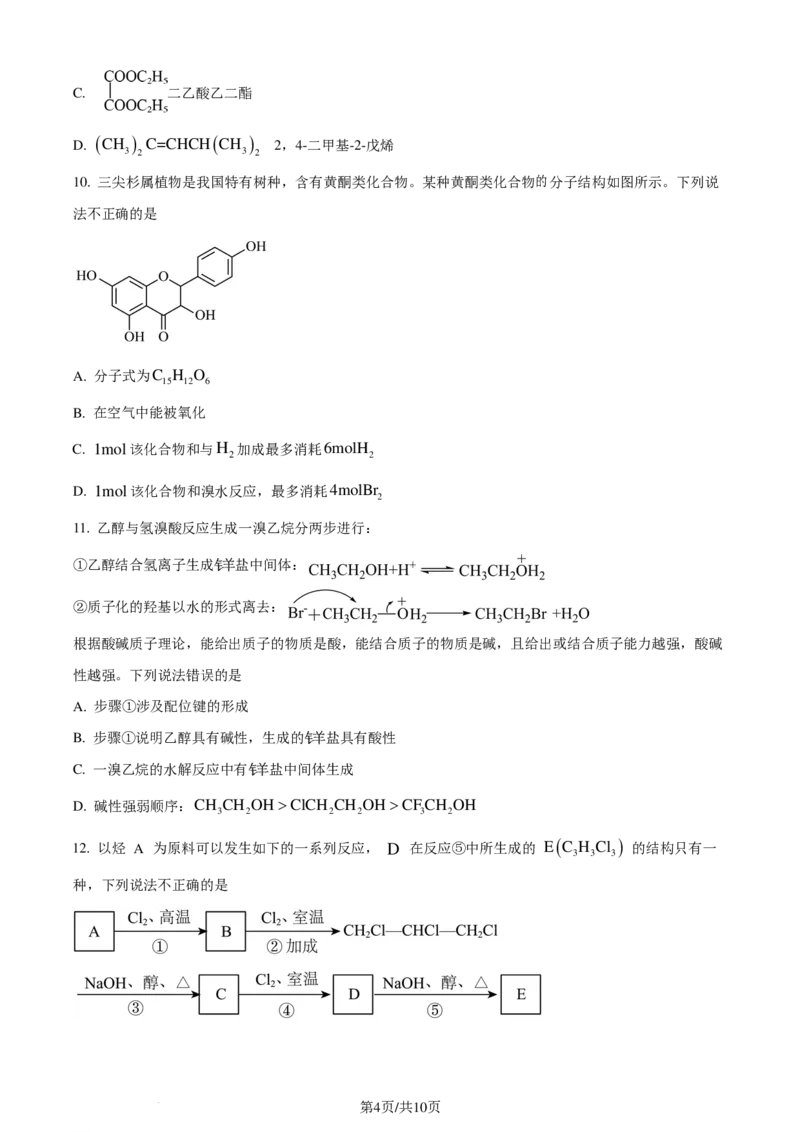
10. 三尖杉属植物是我国特有树种,含有黄酮类化合物。某种黄酮类化合物的分子结构如图所示。下列说
法不正确的是
A. 分子式为C H O
15 12 6
B. 在空气中能被氧化
C. 1mol该化合物和与H 加成最多消耗6molH
2 2
D. 1mol该化合物和溴水反应,最多消耗4molBr
2
11. 乙醇与氢溴酸反应生成一溴乙烷分两步进行:
①乙醇结合氢离子生成 盐中间体:
②质子化的羟基以水的形式离去:
根据酸碱质子理论,能给出质子的物质是酸,能结合质子的物质是碱,且给出或结合质子能力越强,酸碱
性越强。下列说法错误的是
A. 步骤①涉及配位键的形成
B. 步骤①说明乙醇具有碱性,生成的 盐具有酸性
C. 一溴乙烷的水解反应中有 盐中间体生成
D. 碱性强弱顺序:CH CH OH>ClCH CH OH>CFCH OH
3 2 2 2 3 2
( )
12. 以烃 A 为原料可以发生如下的一系列反应, D 在反应⑤中所生成的 E C H Cl 的结构只有一
3 3 3
种,下列说法不正确的是
第4页/共10页
学科网(北京)股份有限公司A. 烃 A 的结构简式为 CH CH=CH
3 2
B. ①是取代反应,③和⑤是消去反应
C. 满足题意的 C 的结构简式为 CHCl=CH−CH Cl
2
D. 满足题意的D的核磁共振氢谱只有一个峰
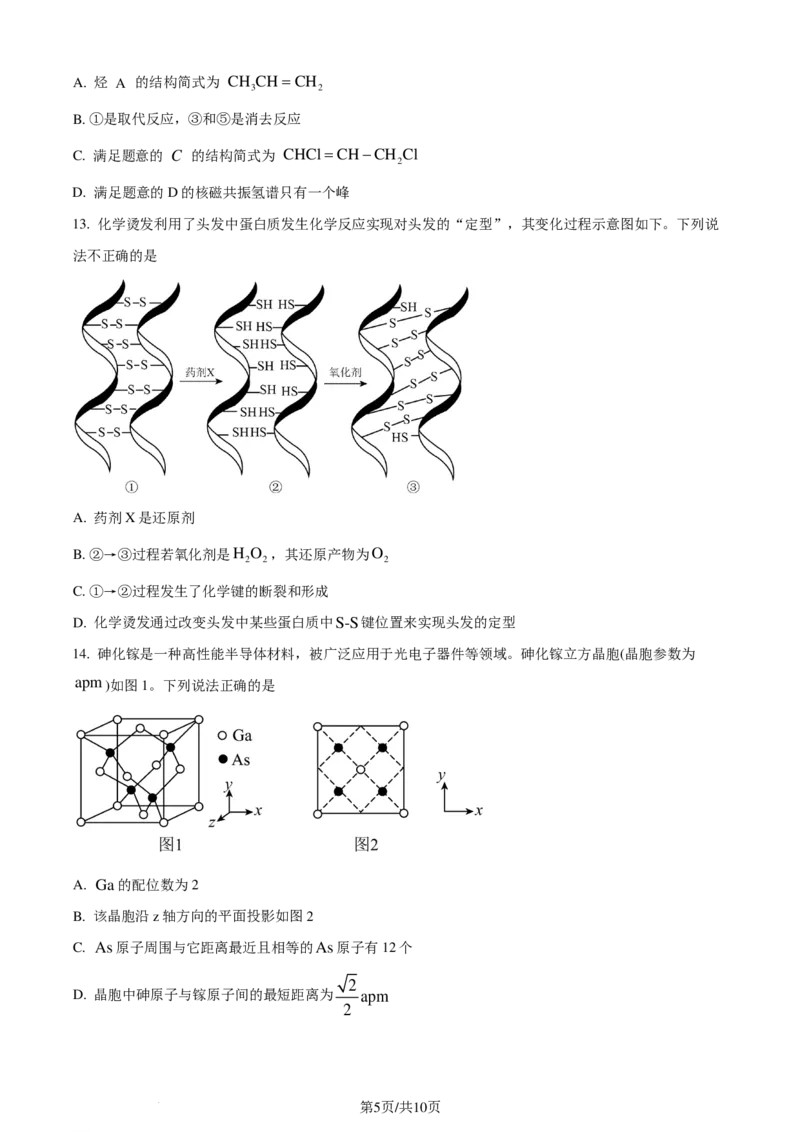
13. 化学烫发利用了头发中蛋白质发生化学反应实现对头发的“定型”,其变化过程示意图如下。下列说
法不正确的是
A. 药剂X是还原剂
B. ②→③过程若氧化剂是H O ,其还原产物为O
2 2 2
C. ①→②过程发生了化学键的断裂和形成
D. 化学烫发通过改变头发中某些蛋白质中S-S键位置来实现头发的定型
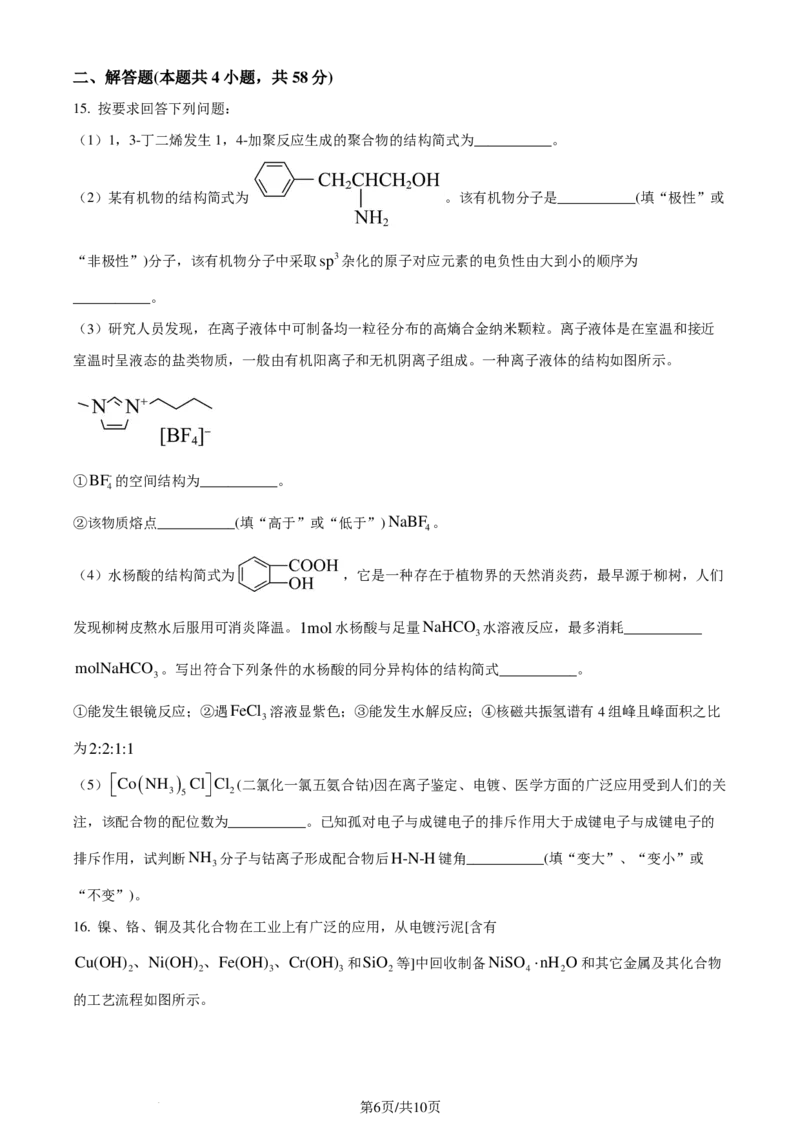
14. 砷化镓是一种高性能半导体材料,被广泛应用于光电子器件等领域。砷化镓立方晶胞(晶胞参数为
apm )如图1。下列说法正确的是
A. Ga的配位数为2
B. 该晶胞沿z轴方向的平面投影如图2
C. As原子周围与它距离最近且相等的As原子有12个
2
D. 晶胞中砷原子与镓原子间的最短距离为 apm
2
第5页/共10页
学科网(北京)股份有限公司二、解答题(本题共 4小题,共 58分)
15. 按要求回答下列问题:
(1)1,3-丁二烯发生1,4-加聚反应生成的聚合物的结构简式为___________。
(2)某有机物的结构简式为 。该有机物分子是___________(填“极性”或
“非极性”)分子,该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为
___________。
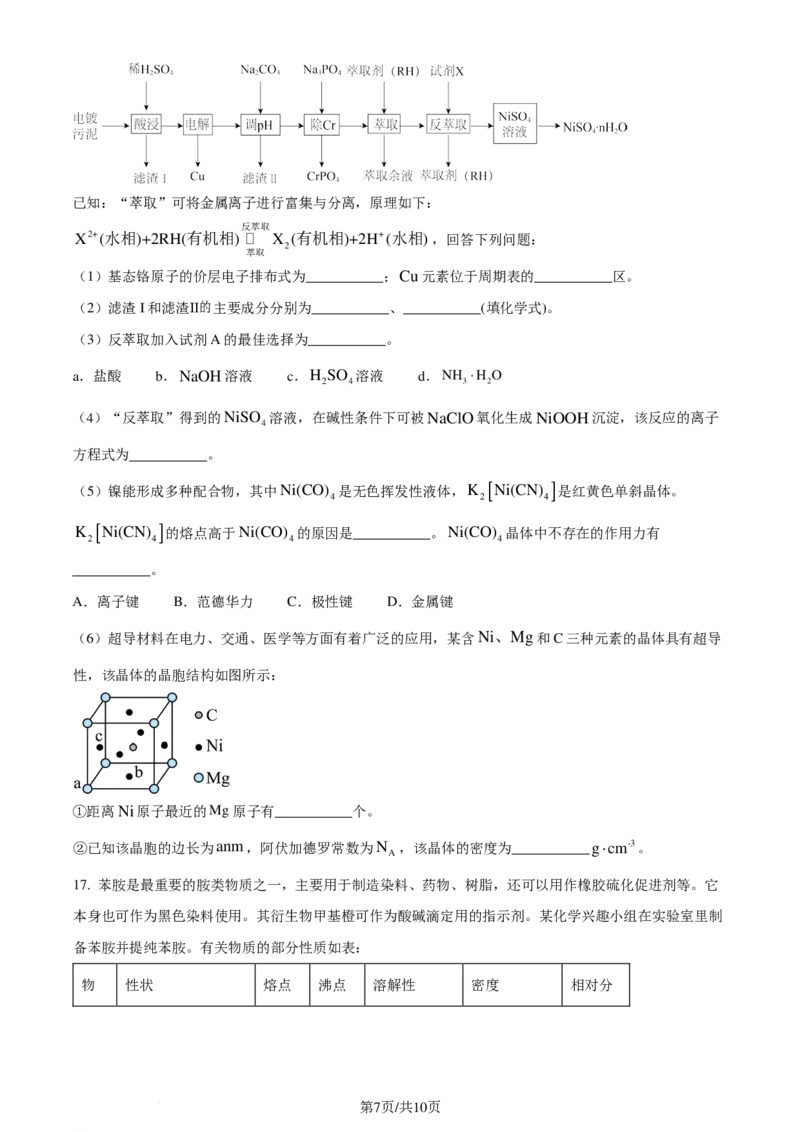
(3)研究人员发现,在离子液体中可制备均一粒径分布的高熵合金纳米颗粒。离子液体是在室温和接近
室温时呈液态的盐类物质,一般由有机阳离子和无机阴离子组成。一种离子液体的结构如图所示。
①BF-的空间结构为___________。
4
②该物质熔点___________(填“高于”或“低于”)NaBF 。
4
(4)水杨酸的结构简式为 ,它是一种存在于植物界的天然消炎药,最早源于柳树,人们
发现柳树皮熬水后服用可消炎降温。1mol水杨酸与足量NaHCO 水溶液反应,最多消耗___________
3
molNaHCO 。写出符合下列条件的水杨酸的同分异构体的结构简式___________。
3
①能发生银镜反应;②遇FeCl 溶液显紫色;③能发生水解反应;④核磁共振氢谱有4组峰且峰面积之比
3
为2:2:1:1
(5)
Co ( NH
3
)
5
Cl
Cl
2
(二氯化一氯五氨合钴)因在离子鉴定、电镀、医学方面的广泛应用受到人们的关
注,该配合物的配位数为___________。已知孤对电子与成键电子的排斥作用大于成键电子与成键电子的
排斥作用,试判断NH 分子与钴离子形成配合物后H-N-H键角___________(填“变大”、“变小”或
3
“不变”)。
16. 镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有
Cu(OH) 、Ni(OH) 、Fe(OH)、Cr(OH) 和SiO 等]中回收制备NiSO ⋅nH O和其它金属及其化合物
2 2 3 3 2 4 2
的工艺流程如图所示。
第6页/共10页
学科网(北京)股份有限公司已知:“萃取”可将金属离子进行富集与分离,原理如下:
反萃取
X2+(水相)+2RH(有机相) X (有机相)+2H+(水相),回答下列问题:
2
萃取
(1)基态铬原子的价层电子排布式为___________;Cu元素位于周期表的___________区。
(2)滤渣I和滤渣Ⅱ的主要成分分别为___________、___________(填化学式)。
(3)反萃取加入试剂A的最佳选择为___________。
a.盐酸 b.NaOH溶液 c.H SO 溶液 d.NH ⋅H O
2 4 3 2
(4)“反萃取”得到的NiSO 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子
4
方程式为___________。
[ ]
(5)镍能形成多种配合物,其中Ni(CO) 是无色挥发性液体,K Ni(CN) 是红黄色单斜晶体。
4 2 4
[ ]
K Ni(CN) 的熔点高于Ni(CO) 的原因是___________。Ni(CO) 晶体中不存在的作用力有
2 4 4 4
___________。
A.离子键 B.范德华力 C.极性键 D.金属键
(6)超导材料在电力、交通、医学等方面有着广泛的应用,某含Ni、Mg和C三种元素的晶体具有超导
性,该晶体的晶胞结构如图所示:
①距离Ni原子最近的Mg原子有___________个。
②已知该晶胞的边长为anm,阿伏加德罗常数为N ,该晶体的密度为___________g⋅cm-3。
A
17. 苯胺是最重要的胺类物质之一,主要用于制造染料、药物、树脂,还可以用作橡胶硫化促进剂等。它
本身也可作为黑色染料使用。其衍生物甲基橙可作为酸碱滴定用的指示剂。某化学兴趣小组在实验室里制
备苯胺并提纯苯胺。有关物质的部分性质如表:
物 性状 熔点 沸点 溶解性 密度 相对分
第7页/共10页
学科网(北京)股份有限公司质 /℃ /℃ / ( g⋅cm-3 ) 子质量
苯 无色油状液体,空 微溶于水,
-6.3 184 1.02 93
胺 气中易被氧化 易溶于乙醚
硝
无色或微黄色具苦 难溶于水,
基 5.7 210.9 1.23 123
杏仁味的油状液体 易溶于乙醚
苯
乙 是一种无色有甜味
-116.2 34.6 微溶于水 0.7134
醚 的液体
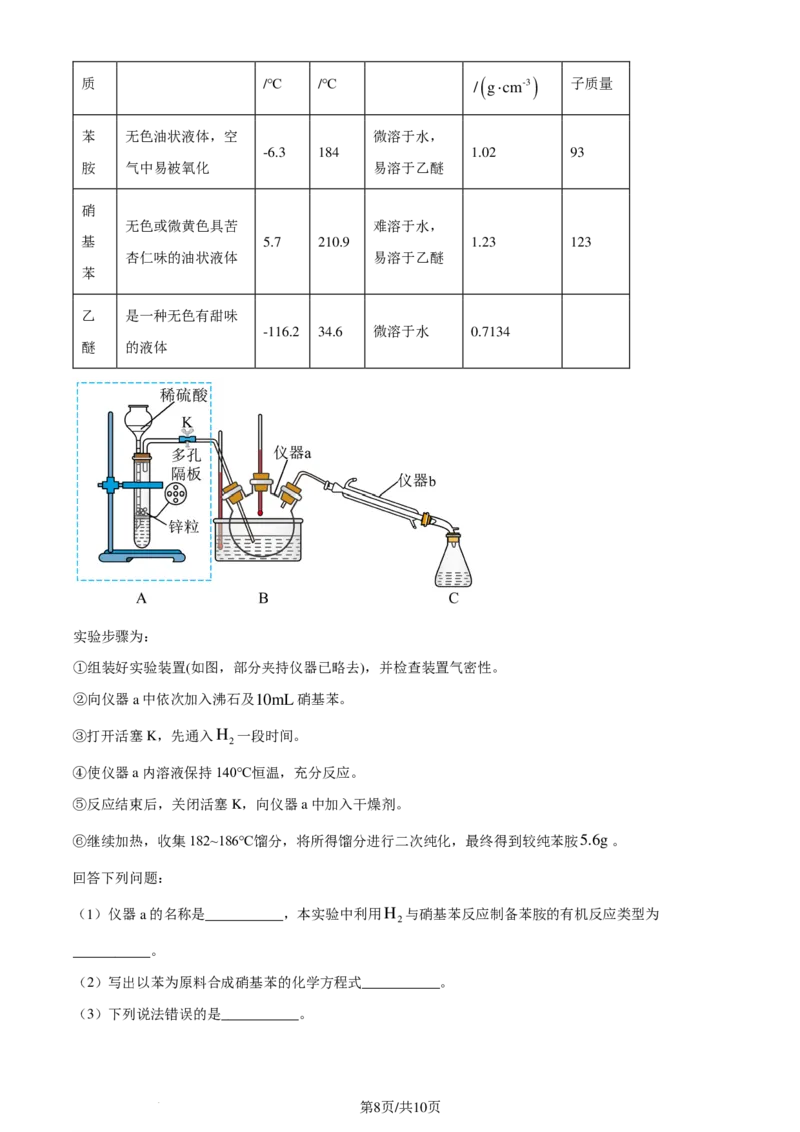
实验步骤为:
①组装好实验装置(如图,部分夹持仪器已略去),并检查装置气密性。
②向仪器a中依次加入沸石及10mL硝基苯。
③打开活塞K,先通入H 一段时间。
2
④使仪器a内溶液保持140℃恒温,充分反应。
⑤反应结束后,关闭活塞K,向仪器a中加入干燥剂。
⑥继续加热,收集182~186℃馏分,将所得馏分进行二次纯化,最终得到较纯苯胺5.6g。
回答下列问题:
(1)仪器a的名称是___________,本实验中利用H 与硝基苯反应制备苯胺的有机反应类型为
2
___________。
(2)写出以苯为原料合成硝基苯的化学方程式___________。
(3)下列说法错误的是___________。
第8页/共10页
学科网(北京)股份有限公司A. 装置A也可以用于电石与水反应制备乙炔气体
B. 蒸馏时温度计水银球应置于蒸馏烧瓶支管口附近
C. 如果加热后发现忘加沸石,应立刻补加
D. 仪器b的作用是冷凝回收馏分,也可以用球形冷凝管替代
(4)若实验中未先通入H 一段时间,则可能导致___________。步骤④中装置B选择的热传导介质为
2
___________(填“水”或“油”)。
(5)二次纯化并测定产率:
蒸馏所得苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:
①氨基的N原子上存在孤对电子,易与H+结合,故显碱性,写出苯胺与盐酸反应的化学方程式:
___________。
②第二步中乙醚的作用为___________,“液相”是___________(填“水层”或“有机层”)。
(6)本实验的产率为___________(保留一位小数)。
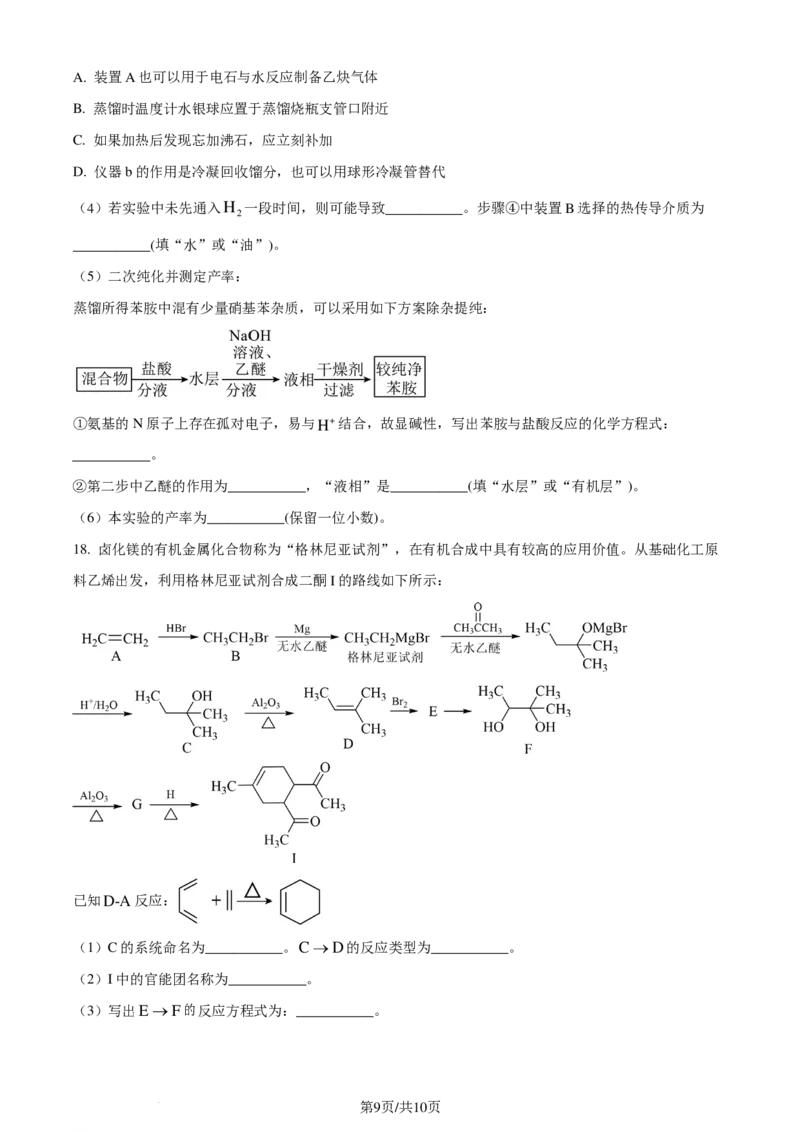
18. 卤化镁的有机金属化合物称为“格林尼亚试剂”,在有机合成中具有较高的应用价值。从基础化工原
料乙烯出发,利用格林尼亚试剂合成二酮I的路线如下所示:
已知D-A反应:
(1)C的系统命名为___________。C→D的反应类型为___________。
(2)I中的官能团名称为___________。
(3)写出E→F的反应方程式为:___________。
第9页/共10页
学科网(北京)股份有限公司(4)已知G→I为D-A反应,H的结构简式为___________。
(5)D的一种同分异构体存在顺反异构,其中反式异构体的结构简式为___________。
(6)F的一种同分异构体与F具有相同官能团,核磁共振氢谱有三组峰,峰面积之比为3:2:1,该同分异
构体的结构简式为___________。
(7)由合成路线可知,“格林尼亚试剂'在有机合成中的主要作用是___________。
A. 保护羰基 B. 形成碳环 C. 增长碳链 D. 催化反应
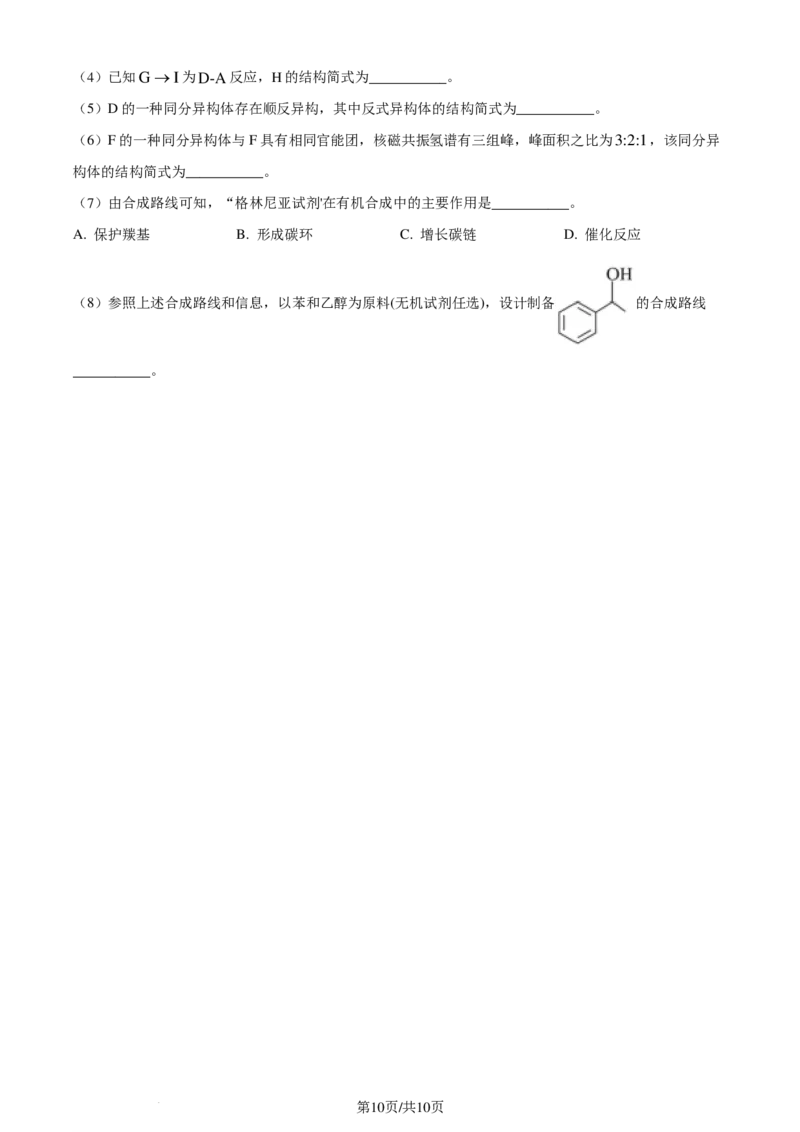
(8)参照上述合成路线和信息,以苯和乙醇为原料(无机试剂任选),设计制备 的合成路线
___________。
第10页/共10页
学科网(北京)股份有限公司