文档内容
河南省信阳高级中学北湖校区
2024-2025 学年高二上期期中测试
化学试题
出题人:曹磊 审题人:刘胜兰 龚珂珂
可能用到的相对原子质量:H1 C12 N14 O16
第1卷(选择題)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与生产、生活和科技密切相关。下列说法错误的是
A.制作豆腐过程中,常在豆浆中加入氯化镁、硫縱钻等凝固剂
B.利用油脂在酸性条件下水解生成的高级脂肪酸盐来制取肥皂
C.将易府败的食物储存在冰箱里,可延长储存食物的时间
D.高纯度硅可用于制作光优电站、人造卫星等的太阳能电池
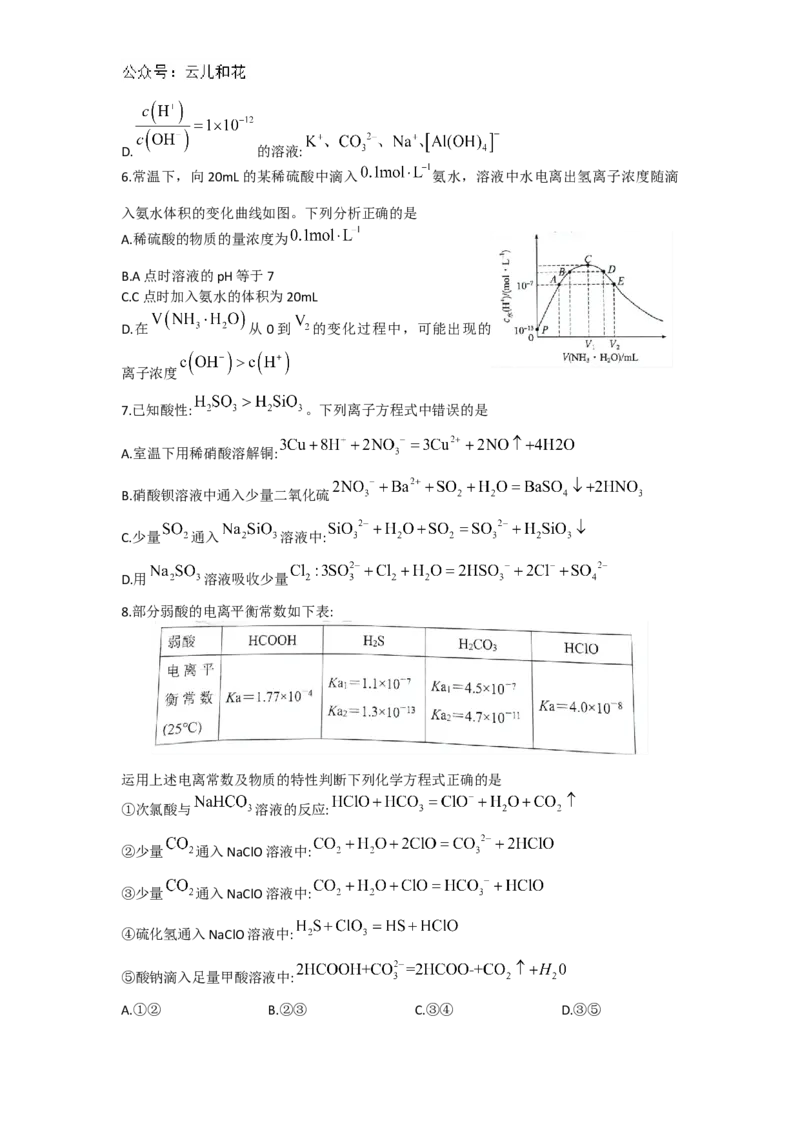
2.橙花醇的结构简式如图,根据乙烯和乙醇的有关性质,下列有关橙花碻的说法不正确的
是
A.分子式为
B.能发生取代反应、加成反应
C.所有的C原子有可能共平面
D.能用酸性高锰酸钾溶液检验其中是否含有碳碳双键
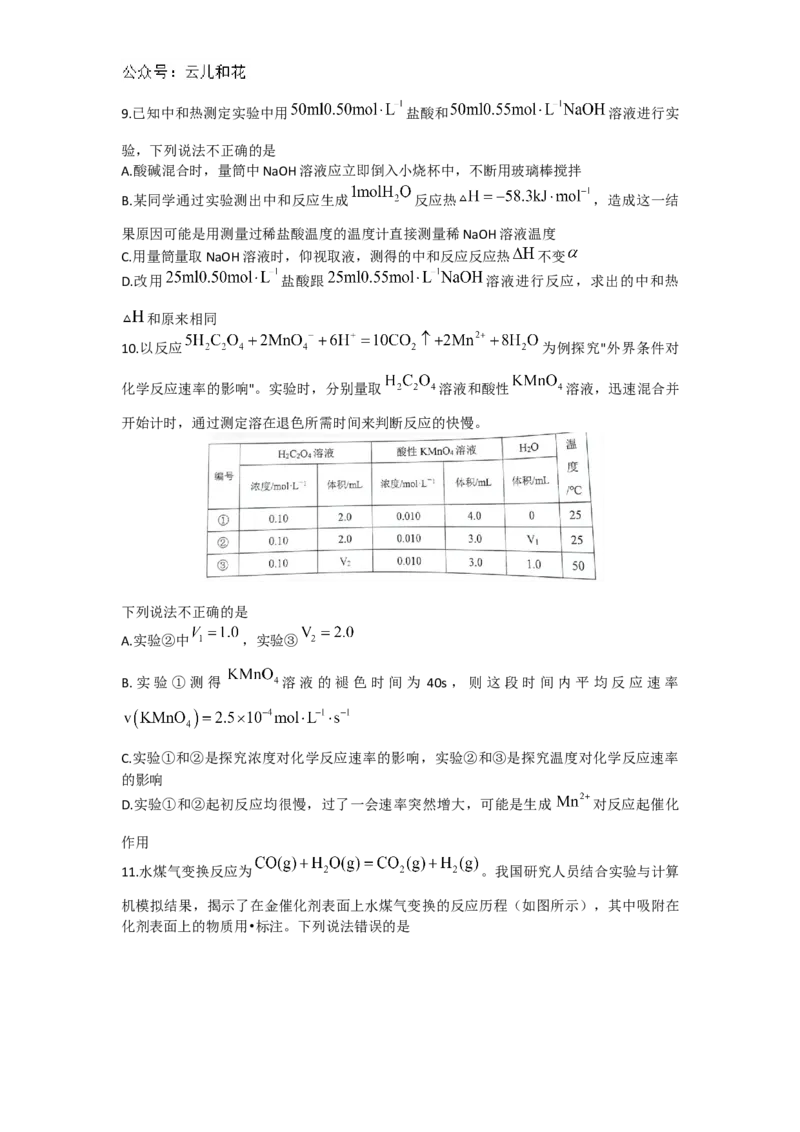
3.下列操作规范且能达到实验目的的是
4.下列事实还能用勒夏特列原理解释的是
A.向 溶液中加入KSCN溶液,溶液颜色变深
B.新制氯水在光照条件下颜色变浅
C..工业上选择在温度为 的条件下合成氨
D.将装有 和 的混合气体的烧瓶置于热水中的颜色深于冷水中颜色
5.常温下,下列各组离子,在指定条件下定能大量共存的是
A.无色透明的水溶液中:
B.新制氯水在光照条件下颜色变浅
C水电离出的 的溶液:D. 的溶液:
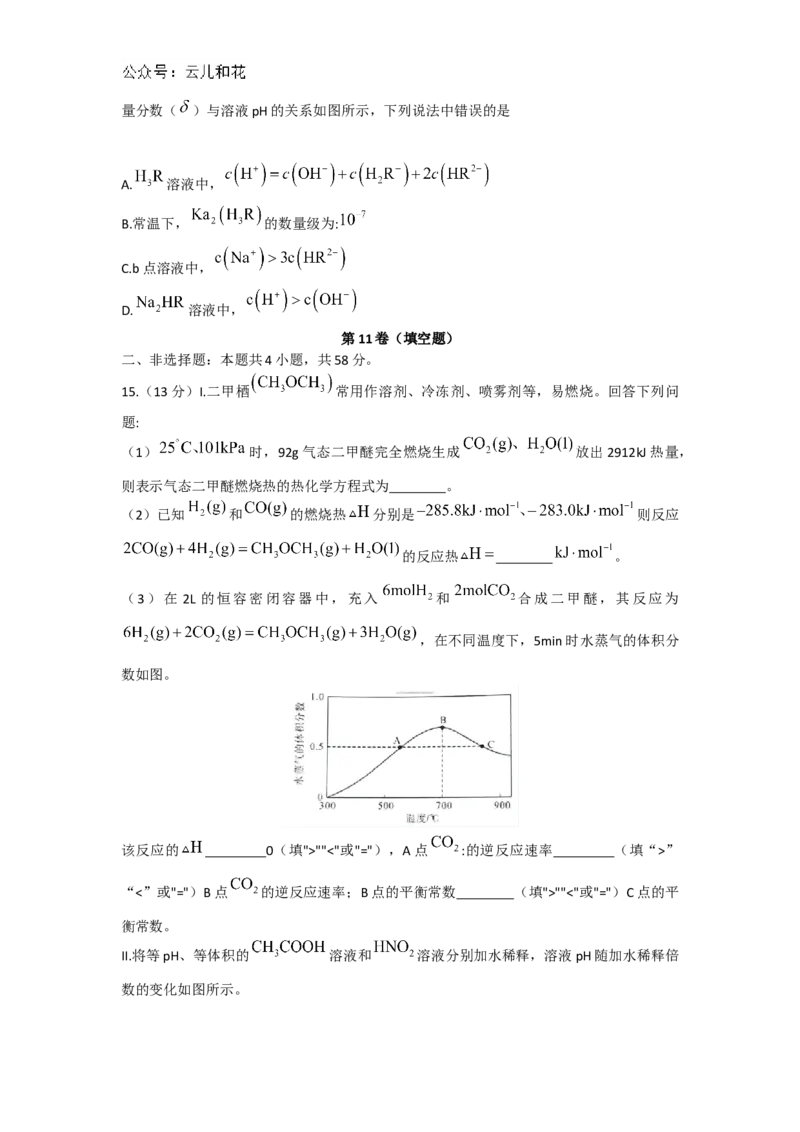
6.常温下,向20mL的某稀硫酸中滴入 氨水,溶液中水电离出氢离子浓度随滴
入氨水体积的变化曲线如图。下列分析正确的是
A.稀硫酸的物质的量浓度为
B.A点时溶液的pH等于7
C.C点时加入氨水的体积为20mL
D.在 从0到 的变化过程中,可能出现的
离子浓度
7.已知酸性: 。下列离子方程式中错误的是
A.室温下用稀硝酸溶解铜:
B.硝酸钡溶液中通入少量二氧化硫
C.少量 通入 溶液中:
D.用 溶液吸收少量
8.部分弱酸的电离平衡常数如下表:
运用上述电离常数及物质的特性判断下列化学方程式正确的是
①次氯酸与 溶液的反应:
②少量 通入NaClO溶液中:
③少量 通入NaClO溶液中:
④硫化氢通入NaClO溶液中:
⑤酸钠滴入足量甲酸溶液中:
A.①② B.②③ C.③④ D.③⑤9.已知中和热测定实验中用 盐酸和 溶液进行实
验,下列说法不正确的是
A.酸碱混合时,量筒中NaOH溶液应立即倒入小烧杯中,不断用玻璃棒搅拌
B.某同学通过实验测出中和反应生成 反应热 ,造成这一结
果原因可能是用测量过稀盐酸温度的温度计直接测量稀NaOH溶液温度
C.用量筒量取NaOH溶液时,仰视取液,测得的中和反应反应热 不变
D.改用 盐酸跟 溶液进行反应,求出的中和热
和原来相同
10.以反应 为例探究"外界条件对
化学反应速率的影响"。实验时,分别量取 溶液和酸性 溶液,迅速混合并
开始计时,通过测定溶在退色所需时间来判断反应的快慢。
下列说法不正确的是
A.实验②中 ,实验③
B.实验①测得 溶液的褪色时间为 40s,则这段时间内平均反应速率
C.实验①和②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率
的影响
D.实验①和②起初反应均很慢,过了一会速率突然增大,可能是生成 对反应起催化
作用
11.水煤气变换反应为 。我国研究人员结合实验与计算
机模拟结果,揭示了在金催化剂表面上水煤气变换的反应历程(如图所示),其中吸附在
化剂表面上的物质用•标注。下列说法错误的是A.水煤气变换反应的
B.该总反应含6个基元反应
C.该历程中最大能垒(活化能)
D.升温和加入催化剂均能增加反应物的活化分子百分数,加快反应速率
12.硼酸 的电离方程式为 。已知常温下,
、 。下列说法错误的是
A. 为一元酸
B.常温下, 溶液的PH约为6
C.常温下, 和 溶液均为 的PH:前者>后者
D. 的 溶液中加水稀释,溶液中 变小
13. 在 一 定 条 件 下 , 取 一 定 量 的 A 和 B 在 恒 容 密 闭 容 器 中 发 应 :
达 到 平
衡时,M的浓度与温度和容器容积的关系如图所示。下列
有关说法错误的是
A.该反应为吸热反应
B.
C.达到平衡后,增大B的量不会提高A的转化率
D.若 ,则恒温恒容条件下容器内压强不再变化时
不能判断反应达到平衡状态
14.已知 是二元弱酸,常温下向其溶液中加入
NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数( )与溶液pH的关系如图所示,下列说法中错误的是
A. 溶液中,
B.常温下, 的数量级为:
C.b点溶液中,
D. 溶液中,
第11卷(填空题)
二、非选择题:本题共4小题,共58分。
15.(13分)I.二甲梄 常用作溶剂、冷冻剂、喷雾剂等,易燃烧。回答下列问
题:
(1) 时,92g气态二甲醚完全燃烧生成 放出2912kJ热量,
则表示气态二甲醚燃烧热的热化学方程式为 。
(2)已知 和 的燃烧热 分别是 则反应
的反应热 。
(3)在 2L 的恒容密闭容器中,充入 和 合成二甲醚,其反应为
,在不同温度下,5min时水蒸气的体积分
数如图。
该反应的 0(填">""<"或"="),A点 :的逆反应速率 (填“>”
“<”或"=")B点 的逆反应速率;B点的平衡常数 (填">""<"或"=")C点的平
衡常数。
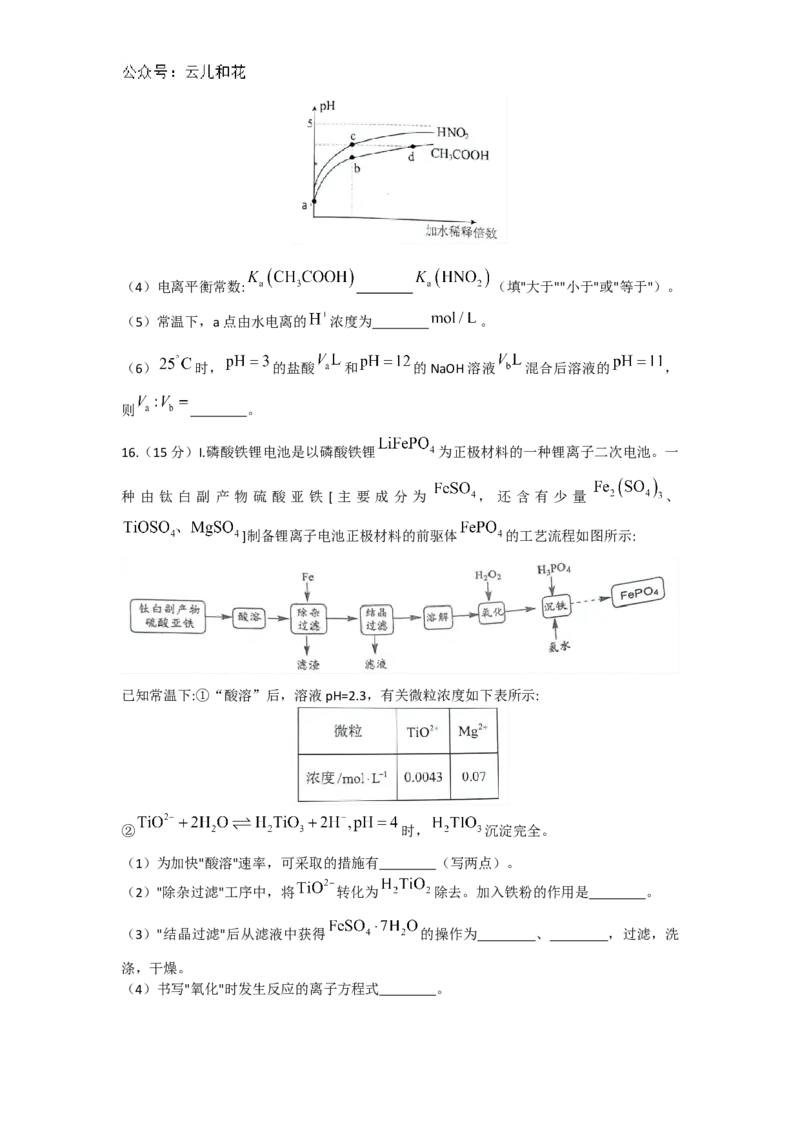
II.将等pH、等体积的 溶液和 溶液分别加水稀释,溶液pH随加水稀释倍
数的变化如图所示。(4)电离平衡常数: (填"大于""小于"或"等于")。
(5)常温下,a点由水电离的 浓度为 。
(6) 时, 的盐酸 和 的NaOH溶液 混合后溶液的 ,
则 。
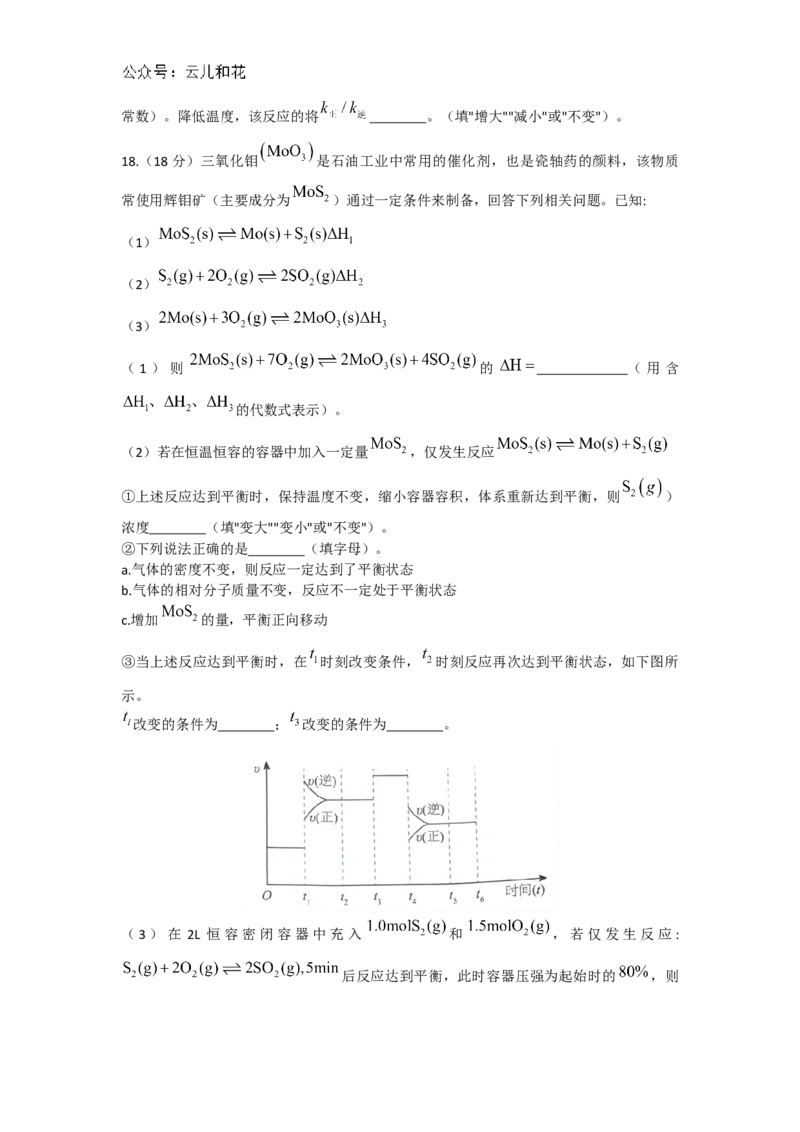
16.(15分)I.磷酸铁锂电池是以磷酸铁锂 为正极材料的一种锂离子二次电池。一
种 由 钛 白 副 产 物 硫 酸 亚 铁 [ 主 要 成 分 为 , 还 含 有 少 量 、
]制备锂离子电池正极材料的前驱体 的工艺流程如图所示:
已知常温下:①“酸溶”后,溶液pH=2.3,有关微粒浓度如下表所示:
② 时, 沉淀完全。
(1)为加快"酸溶"速率,可采取的措施有 (写两点)。
(2)"除杂过滤"工序中,将 转化为 除去。加入铁粉的作用是 。
(3)"结晶过滤"后从滤液中获得 的操作为 、 ,过滤,洗
涤,干燥。
(4)书写"氧化"时发生反应的离子方程式 。II.测定过硫酸钠 产品纯度:称取0.3000g样品,用蒸馏水溶解,加入过量 KI,
充分反应后,再滴加几滴指示剂,用 标准溶液滴定,达到滴定终
点 时 , 消 耗 标 准 溶 液 的 体 积 为 20.00mL 。 ( 已 知 : ,
的摩尔质量 。
(5) 标准溶液盛放在 (填"酸式"或"碱式")滴定管中;
达到滴定终点的现象是: 。
(6)下列操作导致测定结果偏低的是
A.未用 标准溶液润洗滴定管
B.用待测液润洗锥形瓶
C.滴定前俯视读数,滴定后仰视读数
D.滴定前无气泡,滴定后尖嘴处有气泡
(7)样品的纯度为 (保留三位有效数字)。
17.(12分)硫酸是中学化学实验的重要试剂。回答下列问题:
I.某反应 的速率方程为 ,。改变反应物浓
度时,反应的瞬时速率如表所示:
(1)速率方程中的 , 。
(2)该反应的速率常数 。
II.温度为T时,在容积为1L的密闭容器中进行反应 ,已知该
反应通过以下两步完成:
i. (快反应)
ii. (慢反应)
(3)写出第ii步的反应方程式:
(4)该反应的决速步骤为 (填"第1步"或"第ii步"),
(5)总反应的 ( 为正、逆反应速率常数)。降低温度,该反应的将 。(填"增大""减小"或"不变")。
18.(18分)三氧化钼 是石油工业中常用的催化剂,也是瓷轴药的颜料,该物质
常使用辉钼矿(主要成分为 )通过一定条件来制备,回答下列相关问题。已知:
(1)
(2)
(3)
( 1 ) 则 的 ( 用 含
的代数式表示)。
(2)若在恒温恒容的容器中加入一定量 ,仅发生反应
①上述反应达到平衡时,保持温度不变,缩小容器容积,体系重新达到平衡,则 )
浓度 (填"变大""变小"或"不变")。
②下列说法正确的是 (填字母)。
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加 的量,平衡正向移动
③当上述反应达到平衡时,在 时刻改变条件, 时刻反应再次达到平衡状态,如下图所
示。
改变的条件为 ; 改变的条件为 。
(3)在 2L 恒容密闭容器中充入 和 ,若仅发生反应:
后反应达到平衡,此时容器压强为起始时的 ,则内, 的反应速率为 。
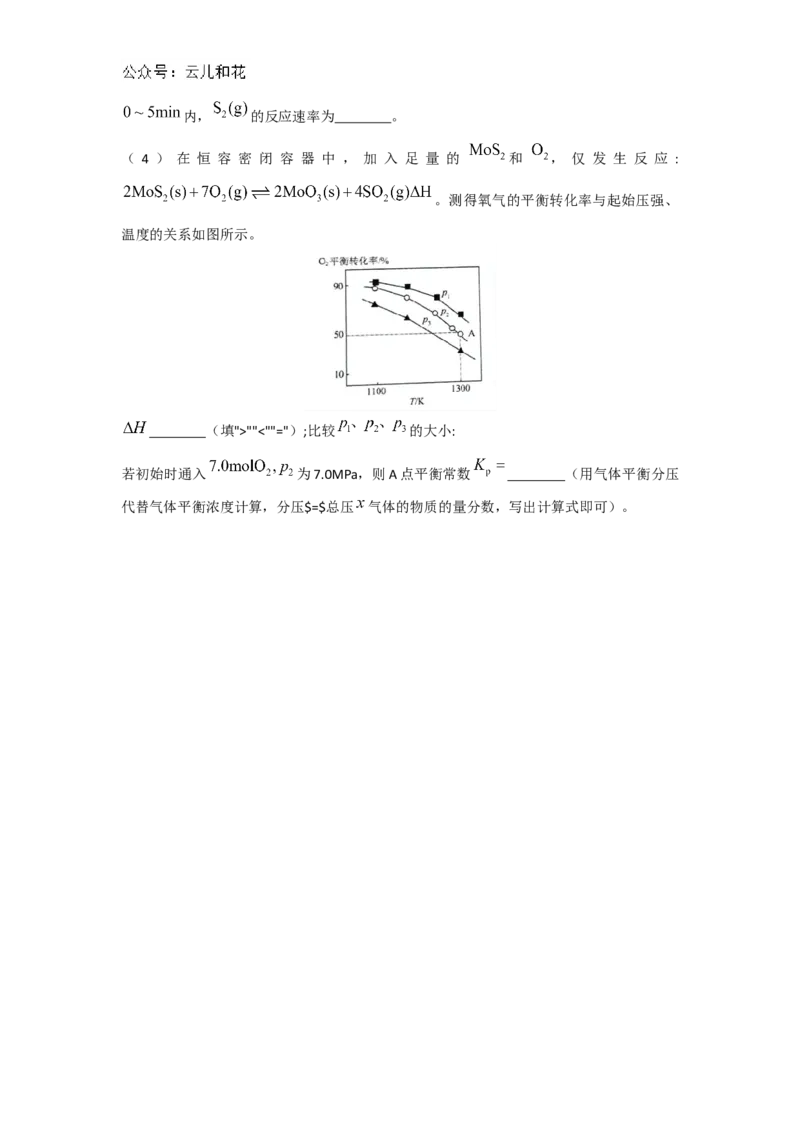
( 4 ) 在 恒 容 密 闭 容 器 中 , 加 入 足 量 的 和 , 仅 发 生 反 应 :
。测得氧气的平衡转化率与起始压强、
温度的关系如图所示。
(填">""<""=");比较 的大小:
若初始时通入 为7.0MPa,则A点平衡常数 (用气体平衡分压
代替气体平衡浓度计算,分压$=$总压 气体的物质的量分数,写出计算式即可)。河南省信阳高级中学北湖校区
2024-2025 学年高二上期期中测试
化学答案
题号 1 2 3 4 5 6 7 8 9 10
答案 B D A C D C B D B B
题号 11 12 13 14
答案 B C B D
15.【答案】(13 分)
(1) (1) (2分)
(2) (2分)
(3)<(1分);<(1分);>(1分);
(4)小于(2分)
(5) (2分)
(6) (2分)
16. 【答案】(15 分)
(1))搅拌、加热、适当提高酸的浓度等合理答案均可(2分)
(2)还原 ;调节pH,使 转化为 (2分)
(3)蒸发浓缩(1 分);冷却结晶(1 分)
(4) (2分)
(5)碱式(1 分);当滴入最后半点标准液时,溶液由蓝色变为无色,且半分钟内不恢复
原色(2分)
(6)D(2分)
(7) (2分)
17. 【答案】(12分)
(1)1(2分);0(2分)
(2) (2分)
(3) (g) (2分)
(4)第 步(2 分)
(5)增大(2分)
18. 答案 (18 分)
(1) (2分)(2)不变(2分); (2分); 增大 的浓度(2分); 加入催化剂(2分);
(3) (2分)
(4)<(2分); (2分); (2分);