文档内容
2025 新高考单科模拟综合卷(三)
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答卷前,考生务必将自己的姓名、准考证号填写在本试卷和答题卡相应位置上。
3.请按照题号顺序在各题的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试
题卷上答题无效。
4.考试结束后,将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H1 C12 O16 P31 S32 K39 Ca40 La139
一、选择题:本大题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项符合题目要求。
1.化学与生产、生活、科技、环境等密切相关,下列说法错误的是( )
A.“神舟十七号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
B.家庭装修中用的水性漆以水作稀释剂,相比油性漆更有利于人类健康
C.推广使用风能、太阳能等新能源能够减少温室气体的排放
D.稀土元素被称为“冶金工业的维生素”,合金中加入适量稀土金属,能大大改善合金性能
2.下列有关化学用语表示正确的是( )
A. 的电子式:
B. 分子的球棍模型:
C.基态As原子的电子排布式:
D.反式聚异戊二烯的结构简式:
3.实验室安全至关重要。下列做法正确的是( )
A.取用液溴时,需戴手套和护目镜,在通风橱中进行
B.中学实验室中未用完的钠、钾、白磷等不宜放回原试剂瓶
C.误食钡盐,可通过服用碳酸钠溶液解毒
D.苯酚不慎沾到皮肤上时,先用抹布擦拭,再用65℃以上的水冲洗
4.下列物质应用中涉及氧化还原反应的是( )
A.利用葡萄糖酸—δ—内酯使豆浆凝固 B.使用含氟牙膏预防龋齿
C.将植物油氢化以便于运输和储存 D.利用明矾溶液清除铜镜表面的铜锈5.设 为阿伏加德罗常数的值,下列说法正确的是( )
A. 和 混合固体中含 的数目为
B.向 溶液中通入适量 ,当有 被氧化时,共转移电子的数目为
C.用电解的方法将酸性废水中的 转化为 而除去,阴极为石墨,阳极为铁,理论电路中每通过
6mol电子,就有 个 被还原
D. 含 键的数目为
6.N-杂环取代修饰的菲啰啉- 催化剂(M)结构如图所示。已知 的原子序数为75,M中五元环含有
大 键。下列说法错误的是( )
A. 在元素周期表中位于d区 B.M中元素的第一电离能:
C.M中N原子的杂化方式有2种 D.M中一个五元环 电子数为6
7.布洛芬(N)是一种非甾体抗炎退热类药物,常用的一种合成路线如下。下列说法错误的是( )A.N与苯甲酸互为同系物 B.M分子中存在2个手性碳原子
C.Y分子中最多有11个碳原子共平面 D.X的苯环上一元取代的同分异构体有3种
8.橄榄石是自然界存在最古老的宝石之一,某橄榄石的成分可以表示为 。已知:W、X、
R、Y是原子序数依次增大的前四周期元素,基态 、X原子s轨道上的电子数和p轨道上的电子数都相
等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法正
确的是( )
A.电负性: B.简单氢化物的稳定性:
C.工业上冶炼X、Y单质的方法不同 D.该橄榄石晶体中不存在R、W形成的四面体结构
9.室温下,探究 溶液的性质,下列实验方案能达到探究目的的是( )
选项 实验方案 探究目的
A
向两支试管中分别加入 的 溶液,再向两 比较 和 的催化效率
支试管中滴入3滴浓度均为 的 和
,观察产生气体的速率
B
向 溶液中加入 是否为可逆反应
溶液,充分振荡后滴加 溶液,观察颜色变化
C
向苯酚溶液中滴加几滴 溶液,溶液呈 与苯酚发生了氧化还原反应
紫色
D
将 溶液和 与 发生了双水解反应
溶液混合,生成红褐色沉淀和气体
10.某铜冶炼厂烟气净化工序含砷废水中主要含有 和硫酸及少量 等,以其为原料制备
的工艺流程如下:
已知:有关金属离子形成氢氧化物沉淀的 范围:
金属离子
开始沉淀的pH 1.5 4.7
沉淀完全的pH 3.7 6.6
下列说法错误的是( )A.“沉铁”调 的范围是
B.“滤渣2”主要成分为 和
C.“还原”过程中生成红盐的化学方程式:
D.“一系列操作”仅涉及物理变化
11. ,在储氢和超导等领域具有重要应用。高压下, 中的每个H结合4个H形成类似 的
结构独立存在,即得到晶体 ,。设 为阿伏加德罗常数的值,下列说法错误的是( )
A.晶体 中 B. 晶体中La的配位数为8
C.晶体中H和H的最短距离: D.晶体 的密度为
12.科研人员利用高压 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微
粒转化关系如图1所示,相对能量变化关系如图2所示,吸附在催化剂表面的物质用“*”标注。下列说法
正确的是( )
A.反应过程中存在非极性键的断裂与形成及极性键的断裂
B.由图1反应历程可以看出,生成 需要消耗
C.II表示的微粒符号是D.反应历程中化学反应速率最慢的反应是
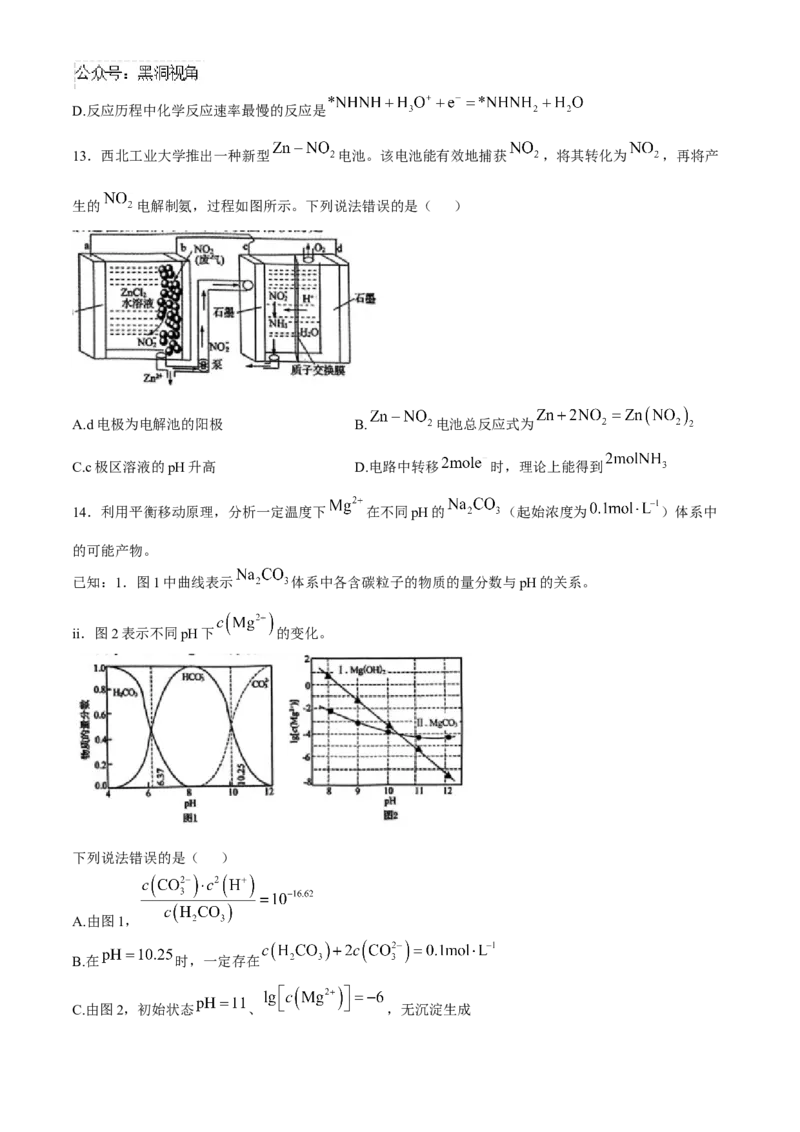
13.西北工业大学推出一种新型 电池。该电池能有效地捕获 ,将其转化为 ,再将产
生的 电解制氨,过程如图所示。下列说法错误的是( )
A.d电极为电解池的阳极 B. 电池总反应式为
C.c极区溶液的pH升高 D.电路中转移 时,理论上能得到
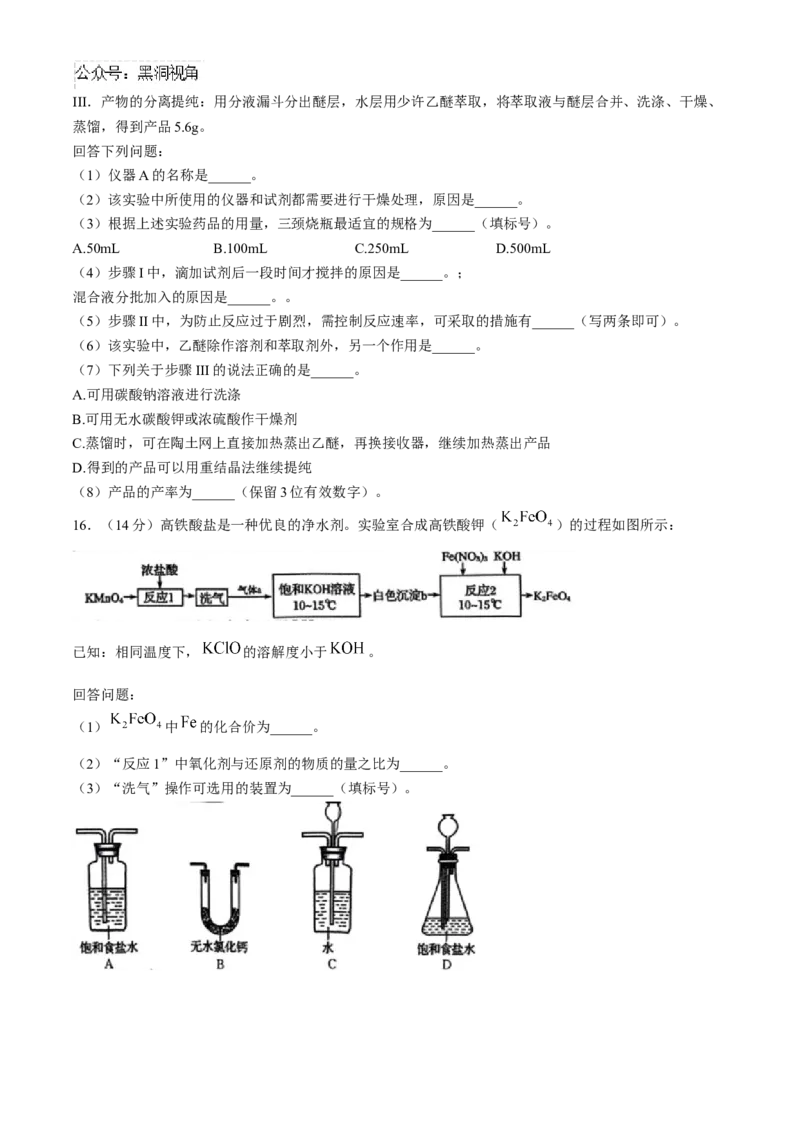
14.利用平衡移动原理,分析一定温度下 在不同pH的 (起始浓度为 )体系中
的可能产物。
已知:1.图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
ii.图2表示不同pH下 的变化。
下列说法错误的是( )
A.由图1,
B.在 时,一定存在
C.由图2,初始状态 、 ,无沉淀生成D.由图1和图2,初始状态 、 ,主要生成 沉淀
二、非选择题:本大题共4小题,共58分。
15.(14分)实验室中常用格氏试剂(有机金属镁试剂)与醛豴反应合成醇。以正溴丁烷(
)、金属镁、乙醚和丙酮为主要原料制备2—甲基—2—己醇的反应原理及主要制取装置如下:
可能发生的副反应有:
(偶联反应, 代表烃基)
已知:
①实验中相关物质的部分性质如表所示。
物质 相对分子质量 熔点/℃ 沸点/℃
密度/
乙醚 74 34.5 0.714
丙酮 58 56.5 0.790
正溴丁烷 137 101.6 1.270
2—甲基—2—己醇 116 141 0.812
②乙醚遇明火易燃。
实验步骤:
I.制备格氏试剂:向三颈烧瓶中加入2.4g镁屑和15.00mL无水乙醚,向仪器A中加入10.80mL正溴丁烷
和15.00mL无水乙醚的混合液。通入冷却水,向三颈烧瓶中滴加4.00mL混合液,引发反应。一段时间后
搅拌,并缓慢滴加剩余混合液,保持微沸状态。滴加完成后,由冷凝管上口补加25.00mL无水乙醚,继续
反应15分钟,使镁屑反应完全。
II.合成2—甲基—2—己醇:向三颈烧瓶中加入7.40mL丙酮和10.00mL无水乙醚的混合液,维持微沸状态,
继续搅拌15分钟。向三颈烧瓶中分批加入50.00mL20%的硫酸溶液,充分反应。III.产物的分离提纯:用分液漏斗分出醚层,水层用少许乙醚萃取,将萃取液与醚层合并、洗涤、干燥、
蒸馏,得到产品5.6g。
回答下列问题:
(1)仪器A的名称是______。
(2)该实验中所使用的仪器和试剂都需要进行干燥处理,原因是______。
(3)根据上述实验药品的用量,三颈烧瓶最适宜的规格为______(填标号)。
A.50mL B.100mL C.250mL D.500mL
(4)步骤I中,滴加试剂后一段时间才搅拌的原因是______。;
混合液分批加入的原因是______。。
(5)步骤II中,为防止反应过于剧烈,需控制反应速率,可采取的措施有______(写两条即可)。
(6)该实验中,乙醚除作溶剂和萃取剂外,另一个作用是______。
(7)下列关于步骤III的说法正确的是______。
A.可用碳酸钠溶液进行洗涤
B.可用无水碳酸钾或浓硫酸作干燥剂
C.蒸馏时,可在陶土网上直接加热蒸出乙醚,再换接收器,继续加热蒸出产品
D.得到的产品可以用重结晶法继续提纯
(8)产品的产率为______(保留3位有效数字)。
16.(14分)高铁酸盐是一种优良的净水剂。实验室合成高铁酸钾( )的过程如图所示:
已知:相同温度下, 的溶解度小于 。
回答问题:
(1) 中 的化合价为______。
(2)“反应1”中氧化剂与还原剂的物质的量之比为______。
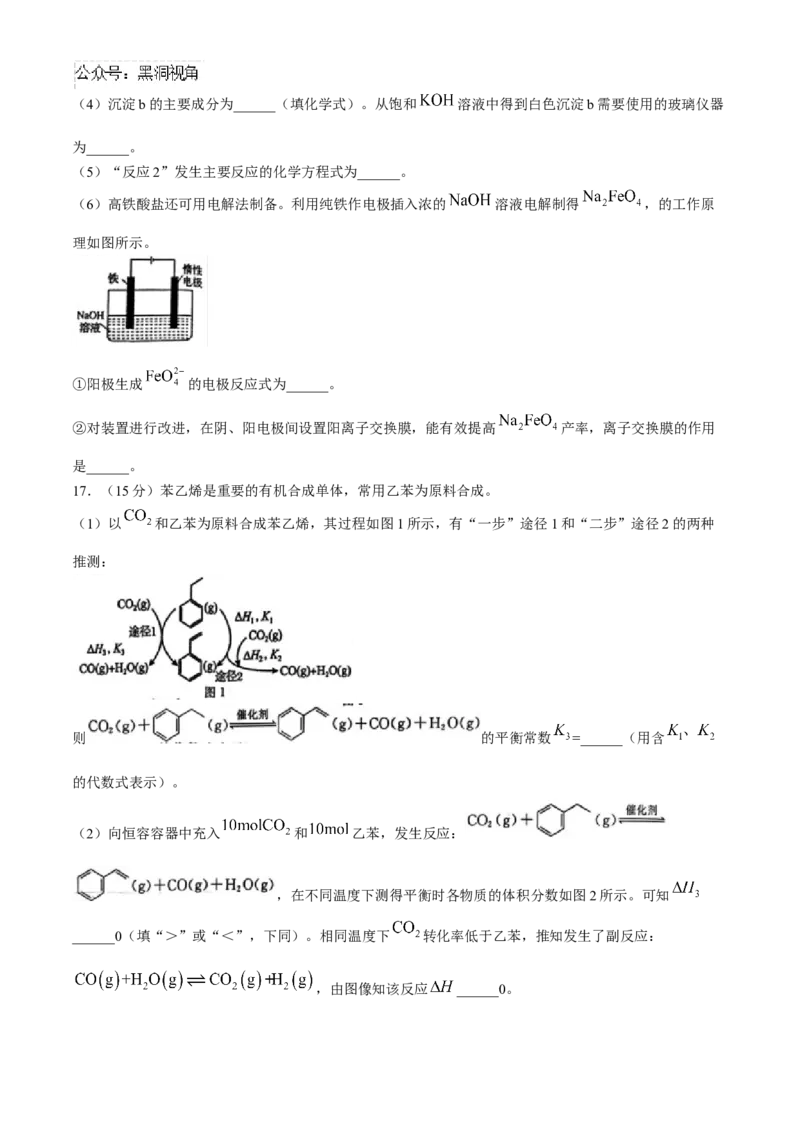
(3)“洗气”操作可选用的装置为______(填标号)。(4)沉淀b的主要成分为______(填化学式)。从饱和 溶液中得到白色沉淀b需要使用的玻璃仪器
为______。
(5)“反应2”发生主要反应的化学方程式为______。
(6)高铁酸盐还可用电解法制备。利用纯铁作电极插入浓的 溶液电解制得 ,的工作原
理如图所示。
①阳极生成 的电极反应式为______。
②对装置进行改进,在阴、阳电极间设置阳离子交换膜,能有效提高 产率,离子交换膜的作用
是______。
17.(15分)苯乙烯是重要的有机合成单体,常用乙苯为原料合成。
(1)以 和乙苯为原料合成苯乙烯,其过程如图1所示,有“一步”途径1和“二步”途径2的两种
推测:
则 的平衡常数 =______(用含
的代数式表示)。
(2)向恒容容器中充入 和 乙苯,发生反应:
,在不同温度下测得平衡时各物质的体积分数如图2所示。可知
______0(填“>”或“<”,下同)。相同温度下 转化率低于乙苯,推知发生了副反应:
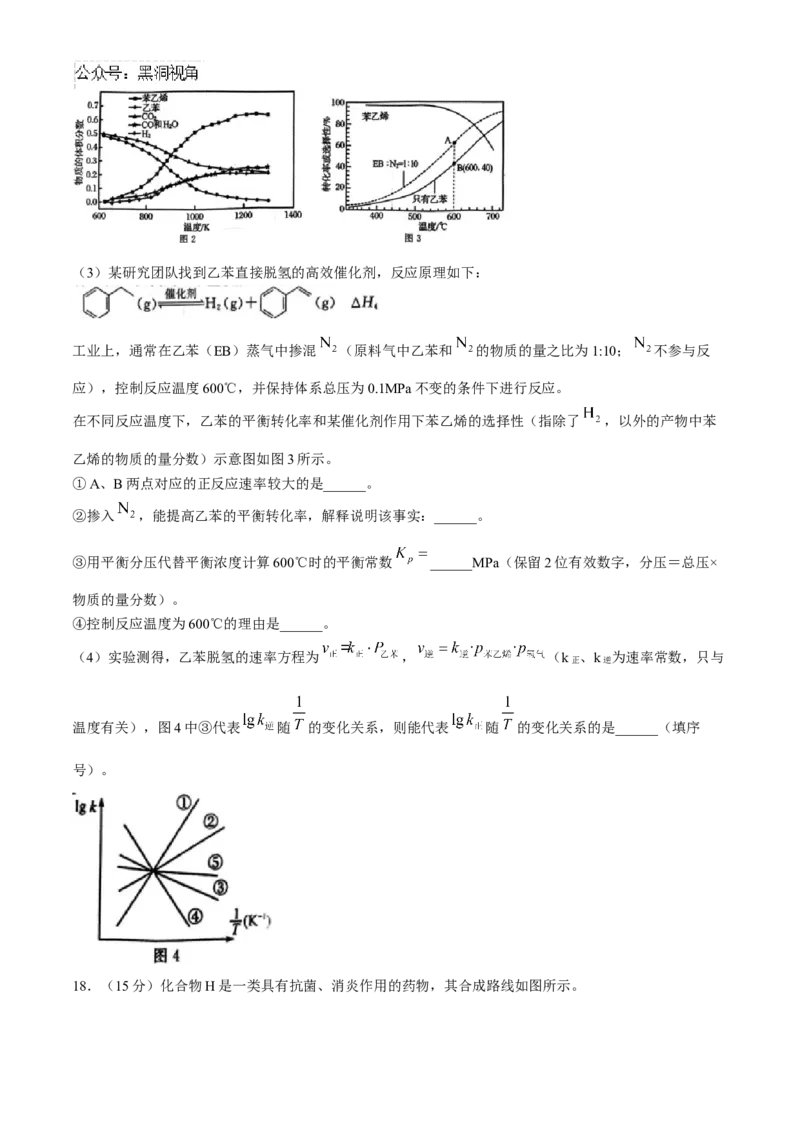
,由图像知该反应 ______0。(3)某研究团队找到乙苯直接脱氢的高效催化剂,反应原理如下:
工业上,通常在乙苯(EB)蒸气中掺混 (原料气中乙苯和 的物质的量之比为1:10; 不参与反
应),控制反应温度600℃,并保持体系总压为0.1MPa不变的条件下进行反应。
在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了 ,以外的产物中苯
乙烯的物质的量分数)示意图如图3所示。
①A、B两点对应的正反应速率较大的是______。
②掺入 ,能提高乙苯的平衡转化率,解释说明该事实:______。
③用平衡分压代替平衡浓度计算600℃时的平衡常数 ______MPa(保留2位有效数字,分压=总压×
物质的量分数)。
④控制反应温度为600℃的理由是______。
(4)实验测得,乙苯脱氢的速率方程为 , (k 、k 为速率常数,只与
正 逆
温度有关),图4中③代表 随 的变化关系,则能代表 随 的变化关系的是______(填序
号)。
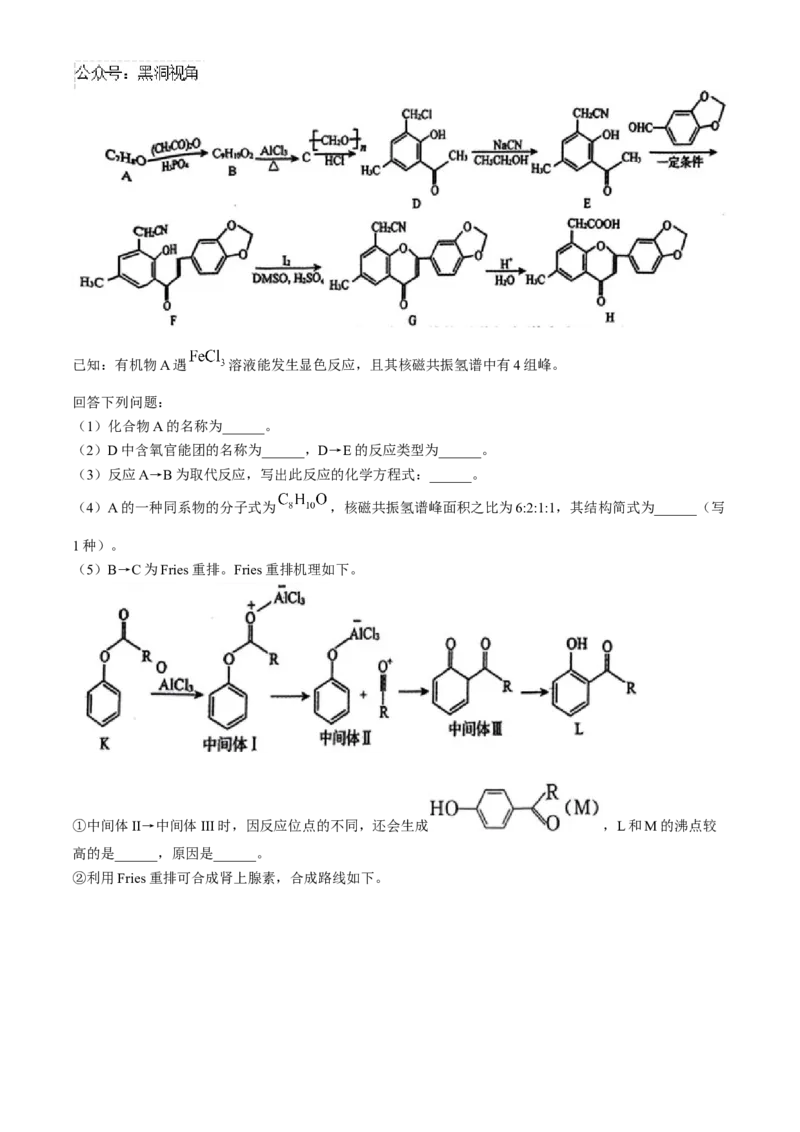
18.(15分)化合物H是一类具有抗菌、消炎作用的药物,其合成路线如图所示。已知:有机物A遇 溶液能发生显色反应,且其核磁共振氢谱中有4组峰。
回答下列问题:
(1)化合物A的名称为______。
(2)D中含氧官能团的名称为______,D→E的反应类型为______。
(3)反应A→B为取代反应,写出此反应的化学方程式:______。
(4)A的一种同系物的分子式为 ,核磁共振氢谱峰面积之比为6:2:1:1,其结构简式为______(写
1种)。
(5)B→C为Fries重排。Fries重排机理如下。
①中间体II→中间体III时,因反应位点的不同,还会生成 ,L和M的沸点较
高的是______,原因是______。
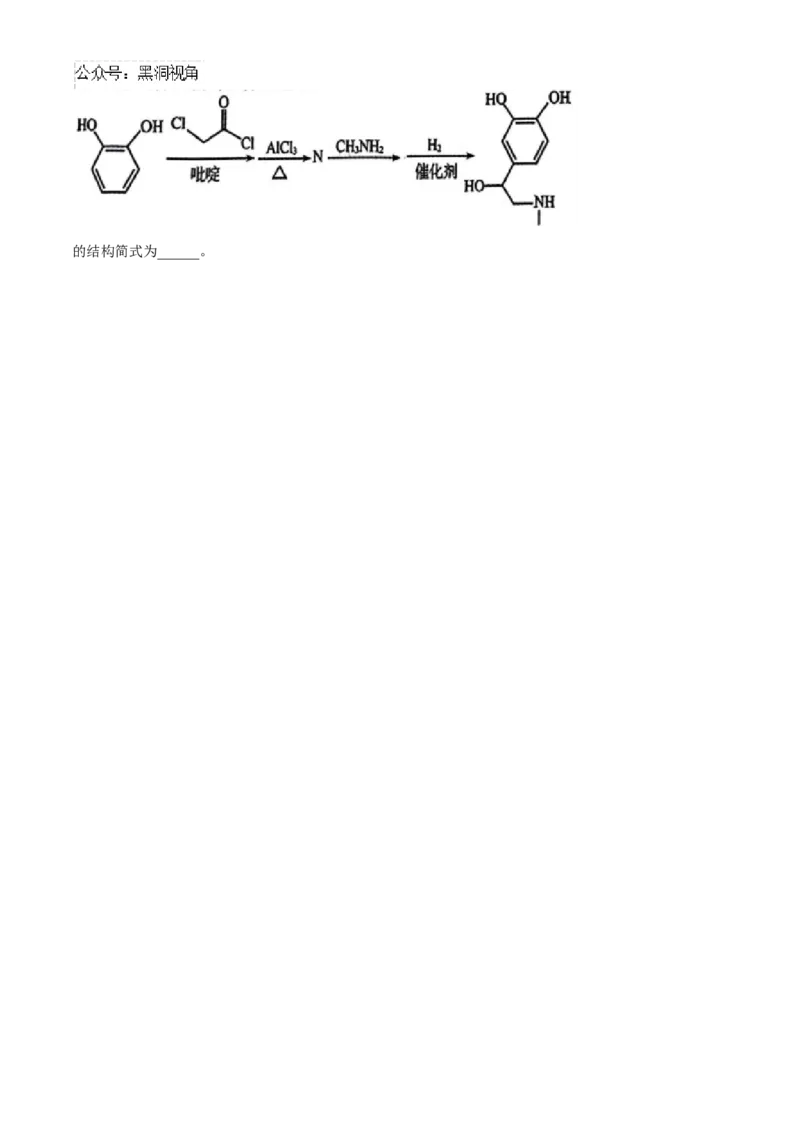
②利用Fries重排可合成肾上腺素,合成路线如下。的结构简式为______。2025 新高考单科模拟综合卷(三)
化学·参考答案
1.A高温结构陶瓷由氧化物或氮化物组成,其中主要成分有氧化铝、氧化锆、氧化硼等,不含硅酸盐,A
错误;水性涂料是用水作溶剂或者作分散介质的涂料,以水作为稀释剂,对人体比较健康,而油性涂料则
是以香蕉水或者天拿水作为稀释剂,含有二甲苯等有害致癌物质,B正确;推广使用风能、太阳能等新能
源能够减少 等温室气体的排放,C正确;稀土元素被称为“冶金工业的维生素”,合金中加入适量稀
土金属,能大大改善合金性能,D正确。
2.C 的电子式: ,A错误; 分子的球棍模型: ,B错误; 的原子序数为
33,基态 原子的电子排布式为 ,C正确;反式聚异戊二烯的结构简式为
D错误。
3.A溴易挥发且有毒,取用液溴时,需戴手套和护目镜,在通风梪中进行,A正确;钠、钾、白磷等物质,
不能随意丢弃,未用完应放回原试剂瓶,B错误;碳酸钡可溶于胃酸,误食钡盐不能通过服用纯碱溶液解
毒,C错误; 以上的水会导致烫伤,应先用酒精擦洗,再用温水冲洗,D错误。
4.C豆浆的凝固过程属于胶体的聚沉,没有发生氧化还原反应,A不符合题意;含氟牙育预防龋齿涉及难
溶电解质间的转化,不属于氧化还原反应,B不符合题意;植物油氢化即稙物油与氢气发生加成反应,属
于氧化还原反应,C符合题意;明矾中 水解使溶液呈酸性,可用于清除铜镜表面的铜锈[主要成分为
],不属于氧化还原反应,D不符合题意。
5.D已知固体 中只含 和 ,不含 ,故 和 混合固体中含
的数目小于 ,A错误; 的还原性大于 ,向溶液中通入适量 ,氯气优先氧化 ,当有
被氧化时, 已全部被氧化,故转移电子总数为 ,B错误;铁为阳极,电极反应式为
与 发生氧化还原反应生成 和 ,其离子方程式为
,得关系式: ,则理论上电路中每通过6mol电子,阳极区生成 ,被还原的重铬酸根离子的数目为 ,C错误;
由题干信息可知, 中含有 键,则 中含 键的数目为
,D正确。
6.C 的原子序数为75, 处在第六周期第VIIB族,即Re位于d区,A正确;同一周期元素,其第
一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,但H
的s轨道为半充满稳定结构,第一电离能比碳略大,则M中元素第一电离能大小顺序是 ,B正
确;M中N原子均采用 杂化,C错误;M中五元环含有大 键 I,即五元环 电子数为6,D正确。
7.B由题干N的结构简式可知,N中含有苯环和羧基,其余烃基均为饱和烃基,故其与苯甲酸结构相似,
组成上相差6个 ,故互为同系物,A正确;同时连有4个互不相同的原子或原子团的碳原子为手性碳
原子,结合题干信息M的结构简式可知,M分子中存在1个手性碳原子,即连有羟基的碳原子,B错误;
由题干图示信息可知,Y的结构中含有苯环和酮羰基平面结构,根据单键可以任意旋转可知,Y分子中最
多有11个碳原子(同时连有2个甲基的碳原子最多只能有一个碳原子与之共面)共平面,C正确;由题干
图示信息可知,X的苯环上一元取代的同分异构体有邻、间、对3种,D正确。
8.C 基态R原子核外有14种不同运动状态的电子,R是 是原子序数依次增大的前四
周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,则W是 是 的原子
序数为X与R的原子序数之和,Y是 。一般情况下,同周期元素从左到右,电负性逐渐增大,则电负
性: ,同主族元素从上到下,电负性逐渐减小,则电负性:O>S,故电负性: ,
A错误;元素的非金属性越强,其简单氢化物越稳定,非金属性: ,则简单氢化物的稳定性:
,B错误;镁比较活泼,工业上采用电解法冶炼镁,铁的活泼性相对较弱,工业上采用热还原
法冶炼铁,两者冶炼方法不同,C正确;由元素推断可知,该橄榄石为硅酸盐,则其晶体中存在硅氧四面
体结构,D错误。
9.D 和 溶液中阴离子不同,应控制阴离子相同,探究 和 的催化效果,A错误;发生反应: ,且 溶液过量,反应后加KSCN溶液为血红色,
检验铁离子不能证明反应存在限度,应控制氯化铁溶液不足,B错误;苯酚溶液中加入几滴 溶液,
发生显色反应,生成配合物,没有元素化合价发生改变,故与氧化还原反应无关,C错误;已知 溶
液由于 水解而呈酸性, 溶液由于碳酸氢根水解大于电离而呈碱性,故将
溶液和 溶液混合,由于 与 发生了双水解反
应: ,生成红褐色沉淀和气体,D正确。
10.D含砷废水中主要含有 和硫酸及少量 、 等,加入 溶液将 转化为
沉淀,过滤后向滤液中加入 和 溶液,调节 沉-As得到 和
,向滤渣中加入水调浆后通入 还原得到 ,过滤后的滤液经过一系列操
作得到 。“沉铁”时需要使铁盐完全沉淀而铜离子不沉淀,调pH的范围是 ,A正确;由
分析可知,“滤渣2”主要成分为 和 ,B正确;“还原”过程中 和
发生氧化还原反应生成 和 ,根据得失电子守恒和原子守恒配平化学方程
式为 ,C正确;“还原”后过
滤得到的滤液中含有 转化为 的过程中一定涉及化学变化,D错误。
11.A由题干信息可知,1个 晶胞中含有 个La,每个H结合4个H形成类似
的结构独立存在,含有 个H原子,La和H的个数比为1:10,晶体 中 ,A错误;由
的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H原子,若以顶点La研
究,与之最近的H原子有8个,则La的配位数为8,B正确;由晶胞结构可知,每个H结合4个H形成类
似 的结构,H和H之间的最短距离变小,则晶体中H和H的最短距离: ,C正确:晶体 中含有 个La,由化学式可知,其中含有8个H原子,则晶体 的密度为
,D正确。
12.D 反应过程中发生氮氮非极性键的断裂、氢氧极性键的断裂、氮氢极性键的形成,A错误;根据元
素守恒,生成 消耗 ,B错误;生成II的方程式为
,II为 ,C错误;反应历程中化学反应速率最慢的反应是
和 、 生成I的反应,方程式为 ,D正确。
13.D由图可知,锌为活泼金属,失去电子发生氧化反应,a为负极、b为正极,则c为阴极、d为阳极。
由分析可知,d电极为电解池的阳极,A正确; 电池总反应为锌和二氧化氮反应生成亚硝酸锌:
,B正确;c极区为阴极区,亚硝酸根离子发生还原反应生成 ,溶液碱性增
强,故溶液的pH升高,C正确:c极区为阴极区,亚硝酸根离子发生还原反应生成 ,电子转移为
,则电路中转移 时,理论上能得到 ,D错误。
14.B 由图1知, 的 ,
,
故 ,A正确;
时,可能有 生成,根据物料守恒,溶液中
,故 不一定等于 ,
B错误;从图2可以看出 、 时,该点位于曲线I和曲线II的下方,不会产生碳酸镁沉淀或氢氧化镁沉淀,C正确; 时,溶液中主要含碳微粒是 ,
,时,该点位于曲线II的上方,生成碳酸镁沉淀,D正确。
15.(1)恒压滴液漏斗(1分)
(2)防止生成的格氏试剂与水反应(1分)
(3)C(1分)
(4)保持反应物局部浓度较大,有利于引发反应 防止正溴丁烷的浓度较大,发生偶联反应(各2分)
(5)控制反应物的滴加速度,使用冷水浴(1分)
(6)产生的乙醚蒸气可排出装置中的空气(2分)
(7)A(2分)
(8)48.3%(2分)
16.(1)+6(1分)
(2)1:5(2分)
(3)AD(填对1个得1分,填错不得分,共2分)
(4) (1分) 烧杯、玻璃棒、漏斗(填对但不全得1分,填错不得分,共2分)
(5) (2分)
(6)(1) (2分)
(2)避免 在阴极上被还原(2分)
17.(1) (2分)
(2)> >(各1分)
(3)①B(2分)
②正反应方向气体分子数增加,加入氮气稀释,相当于起减压的效果(2分)
③0.019(3分)
④600℃时,乙苯的转化率和苯乙烯的选择性均较高;温度过低,反应速率慢,转化率低;温度过高,选
择性下降,高温还可能使催化剂失活,且能耗大(2分)
(4)④(2分)
18.(1)对甲基苯酚(或4-甲基苯酚)(2分)
(2)(酚)羟基和酮羰基(2分) 取代反应(1分)(5)①M(1分)L能形成分子内氢键,M无法形成分子内氢键,分子内氢键使得L的沸点降低,与M
的沸点相差较大(答案合理即可)(2分)
②