文档内容
2024/2025学年度第二学期联盟校期中学情调研检测高二年级
化学参考答案及评分标准
第Ⅰ卷 (选择题 共39分)
一、单项选择题:(本大题共13个小题,每小题3分,共39分.)
1 2 3 4 5 6 7
B D B D B C A
8 9 10 11 12 13
D A D A C C
第Ⅱ卷 (非选择题 共 61分)
14.(共15分)
(1)100 mL容量瓶 (2分)
(2) 3d104s¹(2分)
(3)① CuO+HSO=CuSO+HO (2分)
2 4 4 2
② 充当氧化剂;搅拌溶液,加快反应速率 (共2分,答对其中一点给1分)
(4)随着Cl-浓度的增大,CuCl与Cl-反应生成可溶于水的离子[CuCl]- (2分)
2
(5) 25.00 mL溶液中:n(KCrO)=0.020 0 mol·L-1×20.00×10-3 L=4×10-4 mol(1
2 2 7
分)
n(CuCl)=n(Fe2+)=6n(KCrO)=2.4×10-3 mol(2分)
2 2 7
CuCl的质量分数为×100%=95.52% (2分)
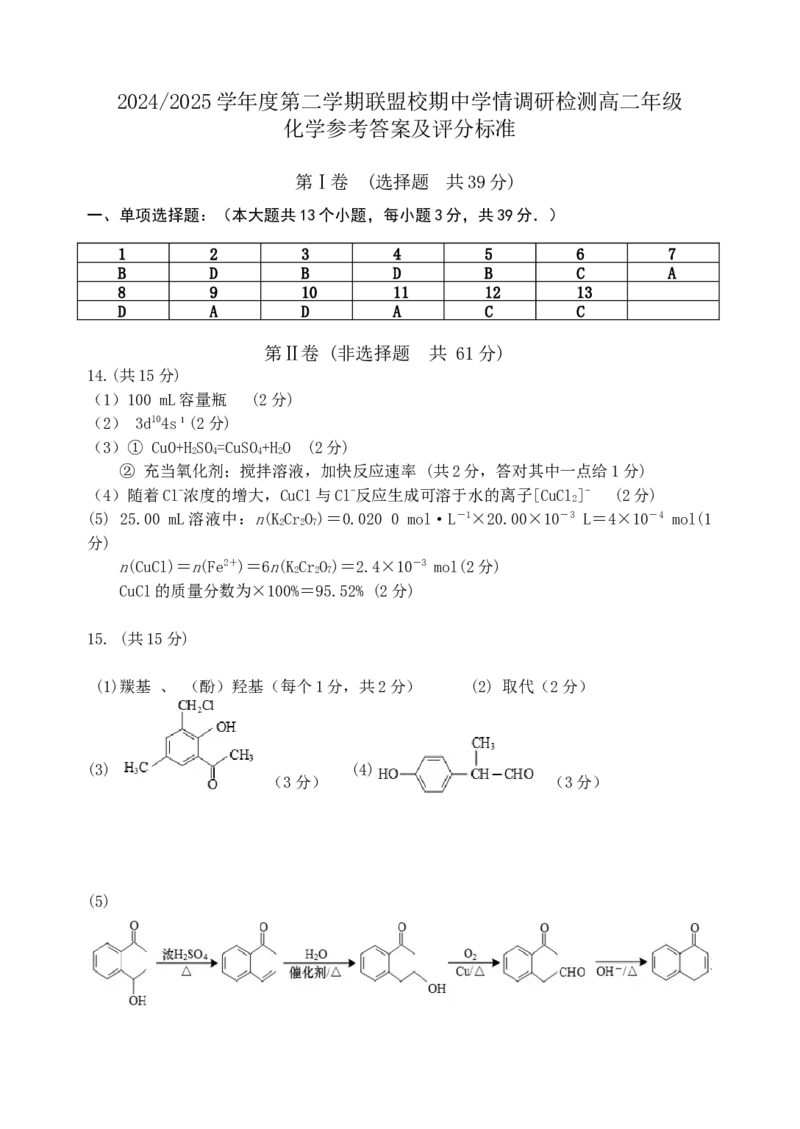
15. (共15分)
(1)羰基 、 (酚)羟基(每个1分,共2分) (2) 取代(2分)
(3) (4)
(3分) (3分)
(5)或
(共5分)
16. (共16分)
(1) ClO- + CO(NH
2
)
2
+ 2OH- === Cl-+ N2H4 .H
2
O + CO3 2- (3分)
(2) N2H4 .H
2
O 易被NaClO氧化 (2分)
(3) ①OH- (2分)
②ClO- +2e-+HO === Cl-+ 2OH- (3分)
2
(4) ①配位键 (1分)
②加入蒸馏水稀释水合肼溶液至3.0~3.25 mol·L-1(1分),加入适量氢氧
化钠固体,(1分)边搅拌边逐滴加入铜氨废液,加热使其充分反应,(1
分)同时用2 mol·L-1的硫酸吸收反应中放出的NH3,(1分)直至溶液中
无气泡产生,停止滴加。(1分) (每点1分,共5分)
17. (共15分)
(1) ① -759.8(2分) ② BC(2分)
(2) ① 4NH+4NO+O=====4N+6HO (3分)
3 2 2 2
② NH 中N和V—O—H中的H形成N…H—O氢键;NH 中H和V=O中的O形成N
3 3
—H…O氢键(2分)
(3) ① 反应温度较低时,反应速率慢(1分)。此时空速越大,反应气体与催化剂
的接触时间越短,反应不够充分,NO 转化率越低(1分)。空速越小,反应气
x
体与催化剂的接触时间长,反应充分,NO 转化率越高(1分) (共3分,答
x
对其中一点给1分)
② 高于350 ℃时,温度升高,催化剂活性下降;NH 与O 反应生成了NO(共3
3 2 x
分,答对其中一点即给2分;两点都答对即给3分。)