文档内容
2023~2024 学年度高三年级第四次模拟
化 学
注意事项:
1.本卷满分100分,考试时间75分钟。答题前,先将自己的姓名、准考证号填写在试题卷
和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写
在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和
答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
5.可能用到的相对原子质量:
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学和生活、科技、社会发展息息相关,下列说法正确的是( )。
A.建筑材料石膏的主要成分 是弱电解质
B.医用外科口罩使用的材料聚丙烯,不能使酸性高锰酸钾溶液褪色
C.成都大运会的奖牌“蓉光”的绶带为织纹精细的蜀锦.蜀锦的主要成分是纤维素
D.我国建造的“海基一号”成功从深海开采石油和天然气水合物,天然气属于新能源
2.下列化学用语表示正确的是( )。
A.基态硒原子的电子排布式:
B,甲醛的电子式:
C.邻羟基苯甲醛分子内氢键示意图:
D.Cl—Cl形成的p-p 键模型:
3.设 为阿伏加德罗常数的值,下列说法不正确的是( )。
A.标准状况下,11.2L由 和 组成的混合气体中含氢原子数目为
学科网(北京)股份有限公司B.标准状况下,44.8L NO和 反应后的分子数小于
C.0.1mol HCl与足量 完全反应时,生成的 分子数目为
D.常温下,1L pH=9的 溶液中,水电离出的 数目为
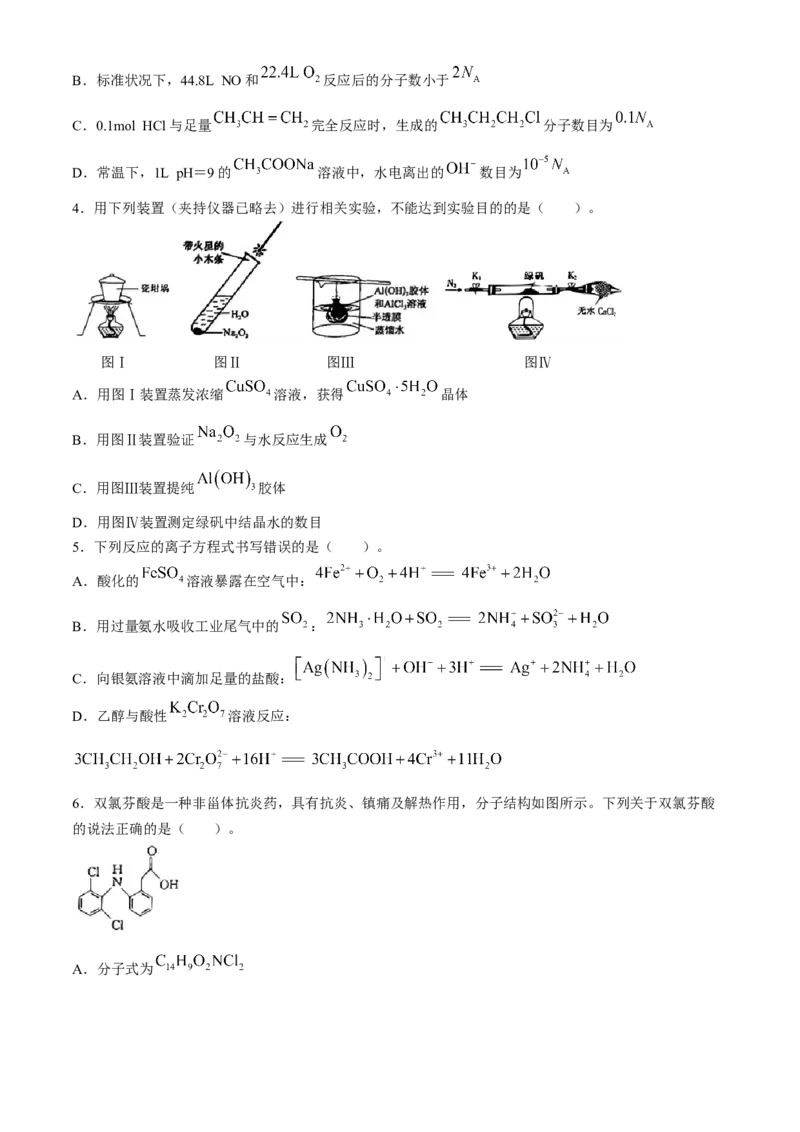
4.用下列装置(夹持仪器已略去)进行相关实验,不能达到实验目的的是( )。
图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
A.用图Ⅰ装置蒸发浓缩 溶液,获得 晶体
B.用图Ⅱ装置验证 与水反应生成
C.用图Ⅲ装置提纯 胶体
D.用图Ⅳ装置测定绿矾中结晶水的数目
5.下列反应的离子方程式书写错误的是( )。
A.酸化的 溶液暴露在空气中:
B.用过量氨水吸收工业尾气中的 :
C.向银氨溶液中滴加足量的盐酸:
D.乙醇与酸性 溶液反应:
6.双氯芬酸是一种非甾体抗炎药,具有抗炎、镇痛及解热作用,分子结构如图所示。下列关于双氯芬酸
的说法正确的是( )。
A.分子式为
学科网(北京)股份有限公司B.1mol该有机物最多能与 发生加成反应
C.分子中碳原子的杂化方式有 、sp两种
D.能与 溶液反应制得水溶性更好的双氯芬酸钠
7.下列有关物质结构的说法正确的是( )。
A.键角:
B. 的相对分子质量比 的大,故 比 稳定
C. 中的配体是 ,该配体中 键与 键的数目之比是
D.比较Fe和Mn的第三电离能,可得 大于
8.CuH是为数不多常温下存在的氢化物,能与盐酸反应放出气体。将次磷酸 加入 溶液
中,加热到50℃,制备出红棕色的难溶物CuH,反应后的溶液是磷酸和硫酸的混合物。下列说法正确的是
( )。
A.上述制备反应中CuH是氧化产物
B.参加反应的 与 的物质的量之比为
C.还原性:
D.CuH只具有还原性
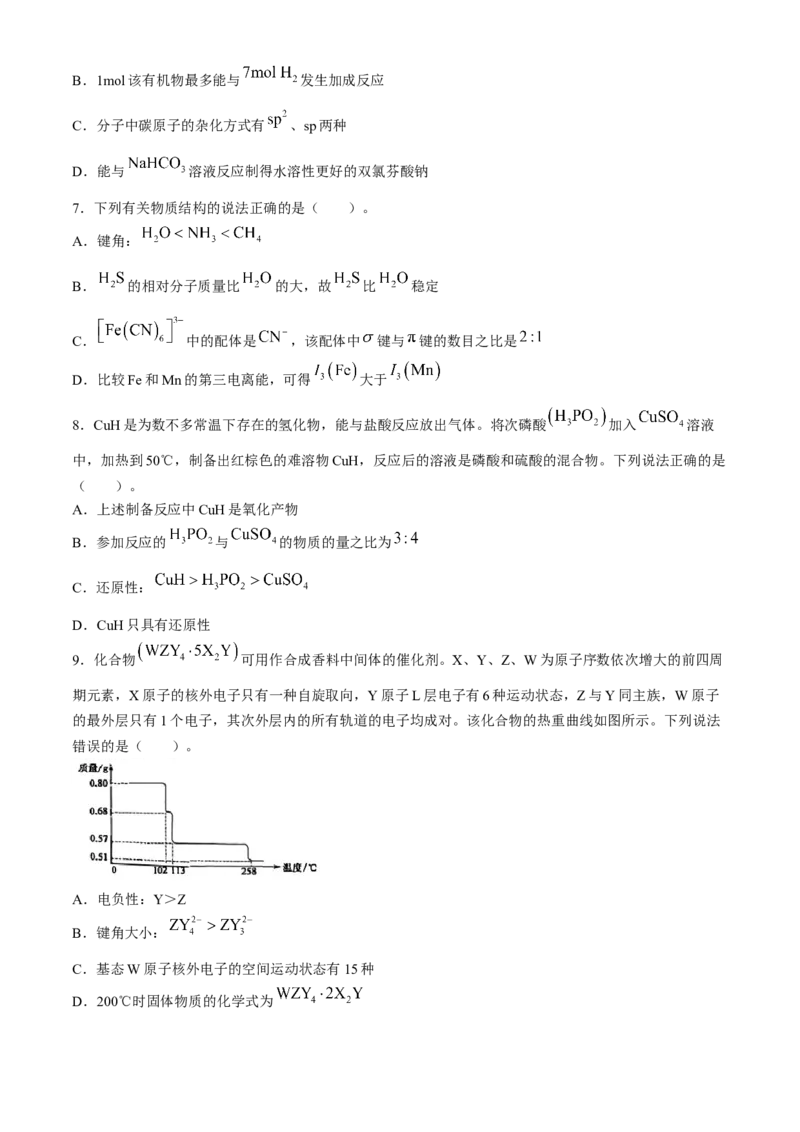
9.化合物 可用作合成香料中间体的催化剂。X、Y、Z、W为原子序数依次增大的前四周
期元素,X原子的核外电子只有一种自旋取向,Y原子L层电子有6种运动状态,Z与Y同主族,W原子
的最外层只有1个电子,其次外层内的所有轨道的电子均成对。该化合物的热重曲线如图所示。下列说法
错误的是( )。
A.电负性:Y>Z
B.键角大小:
C.基态W原子核外电子的空间运动状态有15种
D.200℃时固体物质的化学式为
学科网(北京)股份有限公司10.下列实验操作和现象及所得到的结论均正确的是( )。
选项 实验操作和现象 结论
A
将新制氯水光照一段时间.用pH计测溶液pH变小
光照能促进HClO的电离
将白色固体溶解,滴加足量稀盐酸,将样品产生的气
B 该白色固体为亚硫酸盐
体通入品红溶液,品红褪色
向等浓度、等体积的 中分别加入等浓度、等体 的催化效果比 好
C
积的 溶液和 溶液,前者产生气泡速率
快
将银和 溶液与铁和 、
D 形成原电池,铁作负极
溶液用盐桥连接组成原电池,连通后
铁电极附近溶液产生蓝色沉淀
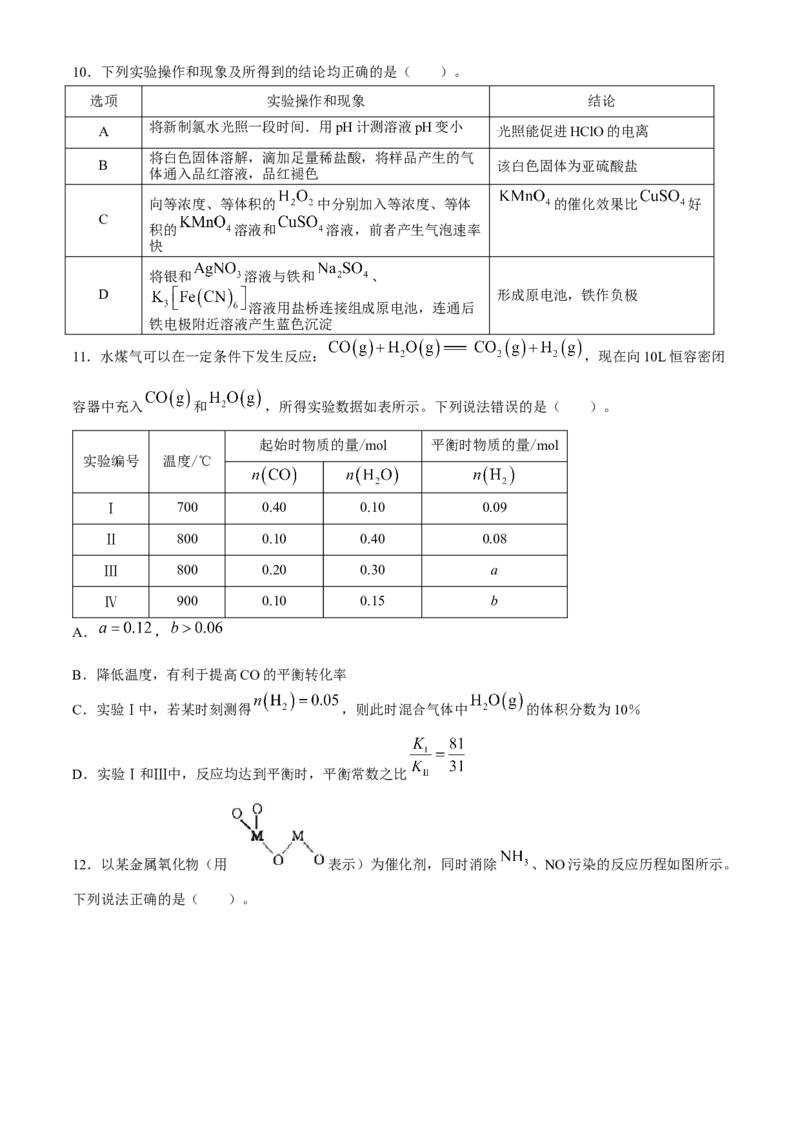
11.水煤气可以在一定条件下发生反应: ,现在向10L恒容密闭
容器中充入 和 ,所得实验数据如表所示。下列说法错误的是( )。
起始时物质的量/mol 平衡时物质的量/mol
实验编号 温度/℃
Ⅰ 700 0.40 0.10 0.09
Ⅱ 800 0.10 0.40 0.08
Ⅲ 800 0.20 0.30 a
Ⅳ 900 0.10 0.15 b
A. ,
B.降低温度,有利于提高CO的平衡转化率
C.实验Ⅰ中,若某时刻测得 ,则此时混合气体中 的体积分数为10%
D.实验Ⅰ和Ⅲ中,反应均达到平衡时,平衡常数之比
12.以某金属氧化物(用 表示)为催化剂,同时消除 、NO污染的反应历程如图所示。
下列说法正确的是( )。
学科网(北京)股份有限公司A.上述反应历程中没有涉及非极性键的断裂和形成
B.在相同条件下,NO比 更易与M成键
C.若X为常见的非金属单质,则反应⑤可能为
D.通过定量测定发现,反应历程中物质Ⅳ含量最少,其原因可能是反应③为慢反应,反应④为快反应
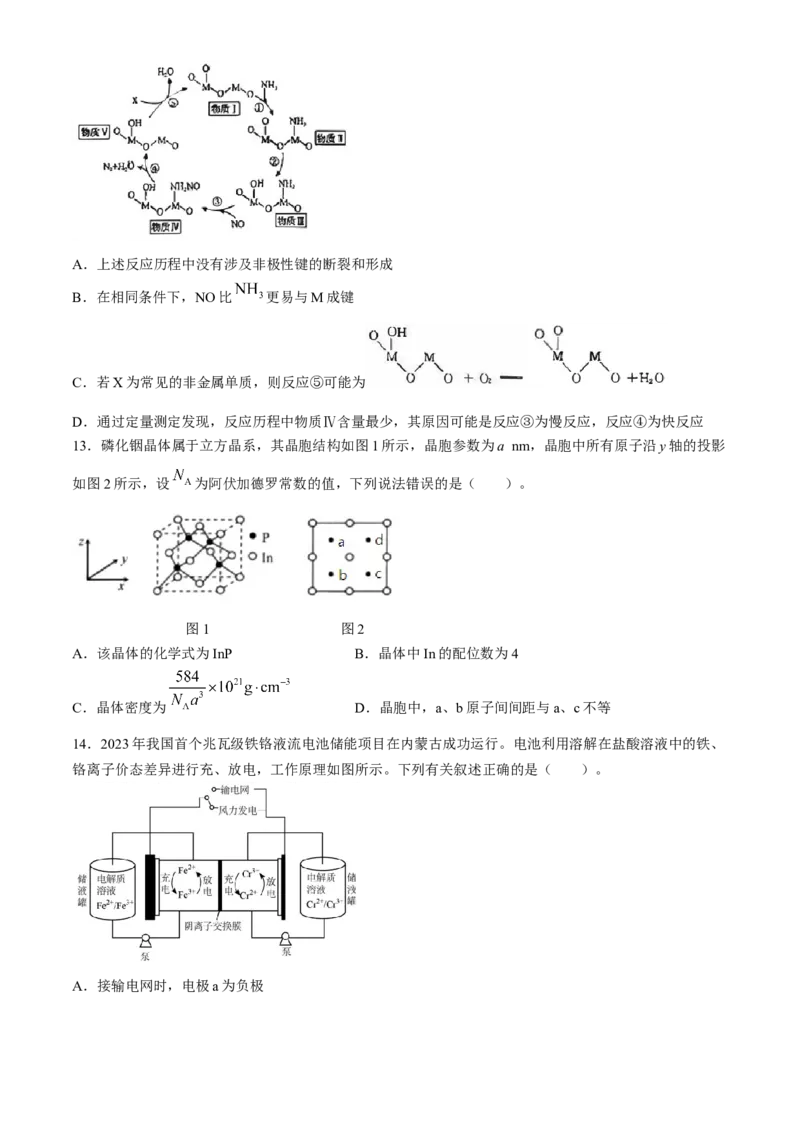
13.磷化铟晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为a nm,晶胞中所有原子沿y轴的投影
如图2所示,设 为阿伏加德罗常数的值,下列说法错误的是( )。
图1 图2
A.该晶体的化学式为InP B.晶体中In的配位数为4
C.晶体密度为 D.晶胞中,a、b原子间间距与a、c不等
14.2023年我国首个兆瓦级铁铬液流电池储能项目在内蒙古成功运行。电池利用溶解在盐酸溶液中的铁、
铬离子价态差异进行充、放电,工作原理如图所示。下列有关叙述正确的是( )。
A.接输电网时,电极a为负极
学科网(北京)股份有限公司B.阳极在充电过程中可能会产生
C.充电时,阳极的电极反应为
D.放电时,每 被氧化,电池中有 通过交换膜向b极转移
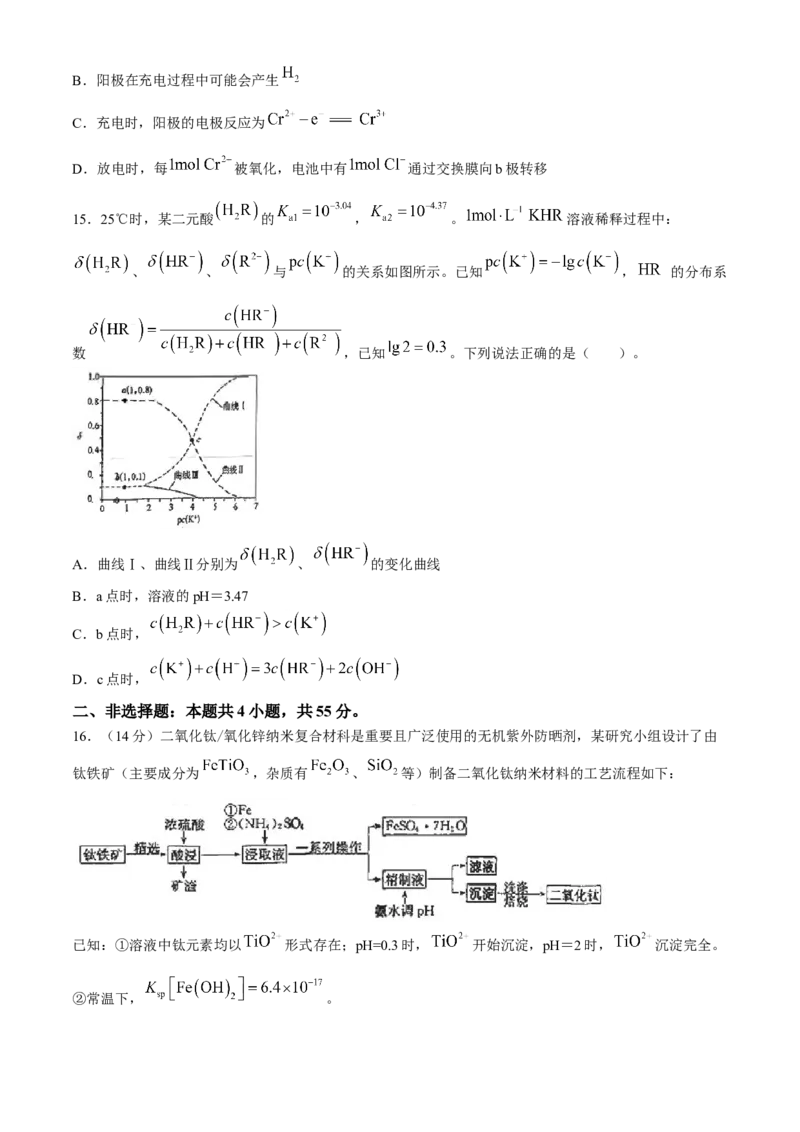
15.25℃时,某二元酸 的 , 。 溶液稀释过程中:
、 、 与 的关系如图所示。已知 , 的分布系
数 ,已知 。下列说法正确的是( )。
A.曲线Ⅰ、曲线Ⅱ分别为 、 的变化曲线
B.a点时,溶液的pH=3.47
C.b点时,
D.c点时,
二、非选择题:本题共4小题,共55分。
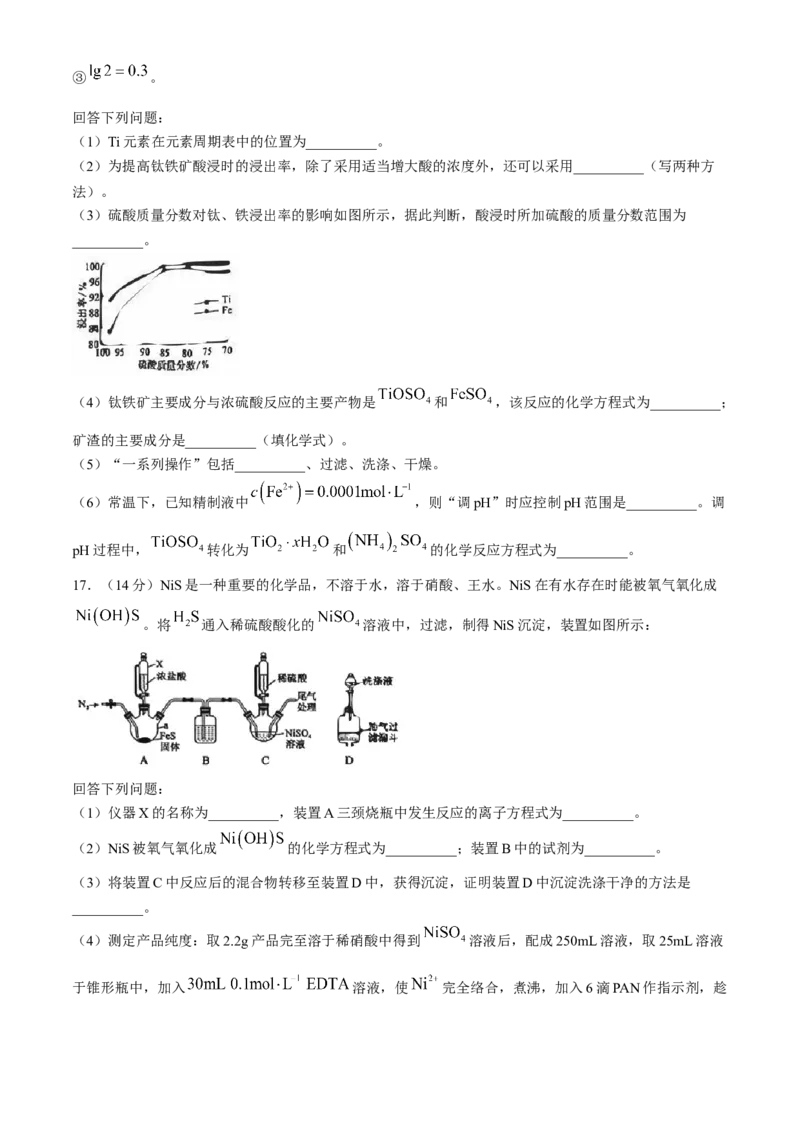
16.(14分)二氧化钛/氧化锌纳米复合材科是重要且广泛使用的无机紫外防晒剂,某研究小组设计了由
钛铁矿(主要成分为 ,杂质有 、 等)制备二氧化钛纳米材料的工艺流程如下:
已知:①溶液中钛元素均以 形式存在;pH=0.3时, 开始沉淀,pH=2时, 沉淀完全。
②常温下, 。
学科网(北京)股份有限公司③ 。
回答下列问题:
(1)Ti元素在元素周期表中的位置为__________。
(2)为提高钛铁矿酸浸时的浸出率,除了采用适当增大酸的浓度外,还可以采用__________(写两种方
法)。
(3)硫酸质量分数对钛、铁浸出率的影响如图所示,据此判断,酸浸时所加硫酸的质量分数范围为
__________。
(4)钛铁矿主要成分与浓硫酸反应的主要产物是 和 ,该反应的化学方程式为__________;
矿渣的主要成分是__________(填化学式)。
(5)“一系列操作”包括__________、过滤、洗涤、干燥。
(6)常温下,已知精制液中 ,则“调pH”时应控制pH范围是__________。调
pH过程中, 转化为 和 的化学反应方程式为__________。
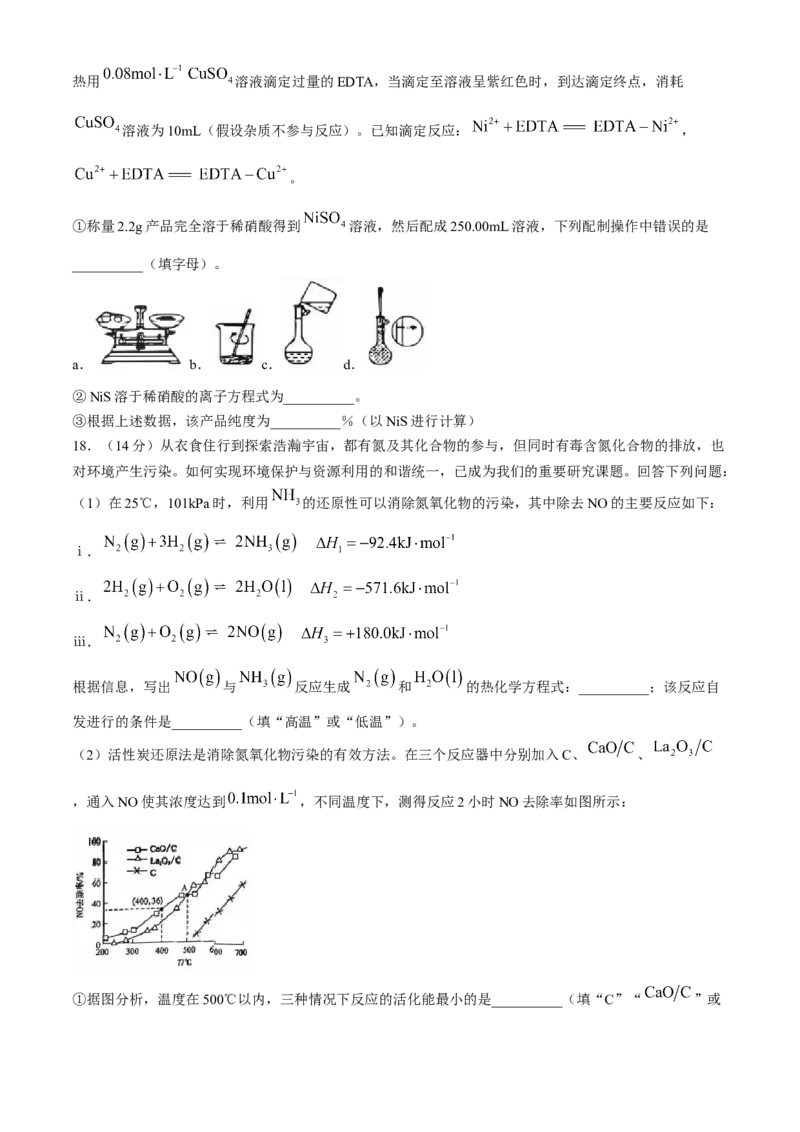
17.(14分)NiS是一种重要的化学品,不溶于水,溶于硝酸、王水。NiS在有水存在时能被氧气氧化成
。将 通入稀硫酸酸化的 溶液中,过滤,制得NiS沉淀,装置如图所示:
回答下列问题:
(1)仪器X的名称为__________,装置A三颈烧瓶中发生反应的离子方程式为__________。
(2)NiS被氧气氧化成 的化学方程式为__________;装置B中的试剂为__________。
(3)将装置C中反应后的混合物转移至装置D中,获得沉淀,证明装置D中沉淀洗涤干净的方法是
__________。
(4)测定产品纯度:取2.2g产品完至溶于稀硝酸中得到 溶液后,配成250mL溶液,取25mL溶液
于锥形瓶中,加入 溶液,使 完全络合,煮沸,加入6滴PAN作指示剂,趁
学科网(北京)股份有限公司热用 溶液滴定过量的EDTA,当滴定至溶液呈紫红色时,到达滴定终点,消耗
溶液为10mL(假设杂质不参与反应)。已知滴定反应: ,
。
①称量2.2g产品完全溶于稀硝酸得到 溶液,然后配成250.00mL溶液,下列配制操作中错误的是
__________(填字母)。
a. b. c. d.
②NiS溶于稀硝酸的离子方程式为__________。
③根据上述数据,该产品纯度为__________%(以NiS进行计算)
18.(14分)从衣食住行到探索浩瀚宇宙,都有氮及其化合物的参与,但同时有毒含氮化合物的排放,也
对环境产生污染。如何实现环境保护与资源利用的和谐统一,已成为我们的重要研究课题。回答下列问题:
(1)在25℃,101kPa时,利用 的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:
ⅰ.
ⅱ.
ⅲ.
根据信息,写出 与 反应生成 和 的热化学方程式:__________;该反应自
发进行的条件是__________(填“高温”或“低温”)。
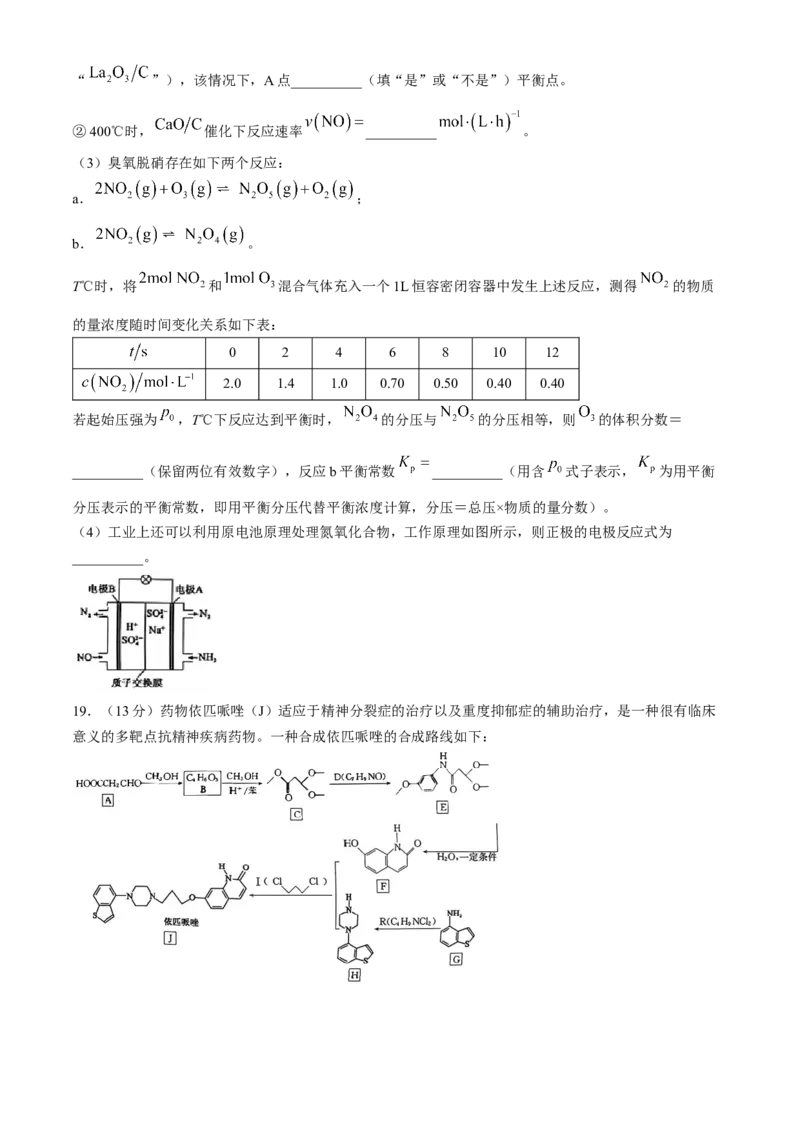
(2)活性炭还原法是消除氮氧化物污染的有效方法。在三个反应器中分别加入C、 、
,通入NO使其浓度达到 ,不同温度下,测得反应2小时NO去除率如图所示:
①据图分析,温度在500℃以内,三种情况下反应的活化能最小的是__________(填“C”“ ”或
学科网(北京)股份有限公司“ ”),该情况下,A点__________(填“是”或“不是”)平衡点。
②400℃时, 催化下反应速率 __________ 。
(3)臭氧脱硝存在如下两个反应:
a. ;
b. 。
T℃时,将 和 混合气体充入一个1L恒容密闭容器中发生上述反应,测得 的物质
的量浓度随时间变化关系如下表:
0 2 4 6 8 10 12
2.0 1.4 1.0 0.70 0.50 0.40 0.40
若起始压强为 ,T℃下反应达到平衡时, 的分压与 的分压相等,则 的体积分数=
__________(保留两位有效数字),反应b平衡常数 __________(用含 式子表示, 为用平衡
分压表示的平衡常数,即用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)工业上还可以利用原电池原理处理氮氧化合物,工作原理如图所示,则正极的电极反应式为
__________。
19.(13分)药物依匹哌唑(J)适应于精神分裂症的治疗以及重度抑郁症的辅助治疗,是一种很有临床
意义的多靶点抗精神疾病药物。一种合成依匹哌唑的合成路线如下:
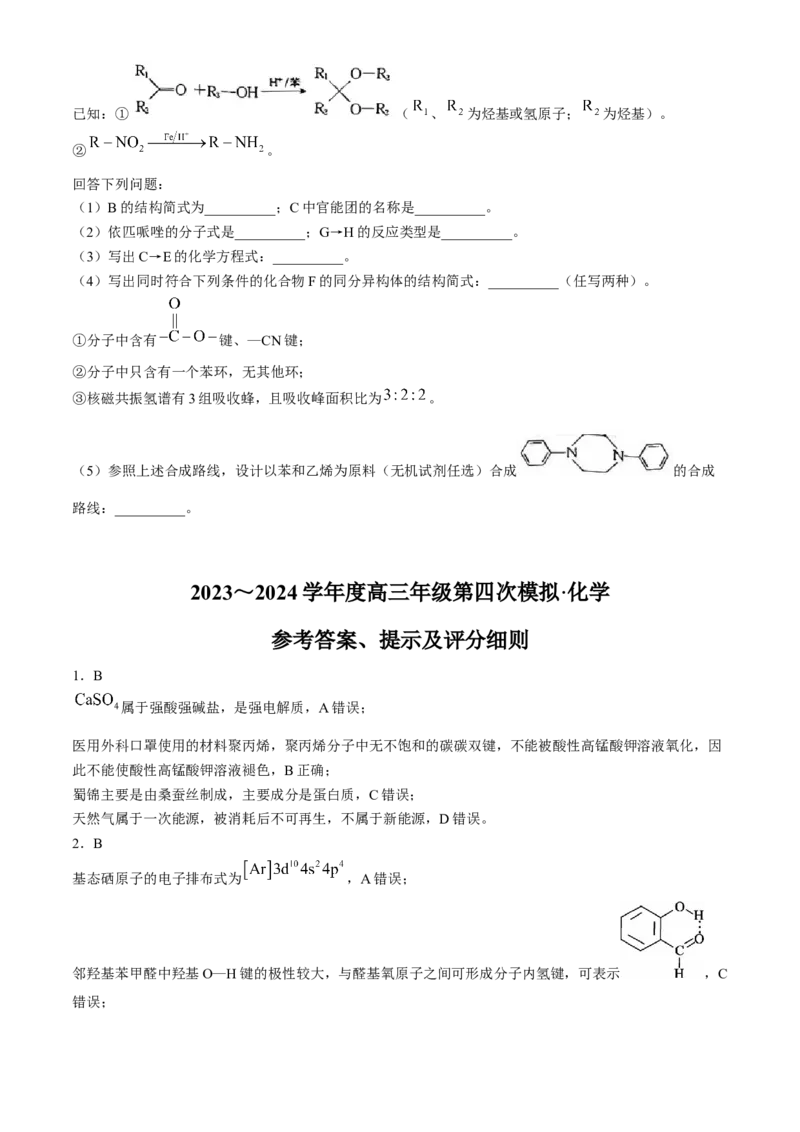
学科网(北京)股份有限公司已知:① ( 、 为烃基或氢原子; 为烃基)。
② 。
回答下列问题:
(1)B的结构简式为__________;C中官能团的名称是__________。
(2)依匹哌唑的分子式是__________;G→H的反应类型是__________。
(3)写出C→E的化学方程式:__________。
(4)写出同时符合下列条件的化合物F的同分异构体的结构简式:__________(任写两种)。
①分子中含有 键、—CN键;
②分子中只含有一个苯环,无其他环;
③核磁共振氢谱有3组吸收蜂,且吸收峰面积比为 。
(5)参照上述合成路线,设计以苯和乙烯为原料(无机试剂任选)合成 的合成
路线:__________。
2023~2024 学年度高三年级第四次模拟·化学
参考答案、提示及评分细则
1.B
属于强酸强碱盐,是强电解质,A错误;
医用外科口罩使用的材料聚丙烯,聚丙烯分子中无不饱和的碳碳双键,不能被酸性高锰酸钾溶液氧化,因
此不能使酸性高锰酸钾溶液褪色,B正确;
蜀锦主要是由桑蚕丝制成,主要成分是蛋白质,C错误;
天然气属于一次能源,被消耗后不可再生,不属于新能源,D错误。
2.B
基态硒原子的电子排布式为 ,A错误;
邻羟基苯甲醛中羟基O—H键的极性较大,与醛基氧原子之间可形成分子内氢键,可表示 ,C
错误;
学科网(北京)股份有限公司Cl—Cl形成的p-p 键模型为 ,D错误。
3.C
1分子 和 中含氢原子数目均为4,标准状况下,11.2L由 和 组成的混合气体为
0.5mol,含氢原子数目为 ,A正确;
标况下44.8L NO和 反应后生成 ,有一部分 转化为 ,因此反应后的分子数小于
,B正确;
丙烯与氯化氢发生加成反应可以生成1-氯丙烷和2-氯丙烷,则无法计算0.1mol氯化氢与丙烯生成1-氯丙烷
的分子数目,C错误;
1L pH=9的 溶液中, 都来源于水的电离, ,
所以水电离出的 数目为 ,D正确。
4.A
溶液的蒸发浓缩应在蒸发皿中进行,A符合题意;
过氧化钠与水反应生成氢氧化钠和氧气,若带火星的小木条复燃可证明有氧气生成,B不符合题意;
胶体粒子不能透过半透膜,溶液可以,C不符合题意;
在硬质玻璃管中隔绝空气加热绿矾,利用氮气将产生气体排至无水氯化钙,通过无水氯化钙的质量变化测
定绿矾中结晶水的数目,D不符合题意。
5.C
酸化的 溶液暴露在空气中,离子方程式为 ,A正确;
过量氨水吸收二氧化硫,两者反应生成铵根离子、亚硫酸根离子和水,B正确;
向银氨溶液中滴加足量的盐酸,离子方程式:
,C错误;
乙醇被酸性重铬酸钾氧化为乙酸,即
,D正确。
6.D
由有机物的结构简式可知,其分子式为 ,A错误;
1mol该有机物最多能与 发生加成反应,B错误;
学科网(北京)股份有限公司分子中碳原子的杂化方式有 、 两种,C错误;
双氯芬酸钠为盐,易溶于水,D正确。
7.A
已知 、 、 中心原子均为 杂化,且 的中心原子O周围含有2对孤电子对, 分
子中心原子N周围有1对孤电子对,孤电子对对成键电子对的排斥最大,键角: ,A
正确;
非金属性O>S,则简单氢化物的稳定性: ,B错误;
中C和N之间是三键,1个 中有1个 键和2个 键,则该配体中 键与 键的数目之比是
1∶2,C错误;
的价电子排布式为 ,处于半满状态,较稳定,而 的3d能级是半满状态,相对稳定,再失去
1个电子变为 时是 的不稳定状态,故 较难失去电子,故第三电离能: ,
D错误。
8.B
次磷酸 与 溶液发生反应的化学方程式为
。上述制备反应中CuH中铜元素和氢元素
的化合价均降低,是还原产物,参加反应的 与 的物质的量之比为3∶4,A错误,B正确;
还原性:还原剂>还原产物,故还原性: ,C错误;
CuH中含有 价的H, 价的Cu,既具有还原性,又具有氧化性,D错误。
9.D
由题意可知,X为H,Y为O,Z为S,W为Cu,化合物 为 。电负性:O
>S,A正确;
中S原子价层电子对数为 ,S原子是 杂化,且没有孤电子对, 中S原
子价层电子对数为 ,S原子是 杂化,且含有1个孤电子对,孤电子对越多,键角
学科网(北京)股份有限公司越小,则键角大小: ,B正确;
基态Cu原子核外电子的空间运动状态有15种,C正确;
分析热重曲线可知,200℃和113℃时的产物相同,可根据113℃的样品质量确定脱水产物,设113℃时产
物的化学式为 ,则有 ,
由比例关系 ,解得n≈4,所以200℃时该固体的化学式为 ,D错误。
10.D
新制氯水含HClO,光照下次氯酸分解生成HCl和氧气,溶液酸性增强,pH变小,不是光照促进HClO的
电离造成的,A错误;
将白色固体溶解,滴加足量稀盐酸,将样品产生的气体通入品红溶液,品红褪色,该白色固体可能含有
、 、 等,B错误;
向等浓度、等体积的 中加入 溶液, 将 氧化为 ,而不是作催化剂,C错误;
连通后形成了原电池,铁电极附近溶液产生蓝色沉淀,说明铁极失去电子,发生氧化反应生成亚铁离子,
D正确。
11.A
根据实验Ⅰ和Ⅱ数据,可知升高温度,平衡时氢气的物质的量减少,故平衡逆向移动,该反应为放热反应,
降低温度,有利于提高CO的平衡转化率,B正确;
该反应是气体的物质的量不变的反应,若某时刻测得 ,则 的物质的量为0.05mol,
故此时混合气体中 的体积分数 %=10%,C正确;
K只与温度有关,根据实验Ⅰ的数据,到平衡时, 、 、
、 ,
,
同理可算出 ,则 ,故 ,D正确;
根据平衡常数可列三段式求出 ,与实验Ⅲ相比,实验Ⅳ起始时反应物的物质的量减半,若温度相
学科网(北京)股份有限公司等,则 ,实验Ⅳ的温度较实验Ⅲ高,故 ,A错误。
12.D
上述反应历程中有非极性键 键的形成,A错误;
由反应①、②可知,在相同条件下, 优先与金属M原子形成配位键,其原因是 中N原子周围电
子云密度比NO中N原子周围电子云密度大,更易提供孤电子对与M形成配位键,B错误;
若X为常见的非金属单质,根据反应前后原子守恒判断,X为 ,
则反应⑤可能为4 ,C错误;
反应历程中,慢反应的生成物在体系中含量低,快反应的反应物在体系中含量低,反应过程中物质Ⅳ含量
最少,其可能原因是反应③为慢反应,反应④为快反应,D正确。
13.D
由晶胞结构可知该晶体的化学式为InP,A正确;
In位于P原子围成的四面体空隙,In的配位数为4,B正确;
晶体密度为 ,C正确;
由晶胞结构可知a、b原子间间距与a、c原子间间距均为面对角线的 ,D错误。
14.D
由图可知,充电时,左侧 失去电子发生氧化反应生成 ,a为阳极;右侧 得到电子发生还原
反应生成 ,b为阴极。接输电网时,该装置为原电池,a为正极,b为负极,A错误;
阴极在充电过程中, 可能得到电子发生还原生成 ,B错误;
充电时,左侧为阳极、右侧为阴极,则左侧 失电子生成 ,阳极的电极反应为 ,
C错误;
放电时,负极上每 被氧化生成 ,则转移1mol电子,则电池中有 通过交换膜
向b(负)极转移,D正确。
15.B
溶液稀释过程中,随着水的加入,因存在电离平衡 和水解平衡
学科网(北京)股份有限公司, 的分布系数开始时变化不大且保持较大,故曲线Ⅱ为 的变
曲线,曲线Ⅰ为 的变化曲线,A错误;
a点时, ,则 , 、 ,
, ,则pH=3.47,B正确;
b点时,根据物料守恒有 ,故 ,C错误;
c点时, ,即 ,
根据电荷守恒有 ,
,D错误。
16.(1)第四周期ⅣB族(1分)
(2)矿石粉碎、连续搅拌、适当升高温度(任选两种,其他合理答案均可,2分)
(3)80%~85%(2分)
(4) (浓) (2分) (1分)
(5)蒸发浓缩(1分) 冷却结晶(1分)
(6) (2分)
(2分)
17.(1)恒压滴液漏斗(1分) (1分)
(2) (2分) 饱和NaHS溶液(2分)
(3)取最后一次洗涤液少许试管中,加入 溶液,若无白色沉淀产生,则证明洗涤干净(2分)
(4)①ac(2分)
② (2分)
③91(2分)
18.(1) (2分) 低温(1
分)
(2)① (2分) 不是(1分) ②0.018(2分)
学科网(北京)股份有限公司(3)27%或0.27(2分,有效数字错0分) (2分)
(4) (2分)
19.(1) (2分) 酯基、醚键(2分)
(2) (1分) 取代反应(1分)
(3)
(4) 、 、 、 (任选两种,2分)
(5) (3分)
学科网(北京)股份有限公司