文档内容
2019年云南省初中学业水平考试化学试题
(全卷四大题,28小题;考试时间90分钟,满分100分)
用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 A1—27 Cl—35.5 Ca—40 Zn—65
第Ⅰ卷(选择题 共45分)
一、选择题(本大题共20小题,其中1~15小题,每小题2分,16~20小题,每小题3分,共45分。每小题只有
一个选项符合题意,多选、错选或不选均不得分)
1.下列变化属于化学变化的是
A.煤的燃烧 B.纺纱织布 C.矿石粉碎 D.铁水铸锅
2.下列图标,属于“国家节水标志”的是
A. B. C. D.
3.空气的成分按体积分数计算含量最多的是
A.稀有气体 B.CO C.O D.N
2 2 2
4.下列食物中,富含维生素的是
A.蔬菜 B.羊肉 C.米饭 D.牛油
5.农作物种植过程中常常需要施用化肥。下列化肥属于复合肥的是
A.NHNO B.KSO C.Ca(HPO) D.KNO
4 3 2 4 2 4 2 3
6.把少量的下列物质分别放入水中,充分搅拌,能形成溶液的是
A.面粉 B.蔗糖 C.花生油 D.泥土
7.“绿色发展”、“低碳生活”等理念逐渐深入民心,下列做法或认识与之不相符的是
A.在空旷的地方焚烧大量的废旧塑料 B.鼓励乘坐公交车或骑自行车出行
C.购物时提倡用布袋等环保袋代替塑料袋 D.植树造林
8.人体内一些液体的正常pH范围如下,其中呈酸性的是
A.血浆7.35~7.45 B.胃液0.9~1.5 C.胆汁7.1~7.3 D.胰液7.5~8.0
9.下列实验基本操作正确的是
A.取用液体药品 B.测定溶液的pH C.过滤 D.仪器的连接
——pH试纸
10.氮化铝(AlN)是一种新型陶瓷材料,其中氮元素的化合价是
A.-3 B.+2 C.+4 D.+5
11.变瘪的乒乓球放入热水中,能恢复原状。下列微观解释正确的是
A.分子质量增大 B.分子体积扩大 C.分子间间隔变大 D.分子个数增多
12.元素周期表中第118号元素是最新公布中文名称的元素,该元素相关信息如图所示。下列说法正确的是
A.该元素的元素符号为Uu B.该元素是金属元素
C.该元素原子的质子数为176 D.该元素的原子序数为118
118 Uuo
13.下列有关实验现象的描述中,正确的是
294
1A.打开盛有浓盐酸的试剂瓶,在瓶口观察到白烟
B.硫在氧气中燃烧,发出蓝紫色火焰
C.细铁丝在空气中燃烧,火星四射,生成黑色固 体
D.镁条在空气中燃烧发出耀眼的白光,生成氧化镁
14.下列粒子结构示意图,表示阴离子的是
A. B. C. D.
+12282 +8 26 +16288 +17287
15.下图是某汽车尾气净化装置中发生反应的微观示意图。下列说法正确的是
氢原子
氧原子
甲 乙 丙 丁 氮原子
催化剂
A.乙、丁属于氧化物 B.该反应的化学方程式为NO+NH======N+HO
2 2 2
C.甲物质由一个氧原子和一个氮原子构成 D.反应前后,原子种类、原子数目不变
16.人体摄入锌不足会引起多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌口服液来补锌。已知葡萄
糖酸锌的化学式为C H O Zn。下列说法正确的是
12 22 14
A.葡萄糖酸锌由碳、氢、氧、锌四种元素组成 B.葡萄糖酸锌中锌元素的质量分数最大
C.葡萄糖酸锌中碳、氢元素的质量比为12:22 D.葡萄糖酸锌的相对分子质量为455g
17.在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法不正确的
是
物质 a b c d
反应前的质量/g 40 5 16 15
反应后的质量/g x 5 30 26
A.b可能是催化剂 B.x的值等于15
C.该反应是分解反应 D.参加反应的c与d的质量比为15:13
18.下列有关实验方案设计正确的是
选项 实验目的 实验方案
A 配制6%的氯化钠溶液50g 称取3g氯化钾固体于47mL水中
取氢氧化钠溶液于烧杯中,滴入几滴酚酞溶
B 证明氢氧化钠溶液与稀盐酸能反应
液,振荡,再滴入稀盐酸至溶液变为无色
C 除去CaCl 溶液中的少量盐酸 加入适量的铁粉
2
D 除去CO 中含有的少量CO 点燃
2
19.甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是
①甲的溶解度随温度的升高而增大 溶解度/g
50 甲
②40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸 - (20,36)
40
乙
发溶剂三种方法
-
③20℃时,向125g溶质质量分数为20%的乙溶液中加入15g乙固体 30
-
并振荡,有固体不溶解 2 0 0 ─ ┴ ┴ 10 ─ ┴ 2 ─ 0 ┴ ─ 30 ┴ ─ 4 ┴ 0 ─
④将相同质量的甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶 -50 60
温度/℃
10
体的质量大
-
A.①② B.③④ C.①③④ D.②③④
220.下列说法和判断合理的是
①用作消毒剂的75%的医用酒精,是指每100体积的医用酒精中含75体积的乙醇
②某温度下,一定质量的氯化钠饱和溶液不能再溶解氯化钠固体,但还能继续溶解一定质量的氯化钾
③一定质量的某气体充分燃烧,生成2.2g二氧化碳和1.8g水,则该气体一定是一氧化碳和氢气的
混合物
气体质量m/g
④等质量的A、B两种物质,分别与等质量的同浓度的稀盐酸充分反应,过程
如图所示。若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,当反应结束 A
B
后只有一种固体剩余,则被消耗完的固体为碳酸钙
A.1条 B.2条 C.3条 D.4条 时间t/s
第Ⅱ卷 非选择题(共55分)
二、填空与简答题(本大题共5个小题,化学方程式每空2分,其余每空1分,共33分)
21.(6分)化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①镁元素 ;②三个氧原子 ;③五个二氧化硫分子 ;④两个氢氧根离子 。
(2)符号“3Ca2+”中的“3”表示 ,“2+”表示 。
22.(7分)化学不仅与我们的生产、生活密切相关,更是人类进步的关键。
(1)请从以下选项中选择适当物质的序号填空:a.生石灰 b.金刚石 c.食盐 d.稀有气体。
①可用来裁玻璃的是 ; ②可用来做干燥剂的是 ;
③可用作调味品的是 ; ④可用于填充霓虹灯的是 。
(2)化学元素与人体健康密切相关,下列说法正确的是 (填字母)。
A.人体中含量最高的常量元素是钙元素
B.过量摄入碘元素会引起甲状腺肿大
C.人体所需的元素从食物中摄取不足时,可以通过食品添加剂补充
D.微量元素钛、铝是人体的必需元素
(3)三大化石燃料是指煤、石油和 ,它们都是不可再生能源。
(4)扑灭森林火灾的有效方法之一,是将大火蔓延路线前的一片树木砍掉。其灭火原理是 。
23.(7分)水是一种重要的资源,爱护水资源,人人有责。
(1)如图所示,电解水的实验中,通电一段时间后,玻璃管a中收集到的气体是 ;通过实验可以得出
水是由 组成的。
(2)请列举一条日常生活中的节水措施 。 活塞— —活塞
(3)下列做法会造成水体污染的是 (填序号)。 a— —
b
①工业废水处理达标后排放 ②随意丢弃废旧电池
③提倡使用无磷洗衣粉 ④合理使用化肥和农药
(4)下列净化水的过程中,说法不正确的是 (填字母)。
A.活性炭可吸附水中的色素和有异味的物质
B.明矾可以使硬水转化为软水
C.自来水厂净化水的方法主要有沉淀、过滤、吸附、消毒杀菌
D.净水方法中,净化程度最高的是蒸馏
(5)日常生活中,常用 区分硬水和软水,实现硬水软化的简单方法是 。
324.(8分)金属及金属材料在生产、生活中有广泛的应用。
(1)近年来,我省多地纷纷开展文明城市创建工作,垃圾分类回收是其中一项重要举措。 某市街道垃圾桶
如右图所示,请回答下列问题: 塑料顶盖
①图中标识的物质,属于金属材料的是 (写出一种即可)。
铁质外筒 铝合金内筒
②使用铝合金做内筒的优点是 (写出一点即可)。
某品牌饮料的空易拉罐应收入 (填“可回收”或“不可
回收”)筒中。
③铁制品锈蚀的过程,实际上是铁制品跟空气中的 发生化
学反应的过程;除去铁制品表
面的铁锈可用稀盐酸,反应的化学方程式为 。
(2)将甲、乙、丙三种金属分别投入稀硫酸中,甲、丙表面有气泡产生,乙无明显现象; 若将甲放入丙的硫酸
盐溶液中,一段时间后,甲的表面有丙析出。由此推断这三种金属的活动性由强到弱的顺序是
。
(3)将一定质量的铁粉加入到Al(NO)、Cu(NO)、AgNO 三种物质的混合溶液中。 充分反应后过滤,得到滤
3 3 3 2 3
液和滤渣。下列有关说法正确的是 (填字母)。
A.若滤液为蓝色,则滤渣中一定有银,可能有 铜
B.若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO—
3
C.若滤液为浅绿色,则滤渣中一定含银、铜、铝
D.若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
25.(5分)推理和判断是学习化学的重要方法。
(1)A、B、C为初中化学常见的三种物质,它们之间的转化关系如图1 所示(“→”表示某一种物质经一步反
应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答下列问题:
①若A、B、C均含有同一种元素,B、C组成元素相同,C的固体俗称“干冰”,则B的化学式
是 。
②若A、B、C是含相同金属元素的化合物,B、C的水溶液为蓝色,三种物质相互间发生的反应均为
复分解反应,则A的化学式可能是 (写出一个即可)。 B
③若A、B、C均为碱,其中B易溶于水,C难溶于水,写出一个由B
A———→C
转化为C的化学方程式: 。 图1
(2)只含一种杂质的硫酸溶液M,加入足量的氢氧化钡溶液后,再加足量的稀盐酸,过程如图 2 所示。下列
判断合理的有 (填序号)。
沉淀的质量/g
①M中一定不含有碳酸钠
a b
②图中ab间(不含a、b两点)滴入酚酞溶液变红色
c
③bc段表示沉淀部分消失,无气泡产生
④c点后溶液中的溶质不少于两种 0 所加溶液的体
积 图2
三、实验与探究(本大题共2个小题,化学方程式每空2分,其余每空1分, 共16
分)
26.(9分)如图是实验室常用的部分实验装置,请按要求回答问题。
①
棉花
a b
—② 石蕊 澄清 4
试液— —石灰水A B C D E F
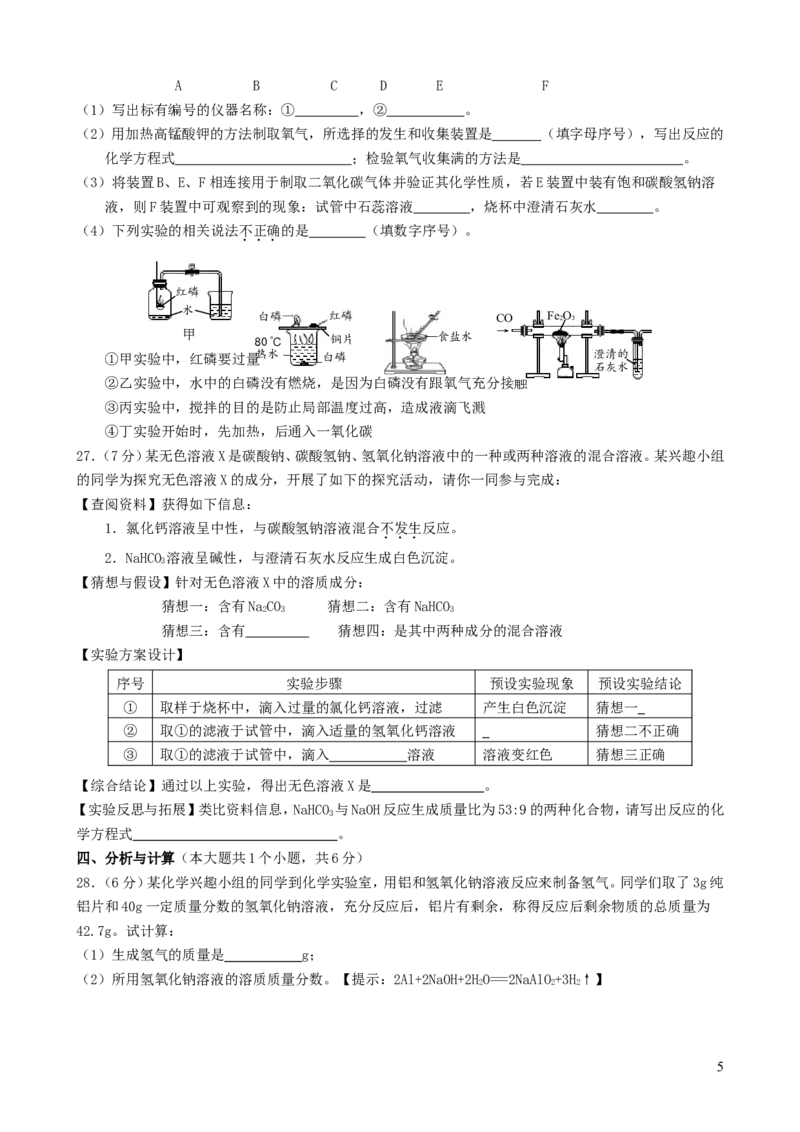
(1)写出标有编号的仪器名称:① ,② 。
(2)用加热高锰酸钾的方法制取氧气,所选择的发生和收集装置是 (填字母序号),写出反应的
化学方程式 ;检验氧气收集满的方法是 。
(3)将装置B、E、F相连接用于制取二氧化碳气体并验证其化学性质,若E装置中装有饱和碳酸氢钠溶
液,则F装置中可观察到的现象:试管中石蕊溶液 ,烧杯中澄清石灰水 。
(4)下列实验的相关说法不正确的是 (填数字序号)。
红磷
水
白磷一 红磷 CO Fe 2 O 3
甲 8 0 ℃ 乙 铜 片 丙 — 食 盐 水 → 丁
①甲实验中,红磷要过量热水 白磷 澄清的
石灰水
②乙实验中,水中的白磷没有燃烧,是因为白磷没有跟氧气充分接触
③丙实验中,搅拌的目的是防止局部温度过高,造成液滴飞溅
④丁实验开始时,先加热,后通入一氧化碳
27.(7分)某无色溶液X是碳酸钠、碳酸氢钠、氢氧化钠溶液中的一种或两种溶液的混合溶液。某兴趣小组
的同学为探究无色溶液X的成分,开展了如下的探究活动,请你一同参与完成:
【查阅资料】获得如下信息:
1.氯化钙溶液呈中性,与碳酸氢钠溶液混合不发生反应。
2.NaHCO 溶液呈碱性,与澄清石灰水反应生成白色沉淀。
3
【猜想与假设】针对无色溶液X中的溶质成分:
猜想一:含有NaCO 猜想二:含有NaHCO
2 3 3
猜想三:含有 猜想四:是其中两种成分的混合溶液
【实验方案设计】
序号 实验步骤 预设实验现象 预设实验结论
① 取样于烧杯中,滴入过量的氯化钙溶液,过滤 产生白色沉淀 猜想一
② 取①的滤液于试管中,滴入适量的氢氧化钙溶液 猜想二不正确
③ 取①的滤液于试管中,滴入 溶液 溶液变红色 猜想三正确
【综合结论】通过以上实验,得出无色溶液X是 。
【实验反思与拓展】类比资料信息,NaHCO 与NaOH反应生成质量比为53:9的两种化合物,请写出反应的化
3
学方程式 。
四、分析与计算(本大题共1个小题,共6分)
28.(6分)某化学兴趣小组的同学到化学实验室,用铝和氢氧化钠溶液反应来制备氢气。同学们取了3g纯
铝片和40g一定质量分数的氢氧化钠溶液,充分反应后,铝片有剩余,称得反应后剩余物质的总质量为
42.7g。试计算:
(1)生成氢气的质量是 g;
(2)所用氢氧化钠溶液的溶质质量分数。【提示:2Al+2NaOH+2HO===2NaAlO+3H↑】
2 2 2
52019年云南省初中学业水平考试化学参考答案及评分标准
说明:化学方程式书写时,化学式错一个不得分,配平、条件、状态不全总扣1分。
一、选择题(本大题共20小题,其中1~15小题,每小题2分,16~20小题,每小题3分,共45分。)
1~5:ABDAD 6~10:BABCA 11~15:CDBCD 16~20:ADBDB
二、填空与简答题(本大题共5个小题,化学方程式每空2分,其余每空1分,共33分)
21.(6分)(1)①Mg ②3O ③5SO ④2OH—
2
(2)三个钙离子 每个钙离子带两个单位的正电荷
22.(7分)(1)①b ②a ③c ④d (2)BC(少、多、错选不得分)
(3)天然气 (4)清除(或隔离)可燃物
23.(7分)(1)氢气(或H) 氢、氧两种元素 (2)洗菜水浇花(合理均可)
2
(3)② (4)B (5)肥皂水 煮沸
24.(8分)(1)①铁质外筒(或铝合金内筒) ②抗腐蚀性强(合理均可) 可回收
③水和氧气 FeO+6HCl===2FeCl+3HO (2)甲>丙>乙 (3)A
2 3 3 2
25.(5分)(1)①CO ②CuO(或CuSO,合理均可) ③2NaOH+CuSO===Cu(OH)↓+NaSO
4 4 2 2 4
(2)①②③④(少选不得分)
三、实验与探究(本大题共2个小题,化学方程式每空2分,其余每空1分,共16分)
26.(9分)(1)①试管 ②锥形瓶(错字、别字不得分) (2)AC(或AE)(少、多、错不得分)
2KMnOKMnO+MnO+O↑ 将带火星的木条放在集气瓶口(或E装置的a处),若木条复燃
4 2 4 2 2
说明已收集满 (3)变红 变浑浊 (4)④
27.(7分)猜想三:NaOH(或氢氧化钠)
6【实验方案设计】①正确 ②无明显现象 ③酚酞
【综合结论】碳酸钠和氢氧化钠(或NaCO 和NaOH)的混合溶液
2 3
【实验反思与拓展】NaHCO+NaOH===NaCO+HO
3 2 3 2
四、分析与计算(本大题共1个小题,共6分)
28.(6分)(1)0.3 1分
(2)解:设氢氧化钠溶液中溶质质量为x。 0.5分
2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
80 6
x 0.3g 1分
== 1分
x=4g 1分
所用氢氧化钠溶液的溶质质量分数为:×100%=10% 1分
答:所用氢氧化钠溶液的溶质质量分数为10%。 0.5分
7