文档内容
江苏省泰州中学2025~2026学年度第一学期期中考试
高二化学试题
(考试时间:75分钟;总分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Ca-40
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 高分子是生产生活中的常见物质。下列物质中不属于高分子的是
A. 油脂 B. 淀粉 C. 蛋白质 D. 酚醛树脂
2. 甲硫醇(CHSH)是合成蛋氨酸的重要原料。反应CHOH+HS――→CHSH+HO可用于甲硫醇的制备。下列
3 3 2 3 2
有关说法正确的是
A. Al3+的结构示意图为 B. HO的电子式为H+ H+
2
C. CHOH的沸点比CHSH低 D. CHOH和CHSH互为同系物
3 3 3 3
3. 实验室进行乙酸乙酯的制备。下列相关原理、装置及操作正确的是
A. 用装置甲混合乙醇与浓硫酸 B. 用装置乙制备乙酸乙酯
C. 用装置丙收集乙酸乙酯 D. 用装置丁提纯乙酸乙酯
4. 联氨(NH)为二元弱碱,在水中性质与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中
2 4
一种反应机理如图所示。下列说法正确的是
A. 微粒半径:r(Cu)> r(Cu2+) B. 电负性:χ(N)> χ(O)> χ(H)
C. 第一电离能:I(O)> I(N)> I(Cu) D. Cu元素位于元素周期表中的d区
1 1 1
阅读下列材料,完成5-7题:
CO 的资源化利用具有重要意义。光催化CO 还原的产物有HCOOH、CHOH、CHOH等。离子液体X(结构如
2 2 3 2 5
题5图)具有较强的吸附CO 的能力,能活化CO 和CHOH反应生成碳酸二甲酯(CHOCOOCH)。在高温高压、
2 2 3 3 3
催化剂下,利用CO 可合成尿素[CO(NH)]:
2 2 2
①2NH(g)+CO(g)=NHCOONH(l);②NHCOONH(l)=CO(NH)(l)+HO(l)
3 2 2 4 2 4 2 2 25. 下列说法正确的是
A. 碳有 、 、 等多种同素异形体
12C 13C 14C
6 6 6
B. X中碳原子轨道的杂化类型只有1种
C. 1 mol碳酸二甲酯中含有11 mol σ键
D. 反应①中断裂的化学键有极性键和非极性键。
题5图
6. 下列化学反应表示正确的是
A. 氨水吸收过量CO:OH−+CO=HCO
2 2
B. CO 和NH 反应生成尿素:2NH+CO――→CO(NH)+HO
2 3 3 2 2 2 2
C. CHCHOH和O 反应生成乙醛:CHCHOH+O ∆――→CHCHO+HO
3 2 2 3 2 2 3 2
D. CO 和CHOH反应生成碳酸二甲酯:CO+2CHOH=CHOCOOCH
2 3 2 3 3 3
7. 下列物质结构与性质不具有对应关系的是
A. 尿素晶体中所有原子共平面,尿素分子具有极性
B. X中的粒子都是带电荷的离子,X相对四氯化碳难挥发
C. HCOOH中O—H键的极性比HCO 的大,HCOOH酸性强于HCO
2 3 2 3
D. 甲醇和碳酸二甲酯形成分子间氢键,两者可形成共沸物
8. 冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别K+,其合成方法如下。下列说法不正确的是
A. 该反应为取代反应 B. a、b均可与NaOH溶液反应
C. c核磁共振氢谱有3组峰 D. c可增加KI在苯中的溶解度
9. 某抗凝血作用的药物Z可用下列反应合成,下列说法不正确的是
A. X分子中所有碳原子一定共平面 B. 1 mol Y水解,最多消耗3 mol NaOH
C. Z可以发生加成、氧化、取代反应 D. 可用酸性KMnO 溶液检验产品Z中是否含有X
4
10. 有机物M在碱性条件下可发生的反应如图所示。下列说法正确的是
A. M分子中酮羰基邻位甲基的C—H键极性较弱,易断键 B. N分子中含有3个手性碳原子
C. 1 mol N最多与2 mol H 发生加成反应 D. 该条件下还可能生成
211. 根据下列实验操作和现象所得到的结论正确的是
选项 实验操作及现象 实验结论
向试管中加5 mL乙醇、15 mL浓硫酸和几片碎瓷片,加热,将产
A 有CH 生成
2 4
生的气体通入酸性KMnO 溶液中,溶液褪色
4
向苯酚溶液中滴加几滴饱和溴水,充分振荡后无白色沉淀生
B 苯酚不与溴水反应
成
麦芽糖与稀HSO 共热后加 NaOH溶液调至碱性,再加入新制
2 4
C 麦芽糖已水解
Cu(OH) 并加热,产生砖红色沉淀
2
向试管中加入某卤代烃(CHCHX)和0.5 mol·L−1 NaOH溶液,加
3 2
D 热,向反应后的溶液中先加入硝酸酸化,再滴加AgNO 溶液, 卤代烃中X为溴原子
3
有浅黄色沉淀生成
12. 固体ZnA 可以催化CO 与环氧乙烷的衍生物转化为环状碳酸酯,可能的机理如下:
2 2
下列说法正确的是
A. CO 中的C提供孤电子对与Zn2+配位
2
B. 过程I、II中都有C—O σ键的断裂
C. 可用18O标记CO 探究过程I的机理
2
D. 反应后通过分液操作回收ZnA
2
13. 利用氢碘酸的还原性和碘的氧化性将5-羟甲基糠醛(HMF)歧化得到5-甲基糠醛(5-MF)和2,5-二甲酰基
呋喃(DFF),其反应机理如图所示。下列说法不正确的是
A. 过程①中HMF发生还原反应
B. 反应中每转移1 mol e−,消耗1 mol
HMF
C. 5-MF与DFF均不存在属于芳香族化合物的同分异构体D. 若以 为反应物,则歧化可得 和
二、非选择题:共4题,共61分。
14.(15分)有机物种类繁多,应用广泛。研究有机物的性质及合成机理具有重要意义。
(1)下列物质的酸性由强到弱的顺序是 ▲ (填序号)。(已知:—SOH结构为 )
3
① ② ③
(2)已知:i. ;
ii. 苯环上原有取代基对新取代基的位置有影响:甲基一般使新取代基在其邻对位,硝基使新
取代基在其间位。
依据题中信息及所学知识,以苯为原料制备 的合成路线流程图见下图。(无机试剂和两碳以
下的有机物任用)
①写出X的结构简式 ▲ 。
②写出 反应的化学方程式 ▲ 。
(3) 为稀硫酸催化下的离子型反应,其反应机理经历3
步转化,请将第2步转化补充完整。
第1步:
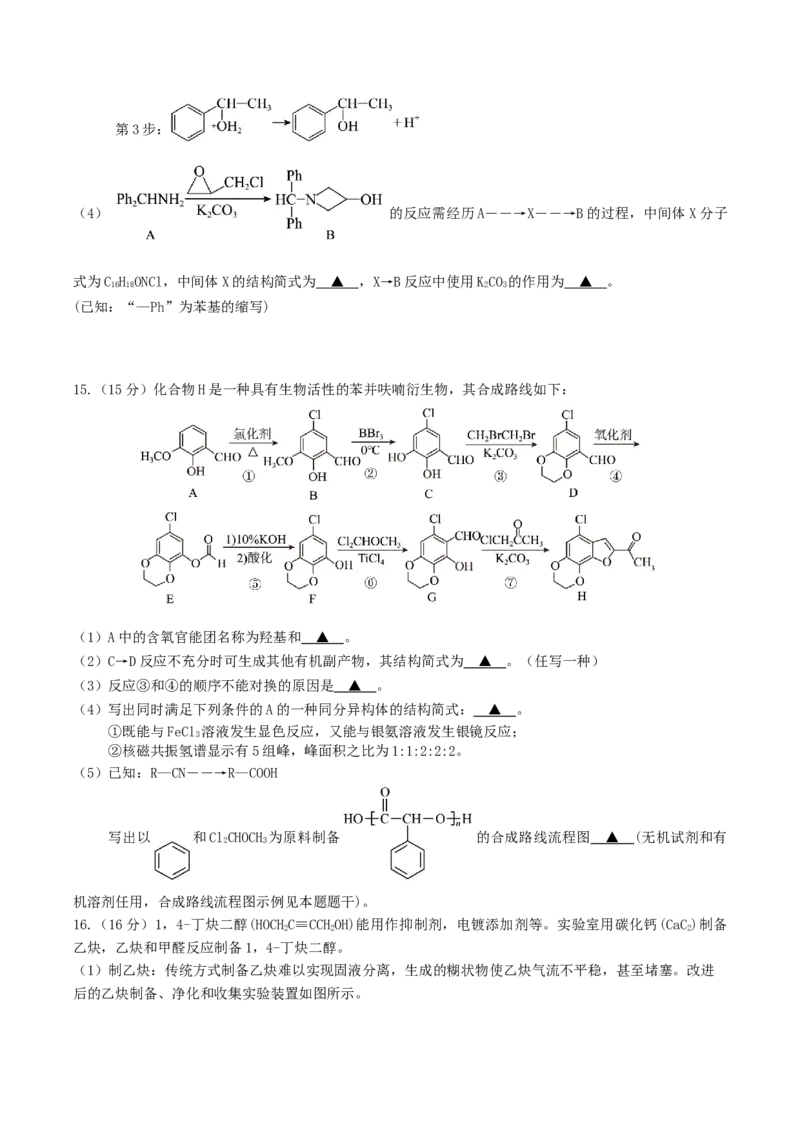
第2步: ▲ ;第3步:
(4) 的反应需经历A――→X――→B的过程,中间体X分子
式为C H ONCl,中间体X的结构简式为 ▲ ,X→B反应中使用KCO 的作用为 ▲ 。
16 18 2 3
(已知:“—Ph”为苯基的缩写)
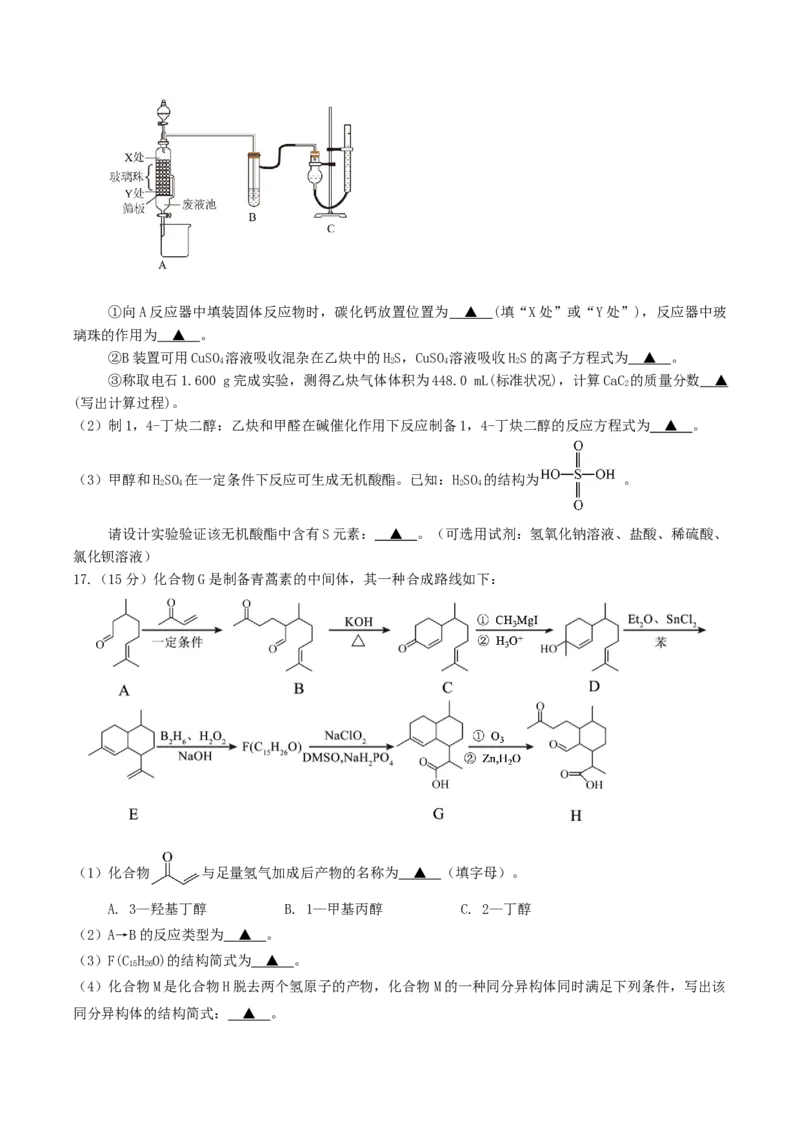
15.(15分)化合物H是一种具有生物活性的苯并呋喃衍生物,其合成路线如下:
(1)A中的含氧官能团名称为羟基和 ▲ 。
(2)C→D反应不充分时可生成其他有机副产物,其结构简式为 ▲ 。(任写一种)
(3)反应③和④的顺序不能对换的原因是 ▲ 。
(4)写出同时满足下列条件的A的一种同分异构体的结构简式: ▲ 。
①既能与FeCl 溶液发生显色反应,又能与银氨溶液发生银镜反应;
3
②核磁共振氢谱显示有5组峰,峰面积之比为1:1:2:2:2。
(5)已知:R—CN――→R—COOH
写出以 和ClCHOCH 为原料制备 的合成路线流程图 ▲ (无机试剂和有
2 3
机溶剂任用,合成路线流程图示例见本题题干)。
16.(16分)1,4-丁炔二醇(HOCHC≡CCHOH)能用作抑制剂,电镀添加剂等。实验室用碳化钙(CaC)制备
2 2 2
乙炔,乙炔和甲醛反应制备1,4-丁炔二醇。
(1)制乙炔:传统方式制备乙炔难以实现固液分离,生成的糊状物使乙炔气流不平稳,甚至堵塞。改进
后的乙炔制备、净化和收集实验装置如图所示。①向A反应器中填装固体反应物时,碳化钙放置位置为 ▲ (填“X处”或“Y处”),反应器中玻
璃珠的作用为 ▲ 。
②B装置可用CuSO 溶液吸收混杂在乙炔中的HS,CuSO 溶液吸收HS的离子方程式为 ▲ 。
4 2 4 2
③称取电石1.600 g完成实验,测得乙炔气体体积为448.0 mL(标准状况),计算CaC 的质量分数 ▲
2
(写出计算过程)。
(2)制1,4-丁炔二醇:乙炔和甲醛在碱催化作用下反应制备1,4-丁炔二醇的反应方程式为 ▲ 。
(3)甲醇和HSO 在一定条件下反应可生成无机酸酯。已知:HSO 的结构为 。
2 4 2 4
请设计实验验证该无机酸酯中含有S元素: ▲ 。(可选用试剂:氢氧化钠溶液、盐酸、稀硫酸、
氯化钡溶液)
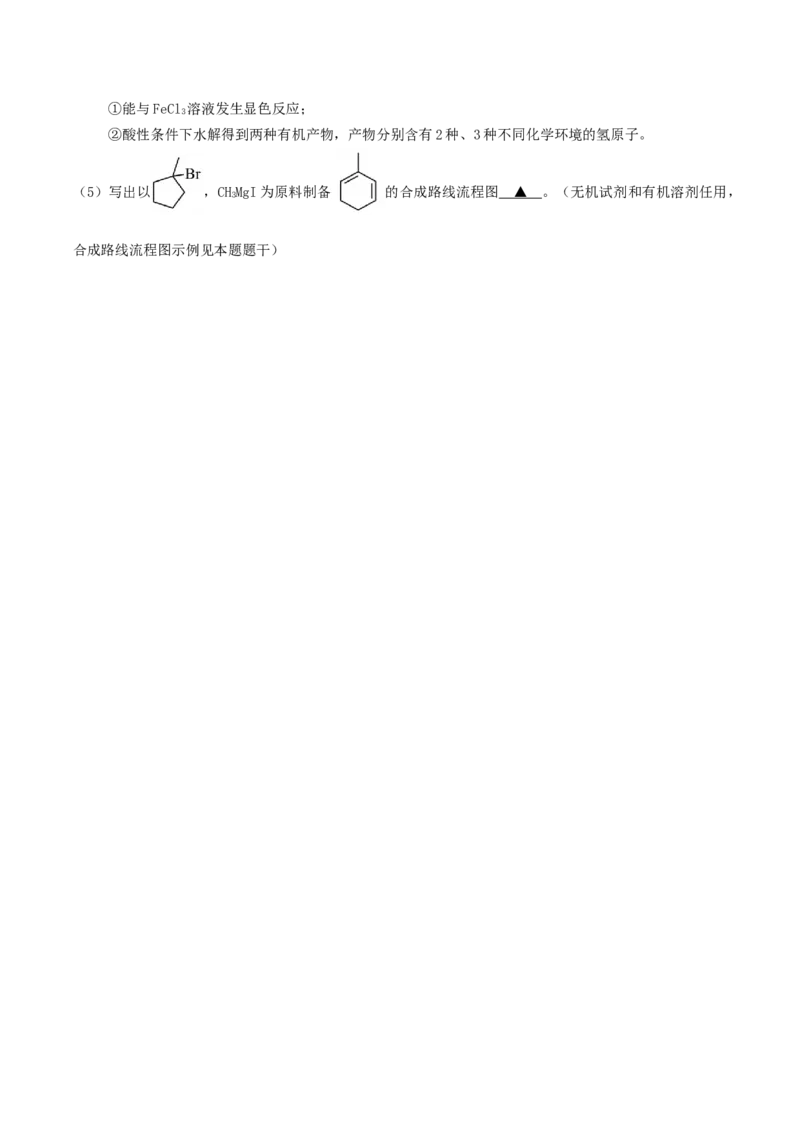
17.(15分)化合物G是制备青蒿素的中间体,其一种合成路线如下:
(1)化合物 与足量氢气加成后产物的名称为 ▲ (填字母)。
A. 3—羟基丁醇 B. 1—甲基丙醇 C. 2—丁醇
(2)A→B的反应类型为 ▲ 。
(3)F(C H O)的结构简式为 ▲ 。
15 26
(4)化合物M是化合物H脱去两个氢原子的产物,化合物M的一种同分异构体同时满足下列条件,写出该
同分异构体的结构简式: ▲ 。①能与FeCl 溶液发生显色反应;
3
②酸性条件下水解得到两种有机产物,产物分别含有2种、3种不同化学环境的氢原子。
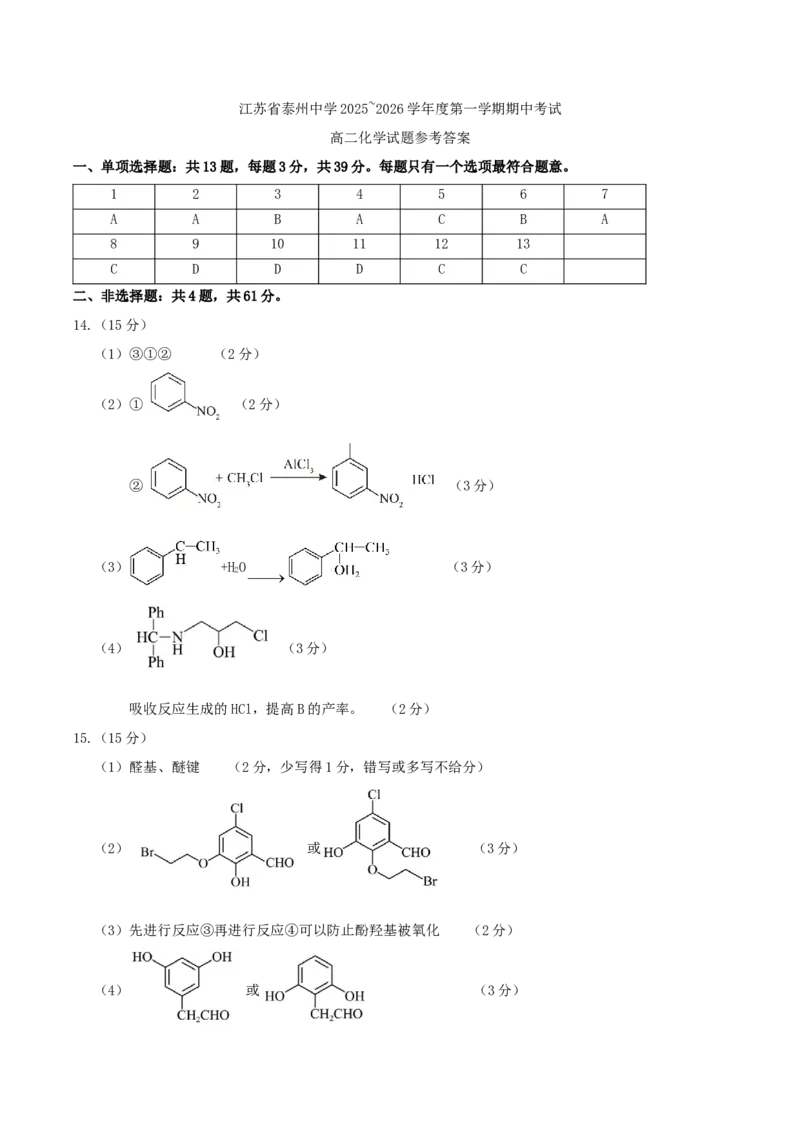
(5)写出以 ,CHMgI为原料制备 的合成路线流程图 ▲ 。(无机试剂和有机溶剂任用,
3
合成路线流程图示例见本题题干)江苏省泰州中学2025~2026学年度第一学期期中考试
高二化学试题参考答案
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1 2 3 4 5 6 7
A A B A C B A
8 9 10 11 12 13
C D D D C C
二、非选择题:共4题,共61分。
14.(15分)
(1)③①② (2分)
(2)① (2分)
② (3分)
(3) +HO (3分)
2
(4) (3分)
吸收反应生成的HCl,提高B的产率。 (2分)
15.(15分)
(1)醛基、醚键 (2分,少写得1分,错写或多写不给分)
(2) 或 (3分)
(3)先进行反应③再进行反应④可以防止酚羟基被氧化 (2分)
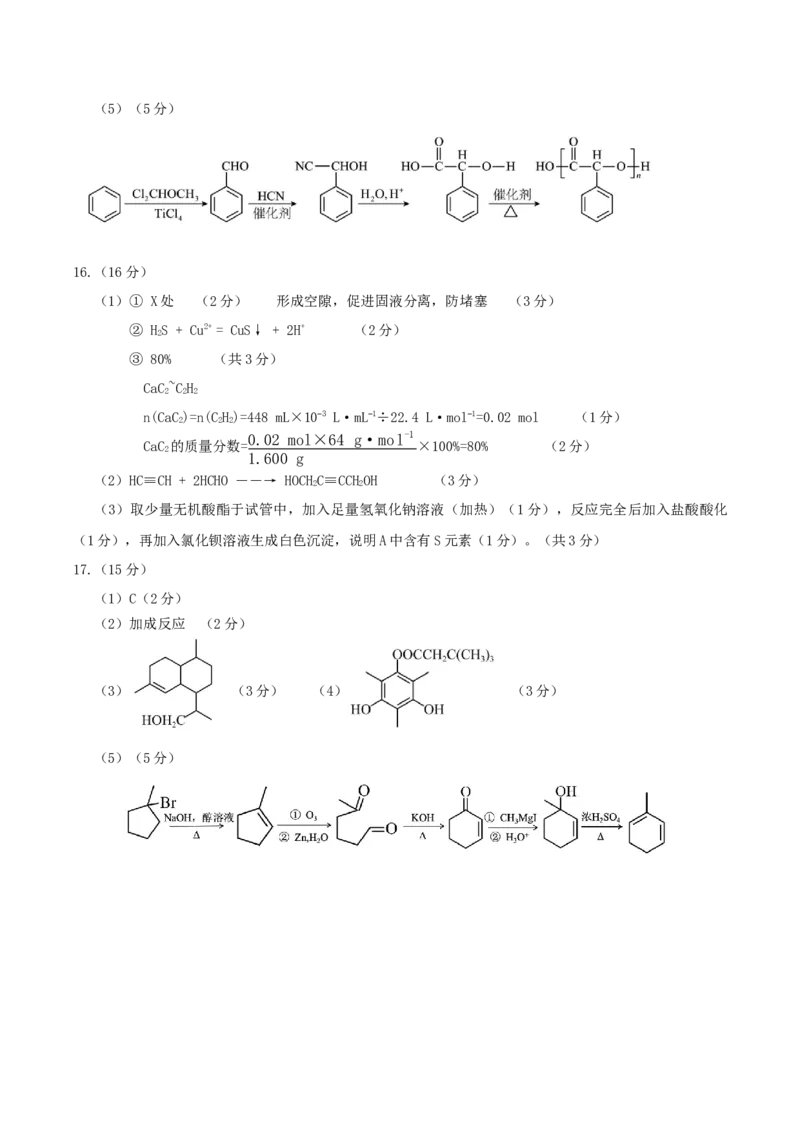
(4) 或 (3分)(5)(5分)
16.(16分)
(1)① X处 (2分) 形成空隙,促进固液分离,防堵塞 (3分)
② HS + Cu2+ = CuS↓ + 2H+ (2分)
2
③ 80% (共3分)
CaC~CH
2 2 2
n(CaC)=n(CH)=448 mL×10−3 L·mL−1÷22.4 L·mol−1=0.02 mol (1分)
2 2 2
0.02 mol×64 g·mol-1
CaC 的质量分数= ×100%=80% (2分)
2
1.600 g
(2)HC≡CH + 2HCHO ――→ HOCHC≡CCHOH (3分)
2 2
(3)取少量无机酸酯于试管中,加入足量氢氧化钠溶液(加热)(1分),反应完全后加入盐酸酸化
(1分),再加入氯化钡溶液生成白色沉淀,说明A中含有S元素(1分)。(共3分)
17.(15分)
(1)C(2分)
(2)加成反应 (2分)
(3) (3分) (4) (3分)
(5)(5分)