文档内容
长沙市明德中学 2024 年下学期高一年级第一阶段检测
化学试卷
可能用到的相对原子质量:
第I卷 选择题(共48分)
一、单选题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 下列关于分散系的说法中正确的是
A. 根据分散剂的不同,将分散系分为溶液、胶体、浊液
B. 用激光笔分别照射溶液和胶体时,均能产生丁达尔效应
C. 胶体区别于其他分散系的本质特征是分散质的微粒直径在 之间
D. 胶体制备的原理是
【答案】C
【解析】
【详解】A.根据分散质粒子直径的不同,将分散系分为溶液、胶体、浊液,A错误;
B.用激光笔分别照射溶液和胶体时,溶液不能产生丁达尔效应,胶体能产生丁达尔效应,B错误;
C.胶体区别于其他分散系的本质是胶体分散质粒子直径为1~100nm,即 之间,C正确;
D.胶体不是沉淀,故 胶体制备的原理是 ,D错误;
故选C。
2. 分类是认识和研究物质及其变化的一种常用的科学方法。下列关于物质分类的组合正确的是
选项 碱 酸 盐 碱性氯化物 酸性氯化物
A 纯碱
B 烧碱
C 石灰石
D 熟石灰A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.纯碱属于盐,A错误;
B. 为不成盐氧化物,B错误;
C. 为盐,C错误;
D.所有物质分类均正确,D正确;
故选D。
3. 下列关于电解质的说法正确的是
A. 液态 不导电,所以 不是电解质
B. 铜丝、石墨均导电,所以它们是电解质
C. 溶于水形成的溶液能导电,所以 是电解质
D. 在水中难导电,但熔融状态下能导电,所以 是电解质
【答案】D
【解析】
【详解】A.液态HCl不导电,但溶于水后能导电,所以HCl是电解质,A错误;
B.铜丝、石墨均为单质,既不是电解质,也不是电解质,B错误;
的
C.NH 溶于水形成 水溶液能导电,是因为NH 与水反应生成 的电离,所以 是电解
3 3
质,NH 是非电解质,C错误;
3
D.BaSO 在水溶液中很难导电,但是熔融状态下能导电,所以BaSO 是电解质,D正确;
4 4
故选D。
4. 下列物质的电离方程式书写不正确的是
A. B.
C. D.
【答案】B
【解析】【详解】A. 为强电解质,完全电离,电离方程式为 ,A正确;
的
B. 为弱酸 酸式盐,电离方程式为 ,B错误;
C. 为强电解质,完全电离,电离方程式为 ,C正确;
D. 为强电解质,完全电离,电离方程式为,D正确;
故选B。
5. 下列离子方程式书写正确的是
A. 氧化铜与稀盐酸混合:
B. 用醋酸除去水垢:
C. 铁与稀盐酸反应:
D. 铜与稀硝酸反应:
【答案】A
【解析】
【详解】A.氧化铜与稀盐酸混合发生反应生成氯化铜和水,离子方程式为: ,
A正确;
B.用醋酸除去水垢发生反应生成醋酸钙、水和二氧化碳,醋酸是弱电解质,离子方程式为:
,B错误;
C.铁与稀盐酸反应生成氯化亚铁和氢气,离子方程式为: ,C错误;
D.铜与稀硝酸反应生成硝酸铜、一氧化氮和水,离子方程式为:
,D错误;
故选A。
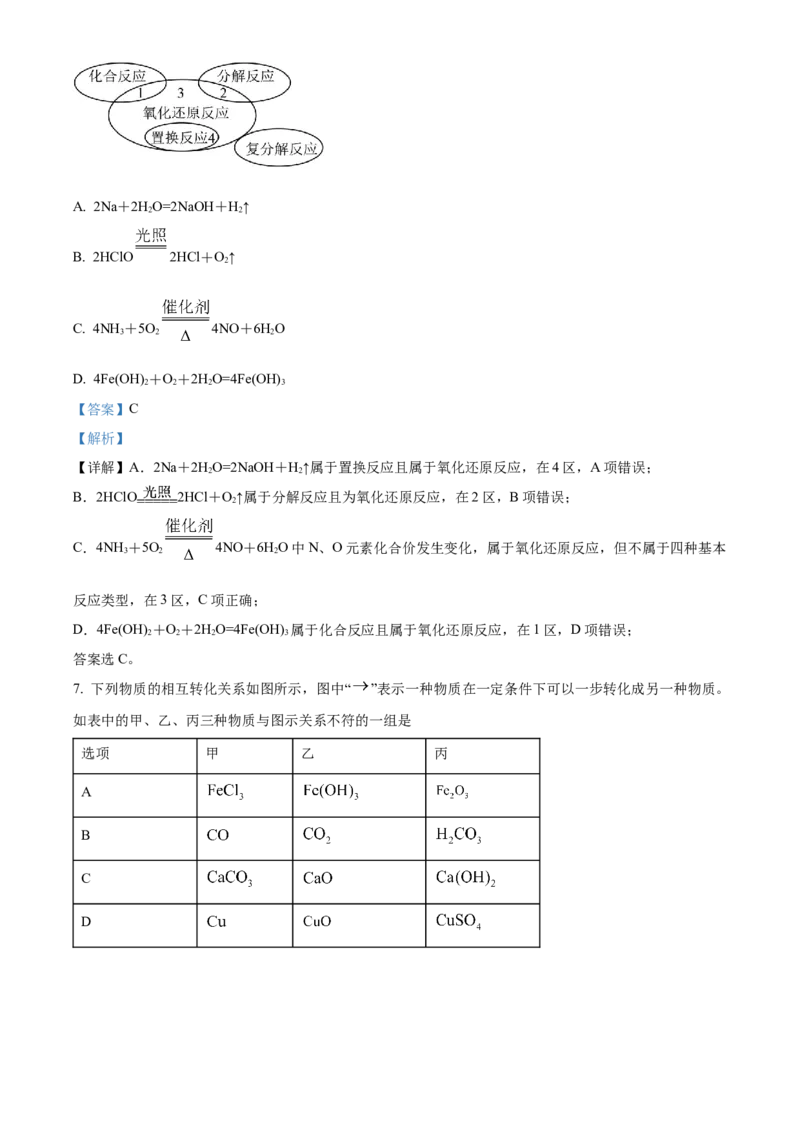
6. 氧化还原反应与四种基本反应类型的关系如图,分析下列四个化学反应,其中属于“3”区的是A. 2Na+2HO=2NaOH+H↑
2 2
B. 2HClO 2HCl+O↑
2
C. 4NH +5O 4NO+6HO
3 2 2
D. 4Fe(OH) +O+2HO=4Fe(OH)
2 2 2 3
【答案】C
【解析】
【详解】A.2Na+2HO=2NaOH+H↑属于置换反应且属于氧化还原反应,在4区,A项错误;
2 2
B.2HClO 2HCl+O↑属于分解反应且为氧化还原反应,在2区,B项错误;
2
C.4NH +5O 4NO+6HO中N、O元素化合价发生变化,属于氧化还原反应,但不属于四种基本
3 2 2
反应类型,在3区,C项正确;
D.4Fe(OH) +O+2HO=4Fe(OH) 属于化合反应且属于氧化还原反应,在1区,D项错误;
2 2 2 3
答案选C。
7. 下列物质的相互转化关系如图所示,图中“ ”表示一种物质在一定条件下可以一步转化成另一种物质。
如表中的甲、乙、丙三种物质与图示关系不符的一组是
选项 甲 乙 丙
A
B
C
DA. A B. B C. C D. D
【答案】B
【解析】
【详解】A.氯化铁与氢氧化钠反应生成氢氧化铁沉淀,氢氧化铁受热分解为氧化铁,氧化铁与盐酸反应
生成氯化铁,符合题意,A正确;
B.碳酸不能通过一步反应生成一氧化碳,不符合题意,B错误;
C.碳酸钙受热分解为氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,符
合题意,C正确;
D.铜和氧气反应生成氧化铜,氧化铜和硫酸反应生成硫酸铜,硫酸铜和铁反应生成铜,符合题意,D正
确;
故选B。
8. 在透明的强酸性溶液中,能大量共存的离子组是
.
A B.
C. D.
【答案】B
【解析】
【详解】A.强酸性溶液中 能与H+反应,不能大量共存,A错误;
B.强酸性溶液中 均不能与H+反应,能大量共存,B正确;
C.强酸性溶液中 能与H+反应,不能大量共存,C错误;
D.强酸性溶液中 能与H+反应,不能大量共存,D错误;
故选B。
9. 下列反应属于氧化还原反应,且水充当还原剂的是
A. B.C. D.
【答案】B
【解析】
【详解】A. 中,水中H的化合价由+1价降低到0价,为氧化剂,A错误;
B. 中,水中的O的化合价由-2升高到0价,为还原剂,B正确;
C. 中无元素化合价变化,为非氧化还原反应,C错误;
D. 中,水中无元素化合价变化,既不是氧化剂也不是还原剂,D错误;
故选B。
10. 下列变化过程中,加入氧化剂才能实现的是
A. NaCO→CO B. Na→Na+
2 3 2
C. SO → D. CuO→Cu
2
【答案】B
【解析】
【分析】化合价升高元素所在的反应物是还原剂,实现化合价升高要加入氧化剂;
【详解】A.NaCO→CO,没有元素化合价变化,不是氧化还原反应,A错误;
2 3 2
B.Na→Na+,元素化合价升高,需要加入氧化剂,B正确;
C.SO → ,没有元素化合价变化,不是氧化还原反应,C错误;
2
D.CuO→Cu,Cu的化合价降低,需要加入还原剂,D错误;
答案选B。
11. 下列反应能用离子方程式 表示的是
A. 将二氧化碳通入氢氧化钠溶液中 B. 氢氧化铜和稀盐酸的反应
C. 氨水和稀硝酸的反应 D. 硫酸氢钠和氢氧化钾的反应
【答案】D
【解析】
【详解】A.二氧化碳通入氢氧化钠溶液中,离子方程式为: ,不能用来表示,A错误;
B.氢氧化铜是沉淀,在书写离子方程式时不能拆,故氢氧化铜和盐酸反应的离子方程式为:
,不能用 来表示,B错误;
C.氨水是弱电解质,在书写离子方程式时不能拆,氨水和稀硝酸的反应的离子方程式为
,不能用 来表示,C错误;
D.硫酸氢钠和氢氧化钾均为强电解质,能完全电离,硫酸氢钠和氢氧化钾的反应的离子方程式为
,D正确;
故选D。
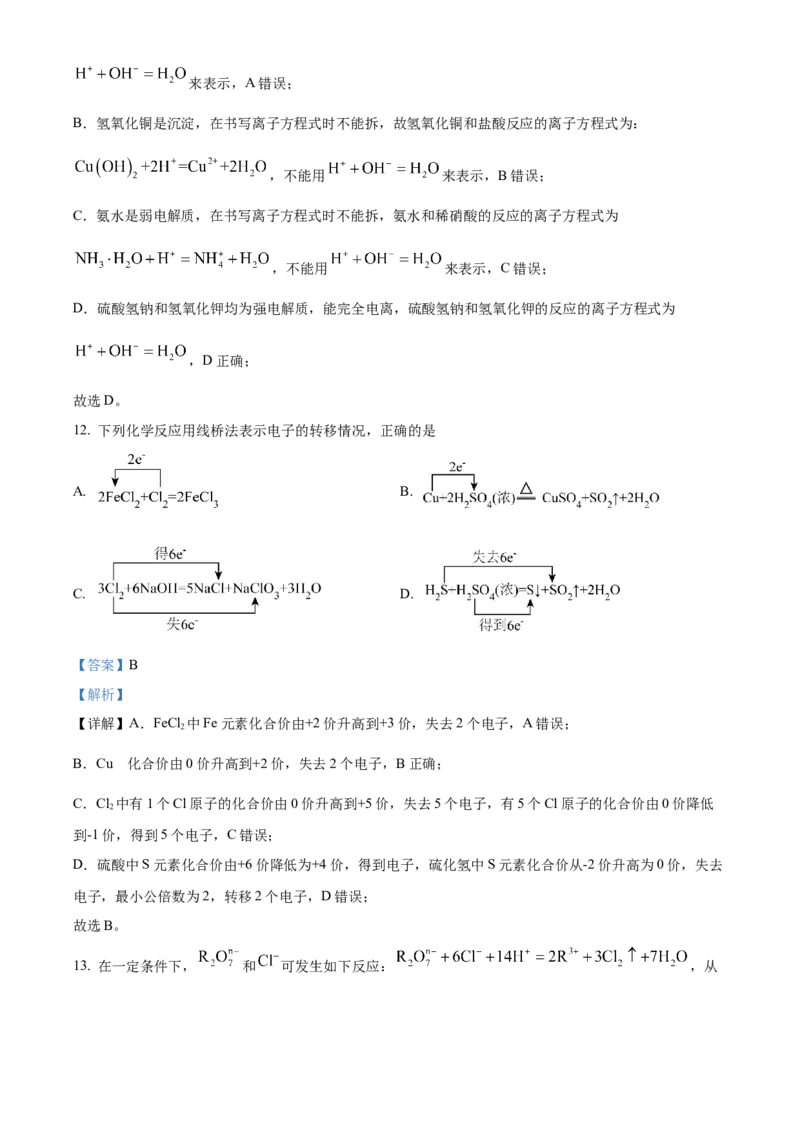
12. 下列化学反应用线桥法表示电子的转移情况,正确的是
A. B.
C. D.
【答案】B
【解析】
【详解】A.FeCl 中Fe元素化合价由+2价升高到+3价,失去2个电子,A错误;
2
的
B.Cu 化合价由0价升高到+2价,失去2个电子,B正确;
C.Cl 中有1个Cl原子的化合价由0价升高到+5价,失去5个电子,有5个Cl原子的化合价由0价降低
2
到-1价,得到5个电子,C错误;
D.硫酸中S元素化合价由+6价降低为+4价,得到电子,硫化氢中S元素化合价从-2价升高为0价,失去
电子,最小公倍数为2,转移2个电子,D错误;
故选B。
13. 在一定条件下, 和 可发生如下反应: ,从而可知在 中,则R的化合价是
A. +4价 B. +5价 C. +6价 D. +7价
【答案】C
【解析】
【详解】根据反应前后电荷守恒,可知:n=2,则根据 中化合价代数和为-2,解得R的化合价为+6
价;
故选C。
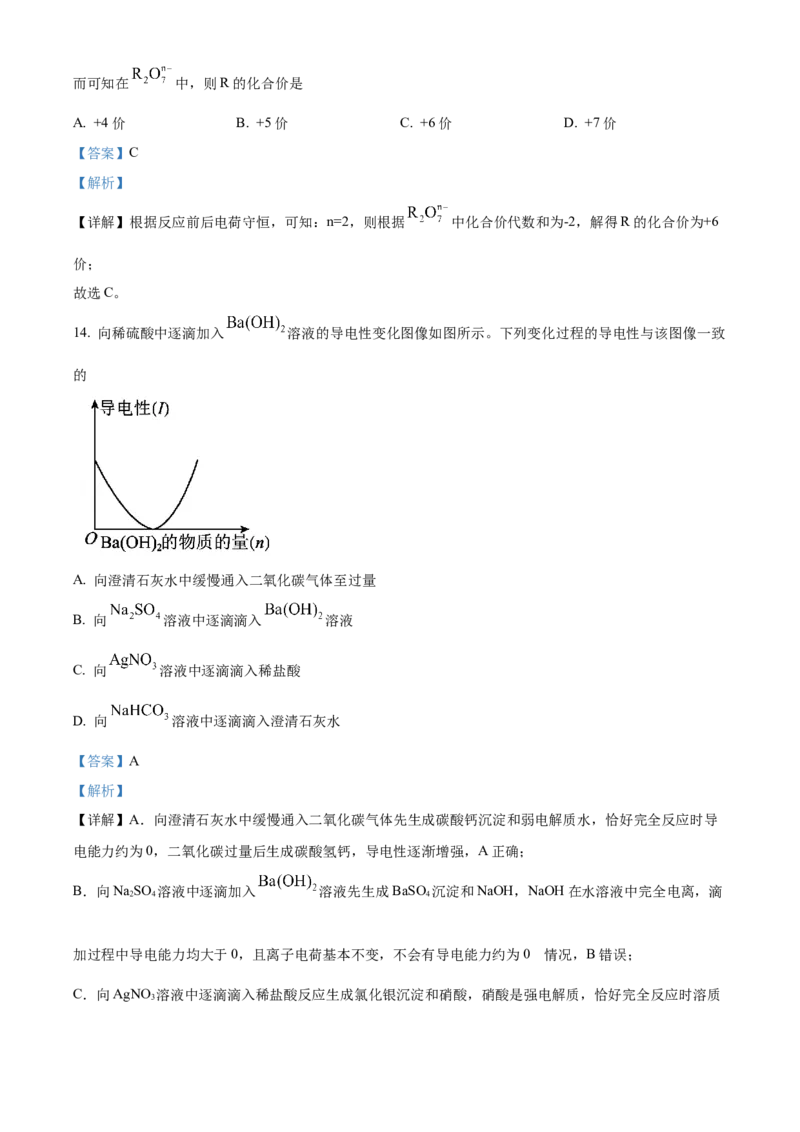
14. 向稀硫酸中逐滴加入 溶液的导电性变化图像如图所示。下列变化过程的导电性与该图像一致
的
A. 向澄清石灰水中缓慢通入二氧化碳气体至过量
B. 向 溶液中逐滴滴入 溶液
C. 向 溶液中逐滴滴入稀盐酸
D. 向 溶液中逐滴滴入澄清石灰水
【答案】A
【解析】
【详解】A.向澄清石灰水中缓慢通入二氧化碳气体先生成碳酸钙沉淀和弱电解质水,恰好完全反应时导
电能力约为0,二氧化碳过量后生成碳酸氢钙,导电性逐渐增强,A正确;
B.向NaSO 溶液中逐滴加入 溶液先生成BaSO 沉淀和NaOH,NaOH在水溶液中完全电离,滴
2 4 4
的
加过程中导电能力均大于0,且离子电荷基本不变,不会有导电能力约为0 情况,B错误;
C.向AgNO 溶液中逐滴滴入稀盐酸反应生成氯化银沉淀和硝酸,硝酸是强电解质,恰好完全反应时溶质
3为HNO,导电能力大于0,C错误;
3
D.向NaHCO 溶液中逐滴滴入澄清石灰水反应生成碳酸钙沉淀、水和氢氧化钠,氢氧化钠是强电解质,
3
滴加过程中导电能力均大于0,D错误;
故选A。
15. 已知常温下在溶液中能发生如下反应:①16H++10Z—+2XO =2X2++5Z+8H O,②2M2++R =2M3++2R-,
2 2 2
③2R-+Z=R +2Z-。由此判断,下列说法中正确的是
2 2
A. 各粒子氧化性由强到弱的顺序是XO >Z>R >M3+
2 2
B. 各粒子还原性由强到弱的顺序是X2+>Z->R->M2+
C. Z元素在①③反应中发生还原反应
D. Z+2M2+=2M3++2Z-不可以进行
2
【答案】A
【解析】
【详解】A.氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,反应16H++10Z-+2 =2X2++
5Z+8HO中,氧化性: >Z;反应2M2++R =2M3++2R-中,氧化性:R >M3+;反应2R-+Z=R
2 2 2 2 2 2 2
+2Z-中,氧化性:Z>R ,即氧化性顺序是 >Z>R >M3+,故A项正确;
2 2 2 2
B.根据反应2M2++R =2M3++2R-,可得还原性顺序是R-<M2+,根据反应2R-+Z=R2++2Z-,可得还
2 2
原性顺序是Z-<R-,根据反应:16H++10Z-+2 =2X2++5Z+8HO,可得还原性顺序是:X2+<Z
2 2
-,即还原性强弱顺序为:X2+<Z-<R-<M2+,故B项错误;
C.Z元素在①中化合价升高,发生氧化反应,在③中化合价降低,发生还原反应,故C项错误;
D.氧化性顺序是 >Z>R >M3+,Z+2M2+ =2M3++2 Z-可以进行,故D项错误;
2 2 2
故本题选A。
16. 用下列方法均可制得氯气
① ② ③
,若要制得相同质量的氯气,①②③反应中电子转移数目之比为
A. B. C. D.
【答案】C
【解析】
【详解】① 中, 中Cl的化合价由-1价升高到0价,每
生成1个Cl,转移2个电子,②, 中, 中Cl的化合价
2
由+5降低到0价, 中Cl的化合价由-1价升高到0价,每生成3个Cl,转移5个电子,③
2
中, 中Cl的化合价由-1价升高到0价,
每生成1个Cl,转移2个电子,若要制得相同质量的氯气,①②③反应中电子转移数目之比为 ,C
2
正确,
故选C。
第Ⅱ卷 非选择题(共52分)
二、非选择题:本题共4小题,共52分。
17. I.写出下列反应的离子方程式:
(1)稀盐酸和石灰石反应制取二氧化碳_______
(2)硫酸铜溶液和氢氧化钡溶液反应_______
Ⅱ.现有以下物质:① 晶体;②盐酸;③石墨;④ 固体;⑤熔融 ;⑥蔗糖;⑦铜;⑧
;⑨氢氧化钡溶液;⑩乙醇。
(3)以上物质中能导电的是_______(填序号,下同)。
(4)以上物质中属于电解质的是_______,属于非电解质的是_______。
(5)以上物质中溶于水,其水溶液能导电的是_______
【答案】(1)
(2)(3)②③⑤⑦⑨ (4) ①. ①④⑤ ②. ⑧⑩
(5)①②④⑤⑧⑨
【解析】
【小问1详解】
稀盐酸和石灰石反应制取二氧化碳的离子方程式为 ;
【小问2详解】
硫酸铜溶液和氢氧化钡溶液反应生成硫酸钡和氢氧化铜沉淀,离子方程式为
【小问3详解】
能够导电的物质是含有能够自由移动的离子或电子的物质,即电解质的水溶液、熔融状态下的电解质,金
属单质或少数能导电的非金属单质,能导电的物质有②盐酸、③石墨、⑤熔融 、⑦铜、⑨氢氧化钡溶
液;
【小问4详解】
电解质是指在水溶液或熔融状态下能够导电的化合物,属于电解质的有:① 晶体、④ 固体、
⑤熔融 ;非电解质是指在水溶液和熔融状态下都不能够导电的化合物,属于非电解质的物质有:⑧
、⑩乙醇;
【小问5详解】
以上物质中溶于水,其水溶液能导电的有① 晶体、②盐酸、④ 固体、⑤熔融 、⑧
、⑨氢氧化钡溶液;
18. I.火药是中国“四大发明”之一,永远值得炎黄子孙骄傲,也永远激励着我们去奋发图强。
(1)黑火药发生爆炸时,发生反应: ,其中木炭发生
_______(填氧化反应/还原反应),氧化剂是_______被氧化的元素是_______。
Ⅱ.已知铜在常温下与稀硝酸反应, 。
(2)该反应中被氧化的元素与被还原的元素的原子个数之比是_______(3)该反应中稀硝酸表现出的性质是_______
A.还原性 B.酸性 C.氧化性
(4)请将该反应改写成离子方程式:_______
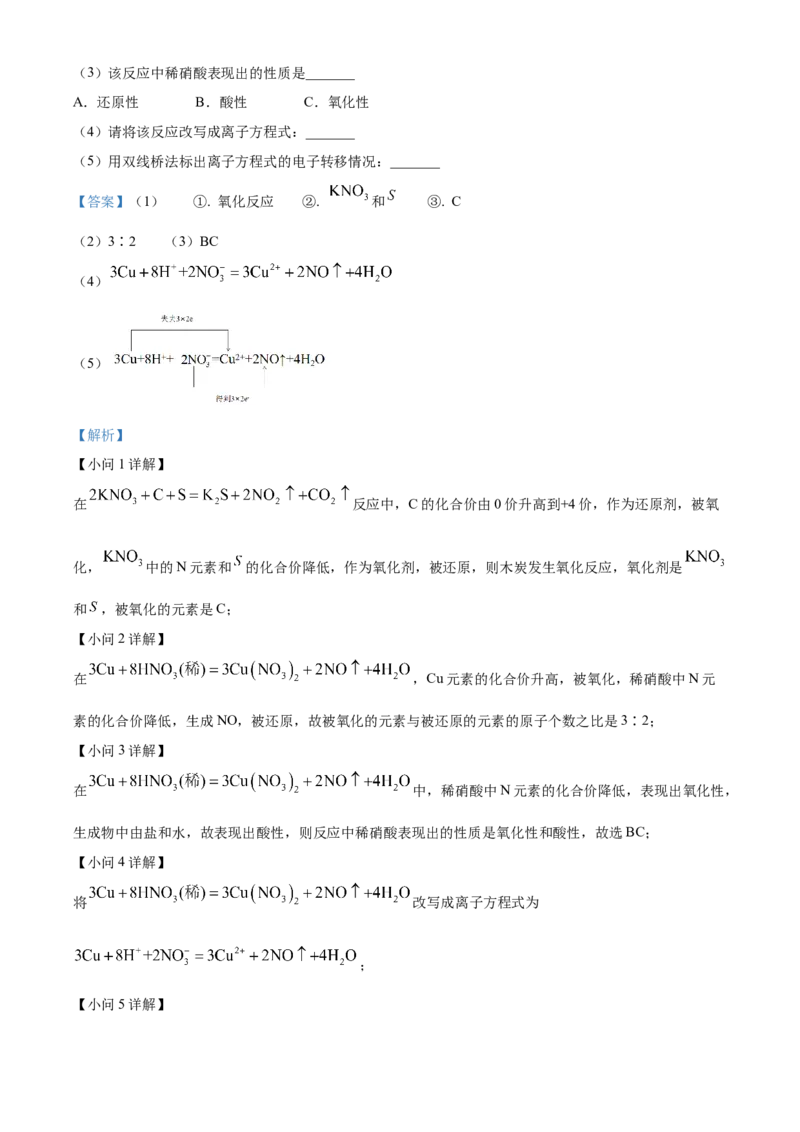
(5)用双线桥法标出离子方程式的电子转移情况:_______
【答案】(1) ①. 氧化反应 ②. 和 ③. C
(2)3∶2 (3)BC
(4)
(5)
【解析】
【小问1详解】
在 反应中,C的化合价由0价升高到+4价,作为还原剂,被氧
化, 中的N元素和 的化合价降低,作为氧化剂,被还原,则木炭发生氧化反应,氧化剂是
和 ,被氧化的元素是C;
【小问2详解】
在 ,Cu元素的化合价升高,被氧化,稀硝酸中N元
素的化合价降低,生成NO,被还原,故被氧化的元素与被还原的元素的原子个数之比是3∶2;
【小问3详解】
在 中,稀硝酸中N元素的化合价降低,表现出氧化性,
生成物中由盐和水,故表现出酸性,则反应中稀硝酸表现出的性质是氧化性和酸性,故选BC;
【小问4详解】
将 改写成离子方程式为
;
【小问5详解】在 中,Cu升高2价,共失去3个电子,N降低3价,共得到
6个电子,用双线桥表示为 。
19. I.氧化还原反应与离子反应在生产生活与科学实验中有重要作用,回答问题。过氧化氢俗名双氧水,
医疗上利用它有杀菌消毒作用来清洗伤口。
(1)根据下列反应回答问题:
A. B.
C. D. 上述
反应中, 仅体现氧化性的反应是_______(填字母序号,下同), 既体现氧化性又体现还原性的
反应是_______, 的氧化性由强到弱的顺序是_______。
Ⅱ.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:
(2) ,则X的化学式是_______,其中 在该反应中_______(填字母)。
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
Ⅲ.某一反应体系有反应物和生成物共六种物质: 。已知 转
化为 。
(3)该反应的还原剂是_______
(4)该反应中氧化剂与氧化产物的质量之比为_______。
【答案】(1) ①. D ②. C ③.
(2) ①. ②. D
(3)还原剂 (4)【解析】
【小问1详解】
A. 中,化合价没有发生变化,不是氧化还原反应;B.
中, 中O元素由-1价升高到0价,被氧化, 作为还原剂,
体现还原性;C. 中, 中O元素由-1价升高到0价,被氧化, 作为氧
化剂,体现氧化性, 中O元素由也由-1价降低到-2价,被还原, 作为还原剂,体现还原性,
则 既作为氧化剂,也作为还原剂;D. 中,
中O元素由-1价降低到-2价,被还原, 作为氧化剂,体现氧化性,故 仅体现氧化性的反应是
D; 既体现氧化性又体现还原性的反应是C; 中 作为氧
化剂, 作为还原剂,故氧化性 > ,在
中, 作为氧化剂, 作为氧化产物,故氧化性 > ,综上,
的氧化性由强到弱的顺序是 ;
【小问2详解】
由原子守恒可得, 中X的化学式是 ,在反应中 的化合价为发
生变化, 在该反应中既不是氧化剂,也不是还原剂;
【小问3详解】
已知 转化为 ,由氧化还原反应的规律可知,由 组成的
氧化还原方程式为 ,该反应中HI中I的化合价由-1价升高到0价,作为还原剂;
【小问4详解】
在 反应中,氧化剂为 ,氧化产物为 ,两者的质量之比
为 。
20. 有一瓶透明澄清的溶液,其中可能含有 ,取该溶液
进行以下实验:
①取 试纸检验,表明溶液呈强酸性
②另取部分溶液逐滴加入 溶液,使溶液从酸性逐渐变为碱性,滴加过程中无沉淀产生
③取上述碱性溶液滴加 溶液,有白色沉淀生成,加入盐酸,沉淀溶解,并产生气泡。
请回答下列问题:
(1)有同学认为不需要实验,根据“透明澄清的溶液”即可肯定不含 ,此说法是否合理?_______
(2)原溶液中一定有的离子是_______,一定没有的离子是_______,可能有的离子是_______。
(3)写出③发生的所有反应的离子方程式_______。
【答案】(1)不合理 (2) ①. ②. ③.
(3) 、
【解析】
【分析】①取pH试纸检验,表明溶液呈强酸性,说明含有大量的H+,而 能与H+反应,因此原溶液
中一定不存在 ;②另取部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中
和滴加完毕后,溶液均无沉淀产生,说明原溶液中一定不含有 Fe3+;③取②碱性溶液滴加NaCO 溶液,有
2 3
白色沉淀生成,说明原溶液中一定存在Ba2+,Ba2+与 反应生成硫酸钡沉淀,因此原溶液中一定不存在
,Ba2+与NaCO 溶液生成碳酸钡,,溶液呈电中性,原溶液中一定存在Cl-, 无法确定,
2 3
据此回答。
【小问1详解】为黄色,但是透明澄清的溶液可以存在有色离子,故根据“透明澄清的溶液”即可肯定不含 ,说
法不合理;
【小问2详解】
由分析知,原溶液中一定有的离子是 ;一定没有的离子是 ;可能有
的离子是 ;
【小问3详解】
取上述碱性溶液滴加 溶液,有白色沉淀生成,发生的反应的离子方程式:
,加入盐酸,沉淀溶解,并产生气泡,发生的反应的离子方程式:
。