文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题一 物质的化学变化
专题 03 质量守恒定律 化学方程式
01考情透视·目标导航
02知识导图·思维引航
03考点突破·考法探究
考点一 质量守恒定律
实验 质量守恒定律的实验验证
考点二 化学方程式
考点三 根据化学方程式进行简单计算
04题型精研·考向洞悉
题型一 质量守恒定律
►考向01 质量守恒定律的内容和适用范围
►考向02 质量守恒定律的微观解释
►考向03 质量守恒定律的实验验证
►考向04 用质量守恒定律解释现象
►考向05 用质量守恒定律确定物质的组成
►考向06 密闭容器中相关图表信息的计算
►考向07 巧用元素守恒进行计算
题型二 化学方程式
►考向01 化学方程式的含义
►考向02 化学方程式的书写
►考向03 根据化学方程式推测化学式
题型三 根据化学方程式进行简单计算
►考向01 不含杂质的计算
►考向02 含杂质的计算
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点要求 课标要求 命题预测
质量守恒定律考查有:利用质量守恒
定律对现象进行解释、从微观角度解释质
认识化学反应遵守质量
量守恒定律的原因、实验验证质量守恒定
守恒定律。理解质量守恒定律的
律、利用质量守恒定律进行计算等;考查
质量守恒定律 微观本质。认识化学反应中的各
题型可以是选择题和计算题,也可以是与
物质间存在定量关系,学习从元
其他知识点结合在填空题、流程题、综合
素守恒视角认识化学反应。
应用题中考查。化学方程式考查内容有:
化学方程式的含义和书写,以及根据化学
方程式推测化学式。 考查题型一般以选
能正确书写常见的化学 择和填空为主,少数穿插于其他题型中。
化学方程式 方程式;能基于守恒和比例关系 根据化学方程式的计算考查:单独考查,
推断化学反应的相关信息。 或与化学式、溶液结合进行综合考查,呈
现方式多样化,有文字叙述、图像图表、
流程图、实验装置图等形式;题型以计算
学习利用质量关系、比 题为主,也经常以选择题呈现,或穿插于
例式关系定量认识化学反应,认 流程题、综合应用题中考查。
根据化学方程式
识定量研究对化学科学发展的重
进行简单计算 大作用。能根据化学方程式进行
简单的计算,并解决生产生活中
的简单问题。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 质量守恒定律
1.质量守恒定律
(1)内容: 。
(2)适用范围:一切 (物理变化不讨论质量守不守衡的关系)。
(3)概念解读:
①是 守恒,不是体积、分子个数等守恒。
②质量范围: 的反应物质量(不包括没有反应完的部分和催化剂的质量)和 的质量。
尤其注意 、 等不要忽略。
【特别提醒】
1 .一切化学反应都遵守质量守恒定律,没有例外。
2 .判断能否用质量守恒定律解释的变化,可以直接转换成判断是否是化学变化即可。
2.微观解释质量守恒定律的原因
(1)化学变化的实质: 成新的分子。
(2)以电解水反应为例分析:
水通电分解前后,从微观角度来看,不变的是: ;变化的是:
。
(3)从微观角度解释质量守恒定律:在化学反应前后, 、 、
。(即原子的“三不变”)。
反应前后原子的种类不变,则元素的 也不变;原子的数目和质量不变,则元素的 也不变,元素的
和
不变,则物质的总质量也不变,这就是质量守恒的原因。
(4)化学反应前后的几个“变与不变”:
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3.质量守恒定律的实验验证
(1)质量“守恒”的实验验证
铜粉加热前后质量变化的测定 铁和硫酸铜反应前后质量变化的测定
实验图示
。天平两次
;天平两次显示
实验现象
显示示数 。
示数 。
化学方程式
实验结论 反应前各物质的总质量=反应后各物质的总质量。
【特别提醒】
1 . 气球的作用是形成密闭体系并缓冲气压;
2 . 气球变瘪是因为消耗了锥形瓶内氧气,使瓶内气体压强小于外界大气压。
(2)质量“不守恒”的实验情况分析
碳酸钠与稀盐酸的反应 镁条的燃烧
实验图示
白色粉末溶解,有 。 产生白色固体(还有少量 产生),
实验现象
天平 。 天平不平衡,发出耀眼的 光,放出热量。
反应原理
氧化镁的质量等于反应的镁条和参加反应的氧气质
反应生成的 是气体,逸散到空气 量总和, 导致质量 。但逸散的白烟质量又大
实验分析
中去,所以质量变小 于增加的气体质量,坩埚钳上可能也粘有一部分氧
化镁,此二者均会造成氧化镁损失,导致质量
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。故实验结果可能会“减小”、“不变”或“增
大”。
实验结论 所有的化学反应 质量守恒定律,表面貌似“不守恒”的实验需要认真加以分析原因。
或 (或者有烟、雾状物质生成)的反应,验证质量守恒定律时,必须在
感悟
容器里进行。
验证质量守恒定律时,选取的实验要求:
1.必须是发生 的实验,质量守恒定律不适用于物理变化。
2.有气体参加或有气体生成的反应,验证质量守恒定律时,必须在 里进行。弹性密闭容器可能会影响实验
结果,比如气球被吹大后会受到浮力作用而影响实验的准确性。
1.(2024·山西·中考真题)在一次实验课上,同学们通过小组合作,完成了对密闭容器中少量小苏打与少量白
醋反应的质量测定。以下分析正确的是
A.反应后小苏打的质量增加 B.反应过程中各物质的质量都不变
C.反应前后各物质的质量总和相等 D.反应前称量的是小苏打和白醋的总质量
考点二 化学方程式
1.化学方程式
用化学式表示化学反应的式子,叫做化学方程式。
2.化学方程式的意义和读法
意义
读法(以C + O CO 为例)
2 2
质的方面 表明反应物、生成物和 碳和氧气在点燃的条件下反应,生成二氧化碳。
量 宏 每12份质量的碳和32份质量的氧气在点燃的条件下恰
反应中各物质间的
的 观 好完全反应,生成44份质量的水。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
方 微 每1个碳原子和1个氧分子在点燃的条件下恰好完全反
反应中各物质间的
面 观 应,生成1个二氧化碳分子。
3.根据化学方程式获得的信息
以2H 2 + O 2 点燃 2 H 2 O为例 以Fe + CuSO 4 FeSO 4 + Cu 为例
获得的信息
4 32 36 56 160 152 64
定 反应物
性 生成物
角 反应条件 无
度 基本反应类型 置换反应
铁、硫酸铜、硫酸亚铁和铜的质量比为
各物质的质量比 氢气、氧气、水的质量比为
定 各物质的微观粒 氢气、氧气、水的分子个数比为 反应的铁、硫酸铜、硫酸亚铁和铜的“微观
量 子个数比 粒子个数比”为
角 反应前后物质质 反应前: 反应前:
度 量总和守恒 反应后: 反应后:
反应前后各原子 氢原子数:反应前 ,反应后 铁、硫、铜原子数:反应前 ,反应后
数目守恒 氧原子数:反应前 ,反应后 氧原子数:反应前 ,反应后
4.化学方程式书写
(1)化学方程式的书写原则
①必须以 为基础,化学式不能写错。
②必须遵守 ,等号两边各原子的种类和数目必须相等。
(2)化学方程式的书写步骤
①描述反应事实:写出反应物和生成物的化学式,注明反应条件。
②配平化学方程式:选取合适的化学计量数,使之遵守质量守恒定律。 注意生成物是否需要标注“↑”
“↓”号。
1.书写化学方程式时,如果反应物和生成物中都有气体,气体生成物就不注“↑”号;溶液中的反应,若反应
物和生成物中都有固体,固体生成物也不注“↓”号。
2.书写化学方程式时,“点燃”不能与“加热”、“∆”混淆,也不能写成“燃烧”,“通电”不能写成“电
解”。
3.根据信息书写陌生化学方程式,反应条件要严格按照题给信息书写,不能擅自改动。如“1200℃”不能写成
“高温”;“一定条件”、“催化剂”、“高温高压”等都要原文照抄,不可改动。
1.下列化学反应方程式与描述相符,且书写完全正确的是
A.用稀盐酸除铁锈:
B.铝放入稀硫酸中:
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.拉瓦锡研究空气成分:
D.碳在氧气中完全燃烧:
考点三 根据化学方程式进行简单计算
1.计算依据:
(1)理论依据:质量守恒定律
(2)基本依据:反应中的各物质的质量比成 关系,等于各物质 (或相对原子质量)与其
的乘积之比。
2.计算步骤:
步骤 举例
设 设未知量 加热分解6g高锰酸钾,可以得到多少克氧气?
解:设生成的O 的 。
写 写出化学方程式 2
Mg 2HCl MgCl
H
+ = + ↑
找出比例关系,写出相关物质的 与
找
2 2
的乘积,以及
Zn 2HCl ZnCl
列 列出比例式,求解 H
+ = + ↑
2 2
答 简明地写出答案
答:加热分解 6g高锰酸钾,可以得到 0.6g氧
气。
3.不纯物质与纯物质的换算关系:
(1)物质的纯度是指纯净物在不纯物质(混合物)中的质量分数,即纯物质的质量分数。
物质的纯度=
变形:纯物质的质量=
不纯物质的质量=
(2)物质的纯度 =
1.解题关键:化学式要正确;化学方程式要配平;相对分子质量的计算要准确;
2.代入化学方程式计算的必须是纯净物的质量,且单位要一致。
3.所设未知数后面不能带单位。
4.关系式中的数据与化学方程式中的化学式要上下对齐。
5.化学方程式体现的是物质之间的质量关系,若涉及体积,则需要通过密度进行换算。
1. 【新考向】(2024·江苏苏州·中考真题)捕集空气中CO 加氢制甲醇(CHOH),可实现CO 资源化利用和
2 3 2
“零碳”排放,其转化流程如图所示。下列说法不正确的是
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.反应①中,电解水生成的H 和O 的分子个数比为2:1
2 2
B.反应②中,生产1.6kgCH OH理论上要消耗2.2kgCO
3 2
C.转化过程中,HO和H 循环转化,无需额外补充
2 2
D.等质量的甲醇制取时消耗的CO 与燃烧时生成的CO 相等,实现“零碳”排放
2 2
题型一 质量守恒定律
►考向01 质量守恒定律的内容和适用范围
1. 【新情境】(2024·安徽马鞍山·三模)2024年4月17日,全球首颗用牡丹制成的钻石亮相洛阳中国国花园。
这颗“牡丹钻石”是通过把牡丹花中的碳元素提取出来制作而成。下列说法错误的是
A.提取过程中碳元素的质量不变 B.制成的钻石中碳原子之间有间隔
C.制成的钻石中碳原子不运动 D.常温下钻石的化学性质很稳定
2. 【新形式】(2024·安徽·中考真题)某实验小组按图a装置验证质量守恒定律,一段时间后,发现锥形瓶内
部分固体变为红棕色。实验过程中瓶内物质或元素质量变化与图b相符的是
A.铁粉的质量 B.氮气的质量 C.氧元素的质量 D.固态物质的质量
►考向02 质量守恒定律的微观解释
3.(2024·江苏徐州·中考真题)为了实现碳的资源化利用,我国科学家用纳米镍粒子作催化剂将二氧化碳合成甲
烷,反应的化学方程式为 。下列说法正确的是
A.X的化学式为HO B.甲烷中碳、氢元素的质量比为3∶1
2 2
C.反应前后分子的数目不变 D.参加反应的CO 和H 的质量比为22∶1
2 2
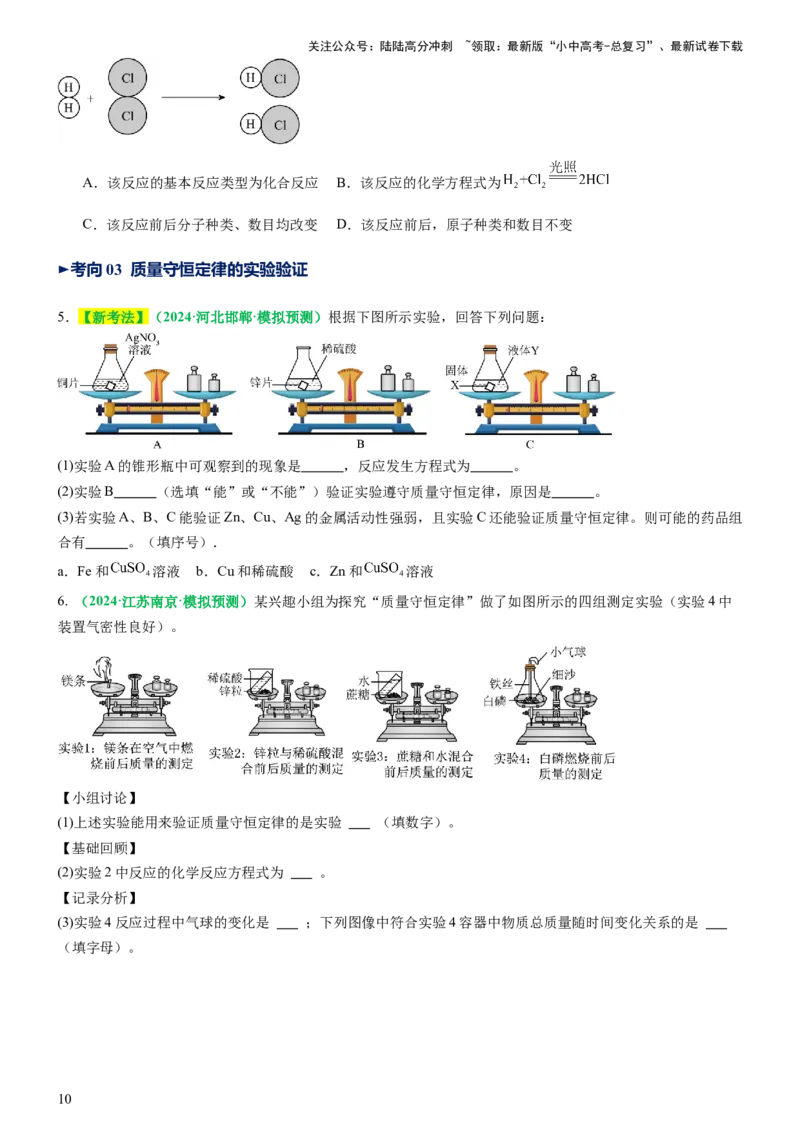
4. (2024·四川南充·中考真题)氢气和氯气的混合气体在强光照射时发生爆炸,微观示意图如下。下列说法错
误的是
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.该反应的基本反应类型为化合反应 B.该反应的化学方程式为
C.该反应前后分子种类、数目均改变 D.该反应前后,原子种类和数目不变
►考向03 质量守恒定律的实验验证
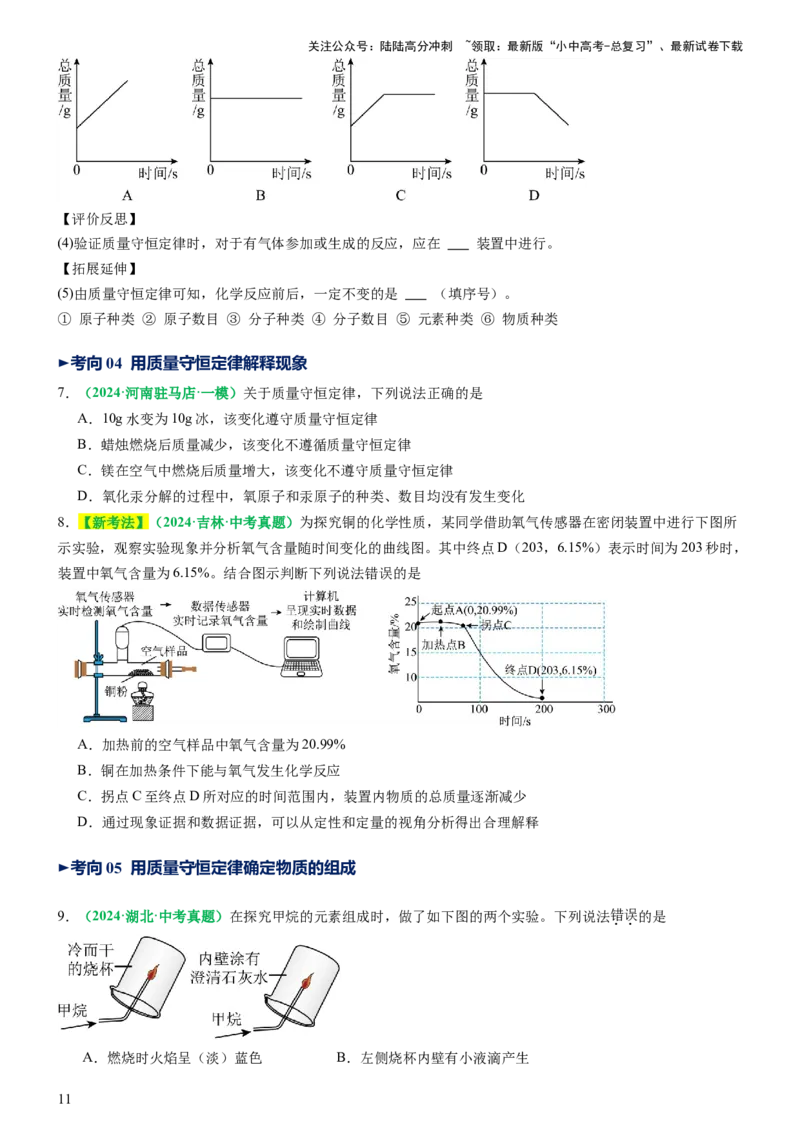
5.【新考法】(2024·河北邯郸·模拟预测)根据下图所示实验,回答下列问题:
(1)实验A的锥形瓶中可观察到的现象是 ,反应发生方程式为 。
(2)实验B (选填“能”或“不能”)验证实验遵守质量守恒定律,原因是 。
(3)若实验A、B、C能验证Zn、Cu、Ag的金属活动性强弱,且实验C还能验证质量守恒定律。则可能的药品组
合有 。(填序号).
a.Fe和 溶液 b.Cu和稀硫酸 c.Zn和 溶液
6. (2024·江苏南京·模拟预测)某兴趣小组为探究“质量守恒定律”做了如图所示的四组测定实验(实验4中
装置气密性良好)。
【小组讨论】
(1)上述实验能用来验证质量守恒定律的是实验 (填数字)。
【基础回顾】
(2)实验2中反应的化学反应方程式为 。
【记录分析】
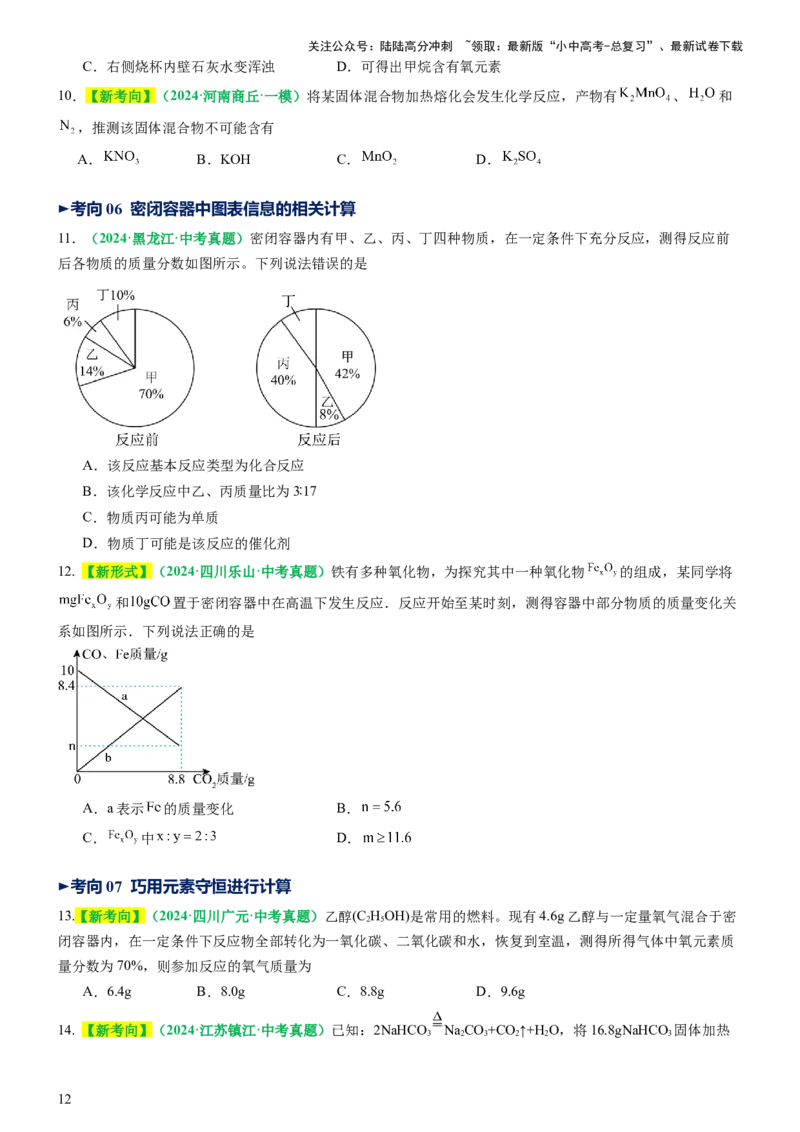
(3)实验4反应过程中气球的变化是 ;下列图像中符合实验4容器中物质总质量随时间变化关系的是
(填字母)。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【评价反思】
(4)验证质量守恒定律时,对于有气体参加或生成的反应,应在 装置中进行。
【拓展延伸】
(5)由质量守恒定律可知,化学反应前后,一定不变的是 (填序号)。
① 原子种类 ② 原子数目 ③ 分子种类 ④ 分子数目 ⑤ 元素种类 ⑥ 物质种类
►考向04 用质量守恒定律解释现象
7.(2024·河南驻马店·一模)关于质量守恒定律,下列说法正确的是
A.10g水变为10g冰,该变化遵守质量守恒定律
B.蜡烛燃烧后质量减少,该变化不遵循质量守恒定律
C.镁在空气中燃烧后质量增大,该变化不遵守质量守恒定律
D.氧化汞分解的过程中,氧原子和汞原子的种类、数目均没有发生变化
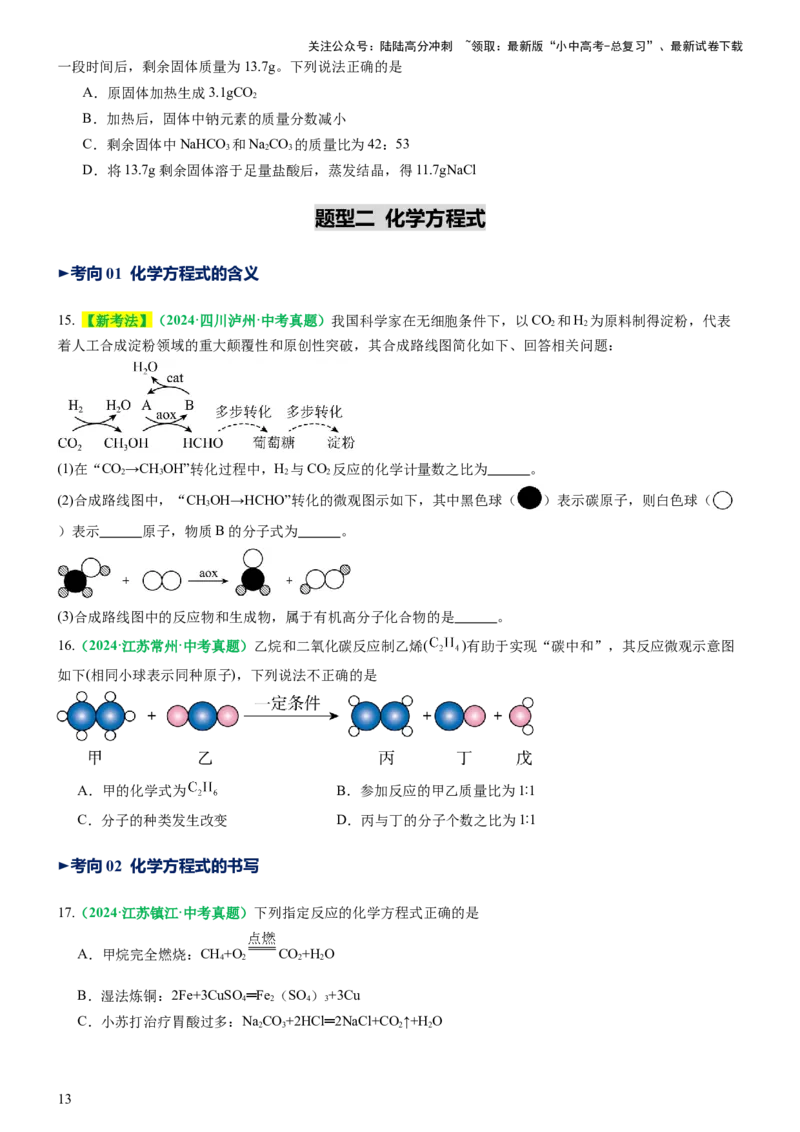
8.【新考法】(2024·吉林·中考真题)为探究铜的化学性质,某同学借助氧气传感器在密闭装置中进行下图所
示实验,观察实验现象并分析氧气含量随时间变化的曲线图。其中终点D(203,6.15%)表示时间为203秒时,
装置中氧气含量为6.15%。结合图示判断下列说法错误的是
A.加热前的空气样品中氧气含量为20.99%
B.铜在加热条件下能与氧气发生化学反应
C.拐点C至终点D所对应的时间范围内,装置内物质的总质量逐渐减少
D.通过现象证据和数据证据,可以从定性和定量的视角分析得出合理解释
►考向05 用质量守恒定律确定物质的组成
9.(2024·湖北·中考真题)在探究甲烷的元素组成时,做了如下图的两个实验。下列说法错误的是
A.燃烧时火焰呈(淡)蓝色 B.左侧烧杯内壁有小液滴产生
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.右侧烧杯内壁石灰水变浑浊 D.可得出甲烷含有氧元素
10.【新考向】(2024·河南商丘·一模)将某固体混合物加热熔化会发生化学反应,产物有 、 和
,推测该固体混合物不可能含有
A. B.KOH C. D.
►考向06 密闭容器中图表信息的相关计算
11.(2024·黑龙江·中考真题)密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前
后各物质的质量分数如图所示。下列说法错误的是
A.该反应基本反应类型为化合反应
B.该化学反应中乙、丙质量比为3∶17
C.物质丙可能为单质
D.物质丁可能是该反应的催化剂
12. 【新形式】(2024·四川乐山·中考真题)铁有多种氧化物,为探究其中一种氧化物 的组成,某同学将
和 置于密闭容器中在高温下发生反应.反应开始至某时刻,测得容器中部分物质的质量变化关
系如图所示.下列说法正确的是
A.a表示 的质量变化 B.
C. 中 D.
►考向07 巧用元素守恒进行计算
13.【新考向】(2024·四川广元·中考真题)乙醇(C HOH)是常用的燃料。现有4.6g乙醇与一定量氧气混合于密
2 5
闭容器内,在一定条件下反应物全部转化为一氧化碳、二氧化碳和水,恢复到室温,测得所得气体中氧元素质
量分数为70%,则参加反应的氧气质量为
A.6.4g B.8.0g C.8.8g D.9.6g
14. 【新考向】(2024·江苏镇江·中考真题)已知:2NaHCO NaCO+CO ↑+H O,将16.8gNaHCO 固体加热
3 2 3 2 2 3
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
一段时间后,剩余固体质量为13.7g。下列说法正确的是
A.原固体加热生成3.1gCO
2
B.加热后,固体中钠元素的质量分数减小
C.剩余固体中NaHCO 和NaCO 的质量比为42:53
3 2 3
D.将13.7g剩余固体溶于足量盐酸后,蒸发结晶,得11.7gNaCl
题型二 化学方程式
►考向01 化学方程式的含义
15. 【新考法】(2024·四川泸州·中考真题)我国科学家在无细胞条件下,以CO 和H 为原料制得淀粉,代表
2 2
着人工合成淀粉领域的重大颠覆性和原创性突破,其合成路线图简化如下、回答相关问题:
(1)在“CO→CHOH”转化过程中,H 与CO 反应的化学计量数之比为 。
2 3 2 2
(2)合成路线图中,“CHOH→HCHO”转化的微观图示如下,其中黑色球( )表示碳原子,则白色球(
3
)表示 原子,物质B的分子式为 。
(3)合成路线图中的反应物和生成物,属于有机高分子化合物的是 。
16.(2024·江苏常州·中考真题)乙烷和二氧化碳反应制乙烯( )有助于实现“碳中和”,其反应微观示意图
如下(相同小球表示同种原子),下列说法不正确的是
A.甲的化学式为 B.参加反应的甲乙质量比为1∶1
C.分子的种类发生改变 D.丙与丁的分子个数之比为1∶1
►考向02 化学方程式的书写
17.(2024·江苏镇江·中考真题)下列指定反应的化学方程式正确的是
A.甲烷完全燃烧:CH+O CO+H O
4 2 2 2
B.湿法炼铜:2Fe+3CuSO═Fe (SO )+3Cu
4 2 4 3
C.小苏打治疗胃酸过多:NaCO+2HCl═2NaCl+CO ↑+H O
2 3 2 2
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.汽车尾气中CO和NO催化转化为无毒气体:2NO+2CO N+2CO
2 2
18.(2023·江苏镇江·中考真题)下列指定反应的化学方程式不正确的是
A.实验室用KClO 制备:2KClO =2KCl+3O ↑
3 3 2
B.乙炔(C H)燃烧形成氧炔焰:2C H+5O 4CO+2H O
2 2 2 2 2 2 2
C.用石灰石浆吸收烟气中的二氧化硫:CaCO +SO+O =CaSO +CO
3 2 2 4 2
D.用氨水中和废水中的硫酸得到氮肥:2NH •H O+HSO =(NH )SO +2H O
3 2 2 4 4 2 4 2
►考向03 根据化学方程式推测化学式
19. 【新情境】(2024·江苏常州·中考真题)在电化学储能领域拥有巨大潜力的 可由以下化学反应制得:
,则可推测X是
A. B. C. D.
20. 【新考向】(2024·青海·中考真题)《天工开物》中有我国古代炼铁的记载,炼铁的主要原理是
,X的化学式为
A. B.CO C. D.
题型三 根据化学方程式的简单计算
►考向01 不含杂质的计算
21. (2024·内蒙古通辽·中考真题)赴九天,问苍穹,中国航天事业正蓬勃发展。我国自主研发的长征二号F型
运载火箭, 使用的火箭推进剂偏二甲肼(C HN)和四氧化二氮(N O)发生反应的化学方程式为:
2 8 2 2 4
C HN+2N O=2CO ↑+4H O↑+3N↑。请从理论上计算6g 偏二甲肼完全反应,需要四氧化二氮的质量是多少(请
2 8 2 2 4 2 2 2
写出计算过程)。
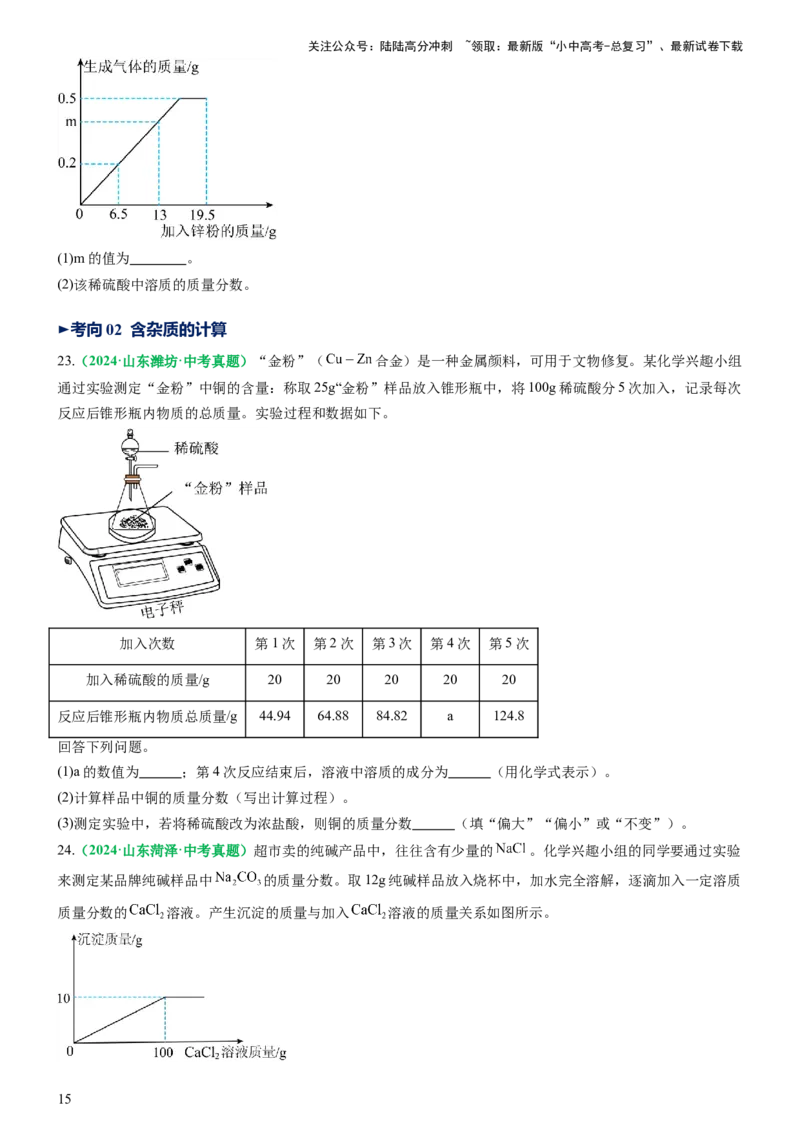
22. (2024·河北·中考真题)为测定某稀硫酸中溶质的质量分数,向盛有 该稀硫酸的烧杯中,分三次加入
一定质量的锌粉,生成气体的质量与加入锌粉质量的关系如图所示。请计算:
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)m的值为 。
(2)该稀硫酸中溶质的质量分数。
►考向02 含杂质的计算
23.(2024·山东潍坊·中考真题)“金粉”( 合金)是一种金属颜料,可用于文物修复。某化学兴趣小组
通过实验测定“金粉”中铜的含量:称取25g“金粉”样品放入锥形瓶中,将100g稀硫酸分5次加入,记录每次
反应后锥形瓶内物质的总质量。实验过程和数据如下。
加入次数 第1次 第2次 第3次 第4次 第5次
加入稀硫酸的质量/g 20 20 20 20 20
反应后锥形瓶内物质总质量/g 44.94 64.88 84.82 a 124.8
回答下列问题。
(1)a的数值为 ;第4次反应结束后,溶液中溶质的成分为 (用化学式表示)。
(2)计算样品中铜的质量分数(写出计算过程)。
(3)测定实验中,若将稀硫酸改为浓盐酸,则铜的质量分数 (填“偏大”“偏小”或“不变”)。
24.(2024·山东菏泽·中考真题)超市卖的纯碱产品中,往往含有少量的 。化学兴趣小组的同学要通过实验
来测定某品牌纯碱样品中 的质量分数。取12g纯碱样品放入烧杯中,加水完全溶解,逐滴加入一定溶质
质量分数的 溶液。产生沉淀的质量与加入 溶液的质量关系如图所示。
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)完全反应后,生成沉淀的质量为 g。
(2)计算纯碱样品中 的质量分数。(精确到0.1%)
16