文档内容
绝密★启用前 A. M B. M2+ C.M3+ D. MO2+
2012 年普通高等学校招生全国统一考试 二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若
化 学 正确答案只包括一个选项,多选得 0分;若正确答案包括两个选项,只选一个且正确得 2分,选
两个且都正确得4分,但只要选错一个就得0分。
注意事项:
7.N 为阿伏加德罗常数的数值,下列说法中正确的是
A
1本试卷分第I卷(选择题)和第ll卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号填写在
A.在密闭容器中加入l.5mol H 和0.5molN ,充分反应后可得到NH 分子数为N B.一定条件下,2.3g
2 2 3 A
答题卡上。
的Na完全与O 反应生成3.6g产物时失去的电子数为0.1N C.1.0L的0.1 mol·L-1Na S溶液中含有的S2-
2 A 2
2回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦 离子数为0.1N
A
干净后,再选涂其它答案标号。写在本试卷上无效。 D.标准状况下,22.4L的CCl 中含有的CCl 分子数为N
4 4 A
3回答第II卷时,将答案写在答题卡上。写在本试卷上无效。 8.两种盐的固体混合物:①加热时有气体产生,②加水溶解时有沉淀生成,且沉淀溶于稀盐酸。满足上述条件
的混合物是
4考试结束后,将本试卷和答题卡 一并交回。
可能用到的相对原子质量:H1 C 12 N14 O16 Na 23 C1 35.5 Zn 65 A . BaCl 2 和(NH 4 ) 2 S0 4 B . AgNO 3 和NH 4 Cl
C.FeCl 和NaHCO D. KCl和Na CO
第 I 卷 3 3 2 3
9.下列有关化学用语使用正确的是
一、选择题:本题共6小题,每小题2分,共12分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.化学与环境密切相关,下列有关说法正确的是 A.NH Br的电子式: B.S2-的结构示意图:
4
A.CO 属于大气污染物 C.乙酸的分子式: CH COOH D.原子核内有l8个中子的氯原子:
2 3
B.酸雨是PH小于7的雨水 10.下列叙述错误的是
C.CO 、NO 或SO 都会导致酸雨的形成 A.生铁中含有碳,抗腐蚀能力比纯铁弱
2 2 2
D.大气中CO 含量的增加会导致温室效应加剧 B.用锡焊接的铁质器件,焊接处易生锈
2
2.下列说法正确的是 C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
A.食用白糖的主要成分是蔗糖 B.小苏打的主要成分是碳酸钠 D.铁管上镶嵌锌块,铁管不易被腐蚀
C.煤气的主要成分是丁烷 D.植物油的主要成分是高级脂肪酸 11.25℃时,a mol·L-1一元酸HA与b mol·L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是
3.下列各组中,每种电解质溶液电解时只生成氢气和氧气的是 A.a=b B.a>b C.c (A-)= c(Na+) D.c (A-)< c(Na+)
A. HCl、 CuCl 、 Ba(OH) B. NaOH、CuSO 、 H SO 12.能正确表示下列反应的离子方程式为
2 2 4 2 4
C. NaOH、H 2 SO 4 、 Ba(OH) 2 D. NaBr、 H 2 SO 4 、 Ba(OH) 2 A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO 3 -+OH–= CO 3 2-+ H 2 O
4.下列实验操作正确的是 B.二氧化硫通入次氯酸钠溶液:SO
2
+ ClO- + 2OH–= SO
4
2-+Cl-+ H
2
O
A.可用氨水除去试管内壁上的银镜 C.硫化钡加入稀硫酸:BaS + 2H+ = H
2
S↑+ Ba2+
B.硅酸钠溶液应保存在带玻璃塞的试剂瓶中 D.新制的氧化铝可溶于氢氧化钠溶液:Al
2
O
3
+2OH–=2AlO
2
–+H
2
O
C.将三氯化铁溶液蒸干,可制得无水三氯化铁 第 II 卷
D.锌与稀硫酸反应时,要加大反应速率可滴加少量硫酸铜
本卷包括必考题和选考题两部分。第 l3题~第17题为必考题,每个试题考生都必需做答。第
5.分子式为C H 的单取代芳烃,其可能的结构有
10 14 l8题~第20题为选考题,考生根据要求做答。
A.2种 B.3种 C.4种 D.5种
13.(8分)
6.将0.195g锌粉加入到200mL的0.100 mol·L-1MO +溶液中,恰好完全反应,则还原产物可能是
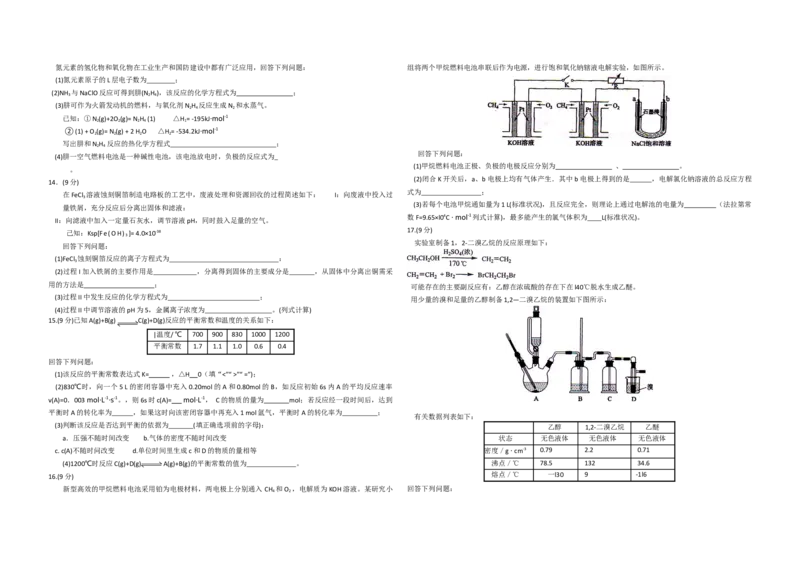
2氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题: 组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图所示。
(1)氮元素原子的L层电子数为 ;
(2)NH 与NaClO反应可得到肼(N H ),该反应的化学方程式为 ;
3 2 4
(3)肼可作为火箭发动机的燃料,与氧化剂N H 反应生成N 和水蒸气。
2 4 2
已知:①N (g)+2O (g)= N H (1) △H = -195kJ·mol-1
2 2 2 4 1
② (1) + O (g)= N (g) + 2 H O △H = -534.2kJ·mol-1
2 2 2 2
写出肼和N H 反应的热化学方程式 ;
2 4
回答下列问题:
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程
14.(9分)
式为 ;
在FeCl 溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下: I:向废液中投入过
3
(3)若每个电池甲烷通如量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为 (法拉第常
量铁屑,充分反应后分离出固体和滤液:
数F=9.65×l04C · mol-1列式计算),最多能产生的氯气体积为 L(标准状况)。
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
17.(9分)
己知:Ksp[Fe(OH) ]= 4.0×10-38
3
实验室制备1,2-二溴乙烷的反应原理如下:
回答下列问题:
(1)FeCl 蚀刻铜箔反应的离子方程式为 :
3
(2)过程I 加入铁屑的主要作用是 ,分离得到固体的主要成分是 ,从固体中分离出铜需采
用的方法是 ;
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
(3)过程II中发生反应的化学方程式为 ;
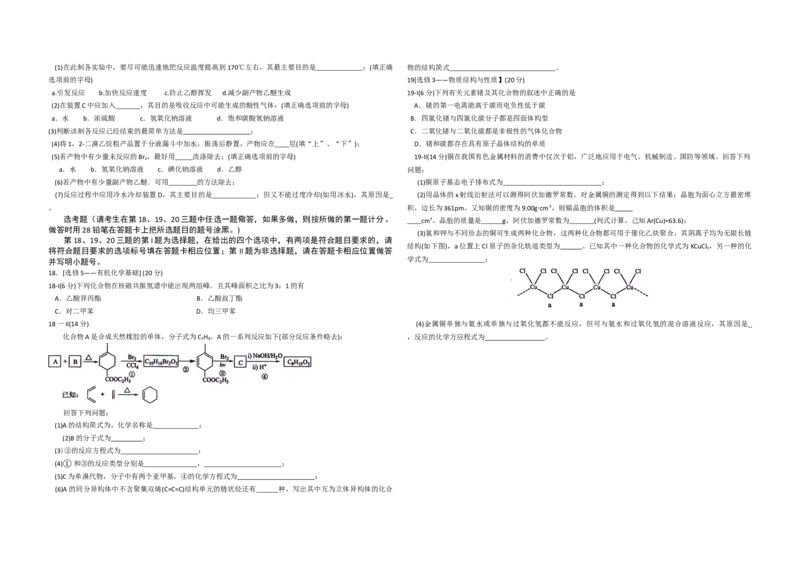
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
(4)过程II中调节溶液的pH为5,金属离子浓度为 。(列式计算)
15.(9分)已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ 700 900 830 1000 1200
平衡常数 1.7 1.1 1.0 0.6 0.4
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率
v(A)=0.003 mol·L-1·s-1。,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到
平衡时A的转化率为 ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
有关数据列表如下:
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母): 乙醇 1,2-二溴乙烷 乙醚
a.压强不随时间改变 b.气体的密度不随时间改变 状态 无色液体 无色液体 无色液体
c. c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等 密度/g · cm-3 0.79 2.2 0.71
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为 。 沸点/℃ 78.5 132 34.6
16.(9分) 熔点/℃ 一l30 9 -1l6
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入 CH 和O ,电解质为KOH溶液。某研究小 回答下列问题:
4 2(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确 物的结构简式 。
选项前的字母) 19[选修3——物质结构与性质】(20分)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成 19-I(6分)下列有关元素锗及其化合物的叙述中正确的是
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母) A.锗的第一电离能高于碳而电负性低于碳
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液 B.四氯化锗与四氯化碳分子都是四面体构型
(3)判断该制各反应已经结束的最简单方法是 ; C.二氧化锗与二氧化碳都是非极性的气体化合物
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”、“下”); D.锗和碳都存在具有原子晶体结构的单质
(5)若产物中有少量未反应的Br ,最好用 洗涤除去;(填正确选项前的字母) 19-II(14分)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列
2
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 问题:
(6)若产物中有少量副产物乙醚.可用 的方法除去; (1)铜原子基态电子排布式为 ;
(7)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 (2)用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆
。 积,边长为361pm。又知铜的密度为9.00g·cm-3,则镉晶胞的体积是
选考题(请考生在第18、19、20三题中任选一题儆答,如果多做,则按所做的第一题计分。 cm3、晶胞的质量是 g,阿伏加德罗常数为 (列式计算,己知Ar(Cu)=63.6);
做答时用28铅笔在答题卡上把所选题目的题号涂黑。)
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链
第18、19、20三题的第I题为选择题,在给出的四个选项中,有两项是符合题目要求的,请
结构(如下图),a位置上Cl原子的杂化轨道类型为 。已知其中一种化合物的化学式为KCuCl ,另一种的化
将符合题目要求的选项标号填在答题卡相应位置;第 II题为非选择题,请在答题卡相应位置做答 3
学式为 ;
并写明小题号。
18.[选修5——有机化学基础] (20分)
18-I(6分)下列化合物在核磁共振氢谱中能出现两组峰.且其峰面积之比为3:1的有
A.乙酸异丙酯 B.乙酸叔丁酯
C.对二甲苯 D.均三甲苯
18一II(14分) (4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
化合物A是合成天然橡胶的单体,分子式为C H 。A的一系列反应如下(部分反应条件略去): ,反应的化学方应程式为 。
5 8
回答下列问题:
(1)A的结构简式为,化学名称是 ;
(2)B的分子式为 ;
(3)②的反应方程式为 ;
(4)①和③的反应类型分别是 , ;
(5)C为单溴代物,分子中有两个亚甲基,④的化学方程式为 :
(6)A的同分异构体中不含聚集双烯(C=C=C)结构单元的链状烃还有 种,写出其中互为立体异构体的化合