文档内容
2019 年北京市高考化学试卷
一、选择题:本部分共7小题,每小题6分,共42分。在每小题列出的四个选项中,选出最符合题目要求的一
项。
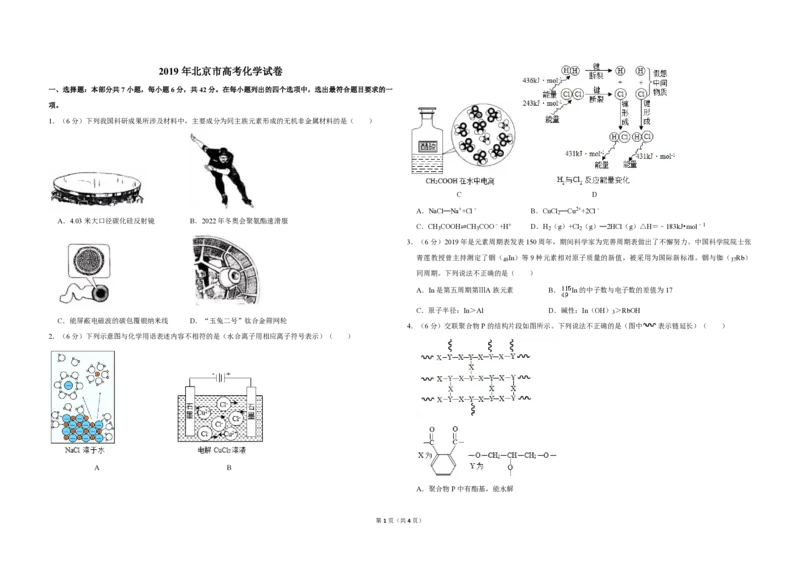
1.(6分)下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是( )
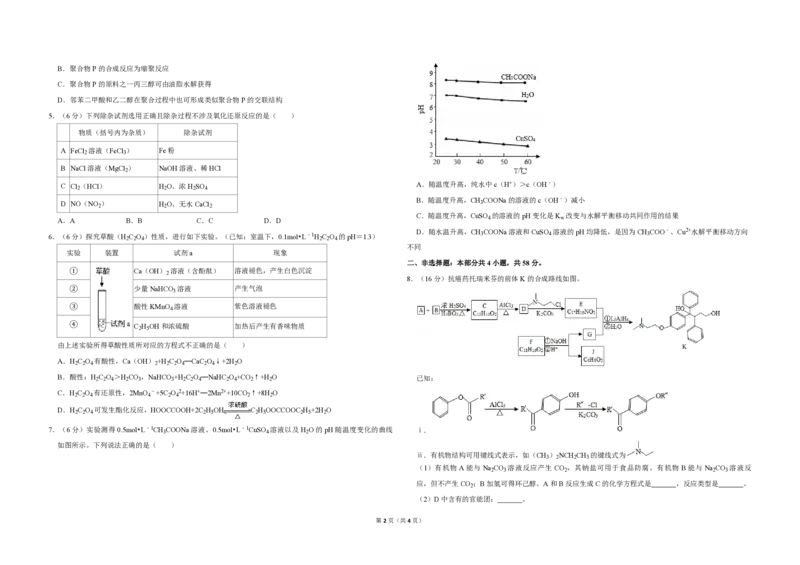
C D
A.NaCl═Na++Cl﹣ B.CuCl ═Cu2++2Cl﹣
2
A.4.03米大口径碳化硅反射镜 B.2022年冬奥会聚氨酯速滑服
C.CH COOH⇌CH COO﹣+H+ D.H (g)+Cl (g)═2HCl(g)△H=﹣183kJ•mol﹣1
3 3 2 2
3.(6分)2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张
青莲教授曾主持测定了铟( In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷( Rb)
49 37
同周期。下列说法不正确的是( )
A.In是第五周期第ⅢA族元素 B. In的中子数与电子数的差值为17
C.原子半径:In>Al D.碱性:In(OH) >RbOH
3
C.能屏蔽电磁波的碳包覆银纳米线 D.“玉兔二号”钛合金筛网轮
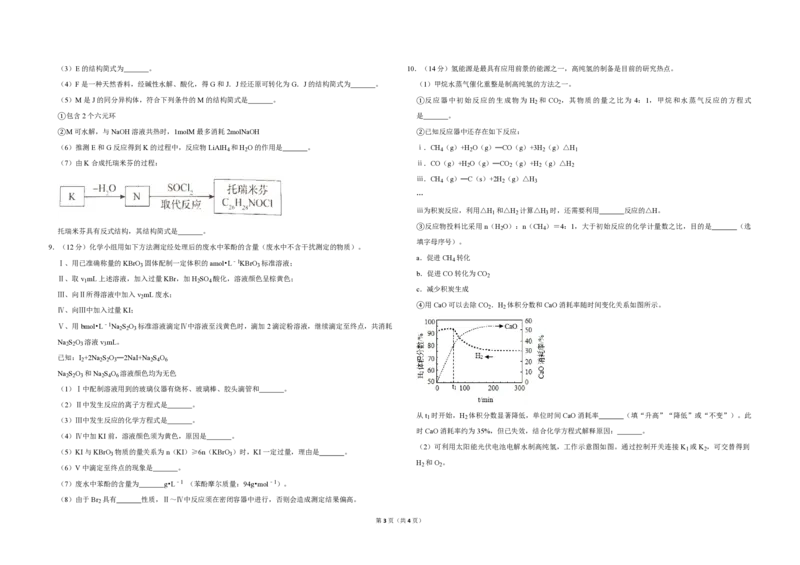
4.(6分)交联聚合物P的结构片段如图所示。下列说法不正确的是(图中 表示链延长)( )
2.(6分)下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)( )
A B
A.聚合物P中有酯基,能水解
第1页(共4页)B.聚合物P的合成反应为缩聚反应
C.聚合物P的原料之一丙三醇可由油脂水解获得
D.邻苯二甲酸和乙二醇在聚合过程中也可形成类似聚合物P的交联结构
5.(6分)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl (HCl) H O、浓H SO
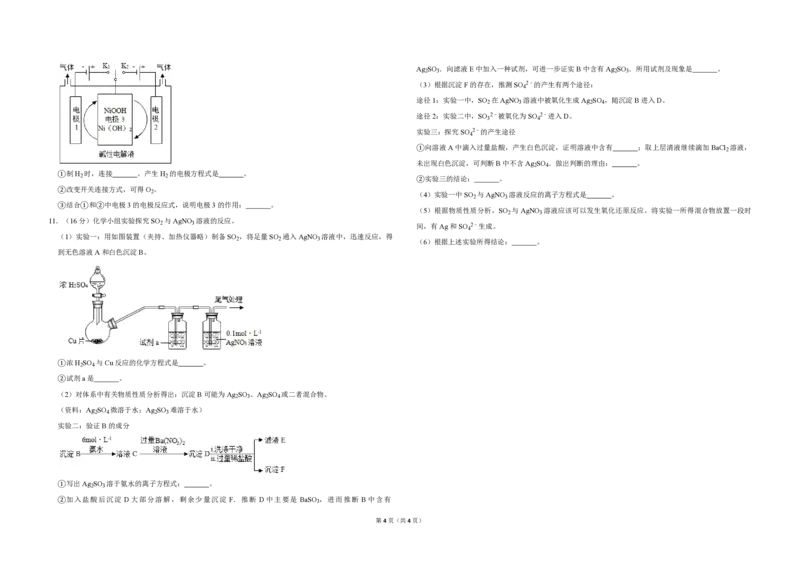
A.随温度升高,纯水中c(H+)>c(OH﹣)
2 2 2 4
B.随温度升高,CH COONa的溶液的c(OH﹣)减小
D NO(NO ) H O、无水CaCl 3
2 2 2
C.随温度升高,CuSO 的溶液的pH变化是K 改变与水解平衡移动共同作用的结果
A.A B.B C.C D.D 4 w
D.随水温升高,CH COONa溶液和CuSO 溶液的pH均降低,是因为CH COO﹣、Cu2+水解平衡移动方向
6.(6分)探究草酸(H C O )性质,进行如下实验。(已知:室温下,0.1mol•L﹣1H C O 的pH=1.3) 3 4 3
2 2 4 2 2 4
不同
实验 装置 试剂a 现象
二、非选择题:本部分共4小题,共58分。
① Ca(OH) 溶液(含酚酞) 溶液褪色,产生白色沉淀
2
8.(16分)抗癌药托瑞米芬的前体K的合成路线如图。
② 少量NaHCO 溶液 产生气泡
3
③ 酸性KMnO 溶液 紫色溶液褪色
4
④ C H OH和浓硫酸 加热后产生有香味物质
2 5
由上述实验所得草酸性质所对应的方程式不正确的是( )
A.H C O 有酸性,Ca(OH) +H C O ═CaC O ↓+2H O
2 2 4 2 2 2 4 2 4 2
B.酸性:H 2 C 2 O 4 >H 2 CO 3 ,NaHCO 3 +H 2 C 2 O 4 ═NaHC 2 O 4 +CO 2 ↑+H 2 O 已知:
C.H C O 有还原性,2MnO ﹣+5C O 2+16H+═2Mn2++10CO ↑+8H O
2 2 4 4 2 4 2 2
D.H C O 可发生酯化反应,HOOCCOOH+2C H OH C H OOCCOOC H +2H O
2 2 4 2 5 2 5 2 5 2
7.(6分)实验测得0.5mol•L﹣1CH
3
COONa溶液、0.5mol•L﹣1CuSO
4
溶液以及H
2
O的pH随温度变化的曲线 ⅰ.
如图所示。下列说法正确的是( )
ⅱ.有机物结构可用键线式表示,如(CH ) NCH CH 的键线式为
3 2 2 3
(1)有机物 A能与 Na CO 溶液反应产生 CO ,其钠盐可用于食品防腐。有机物 B能与 Na CO 溶液反
2 3 2 2 3
应,但不产生CO ;B加氢可得环己醇。A和B反应生成C的化学方程式是 ,反应类型是 。
2
(2)D中含有的官能团: 。
第2页(共4页)(3)E的结构简式为 。 10.(14分)氢能源是最具有应用前景的能源之一,高纯氢的制备是目前的研究热点。
(4)F是一种天然香料,经碱性水解、酸化,得G和J.J经还原可转化为G.J的结构简式为 。 (1)甲烷水蒸气催化重整是制高纯氢的方法之一。
(5)M是J的同分异构体,符合下列条件的M的结构简式是 。 ①反应器中初始反应的生成物为 H 和 CO ,其物质的量之比为 4:1,甲烷和水蒸气反应的方程式
2 2
①包含2个六元环 是 。
②M可水解,与NaOH溶液共热时,1molM最多消耗2molNaOH ②已知反应器中还存在如下反应:
(6)推测E和G反应得到K的过程中,反应物LiAlH 和H O的作用是 。 ⅰ.CH (g)+H O(g)═CO(g)+3H (g)△H
4 2 4 2 2 1
(7)由K合成托瑞米芬的过程: ⅱ.CO(g)+H O(g)═CO (g)+H (g)△H
2 2 2 2
ⅲ.CH (g)═C(s)+2H (g)△H
4 2 3
…
ⅲ为积炭反应,利用△H 和△H 计算△H 时,还需要利用 反应的△H。
1 2 3
③反应物投料比采用n(H O):n(CH )=4:1,大于初始反应的化学计量数之比,目的是 (选
托瑞米芬具有反式结构,其结构简式是 。 2 4
填字母序号)。
9.(12分)化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
a.促进CH 转化
Ⅰ、用已准确称量的KBrO 固体配制一定体积的amol•L﹣1KBrO 标准溶液; 4
3 3
b.促进CO转化为CO
2
Ⅱ、取v mL上述溶液,加入过量KBr,加H SO 酸化,溶液颜色呈棕黄色;
1 2 4
c.减少积炭生成
Ⅲ、向Ⅱ所得溶液中加入v mL废水;
2
④用CaO可以去除CO .H 体积分数和CaO消耗率随时间变化关系如图所示。
Ⅳ、向Ⅲ中加入过量KI; 2 2
Ⅴ、用bmol•L﹣1Na S O 标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
2 2 3
Na S O 溶液v mL。
2 2 3 3
已知:I +2Na S O ═2NaI+Na S O
2 2 2 3 2 4 6
Na S O 和Na S O 溶液颜色均为无色
2 2 3 2 4 6
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
(2)Ⅱ中发生反应的离子方程式是 。
从t 时开始,H 体积分数显著降低,单位时间CaO消耗率 (填“升高”“降低”或“不变”)。此
(3)Ⅲ中发生反应的化学方程式是 。 1 2
时CaO消耗率约为35%,但已失效,结合化学方程式解释原因: 。
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是 。
(2)可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制开关连接K 或K ,可交替得到
1 2
(5)KI与KBrO 物质的量关系为n(KI)≥6n(KBrO )时,KI一定过量,理由是 。
3 3
H 和O 。
(6)V中滴定至终点的现象是 。 2 2
(7)废水中苯酚的含量为 g•L﹣1 (苯酚摩尔质量:94g•mol﹣1)。
(8)由于Br 具有 性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果偏高。
2
第3页(共4页)Ag SO .向滤液E中加入一种试剂,可进一步证实B中含有Ag SO .所用试剂及现象是 。
2 3 2 3
(3)根据沉淀F的存在,推测SO 2﹣的产生有两个途径:
4
途径1:实验一中,SO 在AgNO 溶液中被氧化生成Ag SO ,随沉淀B进入D。
2 3 2 4
途径2:实验二中,SO 2﹣被氧化为SO 2﹣进入D。
3 4
实验三:探究SO 2﹣的产生途径
4
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有 ;取上层清液继续滴加BaCl 溶液,
2
未出现白色沉淀,可判断B中不含Ag SO .做出判断的理由: 。
2 4
①制H 时,连接 。产生H 的电极方程式是 。
2 2 ②实验三的结论: 。
②改变开关连接方式,可得O 。
2
(4)实验一中SO 与AgNO 溶液反应的离子方程式是 。
2 3
③结合①和②中电极3的电极反应式,说明电极3的作用: 。
(5)根据物质性质分析,SO 与AgNO 溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时
2 3
11.(16分)化学小组实验探究SO 与AgNO 溶液的反应。
2 3 间,有Ag和SO 2﹣生成。
4
(1)实验一:用如图装置(夹持、加热仪器略)制备SO ,将足量SO 通入AgNO 溶液中,迅速反应,得
2 2 3 (6)根据上述实验所得结论: 。
到无色溶液A和白色沉淀B。
①浓H SO 与Cu反应的化学方程式是 。
2 4
②试剂a是 。
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag SO 、Ag SO 或二者混合物。
2 3 2 4
(资料:Ag SO 微溶于水;Ag SO 难溶于水)
2 4 2 3
实验二:验证B的成分
①写出Ag SO 溶于氨水的离子方程式: 。
2 3
②加入盐酸后沉淀 D大部分溶解,剩余少量沉淀 F.推断 D中主要是 BaSO ,进而推断 B中含有
3
第4页(共4页)