文档内容
炎德·英才大联考长郡中学 2025 届高三月考试卷(二)
化学
得分:__________
本试题卷分选择题和非选择题两部分,共8页。时量75分钟,满分100分。
可能用到的相对原子质量:H~1 C~12 O~16 Na~23 Al~27 S~32
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。)
1.在巴黎奥运会舞台上,科技与体育双向奔赴,释放更加迷人的魅力。下列说法不正确的是
A.奥运火炬燃料中的丙烷、丁烷属于烃
B.生产橡胶弹性地板的原料天然橡胶是异戊二烯的聚合物
C.中国队领奖服采用的环保再生纤维材料为有机高分子材料
D.比赛乒乓球台可变灯光系统的控制芯片的主要成分为
2.下列化学用语表示正确的是
A.NH Cl的电子式:
4
B.铜的基态原子的简化电子排布式:
C. 的VSEPR模型:
D.HCl中σ键的电子云轮廓图:
3.实验室在进行“电解CuCl 溶液”实验时,与该实验无关的安全注意事项是
2
A.正确使用火源 B.小心用电 C.实验后洗手 D.开启排风扇
4.下列有关物质结构与性质的说法错误的是
A.酸性强弱:氯乙酸>乙酸>丙酸
B.邻羟甲基苯甲醛的沸点低于对羟甲基苯甲醛
C.O 是含有极性键的强极性分子,它在四氯化碳中的溶解度低于在水中的溶解度
3
D.由 与 。构成的离子液体常温下呈液态,与其离子的体积较大有关
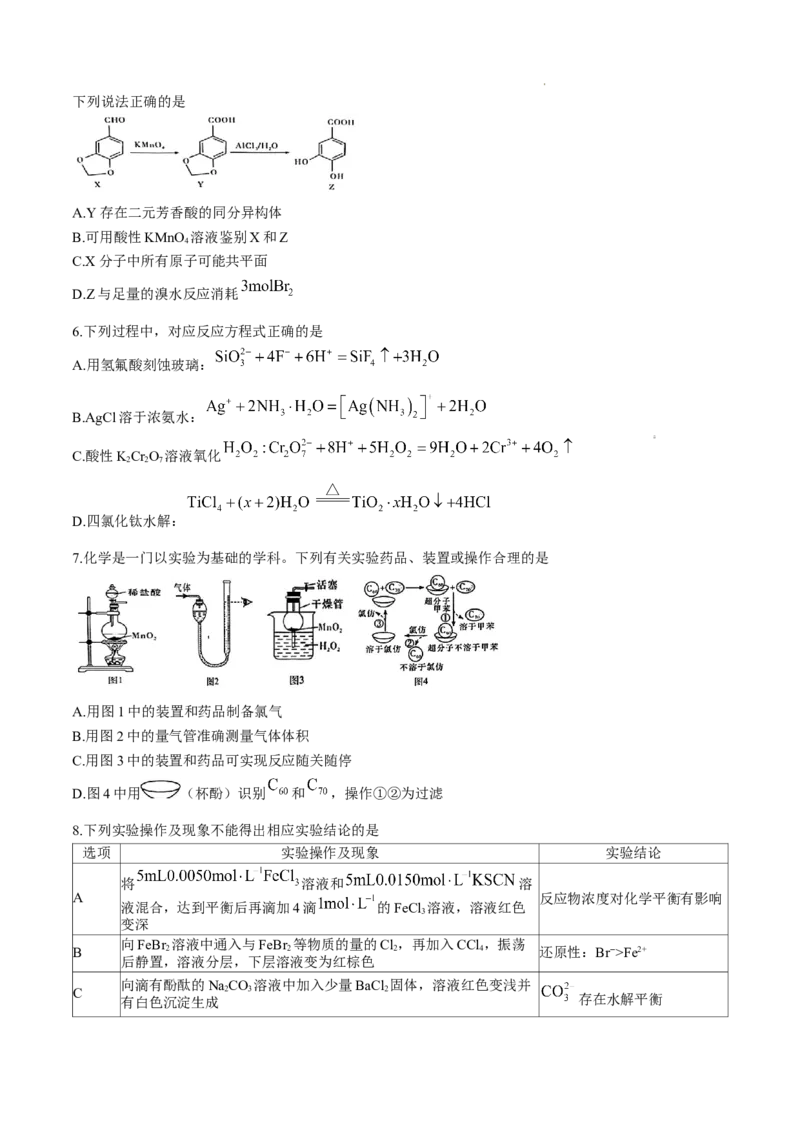
5.原儿茶酸(Z)具有抗菌、抗氧化作用,常用于治疗烧伤、小儿肺炎等疾病,可采用如图所示路线合成。
学科网(北京)股份有限公司下列说法正确的是
A.Y存在二元芳香酸的同分异构体
B.可用酸性KMnO 溶液鉴别X和Z
4
C.X分子中所有原子可能共平面
D.Z与足量的溴水反应消耗
6.下列过程中,对应反应方程式正确的是
A.用氢氟酸刻蚀玻璃:
B.AgCl溶于浓氨水:
C.酸性KCr O 溶液氧化
2 2 7
D.四氯化钛水解:
7.化学是一门以实验为基础的学科。下列有关实验药品、装置或操作合理的是
A.用图1中的装置和药品制备氯气
B.用图2中的量气管准确测量气体体积
C.用图3中的装置和药品可实现反应随关随停
D.图4中用 (杯酚)识别 和 ,操作①②为过滤
8.下列实验操作及现象不能得出相应实验结论的是
选项 实验操作及现象 实验结论
将 溶液和 溶
A 反应物浓度对化学平衡有影响
液混合,达到平衡后再滴加4滴 的FeCl 溶液,溶液红色
3
变深
向FeBr 溶液中通入与FeBr 等物质的量的Cl,再加入CCl ,振荡
B 2 2 2 4 还原性:Br⁻>Fe2+
后静置,溶液分层,下层溶液变为红棕色
向滴有酚酞的NaCO 溶液中加入少量BaCl 固体,溶液红色变浅并
C 2 3 2
有白色沉淀生成 存在水解平衡
学科网(北京)股份有限公司
(1常温下,将 晶体研细后与NH Cl晶体置于烧杯
4 与NH Cl反
D 4
中,快速搅拌混合物,并触摸杯壁,杯壁变凉,同时闻到刺激性气
应对应的 和 均大于0
味
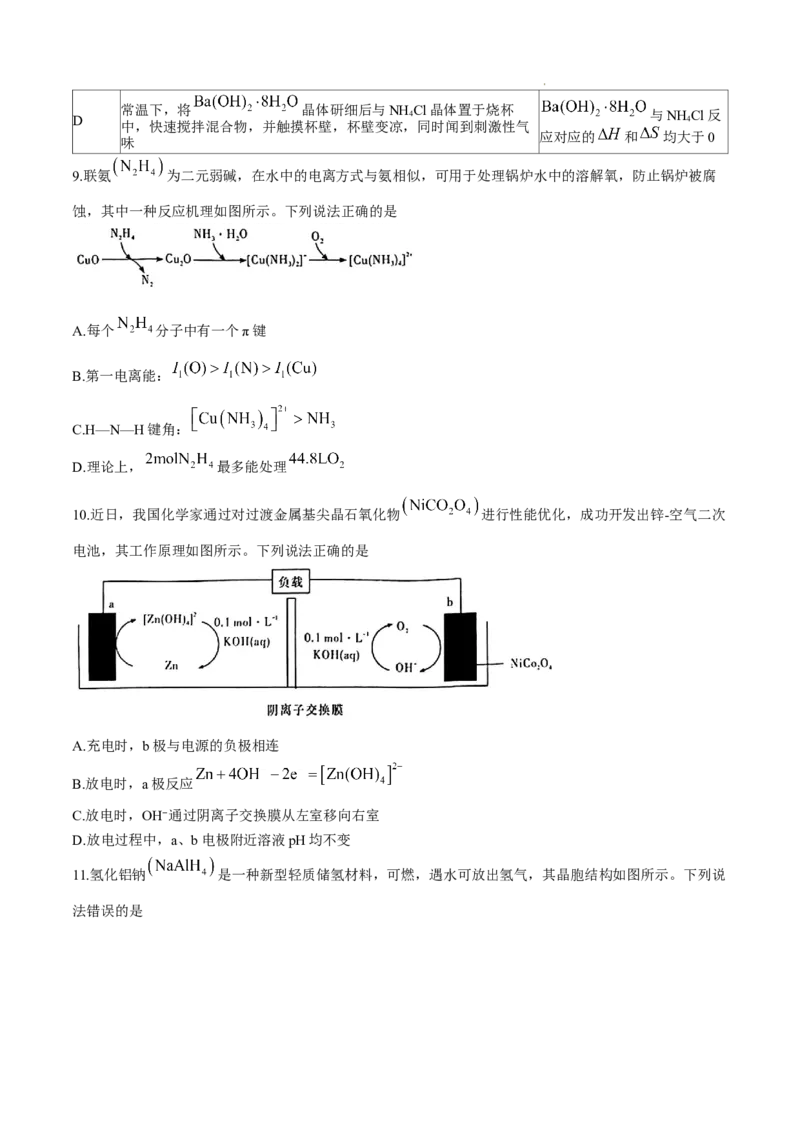
9.联氨 为二元弱碱,在水中的电离方式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐
蚀,其中一种反应机理如图所示。下列说法正确的是
A.每个 分子中有一个π键
B.第一电离能:
C.H—N—H键角:
D.理论上, 最多能处理
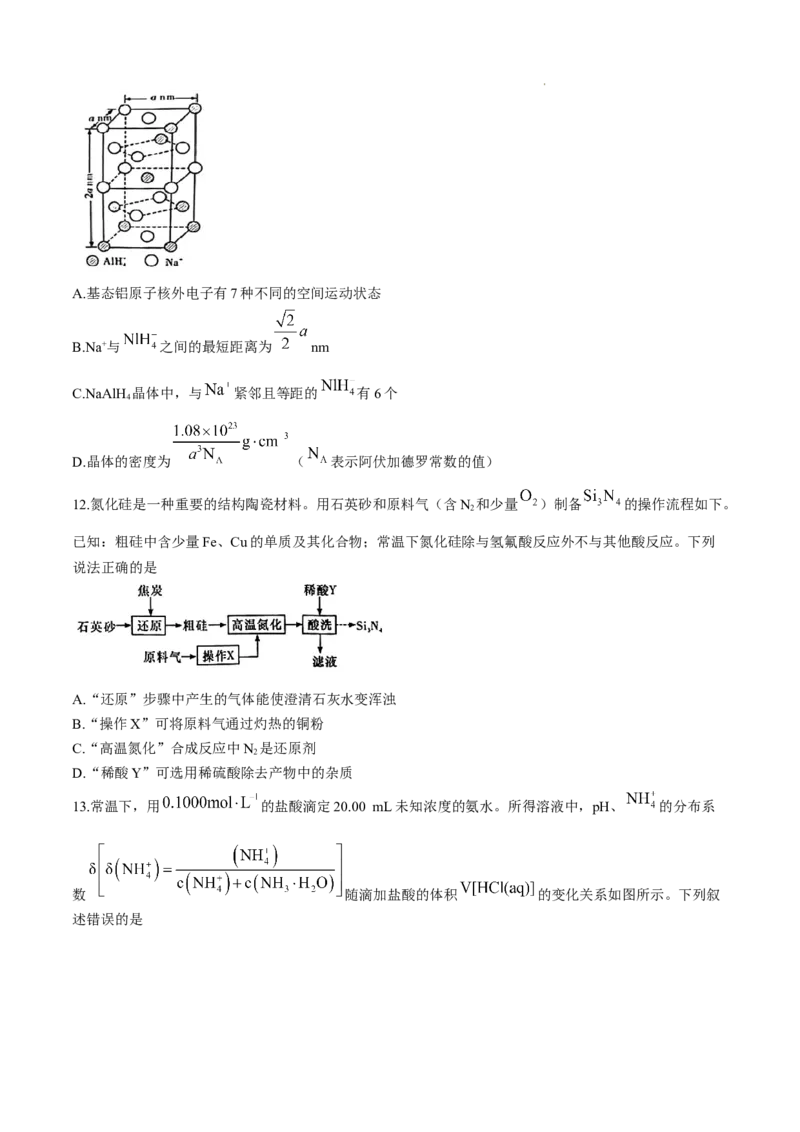
10.近日,我国化学家通过对过渡金属基尖晶石氧化物 进行性能优化,成功开发出锌-空气二次
电池,其工作原理如图所示。下列说法正确的是
A.充电时,b极与电源的负极相连
B.放电时,a极反应
C.放电时,OH⁻ 通过阴离子交换膜从左室移向右室
D.放电过程中,a、b电极附近溶液pH均不变
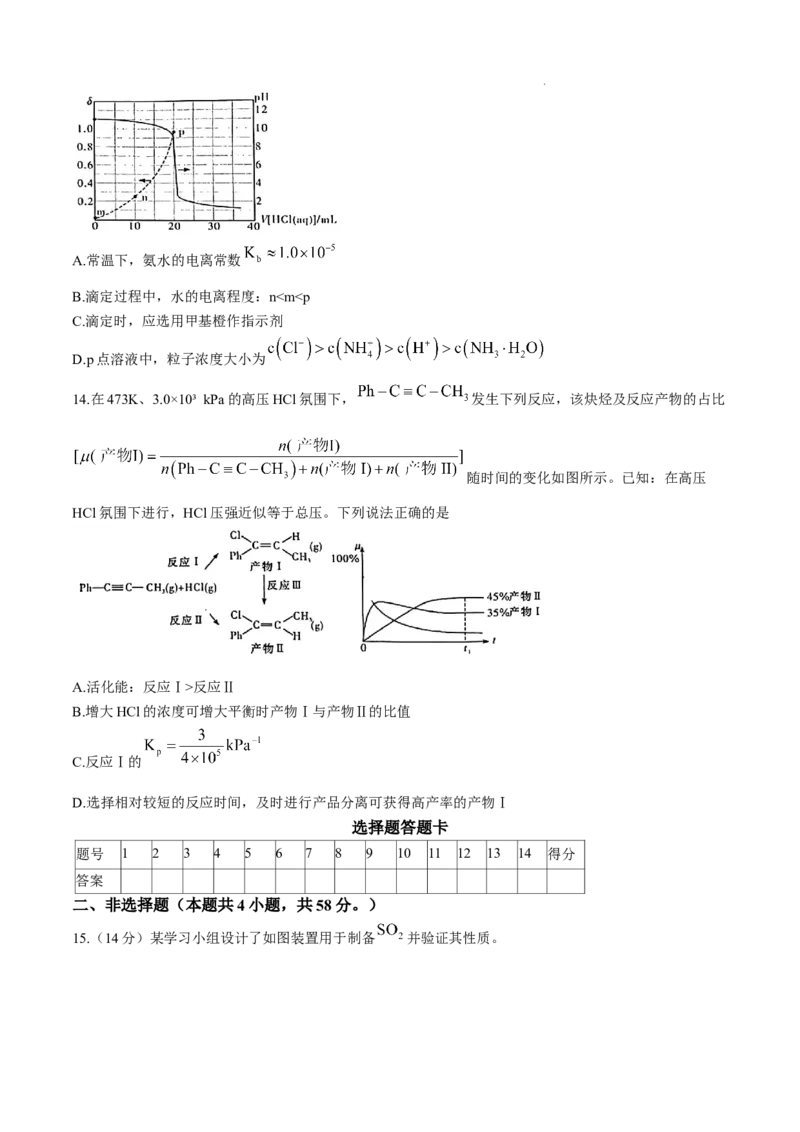
11.氢化铝钠 是一种新型轻质储氢材料,可燃,遇水可放出氢气,其晶胞结构如图所示。下列说
法错误的是
学科网(北京)股份有限公司A.基态铝原子核外电子有7种不同的空间运动状态
B.Na+与 之间的最短距离为 nm
C.NaAlH 晶体中,与 紧邻且等距的 有6个
4
D.晶体的密度为 ( 表示阿伏加德罗常数的值)
12.氮化硅是一种重要的结构陶瓷材料。用石英砂和原料气(含N 和少量 )制备 的操作流程如下。
2
已知:粗硅中含少量Fe、Cu的单质及其化合物;常温下氮化硅除与氢氟酸反应外不与其他酸反应。下列
说法正确的是
A.“还原”步骤中产生的气体能使澄清石灰水变浑浊
B.“操作X”可将原料气通过灼热的铜粉
C.“高温氮化”合成反应中N 是还原剂
2
D.“稀酸Y”可选用稀硫酸除去产物中的杂质
13.常温下,用 的盐酸滴定20.00 mL未知浓度的氨水。所得溶液中,pH、 的分布系
数 随滴加盐酸的体积 的变化关系如图所示。下列叙
述错误的是
学科网(北京)股份有限公司A.常温下,氨水的电离常数
B.滴定过程中,水的电离程度:n反应Ⅱ
B.增大HCl的浓度可增大平衡时产物Ⅰ与产物Ⅱ的比值
C.反应Ⅰ的
D.选择相对较短的反应时间,及时进行产品分离可获得高产率的产物Ⅰ
选择题答题卡
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 得分
答案
二、非选择题(本题共4小题,共58分。)
15.(14分)某学习小组设计了如图装置用于制备 并验证其性质。
学科网(北京)股份有限公司(1)装置A中导管a的作用为________________________________________。
(2)装置B溶液褪色,下列物质均能使品红溶液褪色,其褪色原理基本相同的是________(填标号)。
①活性炭 ②新制氯水 ③二氧化硫 ④臭氧 ⑤过氧化钠 ⑥双氧水
A.①②④ B.②③⑤ C.②④⑤⑥ D.③④⑥
该实验小组的同学甲为了进一步探究 的漂白性,将 和 按照相同的气体流速缓慢通入如下图所
示装置中进行实验,发现品红溶液几乎不褪色。请对该实验现象做出合理解释:
______________________________(用离子方程式表示)。
(3)该实验小组的同学乙利用下图所示装置测定空气中 的含量,若管道中空气流量为a L/min,经过
b min,酸性 溶液恰好褪色,假定样品中的 可被充分吸收,则该空气中 的含量为
________g/L。
(4)装置D中发生反应的化学方程式为________________________________。
(5)该实验小组的同学丙预测装置E中没有白色沉淀产生,但随着反应的进行,发现装置E中产生了少
量白色沉淀。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的 和
溶液,进行如下图所示实验(已知:E与G中所用 溶液的浓度相同):
学科网(北京)股份有限公司烧杯 实验现象
G 无白色沉淀产生,pH传感器测得溶液pH=5.3
H 有白色沉淀产生
I 有白色沉淀产生,I中出现白色沉淀比H中快且多
①据G中现象推测E中产生的白色沉淀的化学式是________________。
②据Ⅰ中出现白色沉淀的速率比H中快的现象,推测其原因可能是_______________________________。
16.(14分)蓝铜矿主要含 ,还含有少量Fe、Si的化合物,工业上以蓝铜矿为原料制
备Cu及 的方法有多种,常见的一种方法的具体步骤如下:
请回答下列问题:
(1)蓝铜矿与焦炭加热可以生成铜、二氧化碳和水,写出该反应的化学方程式:
____________________________________________________________________。
(2)由溶液C获得 ,需要经过加热蒸发、冷却结晶、过滤等操作,加热蒸发至
______________时停止加热。玻璃棒在整个操作中的作用是____________________________、
_________________________。
(3)制备 时,为防止实验过程中有氨气逸出,可选用下列______装置吸收尾气(填标号)。
(4)向硫酸铜溶液中逐滴加入氨水,形成蓝色沉淀,继续滴加氨水;沉淀溶解,得到深蓝色的透明溶液,
再加入乙醇后,析出深蓝色的晶体,请写出该深蓝色晶体的化学式:___________________。
(5) 的结构示意图如下, 中存在的化学键有________(填标号)。
学科网(北京)股份有限公司A.离子键 B.普通共价键 C.配位键 D.氢键
(6)用惰性电极电解硫酸铜溶液一段时间后,加入 固体使硫酸铜溶液复原(复原是指溶
液溶质成分及浓度与原来完全相同),则此电解过程中共转移电子________mol。
17.(14分)研究 与 的反应使之转化为合成气( 和CO)对减缓燃料危机、减轻温室效应具有
重大意义。
(1)若已知相关反应的能量变化如图所示:
则 与 转化为合成气的热化学方程式为___________________________。 和 分子中的中
心原子的价层电子对数均为________。
(2)一定温度下,在容积恒为2L的密闭容器中,充入等物质的量的 与 ,加入催化剂
使其发生反应制备合成气。
①3 min内 减少了2.4 g。则3 min内的平均速率 =_________
②下列说法正确的是_________(填标号)。
A.高温低压有利于提高 的平衡转化率
B.使用催化剂可以提高反应速率和 的平衡转化率
C.容器内的总压强不再变化,说明该反应已达到平衡状态
D.混合气体的密度不再变化,说明该反应已达到平衡状态
(3)若分别在 、 温度下加入催化剂,进行 与 合成CO和 的反应,不同温度下,具有一
定能量的分子百分数与分子能量的关系如图1所示, 是活化分子具有的最低能量,则图中 _________
学科网(北京)股份有限公司(填“>”“=”或“<”)。
(4) 和 反应制备合成气的反应历程分两步:
步骤 反应 正反应速率方程 逆反应速率方程
反应i
反应ii
上述反应中,C(ads)为吸附性活性炭,反应历程的能量变化如上图2所示。
①反应速率快慢比较:反应i__________反应ii(填“>”“<”或“=”)。
②一定温度下,反应 的平衡常数 =_________(用
表示)。
18.(16分)芳香化合物 常用于药物及香料的合成,A有如下转化关系:
已知:
① ;
②
请回答下列问题:
(1)K中所含含氧官能团的名称为________。
(2)由D生成E的反应条件为__________,L的结构简式为__________。
(3)由H生成Ⅰ的化学方程式为______________________________________。
(4)在“转化关系”中,下列物质间的转化所发生的化学反应属于取代反应的是______(填标号)。
a.B→C b.D→E c.E→F d.F→H
学科网(北京)股份有限公司(5)F有多种同分异构体,符合下列条件的同分异构体共有______种(不考虑立体异构)。
①能与碳酸氢钠溶液反应;
②属于芳香化合物,分子中只含一个甲基。
请写出其中核磁共振氢谱峰面积之比为3:2:2:1:1:1的结构简式:____________。
(6)糠叉丙酮( )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇
和糠醛( )为原料制备糠叉丙酮的合成路线(无机试剂任选)。
学科网(北京)股份有限公司炎德·英才大联考长郡中学 2025 届高三月考试卷(二)
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 D C A C A D D B C B C B B D
1.D【解析】丙烷、丁烷属于烷烃,化学性质较稳定,能燃烧,其燃烧热值高,A正确;天然橡胶是以顺式
聚异戊二烯为主要成分的天然高分子,其单体为异戊二烯,B正确;环保再生纤维材料属于有机高分子材
料,C正确;乒乓球台可变灯光系统的控制芯片的主要成分为Si,D错误。
2.C【解析】氯化铵是离子化合物,电子式为 ,故A错误;铜的基态原子的简化电子排布
式为 ,故B错误; 中硫原子价层电子对数为 ,VSEPR模型为四面
体形,故C正确;HCl中氢原子的ls轨道提供的1个未成对电子与氯原子的3p轨道提供的1个未成对电子
形成H—Cl的s-pσ键,电子云轮廓图为 ,故D错误。
3.A【解析】此实验不需要用明火,A符合题意;电解CuCl 溶液需要接通电源,要注意小心用电,B不符
2
合题意;实验结束后,离开实验室前需要用肥皂等清洗双手,C不符合题意;电解CuCl 溶液时在阳极产
2
生氯气,在实验过程中需要排风以免中毒,D不符合题意。
4.C【解析】《选择性必修2》P ——Cl为吸电子基团,导致氯乙酸羧基中的羟基极性增大,更易电离出氢
54
离子,烷基是推电子基团,烷基越长推电子效应越大,导致丙酸羧基中的羟基极性减小,故酸性:氯乙酸
>乙酸>丙酸,A正确;《选择性必修2》P ——邻羟甲基苯甲醛在分子内形成氢键,分子内氢键使物质沸
57
点降低,而对羟甲基苯甲醛只在分子间形成氢键,分子间氢键使物质沸点升高,故邻羟甲基苯甲醛的沸点
低于对羟甲基苯甲醛,B正确;《选择性必修2》P —— 分子有极性,但很微弱,所以它在四氯化碳中
53
的溶解度高于在水中的溶解度,C错误;《选择性必修2》P ——大多数离子液体含有体积很大的阴、阳
88
离子,D正确。
5.A【解析】Y的分子式为 ,不饱和度为6,存在二元芳香酸的同分异构体,A项正确;X中存在
的—CHO、Z中存在的酚羟基均能被酸性 溶液氧化,故无法鉴别,B项错误;X分子中存在饱和
碳原子,所有原子不可能共平面,C项错误;Z的物质的量未明确,不能确定消耗的 的物质的量,D项
错误。
学科网(北京)股份有限公司6.D【解析】玻璃的主要成分为 ,用氢氟酸刻蚀玻璃时, 和氢氟酸反应生成 气体和水,反
应方程式为 ,A错误;AgCl是难溶物,不可拆,离子方程式为
,B错误;酸性KCr O 溶液氧化HO, 被还
2 2 7 2 2
原成 , 被氧化成O,离子方程式为 ,C错误;
2
TiCl 在水中发生水解反应生成 沉淀,同时生成HCl(《选择性必修1》P ),D正确。
4 77
7.D【解析】稀盐酸与二氧化锰不反应,图1中应选浓盐酸,故A错误;图2中要上下移动量气管,使两边
液面平齐时,再读数,故B错误;图3中 是黑色粉末,该装置不能实现反应的随关随停,故C错误;
图4用杯酚识别 和 ,超分子不溶于甲苯,杯酚可溶于氯仿,故操作①②为过滤,故D正确。
8.B【解析】增大 溶液浓度,溶液红色加深,说明平衡正向移动,A正确;等物质的量的FeBr 和Cl
2 2
反应, 先被氧化,剩余Cl
2
与Br⁻ 反应生成Br
2
,无法验证还原性: ,B错误;向滴有酚酞
的 溶液中加入少量BaCl 固体,溶液红色变浅并有白色沉淀生成可证明 存在水解平衡,C正
2
确;烧杯壁变凉说明反应的焓变 ,该反应有氨气生成,则熵变 ,D正确。
9.C【解析】NH 分子中原子间以单键相连接,不含π键,A错误;同周期主族元素,原子序数越大,第一
2 4
电离能呈增大趋势,但氮原子属于半充满结构,第一电离能大于相邻元素,故第一电离能:N>O>Cu,B
错误; 中氮原子孤电子对形成配位键( ), 中含1个孤电子对,孤电子
对与成键电子对间的斥力较大,H—N—H键角小,C正确;未指明气体是否处于标准状况,因此无法计算
能处理的氧气体积,D错误。
10.B【解析】由图可知,放电时,a电极为原电池的负极,碱性条件下锌失去电子发生氧化反应生成四羟
基合锌离子,电极反应式为 ;b电极为正极,水分子作用下氧气在正极
得到电子生成 ,电极反应式为 充电时,a极与电源负极连接,b极与电源
正极连接。
由分析可知,充电时,b极与电源正极连接,A错误;放电时,a电极为原电池的负极,电极反应式为
学科网(北京)股份有限公司,B正确;放电时,阴离子向负极移动, 通过阴离子交换膜从右室
移向左室,C错误;放电过程中,a极电极反应: ,则a电极附近溶液
pH减小,b极电极反应: , 通过阴离子交换膜从右室移向左室,b极反应
消耗水,导致b电极附近溶液pH增大,D错误。
11.C【解析】Al的电子排布式: ,核外含有电子的轨道有 个,A正确;
和 之间的最短距离为下底面面对角线长的一半,为 ,B正确; 晶体中,以体
心的 为例,与之紧邻且等距的Na+位于晶胞棱上、晶胞中上层立方体左右侧面心、晶胞中下层立方体
前后面面心,有8个,结合化学式可知与Na+紧邻且等距的 有8个,C错误;晶胞中 数目为
, 数目为 ,晶胞质量为 ,晶胞体积为
,则晶体的密度为
,D正确。
12.B【解析】“还原”步骤中焦炭和石英砂反应生成粗硅和 ,CO不能
使澄清石灰水变浑浊,A错误;“高温氮化”是Si与N 反应,原料气中含有N 和少量的 , 能与Si
2 2
反应生成 ,灼热的铜粉可与O 反应,从而除去N 中含有的少量O,B正确;“高温氮化”合成反应
2 2 2
为 ,反应中N的化合价降低,被还原,故N 是氧化剂,C错误;“高温氮化”制备
2
的Si N 中含有少量Fe和Cu,Fe与稀硫酸反应,得到可溶于水的FeSO ,但Cu与稀硫酸不反应,D错误。
3 4 4
13.B【解析】达到滴定终点时消耗盐酸的体积是20.00 mL,根据反应方程式
, ,由于二者的体积相同,故它们的浓度相
学科网(北京)股份有限公司等, 。开始滴定前溶液pH=11,则 ,则根据
,可知 ,故NH ·H O的电离平衡常数
3 2
,A正确;向 中滴加盐酸,溶液的碱性逐渐减弱,碱电离产生
的OH⁻ 对水电离的抑制作用逐渐减弱,则在恰好中和前,水的电离程度逐渐增大,因此水的电离程度:
m