文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点提分训练(十二)铁钉生锈的条件
一、选择题
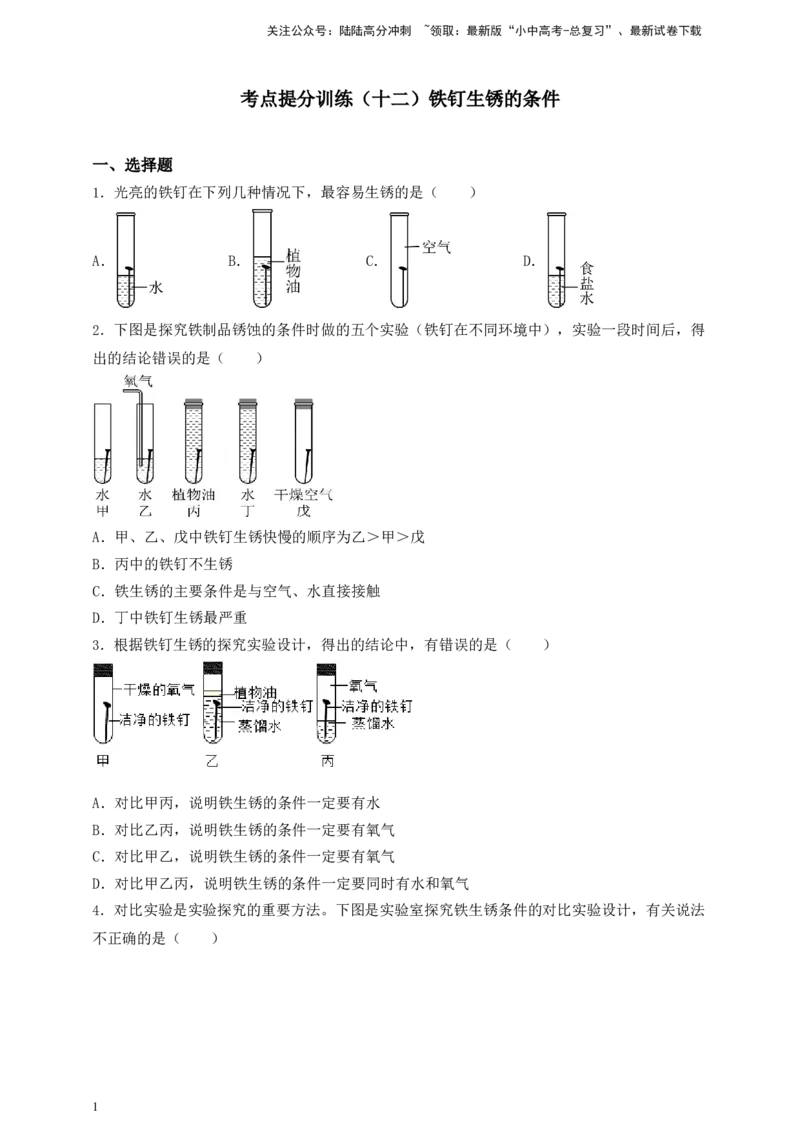
1.光亮的铁钉在下列几种情况下,最容易生锈的是( )
A. B. C. D.
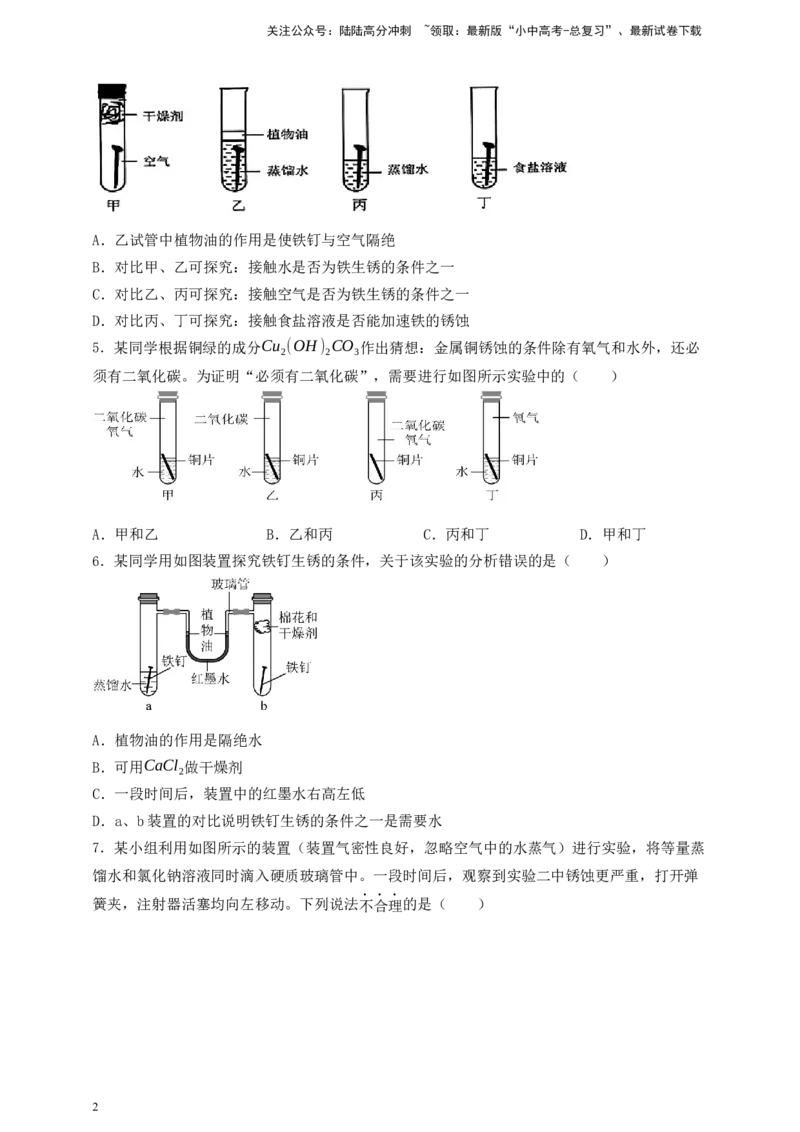
2.下图是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得
出的结论错误的是( )
A.甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊
B.丙中的铁钉不生锈
C.铁生锈的主要条件是与空气、水直接接触
D.丁中铁钉生锈最严重
3.根据铁钉生锈的探究实验设计,得出的结论中,有错误的是( )
A.对比甲丙,说明铁生锈的条件一定要有水
B.对比乙丙,说明铁生锈的条件一定要有氧气
C.对比甲乙,说明铁生锈的条件一定要有氧气
D.对比甲乙丙,说明铁生锈的条件一定要同时有水和氧气
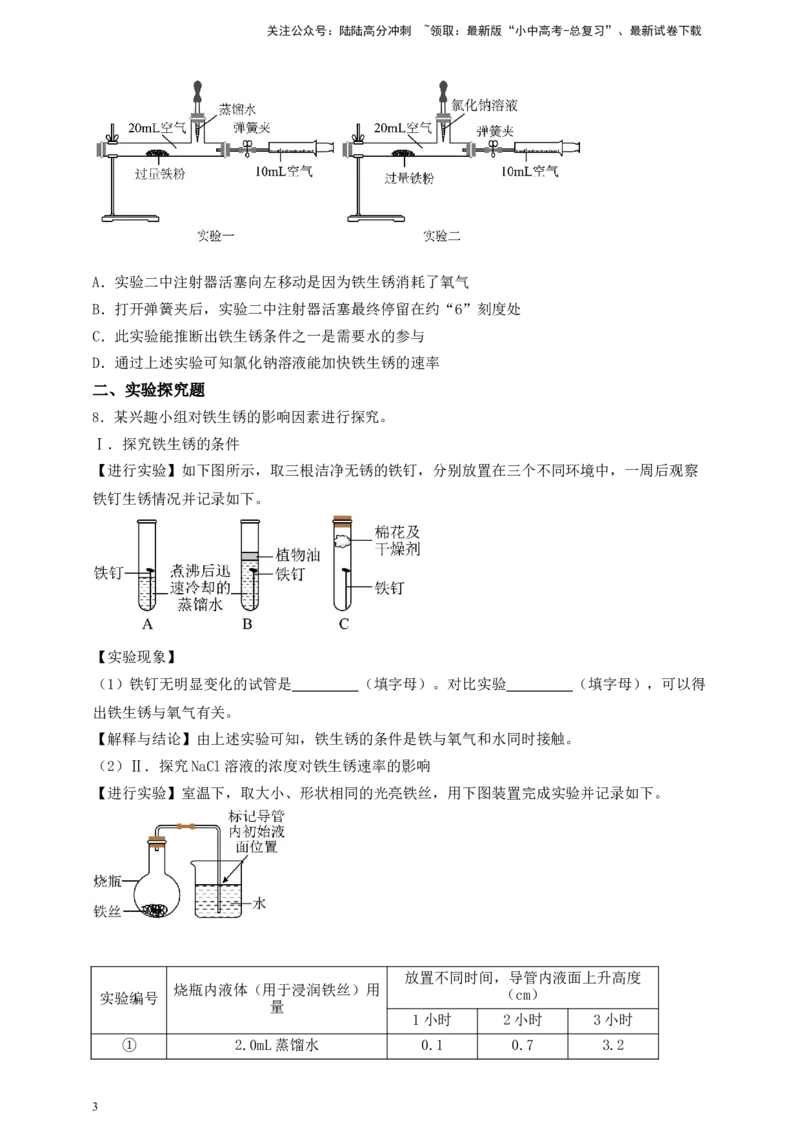
4.对比实验是实验探究的重要方法。下图是实验室探究铁生锈条件的对比实验设计,有关说法
不正确的是( )
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.乙试管中植物油的作用是使铁钉与空气隔绝
B.对比甲、乙可探究:接触水是否为铁生锈的条件之一
C.对比乙、丙可探究:接触空气是否为铁生锈的条件之一
D.对比丙、丁可探究:接触食盐溶液是否能加速铁的锈蚀
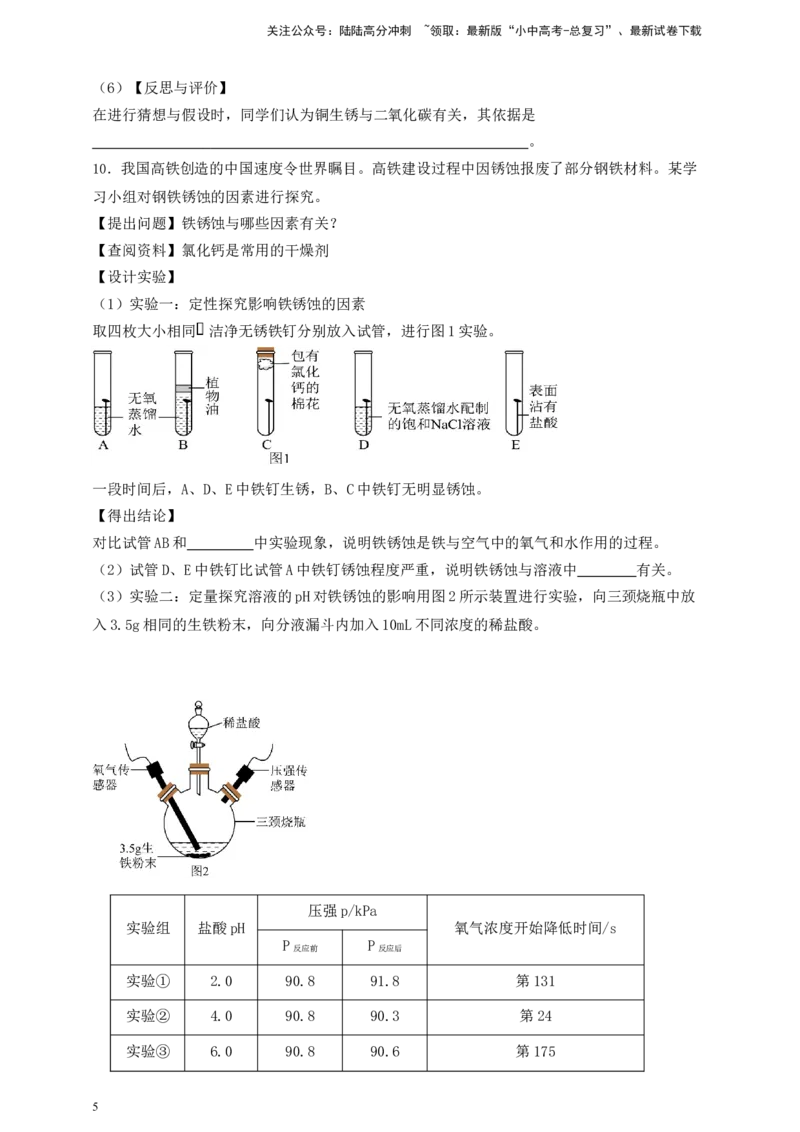
5.某同学根据铜绿的成分Cu (OH) CO 作出猜想:金属铜锈蚀的条件除有氧气和水外,还必
2 2 3
须有二氧化碳。为证明“必须有二氧化碳”,需要进行如图所示实验中的( )
A.甲和乙 B.乙和丙 C.丙和丁 D.甲和丁
6.某同学用如图装置探究铁钉生锈的条件,关于该实验的分析错误的是( )
A.植物油的作用是隔绝水
B.可用CaCl 做干燥剂
2
C.一段时间后,装置中的红墨水右高左低
D.a、b装置的对比说明铁钉生锈的条件之一是需要水
7.某小组利用如图所示的装置(装置气密性良好,忽略空气中的水蒸气)进行实验,将等量蒸
馏水和氯化钠溶液同时滴入硬质玻璃管中。一段时间后,观察到实验二中锈蚀更严重,打开弹
簧夹,注射器活塞均向左移动。下列说法不合理的是( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.实验二中注射器活塞向左移动是因为铁生锈消耗了氧气
B.打开弹簧夹后,实验二中注射器活塞最终停留在约“6”刻度处
C.此实验能推断出铁生锈条件之一是需要水的参与
D.通过上述实验可知氯化钠溶液能加快铁生锈的速率
二、实验探究题
8.某兴趣小组对铁生锈的影响因素进行探究。
Ⅰ.探究铁生锈的条件
【进行实验】如下图所示,取三根洁净无锈的铁钉,分别放置在三个不同环境中,一周后观察
铁钉生锈情况并记录如下。
【实验现象】
(1)铁钉无明显变化的试管是 (填字母)。对比实验 (填字母),可以得
出铁生锈与氧气有关。
【解释与结论】由上述实验可知,铁生锈的条件是铁与氧气和水同时接触。
(2)Ⅱ.探究NaCl溶液的浓度对铁生锈速率的影响
【进行实验】室温下,取大小、形状相同的光亮铁丝,用下图装置完成实验并记录如下。
放置不同时间,导管内液面上升高度
烧瓶内液体(用于浸润铁丝)用
(cm)
实验编号
量
1小时 2小时 3小时
① 2.0mL蒸馏水 0.1 0.7 3.2
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.5mL蒸馏水+0.5mL10%NaCl溶
② 0.3 1.5 5.0
液
③ 1.0mL蒸馏水+1mL10%NaCl溶液 0.8 3.3 7.9
④ 0.5mL蒸馏水+amL10%NaCl溶液 1.1 4.7 9.1
【解释与结论】
导管内液面上升的原因是铁生锈消耗氧气,导致瓶内气压 外界气压,水倒流入导管
中。
(3)实验编号④中的a= 。
(4)依据实验①~④,可以得出的结论是 。
(5)【反思与评价】
综合上述实验结果和生活经验,下列说法合理的是____。
A.铁粉可放入某些食品包装内,用来吸收氧气和水分,以防止食品腐败
B.铁制品的防护需尽量避免与水、氧气、氯化钠接触
C.暖宝宝贴(主要成分为铁粉、木炭、食盐)是利用铁粉的缓慢氧化将化学能转变为热能
9.铜质水龙头在空气中久置使用表面会出现一层绿色的锈渍。某兴趣小组同学设计并进行实
验,探究铜生锈的条件。请回答下列问题。
【提出问题】铜生锈与哪些因素有关?
【查阅资料】①铜表面绿色锈渍的化学成分主要是碱式碳酸铜[ Cu(OH)CO]。
2 2 3
②常温下,亚硫酸钠(NaSO)可与氧气发生化合反应。
2 3
【猜想与假设】常温下,铜生锈可能与氧气、水蒸气、二氧化碳有关。
【进行实验】通过控制与铜条接触的物质,利用上图装置(铜条长度为3cm,试管容积为
20mL)分别进行下列4个实验,并持续观察30天。
序号 主要实验操作 实验现象
1 加入2mL氢氧化钠浓溶液 铜条始终无明显变化
2 先加入2mL浓硫酸,再通入约4mL二氧化碳 铜条始终无明显变化
3 先加入4mL饱和NaSO 溶液,再充满二氧化碳 铜条始终无明显变化
2 3
4 先加入2mL蒸馏水,再通入约4mL二氧化碳 铜条小部分出现绿色锈渍
【解释与结论】
(1)实验1中,氢氧化钠浓溶液的作用是 (用化学方程式表示)。
(2)实验2中,试管内的气体主要含有氮气、二氧化碳、 (填化学式)。
(3)实验3的目的是 。
(4)要得出“铜生锈一定与水蒸气有关”的结论,依据的两个实验是 (填序号)。
(5)由上述实验可推知,铜生锈的条件是 。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(6)【反思与评价】
在进行猜想与假设时,同学们认为铜生锈与二氧化碳有关,其依据是
。
10.我国高铁创造的中国速度令世界瞩目。高铁建设过程中因锈蚀报废了部分钢铁材料。某学
习小组对钢铁锈蚀的因素进行探究。
【提出问题】铁锈蚀与哪些因素有关?
【查阅资料】氯化钙是常用的干燥剂
【设计实验】
(1)实验一:定性探究影响铁锈蚀的因素
取四枚大小相同 洁净无锈铁钉分别放入试管,进行图1实验。
一段时间后,A、D、E中铁钉生锈,B、C中铁钉无明显锈蚀。
【得出结论】
对比试管AB和 中实验现象,说明铁锈蚀是铁与空气中的氧气和水作用的过程。
(2)试管D、E中铁钉比试管A中铁钉锈蚀程度严重,说明铁锈蚀与溶液中 有关。
(3)实验二:定量探究溶液的pH对铁锈蚀的影响用图2所示装置进行实验,向三颈烧瓶中放
入3.5g相同的生铁粉末,向分液漏斗内加入10mL不同浓度的稀盐酸。
压强p/kPa
实验组 盐酸pH 氧气浓度开始降低时间/s
P P
反应前 反应后
实验① 2.0 90.8 91.8 第131
实验② 4.0 90.8 90.3 第24
实验③ 6.0 90.8 90.6 第175
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
已知:铁与盐酸接触即发生反应,分析表中数据回答:实验①反应后压强变大 主要原因是
。(用化学方程式表示)
(4)实验①②③中,铁粉与盐酸、铁粉与氧气的反应 (填“能”或“不能”)同时开
始。
(5)【得出结论】当pH= 时,铁粉的锈蚀程度最大。
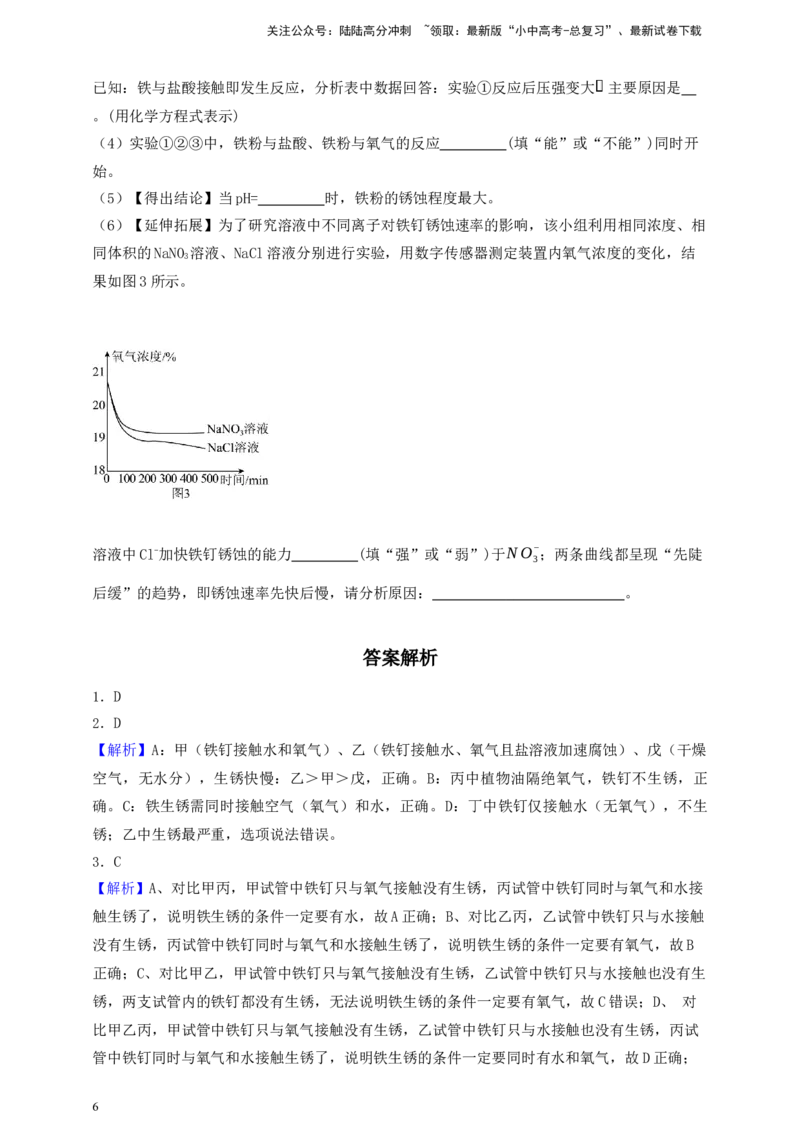
(6)【延伸拓展】为了研究溶液中不同离子对铁钉锈蚀速率的影响,该小组利用相同浓度、相
同体积的NaNO 溶液、NaCl溶液分别进行实验,用数字传感器测定装置内氧气浓度的变化,结
3
果如图3所示。
溶液中Cl-加快铁钉锈蚀的能力 (填“强”或“弱”)于NO−;两条曲线都呈现“先陡
3
后缓”的趋势,即锈蚀速率先快后慢,请分析原因: 。
答案解析
1.D
2.D
【解析】A:甲(铁钉接触水和氧气)、乙(铁钉接触水、氧气且盐溶液加速腐蚀)、戊(干燥
空气,无水分),生锈快慢:乙>甲>戊,正确。B:丙中植物油隔绝氧气,铁钉不生锈,正
确。C:铁生锈需同时接触空气(氧气)和水,正确。D:丁中铁钉仅接触水(无氧气),不生
锈;乙中生锈最严重,选项说法错误。
3.C
【解析】A、对比甲丙,甲试管中铁钉只与氧气接触没有生锈,丙试管中铁钉同时与氧气和水接
触生锈了,说明铁生锈的条件一定要有水,故A正确;B、对比乙丙,乙试管中铁钉只与水接触
没有生锈,丙试管中铁钉同时与氧气和水接触生锈了,说明铁生锈的条件一定要有氧气,故B
正确;C、对比甲乙,甲试管中铁钉只与氧气接触没有生锈,乙试管中铁钉只与水接触也没有生
锈,两支试管内的铁钉都没有生锈,无法说明铁生锈的条件一定要有氧气,故C错误;D、 对
比甲乙丙,甲试管中铁钉只与氧气接触没有生锈,乙试管中铁钉只与水接触也没有生锈,丙试
管中铁钉同时与氧气和水接触生锈了,说明铁生锈的条件一定要同时有水和氧气,故D正确;
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故答案为:C。
4.B
【解析】A. 乙试管中植物油的作用是使铁钉与空气隔绝,故正确,不符合题意;B. 甲试管中
的铁钉只能与干燥的空气接触,乙试管的铁钉只能与水接触,两支试管的铁钉均没有生锈,不
能探究接触水是否为铁生锈的条件之一,故错误,符合题意;C. 乙试管的铁钉只能与水接触,
丙试管中的铁钉能与氧气、水充分接触,一段时间后,丙试管中的铁钉生锈,乙试管的铁钉没
有生锈,可探究接触空气是否为铁生锈的条件之一,故正确,不符合题意;D. 对比丙、丁,丁
中铁钉锈蚀的更严重,可探究接触食盐溶液是否能加速铁的锈蚀,故正确,不符合题意;故答
案为:B。
5.D
【解析】要证明铜锈蚀需二氧化碳,需设计对比实验:一组含CO 、O 、H O(生锈),另一组不
2 2 2
含CO 但含O 、H O(不生锈)。甲:含CO 、O 、H O,生锈;丁:不含CO (用氮气代替),含
2 2 2 2 2 2 2
O 、H O,不生锈。对比甲和丁可证明需CO ,正确。
2 2 2
6.C
【解析】A、植物油的作用是为了隔绝空气,防止空气中的氧气溶于水,不符合题意;B、氯化
钙能够吸收水分,b中的干燥剂可以是氯化钙,不符合题意;C、a管内的铁钉与氧气和水同时
接触,会生锈,试管内压强因氧气的减少而减小,b管只与氧气接触,不会生锈,管内气压不
变,一段时间后,装置中的红墨水液面左高右低,符合题意;D、a、b装置中变量为水,对比
现象可说明铁钉生锈的条件之一是需要水,不符合题意;故答案为:C。
7.C
【解析】A:铁生锈消耗氧气,装置内气压减小,注射器活塞左移,正确。B:空气中氧气约占
1/5,实验二初始空气体积20mL,消耗氧气约4mL,打开弹簧夹后,注射器内10mL空气进入,
总体积20mL-4mL=16mL,活塞应停在10mL-4mL=6mL刻度处,正确。C:实验一和二均有水,无法
推断铁生锈需水,需与无水条件对比,选项说法不合理。D:实验二(氯化钠溶液)比实验一
(蒸馏水)锈蚀更严重,说明氯化钠加速生锈,正确。
8.(1)BC;AB
(2)小于
(3)1.5
(4)在其他条件相同时,随着NaCl溶液浓度的增加,铁生锈速率加快
(5)A;B;C
【解析】(1)铁钉生锈的条件是同时与氧气、水接触,A试管铁钉同时与水和氧气接触会生
锈,B铁钉只和水接触,C铁钉只和氧气接触,所以BC都不会生锈,表面无明显变化,对比实
验需要控制单一变量,要证明铁生锈与氧气有关,变量是氧气,所以通过AB对比实验; (2)
铁生锈消耗氧气,使瓶内气体体积变小,压强变小,气压小于外界大气压,水倒流入导管;
(3) 根据题意是要探究NaCl溶液的浓度对铁生锈速率的影响,实验的变量是氯化钠的浓度,
实验①是空白对照组,取用的是2mL蒸馏水,实验②③④液体体积也要取用2mL,实验④取
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
0.5mL蒸馏水,还需要加1.5mL氯化钠溶液,所以a为1.5;(4)根据数据分析实验①~④氯化
钠溶液的浓度依次增大,其导管内液面上升的高度逐渐增大,说明铁生锈的速率逐渐加快,使
瓶内压强逐渐变小,故答案为: 在其他条件相同时,随着NaCl溶液浓度的增加,铁生锈速率
加快;(5)A、铁粉可以同时和氧气、水反应而生锈,所以可以可放入某些食品包装内,用来
吸收氧气和水分,以防止食品腐败 ,故A符合题意; B、根据以上实验探究可知氯化钠会加剧
铁生锈的速率,故B符合题意; C、暖宝宝贴可以与人体挥发出的水分以及空气中的氧气发生
缓慢氧化,缓慢氧化会放出热量,所以是将化学能转化为热能,故C符合题意;故答案为:
ABC。
9.(1)CO+2NaOH=NaCO+HO
2 2 3 2
(2)O
2
(3)证明铜只和二氧化碳、水蒸气接触不会生锈
(4)2、4
(5)同时与水蒸气、二氧化碳、氧气接触
(6)根据质量守恒定律可知,化学反应前后元素种类不变,碱式碳酸铜中含有碳元素,空气中
只有二氧化碳含有碳元素。
【解析】[解释与结论] (1)实验1中,氢氧化钠浓溶液的作用是吸收空气中的二氧化碳,二
氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式为:CO+2NaOH=NaCO+HO。(2)浓硫酸具
2 2 3 2
有吸水性,所以实验2中,试管内的气体主要成分为脱水后的空气主要成分,所以试管内的气
体主要含有氮气、二氧化碳、氧气,氧气的化学式为O。(3)饱和NaSO 溶液吸收氧气,之后
2 2 3
充满二氧化碳,是为了证明铜只和二氧化碳、水蒸气接触不会生锈。(4)证明铜生锈一定与水
蒸气有关”依据的两个实验是2、4,加入2mL浓硫酸,铜条始终无明显变化,说明二氧化碳、
氧气不是铜生锈的条件,先加入2mL蒸馏水再通入约4mLCO,铜条小部分出现绿色锈渍,说明
2
铜生锈一定与水蒸气有关。(5)实验1证明,铜与水蒸气、氧气同时接触,不会生锈;实验2
证明铜与二氧化碳、氧气同时接触,不会生锈;实验3证明铜与二氧化碳、水蒸气同时接触,
不会生锈;实验4证明铜与水蒸气、二氧化碳、氧气同时接触会生锈。所以由上述实验可推
知,铜生锈的条件是同时与水蒸气、二氧化碳、氧气接触。[反思与评价](6)根据质量守恒定
律可知,化学反应前后元素种类不变,铜生锈生成的碱式碳酸铜中含有碳元素,所以能造成铜
生成铜锈的气体一定有二氧化碳,因为只有二氧化碳中含有碳元素。
10.(1)C
(2)离子
(3)Fe+2HCl=FeCl +H ↑
2 2
(4)不能
(5)4.0
(6)强;刚开始时,氧气及铁的含量充足,反应物接触面积足够,则反应速率快,一段时间
后,氧气含量下降,铁表面被铁锈覆盖,反应接触面积变小,反应速率变慢
【解析】(1)对比AB实验可得出铁生锈与氧气有关,对比AC实验可得出铁生锈与水有关;
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)试管D、E中铁钉比试管A中铁钉锈蚀程度严重,说明铁锈蚀与溶液中离子有关,稀盐酸
和氯化钠溶液中都存在有离子;(3)实验①反应后压强变大是因为铁与稀盐酸反应产生氢气,
使装置内的气压变大;(4)实验①②③中,铁粉与盐酸、铁粉与氧气的反应不能同时开始,因
为分析表格中的数据可以知道氧气浓度降低的时间和压强改变的时间不同;(5)pH=4.0时,
氧气浓度开始降低的时间最早,铁粉的锈蚀程度最大;(6)由图像分析比较,溶液中Cl-加快
铁钉锈蚀的能力强与NO−,锈蚀速率先快后慢,是因为刚开始时,氧气及铁的含量充足,反应
3
物接触面积足够,则反应速率快,一段时间后,氧气含量下降,铁表面被铁锈覆盖,反应接触
面积变小,反应速率变慢。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
10