文档内容
【基础知识】电解池及金属的电化学腐蚀与防护
考点二 电解原理的应用
【必备知识】
1.氯碱工业
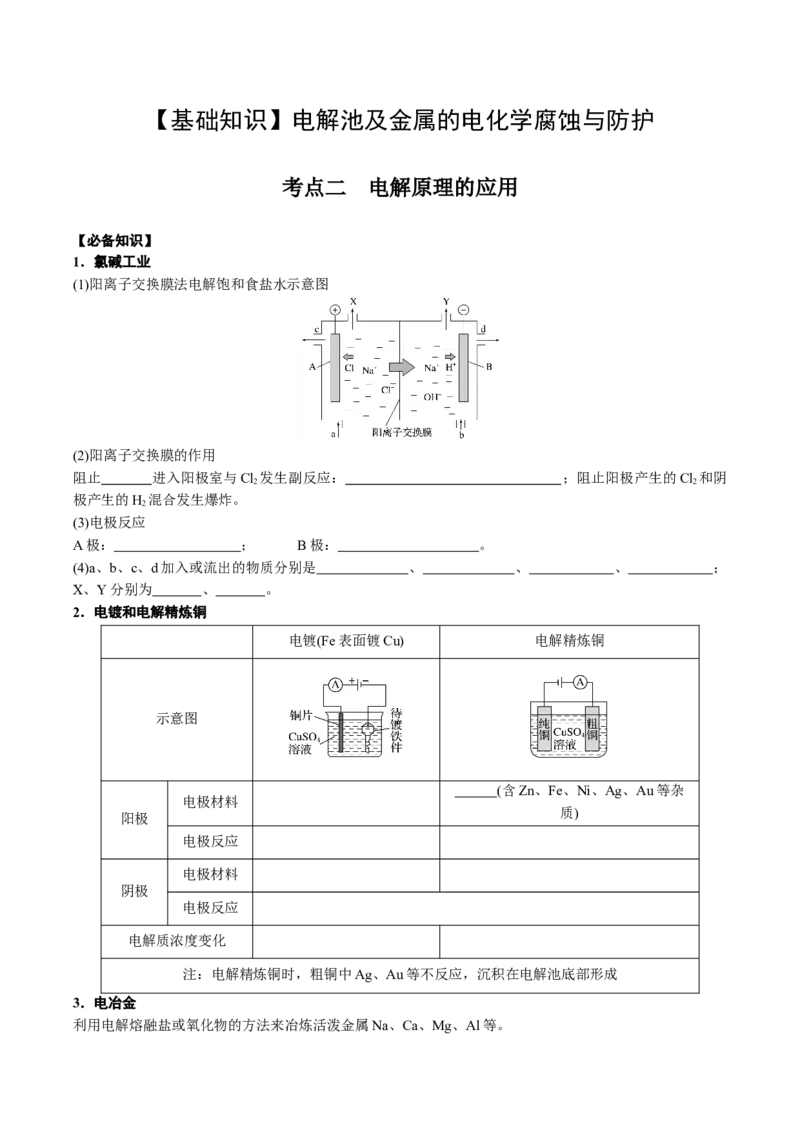
(1)阳离子交换膜法电解饱和食盐水示意图
(2)阳离子交换膜的作用
阻止 进入阳极室与Cl 发生副反应: ;阻止阳极产生的Cl 和阴
2 2
极产生的H 混合发生爆炸。
2
(3)电极反应
A极: ; B极: 。
(4)a、b、c、d加入或流出的物质分别是 、 、 、 ;
X、Y分别为 、 。
2.电镀和电解精炼铜
电镀(Fe表面镀Cu) 电解精炼铜
示意图
(含Zn、Fe、Ni、Ag、Au等杂
电极材料
质)
阳极
电极反应
电极材料
阴极
电极反应
电解质浓度变化
注:电解精炼铜时,粗铜中Ag、Au等不反应,沉积在电解池底部形成
3.电冶金
利用电解熔融盐或氧化物的方法来冶炼活泼金属Na、Ca、Mg、Al等。总反应化学方程式 阳极、阴极反应式
冶炼钠 阳极: 阴极:
冶炼镁 阳极: 阴极:
冶炼铝 阳极: 阴极:
注意
①电解熔融MgCl 冶炼镁,而不能电解熔融MgO冶炼镁,因MgO的熔点很高
2
②电解熔融Al O 冶炼铝,而不能电解AlCl 冶炼铝,因AlCl 是共价化合物,其熔融态不导电
2 3 3 3
【易错辨析】
1.电解饱和食盐水时,两个电极均不能用金属材料( )
2.在镀件上电镀铜时,镀件应连接电源的正极( )
3.根据得失电子守恒可知电解精炼铜时,阳极减少的质量和阴极增加的质量相等( )
4.电镀铜和电解精炼铜时,电解质溶液中c(Cu2+)均保持不变( )
5.电解冶炼镁、铝通常电解熔融的MgCl 和Al O,也可以电解熔融的MgO和AlCl ( )
2 2 3 3
【题型突破】
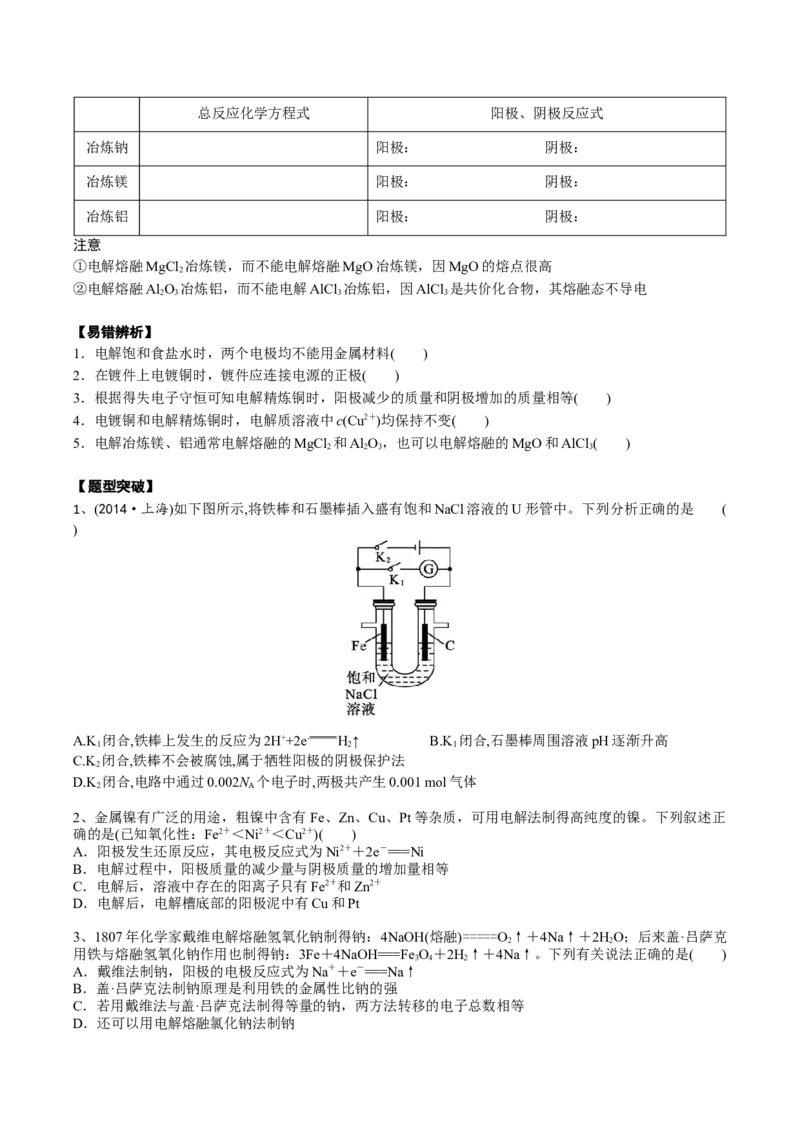
1、(2014·上海)如下图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中。下列分析正确的是 (
)
A.K 闭合,铁棒上发生的反应为2H++2e- H↑ B.K 闭合,石墨棒周围溶液pH逐渐升高
1 2 1
C.K 闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
2
D.K 闭合,电路中通过0.002N 个电子时,两极共产生0.001 mol气体
2 A
2、金属镍有广泛的用途,粗镍中含有Fe、Zn、Cu、Pt等杂质,可用电解法制得高纯度的镍。下列叙述正
确的是(已知氧化性:Fe2+<Ni2+<Cu2+)( )
A.阳极发生还原反应,其电极反应式为Ni2++2e-===Ni
B.电解过程中,阳极质量的减少量与阴极质量的增加量相等
C.电解后,溶液中存在的阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中有Cu和Pt
3、1807年化学家戴维电解熔融氢氧化钠制得钠:4NaOH(熔融)=====O↑+4Na↑+2HO;后来盖·吕萨克
2 2
用铁与熔融氢氧化钠作用也制得钠:3Fe+4NaOH===Fe O+2H↑+4Na↑。下列有关说法正确的是( )
3 4 2
A.戴维法制钠,阳极的电极反应式为Na++e-===Na↑
B.盖·吕萨克法制钠原理是利用铁的金属性比钠的强
C.若用戴维法与盖·吕萨克法制得等量的钠,两方法转移的电子总数相等
D.还可以用电解熔融氯化钠法制钠4、(2022·广东,10)以熔融盐为电解液,以含Cu、Mg和Si等的铝合金废料为阳极进行电解,实现Al的再
生。该过程中( )
A.阴极发生的反应为Mg-2e-===Mg2+ B.阴极上Al被氧化
C.在电解槽底部产生含Cu的阳极泥 D.阳极和阴极的质量变化相等
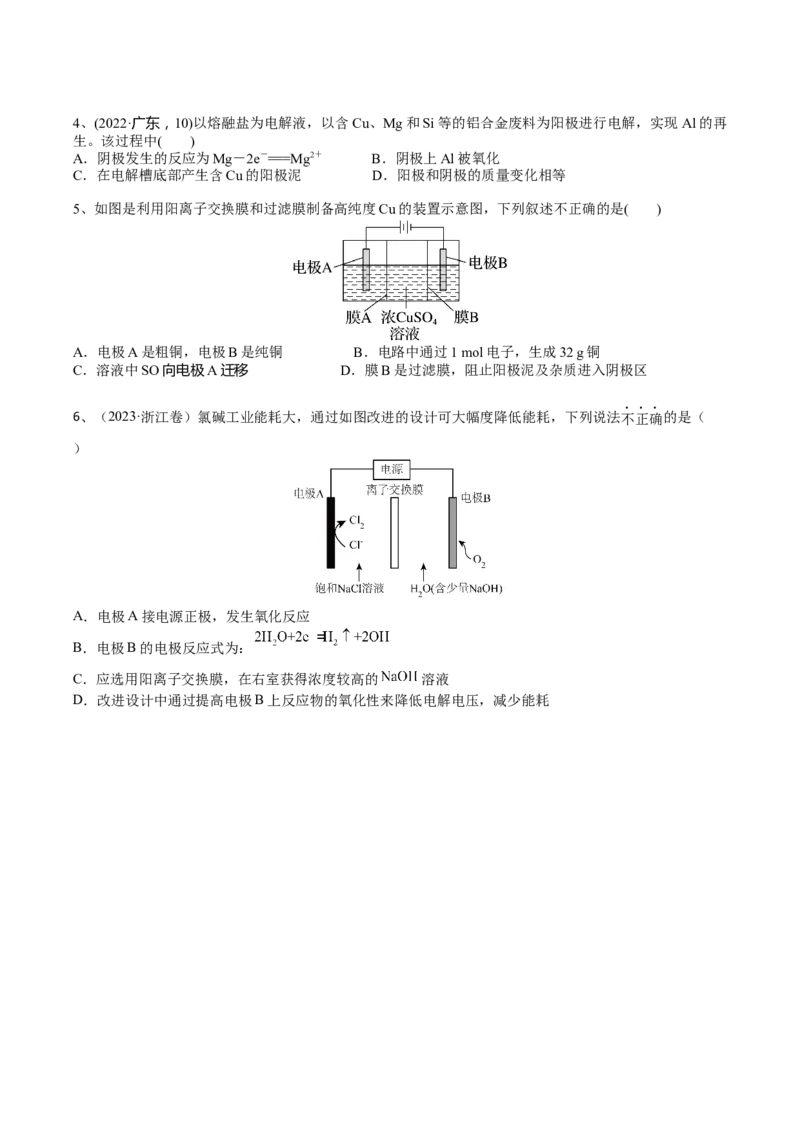
5、如图是利用阳离子交换膜和过滤膜制备高纯度Cu的装置示意图,下列叙述不正确的是( )
A.电极A是粗铜,电极B是纯铜 B.电路中通过1 mol电子,生成32 g铜
C.溶液中SO向电极A迁移 D.膜B是过滤膜,阻止阳极泥及杂质进入阴极区
6、(2023·浙江卷)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正确的是(
)
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗