文档内容
【基础知识】晶体结构与性质
考点四 晶胞参数计算
【知识清单】
1、晶胞参数
晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的夹角α、β、γ,
即晶格特征参数,简称晶胞参数。
2、晶体结构的相关计算
(1)空间利用率=×100%。
(2)金属晶体中体心立方堆积、面心立方堆积中的几组计算公式(设棱长为a)
①面对角线长=a。
②体对角线长=a。
③体心立方堆积4r=a(r为原子半径)。
④面心立方堆积4r=a(r为原子半径)。
NM
(3)晶胞密度ρ==
∝V N
A
【题组练习一】
1、[2020·全国卷Ⅲ,35(4)]研究发现,氨硼烷NH BH 在低温高压条件下为正交晶系结构,晶胞参数分别为
3 3
a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。(N:14 H:1 B:11)
氨硼烷晶体的密度ρ=________ g·cm-3(列出计算式,设N 为阿伏加德罗常数的值)。
A
【答案】
解析 由题意可知,晶胞的体积V(晶胞)=8abc×10-30 cm3。由晶胞结构可知,每个晶胞含有16个NH BH
3 3
分子,则每个晶胞的质量m(晶胞)= g,氨硼烷晶体的密度ρ=== g·cm-3。
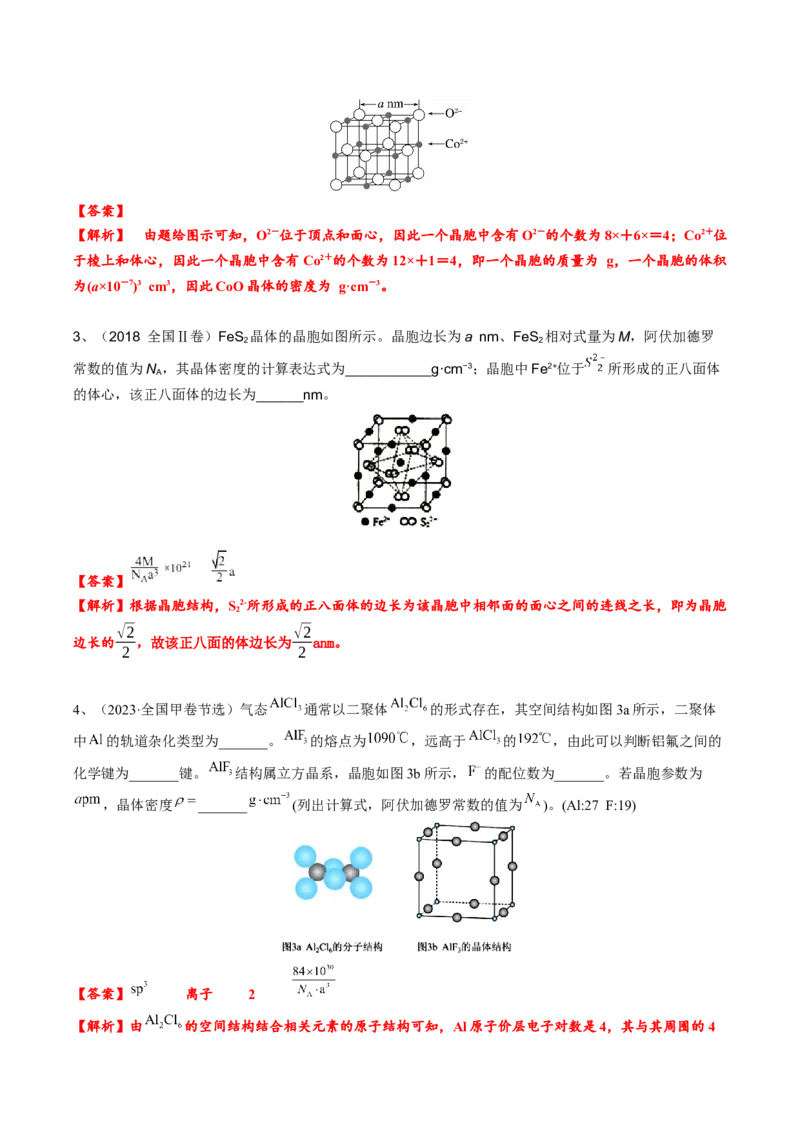
2、[2020·天津,13(2)节选]CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为N ,则CoO晶体的密
A
度为____________g·cm-3。(O:16 Co:59)【答案】
【解析】 由题给图示可知,O2-位于顶点和面心,因此一个晶胞中含有O2-的个数为8×+6×=4;Co2+位
于棱上和体心,因此一个晶胞中含有Co2+的个数为12×+1=4,即一个晶胞的质量为 g,一个晶胞的体积
为(a×10-7)3 cm3,因此CoO晶体的密度为 g·cm-3。
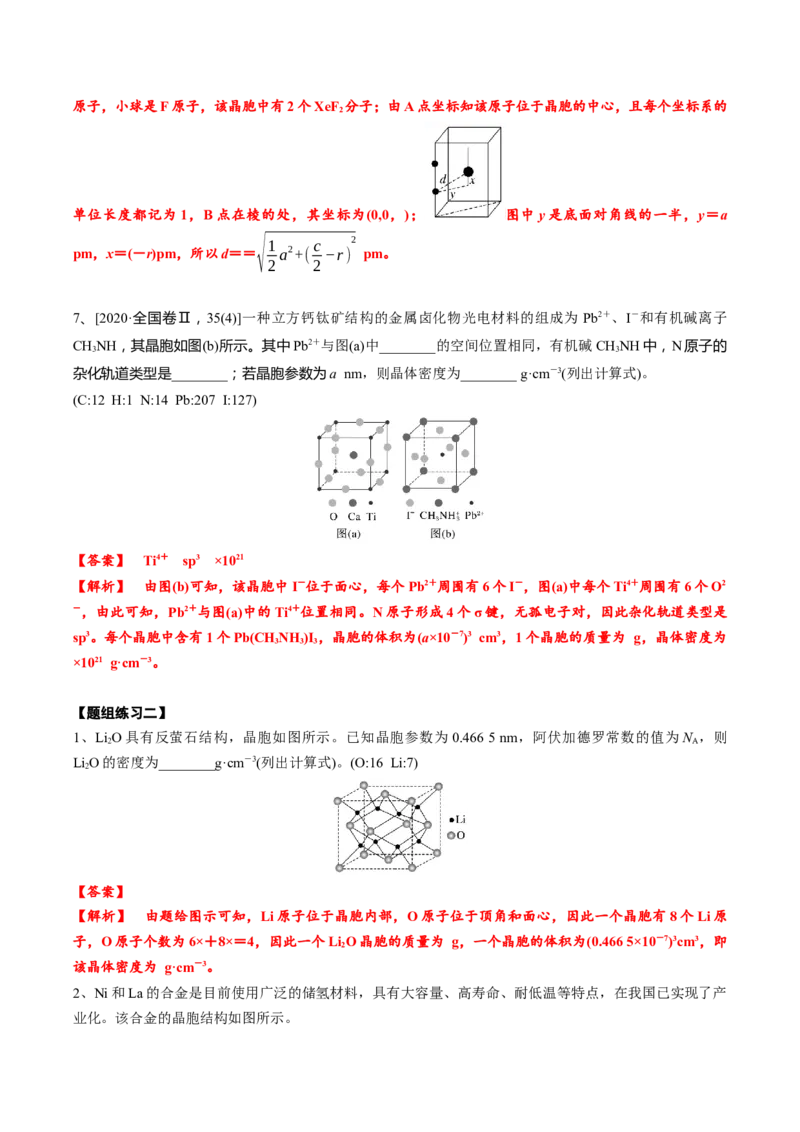
3、(2018 全国Ⅱ卷)FeS 晶体的晶胞如图所示。晶胞边长为a nm、FeS 相对式量为M,阿伏加德罗
2 2
常数的值为N ,其晶体密度的计算表达式为___________g·cm−3;晶胞中Fe2+位于 所形成的正八面体
A
的体心,该正八面体的边长为______nm。
【答案】
【解析】根据晶胞结构,S2-所形成的正八面体的边长为该晶胞中相邻面的面心之间的连线之长,即为晶胞
2
√2 √2
边长的 ,故该正八面的体边长为 anm。
2 2
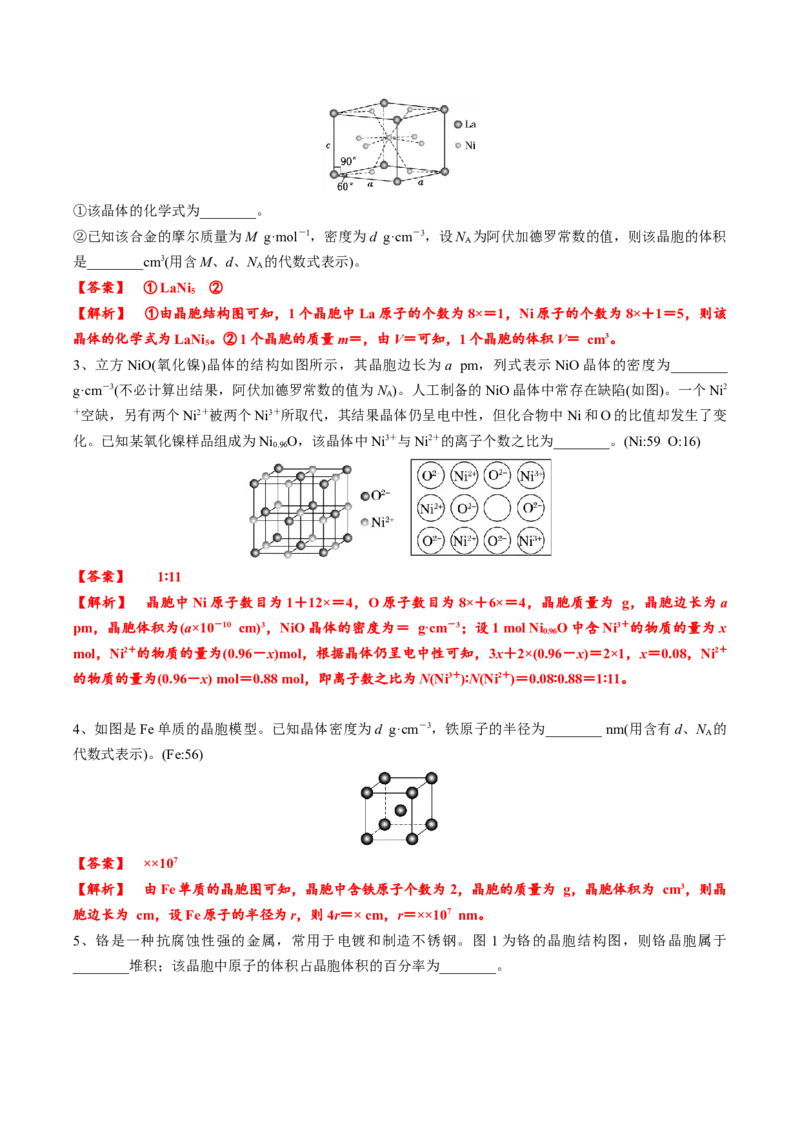
4、(2023·全国甲卷节选)气态 通常以二聚体 的形式存在,其空间结构如图3a所示,二聚体
中 的轨道杂化类型为_______。 的熔点为 ,远高于 的 ,由此可以判断铝氟之间的
化学键为_______键。 结构属立方晶系,晶胞如图3b所示, 的配位数为_______。若晶胞参数为
,晶体密度 _______ (列出计算式,阿伏加德罗常数的值为 )。(Al:27 F:19)
【答案】 离子 2
【解析】由 的空间结构结合相关元素的原子结构可知,Al原子价层电子对数是4,其与其周围的4个氯原子形成四面体结构,因此,二聚体中A1的轨道杂化类型为 。AlF 的熔点为1090℃,远高于
3
AlCl 的192℃,由于F的电负性最大,其吸引电子的能力最强,因此,可以判断铝氟之间的化学键为离子
3
键。由AlF 的晶胞结构可知,其中含灰色球的个数为 ,红色球的个数为 ,则灰色的球为
3
,距 最近且等距的 有2个,则 的配位数为2。若晶胞参数为a pm,则晶胞的体积为
,晶胞的质量为 ,则其晶体密度 。
5、(2023·全国乙卷节选)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿
c轴的投影图如下所示,晶胞中含有_______个 。该物质化学式为_______,B-B最近距离为_______。
【答案】1
【解析】由硼镁化合物的晶体结构可知 位于正六棱柱的顶点和面心,由均摊法可以求出正六棱柱中含
有 个 ,由晶胞沿c轴的投影图可知本题所给晶体结构包含三个晶胞,则晶胞中Mg的个
数为1;晶体结构中 在正六棱柱体内共6个,则该物质的化学式为 ;由晶胞沿c轴的投影图可知,
B原子在图中两个正三角形的重心,该点到顶点的距离是该点到对边中点距离的2倍,顶点到对边的垂线
长度为 ,因此B-B最近距离为 。
6、[2021·山东,16(4)]XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 90°,该晶胞中有
2
___________个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子
2
的分数坐标,如 A点原子的分数坐标为(,,)。已知Xe—F键长为r pm,则B点原子的分数坐标为
______;晶胞中A、B间距离d=______pm。
√1 c 2
【答案】 2 (0,0,) a2+( −r)
2 2
【解析】 图中大球的个数为8×+1=2,小球的个数为8×+2=4,根据XeF 的原子个数比可知大球是Xe
2原子,小球是F原子,该晶胞中有2个XeF 分子;由A点坐标知该原子位于晶胞的中心,且每个坐标系的
2
单位长度都记为1,B点在棱的处,其坐标为(0,0,); 图中y是底面对角线的一半,y=a
√1 c 2
pm,x=(-r)pm,所以d== a2+( −r) pm。
2 2
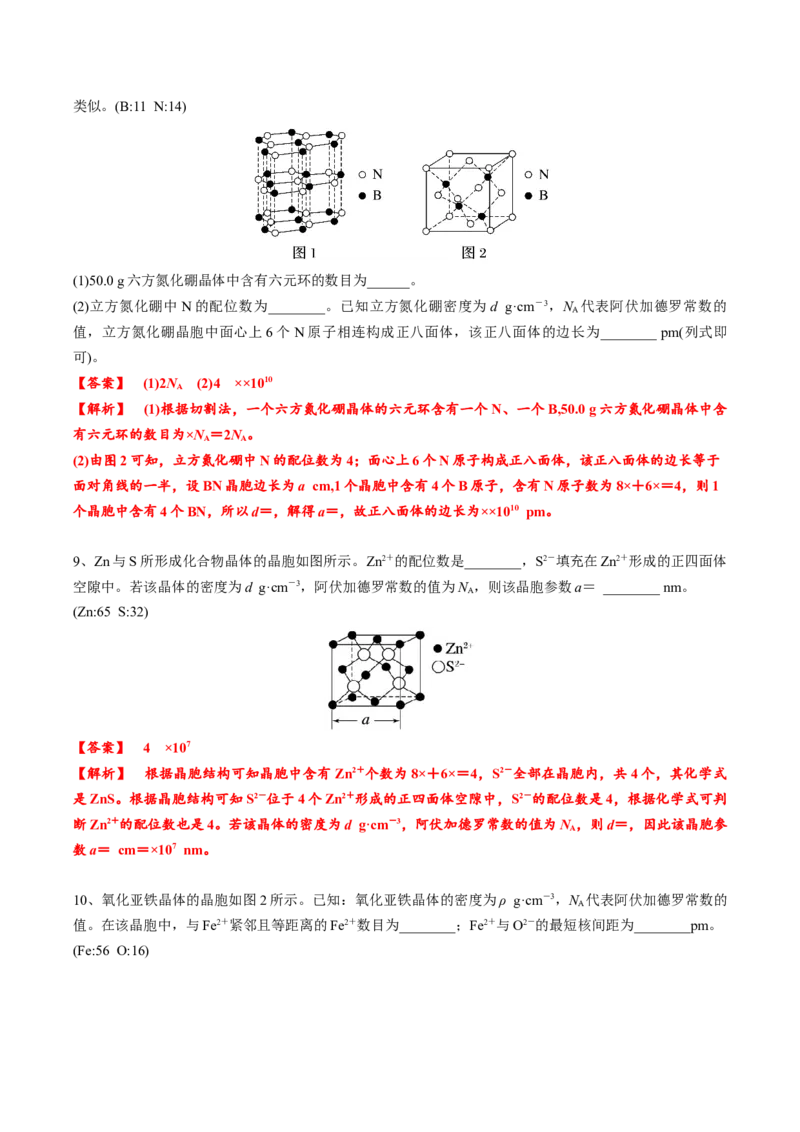
7、[2020·全国卷Ⅱ,35(4)]一种立方钙钛矿结构的金属卤化物光电材料的组成为 Pb2+、I-和有机碱离子
CHNH,其晶胞如图(b)所示。其中Pb2+与图(a)中________的空间位置相同,有机碱CHNH中,N原子的
3 3
杂化轨道类型是________;若晶胞参数为a nm,则晶体密度为________ g·cm-3(列出计算式)。
(C:12 H:1 N:14 Pb:207 I:127)
【答案】 Ti4+ sp3 ×1021
【解析】 由图(b)可知,该晶胞中I-位于面心,每个Pb2+周围有6个I-,图(a)中每个Ti4+周围有6个O2
-,由此可知,Pb2+与图(a)中的Ti4+位置相同。N原子形成4个σ键,无孤电子对,因此杂化轨道类型是
sp3。每个晶胞中含有1个Pb(CH NH )I ,晶胞的体积为(a×10-7)3 cm3,1个晶胞的质量为 g,晶体密度为
3 3 3
×1021 g·cm-3。
【题组练习二】
1、LiO具有反萤石结构,晶胞如图所示。已知晶胞参数为 0.466 5 nm,阿伏加德罗常数的值为N ,则
2 A
LiO的密度为________g·cm-3(列出计算式)。(O:16 Li:7)
2
【答案】
【解析】 由题给图示可知,Li原子位于晶胞内部,O原子位于顶角和面心,因此一个晶胞有8个Li原
子,O原子个数为6×+8×=4,因此一个LiO晶胞的质量为 g,一个晶胞的体积为(0.466 5×10-7)3cm3,即
2
该晶体密度为 g·cm-3。
2、Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在我国已实现了产
业化。该合金的晶胞结构如图所示。①该晶体的化学式为________。
②已知该合金的摩尔质量为M g·mol-1,密度为d g·cm-3,设N 为阿伏加德罗常数的值,则该晶胞的体积
A
是________cm3(用含M、d、N 的代数式表示)。
A
【答案】 ①LaNi ②
5
【解析】 ①由晶胞结构图可知,1个晶胞中La原子的个数为8×=1,Ni原子的个数为8×+1=5,则该
晶体的化学式为LaNi 。②1个晶胞的质量m=,由V=可知,1个晶胞的体积V= cm3。
5
3、立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为________
g·cm-3(不必计算出结果,阿伏加德罗常数的值为N )。人工制备的NiO晶体中常存在缺陷(如图)。一个Ni2
A
+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变
化。已知某氧化镍样品组成为Ni O,该晶体中Ni3+与Ni2+的离子个数之比为________。(Ni:59 O:16)
0.96
【答案】 1∶11
【解析】 晶胞中Ni原子数目为1+12×=4,O原子数目为8×+6×=4,晶胞质量为 g,晶胞边长为a
pm,晶胞体积为(a×10-10 cm)3,NiO晶体的密度为= g·cm-3;设1 mol Ni O中含Ni3+的物质的量为x
0.96
mol,Ni2+的物质的量为(0.96-x)mol,根据晶体仍呈电中性可知,3x+2×(0.96-x)=2×1,x=0.08,Ni2+
的物质的量为(0.96-x) mol=0.88 mol,即离子数之比为N(Ni3+)∶N(Ni2+)=0.08∶0.88=1∶11。
4、如图是Fe单质的晶胞模型。已知晶体密度为d g·cm-3,铁原子的半径为________ nm(用含有d、N 的
A
代数式表示)。(Fe:56)
【答案】 ××107
【解析】 由Fe单质的晶胞图可知,晶胞中含铁原子个数为2,晶胞的质量为 g,晶胞体积为 cm3,则晶
胞边长为 cm,设Fe原子的半径为r,则4r=× cm,r=××107 nm。
5、铬是一种抗腐蚀性强的金属,常用于电镀和制造不锈钢。图 1为铬的晶胞结构图,则铬晶胞属于
________堆积;该晶胞中原子的体积占晶胞体积的百分率为________。【答案】 体心立方 68%
【解析】 (1)由图1可以看出铬晶胞属于体心立方堆积;设晶胞参数(晶胞边长)为a nm,则晶胞体积为a3
nm3,铬原子半径为a nm,根据切割法知晶胞中铬原子个数为 8×+1=2,故铬原子总体积为 π×(a)3×2
¿( , )π×( ¿(¿( ), )a)3×2
nm3,所以该晶胞中原子体积占晶胞体积的百分率为
a3
𝐞𝐪 𝟒 𝟑 𝐞𝐪 𝟑 𝟒
×100%≈68%。
6、钴晶体的一种晶胞(如图2所示)的边长为a nm,密度为ρ g·cm-3,N 表示阿伏加德罗常数的值,则钴
A
原子半径为________nm,钴的相对原子质量可表示为________。
【答案】 a 5a3ρN ×10-22
A
【解析】 由钴晶体的晶胞可知,晶胞中含有钴原子的数目为 8×+1=2,晶胞体积V=(a×10-7cm)3,由
于体对角线的长度是钴原子半径的 4倍,钴原子半径为a nm,设钴的相对原子质量为M,ρ=,则M=
5a3ρN ×10-22。
A
7、立方氮化硼的硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于
__________晶体,其中硼原子的配位数为________。已知:立方氮化硼的密度为d g·cm-3,B原子半径为
x pm,N 原子半径为 y pm,阿伏加德罗常数的值为 N ,则该晶胞中原子的空间利用率为
A
______________(列出化简后的计算式)。(B:11 N:14)
【答案】 共价 4 ×100%
【解析】 立方氮化硼的硬度仅次于金刚石,晶体类型类似于金刚石,是共价晶体;晶胞中每个 N原子连
接4个B原子,氮化硼的化学式为BN,所以晶胞中每个B原子也连接4个N原子,即硼原子的配位数为
4;晶胞中N原子数为4,B原子数为8×+6×=4,晶胞的质量m= g,晶胞的体积V== cm3= cm3,
B、N 原子总体积 V′=4×[+]=×(x3+y3)×10-30 cm3,晶胞中原子的空间利用率为×100%=×100%=
×100%。
8、氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼(图1)和立方氮化硼(图2)。前者与石墨结构类似。(B:11 N:14)
(1)50.0 g六方氮化硼晶体中含有六元环的数目为______。
(2)立方氮化硼中N的配位数为________。已知立方氮化硼密度为d g·cm-3,N 代表阿伏加德罗常数的
A
值,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边长为________ pm(列式即
可)。
【答案】 (1)2N (2)4 ××1010
A
【解析】 (1)根据切割法,一个六方氮化硼晶体的六元环含有一个N、一个B,50.0 g六方氮化硼晶体中含
有六元环的数目为×N =2N 。
A A
(2)由图2可知,立方氮化硼中N的配位数为4;面心上6个N原子构成正八面体,该正八面体的边长等于
面对角线的一半,设BN晶胞边长为a cm,1个晶胞中含有4个B原子,含有N原子数为8×+6×=4,则1
个晶胞中含有4个BN,所以d=,解得a=,故正八面体的边长为××1010 pm。
9、Zn与S所形成化合物晶体的晶胞如图所示。Zn2+的配位数是________,S2-填充在Zn2+形成的正四面体
空隙中。若该晶体的密度为d g·cm-3,阿伏加德罗常数的值为N ,则该晶胞参数a= ________ nm。
A
(Zn:65 S:32)
【答案】 4 ×107
【解析】 根据晶胞结构可知晶胞中含有Zn2+个数为8×+6×=4,S2-全部在晶胞内,共4个,其化学式
是ZnS。根据晶胞结构可知S2-位于4个Zn2+形成的正四面体空隙中,S2-的配位数是4,根据化学式可判
断Zn2+的配位数也是4。若该晶体的密度为d g·cm-3,阿伏加德罗常数的值为N ,则d=,因此该晶胞参
A
数a= cm=×107 nm。
10、氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρ g·cm-3,N 代表阿伏加德罗常数的
A
值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为________;Fe2+与O2-的最短核间距为________pm。
(Fe:56 O:16)【答案】 12 ×1010
【解析】 根据图2晶胞结构可知,Fe2+位于顶角和面心,与Fe2+紧邻且等距离的Fe2+有12个;用切割法
可得晶胞中Fe2+的数目为8×+6×=4,O2-的数目为12×+1=4,晶体的化学式为FeO,根据晶体密度计算
公式可知,晶胞的边长为 cm,Fe2+与O2-的最短核间距为× cm= cm=×1010 pm。
11、MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的
晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a′=0.448
nm,则r(Mn2+)为________nm。
【答案】 0.148 0.076
【解析】 因为O2-是面心立方最密堆积方式,面对角线是O2-半径的4倍,即4r(O2-)=a,解得r(O2-)=
×0.420 nm≈0.148 nm;MnO也属于NaCl型结构,根据晶胞的结构,晶胞参数=2r(O2-)+2r(Mn2+),则
r(Mn2+)==0.076 nm。
12、萤石(CaF )晶胞结构如图所示,晶胞边长为 a pm,Ca2+和F-半径大小分别为r 和r 。该晶胞中Ca2+
2 1 2
的配位数为 ,Ca2+和F-的最近距离为 。
【答案】 8
【解析】 根据晶胞可知,Ca2+和F-最近距离是体对角线的,即为a pm。
13、镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。
已知一定条件下晶胞的棱长为a nm,用NA表示阿伏伽德罗常数的值,在该条件下该晶体的摩尔体积为
m3·mol-1。(用含a、NA的代数式表示)【答案】 N ·a3·10-27
A
14、GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其晶胞结构如图3所示。该晶体的类型为________,Ga
与As以________键合。Ga和As的摩尔质量分别为 M(Ga) g·mol-1和M(As) g·mol-1,原子半径分别为
r(Ga) pm 和 r(As) pm,阿伏加德罗常数值为 N ,则 GaAs 晶胞中原子的体积占晶胞体积的百分率为
A
________。
【答案】共价晶体 共价键 ×100%
【解析】GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其晶胞结构如题图3所示,熔点很高,所以晶体的类
型为共价晶体,其中Ga与As以共价键键合。根据晶胞结构可知晶胞中Ga和As的个数均是4个,所以晶
胞的体积是,二者的原子半径分别为r(Ga) pm和r(As) pm,阿伏加德罗常数值为N ,则GaAs晶胞中原
A
子的体积占晶胞体积的百分率为×100%=×100%。
15、磷化硼是一种超硬耐磨的涂层材料,其晶胞如图所示。P原子与B原子的最近距离为a cm,则磷化硼
晶胞的边长为________cm(用含a的代数式表示)。
【答案】
【解析】P原子与B原子的最近距离为a cm,为晶胞体对角线长的,晶胞体对角线长等于棱长的倍,则晶
胞棱长 cm。