文档内容
2022 届高三化学二轮复习合成有机高分子化合物专题练习
一、选择题(共17题)
1.现有两种高聚物A、B,A能溶于苯、四氯化碳等有机溶剂,并加热到一定温度下熔融成粘稠状的液体,
B不溶于任何溶剂,加热不会变软或熔融,则下列叙述中不正确的是( )。
A.高聚物A可能具有弹性,而高聚物B没有弹性
B.高聚物A一定是线型高分子材料
C.高聚物A一定是体型高分子材料
D.高聚物B一定是体型高分子材料
2.下列物质一定属于有机高分子化合物的是
A.油脂 B.糖类 C.蛋白质 D.四氟乙烯
3.能形成高分子化合物的反应类型是
A.消去反应 B.复分解反应 C.置换反应 D.聚合反应
4.下列关于有机化合物的说法正确的是
A.淀粉、油脂、蛋白质都属于高分子化合物
B.乙醇、乙酸、乙酸乙酯都能发生取代反应
C.聚乙烯、苯乙烯都能使溴的四氯化碳溶液和酸性KMnO 溶液褪色
4
D.硝基苯分子中苯环上的一个H被—C H 取代后形成的有机物共有9种
4 9
5.“喷水溶液法”是一种使沙漠变绿洲的新技术,它是先在沙漠中喷洒一定量的聚丙烯酸酯水溶液,水
溶液中的高分子与沙土粒子结合,在地表下30~50cm处形成一个厚0.5cm的隔水层,既能阻止地下的盐
分上升,又有拦截、蓄积雨水的作用.下列关于聚丙烯酸酯的说法错误是
A.单体的结构式为CH=CH-COOR
2
B.由单体合成聚丙烯酸酯属加聚反应
C.在一定条件下能发生水解反应
D.有固定的熔沸点
6.丁苯橡胶的化学组成为 ,其单体一定有( )
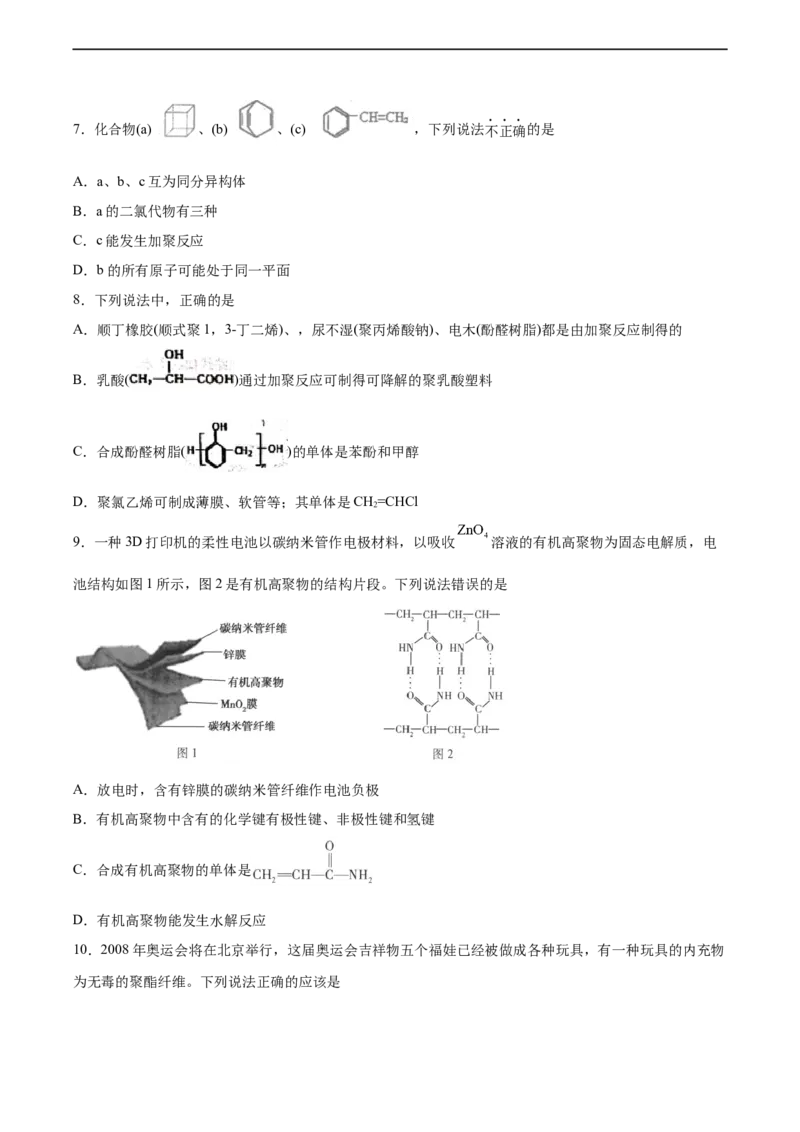
A.2﹣丁炔 B.1,3﹣丁二烯 C.乙苯 D.乙烯7.化合物(a) 、(b) 、(c) ,下列说法不正确的是
A.a、b、c互为同分异构体
B.a的二氯代物有三种
C.c能发生加聚反应
D.b的所有原子可能处于同一平面
8.下列说法中,正确的是
A.顺丁橡胶(顺式聚1,3-丁二烯)、,尿不湿(聚丙烯酸钠)、电木(酚醛树脂)都是由加聚反应制得的
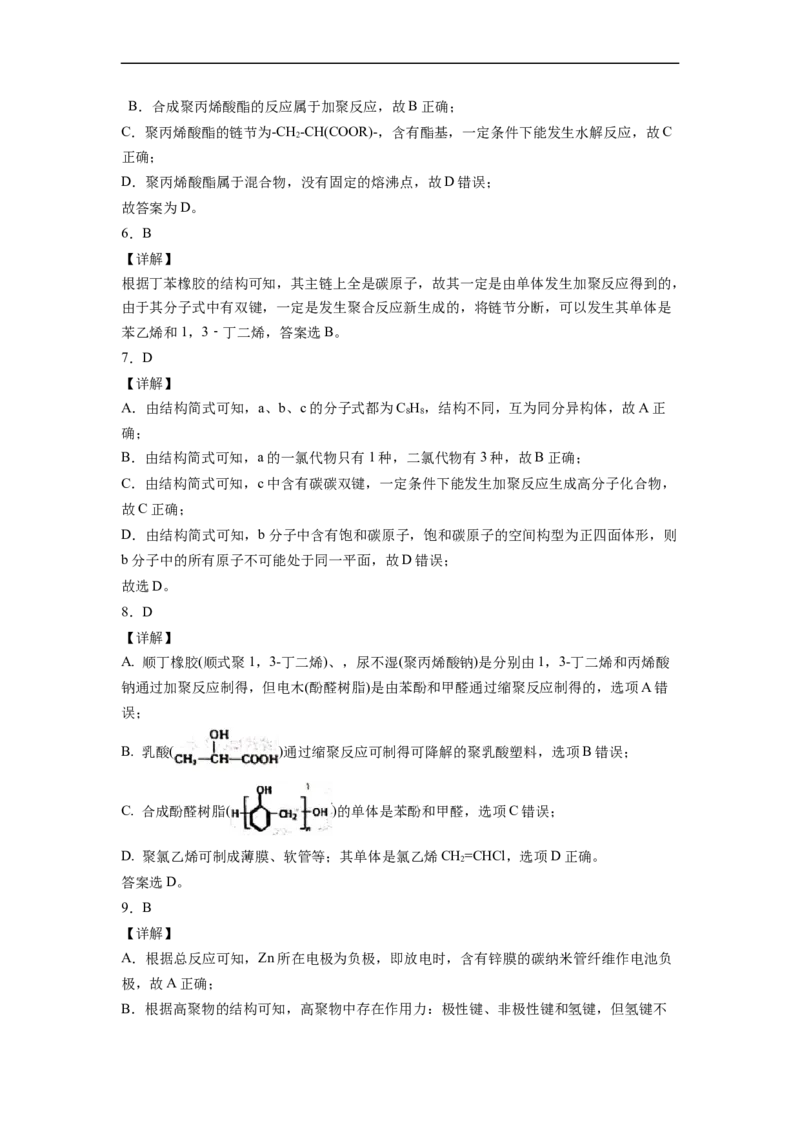
B.乳酸( )通过加聚反应可制得可降解的聚乳酸塑料
C.合成酚醛树脂( )的单体是苯酚和甲醇
D.聚氯乙烯可制成薄膜、软管等;其单体是CH=CHCl
2
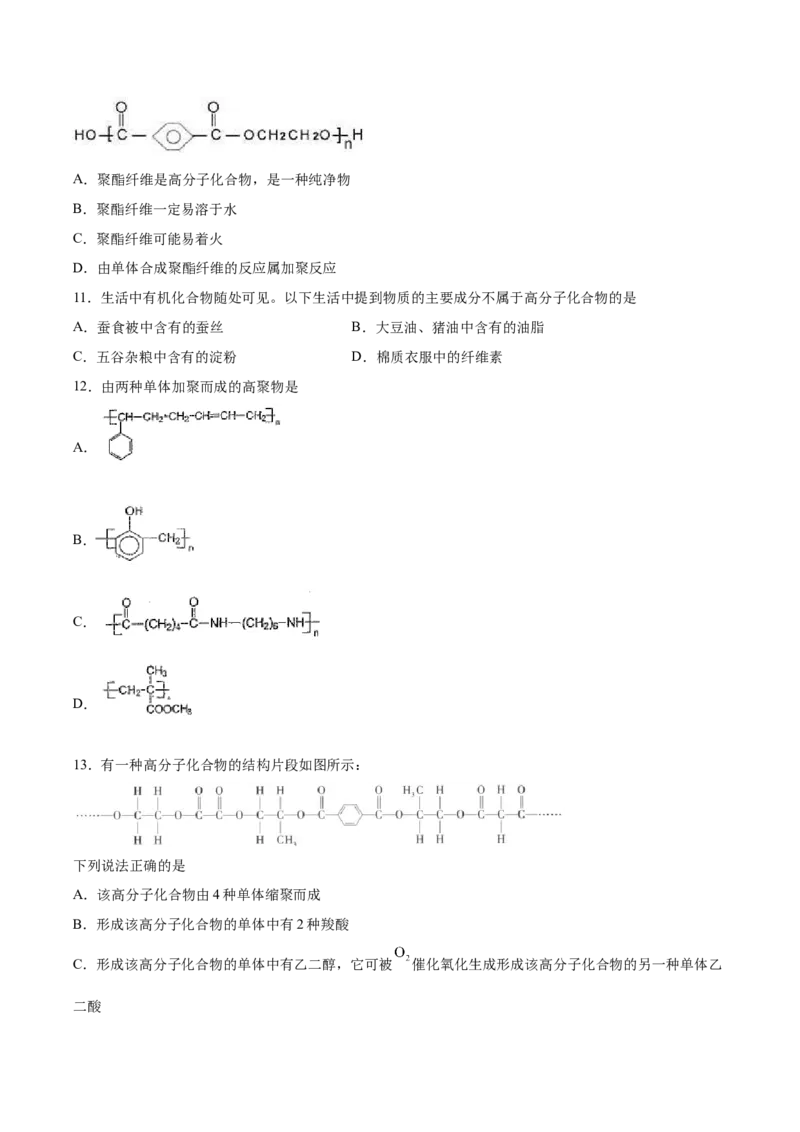
9.一种3D打印机的柔性电池以碳纳米管作电极材料,以吸收 溶液的有机高聚物为固态电解质,电
池结构如图1所示,图2是有机高聚物的结构片段。下列说法错误的是
A.放电时,含有锌膜的碳纳米管纤维作电池负极
B.有机高聚物中含有的化学键有极性键、非极性键和氢键
C.合成有机高聚物的单体是
D.有机高聚物能发生水解反应
10.2008年奥运会将在北京举行,这届奥运会吉祥物五个福娃已经被做成各种玩具,有一种玩具的内充物
为无毒的聚酯纤维。下列说法正确的应该是A.聚酯纤维是高分子化合物,是一种纯净物
B.聚酯纤维一定易溶于水
C.聚酯纤维可能易着火
D.由单体合成聚酯纤维的反应属加聚反应
11.生活中有机化合物随处可见。以下生活中提到物质的主要成分不属于高分子化合物的是
A.蚕食被中含有的蚕丝 B.大豆油、猪油中含有的油脂
C.五谷杂粮中含有的淀粉 D.棉质衣服中的纤维素
12.由两种单体加聚而成的高聚物是
A.
B.
C.
D.
13.有一种高分子化合物的结构片段如图所示:
下列说法正确的是
A.该高分子化合物由4种单体缩聚而成
B.形成该高分子化合物的单体中有2种羧酸
C.形成该高分子化合物的单体中有乙二醇,它可被 催化氧化生成形成该高分子化合物的另一种单体乙
二酸D.该高分子化合物有固定的熔、沸点
14.下列有关说法不正确的是
A.“蚕月条桑……八月载绩”,描述的是采桑与织麻布,鉴别丝绸与棉麻制品可采用灼烧的方法
B.尼龙绳、宣纸、羊绒衫、棉衬衣这些生活用品中都主要由合成纤维制造
C.古代造纸是以树皮、麻头、破布、鱼网等植物纤维为原料,纤维素是天然的高分子材料
D.加热能杀死流感病毒是因为蛋白质受热变性
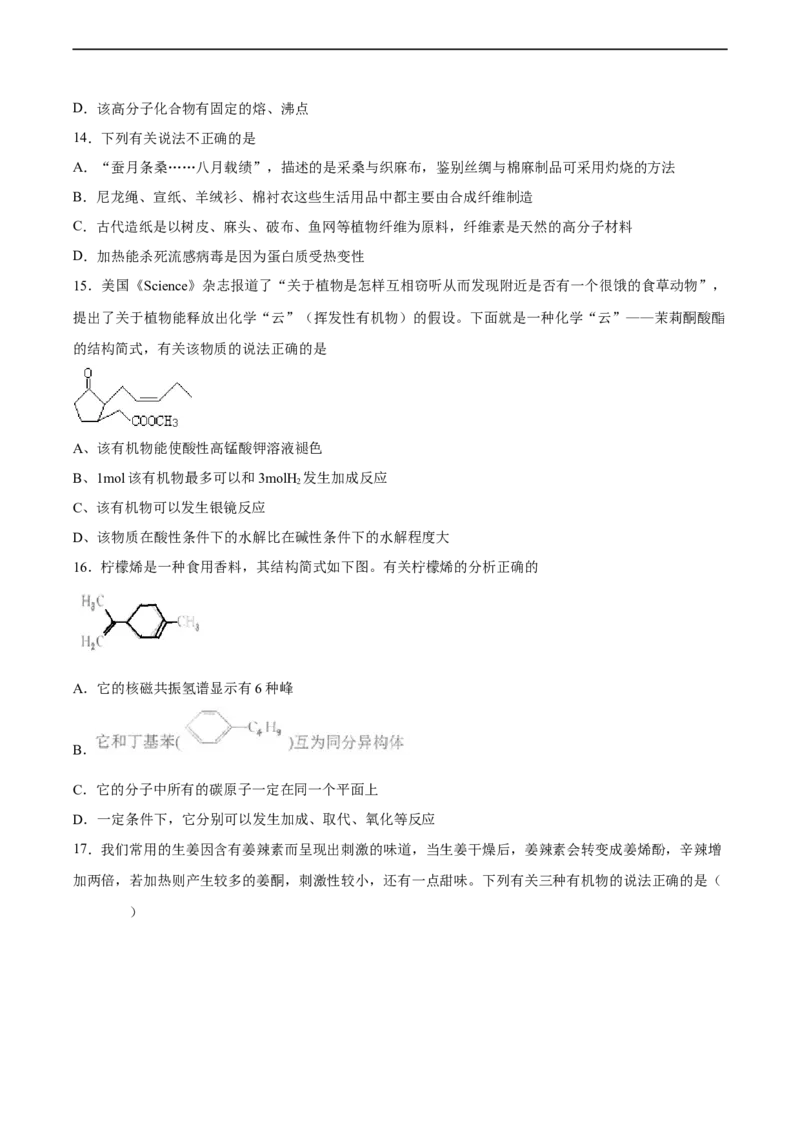
15.美国《Science》杂志报道了“关于植物是怎样互相窃听从而发现附近是否有一个很饿的食草动物”,
提出了关于植物能释放出化学“云”(挥发性有机物)的假设。下面就是一种化学“云”——茉莉酮酸酯
的结构简式,有关该物质的说法正确的是
A、该有机物能使酸性高锰酸钾溶液褪色
B、1mol该有机物最多可以和3molH 发生加成反应
2
C、该有机物可以发生银镜反应
D、该物质在酸性条件下的水解比在碱性条件下的水解程度大
16.柠檬烯是一种食用香料,其结构简式如下图。有关柠檬烯的分析正确的
A.它的核磁共振氢谱显示有6种峰
B.
C.它的分子中所有的碳原子一定在同一个平面上
D.一定条件下,它分别可以发生加成、取代、氧化等反应
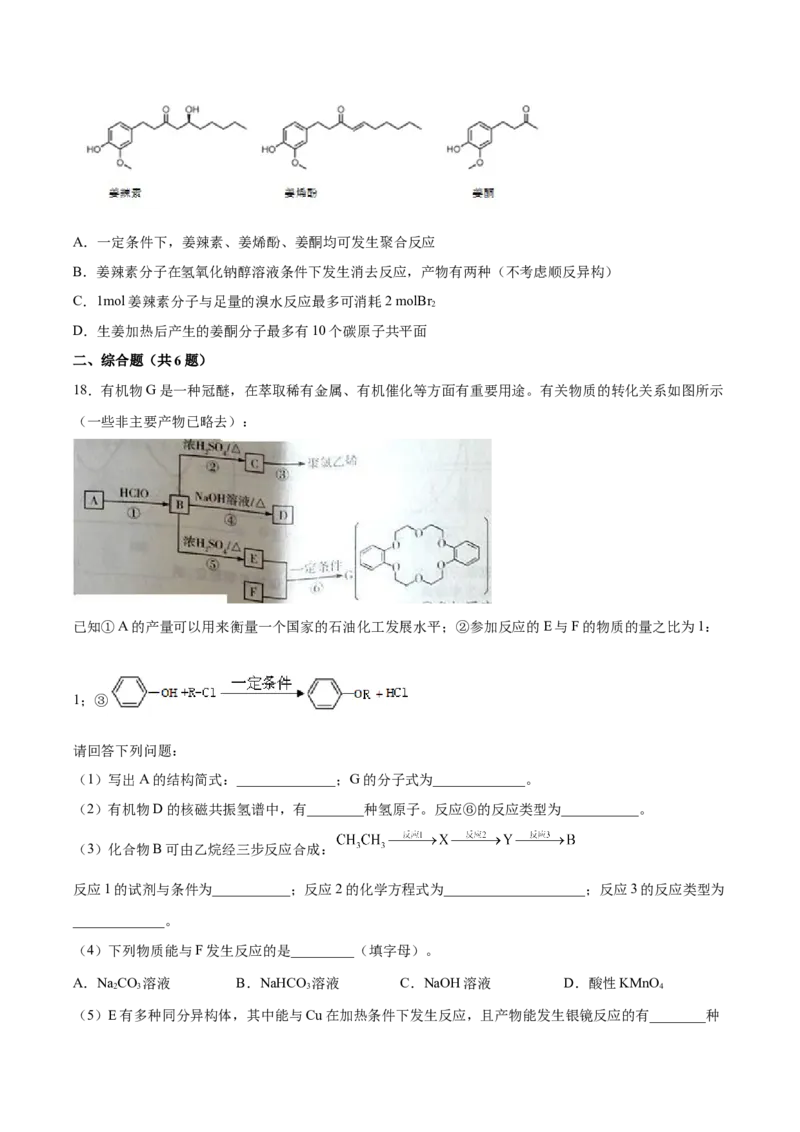
17.我们常用的生姜因含有姜辣素而呈现出刺激的味道,当生姜干燥后,姜辣素会转变成姜烯酚,辛辣增
加两倍,若加热则产生较多的姜酮,刺激性较小,还有一点甜味。下列有关三种有机物的说法正确的是(
)A.一定条件下,姜辣素、姜烯酚、姜酮均可发生聚合反应
B.姜辣素分子在氢氧化钠醇溶液条件下发生消去反应,产物有两种(不考虑顺反异构)
C.1mol姜辣素分子与足量的溴水反应最多可消耗2 molBr
2
D.生姜加热后产生的姜酮分子最多有10个碳原子共平面
二、综合题(共6题)
18.有机物G是一种冠醚,在萃取稀有金属、有机催化等方面有重要用途。有关物质的转化关系如图所示
(一些非主要产物已略去):
已知①A的产量可以用来衡量一个国家的石油化工发展水平;②参加反应的E与F的物质的量之比为1:
1;③
请回答下列问题:
(1)写出A的结构简式:______________;G的分子式为_____________。
(2)有机物D的核磁共振氢谱中,有________种氢原子。反应⑥的反应类型为___________。
(3)化合物B可由乙烷经三步反应合成:
反应1的试剂与条件为___________;反应2的化学方程式为____________________;反应3的反应类型为
_____________。
(4)下列物质能与F发生反应的是_________(填字母)。
A.NaCO 溶液 B.NaHCO 溶液 C.NaOH溶液 D.酸性KMnO
2 3 3 4
(5)E有多种同分异构体,其中能与Cu在加热条件下发生反应,且产物能发生银镜反应的有________种(不考虑立体异构)。
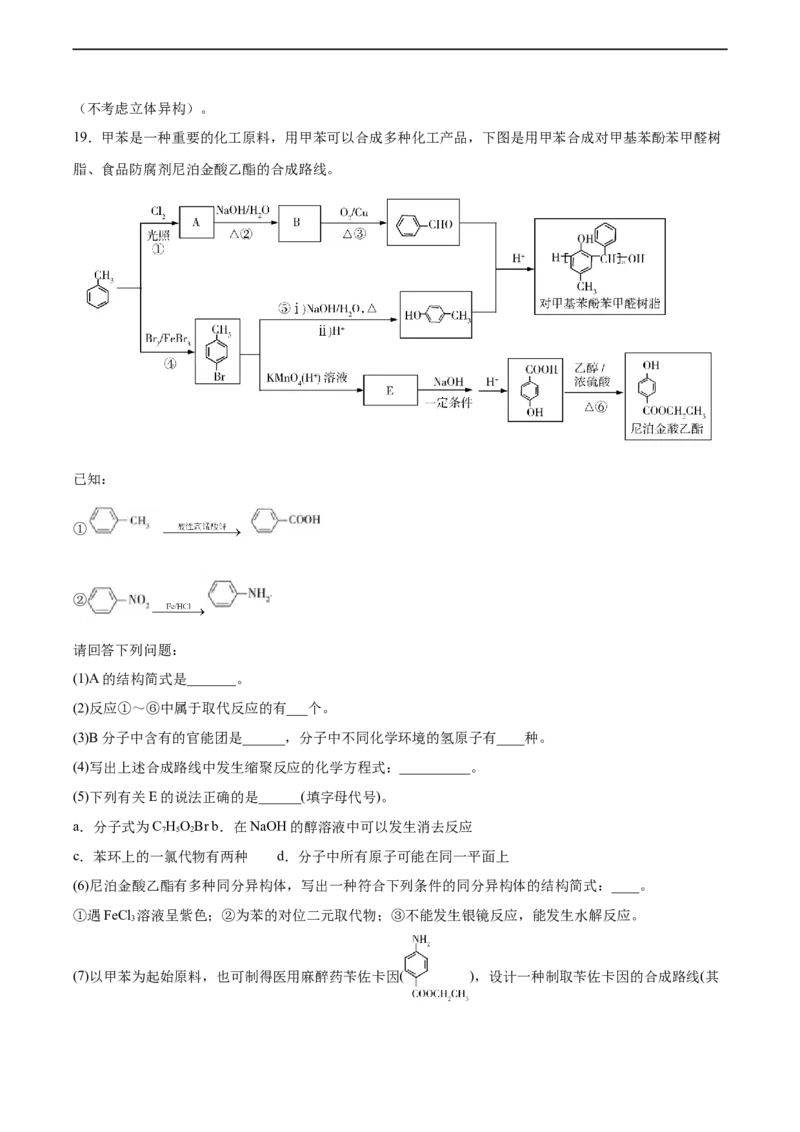
19.甲苯是一种重要的化工原料,用甲苯可以合成多种化工产品,下图是用甲苯合成对甲基苯酚苯甲醛树
脂、食品防腐剂尼泊金酸乙酯的合成路线。
已知:
①
②
请回答下列问题:
(1)A的结构简式是_______。
(2)反应①~⑥中属于取代反应的有___个。
(3)B分子中含有的官能团是______,分子中不同化学环境的氢原子有____种。
(4)写出上述合成路线中发生缩聚反应的化学方程式:__________。
(5)下列有关E的说法正确的是______(填字母代号)。
a.分子式为C HOBr b.在NaOH的醇溶液中可以发生消去反应
7 5 2
c.苯环上的一氯代物有两种 d.分子中所有原子可能在同一平面上
(6)尼泊金酸乙酯有多种同分异构体,写出一种符合下列条件的同分异构体的结构简式:____。
①遇FeCl 溶液呈紫色;②为苯的对位二元取代物;③不能发生银镜反应,能发生水解反应。
3
(7)以甲苯为起始原料,也可制得医用麻醉药苄佐卡因( ),设计一种制取苄佐卡因的合成路线(其他反应物自选)_____________。
20.X、 Y、Z均为非金属元素(X的原子序数小于Y的原子序数),三者形成多种化合物。其中分子式为
XYZ 的化合物被认为是潜在的储氢材料,氢的质量分数达19.6%。
6
(1)通过计算说明X、Y、Z各是什么元素___________、___________、___________。
(2)下图示出XYZ 及相关化合物的生成与转化的流程图:
6
其中,实线箭头表示在一定条件的转化过程,虚线仅表示分子式的关联关系:由A和B制备XYZ 的过程
6
中给出了所有的反应物和产物,而其他过程仅给出所有反应物及其参与反应的计量系数的比例(例如,A →
C,箭头上的1/2B表示“2A+B”反应, 产物为C或者C和其他可能的物质,计量系数未给出); B和D的
结构中均含有正四面体构型的负离子基团,E、F和G均为六元环结构。根据图中的关系与所述条件,写
出化合物A、B.C、D、E、F、G、H和I的化学式:___________、画出D和G的结构简式___________;
写出D与A产生C的反应方程式___________。
21.天宫二号空间实验室已于2016 年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问
题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是______(填化学式)
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂
的反应类型是_____________。
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命
和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是_____,其能量转化方式为_____。
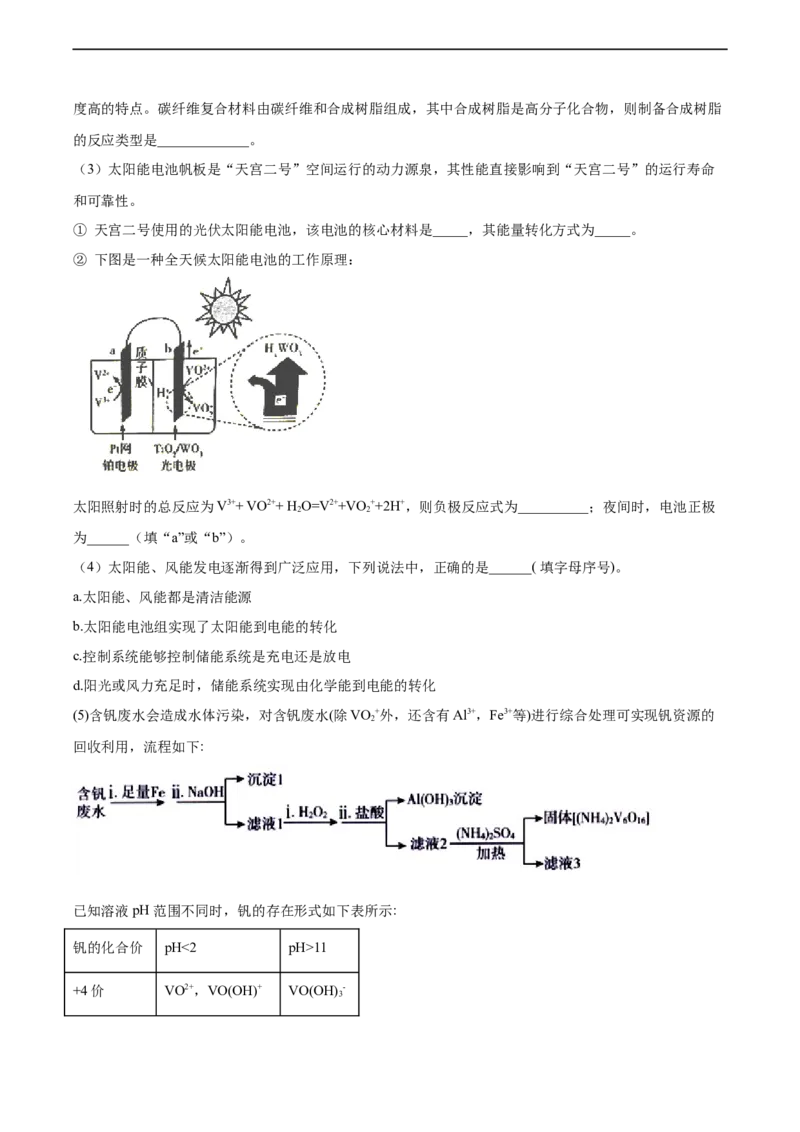
② 下图是一种全天候太阳能电池的工作原理:
太阳照射时的总反应为V3++ VO2++ H O=V2++VO++2H+,则负极反应式为__________;夜间时,电池正极
2 2
为______(填“a”或“b”)。
(4)太阳能、风能发电逐渐得到广泛应用,下列说法中,正确的是______( 填字母序号)。
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(5)含钒废水会造成水体污染,对含钒废水(除VO +外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的
2
回收利用,流程如下:
已知溶液pH 范围不同时,钒的存在形式如下表所示:
钒的化合价 pH<2 pH>11
+4价 VO2+,VO(OH)+ VO(OH) -
3+5价 VO + VO 3-
2 4
①加入NaOH 调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入
NaOH 后生成沉淀1的反应过程为_______、_______;所得滤液1中,铝元素的存在形式为__________。
②向碱性的滤液1 ( V的化合价为+4 )中加入HO 的作用是________(用离子方程式表示)。
2 2
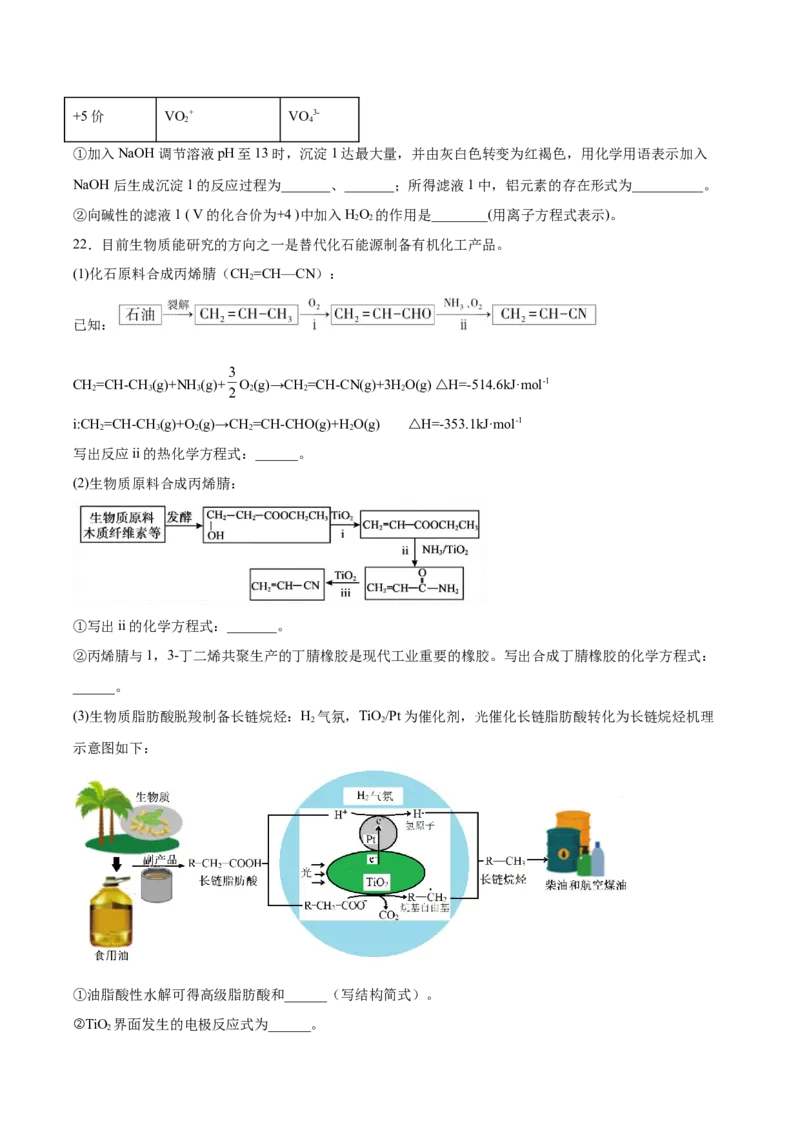
22.目前生物质能研究的方向之一是替代化石能源制备有机化工产品。
(1)化石原料合成丙烯腈(CH=CH—CN):
2
已知:
CH=CH-CH(g)+NH (g)+ O(g)→CH =CH-CN(g)+3H O(g) △H=-514.6kJ·mol-1
2 3 3 2 2 2
i:CH =CH-CH(g)+O(g)→CH =CH-CHO(g)+H O(g) △H=-353.1kJ·mol-1
2 3 2 2 2
写出反应ii的热化学方程式:______。
(2)生物质原料合成丙烯腈:
①写出ii的化学方程式:_______。
②丙烯腈与1,3-丁二烯共聚生产的丁腈橡胶是现代工业重要的橡胶。写出合成丁腈橡胶的化学方程式:
______。
(3)生物质脂肪酸脱羧制备长链烷烃:H 气氛,TiO/Pt为催化剂,光催化长链脂肪酸转化为长链烷烃机理
2 2
示意图如下:
①油脂酸性水解可得高级脂肪酸和______(写结构简式)。
②TiO 界面发生的电极反应式为______。
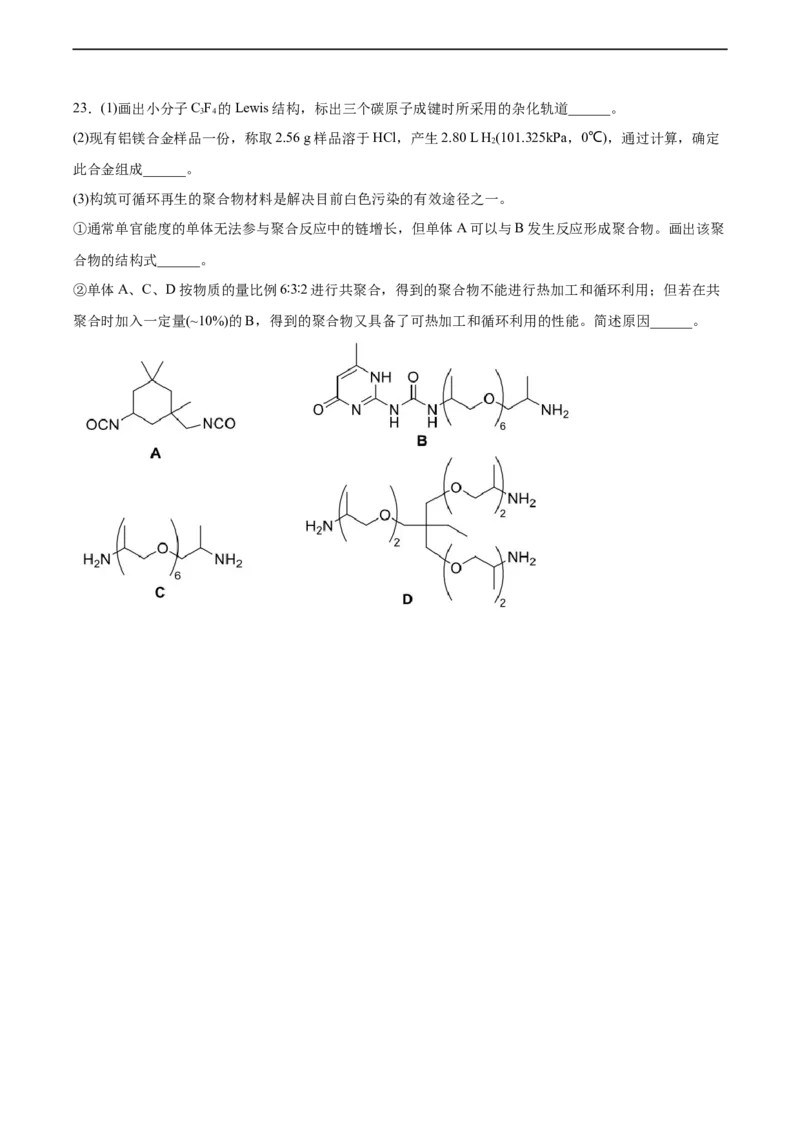
223.(1)画出小分子C F 的Lewis结构,标出三个碳原子成键时所采用的杂化轨道______。
3 4
(2)现有铝镁合金样品一份,称取2.56 g样品溶于HCl,产生2.80 L H (101.325kPa,0℃),通过计算,确定
2
此合金组成______。
(3)构筑可循环再生的聚合物材料是解决目前白色污染的有效途径之一。
①通常单官能度的单体无法参与聚合反应中的链增长,但单体A可以与B发生反应形成聚合物。画出该聚
合物的结构式______。
②单体A、C、D按物质的量比例6∶3∶2进行共聚合,得到的聚合物不能进行热加工和循环利用;但若在共
聚合时加入一定量(~10%)的B,得到的聚合物又具备了可热加工和循环利用的性能。简述原因______。参考答案
1.C
【详解】
A具有热塑性,应是线型结构,因而A可能有弹性和一定的溶解性;
B具有热固性,应是体型结构,没有弹性,一般也不溶解于溶剂。
2.C
【详解】
分析:本题考查的是有机高分子的定义,注意油脂不属于高分子化合物。
详解:A.油脂不是高分子化合物,故错误;B.糖类中的单糖和二糖都不是高分子化合物,
故错误;C.蛋白质是高分子化合物,故正确;D.四氟乙烯不是高分子化合物,故错误。故
选C。
3.D
【分析】
消去反应是指在一定条件下,有机物脱去小分子生成含有不饱和的有机物的反应;
复分解反应为两种化合物反应生成两种新的化合物的反应;
置换反应为单质与化合物反应生成新的单质和化合物的反应;
聚合反应:由相对分子质量小的化合物分子相互结合成相对分子质量大的高分子的反应叫
做聚合反应,根据以上概念进行判断。
【详解】
A.消去反应为有机物脱去小分子形成不饱和有机物的反应,如乙醇通过消去反应生成乙
烯,该反应中不会生成高分子化合物,选项A错误;
B.复分解反应为无机反应类型,反应中不会生成高分子化合物,选项B错误;
C.置换反应为单质与化合物反应生成新的单质和化合物的反应,不会生成高分子化合物,
选项C错误;
D.聚合反应分为加聚反应和缩聚反应,反应中生成高分子化合物,选项D正确;
答案选D。
4.B
【解析】A项,淀粉、蛋白质的相对分子质量很大,都属于高分子化合物,油脂是小分子
化合物,故A错误;B项,乙醇、乙酸的羟基和乙酸乙酯的酯基都可以发生取代反应,其
与碳相连的氢原子也可以与卤素原子发生取代反应,故B正确;C项,苯乙烯结构中含有
碳碳双键,能与溴单质发生加成反应,能被酸性KMnO 溶液氧化,所以苯乙烯能使溴的四
4
氯化碳溶液和酸性KMnO 溶液褪色,而聚乙烯结构中无碳碳双键,因此不能发生上述变化,
4
故C错误;D项,-C H 可形成4种取代基,每一种取代基都可以在苯环上硝基的邻位、间
4 9
位和对位形成三种异构体,所以共形成3×4=12种有机物,故D错误。综上,选B。
5.D
【详解】
A.由高分子化合物的结构简式可知其单体为CH=CHCOOR,故A正确;
2B.合成聚丙烯酸酯的反应属于加聚反应,故B正确;
C.聚丙烯酸酯的链节为-CH-CH(COOR)-,含有酯基,一定条件下能发生水解反应,故C
2
正确;
D.聚丙烯酸酯属于混合物,没有固定的熔沸点,故D错误;
故答案为D。
6.B
【详解】
根据丁苯橡胶的结构可知,其主链上全是碳原子,故其一定是由单体发生加聚反应得到的,
由于其分子式中有双键,一定是发生聚合反应新生成的,将链节分断,可以发生其单体是
苯乙烯和1,3﹣丁二烯,答案选B。
7.D
【详解】
A.由结构简式可知,a、b、c的分子式都为C H,结构不同,互为同分异构体,故A正
8 8
确;
B.由结构简式可知,a的一氯代物只有1种,二氯代物有3种,故B正确;
C.由结构简式可知,c中含有碳碳双键,一定条件下能发生加聚反应生成高分子化合物,
故C正确;
D.由结构简式可知,b分子中含有饱和碳原子,饱和碳原子的空间构型为正四面体形,则
b分子中的所有原子不可能处于同一平面,故D错误;
故选D。
8.D
【详解】
A. 顺丁橡胶(顺式聚1,3-丁二烯)、,尿不湿(聚丙烯酸钠)是分别由1,3-丁二烯和丙烯酸
钠通过加聚反应制得,但电木(酚醛树脂)是由苯酚和甲醛通过缩聚反应制得的,选项A错
误;
B. 乳酸( )通过缩聚反应可制得可降解的聚乳酸塑料,选项B错误;
C. 合成酚醛树脂( )的单体是苯酚和甲醛,选项C错误;
D. 聚氯乙烯可制成薄膜、软管等;其单体是氯乙烯CH=CHCl,选项D正确。
2
答案选D。
9.B
【详解】
A.根据总反应可知,Zn所在电极为负极,即放电时,含有锌膜的碳纳米管纤维作电池负
极,故A正确;
B.根据高聚物的结构可知,高聚物中存在作用力:极性键、非极性键和氢键,但氢键不是化学键,故B错误;
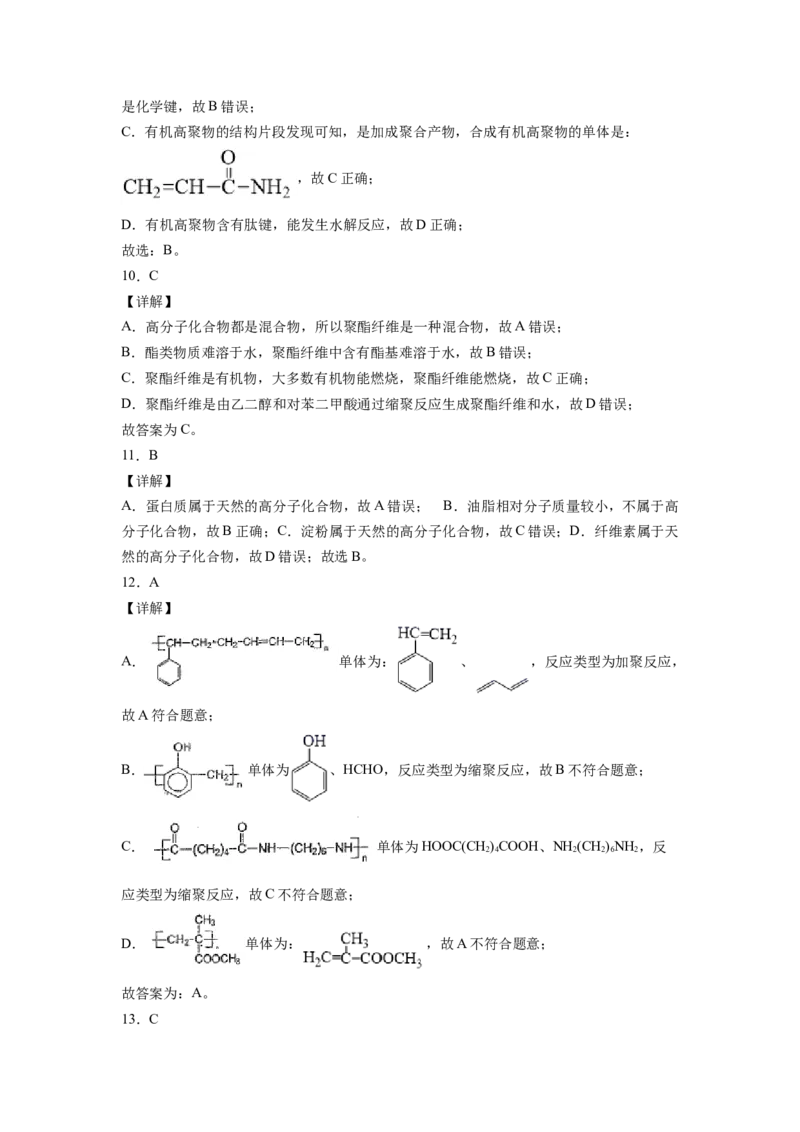
C.有机高聚物的结构片段发现可知,是加成聚合产物,合成有机高聚物的单体是:
,故C正确;
D.有机高聚物含有肽键,能发生水解反应,故D正确;
故选:B。
10.C
【详解】
A.高分子化合物都是混合物,所以聚酯纤维是一种混合物,故A错误;
B.酯类物质难溶于水,聚酯纤维中含有酯基难溶于水,故B错误;
C.聚酯纤维是有机物,大多数有机物能燃烧,聚酯纤维能燃烧,故C正确;
D.聚酯纤维是由乙二醇和对苯二甲酸通过缩聚反应生成聚酯纤维和水,故D错误;
故答案为C。
11.B
【详解】
A.蛋白质属于天然的高分子化合物,故A错误; B.油脂相对分子质量较小,不属于高
分子化合物,故B正确;C.淀粉属于天然的高分子化合物,故C错误;D.纤维素属于天
然的高分子化合物,故D错误;故选B。
12.A
【详解】
A. 单体为: 、 ,反应类型为加聚反应,
故A符合题意;
B. 单体为 、HCHO,反应类型为缩聚反应,故B不符合题意;
C. 单体为HOOC(CH )COOH、NH (CH)NH ,反
2 4 2 2 6 2
应类型为缩聚反应,故C不符合题意;
D. 单体为: ,故A不符合题意;
故答案为:A。
13.C【详解】
A.形成该高分子化合物的单体有 、 ,
共5种,故A错误;
B.形成该高分子化合物的单体中有乙二酸、对苯二甲酸和丙二酸,共有3种羧酸,故B
错误;
C.结合前面的分析及乙二醇可被 催化氧化生成乙二酸可知,故C正确;
D.该高分子化合物没有固定的熔、沸点,故D错误;
故选:C。
14.B
【详解】
A、丝绸是蛋白质,灼烧时有烧焦羽毛的气味,棉麻制品是纤维素,灼烧时没有气味,可
以鉴别,选项A正确;B、宣纸、棉衬衣中主要成分为纤维素,羊绒衫主要成分为蛋白质,
选项B错误;C、古代造纸是以树皮、麻头、破布、鱼网等植物纤维为原料,纤维素是天
然的高分子材料,选项C正确;D、加热能杀死流感病毒是因为蛋白质受热变性,选项D
正确。答案选B。
15.A
【解析】
试题分析:B项最多可以和2molH 发生加成反应;C项有机物中没有醛基,不能发生银镜
2
反应;D项该物质在碱性条件下的水解程度大。
考点:有机物的结构和性质。
16.D
【解析】
试题分析:柠檬烯中有8种不同环境的H原子,即核磁共振氢谱显示有8种峰,A不正确;
柠檬烯的分子式是C H ,丁基苯的分子式是C H ,选项B不正确;柠檬烯分子中所有的
10 16 10 14
碳原子不可能在同一平面内,选项C不正确;碳碳双键可发生加成、氧化反应,烃基上的
H可以被取代,选项D正确。
考点:有机物的性质 涉及同分异构体、碳碳双键的结构和性质
17.A
【详解】
A. 姜辣素含有两个羟基,可以进行缩聚反应,姜烯酚含有碳碳双键,可以进行加聚反应,
姜酮只有一个羟基,一定条件下,可以转化出两个羟基,也可以发生加聚反应,A项正确;
B. 氢氧化钠醇溶液能使卤代烃发生消去反应,姜辣素不含卤元素,不能发生消去反应,B
项错误;
C. 姜辣素分子存在酚羟基,Br 可取代酚羟基邻位、对位的H,姜辣素只存在一个邻位
2H,1mol姜辣素与足量的溴水反应最多可消耗1 molBr ,C项错误;
2
D. 生姜加热后产生的姜酮分子最多有11个碳原子共平面,D项错误。
答案选A。
18.CH=CH C H O 2 取代反应 Cl/光照 CHCHCl+NaOH
2 2 20 24 6 2 3 2
CH=CH ↑+NaCl+HO 加成反应 acd 9
2 2 2
【详解】
试题分析:根据已知条件可知A是CH=CH ,由氯乙烯可逆推知C是CH=CHCl,结合②的
2 2 2
反应条件知道B是Cl;D 是HOCH CHOH;根据G的结构简式,结合B的组成及反应条
2 2
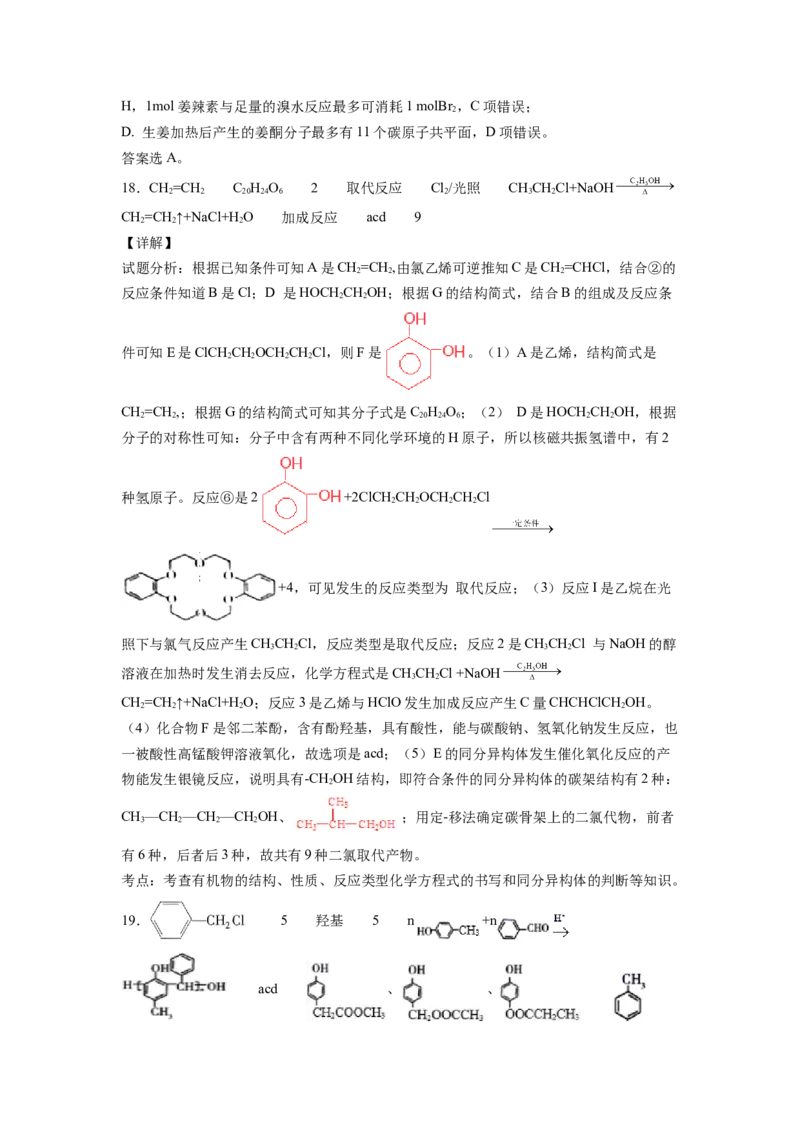
件可知E是ClCH CHOCH CHCl,则F是 。(1)A是乙烯,结构简式是
2 2 2 2
CH=CH ,;根据G的结构简式可知其分子式是C H O;(2) D是HOCH CHOH,根据
2 2 20 24 6 2 2
分子的对称性可知:分子中含有两种不同化学环境的H原子,所以核磁共振氢谱中,有2
种氢原子。反应⑥是2 +2ClCH CHOCH CHCl
2 2 2 2
+4,可见发生的反应类型为 取代反应;(3)反应I是乙烷在光
照下与氯气反应产生CHCHCl,反应类型是取代反应;反应2是CHCHCl 与NaOH的醇
3 2 3 2
溶液在加热时发生消去反应,化学方程式是CHCHCl +NaOH
3 2
CH=CH ↑+NaCl+HO;反应3是乙烯与HClO发生加成反应产生C量CHCHClCH OH。
2 2 2 2
(4)化合物F是邻二苯酚,含有酚羟基,具有酸性,能与碳酸钠、氢氧化钠发生反应,也
一被酸性高锰酸钾溶液氧化,故选项是acd;(5)E的同分异构体发生催化氧化反应的产
物能发生银镜反应,说明具有-CHOH结构,即符合条件的同分异构体的碳架结构有2种:
2
CH—CH—CH—CHOH、 ;用定-移法确定碳骨架上的二氯代物,前者
3 2 2 2
有6种,后者后3种,故共有9种二氯取代产物。
考点:考查有机物的结构、性质、反应类型化学方程式的书写和同分异构体的判断等知识。
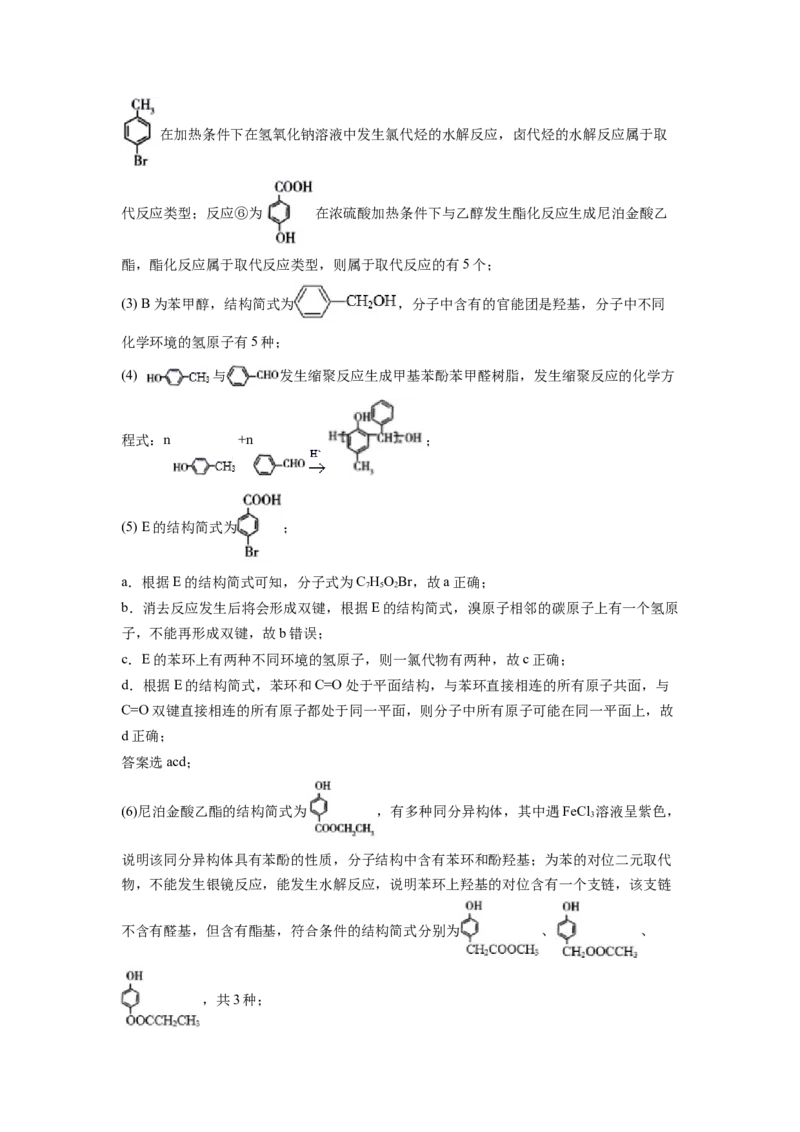
19. 5 羟基 5 n +n
acd 、 、【分析】
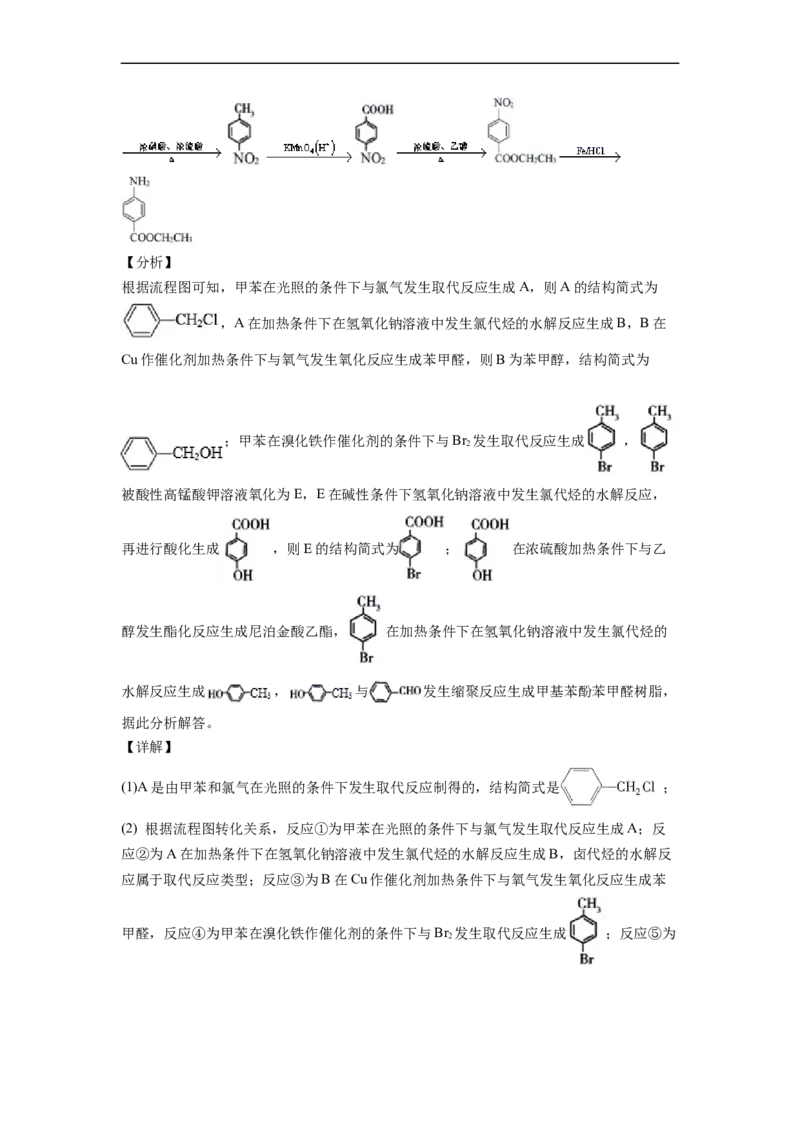
根据流程图可知,甲苯在光照的条件下与氯气发生取代反应生成A,则A的结构简式为
,A在加热条件下在氢氧化钠溶液中发生氯代烃的水解反应生成B,B在
Cu作催化剂加热条件下与氧气发生氧化反应生成苯甲醛,则B为苯甲醇,结构简式为
;甲苯在溴化铁作催化剂的条件下与Br 发生取代反应生成 ,
2
被酸性高锰酸钾溶液氧化为E,E在碱性条件下氢氧化钠溶液中发生氯代烃的水解反应,
再进行酸化生成 ,则E的结构简式为 ; 在浓硫酸加热条件下与乙
醇发生酯化反应生成尼泊金酸乙酯, 在加热条件下在氢氧化钠溶液中发生氯代烃的
水解反应生成 , 与 发生缩聚反应生成甲基苯酚苯甲醛树脂,
据此分析解答。
【详解】
(1)A是由甲苯和氯气在光照的条件下发生取代反应制得的,结构简式是 ;
(2) 根据流程图转化关系,反应①为甲苯在光照的条件下与氯气发生取代反应生成A;反
应②为A在加热条件下在氢氧化钠溶液中发生氯代烃的水解反应生成B,卤代烃的水解反
应属于取代反应类型;反应③为B在Cu作催化剂加热条件下与氧气发生氧化反应生成苯
甲醛,反应④为甲苯在溴化铁作催化剂的条件下与Br 发生取代反应生成 ;反应⑤为
2在加热条件下在氢氧化钠溶液中发生氯代烃的水解反应,卤代烃的水解反应属于取
代反应类型;反应⑥为 在浓硫酸加热条件下与乙醇发生酯化反应生成尼泊金酸乙
酯,酯化反应属于取代反应类型,则属于取代反应的有5个;
(3) B为苯甲醇,结构简式为 ,分子中含有的官能团是羟基,分子中不同
化学环境的氢原子有5种;
(4) 与 发生缩聚反应生成甲基苯酚苯甲醛树脂,发生缩聚反应的化学方
程式:n +n ;
(5) E的结构简式为 ;
a.根据E的结构简式可知,分子式为C HOBr,故a正确;
7 5 2
b.消去反应发生后将会形成双键,根据E的结构简式,溴原子相邻的碳原子上有一个氢原
子,不能再形成双键,故b错误;
c.E的苯环上有两种不同环境的氢原子,则一氯代物有两种,故c正确;
d.根据E的结构简式,苯环和C=O处于平面结构,与苯环直接相连的所有原子共面,与
C=O双键直接相连的所有原子都处于同一平面,则分子中所有原子可能在同一平面上,故
d正确;
答案选acd;
(6)尼泊金酸乙酯的结构简式为 ,有多种同分异构体,其中遇FeCl 溶液呈紫色,
3
说明该同分异构体具有苯酚的性质,分子结构中含有苯环和酚羟基;为苯的对位二元取代
物,不能发生银镜反应,能发生水解反应,说明苯环上羟基的对位含有一个支链,该支链
不含有醛基,但含有酯基,符合条件的结构简式分别为 、 、
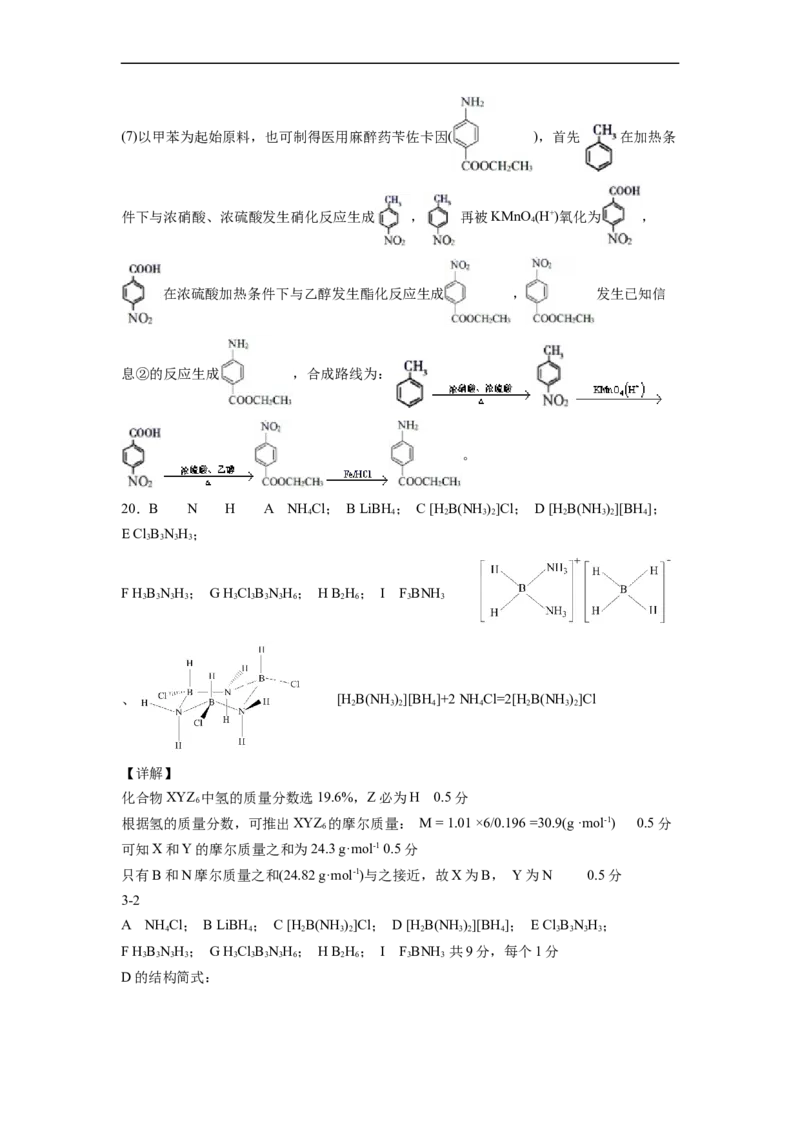
,共3种;(7)以甲苯为起始原料,也可制得医用麻醉药苄佐卡因( ),首先 在加热条
件下与浓硝酸、浓硫酸发生硝化反应生成 , 再被KMnO (H+)氧化为 ,
4
在浓硫酸加热条件下与乙醇发生酯化反应生成 , 发生已知信
息②的反应生成 ,合成路线为:
。
20.B N H A NH Cl; B LiBH; C [H B(NH )]Cl; D [HB(NH )][BH ];
4 4 2 3 2 2 3 2 4
E Cl B NH;
3 3 3 3
F HB NH; G HClB NH; H B H; I F BNH
3 3 3 3 3 3 3 3 6 2 6 3 3
、 [H B(NH )][BH ]+2 NH Cl=2[H B(NH )]Cl
2 3 2 4 4 2 3 2
【详解】
化合物XYZ 中氢的质量分数选19.6%,Z必为H 0.5分
6
根据氢的质量分数,可推出XYZ 的摩尔质量: M = 1.01 ×6/0.196 =30.9(g ·mol-1) 0.5分
6
可知X和Y的摩尔质量之和为24.3 g·mol-1 0.5分
只有B和N摩尔质量之和(24.82 g·mol-1)与之接近,故X为B, Y为N 0.5分
3-2
A NH Cl; B LiBH; C [H B(NH )]Cl; D [HB(NH )][BH ]; E Cl B NH;
4 4 2 3 2 2 3 2 4 3 3 3 3
F HB NH; G HClB NH; H B H; I F BNH 共9分,每个1分
3 3 3 3 3 3 3 3 6 2 6 3 3
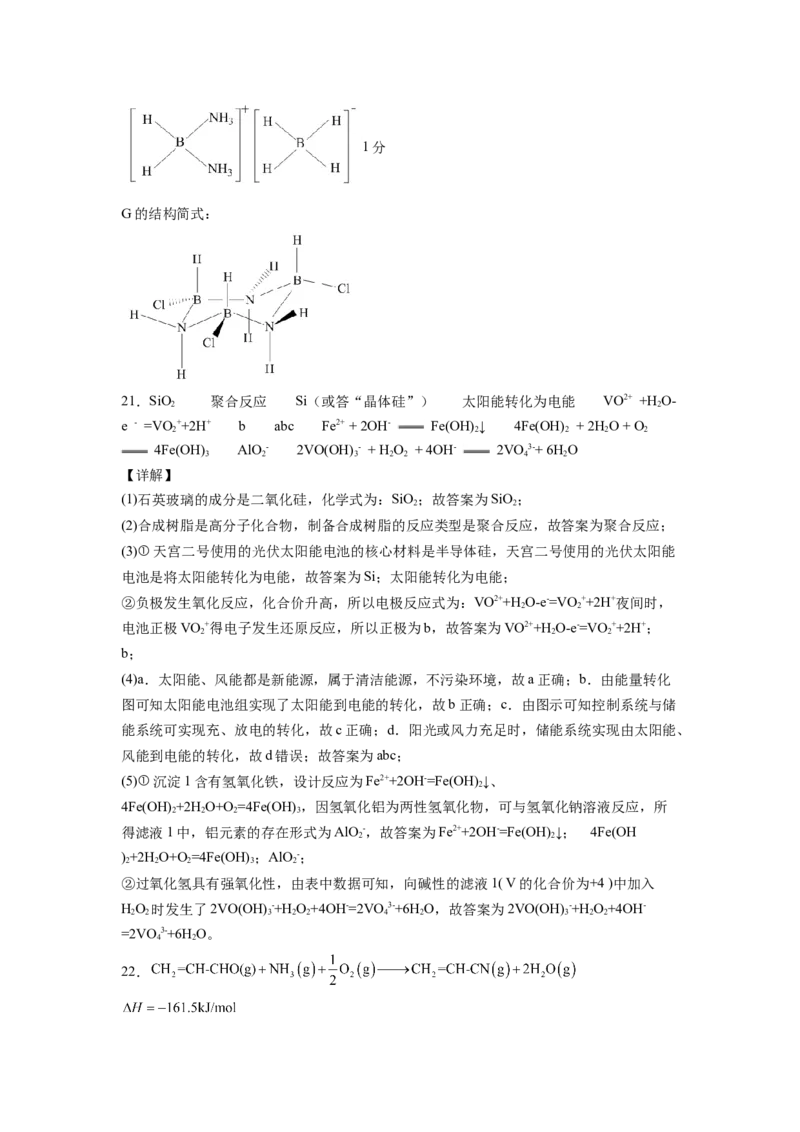
D的结构简式:1分
G的结构简式:
21.SiO 聚合反应 Si(或答“晶体硅”) 太阳能转化为电能 VO2+ +H O-
2 2
e - =VO++2H+ b abc Fe2+ + 2OH- Fe(OH) ↓ 4Fe(OH) + 2H O + O
2 2 2 2 2
4Fe(OH) AlO - 2VO(OH) - + H O + 4OH- 2VO 3-+ 6H O
3 2 3 2 2 4 2
【详解】
(1)石英玻璃的成分是二氧化硅,化学式为:SiO;故答案为SiO;
2 2
(2)合成树脂是高分子化合物,制备合成树脂的反应类型是聚合反应,故答案为聚合反应;
(3)①天宫二号使用的光伏太阳能电池的核心材料是半导体硅,天宫二号使用的光伏太阳能
电池是将太阳能转化为电能,故答案为Si;太阳能转化为电能;
②负极发生氧化反应,化合价升高,所以电极反应式为:VO2++H O-e-=VO++2H+夜间时,
2 2
电池正极VO +得电子发生还原反应,所以正极为b,故答案为VO2++H O-e-=VO++2H+;
2 2 2
b;
(4)a.太阳能、风能都是新能源,属于清洁能源,不污染环境,故a正确;b.由能量转化
图可知太阳能电池组实现了太阳能到电能的转化,故b正确;c.由图示可知控制系统与储
能系统可实现充、放电的转化,故c正确;d.阳光或风力充足时,储能系统实现由太阳能、
风能到电能的转化,故d错误;故答案为abc;
(5)①沉淀1含有氢氧化铁,设计反应为Fe2++2OH-=Fe(OH) ↓、
2
4Fe(OH) +2H O+O=4Fe(OH) ,因氢氧化铝为两性氢氧化物,可与氢氧化钠溶液反应,所
2 2 2 3
得滤液1中,铝元素的存在形式为AlO-,故答案为Fe2++2OH-=Fe(OH) ↓; 4Fe(OH
2 2
)+2H O+O=4Fe(OH) ;AlO-;
2 2 2 3 2
②过氧化氢具有强氧化性,由表中数据可知,向碱性的滤液1( V的化合价为+4 )中加入
HO 时发生了2VO(OH) -+H O+4OH-=2VO3-+6H O,故答案为2VO(OH) -+H O+4OH-
2 2 3 2 2 4 2 3 2 2
=2VO3-+6H O。
4 2
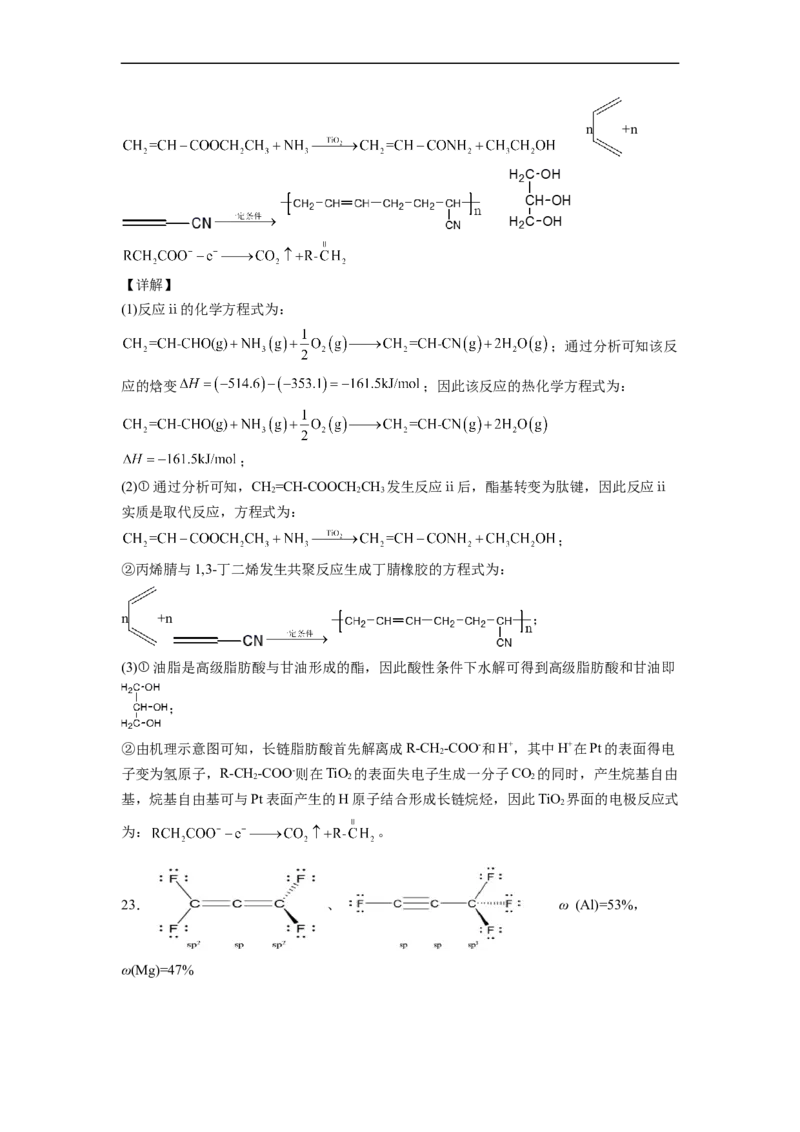
22.n +n
【详解】
(1)反应ⅱ的化学方程式为:
;通过分析可知该反
应的焓变 ;因此该反应的热化学方程式为:
;
(2)①通过分析可知,CH=CH-COOCH CH 发生反应ⅱ后,酯基转变为肽键,因此反应ⅱ
2 2 3
实质是取代反应,方程式为:
;
②丙烯腈与1,3-丁二烯发生共聚反应生成丁腈橡胶的方程式为:
n +n ;
(3)①油脂是高级脂肪酸与甘油形成的酯,因此酸性条件下水解可得到高级脂肪酸和甘油即
;
②由机理示意图可知,长链脂肪酸首先解离成R-CH-COO-和H+,其中H+在Pt的表面得电
2
子变为氢原子,R-CH-COO-则在TiO 的表面失电子生成一分子CO 的同时,产生烷基自由
2 2 2
基,烷基自由基可与Pt表面产生的H原子结合形成长链烷烃,因此TiO 界面的电极反应式
2
为: 。
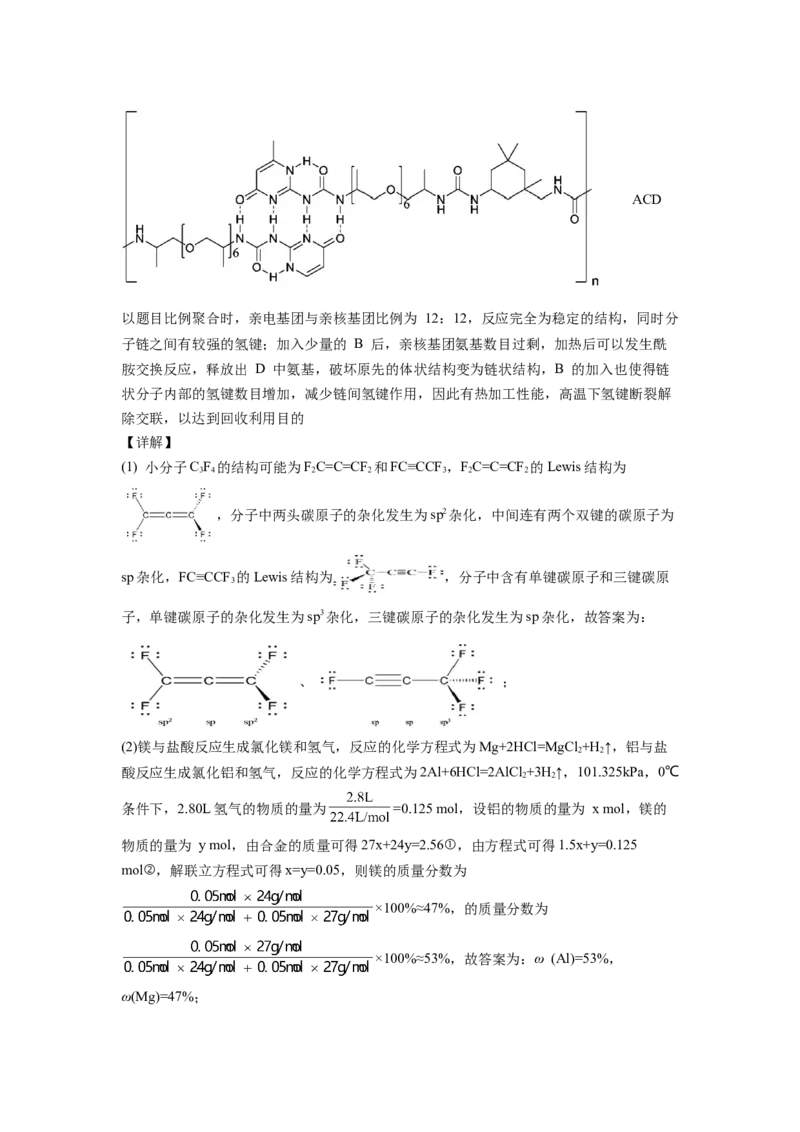
23. 、 ω (Al)=53%,
ω(Mg)=47%ACD
以题目比例聚合时,亲电基团与亲核基团比例为 12:12,反应完全为稳定的结构,同时分
子链之间有较强的氢键;加入少量的 B 后,亲核基团氨基数目过剩,加热后可以发生酰
胺交换反应,释放出 D 中氨基,破坏原先的体状结构变为链状结构,B 的加入也使得链
状分子内部的氢键数目增加,减少链间氢键作用,因此有热加工性能,高温下氢键断裂解
除交联,以达到回收利用目的
【详解】
(1) 小分子C F 的结构可能为FC=C=CF 和FC≡CCF ,FC=C=CF 的Lewis结构为
3 4 2 2 3 2 2
,分子中两头碳原子的杂化发生为sp2杂化,中间连有两个双键的碳原子为
sp杂化,FC≡CCF 的Lewis结构为 ,分子中含有单键碳原子和三键碳原
3
子,单键碳原子的杂化发生为sp3杂化,三键碳原子的杂化发生为sp杂化,故答案为:
、 ;
(2)镁与盐酸反应生成氯化镁和氢气,反应的化学方程式为Mg+2HCl=MgCl +H ↑,铝与盐
2 2
酸反应生成氯化铝和氢气,反应的化学方程式为2Al+6HCl=2AlCl +3H ↑,101.325kPa,0℃
2 2
条件下,2.80L氢气的物质的量为 =0.125 mol,设铝的物质的量为 x mol,镁的
物质的量为 y mol,由合金的质量可得27x+24y=2.56①,由方程式可得1.5x+y=0.125
mol②,解联立方程式可得x=y=0.05,则镁的质量分数为
×100%≈47%,的质量分数为
×100%≈53%,故答案为:ω (Al)=53%,
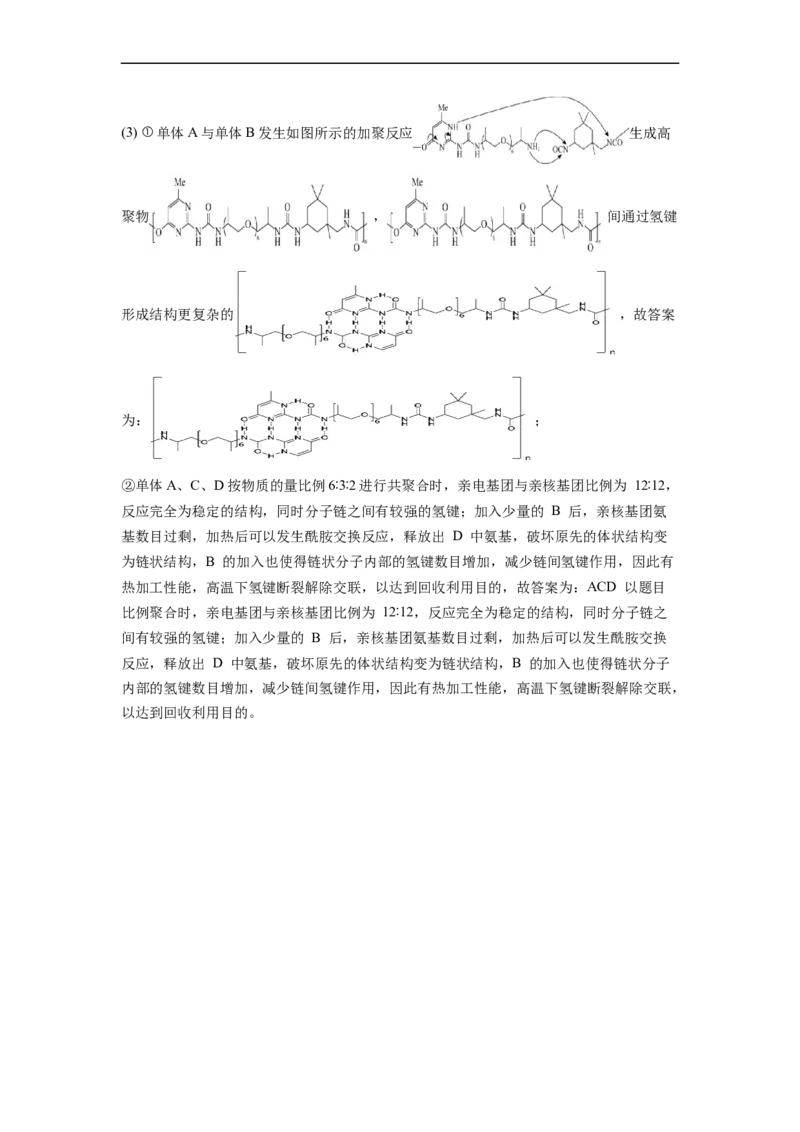
ω(Mg)=47%;(3) ①单体A与单体B发生如图所示的加聚反应 生成高
聚物 , 间通过氢键
形成结构更复杂的 ,故答案
为: ;
②单体A、C、D按物质的量比例6∶3∶2进行共聚合时,亲电基团与亲核基团比例为 12∶12,
反应完全为稳定的结构,同时分子链之间有较强的氢键;加入少量的 B 后,亲核基团氨
基数目过剩,加热后可以发生酰胺交换反应,释放出 D 中氨基,破坏原先的体状结构变
为链状结构,B 的加入也使得链状分子内部的氢键数目增加,减少链间氢键作用,因此有
热加工性能,高温下氢键断裂解除交联,以达到回收利用目的,故答案为:ACD 以题目
比例聚合时,亲电基团与亲核基团比例为 12∶12,反应完全为稳定的结构,同时分子链之
间有较强的氢键;加入少量的 B 后,亲核基团氨基数目过剩,加热后可以发生酰胺交换
反应,释放出 D 中氨基,破坏原先的体状结构变为链状结构,B 的加入也使得链状分子
内部的氢键数目增加,减少链间氢键作用,因此有热加工性能,高温下氢键断裂解除交联,
以达到回收利用目的。