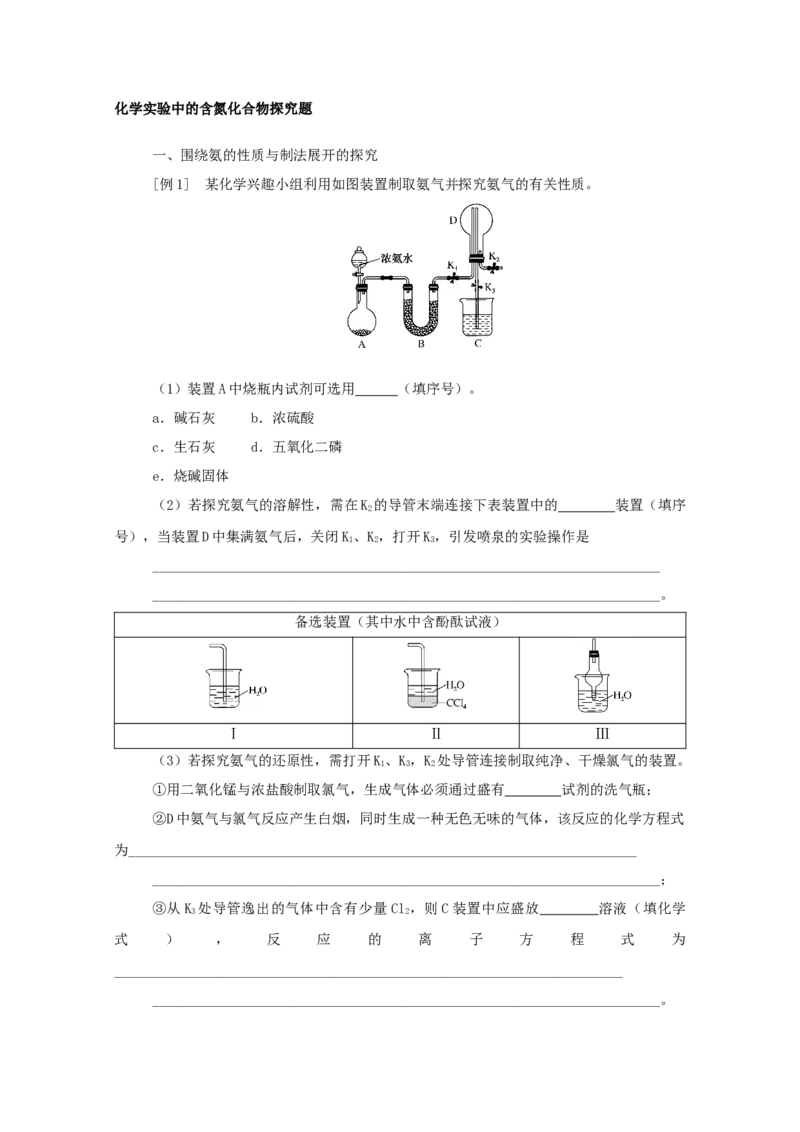
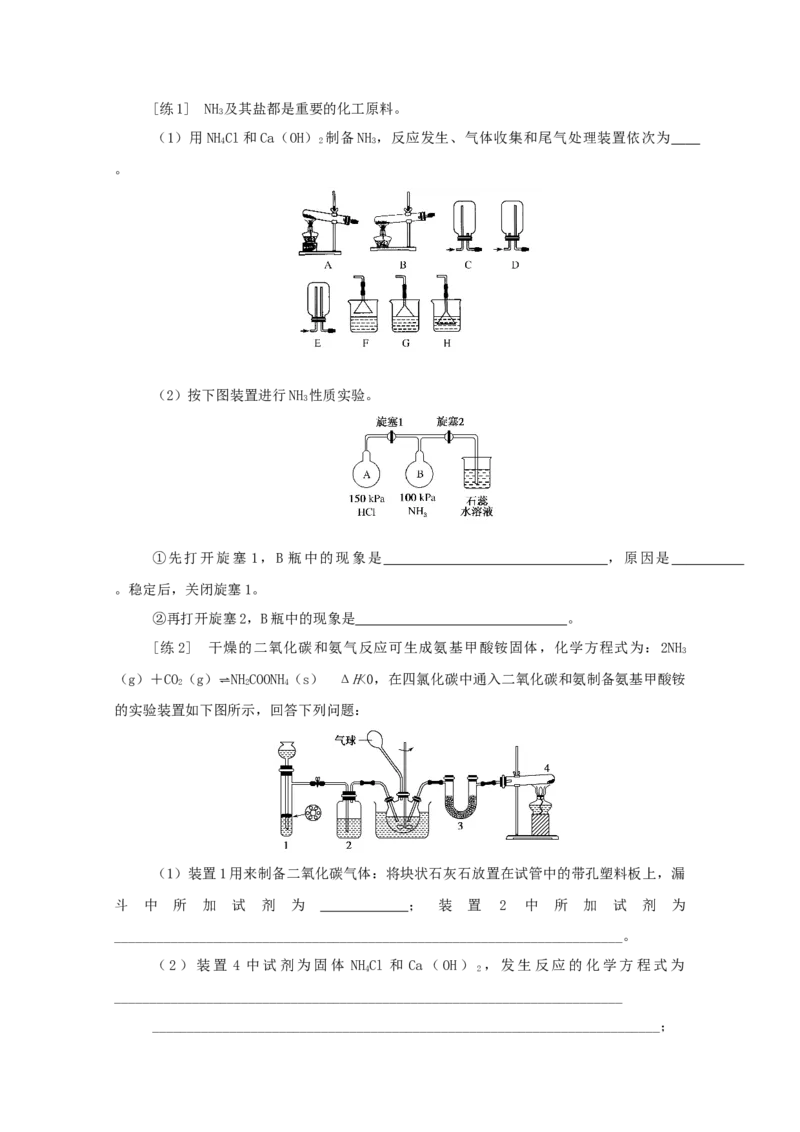
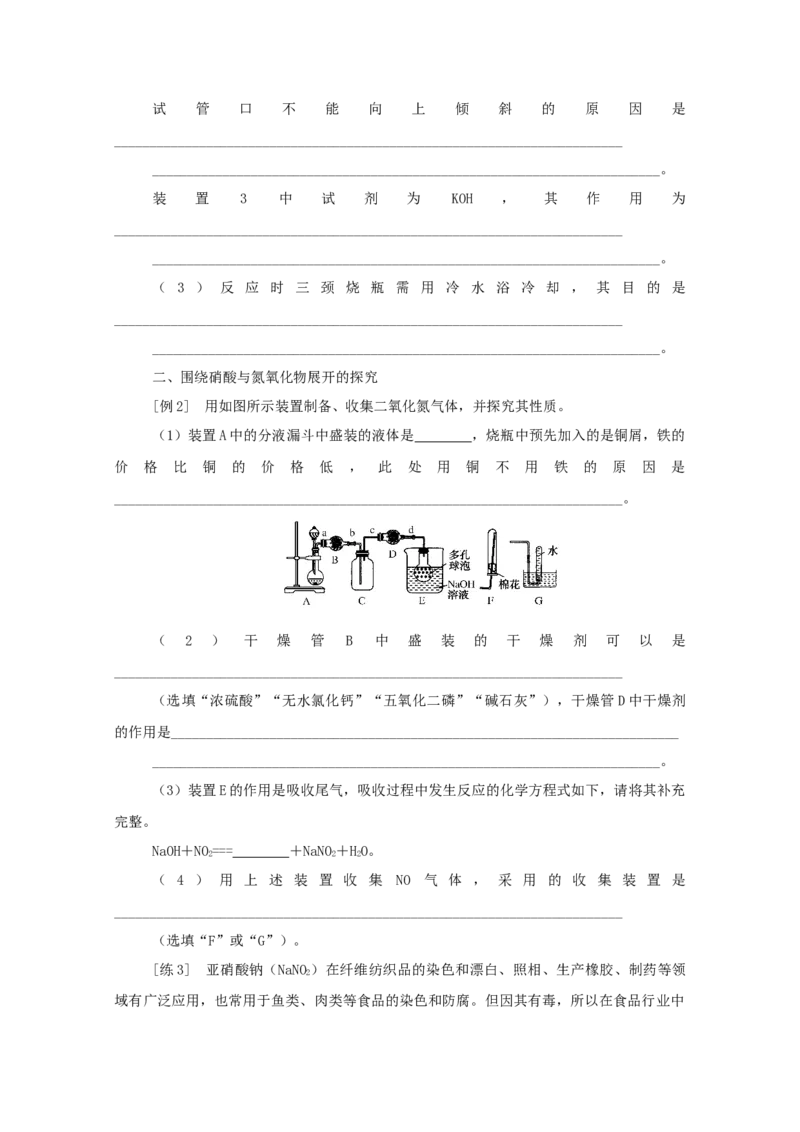
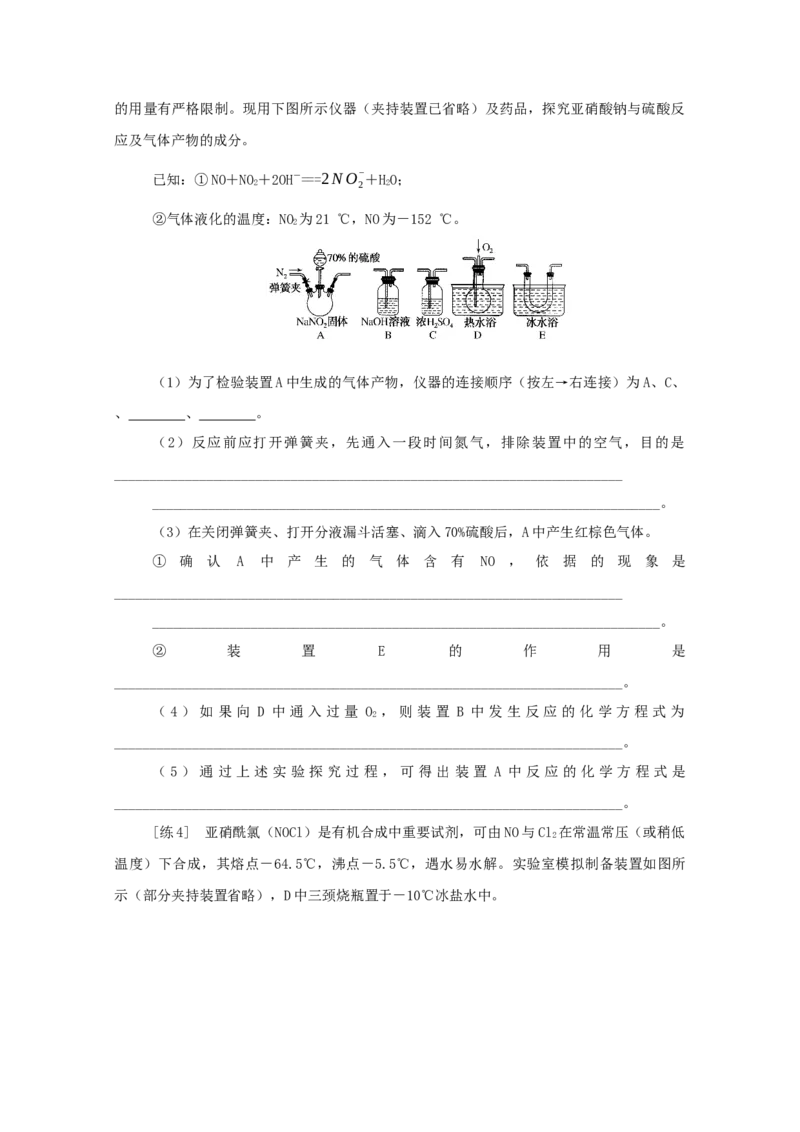
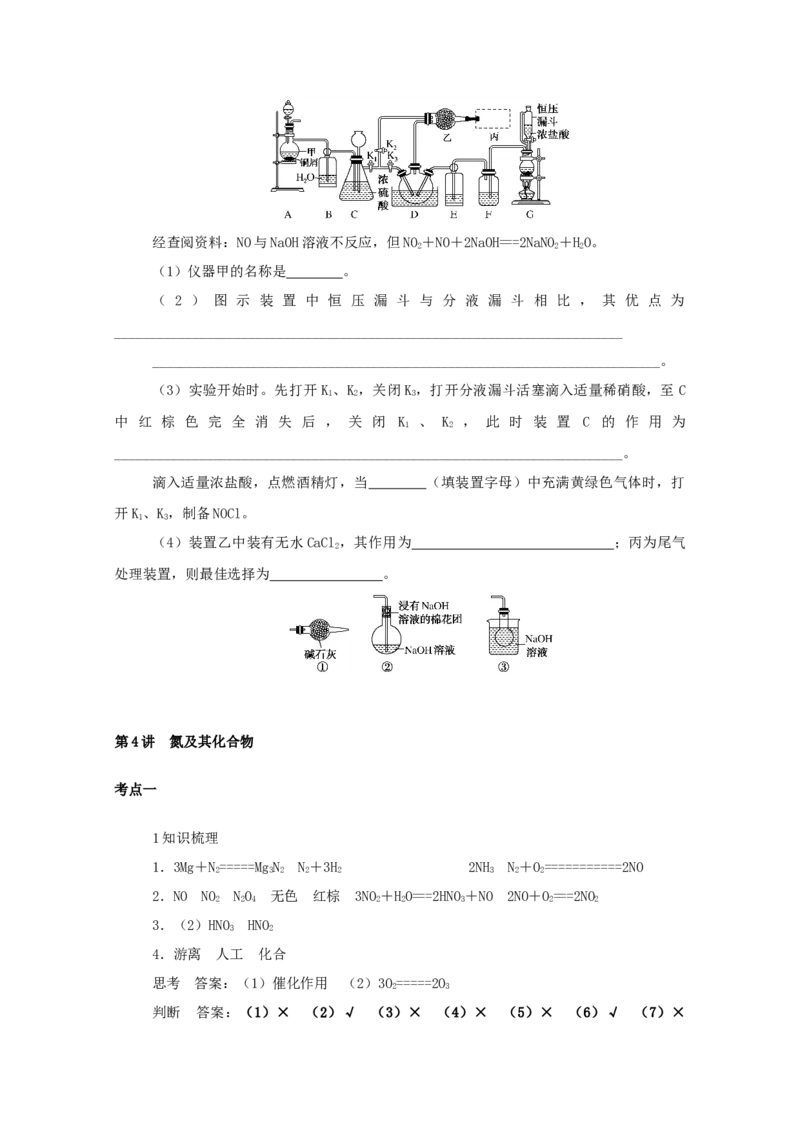
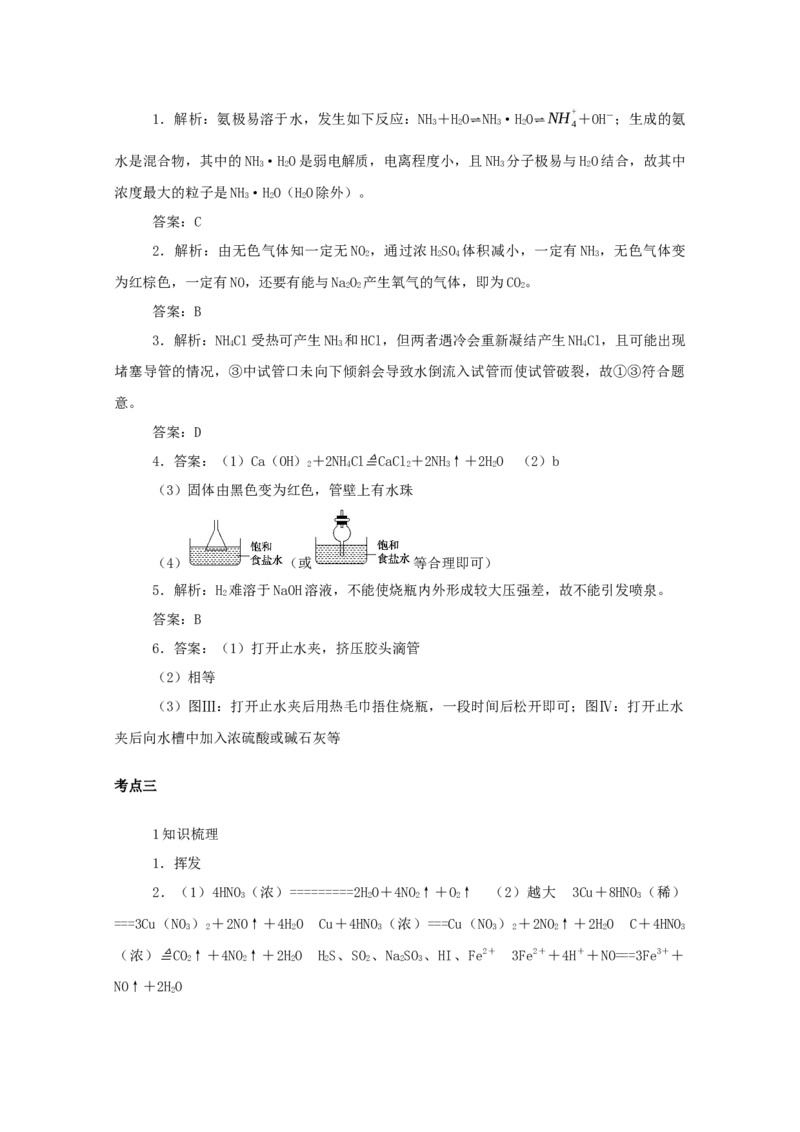
文档内容
第4讲 氮及其化合物
[考纲要求]
1.掌握氮元素单质及其重要化合物的主要性质和应用。2.掌握氮元素重要化合物对环
境质量的影响。3.了解氮元素单质及其重要化合物的制备方法。
考点一 氮气和氮的氧化物
1 知识梳理
1.氮气的性质
写出有关化学方程式:
①________________________________________________________________________
;
②________________________________________________________________________
;
③________________________________________________________________________
。
2.氮的氧化物
氮有多种价态的氧化物,如NO、 、 、 、NO、NO 等。
2 2 3 2 5
NO与NO 性质的比较
2
性质 NO NO
2
颜色状
气体 色有刺激性气味的气体
态气味
溶解性 难溶于水 与水反应
毒性 有毒(跟血红蛋白结合) 有毒
与水
不反应
反应
与氧气
不反应
反应3.氮氧化物对环境的污染
(1)光化学烟雾:NO 在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生
x
了一种有毒的烟雾。
(2)酸雨:NO 排入大气中后,与水反应生成 和 ,随雨雪降到地面。
x
(3)破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加。
2
(4)NO与血红蛋白结合使人中毒。
4.氮的固定
[思考]
汽车排放的尾气中含有NO ,NO 是城市大气污染的主要污染物之一。在日光照射下,
2 2
NO 发生一系列光化学烟雾的循环反应,从而不断产生 O ,加重空气污染。反应过程为
2 3
①2NO===2NO+2O,②2NO+O===2NO,③O+O===O。
2 2 2 2 3
问 题 : ( 1 ) NO 在 反 应 过 程 中 的 作 用
2
________________________________________________________________________。
( 2 ) 生 成 O 的 总 反 应 方 程 式 为
3
________________________________________________________________________。
[判断] (正确的打“√”,错误的打“×”)
(1)通过灼热的镁粉,可除N 中的少量氧气( )
2
(2)工业上利用合成氨实现人工固氮涉及氧化还原反应( )
(3)在实验室里,NO和NO 均用排水法收集( )
2
(4)NO 溶于水时,NO 是氧化剂,水是还原剂( )
2 2
(5)可用NO 与水反应制取硝酸,故NO 是酸性氧化物( )
2 2
(6)NO
与水反应的离子方程式:3NO+HO===2H++2NO−
+NO( )
2 2 2 3
(7)密闭容器中2 mol NO与1 mol O 充分反应,产物的分子数为2N( )
2 A
(8)标准状况下,6.72 L NO 与水充分反应转移的电子数目为0.1N( )
2 A
(9)NO能与人体里血红蛋白结合,造成人体缺氧中毒( )
[提醒]1.NO只能用排水法收集,不能用排空气法收集;而NO 只能用向上排空气法收集,不
2
能用排水法收集。
2.NO 虽然与水反应生成HNO ,但不是硝酸的酸酐。硝酸的酸酐是NO ;NO 不是酸性
2 3 2 5 2
氧化物。
3.NO 能使湿润的淀粉—碘化钾试纸变蓝,原因是二氧化氮先与水反应生成 HNO,HNO
2 3 3
再将碘化钾氧化为I,最终淀粉遇I 变蓝。
2 2
2 对点速练
练点一 氮的氧化物的性质
1.下列有关氮气的说法正确的是( )
A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼
B.1 mol N 可与3 mol H 完全反应生成2 mol NH
2 2 3
C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是 N +
2
2O===2NO
2 2
D.NO、NO 在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物
2
2.Murad 等三位教授提出 NO 在人体内有独特的功能,关于 NO 的叙述正确的是
( )
①NO可以是某些含低价氮物质氧化的产物 ②NO是亚硝酸的酸酐 ③NO可以是某些
含高价氮物质还原的产物
④NO是无色气体,在空气中可变为红棕色
A.全部 B.①③④
C.②③④ D.①④
3.将充有m mL NO和n mL NO 的量筒倒立于水槽中,然后通入m mL O ,若m