文档内容
第 43 讲 无机化工流程题的解题策略
复习目标 1.培养从试题提供的新信息中准确地提取实质性内容,并与已有知识块整合重
组为新知识块的能力。2.培养将实际问题分解,通过运用相关知识,采用分析、综合的方法,
解决简单化学问题的能力。3.培养将分析和解决问题的过程及成果用正确的化学术语及文字、
图表、模型、图形等表达并做出解释的能力。
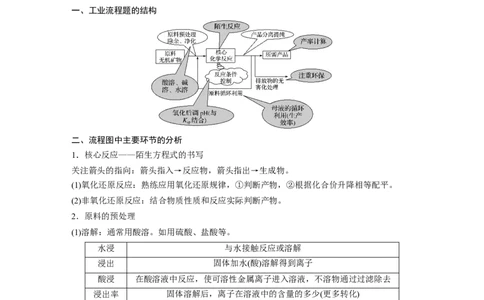
一、工业流程题的结构
二、流程图中主要环节的分析
1.核心反应——陌生方程式的书写
关注箭头的指向:箭头指入→反应物,箭头指出→生成物。
(1)氧化还原反应:熟练应用氧化还原规律,①判断产物,②根据化合价升降相等配平。
(2)非氧化还原反应:结合物质性质和反应实际判断产物。
2.原料的预处理
(1)溶解:通常用酸溶。如用硫酸、盐酸等。
水浸 与水接触反应或溶解
浸出 固体加水(酸)溶解得到离子
酸浸 在酸溶液中反应,使可溶性金属离子进入溶液,不溶物通过过滤除去
浸出率 固体溶解后,离子在溶液中的含量的多少(更多转化)
(2)灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解。
(3)审题时要“瞻前顾后”,注意物质性质及反应原理的前后联系。
3.常用的控制反应条件的方法
(1)调节溶液的pH。常用于使某些金属离子形成氢氧化物沉淀。调节 pH所需的物质一般应
满足两点:
①能与H+反应,使溶液pH增大;
②不引入新杂质。例如:若要除去Cu2+中混有的Fe3+,可加入CuO、CuCO 、Cu(OH) 、Cu (OH) CO 等物质
3 2 2 2 3
来调节溶液的pH,不可加入NaOH溶液、氨水等。
(2)控制温度。根据需要升温或降温,改变反应速率或使平衡向需要的方向移动。
(3)趁热过滤。防止某物质降温时会析出。
(4)冰水洗涤。洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
4.常用的提纯方法
(1)水溶法:除去可溶性杂质。
(2)酸溶法:除去碱性杂质。
(3)碱溶法:除去酸性杂质。
(4)氧化剂或还原剂法:除去还原性或氧化性杂质。
(5)加热灼烧法:除去受热易分解或易挥发的杂质。
(6)调节溶液的pH法:如除去酸性溶液中的Fe3+等。
5.常用的分离方法
(1)过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
(2)萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用 CCl 或苯
4
萃取溴水中的溴。
(3)蒸发结晶:提取溶解度随温度变化不大的溶质,如从溶液中提取NaCl。
(4)冷却结晶:提取溶解度随温度变化较大的溶质、易水解的溶质或结晶水合物,如KNO 、
3
FeCl 、CuCl 、CuSO ·5H O、FeSO ·7H O等。
3 2 4 2 4 2
(5)蒸馏或分馏:分离沸点不同且互溶的液体混合物,如分离乙醇和甘油。
(6)冷却法:利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中
的氨气。
1.(2019·全国卷Ⅲ,26)高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然
二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如图所示。回答
下列问题:
相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9(1)“滤渣1”含有S和________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式:
__________________________________________________________________________。
(2)“氧化”中添加适量的MnO 的作用是_____________________________________。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为________~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是_______________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原
2
因是____________________________________________________________________________。
(6)写出“沉锰”的离子方程式:___________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为 LiNiCoMnO ,其中Ni、
x y z 2
Co、Mn的化合价分别为+2、+3、+4。当x=y=时,z=________。
答案 (1)SiO(或不溶性硅酸盐) MnO +MnS+2HSO ===2MnSO +S+2HO (2)将Fe2+
2 2 2 4 4 2
氧化为Fe3+ (3)4.7 (4)NiS和ZnS (5)F-与H+结合形成弱电解质HF,MgF (s)Mg2+
2
(aq)+2F-(aq)平衡向右移动 (6)Mn2++2HCO===MnCO ↓+CO↑+HO (7)
3 2 2
解析 (1)硫化锰矿中硅元素主要以SiO 或不溶性硅酸盐形式存在,则“滤渣1”的主要成
2
分为S和SiO(或不溶性硅酸盐)。结合“滤渣1”中含S,可知“溶浸”时MnO 与MnS在
2 2
酸性条件下发生氧化还原反应生成 MnSO 和S,根据化合价升降法可配平该反应的化学方
4
程式。(2)“溶浸”后溶液中含Fe2+,“氧化”中加入的适量MnO 能将Fe2+氧化为Fe3+。
2
(3)“调pH”除去Fe3+和Al3+时,结合表格中数据信息可知需控制溶液的pH在4.7~6之间。
(4)“除杂1”中加入NaS能将Zn2+和Ni2+分别转化为沉淀除去,故“滤渣3”的主要成分
2
为NiS和ZnS。(5)“除杂2”中F-与Mg2+反应生成MgF 沉淀,若溶液酸度过高,则F-与
2
H+结合生成弱电解质HF,导致MgF (s)Mg2+(aq)+2F-(aq)平衡向右移动,Mg2+不能完
2
全除去。(6)“沉锰”时Mn2+与HCO反应生成MnCO 并放出CO ,由此可写出离子方程式。
3 2
(7)化合物LiNiCoMnO 中,当x=y=时,根据化合物中正负化合价代数和为0知1+2×+
x y z 2
3×+4z-2×2=0,解得z=。
2.(2020·济宁模拟)钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广
泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc O)的一种流程如图:
2 3
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定
比例混合而成。混合的实验操作是__________________________________________。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是____________;再向滤液中加入氨水调
节pH=6,滤液中Sc3+的浓度为__________。(已知:25 ℃时,K [Mn (OH) ]=1.9×10-
sp 2
13,K [Fe(OH) ]=2.6×10-39,K [Sc(OH) ]=9.0×10-31)
sp 3 sp 3(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中 =________________(保留两位有效数字)。
写出“沉钪”得到草酸钪的离子方程式:______________________________。[已知:25 ℃
时,K (H C O)=5.9×10-2,K (H C O)=6.4×10-5]
a1 2 2 4 a2 2 2 4
(4)草酸钪“灼烧”氧化的化学方程式为____________________________________________。
(5)废酸中含钪量为15 mg·L-1,V L废酸最多可提取Sc O 的质量为________________。
2 3
答案 (1)将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入双
氧水中,并不断搅拌
(2)Fe(OH) 9.0×10-7mol·L-1
3
(3)3.8×10-2 2Sc3++3HC O===Sc (C O)↓+6H+
2 2 4 2 2 4 3
(4)2Sc (C O)+3O=====2Sc O+12CO
2 2 4 3 2 2 3 2
(5)0.023V g
解析 (1)在混合不同的液体时,一般先加密度较小、易挥发的,后加密度大、难挥发的,
若混合时放热,则最后加受热易分解的,因此混合的实验操作是将浓硫酸沿烧杯内壁慢慢注
入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入双氧水中,并不断搅拌。(3)25 ℃时pH
=2的草酸溶液中=××=K (H C O)×
a2 2 2 4
K (H C O)×=6.4×10-5×5.9×10-2×≈3.8×10-2。“沉钪”得到草酸钪的离子方程式为
a1 2 2 4
2Sc3++3HC O===Sc (C O)↓+6H+。(4)草酸钪“灼烧”氧化的化学方程式为2Sc (C O)
2 2 4 2 2 4 3 2 2 4 3
+3O=====2Sc O +12CO 。(5)废酸中含钪量为15 mg·L-1,则V L废酸中含钪的质量为
2 2 3 2
15×10-3 g·L-1×V L=0.015V g,所以最多可提取Sc O 的质量为=0.023V g。
2 3
3.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革
工业污泥Cr(Ⅲ)的处理工艺流程如图:
已知硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有__________、__________。(答出两点)
(2)H O 的作用是将滤液Ⅰ中的Cr3+转化为Cr O,则此反应中氧化剂和还原剂物质的量之比
2 2 2
为__________。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
阳离子 Fe3+ Al3+ Cr3+
开始沉淀时的pH 2.7 - -
沉淀完全时的pH 3.7 5.4(>8溶解) 9(>9溶解)
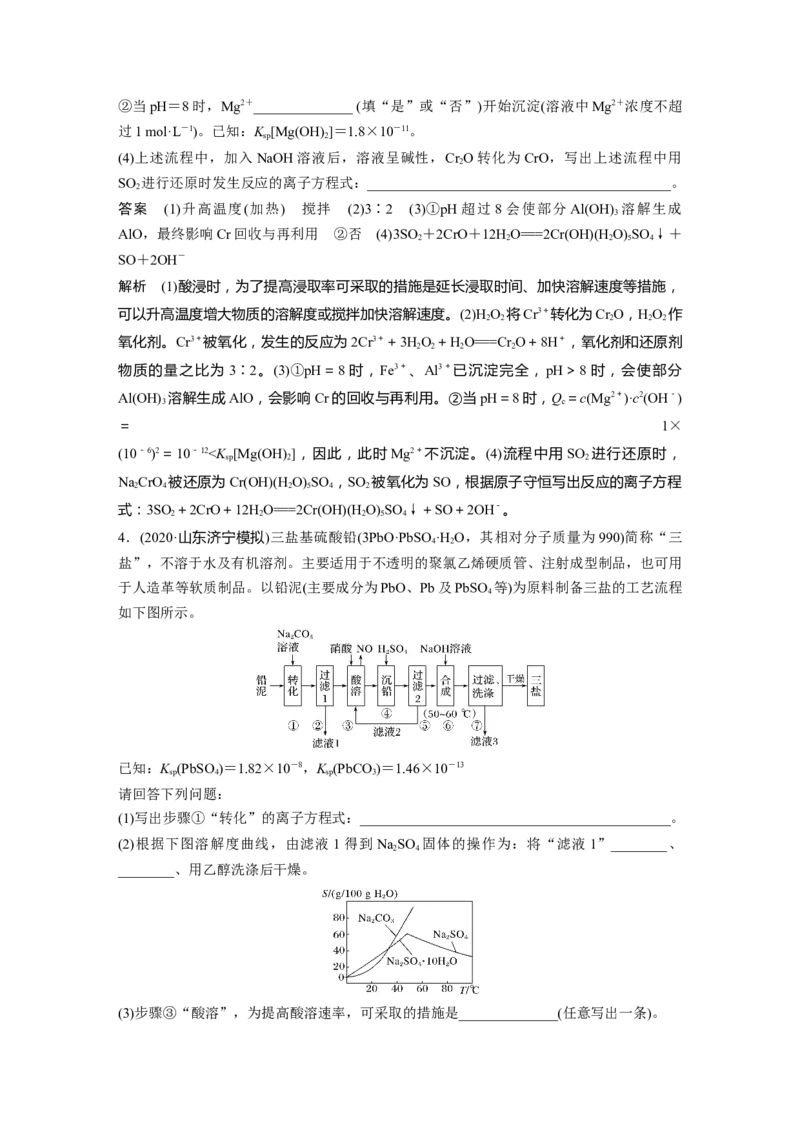
①用NaOH调节溶液的pH不能超过8,其理由是_____________________________________。②当pH=8时,Mg2+______________ (填“是”或“否”)开始沉淀(溶液中Mg2+浓度不超
过1 mol·L-1)。已知:K [Mg(OH) ]=1.8×10-11。
sp 2
(4)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr O转化为CrO,写出上述流程中用
2
SO 进行还原时发生反应的离子方程式:___________________________________________。
2
答案 (1)升高温度(加热) 搅拌 (2)3∶2 (3)①pH 超过 8 会使部分 Al(OH) 溶解生成
3
AlO,最终影响Cr回收与再利用 ②否 (4)3SO +2CrO+12HO===2Cr(OH)(HO) SO ↓+
2 2 2 5 4
SO+2OH-
解析 (1)酸浸时,为了提高浸取率可采取的措施是延长浸取时间、加快溶解速度等措施,
可以升高温度增大物质的溶解度或搅拌加快溶解速度。(2)H O 将Cr3+转化为Cr O,HO 作
2 2 2 2 2
氧化剂。Cr3+被氧化,发生的反应为2Cr3++3HO +HO===Cr O+8H+,氧化剂和还原剂
2 2 2 2
物质的量之比为 3∶2。(3)①pH=8 时,Fe3+、Al3+已沉淀完全,pH>8 时,会使部分
Al(OH) 溶解生成AlO,会影响Cr的回收与再利用。②当pH=8时,Q=c(Mg2+)·c2(OH-)
3 c
= 1×
(10-6)2=10-12K (PbCO )=1.46×10-13,所以步骤①加入碳酸钠溶
sp 4 sp 3
液,把硫酸铅转化为碳酸铅,反应的离子方程式为 PbSO (s)+CO(aq)PbCO (s)+
4 3
SO(aq)。
(2)滤液1的溶质主要是NaSO 和过量的NaCO ,将“滤液1”升温结晶、趁热过滤、用乙
2 4 2 3
醇洗涤后干燥得到NaSO 固体。
2 4
(4)Pb、PbO和PbCO 在硝酸的作用下转化成Pb(NO ),Pb(NO ) 中加硫酸转化成PbSO 和硝
3 3 2 3 2 4
酸,HNO 可循环利用;根据K (PbSO )=1.82×10-8,若滤液中c(Pb2+)=1.82×10-5mol·L-
3 sp 4
1,则溶液中的c(SO)== mol·L-1=1×10-3mol·L-1。
(6)设铅泥中铅元素的质量分数为x,根据铅元素守恒可得:=×4,解得x=0.552 0,所以铅
泥中铅元素的质量分数为55.20%。
5.(2020·东北三省四市联合模拟)碱式碳酸铜在烟火、农药、颜料、杀菌剂等方面应用广泛。
一种以辉铜矿(Cu S,含有SiO 和少量Fe O 等杂质)为原料制备碱式碳酸铜的流程如图所示:
2 2 2 3
已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 Fe2+ Fe3+ Cu2+ Mn2+
开始沉淀的pH 7.5 2.7 5.6 8.3
完全沉淀的pH 9.0 3.7 6.7 9.8
②[Cu(NH )]SO 常温稳定,在热水中会分解生成NH ;
3 4 4 3
③K [Fe(OH) ]=4.0×10-38。
sp 3
回答下列问题:
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有____________(任写一种)。(2)滤渣Ⅰ经 CS 提取后可获得一种淡黄色副产品,则滤渣Ⅰ中的主要成分是
2
____________(填化学式)。回收淡黄色副产品过程中温度控制在50~60 ℃之间,不宜过高
或 过 低 的 原 因 是
________________________________________________________________________。
(3)常温下“除铁”时加入的试剂A可用CuO,调节pH的范围为__________,若加A后将
溶液的pH调为5,则溶液中Fe3+的浓度为__________________mol·L-1。
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式:_______________________________。
(5)“赶氨”时,最适宜的操作方法是___________________________________________。
(6)测定副产品MnSO ·H O样品的纯度:准确称取样品14.00 g,加蒸馏水配成100 mL溶液,
4 2
取出25.00 mL用标准的BaCl 溶液测定,完全反应后得到了4.66 g沉淀,则此样品的纯度为
2
________(保留到小数点后两位)。
答案 (1)搅拌(或适当增加硫酸浓度、适当加热等)
(2)SiO 、S、MnO 温度过低,硫的溶解速率小,温度过高,CS 易挥发 (3)3.7~5.6(或
2 2 2
3.7≤pH<5.6) 4.0×10-11 (4)Mn2++HCO+NH ===MnCO ↓+NH (5)将溶液加热
3 3
(6)96.57%
解析 辉铜矿主要成分为Cu S,含少量Fe O 、SiO 等杂质,加入稀硫酸和二氧化锰浸取,
2 2 3 2
Cu S在酸性条件下被二氧化锰氧化,SiO 不溶于稀硫酸,滤渣Ⅰ经CS 提取后可获得一种淡
2 2 2
黄色副产品,说明滤渣Ⅰ中含有S,过滤得到的滤渣中含有MnO 、SiO、单质S,滤液中含
2 2
有Fe3+、Mn2+、Cu2+,加入A,调节溶液的pH使铁离子形成氢氧化铁沉淀,除去铁;加入
碳酸氢铵溶液沉淀锰,过滤得到碳酸锰,用硫酸溶解,生成硫酸锰晶体,滤液赶出氨气,参
与循环使用,同时得到碱式碳酸铜,据此分析解答。
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可以适当增加硫酸的浓度,充分搅拌,加热
等。(2)滤渣Ⅰ的主要成分是MnO 、SiO 、单质S;回收淡黄色副产品(S)的过程中温度控制
2 2
在50~60 ℃之间,不宜过高或过低,原因是温度过低,硫的溶解速率小,温度过高,CS
2
易挥发。(3)加入的试剂A是用于调节溶液的pH,促进铁离子的水解,但不能引入杂质,因
最后要制备碱式碳酸铜,则可加入氧化铜、氢氧化铜等;根据有关金属离子形成氢氧化物沉
淀的pH范围,“除铁”时溶液pH应该介于3.7~5.6( 或3.7≤pH<5.6),若加A后将溶液
的pH调为5,则c(OH-)=10-9mol·L-1,K [Fe(OH) ]=4.0×10-38,则溶液中铁离子浓度为
sp 3
mol·L-1=4.0×10-11 mol·L-1。(4)“沉锰”(除Mn2+)过程中,加入碳酸氢铵和氨气,生成碳
酸锰沉淀,反应的离子方程式为Mn2++HCO+NH ===MnCO ↓+NH。(5)氨气易挥发,
3 3
“赶氨”时,最适宜的操作方法是将溶液加热。(6)反应得到的沉淀硫酸钡的物质的量为=
0.02 mol,n(MnSO ·H O)=n(BaSO)=0.02 mol,则此样品中MnSO ·H O物质的量为0.02
4 2 4 4 2
mol×=0.08 mol,则样品中MnSO ·H O的纯度为×100%≈96.57%。
4 2
化学工艺流程题的分析方法主线分析“原料→中间转化物质→目标产物”
(1)反应与物质的转化:分析每一步操作的目的及所发生的化学反应,跟踪物质转化的形式。
尤其要注意原料中的杂质在流程中是如何被除去的。滤渣、滤液成分的确定:反应过程中哪
些物质(离子)发生了变化?产生了哪些新离子?这些离子间是否能发生化学反应?所加试剂
是否过量?
(2)循环物质的确定
(3)副产品的判断
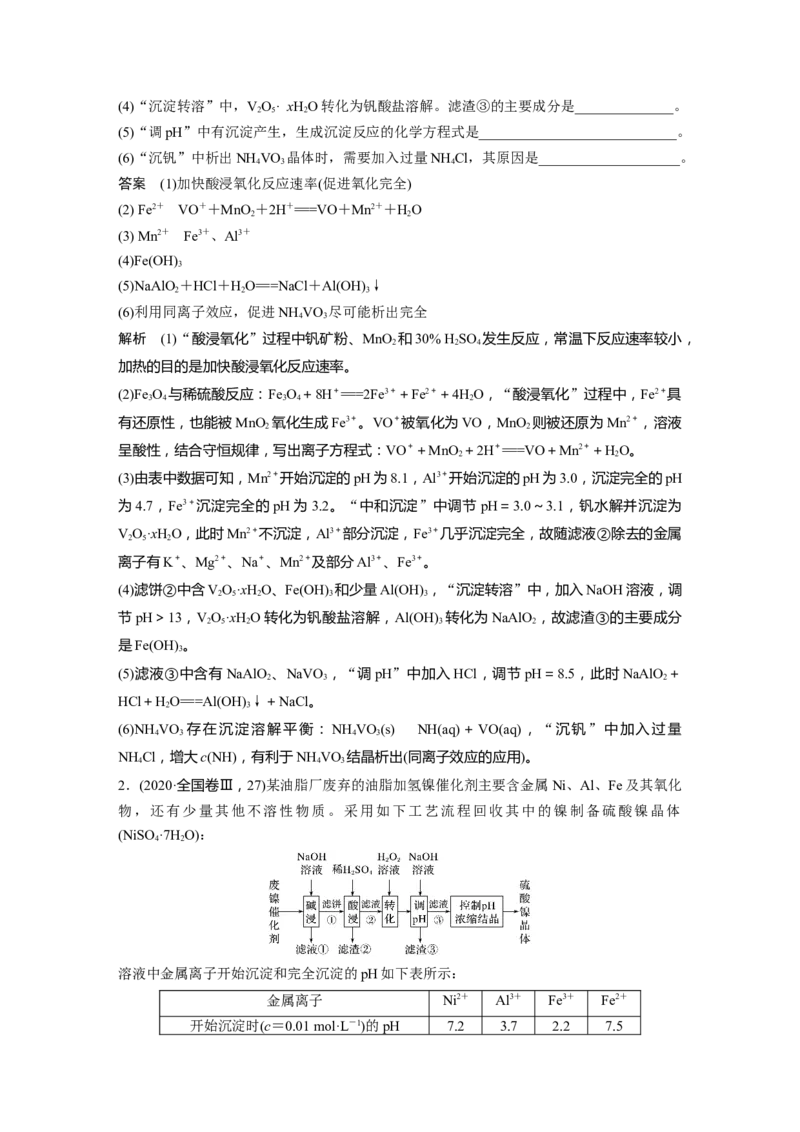
1.(2020·全国卷Ⅰ,26)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存
在,还包括钾、镁的铝硅酸盐,以及SiO 、Fe O 。采用以下工艺流程可由黏土钒矿制备
2 3 4
NH VO 。
4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是______________________________________________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________离子被氧化。写出VO+
转化为VO反应的离子方程式____________________________________________________。
(3)“中和沉淀”中,钒水解并沉淀为VO· xHO,随滤液②可除去金属离子K+、Mg2+、
2 5 2
Na+、________,以及部分的________。(4)“沉淀转溶”中,VO· xHO转化为钒酸盐溶解。滤渣③的主要成分是______________。
2 5 2
(5)“调pH”中有沉淀产生,生成沉淀反应的化学方程式是____________________________。
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是____________________。
4 3 4
答案 (1)加快酸浸氧化反应速率(促进氧化完全)
(2) Fe2+ VO++MnO +2H+===VO+Mn2++HO
2 2
(3) Mn2+ Fe3+、Al3+
(4)Fe(OH)
3
(5)NaAlO +HCl+HO===NaCl+Al(OH) ↓
2 2 3
(6)利用同离子效应,促进NH VO 尽可能析出完全
4 3
解析 (1)“酸浸氧化”过程中钒矿粉、MnO 和30% H SO 发生反应,常温下反应速率较小,
2 2 4
加热的目的是加快酸浸氧化反应速率。
(2)Fe O 与稀硫酸反应:Fe O +8H+===2Fe3++Fe2++4HO,“酸浸氧化”过程中,Fe2+具
3 4 3 4 2
有还原性,也能被MnO 氧化生成Fe3+。VO+被氧化为VO,MnO 则被还原为Mn2+,溶液
2 2
呈酸性,结合守恒规律,写出离子方程式:VO++MnO +2H+===VO+Mn2++HO。
2 2
(3)由表中数据可知,Mn2+开始沉淀的pH为8.1,Al3+开始沉淀的pH为3.0,沉淀完全的pH
为4.7,Fe3+沉淀完全的pH为3.2。“中和沉淀”中调节pH=3.0~3.1,钒水解并沉淀为
VO·xHO,此时Mn2+不沉淀,Al3+部分沉淀,Fe3+几乎沉淀完全,故随滤液②除去的金属
2 5 2
离子有K+、Mg2+、Na+、Mn2+及部分Al3+、Fe3+。
(4)滤饼②中含VO·xHO、Fe(OH) 和少量Al(OH) ,“沉淀转溶”中,加入NaOH溶液,调
2 5 2 3 3
节pH>13,VO·xHO转化为钒酸盐溶解,Al(OH) 转化为NaAlO ,故滤渣③的主要成分
2 5 2 3 2
是Fe(OH) 。
3
(5)滤液③中含有NaAlO 、NaVO ,“调pH”中加入HCl,调节pH=8.5,此时NaAlO +
2 3 2
HCl+HO===Al(OH) ↓+NaCl。
2 3
(6)NH VO 存在沉淀溶解平衡:NH VO (s)NH(aq)+VO(aq),“沉钒”中加入过量
4 3 4 3
NH Cl,增大c(NH),有利于NH VO 结晶析出(同离子效应的应用)。
4 4 3
2.(2020·全国卷Ⅲ,27)某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化
物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L-1)的pH 7.2 3.7 2.2 7.5沉淀完全时(c=1.0×10-5 mol·L-1)的pH 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是____________________________。为回收金属,用
稀 硫 酸 将 “ 滤 液 ① ” 调 为 中 性 , 生 成 沉 淀 。 写 出 该 反 应 的 离 子 方 程 式
_____________________。
(2)“滤液②”中含有的金属离子是________________。
(3)“转化”中可替代HO 的物质是________________。若工艺流程改为先“调pH”后“转
2 2
化”,即 ,“滤液③”中可能含有的杂质离子为_______。
(4)利用上述表格数据,计算Ni(OH) 的K =__________________________ (列出计算式)。
2 sp
如果“转化”后的溶液中 Ni2+浓度为 1.0 mol·L-1,则“调 pH”应控制的 pH 范围是
________。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出
该反应的离子方程式_____________________________________________________________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________________________。
答案 (1)除去油脂,溶解铝及其氧化物 AlO+H++HO===Al(OH) ↓
2 3
(2)Ni2+、Fe2+、Fe3+
(3)O 或空气 Fe3+
2
(4)0.01×(107.2-14)2[或10-5×(108.7-14)2] 3.2~6.2
(5)2Ni2++ClO-+4OH-===2NiOOH↓+ Cl-+HO
2
(6)提高镍的回收率
解析 (1)因为废镍催化剂表面沾有油脂,所以“碱浸”的目的是除去油脂,同时还可以溶
解催化剂中混有的铝及氧化铝杂质。滤液①中存在的金属元素有铝元素和钠元素,铝元素以
AlO 的形式存在,当加酸调到中性时,发生反应的离子方程式为 AlO+H++
HO===Al(OH) ↓。
2 3
(2)滤饼①加稀硫酸酸浸,产生的滤液中的金属离子有Ni2+、Fe2+、Fe3+。
(3)过程中加入HO 的目的是氧化Fe2+,由于Fe2+的还原性强,能与氧气反应,因此也可以
2 2
用氧气或空气代替HO 。如果过程中先“调pH”后“转化”,结合金属离子沉淀的有关
2 2
pH数据可知,当调节pH小于7.2时,Fe2+不能形成沉淀,加入HO 后Fe2+被氧化为Fe3+,
2 2
因此滤液③中可能混有Fe3+。
(4)根据溶度积的表达式得 K [Ni(OH)]=c(Ni2+)·c2(OH-)=0.01×(107.2-14)2[或10-5×(108.7-
sp 2
14)2] 。 当 溶 液 中 c(Ni2 + ) = 1.0 mol·L - 1 时 , c(OH - ) = = mol·L - 1 =10-7.8 mol·L-1,c(H+)== mol·L-1=10-6.2 mol·L-1,pH=-lg c(H+)=-lg 10-6.2
=6.2。所以当pH=6.2时,Ni2+开始产生沉淀,根据流程图可知,调pH的目的是让Fe3+沉
淀完全,所以应控制pH的范围为3.2~6.2。
(6)分离出硫酸镍晶体后的母液中仍有Ni2+,采用循环使用的意义是提高镍的回收率。
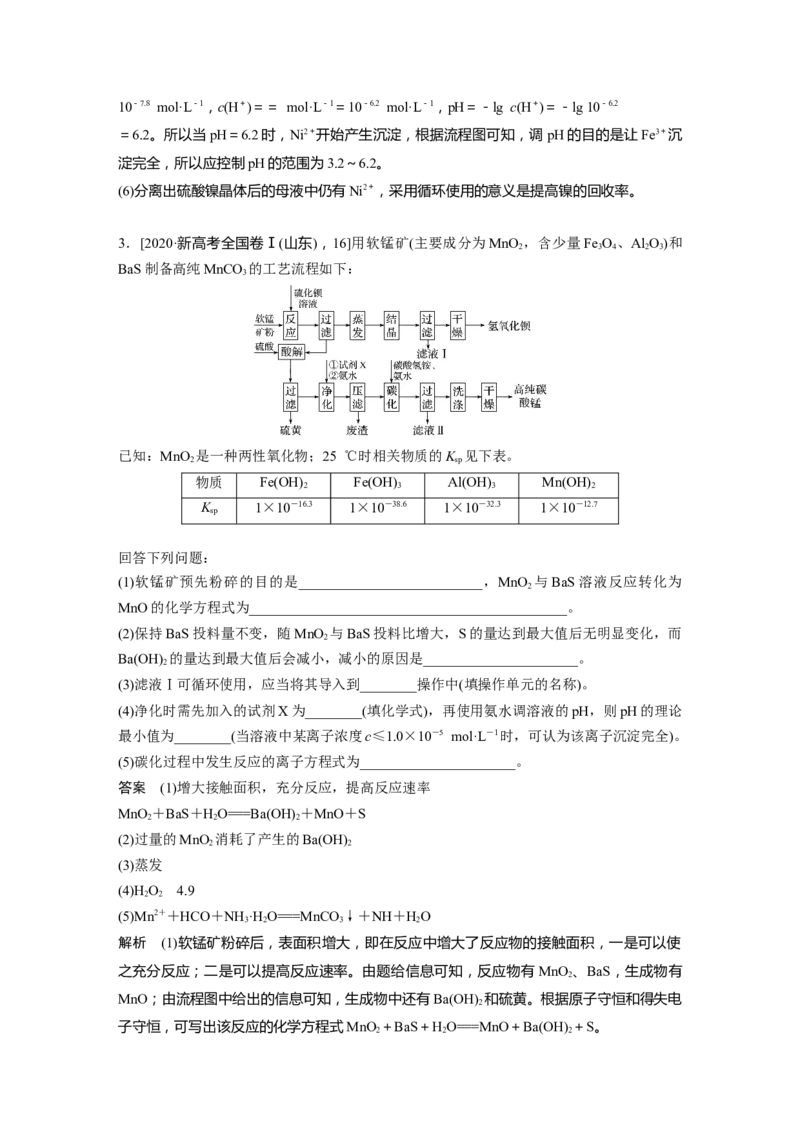
3.[2020·新高考全国卷Ⅰ(山东),16]用软锰矿(主要成分为MnO ,含少量Fe O 、Al O)和
2 3 4 2 3
BaS制备高纯MnCO 的工艺流程如下:
3
已知:MnO 是一种两性氧化物;25 ℃时相关物质的K 见下表。
2 sp
物质 Fe(OH) Fe(OH) Al(OH) Mn(OH)
2 3 3 2
K 1×10-16.3 1×10-38.6 1×10-32.3 1×10-12.7
sp
回答下列问题:
(1)软锰矿预先粉碎的目的是__________________________,MnO 与BaS溶液反应转化为
2
MnO的化学方程式为_____________________________________________。
(2)保持BaS投料量不变,随MnO 与BaS投料比增大,S的量达到最大值后无明显变化,而
2
Ba(OH) 的量达到最大值后会减小,减小的原因是______________________。
2
(3)滤液Ⅰ可循环使用,应当将其导入到________操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为________(填化学式),再使用氨水调溶液的pH,则pH的理论
最小值为________(当溶液中某离子浓度c≤1.0×10-5 mol·L-1时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为______________________。
答案 (1)增大接触面积,充分反应,提高反应速率
MnO +BaS+HO===Ba(OH) +MnO+S
2 2 2
(2)过量的MnO 消耗了产生的Ba(OH)
2 2
(3)蒸发
(4)H O 4.9
2 2
(5)Mn2++HCO+NH ·H O===MnCO ↓+NH+HO
3 2 3 2
解析 (1)软锰矿粉碎后,表面积增大,即在反应中增大了反应物的接触面积,一是可以使
之充分反应;二是可以提高反应速率。由题给信息可知,反应物有MnO 、BaS,生成物有
2
MnO;由流程图中给出的信息可知,生成物中还有Ba(OH) 和硫黄。根据原子守恒和得失电
2
子守恒,可写出该反应的化学方程式MnO +BaS+HO===MnO+Ba(OH) +S。
2 2 2(2)增大MnO 与BaS的投料比,S的量达到最大值后不再变化,说明过量的MnO 与S不反
2 2
应;Ba(OH) 的量达到最大值后会减小,说明过量的 MnO 与Ba(OH) 发生了反应,消耗了
2 2 2
产生的Ba(OH) 。
2
(3)滤液Ⅰ中还含有未结晶的Ba(OH) ,可循环使用,应将其导入蒸发操作中。
2
(4)软锰矿中含有的Fe O 、Al O 杂质与硫酸反应生成FeSO 、Fe (SO ) 、Al (SO ) ,要除去
3 4 2 3 4 2 4 3 2 4 3
Fe2+,应先将Fe2+氧化为Fe3+,为了不引入其他杂质,加入的氧化剂 X可选用HO 。因
2 2
Fe(OH) 和Al(OH) 的组成相似,且Fe(OH) 的K 小于Al(OH) 的,因此当Al3+完全沉淀时,
3 3 3 sp 3
Fe3+也完全沉淀,由K [Al(OH) ]=1×10-32.3可知,c(Al3+)·c3(OH-)=1×10-32.3,由题意知,
sp 3
当 c(Al3 + )
≤1.0×10-5 mol·L-1时沉淀完全,可求得 c(OH-)≥1×10-9.1 mol·L-1,即 c(H+)≤1×
10-4.9 mol·L-1,pH的理论最小值为4.9。
(5)由流程图提供的信息可知,碳化时的反应物有碳酸氢铵、氨水、Mn2+,生成物有
MnCO ,由此可写出该反应的离子方程式为 Mn2++HCO+NH ·H O===MnCO ↓+NH+
3 3 2 3
HO。
2
1.软锰矿的主要成分为MnO ,还含有Fe O 、MgO、Al O 、CaO、SiO 等杂质,工业上用
2 2 3 2 3 2
软锰矿制取MnSO ·H O的流程如下:
4 2
已知:①部分金属阳离子完全沉淀时的pH如下表
金属阳离子 Fe3+ Al3+ Mn2+ Mg2+
完全沉淀时的pH 3.2 5.2 10.4 12.4
②温度高于27 ℃时,MnSO 晶体的溶解度随温度的升高而逐渐降低。
4
(1)“浸出”过程中MnO 转化为Mn2+的离子方程式为_____________________________。
2
(2)第1步除杂中加入HO 的目的是_____________________________________________。
2 2
(3)第1步除杂中形成滤渣1的主要成分为__________(填化学式),调pH至5~6所加的试剂,
可选择________(填字母)。
a.CaO b.MgO c.Al O d.氨水
2 3
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF 除去Mg2+的
2
离子方程式:___________________________________________________________________,
该反应的平衡常数为________。(已知:MnF 的K =5.3×10-3;CaF 的K =1.5×10-10;MgF 的K =7.4×10-11)
2 sp 2 sp 2 sp
(5)采用“趁热过滤”操作的原因是_______________________________________________。
(6)取少量 MnSO ·H O 溶于水,配成溶液,测其 pH 发现该溶液显酸性,原因是
4 2
_______________
____________________________________________________________(用离子方程式表示)。
答案 (1)MnO +SO ===SO+Mn2+
2 2
(2)将Fe2+氧化为Fe3+
(3)Al(OH) 、Fe(OH) ab
3 3
(4)MnF +Mg2+Mn2++MgF 7.2×107
2 2
(5)减少MnSO ·H O在水中的溶解,得到更多产品
4 2
(6)Mn2++2HOMn(OH) +2H+
2 2
解析 (1)“浸出”过程中MnO 与SO 发生氧化还原反应,离子方程式为MnO +SO ===SO
2 2 2 2
+Mn2+。
(2)第1步除杂中加入 HO 的目的是将溶液中可能存在的 Fe2+氧化为Fe3+,以便于形成
2 2
Fe(OH) 沉淀,过滤将沉淀除去。
3
(3)第1步除杂时调整溶液的pH至5~6,可以使溶液中的Al3+、Fe3+分别形成Al(OH) 、
3
Fe(OH) 沉淀,所以形成滤渣1的主要成分为Al(OH) 、Fe(OH) ;在调pH至5~6时,为了
3 3 3
不引入新的杂质离子,所加的试剂应该可以与酸发生反应,可选择含有Ca2+、Mg2+的化合
物CaO、MgO,a、b正确。
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应的氟化物沉淀除去,MnF 除去Mg2+的离
2
子方程式是MnF +Mg2+Mn2++MgF ;该反应的平衡常数K===≈7.2×107。
2 2
(5)由已知②温度高于27 ℃时,MnSO 晶体的溶解度随温度的升高而逐渐降低,故采用“趁
4
热过滤”操作可以减少MnSO ·H O在水中的溶解,得到更多产品。
4 2
(6)MnSO 是强酸弱碱盐,Mn2+发生水解反应。
4
2.(2020·汕头市高三模拟)溴酸镉[Cd(BrO )]常用作分析试剂、生产荧光粉等。以镉铁矿(成
3 2
分为 CdO、Fe O、FeO 及少量的Al O 和SiO)为原料制备[Cd(BrO )]的工艺流程如下:
2 2 3 2 3 2 3 2
已知 Cd(SO ) 溶于水,回答下列问题:
4 2
(1)为提高镉的浸取率,酸浸时可采取的措施有____________________(任写两种即可)。(2)还原镉时,产生能使澄清石灰水变浑浊的气体,发生反应的离子方程式为
______________
______________________________________________________________________________。
(3)加入HO 溶液的目的是______________________________________________________。
2 2
(4)滤渣2 的主要成分为__________________(填化学式);为检验滤液中是否含有 Fe3+,可
选用的化学试剂是_______________________________________________________________。
(5)实际工业生产中,有时还采用阳离子交换树脂法来测定沉镉后溶液中 Cd2+的含量,其原
理:Cd2++ 2NaR===2Na++ CdR ,其中NaR为阳离子交换树脂。常温下,将沉镉后的
2
溶液(此时溶液 pH=6)经过阳离子交换树脂后,测得溶液中的 Na+比交换前增加了 0.055 2
g·L-1,则该条件下Cd(OH) 的K 值为______________。
2 sp
(6)已知镉铁矿中CdO 的含量为72%,整个流程中镉元素的损耗率为10%,则2 t该镉铁矿
2
可制得Cd(BrO)(摩尔质量为 368 g·mol-1)质量为____________kg。
3 2
答案 (1)增大稀硫酸浓度、将固体粉碎、用玻璃棒搅拌或适当加热等措施(写出两种即可)
(2)3Cd4++CHOH+HO===3Cd2++CO↑+6H+ (3)将溶液中的Fe2+氧化为Fe3+
3 2 2
(4)Al(OH) 、Fe(OH) KSCN溶液 (5)1.2×10-19
3 3
(6)3 312
解析 用稀硫酸溶解镉铁矿,其中SiO 不溶于水和酸,通过过滤除去,即滤渣1为SiO ;
2 2
滤液中主要含有Fe2+、Fe3+、Al3+和Cd4+,加入CHOH将Cd4+还原为Cd2+,然后加入
3
HO 溶液,将溶液中的Fe2+氧化为Fe3+,再调节溶液pH使溶液中的Al3+和Fe3+完全转化为
2 2
Al(OH) 、Fe(OH) 沉淀,过滤除去不溶物(滤渣2),向含有CdSO 的滤液中加入KCO 生成
3 3 4 2 3
CdCO 沉淀,再过滤将沉淀溶于HBrO ,最后将溶液蒸发结晶即可得到溴酸镉,据此分析。
3 3
(1)固体溶解于稀硫酸时,采取增大稀硫酸浓度、将固体粉碎、用玻璃棒搅拌或适当加热等
措施,可提高镉的浸出率。(2)CH OH将Cd4+还原为Cd2+时,产生使澄清石灰水变浑浊的气
3
体,此气体为CO ,结合守恒法,可知反应的离子方程式为 3Cd4++CHOH+HO===3Cd2+
2 3 2
+CO↑+6H+。(3)加入HO 溶液的目的是将溶液中的Fe2+氧化为Fe3+。(4)滤渣2的主要
2 2 2
成分为Al(OH) 、Fe(OH) ;为检验滤液中是否含有 Fe3+,可选用的化学试剂是KSCN溶液。
3 3
(5)沉淀后的溶液pH=6,则c(OH-)=10-8mol·L-1,经阳离子交换树脂后,测得溶液中Na+
比交换前增加了0.055 2 g·L-1,即Na+物质的量浓度增加了=0.002 4 mol·L-1,根据Cd2++
2NaR===2Na++CdR ,可知原溶液中c(Cd2+)=0.001 2 mol·L-1,则Cd(OH) 的K =c(Cd2
2 2 sp
+)·c2(OH-)=1.2×10-19。(6)2 t该矿石中CdO 的质量为2×106 g×72%=1.44×106g,其物
2
质的量为=1×104 mol,整个流程中镉元素的损耗率为10%,根据原子守恒可知Cd(BrO)
3 2
的 物 质 的 量 为 104 mol×(1 - 10%) = 9×103mol , 其 质 量 为 9×
103 mol×368 g·mol-1=3 312 000 g=3 312 kg。
3.(2020·江西省重点中学盟校高三联考)高纯MnCO 在电子工业中有重要的应用,工业上利
3用软锰矿(主要成分是MnO ,还含有Fe O 、CaCO 、CuO等杂质)制取碳酸锰的流程如图所
2 2 3 3
示:
已知:还原焙烧主反应为2MnO +C=====2MnO+CO↑。
2 2
可能用到的数据如下:
氢氧化物 Fe(OH) Fe(OH) Cu(OH) Mn(OH)
3 2 2 2
开始沉淀pH 1.5 6.5 4.2 8.1
沉淀完全pH 3.7 9.7 7.4 10.1
根据要求回答下列问题:
(1)在实验室进行步骤A,混合物应放在_______________________中加热;步骤C中的滤渣
为____________。
(2)步骤D中氧化剂与还原剂的物质的量之比为____________。
(3)步骤E中调节pH的范围为___________________________________________,其目的是
_____________________________________________________________________________。
(4)步骤G,温度控制在35 ℃以下的原因是________________________,若Mn2+恰好沉淀
完 全 时 测 得 溶 液 中 CO 的 浓 度 为 2.2×10 - 6mol·L - 1 , 则 K (MnCO ) =
sp 3
____________________。
(5) 生 成 的 MnCO 沉 淀 需 经 充 分 洗 涤 , 检 验 洗 涤 是 否 干 净 的 方 法 是
3
_______________________。
(6)现用滴定法测定产品中锰元素的含量。实验步骤:称取3.300 g试样,向其中加入稍过量
的磷酸和硝酸,加热使产品中MnCO 完全转化为[Mn(PO )]3-(其中NO完全转化为NO);加
3 4 2
入稍过量的硫酸铵,发生反应NO+NH===N↑+2HO以除去NO;加入稀硫酸酸化,再加
2 2
入60.00 mL 0.500 mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO )]3-+Fe2+===Mn2++Fe3
4 2
++2PO;用5.00 mL 0.500 mol·L-1酸性KCr O 溶液恰好除去过量的Fe2+。
2 2 7
①酸性KCr O 溶液与Fe2+反应的离子方程式为_____________________________________。
2 2 7
②试样中锰元素的质量分数为____________________。
答案 (1)坩埚 C、Cu和CaSO (2)1∶2 (3)3.7≤pH<8.1 使Fe3+转化为Fe(OH) 而除去,
4 3
且不影响Mn2+ (4)减少碳酸氢铵的分解,提高原料利用率 2.2×10-11 (5)取少量最后一
次的洗涤液于试管中,向其中滴加用盐酸酸化的BaCl 溶液,若无白色沉淀产生,则表明已
2
洗涤干净 (6)①6Fe2++Cr O+14H+===6Fe3++2Cr3++7HO ②25%
2 2
解析 (1)高温焙烧物质应在坩埚中进行;根据分析可知滤渣为 C、Cu和CaSO 。(2)步骤D
4
中MnO 被还原成Mn2+,化合价降低2价,Fe2+被氧化成Fe3+,化合价升高1价,根据得失
2电子守恒,氧化剂与还原剂的物质的量之比为1∶2。(3)此时溶液中的杂质主要为Fe3+,结
合表中数据可知步骤E中调节pH的范围为3.7≤pH<8.1,其目的是使铁离子转化为氢氧化
铁而除去,而不影响Mn2+。(4)铵盐不稳定,受热易分解,所以步骤G中温度需控制在35
℃以下,减少碳酸氢铵的分解,提高原料利用率;Mn2+恰好沉淀完全时可认为c(Mn2+)=
10-5 mol·L-1,K (MnCO )=c(Mn2+)·c(CO)=10-5×2.2×10-6=2.2×10-11。(5)生成的
sp 3
MnCO 沉淀可能附着有硫酸盐,所以检验是否含有硫酸根即可确认沉淀是否洗涤干净,具
3
体操作:取少量最后一次的洗涤液于试管中,向其中滴加用盐酸酸化的BaCl 溶液,若无白
2
色沉淀产生,则表明已洗涤干净。(6)①酸性KCr O 具有强氧化性,可以把亚铁离子氧化成
2 2 7
铁离子,自身被还原成=Cr3+,根据电子守恒、电荷守恒和原子守恒可得离子方程式为6Fe2+
+Cr O+14H+===6Fe3++2Cr3++7HO。②根据方程式6Fe2++Cr O+14H+===6Fe3++2Cr3
2 2 2
++7HO可知反应的n(Fe2+)=0.500 mol·L-1×0.005 L×6=0.015 mol,则与[Mn(PO )]3-反
2 4 2
应的n(Fe2+)=0.500 mol·L-1×0.06 L-0.015 mol=0.015 mol,根据方程式[Mn(PO )]3-+Fe2
4 2
+===Mn2++Fe3++2PO可知n(Mn)=0.015 mol,所以锰元素的质量分数为×100%=25%。
4.(2020·咸阳市高三模拟)硼酸和硫酸镁是重要的化工原料。以硼铁混合精矿[主要成分为
MgBO (OH)、UO 和Fe O,还有少量的Fe O、FeO、SiO]为原料制备硼酸和硫酸镁的工艺
2 2 3 4 2 3 2
流程如下:
已知:①UO在pH为4~5的溶液中生成UO (OH) 沉淀;②Fe2+和Fe3+沉淀完全的pH分
2 2
别为9.7、3.7。
(1)酸浸过程中MgBO (OH)与硫酸反应的离子方程式为_______________________________。
2
(2)酸浸过程中加入HO 的目的是______________________________________(写出两条),
2 2
滤渣1的主要成分是________________(填化学式)。
(3)试剂1最好选择______________________(填化学式)。若调节溶液pH前,溶液中c(Mg2+)
=0.2 mol·L-1,当溶液 pH 调至 5 时,UO 沉淀完全,此时是否有 Mg(OH) 沉淀生成
2
______________。{通过计算说明,K [Mg(OH) ]=5.6×10-12}
sp 2
(4)操作1的名称是________________。
(5)MgSO ·H O 加 热 脱 水 可 以 得 无 水 MgSO , 那 么 MgCl ·6H O 晶 体 直 接 加 热
4 2 4 2 2
____________( 填 “ 能 ” 或 “ 不 能 ” ) 得 到 无 水 MgCl , 理 由 是
2
_________________________________。
(6)已知:HCO 的K =4.4×10-7,K =4.7×10-11;HBO 的K=5.8×10-10。向碳酸钠溶
2 3 a1 a2 3 3 a液里逐滴加入硼酸溶液__________(填“有”或“无”)气泡产生,理由是____________。
答案 (1)MgBO (OH)+2H+===Mg2++HBO
2 3 3
(2)将Fe2+氧化为Fe3+,将UO 氧化成UO,便于后续过程除去 SiO
2 2
(3)MgO[或Mg(OH) 或MgCO ] c(Mg2+)·c2(OH-)=0.2×(10-9)2=2×10-19<K [Mg (OH) ]=
2 3 sp 2
5.6×10-12,因此不会产生Mg (OH) 沉淀 (4)趁热过滤 (5)不能 加热时促进了MgCl 的
2 2
水解,最终得到氢氧化镁、氧化镁或碱式碳酸镁 (6)无 硼酸的酸性比碳酸弱
解析 用硫酸酸化的HO 溶解硼铁混合精矿,其中SiO 不溶于水和酸,经过滤可除去,所
2 2 2
得滤液中主要含有 UO、Fe3+、Mg2+及HBO ,用 MgO 或Mg(OH) 或MgCO 调节溶液
3 3 2 3
pH,使溶液中Fe3+完全转化为Fe(OH) 沉淀,UO转化为UO (OH) 沉淀,并经过滤得滤渣
3 2 2
2,将滤液蒸发、浓缩,趁热过滤,获得MgSO ·H O晶体,将滤液冷却结晶,过滤可得粗硼
4 2
酸,据此分析解题。
(1)酸浸过程中MgBO (OH)与硫酸反应,生成硼酸和硫酸镁,发生反应的离子方程式为
2
MgBO (OH)+2H+===Mg2++HBO 。(2)酸浸过程中加入HO ,利用HO 的氧化性,将Fe2
2 3 3 2 2 2 2
+氧化为Fe3+,同时将UO 氧化成UO便于后续过程除去;SiO 不溶于水和酸,则滤渣1的
2 2
主要成分是SiO 。(3)添加试剂1是调节溶液pH,则试剂1能与酸反应,且不引入新的杂质,
2
故最好选择MgO或Mg(OH) 或MgCO ;c(Mg2+)=0.2 mol·L-1,当溶液pH调至5时,c(OH
2 3
-)=1×10-9mol·L-1,则c(Mg2+)·c2(OH-)=0.2×(10-9)2=2×10-19<K [Mg (OH) ]=5.6×
sp 2
10-12,因此不会产生Mg (OH) 沉淀。(4)结合以上分析可知,将滤液蒸发、浓缩,趁热过滤,
2
获得MgSO ·H O晶体,所以操作1的名称是趁热过滤。(5)MgCl 能水解生成Mg (OH) 和
4 2 2 2
HCl,MgCl ·6H O晶体直接加热时,促进Mg2+水解,且HCl挥发,则最终得到氢氧化镁、
2 2
氧化镁或碱式碳酸镁,而不能得到无水MgCl 。
2
5.(2020·咸阳市高三模拟)氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:
已知:①菱锰矿石主要成分是MnCO ,还含有少量Fe、Al、Ca、Mg等元素;
3
②相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀时的pH如下:
金属离子 Al3+ Fe3+ Fe2+ Ca2+ Mn2+ Mg2+
开始沉淀的pH 3.8 1.5 6.5 10.6 8.1 9.6
沉淀完全的pH 5.2 3.7 9.7 12.6 10.1 11.6
③常温下,CaF 、MgF 的溶度积分别为1.46×10-10、7.42×10-11
2 2
回答下列问题:(1)“焙烧”时发生的主要反应的化学方程式为__________________________。
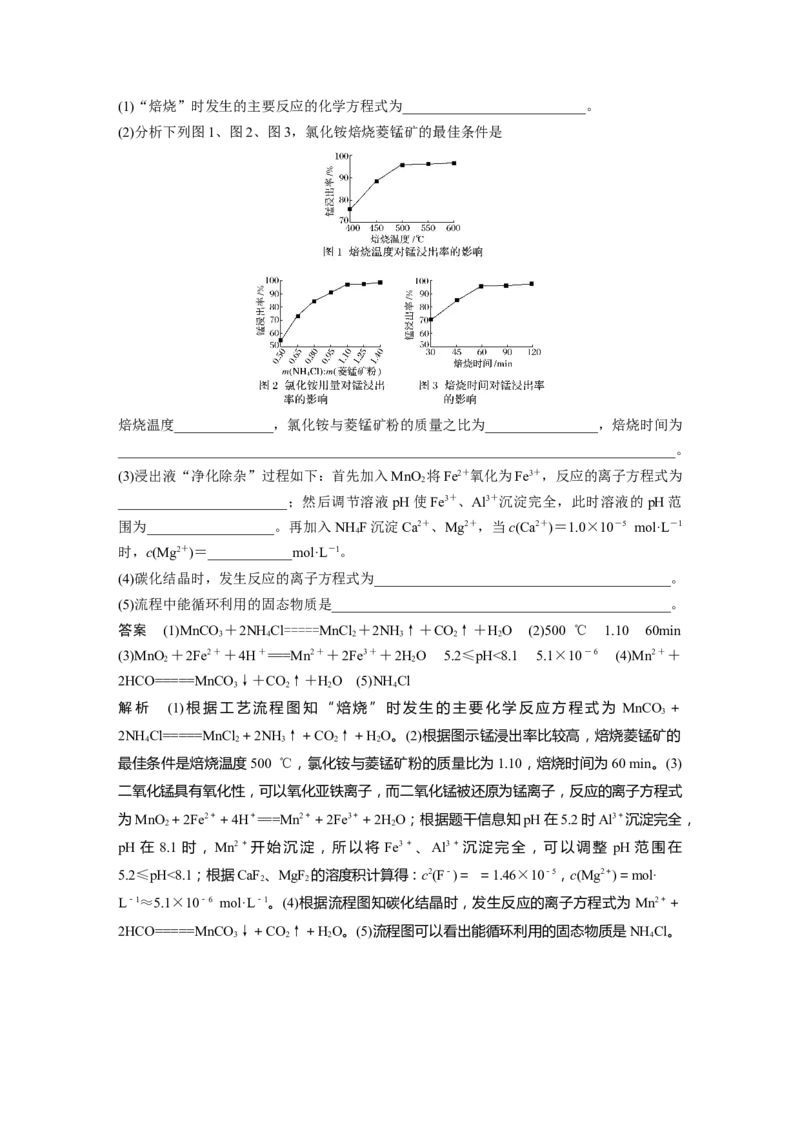
(2)分析下列图1、图2、图3,氯化铵焙烧菱锰矿的最佳条件是
焙烧温度______________,氯化铵与菱锰矿粉的质量之比为________________,焙烧时间为
_______________________________________________________________________________。
(3)浸出液“净化除杂”过程如下:首先加入MnO 将Fe2+氧化为Fe3+,反应的离子方程式为
2
________________________;然后调节溶液pH使Fe3+、Al3+沉淀完全,此时溶液的pH范
围为__________________。再加入NH F沉淀Ca2+、Mg2+,当c(Ca2+)=1.0×10-5 mol·L-1
4
时,c(Mg2+)=____________mol·L-1。
(4)碳化结晶时,发生反应的离子方程式为__________________________________________。
(5)流程中能循环利用的固态物质是________________________________________________。
答案 (1)MnCO +2NH Cl=====MnCl +2NH ↑+CO↑+HO (2)500 ℃ 1.10 60min
3 4 2 3 2 2
(3)MnO +2Fe2++4H+===Mn2++2Fe3++2HO 5.2≤pH<8.1 5.1×10-6 (4)Mn2++
2 2
2HCO=====MnCO ↓+CO↑+HO (5)NH Cl
3 2 2 4
解析 (1)根据工艺流程图知“焙烧”时发生的主要化学反应方程式为 MnCO +
3
2NH Cl=====MnCl +2NH ↑+CO↑+HO。(2)根据图示锰浸出率比较高,焙烧菱锰矿的
4 2 3 2 2
最佳条件是焙烧温度500 ℃,氯化铵与菱锰矿粉的质量比为1.10,焙烧时间为60 min。(3)
二氧化锰具有氧化性,可以氧化亚铁离子,而二氧化锰被还原为锰离子,反应的离子方程式
为MnO +2Fe2++4H+===Mn2++2Fe3++2HO;根据题干信息知pH在5.2时Al3+沉淀完全,
2 2
pH 在 8.1 时,Mn2+开始沉淀,所以将 Fe3+、Al3+沉淀完全,可以调整 pH 范围在
5.2≤pH<8.1;根据CaF 、MgF 的溶度积计算得:c2(F-)= =1.46×10-5,c(Mg2+)=mol·
2 2
L-1≈5.1×10-6 mol·L-1。(4)根据流程图知碳化结晶时,发生反应的离子方程式为 Mn2++
2HCO=====MnCO ↓+CO↑+HO。(5)流程图可以看出能循环利用的固态物质是NH Cl。
3 2 2 4