文档内容
2023届高三化学高考备考一轮专题训练:计算题
一、计算题
1.(2022·浙江温州·高三阶段练习)已知硫粉和 溶液反应可以生成多硫化钠( ),离子反应为:
、 ……,现有1.11mol/L 溶液100mL,往其中加入6.72g硫粉,控制一定条
件使硫粉恰好完全反应,反应后溶液的阴离子有 、 、 (忽略其他阴离子,假设溶液体积不变),
且物质的量之比为1:10:100,请计算:
(1)加入硫粉的物质的量:n(S)=_______mol。
(2)反应后: _______mol。
(3)反应后: _______mol。
2.(2022·广西·昭平中学高三阶段练习)将0.1mol镁和铝的混合物溶于100mL2mol·L-1硫酸中,然后滴
加1mol·L-1NaOH溶液。回答下列问题:
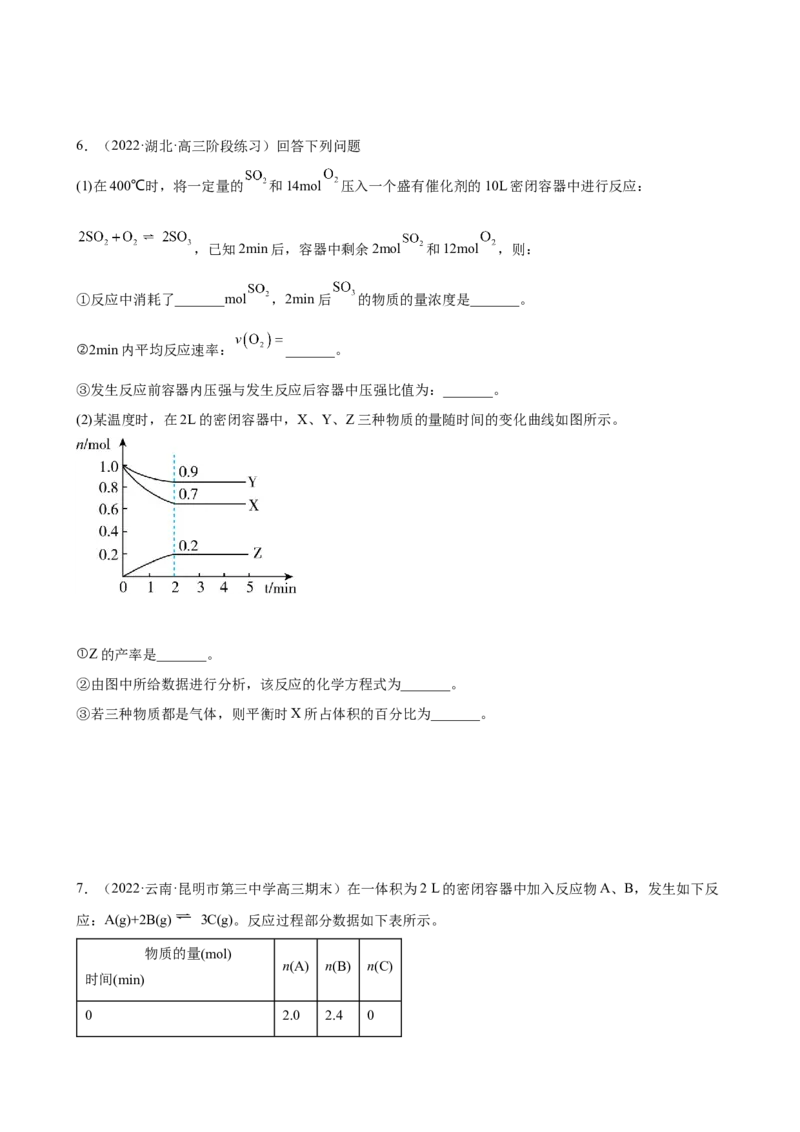
(1)若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示。
①有关反应的离子方程式为____。
②当V=160时,金属粉末中n(Mg)=____mol,V=___。
1 2
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为___。
(3)若混合物仍为0.1mol,其中镁粉的物质的量分数为a,用100mL2mol·L-1硫酸溶解此混合物后,再加入
450mL1mol·L-1NaOH溶液,所得沉淀中无Al(OH) ,写出满足此条件的a的取值范围:____。
33.(2022·江苏徐州·高三阶段练习)恒温恒容下,将2 mol红棕色气体A和1.5 mol无色气体B通入体积
为1 L的密闭容器中发生如下反应: ,2 min时反应达到平衡状态,此时剩余
1.1 mol B,并测得C的浓度为1.2 mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_______mol/(L·min)
(2)x=_______;A的转化率与B的转化率之比为_______
(3)写出该温度下的平衡常数表达式_______(用相关字母表示),数值_______
(4)向平衡后的容器中继续充入0.8 molA(g)、0.9 molB(g)、0.8 molC(g)、1.2mol D(s),此时,
v(正)_______v(逆)。(填“>”、“=”或“<”)
4.(2022·江西·赣州市赣县第三中学高三阶段练习)按要求作答:
(1)乙醇和乙酸反应可生成乙酸乙酯,反应方程式为:_______。在密闭容器中,利用该反应制备乙酸乙酯,
实验中若起始时在容器中加入3mol乙醇、1mol乙酸和一定量的浓硫酸,充分反应后容器中残留的乙醇可
能为_______。
A.2mol B.2.6mol C.2.8mol D.3mol
(2)向27.2 g Cu和Cu O的混合物中加入某浓度的稀HNO500 mL,反应过程中产生的气体只有NO。固体
2 3
完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1 L 1 mol·L-1的NaOH溶液使金属离子恰好完全沉
淀,此时溶液呈中性,所得沉淀质量为39.2 g。
①Cu与Cu O 的物质的量之比为_______。
2
②HNO 的物质的量浓度为_______mol·L-1。
3
5.(2022·广西河池·高三阶段练习)将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO
和 混合气体在标准状况下的体积为11.2L。请回答:
(1)被还原的硝酸的物质的量是_______;
(2)NO的体积为_______L, 的体积为_______L。
(3)产生的气体全部与氧气混合,将混合气体溶于水,若全部恰好溶解需要通入的氧气在标准状况下的体
积是_______。6.(2022·湖北·高三阶段练习)回答下列问题
(1)在400℃时,将一定量的 和14mol 压入一个盛有催化剂的10L密闭容器中进行反应:
,已知2min后,容器中剩余2mol 和12mol ,则:
①反应中消耗了_______mol ,2min后 的物质的量浓度是_______。
②2min内平均反应速率: _______。
③发生反应前容器内压强与发生反应后容器中压强比值为:_______。
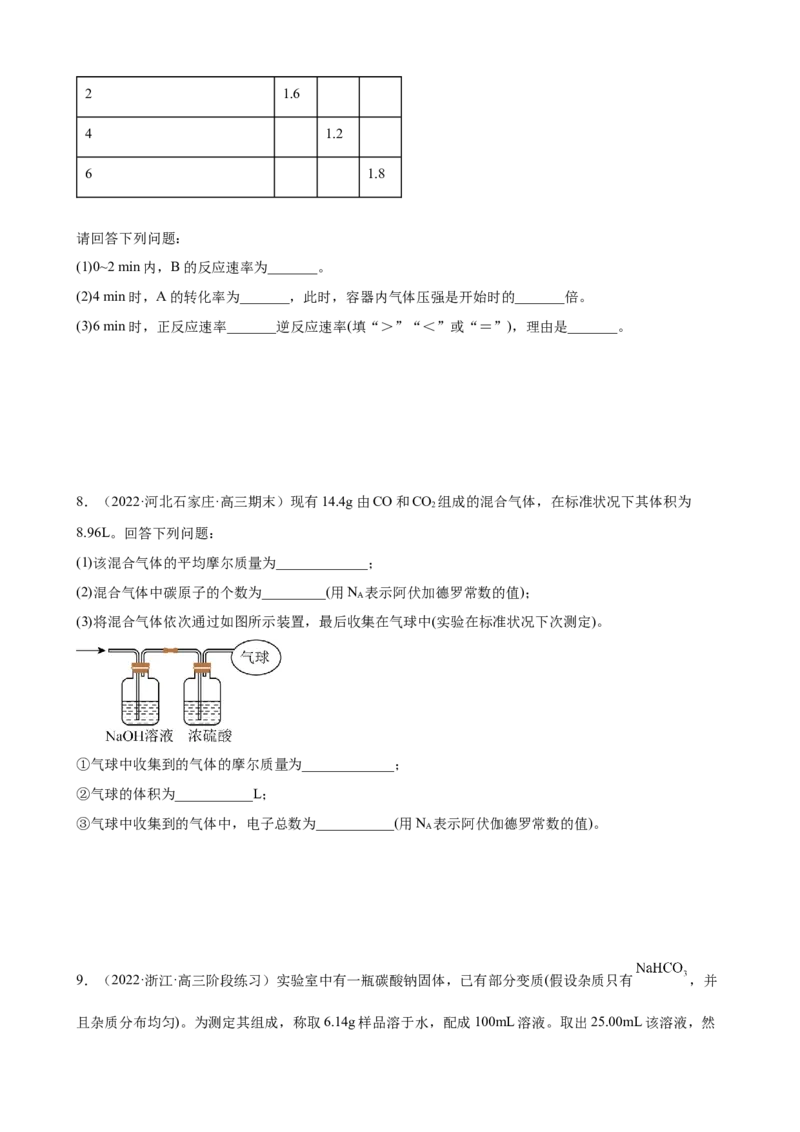
(2)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
①Z的产率是_______。
②由图中所给数据进行分析,该反应的化学方程式为_______。
③若三种物质都是气体,则平衡时X所占体积的百分比为_______。
7.(2022·云南·昆明市第三中学高三期末)在一体积为2 L的密闭容器中加入反应物A、B,发生如下反
应:A(g)+2B(g) 3C(g)。反应过程部分数据如下表所示。
物质的量(mol)
n(A) n(B) n(C)
时间(min)
0 2.0 2.4 02 1.6
4 1.2
6 1.8
请回答下列问题:
(1)0~2 min内,B的反应速率为_______。
(2)4 min时,A的转化率为_______,此时,容器内气体压强是开始时的_______倍。
(3)6 min时,正反应速率_______逆反应速率(填“>”“<”或“=”),理由是_______。
8.(2022·河北石家庄·高三期末)现有14.4g由CO和CO 组成的混合气体,在标准状况下其体积为
2
8.96L。回答下列问题:
(1)该混合气体的平均摩尔质量为_____________;
(2)混合气体中碳原子的个数为_________(用N 表示阿伏加德罗常数的值);
A
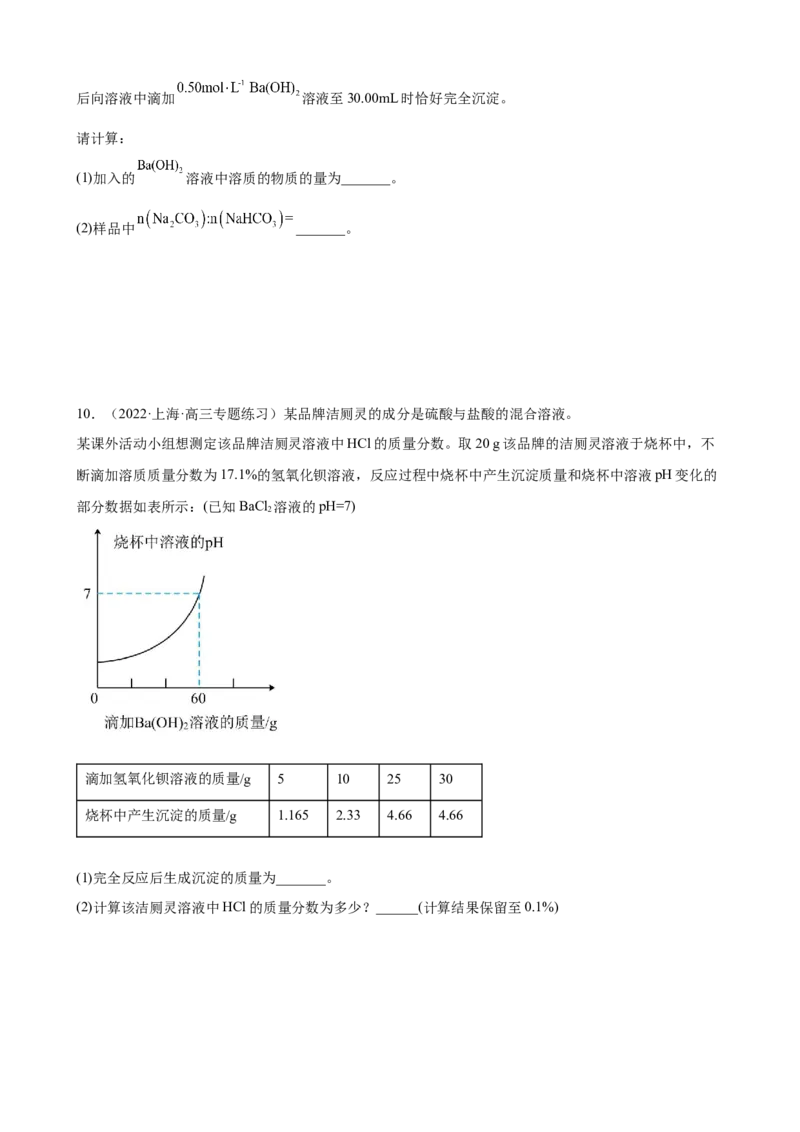
(3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下次测定)。
①气球中收集到的气体的摩尔质量为_____________;
②气球的体积为___________L;
③气球中收集到的气体中,电子总数为___________(用N 表示阿伏伽德罗常数的值)。
A
9.(2022·浙江·高三阶段练习)实验室中有一瓶碳酸钠固体,已有部分变质(假设杂质只有 ,并
且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加 溶液至30.00mL时恰好完全沉淀。
请计算:
(1)加入的 溶液中溶质的物质的量为_______。
(2)样品中 _______。
10.(2022·上海·高三专题练习)某品牌洁厕灵的成分是硫酸与盐酸的混合溶液。
某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量分数。取20 g该品牌的洁厕灵溶液于烧杯中,不
断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的
部分数据如表所示:(已知BaCl 溶液的pH=7)
2
滴加氢氧化钡溶液的质量/g 5 10 25 30
烧杯中产生沉淀的质量/g 1.165 2.33 4.66 4.66
(1)完全反应后生成沉淀的质量为_______。
(2)计算该洁厕灵溶液中HCl的质量分数为多少?______(计算结果保留至0.1%)11.(2022·上海·高三专题练习)取硫酸钠和氯化钠的混合物15g,加入180g水使其完全溶解,再加入
100g氯化钡溶液恰好完全反应,过滤,得271.7g滤液(不考虑实验过程中质量损失)。计算:
(1)该混合物中硫酸钠的质量分数(计算结果精确到0.1%)____。
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)____。
12.(2022·浙江大学附属中学高三阶段练习)某合金(仅含铜、铁)中铜和铁的物质的量之和为 ,其
中 的物质的量分数为b,将其全部投入 的稀硝酸中,加热使其充分反应(假设 是唯一的还原产
物)。
(1)若产生标准状况下 ,则反应转移电子的物质的量为________________
(2)若 ,溶液中的 与 的物质的量之比 ,标准状况下产生 , ___
13.(2022·上海·高三专题练习)CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状
2 2
况)。试回答:
(1)混合气体中CO的质量是_______g。
(2)混合气体中CO 在标准状况下的体积是多少_______L。
2
(3)等质量CO和CO 分子个数比是_______;原子个数比是_______;等温等压下体积比是_______。
2
14.(2022·浙江·温州中学模拟预测)由C、H、O三种元素组成的有机物X, ,X
含有两种官能团。称取8.8g X,与足量金属钠充分反应,生成1.12L氢气(标准状况)。另取8.8g X,在Cu丝作用下,加热与足量 反应得到产物Y,Y与足量新制氢氧化铜溶液反应,析出砖红色固体,经洗涤、
干燥称量得28.8g。试求出X的相对分子质量以及写出X的结构简式。
(1)X的相对分子质量_______
(2)X的结构简式_______(要求写出简要推理过程)
15.(2022·吉林松原·高三阶段练习)化学计量在化学中占有重要地位,请回答下列问题:
(1)青蒿素C H O 的摩尔质量为_______。
15 22 5
(2)在标准状况下,22.4 L由O 和N 组成的混合气体中,含有的分子总数约为_______。
2 2
(3)在标准状况下,含有 个氦原子的氦气的体积约为_______。
(4)某消毒小组人员用17 mol/L的浓硫酸配制 的稀硫酸用于增强84消毒液的消毒能力,
需取用浓硫酸的体积为_______ ;所配溶液中的 的物质的量浓度为_______。
(5)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。标
准状况下,向Ⅰ中充入8 g SO ,Ⅱ中充入8 g O,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_______。
2 2
(6)把7.8克镁铝合金的粉末放入过量的盐酸中,得到8.96 LH (标准状况)。该合金中铝和镁的物质的量之
2
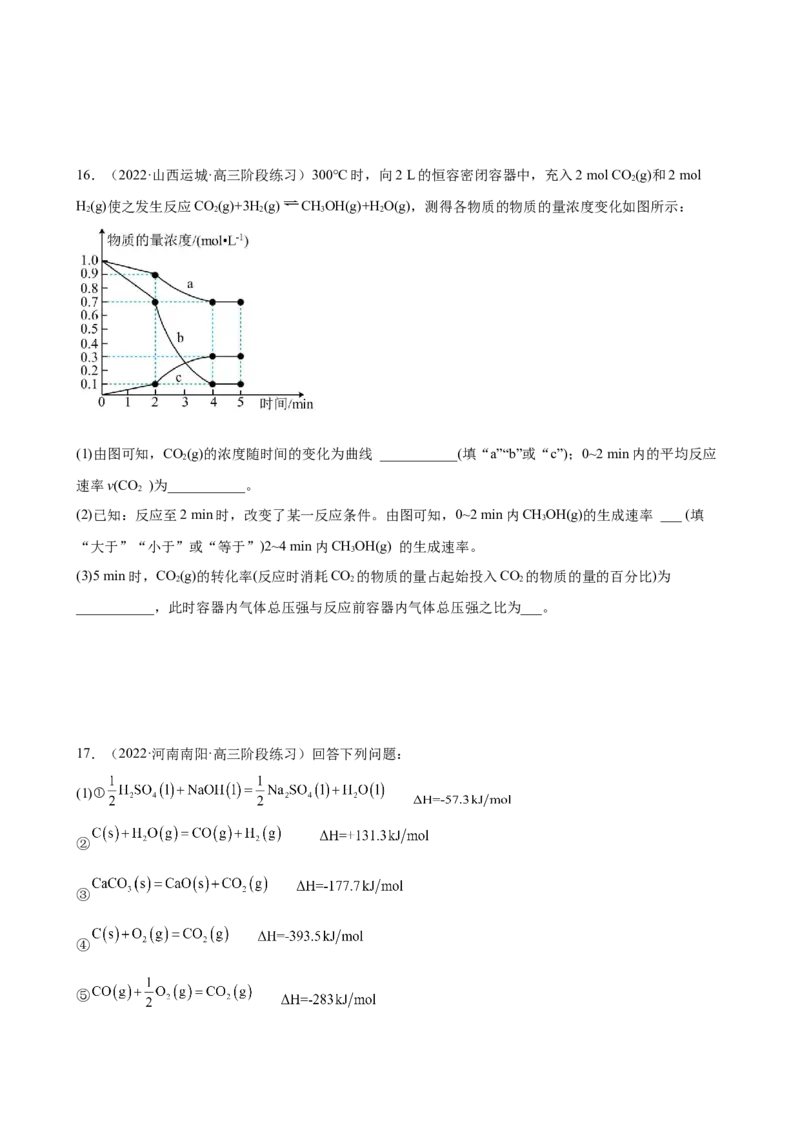
比_______。16.(2022·山西运城·高三阶段练习)300°C时,向2 L的恒容密闭容器中,充入2 mol CO (g)和2 mol
2
H(g)使之发生反应CO(g)+3H(g) CHOH(g)+H O(g),测得各物质的物质的量浓度变化如图所示:
2 2 2 3 2
(1)由图可知,CO(g)的浓度随时间的变化为曲线 ___________(填“a”“b”或“c”);0~2 min内的平均反应
2
速率v(CO )为___________。
2
(2)已知:反应至2 min时,改变了某一反应条件。由图可知,0~2 min内CHOH(g)的生成速率 ___ (填
3
“大于”“小于”或“等于”)2~4 min内CHOH(g) 的生成速率。
3
(3)5 min时,CO(g)的转化率(反应时消耗CO 的物质的量占起始投入CO 的物质的量的百分比)为
2 2 2
___________,此时容器内气体总压强与反应前容器内气体总压强之比为___。
17.(2022·河南南阳·高三阶段练习)回答下列问题:
(1)①
②
③
④
⑤⑥
⑦
(a)若上述反应放出或吸收的热量数值均正确,则上述热化学方程式中,不正确的有_______(填序号)。
(b)根据上述信息,写出C转化为CO的热化学方程式_______。
(2)已知热化学方程式: ,其逆反应的活化能为 ,
则其正反应的活化能为_______kJ/mol。
(3)用 催化还原 可以消除氮氧化物的污染。例如:
若用标准状况下 还原 生成 ,反应中转移的电子总数为_______(阿伏加德罗常数用 表
示),放出的热量为_______kJ。
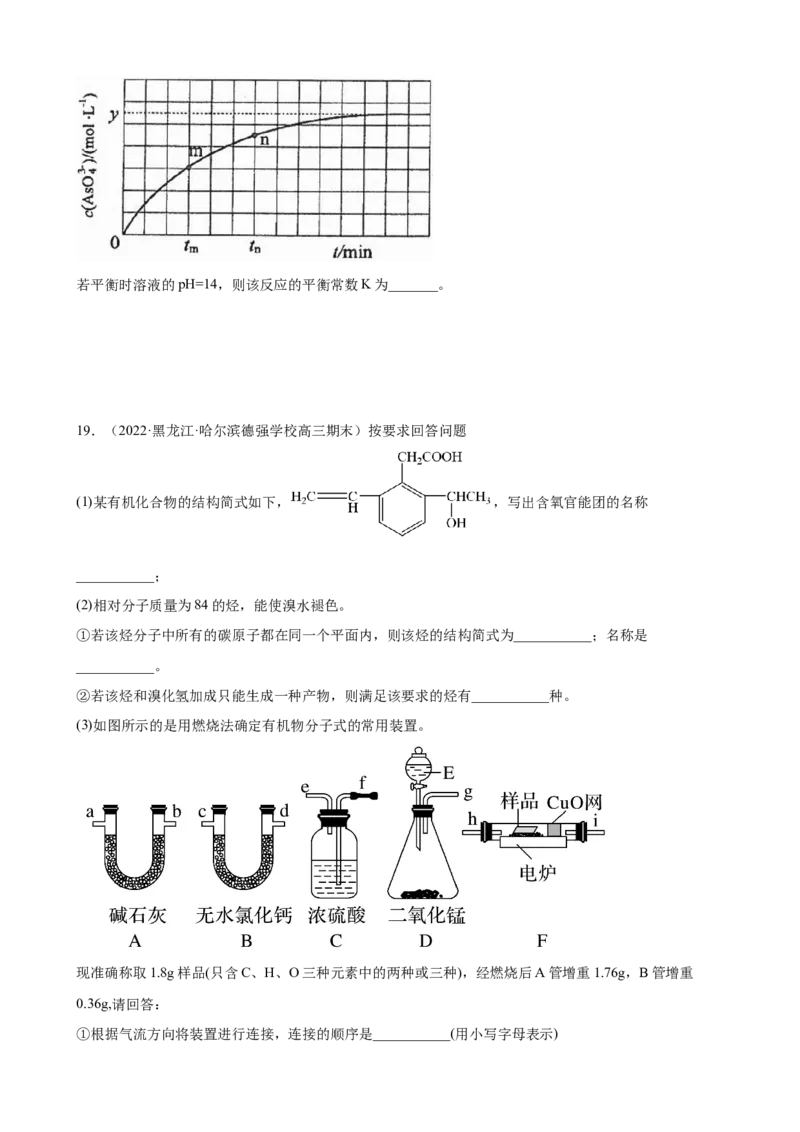
18.(2022·河北石家庄·高三专题练习)砷(As)是第四周期VA族元素,可以形成As S、As O、
2 3 2 5
HAsO 、HAsO 等化合物,有着广泛的用途。298 K时,将20 mL 3x mol·L−1 Na AsO 、20 mL 3x mol·L−1
3 3 3 4 3 3
I 和20 mL NaOH溶液混合,发生反应: (aq)+I (aq)+2OH−(aq) (aq)+2I−(aq)+ HO(l)。溶液中
2 2 2
⇌
c( )与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为_______。
19.(2022·黑龙江·哈尔滨德强学校高三期末)按要求回答问题
(1)某有机化合物的结构简式如下, ,写出含氧官能团的名称
___________;
(2)相对分子质量为84的烃,能使溴水褪色。
①若该烃分子中所有的碳原子都在同一个平面内,则该烃的结构简式为___________;名称是
___________。
②若该烃和溴化氢加成只能生成一种产物,则满足该要求的烃有___________种。
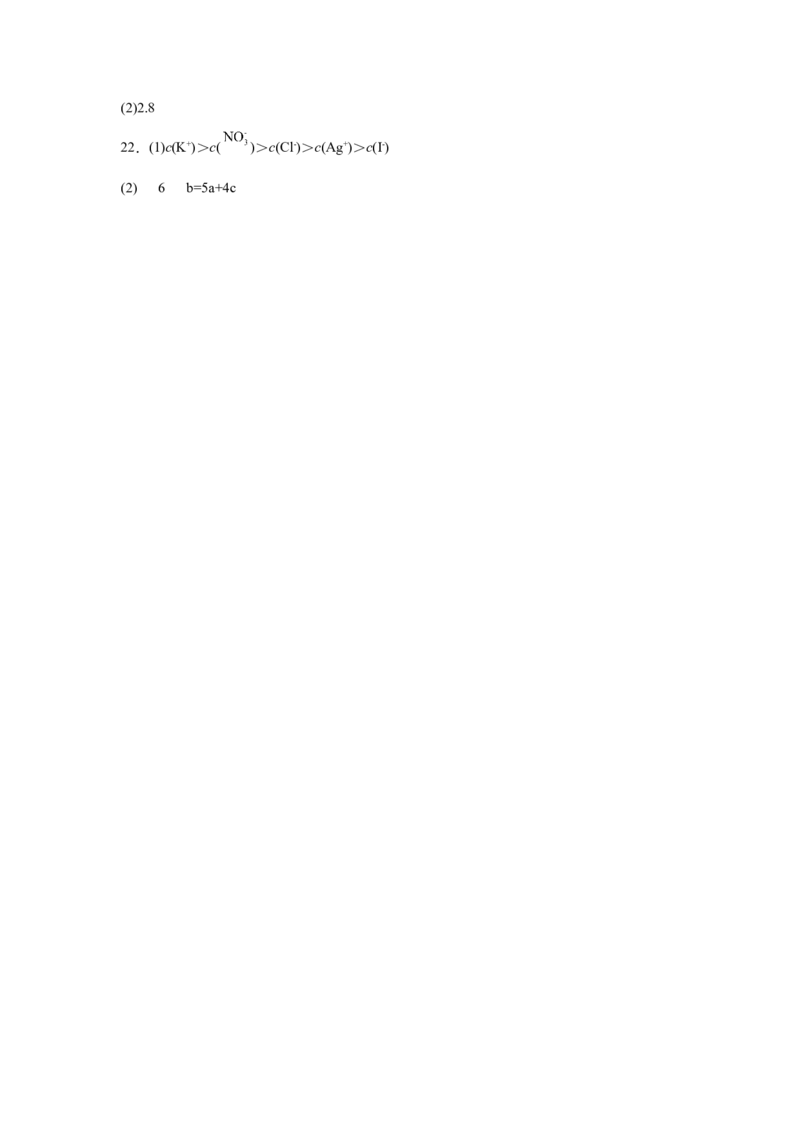
(3)如图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取1.8g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76g,B管增重
0.36g,请回答:
①根据气流方向将装置进行连接,连接的顺序是___________(用小写字母表示)②该有机物的最简式为___________。
③该有机物蒸汽密度相对于氢气为45,核磁共振氢谱显示只有一组峰,写出结构简式___________。
20.(2022·河北唐山·高三期末)请计算:
(1)已知N 和H 反应生成NH 时,若生成2mol NH 放出的能量为92.4kJ,请计算断开1mol N-H键需要吸
2 2 3 3
收的能量为_______。(已知H-H键,N≡N键键能分别为435kJ/mol,943kJ/mol,计算结果保留整数)
(2)已知下列热化学方程式:
C(s)+O(g)=CO (g) ΔH=-393.5kJ·mol-1
2 2
2H(g)+O(g)=2HO(g) ΔH=-483.6kJ·mol-1
2 2 2
现有0.2mol的氢气和碳粉组成的气、固混合物在氧气中完全燃烧,共放出63.53kJ热量,则氢气与碳粉的
物质的量之比为_______。
21.(2022·浙江绍兴·高三阶段练习)取30.8g甲酸铜[(HCOO) Cu]在隔绝空气的条件下加热分解,会生
2
成含两种红色固体(Cu和 )的混合物A和混合气体B;若相同质量的甲酸铜在空气中充分加热,则生
成黑色固体D和 、 ,固体A和D质量相差2.4g。请计算:
(1)红色固体A中Cu单质的物质的量为_______mol,同时写出简要的计算过程。
(2)将混合气体B置于 中充分燃烧,消耗 的体积是_______L(换算为标准状况)。
22.(2021·陕西·西北工业大学附属中学高三期末)完成下列各题。
(1)已知25℃时,AgI的饱和溶液中c(Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5
mol/L。若在5 mL含KCl和KI各为0.01 mol/L的溶液中,加入8 mL0.01 mol/L AgNO 溶液,这时溶液中
3
所含溶质的离子浓度由大到小的次序是_______。[已知:25℃时K (AgC1)=1.6×10-10,K (AgI)=8.5×10-17]
sp sp
(2)如图所示,无摩擦、无质量的活塞1,2,3和4将反应器隔成甲、乙、丙和丁4部分,分别进行反应:
A(g)+B(g) C(g),起始时物质的量已标在图中。某温度和100 kPa下达到平衡时,各部分的体积分别为V
、V 、V⇌ 和V 。这时若抽掉活塞1或3均不会引起其它活塞移动。
甲 乙 丙 丁①据题意计算x=_______。
②a、b、c必须满足的一般条件是(请用含有a、b、c的方程表示):_______。参考答案:
1.(1)0.21
(2)0.111
(3)1.00
2.(1) OH-+H+=H O、Mg2++2OH-=Mg(OH) ↓、Al3++3OH-=Al(OH) ↓、Al(OH) +OH-=
2 2 3 3
+2H O 0.06 440
2
(2)400
(3)0.5≤a<1
3.(1)0.6
(2) 3 3:2
(3) K= 1.09
(4)>
4.(1) CHCOOH+CH CHOH CHCOOCH CH+H O BC
3 3 2 3 2 3 2
(2) 2:1 2.4
5.(1)0.5mol
(2) 5.824 5.376
(3)5.712
6.(1) 4 0.4mol/L 0.1mol/(L·min) 10:9
(2) 30% 38.9%
7.(1)0.2 mol·L-1·min-1
(2) 30% 1
(3) = 此时反应物和生成物各组分物质的量(浓度)都不再改变
8.(1)36g/mol
(2)0.4N
A
(3) 28g/mol 4.48 2.8N
A
9.(1)0.015mol
(2)5:1
10.(1)4.66 g
(2)14.6%11.(1)94.7%
(2)4.6%
12.(1)0.30
(2)2.0
13.(1)7
(2)5.6
(3) 11:7 22:21 11:7
14.(1)88
(2)HOCHCHCHCHO、HOCH CH(CH )CHO
2 2 2 2 3
15.(1)282 g/mol
(2)6.02×1023
(3)11.2 L
(4) 100 6.8 mol/L
(5)1:2
(6)2:1
16.(1) a 0.05 mol·L-1 ·min -1
(2)小于
(3) 30% 7:10
17.(1) ①③ C(s)+ O(g)=CO (g)ΔH=—110.5kJ/mol
2 2
(2)167.2
(3) 16N 1734
A
18.
19.(1)羟基、羧基
(2) (CH)C=C(CH ) 2,3-二甲基-2-丁烯 CHCHC = CCH CH、(CH)C=
3 2 3 2 3 2 2 3 3 2
C(CH)
3 2
(3) g接f,e接h,I接 c或(d),d或(c)接a或(b) CHO HOOC-COOH
2
20.(1)390kJ
(2)1:1
21.(1)0.1(2)2.8
22.(1)c(K+)>c( )>c(Cl-)>c(Ag+)>c(I-)
(2) 6 b=5a+4c