文档内容
2023届高考化学一轮专题复习练习题:元素或物质推断题
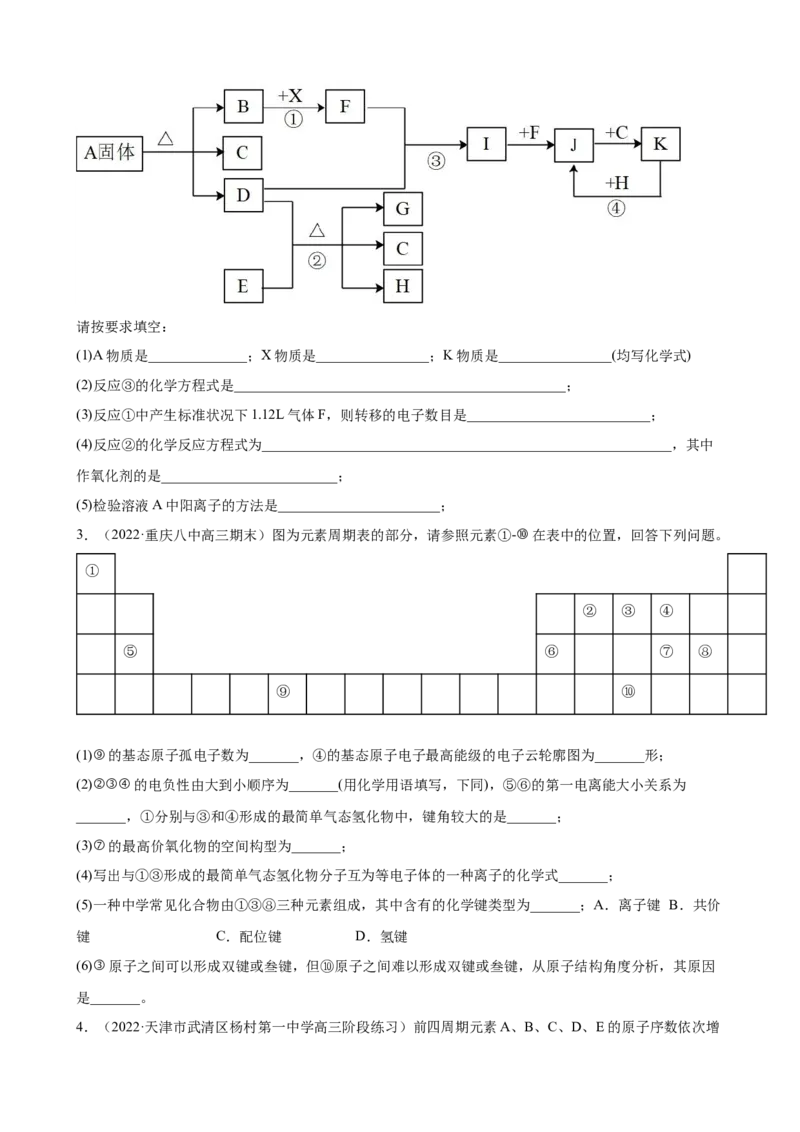
1.(2022·黑龙江·哈九中高三期末)下表列出了①~⑩所代表的十种元素在周期表中的位置,按要求填写
下列空白:
主族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
一 ①
二 ② ③ ④
三 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)①、③按原子个数比为3:1组成的分子的电子式_______。当今,考古工作者是利用②的一种核素
_______(请写出其核素符号)衰变测定装置,对文物进行年代的测定和研究。④⑤⑥三种元素的简单离子
半径从大到小排序_______(用离子符号表示),元素X与⑦同一主族,X原子比⑦原子多一个电子层,X
的原子结构示意图为_______。元素Y与⑧同一主族,位于周期表第四周期,其氢化物的化学式为
_______。
(2)以下组合的原子间反应最容易形成离子键的是_______(选填A、B、C、D)
A.④和⑥ B.①和④ C.④和⑤ D.⑤和⑩
非金属性最强的元素的氢化物在水中的电离方程式为_______。
(3)写出⑥元素的最高价氧化物与氢氧化钠溶液反应的化学方程式_______﹔磁性氧化铁溶解于元素⑩的氢
化物的浓溶液发生反应的离子方程式为_______。
(4)高铁的快速发展方便了人们的出行,工业上利用⑥的单质参与的反应焊接钢轨间的缝隙,反应的化学
方程式为_______。其中⑥的单质发生_______(填:氧化或还原)反应。
(5)只含元素①和元素⑤的化合物可在野外作供氢剂。请写出该化合物跟水反应的化学方程式_______。1
mol 该化合物溶于足量水中完全反应,共转移_______mol电子。
2.(2022·辽宁·沈阳市第三十一中学高三阶段练习)下图表示各物质之间的转化关系。已知:常温下
B、D、F、G、I、J是气体,F、G是空气中的主要成分,D是一种碱性气体;A中阴、阳离子个数比是
1:1,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)请按要求填空:
(1)A物质是______________;X物质是________________;K物质是________________(均写化学式)
(2)反应③的化学方程式是_______________________________________________;
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是__________________________;
(4)反应②的化学反应方程式为__________________________________________________________,其中
作氧化剂的是_________________________;
(5)检验溶液A中阳离子的方法是_______________________;
3.(2022·重庆八中高三期末)图为元素周期表的部分,请参照元素①-⑩在表中的位置,回答下列问题。
①
② ③ ④
⑤ ⑥ ⑦ ⑧
⑨ ⑩
(1)⑨的基态原子孤电子数为_______,④的基态原子电子最高能级的电子云轮廓图为_______形;
(2)②③④的电负性由大到小顺序为_______(用化学用语填写,下同),⑤⑥的第一电离能大小关系为
_______,①分别与③和④形成的最简单气态氢化物中,键角较大的是_______;
(3)⑦的最高价氧化物的空间构型为_______;
(4)写出与①③形成的最简单气态氢化物分子互为等电子体的一种离子的化学式_______;
(5)一种中学常见化合物由①③⑧三种元素组成,其中含有的化学键类型为_______;A.离子键 B.共价
键 C.配位键 D.氢键
(6)③原子之间可以形成双键或叁键,但⑩原子之间难以形成双键或叁键,从原子结构角度分析,其原因
是_______。
4.(2022·天津市武清区杨村第一中学高三阶段练习)前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原
子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单
离子中最小。回答下列问题:
(1)E的元素名称为_______。它位于元素周期表的_______区。
(2)元素A、B、C中,电负性最大的是_______(填元素符号,下同),元素B、C、D第一电离能由大到小
的顺序为_______。
(3)与同族其他元素X形成的 相比, 易液化的原因是_______; 分子中键角_______ (填
“>”“<”或“=”)。
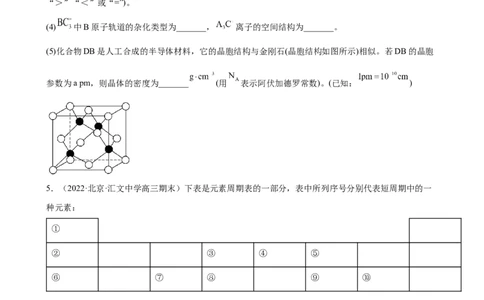
(4) 中B原子轨道的杂化类型为_______, 离子的空间结构为_______。
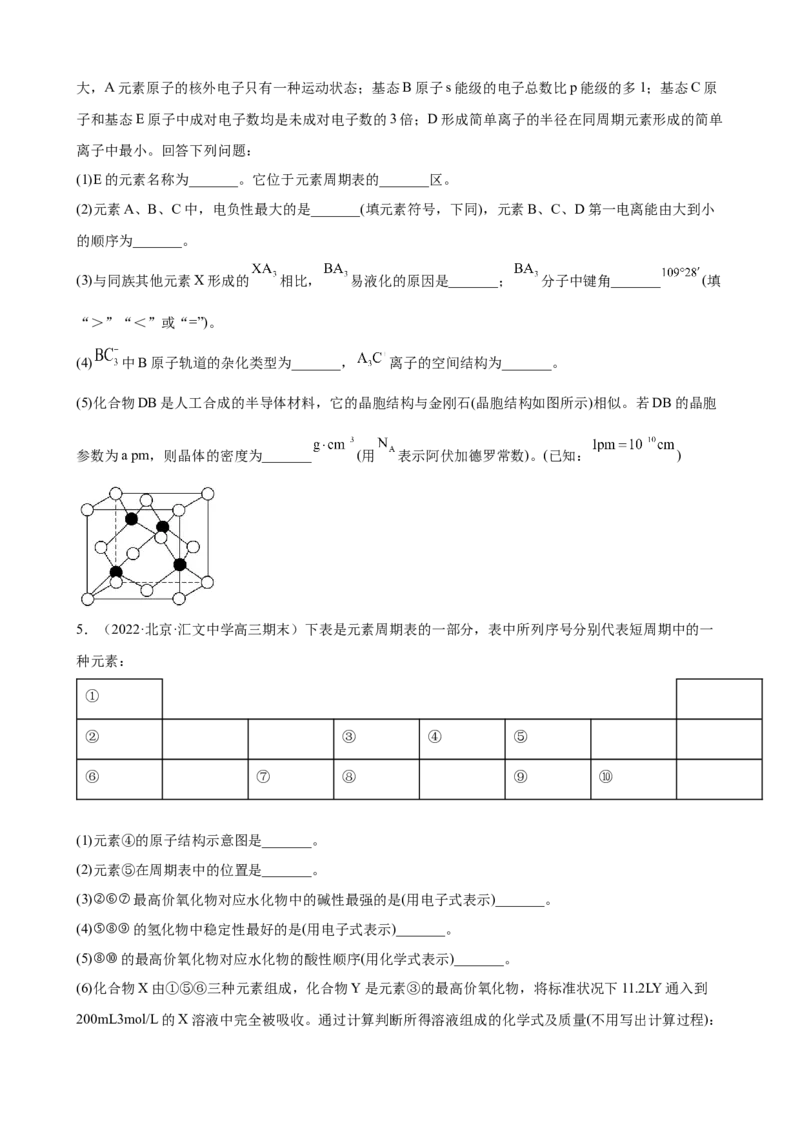
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞
参数为a pm,则晶体的密度为_______ (用 表示阿伏加德罗常数)。(已知: )
5.(2022·北京·汇文中学高三期末)下表是元素周期表的一部分,表中所列序号分别代表短周期中的一
种元素:
①
② ③ ④ ⑤
⑥ ⑦ ⑧ ⑨ ⑩
(1)元素④的原子结构示意图是_______。
(2)元素⑤在周期表中的位置是_______。
(3)②⑥⑦最高价氧化物对应水化物中的碱性最强的是(用电子式表示)_______。
(4)⑤⑧⑨的氢化物中稳定性最好的是(用电子式表示)_______。
(5)⑧⑩的最高价氧化物对应水化物的酸性顺序(用化学式表示)_______。
(6)化合物X由①⑤⑥三种元素组成,化合物Y是元素③的最高价氧化物,将标准状况下11.2LY通入到
200mL3mol/L的X溶液中完全被吸收。通过计算判断所得溶液组成的化学式及质量(不用写出计算过程):_______。
6.(2022·重庆市长寿中学校高三阶段练习)已知X、Y、Z、W、Q是原子序数依次增大的前四周期元
素。X原子核外有6种不同运动状态的电子;Y基态原子中s电子总数与p电子总数相等;Z最高价氧化
物对应水化物的碱性在同周期元素中最强;W基态原子的最外层p轨道有2个电子的自旋状态与其他电
子的自旋状态相反。
(1)基态X原子中电子占据的最高能级的原子轨道形状为_______。原子中运动的电子有两种相反的自旋状
态,若一种自旋状态用 表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态X原子,
其核外电子自旋磁量子数的代数和为_______。
(2)Y、Z、W的简单离子半径由大到小的顺序为_______。(用离子符号表示)
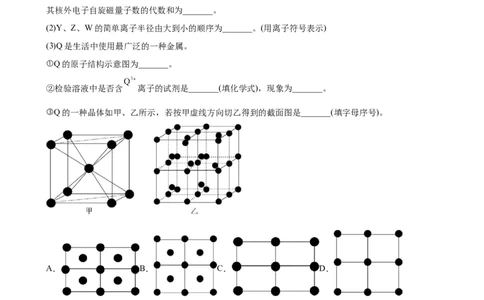
(3)Q是生活中使用最广泛的一种金属。
①Q的原子结构示意图为_______。
②检验溶液中是否含 离子的试剂是_______(填化学式),现象为_______。
③Q的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是_______(填字母序号)。
A. B. C. D.
7.(2022·福建省厦门集美中学高三阶段练习)A、B、C、D、E、F六种短周期元素,其原子序数依次
增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素原子的s能级电子
总数与p能级的相等,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常
压下有三种是气体,三种是固体。请回答下列问题:
(1)A是_______(填元素符号,下同),B是_______,C是_______,D是_______,F是_______。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是_______(用离子符号表示)。
(3)由A、B、C三种元素以原子个数比4∶2∶3可形成一种离子化合物,其阳离子电子式为_______。(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:_______。若E是
非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_______。
8.(2022·重庆·高三期末)原子序数由小到大排列的四种短周期元素X、Y、Z、W的原子序数之和为
32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与
W同周期。
(1)M在元素周期表中的位置___________。
(2)Z、M、W三种元素离子半径由小到大的顺序是 ___________ (填相应的离子符号)。
(3)X与Z可分别形成10电子分子A和18电子的分子B。A的分子空间构型为___________,B分子的电
子式___________。
(4)由X、Y、Z、W四种元素组成的一种盐,该盐中含有的化学键类型为___________。
(5)Z非金属性强于W,下列选项中能证明这一事实的是___________。
A.常温下W单质熔沸点比Z单质的高
B.Z的简单氢化物比W的氢化物更稳定
C.在一定条件下可发生反应:Z + 2X W = 2W + 2X Z
2 2 2
D.XW的酸性比XZ强
2 2
(6)在一定温度下,向由X、M、Z三种元素组成的化合物的溶液中通入Cl,所得溶液中
2
,写出总反应的离子方程式___________
9.(2022·河北·石家庄市藁城区第一中学高三阶段练习)A~H都是初中化学中的常见物质,它们之间的
转化关系如图所示。A是天然气的主要成分,E是一种常见的食品干燥剂。请回答:
(1)A的化学式为____。
(2)反应②的化学方程式为____。
(3)反应③的化学方程式为____,基本反应类型是____。
(4)反应④的化学方程式为____;基本反应类型是____。
(5)实验室检验D物质常用方法是____。
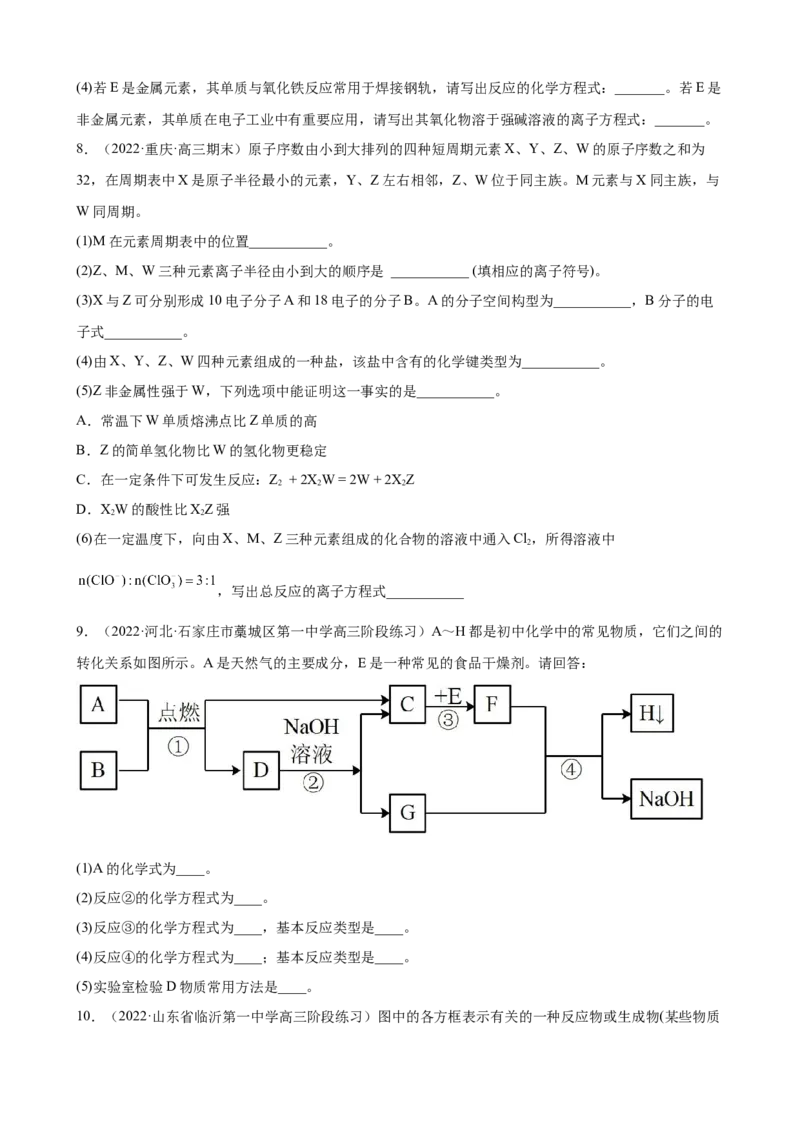
10.(2022·山东省临沂第一中学高三阶段练习)图中的各方框表示有关的一种反应物或生成物(某些物质已经略去),X加热分解生成的各种产物物质的量相等。其中常温下A、C、D、E为无色气体,F为红棕
色气体。
(1)写出下列各物质的化学式:X:_______。
(2)写出A的电子式_______。
(3)写出下列变化的反应方程式:
A→D:_______。
C→E:_______。
(4)在 的反应中氧化剂与还原剂的物质的量之比为_______。
11.(2022·河南·高三阶段练习)M、Q、R、X、Y、Z是前36号元素,它们的原子序数依次增大,其中
M、R原子的3p轨道都有2个未成对电子,X、Y和Z原子的最外层都只有1个电子。回答下列问题:
(1)Y元素的基态原子核外共有____种不同运动状态的电子、____个未成对电子。
(2)在周期表的五个分区中,Z在____区,其基态原子的价层电子排布式是____。
(3)M、Q、R的电负性由小到大的顺序为____(用元素符号表示),说明理由:____。
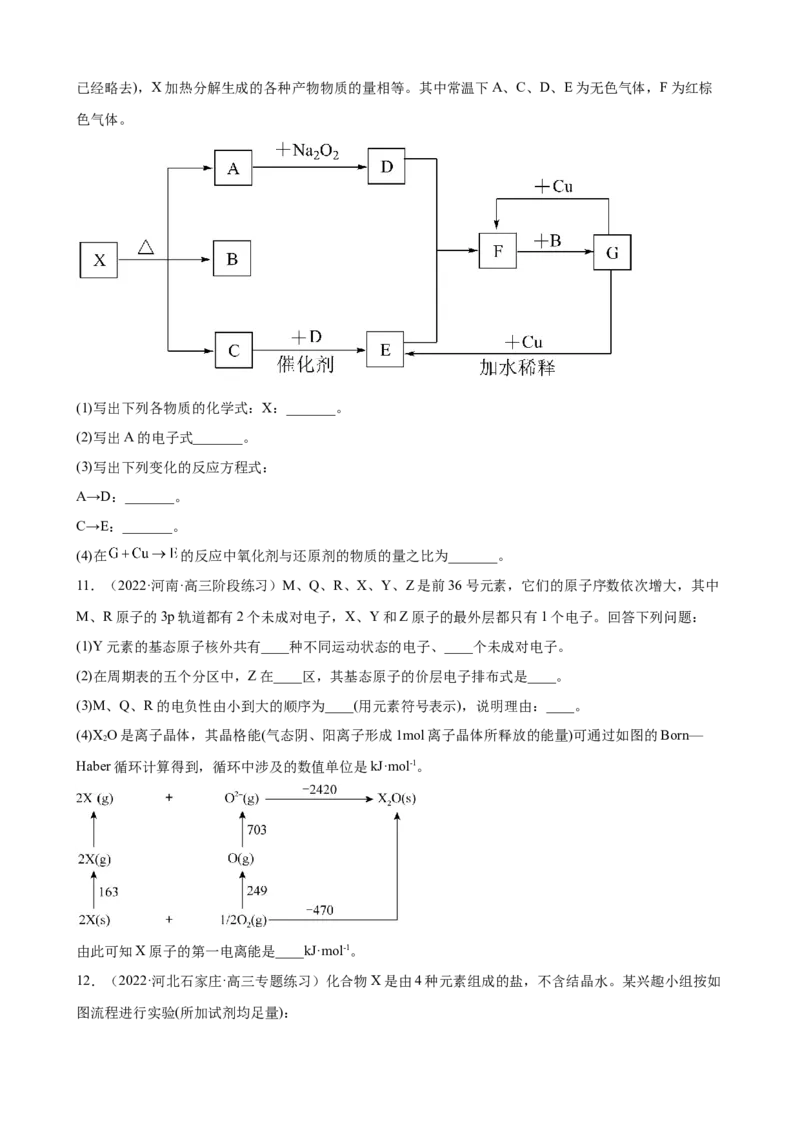
(4)X O是离子晶体,其晶格能(气态阴、阳离子形成1mol离子晶体所释放的能量)可通过如图的Born—
2
Haber循环计算得到,循环中涉及的数值单位是kJ·mol-1。
由此可知X原子的第一电离能是____kJ·mol-1。
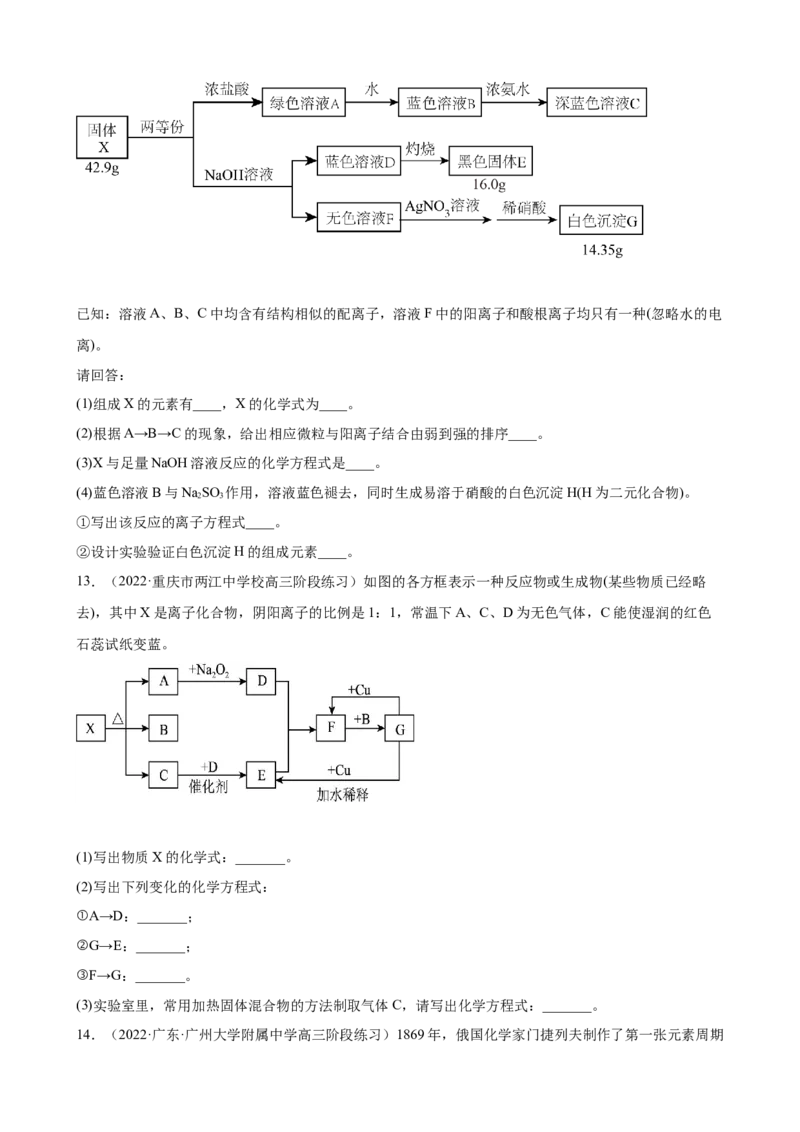
12.(2022·河北石家庄·高三专题练习)化合物X是由4种元素组成的盐,不含结晶水。某兴趣小组按如
图流程进行实验(所加试剂均足量):已知:溶液A、B、C中均含有结构相似的配离子,溶液F中的阳离子和酸根离子均只有一种(忽略水的电
离)。
请回答:
(1)组成X的元素有____,X的化学式为____。
(2)根据A→B→C的现象,给出相应微粒与阳离子结合由弱到强的排序____。
(3)X与足量NaOH溶液反应的化学方程式是____。
(4)蓝色溶液B与NaSO 作用,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀H(H为二元化合物)。
2 3
①写出该反应的离子方程式____。
②设计实验验证白色沉淀H的组成元素____。
13.(2022·重庆市两江中学校高三阶段练习)如图的各方框表示一种反应物或生成物(某些物质已经略
去),其中X是离子化合物,阴阳离子的比例是1:1,常温下A、C、D为无色气体,C能使湿润的红色
石蕊试纸变蓝。
(1)写出物质X的化学式:_______。
(2)写出下列变化的化学方程式:
①A→D:_______;
②G→E:_______;
③F→G:_______。
(3)实验室里,常用加热固体混合物的方法制取气体C,请写出化学方程式:_______。
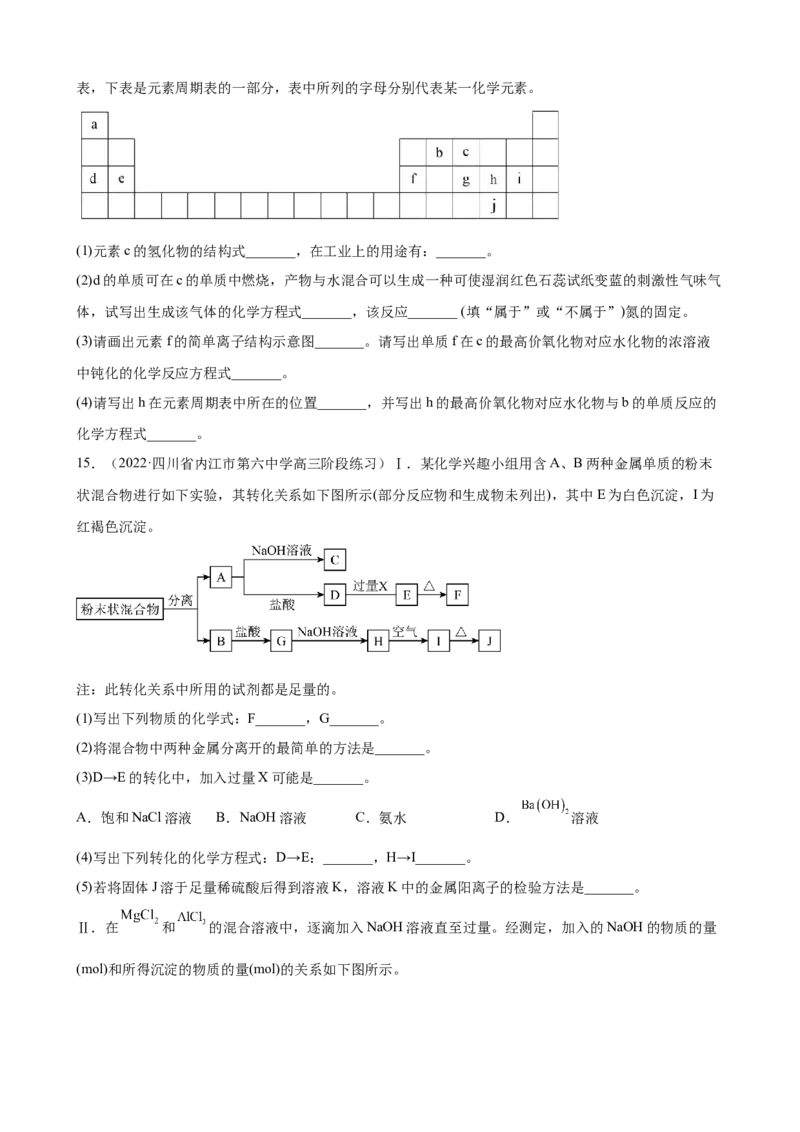
14.(2022·广东·广州大学附属中学高三阶段练习)1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
(1)元素c的氢化物的结构式_______,在工业上的用途有:_______。
(2)d的单质可在c的单质中燃烧,产物与水混合可以生成一种可使湿润红色石蕊试纸变蓝的刺激性气味气
体,试写出生成该气体的化学方程式_______,该反应_______ (填“属于”或“不属于”)氮的固定。
(3)请画出元素f的简单离子结构示意图_______。请写出单质f在c的最高价氧化物对应水化物的浓溶液
中钝化的化学反应方程式_______。
(4)请写出h在元素周期表中所在的位置_______,并写出h的最高价氧化物对应水化物与b的单质反应的
化学方程式_______。
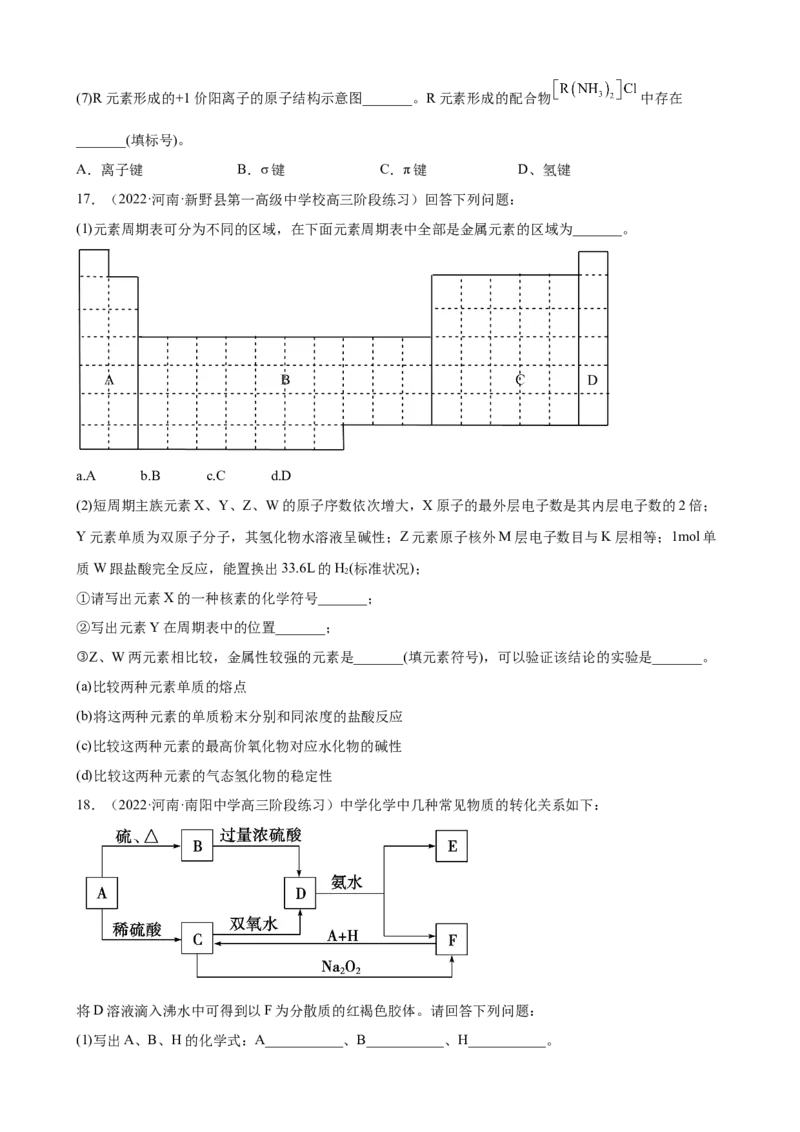
15.(2022·四川省内江市第六中学高三阶段练习)Ⅰ.某化学兴趣小组用含A、B两种金属单质的粉末
状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色沉淀,I为
红褐色沉淀。
注:此转化关系中所用的试剂都是足量的。
(1)写出下列物质的化学式:F_______,G_______。
(2)将混合物中两种金属分离开的最简单的方法是_______。
(3)D→E的转化中,加入过量X可能是_______。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D. 溶液
(4)写出下列转化的化学方程式:D→E:_______,H→I_______。
(5)若将固体J溶于足量稀硫酸后得到溶液K,溶液K中的金属阳离子的检验方法是_______。
Ⅱ.在 和 的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量
(mol)和所得沉淀的物质的量(mol)的关系如下图所示。(6)写出下列线段内发生反应的离子方程式:OD段_______,CD段_______。
(7)原溶液中 、 的物质的量浓度之比为_______。
(8)图中C点表示当加入_______mol NaOH时,Al元素的存在形式为_______,Mg元素的存在形式已经
_______。(填化学式)
(9)图中线段OA:AB=_______。
16.(2022·内蒙古·元宝山平煤高中高三阶段练习)有A—F六种短周期元素,它们的结构、性质等信息
如下表所示:
元素 结构,性质等信息
是短周期元素(稀有气体元素除外)中原子半径最大
A 的元素,含该元素的某种合金是原子反应堆的导热
剂
B 与A同周期,其最高价氧化物对应的水化物呈两性
C 其气态氢化物极易落于水,液态时常用作制冷剂
是海水中除氢、氧元素外含量最多的元素,其单质
D
或化合物也是自来水生产过程中常用的杀菌消毒剂
E 元素原子的L电子层上有2对成对电子
F 与E同主族
R 基态原子M层全充满,N层只有一个电子
请根据表中信息回答下列问题
(1)A元素原子的核外价电子排布图为_______。
(2)B元素在元素周期表中的位置为_______;离子半径:B_______A(填“>”或“<”)。
(3)C元素可形成[ ]离子,试利用等电子原理写出其电子式_______。
(4)第四周期中与D元素原子具有相同的未成对电子数的元素有_______种。
(5)E元素的气态氢化物是_______分子(填极性或非极性)。
(6)F元素的阴离子[ ]的等电子体中属于分子的是_______。(写1个)(7)R元素形成的+1价阳离子的原子结构示意图_______。R元素形成的配合物 中存在
_______(填标号)。
A.离子键 B.σ键 C.π键 D、氢键
17.(2022·河南·新野县第一高级中学校高三阶段练习)回答下列问题:
(1)元素周期表可分为不同的区域,在下面元素周期表中全部是金属元素的区域为_______。
a.A b.B c.C d.D
(2)短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍;
Y元素单质为双原子分子,其氢化物水溶液呈碱性;Z元素原子核外M层电子数目与K层相等;1mol单
质W跟盐酸完全反应,能置换出33.6L的H(标准状况);
2
①请写出元素X的一种核素的化学符号_______;
②写出元素Y在周期表中的位置_______;
③Z、W两元素相比较,金属性较强的元素是_______(填元素符号),可以验证该结论的实验是_______。
(a)比较两种元素单质的熔点
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)比较这两种元素的最高价氧化物对应水化物的碱性
(d)比较这两种元素的气态氢化物的稳定性
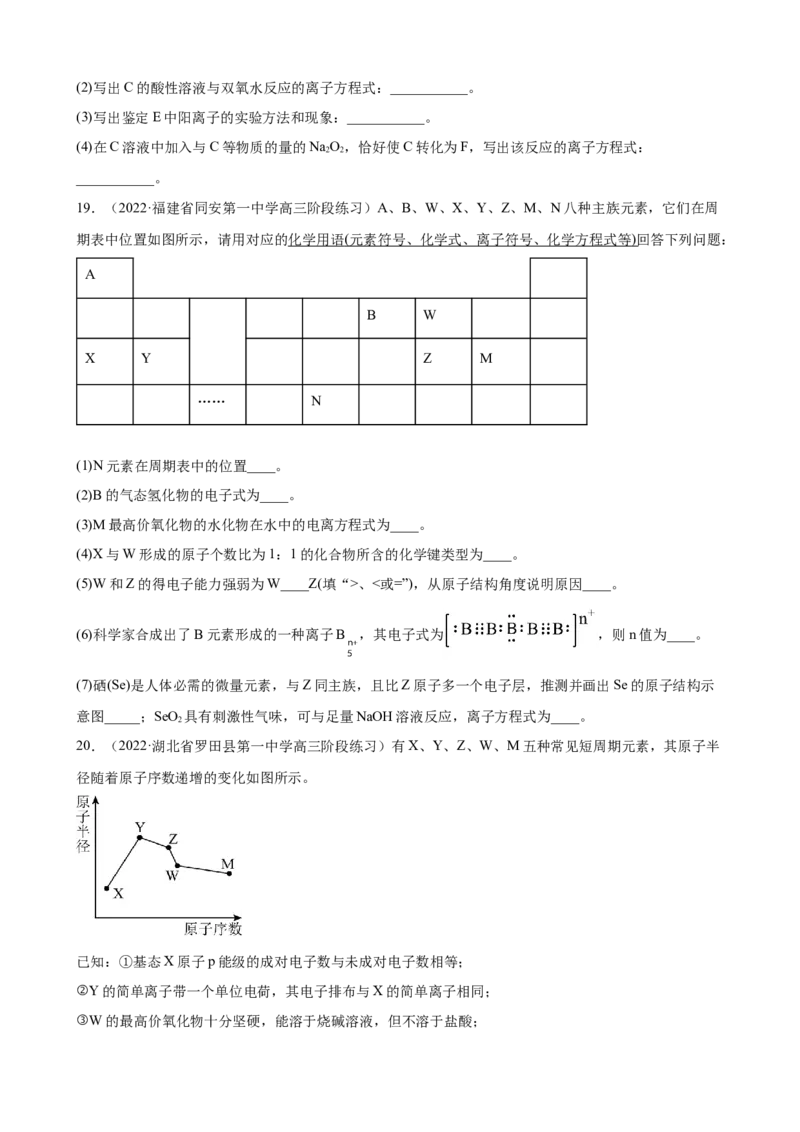
18.(2022·河南·南阳中学高三阶段练习)中学化学中几种常见物质的转化关系如下:
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)写出A、B、H的化学式:A___________、B___________、H___________。(2)写出C的酸性溶液与双氧水反应的离子方程式:___________。
(3)写出鉴定E中阳离子的实验方法和现象:___________。
(4)在C溶液中加入与C等物质的量的NaO,恰好使C转化为F,写出该反应的离子方程式:
2 2
___________。
19.(2022·福建省同安第一中学高三阶段练习)A、B、W、X、Y、Z、M、N八种主族元素,它们在周
期表中位置如图所示,请用对应的 化学用语 ( 元素符号、化学式、离子符号、化学方程式等 )回答下列问题:
A
B W
X Y Z M
…… N
(1)N元素在周期表中的位置____。
(2)B的气态氢化物的电子式为____。
(3)M最高价氧化物的水化物在水中的电离方程式为____。
(4)X与W形成的原子个数比为1:1的化合物所含的化学键类型为____。
(5)W和Z的得电子能力强弱为W____Z(填“>、<或=”),从原子结构角度说明原因____。
(6)科学家合成出了B元素形成的一种离子B ,其电子式为 ,则n值为____。
(7)硒(Se)是人体必需的微量元素,与Z同主族,且比Z原子多一个电子层,推测并画出Se的原子结构示
意图_____;SeO 具有刺激性气味,可与足量NaOH溶液反应,离子方程式为____。
2
20.(2022·湖北省罗田县第一中学高三阶段练习)有X、Y、Z、W、M五种常见短周期元素,其原子半
径随着原子序数递增的变化如图所示。
已知:①基态X原子p能级的成对电子数与未成对电子数相等;
②Y的简单离子带一个单位电荷,其电子排布与X的简单离子相同;
③W的最高价氧化物十分坚硬,能溶于烧碱溶液,但不溶于盐酸;④M的单质常温下是一种黄绿色气体,且Y、Z的最高价氧化物对应的水化物及M的氢化物的水溶液两
两皆能反应。回答下列问题:
(1)基态Z原子的核外电子排布式为______;X、Y、Z、M的简单离子半径由小到大的顺序为______(用离
子符号表示)。
(2)X、Y按原子个数比1∶1形成的化合物的电子式为______,含有的化学键类型为______。
(3)某元素的电负性与第一电离能都大于X元素,其单质在加热条件下与等物质的量的烧碱完全反应,生
成钠盐、HO和一种气体OF ,OF 空间结构为_______。
2 2 2
(4)Z与M形成的化合物为气体,其分子式为ZM,每个原子最外层都达到8电子结构,写出其结构式:
2 6
______。
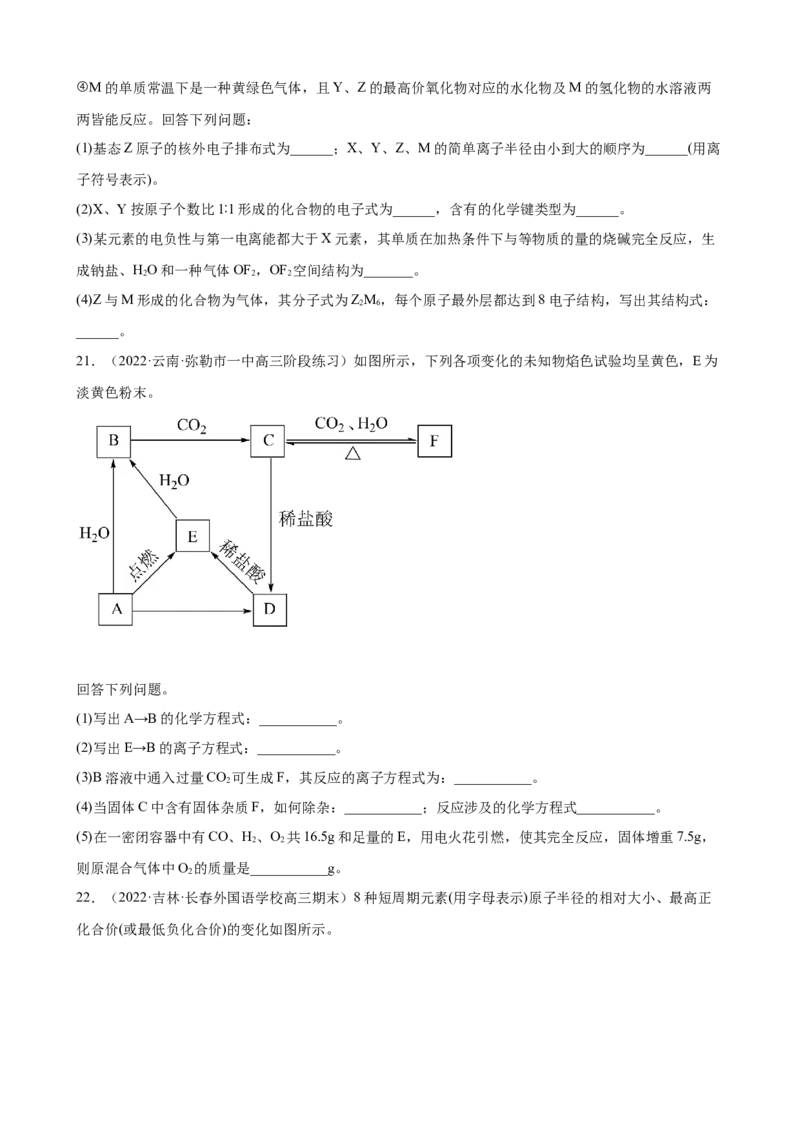
21.(2022·云南·弥勒市一中高三阶段练习)如图所示,下列各项变化的未知物焰色试验均呈黄色,E为
淡黄色粉末。
回答下列问题。
(1)写出A→B的化学方程式:___________。
(2)写出E→B的离子方程式:___________。
(3)B溶液中通入过量CO 可生成F,其反应的离子方程式为:___________。
2
(4)当固体C中含有固体杂质F,如何除杂:___________;反应涉及的化学方程式___________。
(5)在一密闭容器中有CO、H、O 共16.5g和足量的E,用电火花引燃,使其完全反应,固体增重7.5g,
2 2
则原混合气体中O 的质量是___________g。
2
22.(2022·吉林·长春外国语学校高三期末)8种短周期元素(用字母表示)原子半径的相对大小、最高正
化合价(或最低负化合价)的变化如图所示。已知:X为元素周期表中相对原子质量最小的元素。请回答下列问题:
(1)A在元素周期表中的位置是___________; G的下一周期同主族元素的原子序数为___________。
(2)E D 电子式为___________,含___________键(填“序号”,下同),属于___________。
2 2
a.离子键 b.极性键 c.非极性键 d.离子化合物 e.共价化合物
(3)写出E的最高价氧化物的水化物的水溶液与单质G反应的离子方程式___________。
(4)下列有关物质性质的推断,正确的是___________(填“序号”)。
a.金属性:E>G
b.氢化物的稳定性:DN>C Mg>Al NH
3
(3)平面三角形
(4)H O+
3
(5)ABC
(6)As原子半径大,以“头碰头”形成σ键后,p轨道难以形成“肩并肩”重叠,所以As
不能形成π键
4.(1) 铬 d
(2) O N>O>Al
(3) 分子间易形成氢键 <(4) 三角锥形
(5)
5.(1)
(2)第二周期第VIA族
(3)
(4)
(5)HClO >H SiO
4 2 3
(6)m(NaHCO )=33.6g、m(Na CO)=10.6g
3 2 3
6.(1) 哑铃形, (或 )
(2)
(3) KSCN 溶液变红 A
7.(1) H N O Na S
(2)S2-> O2-> Na+
(3)
(4)
8.(1)第三周期第ⅠA族
(2)(3) V形
(4)共价键(或极性键),离子键
(5)BC
(6)
9.(1)CH
4
(2)2NaOH+CO =Na CO+H O
2 2 3 2
(3) CaO+H O=Ca(OH) 化合反应
2 2
(4) Ca(OH) +Na CO=CaCO ↓+2NaOH 复分解反应
2 2 3 3
(5)通入到澄清石灰水中,澄清石灰水变浑浊
10.(1)
(2)
(3)
(4)2∶3
11.(1) 24 6
(2) ds 3d104s1
(3) Si O和S同主族,O的原子半径小
(6)1
(7) SeO+2OH-=SeO +H O
2 2
20.(1) 1s22s22p63s23p1 Al3+Cl,原
子半径I>Cl,原子得电子能力I