文档内容
课时素养评价 二十
金属矿物的开发利用 海水资源的开发利用
(30分钟 50分)
一、选择题(本题包括4小题,每小题5分,共20分)
1.(2019·邢台高一检测)金属锂是密度最小的金属,等质量的不同金属,锂可以
释放出更多的电子,故常用来制造高性能电池。已知锂的金属性介于钠和镁之
间,则冶炼金属锂应采用的方法是 ( )
A.电解法 B.热还原法 C.热分解法 D.铝热法
【解析】选A。金属的冶炼方法与金属活动性顺序的关系:
金属锂的活动性介于钠与镁之间,应采用电解法冶炼金属锂。
2.电解无水MgCl 所得镁蒸气冷却后即得固体镁。镁可在下列哪种气体氛围中
2
冷却 ( )
A.H B.CO C.O D.空气
2 2 2
【解析】选A。Mg在加热条件下可与O 、CO 、N 反应。
2 2 2
【补偿训练】金属K与Na金属性相近,用K与钠盐共熔时,很难将Na从混合物中分离。
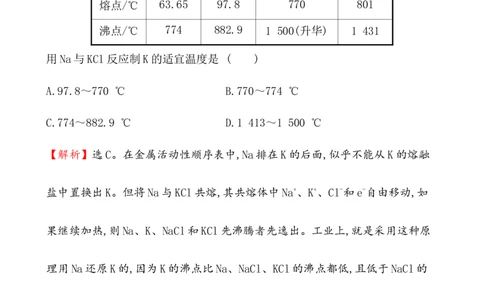
若调整温度到一定程度,则可用Na与KCl反应制取金属K。已知四种物质的熔、
沸点如下:
K Na KCl NaCl
熔点/℃ 63.65 97.8 770 801
沸点/℃ 774 882.9 1 500(升华) 1 431
用Na与KCl反应制K的适宜温度是 ( )
A.97.8~770 ℃ B.770~774 ℃
C.774~882.9 ℃ D.1 413~1 500 ℃
【解析】选C。在金属活动性顺序表中,Na排在K的后面,似乎不能从K的熔融
盐中置换出K。但将Na与KCl共熔,其共熔体中Na+、K+、Cl-和e-自由移动,如
果继续加热,则Na、K、NaCl和KCl先沸腾者先逸出。工业上,就是采用这种原
理用Na还原K的,因为K的沸点比Na、NaCl、KCl的沸点都低,且低于NaCl的
熔点。
3.地球上的大部分水是以海水形式存在的,若能找到海水淡化的大规模生产方
法,将极大地缓解目前人类面临的水资源日益紧缺的状况。下列有关海水淡化
的方法在原理上完全不可行的是 ( )A.加明矾使海水中的盐分沉淀而淡化
B.利用太阳能使海水蒸馏淡化
C.将海水缓慢凝固以获取淡化的饮用水
D.将海水通过离子交换树脂,以除去所含离子
【解析】选A。明矾不能使海水中的Na+、Mg2+、K+等离子沉淀,加入明矾不能使
海水淡化。
【补偿训练】
(2019·西安高一检测)据报道,挪威和荷兰正在开发一种新能源——盐能。
当海水和淡水混合时,温度将升高0.1 ℃,世界所有入海口的这种能源相当于电
力需求的20%。海水和淡水混合时,温度升高最可能的原因是( )
A.发生了盐分解反应
B.发生了水分解反应
C.由于浓度差产生放热
D.盐的溶解度增大
【解析】选C。海水与淡水混合时,不可能发生化学反应,故A、B两项错误;温
度升高可以使盐的溶解度增大,而盐的溶解度增大不可能使温度升高,所以D选
项错误。4.(2019·泰安高一检测)海水综合利用的工艺流程如图所示(粗盐中的可溶性
杂质有MgCl 、CaCl 、Na SO )。下列说法错误的是 ( )
2 2 2 4
A.过程①加入的药品顺序为Na CO 溶液→BaCl 溶液→NaOH溶液→过滤后加盐
2 3 2
酸
B.从过程③到过程⑤的目的是为了浓缩富集溴
C.火力发电厂燃煤排放的含SO 的烟气经处理后可用在过程④反应中
2
D.在过程③或⑤反应中每氧化0.2 mol Br-需消耗标准状况下2.24 L Cl
2
【解析】选A。过程①的提纯中需除去镁离子、钙离子、硫酸根离子,碳酸钠一
定在氯化钡之后,可除去过量的钡离子,故A错误;溴离子被氧化为溴单质后,被
二氧化硫吸收生成溴离子,加入氧化剂氧化溴离子为溴单质,富集溴元素,从过
程③到过程⑤的目的是浓缩富集溴,故B正确;火力发电厂燃煤排放的含SO 的
2
烟气经处理后可以吸收氧化得到的溴单质,发生氧化还原反应得到HBr,通入氧
化剂得到单质溴,起到富集溴元素作用,故C正确;过程③或⑤发生反应的离子方程式为2Br-+Cl Br +2Cl-,每氧化0.2 mol Br-需消耗0.1 mol Cl ,0.1 mol
2 2 2
Cl 在标准状况下的体积为2.24 L,故D正确。
2
【补偿训练】
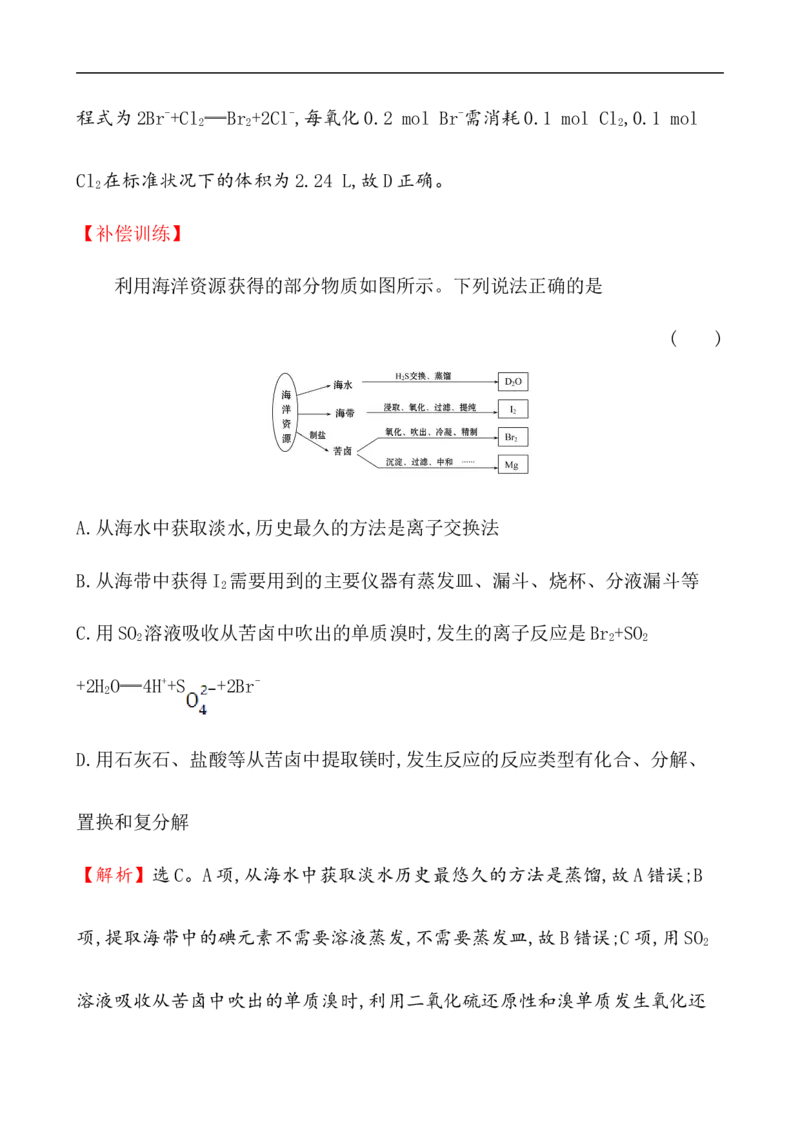
利用海洋资源获得的部分物质如图所示。下列说法正确的是
( )
A.从海水中获取淡水,历史最久的方法是离子交换法
B.从海带中获得I 需要用到的主要仪器有蒸发皿、漏斗、烧杯、分液漏斗等
2
C.用SO 溶液吸收从苦卤中吹出的单质溴时,发生的离子反应是Br +SO
2 2 2
+2H O 4H++S +2Br-
2
D.用石灰石、盐酸等从苦卤中提取镁时,发生反应的反应类型有化合、分解、
置换和复分解
【解析】选C。A项,从海水中获取淡水历史最悠久的方法是蒸馏,故A错误;B
项,提取海带中的碘元素不需要溶液蒸发,不需要蒸发皿,故B错误;C项,用SO
2
溶液吸收从苦卤中吹出的单质溴时,利用二氧化硫还原性和溴单质发生氧化还原反应生成溴化氢和硫酸,发生的离子反应是Br +SO +2H O 4H++S +2Br-,故
2 2 2
C正确;D项,海水提取镁单质的过程中发生的反应有CaCO CaO+CO ↑、
3 2
CaO+H O
2
Ca(OH) 、MgCl +Ca(OH) Mg(OH) +CaCl 、Mg(OH) +2HCl MgCl +2H O、
2 2 2 2 2 2 2 2
MgCl (熔融) Mg+Cl ↑,所以涉及的反应有化合反应、复分解反应和分解反应,
2 2
不涉及置换反应,故D错误。
二、非选择题(本题包括1小题,共10分)
5.(2019·武汉高一检测)海带是海洋中的一种褐藻,海带中含有丰富的碘,是人
类经常食用的一种补碘食物。某资料中有“海带中碘的检验”的选做实验,操
作步骤如下:
①取3 g左右干海带,除去表面杂质,剪碎,用酒精润湿,放在坩埚中灼烧成灰,冷
却;
②将海带灰转移到小烧杯中加蒸馏水,搅拌,煮沸2~3 min,使可溶物质溶解,过
滤;
③向滤液中滴入几滴硫酸,再加入约1 mL 过氧化氢溶液,观察现象;
④取少量上述所得溶液,滴加几滴淀粉溶液,观察现象;⑤向③剩余的滤液中加入1 mL 四氯化碳,振荡静置,观察现象;
⑥向加有四氯化碳的溶液中加入氢氧化钠溶液,充分振荡后,将混合液的下层液
体放入指定的容器中。
请回答下列问题:
(1)海带中碘元素是________(填“碘离子”“碘单质”或“碘酸盐”),步骤①
中除去海带表面的杂质一般用刷子刷净,不用水清洗,原因是____________
__________________。
(2)可说明海带中含有碘的现象有 __________________。
(3)操作⑤叫做________,操作⑥的目的是__________________ __。
【解析】海带中碘元素以碘离子的形式存在,且易溶于水,为防止碘元素的损失,
除去海带表面的杂质一般用刷子刷净,不用水清洗;实验中步骤④中加入淀粉溶
液后变蓝;步骤⑤中下层液体呈紫红色可以说明海带中含有碘。操作⑤是萃取
碘水中的碘,操作⑥是为了回收四氯化碳。
答案:(1)碘离子 防止碘元素的损失
(2)步骤④中加入淀粉溶液后变蓝,步骤⑤中下层液体呈紫红色 (3)萃取 回
收四氯化碳
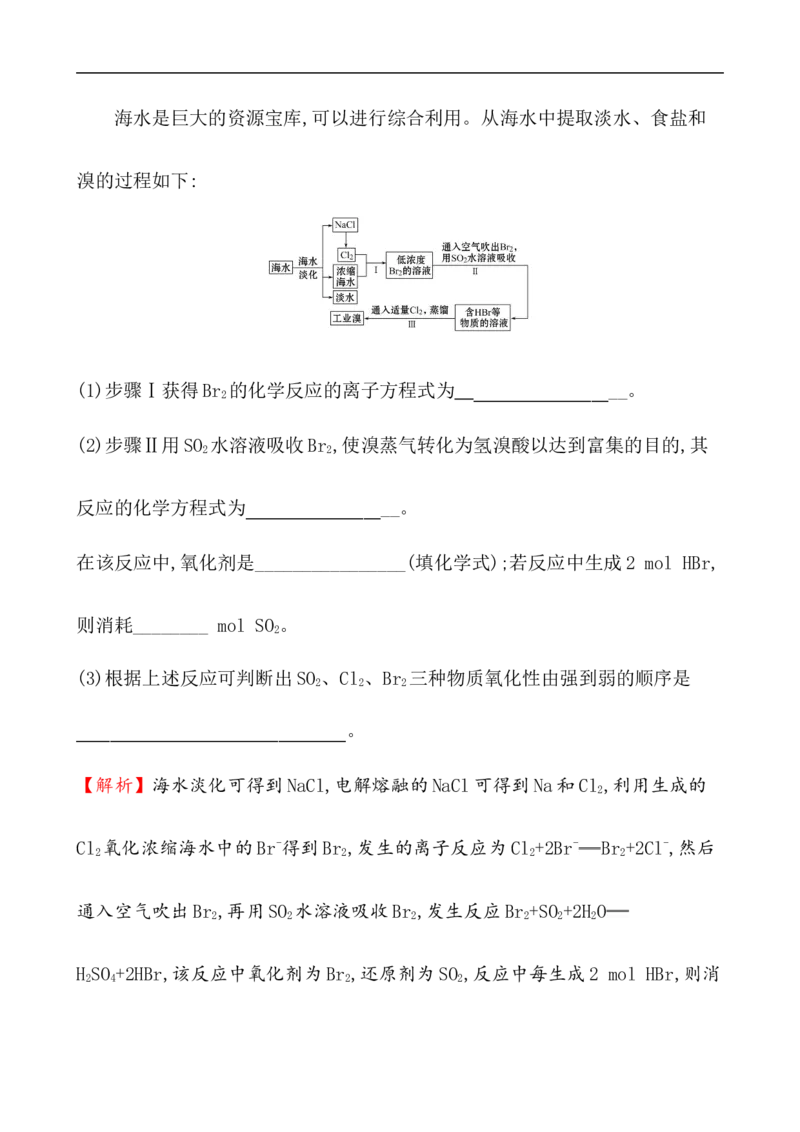
【补偿训练】海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和
溴的过程如下:
(1)步骤Ⅰ获得Br 的化学反应的离子方程式为 __________________。
2
(2)步骤Ⅱ用SO 水溶液吸收Br ,使溴蒸气转化为氢溴酸以达到富集的目的,其
2 2
反应的化学方程式为__________________。
在该反应中,氧化剂是________________(填化学式);若反应中生成2 mol HBr,
则消耗________ mol SO 。
2
(3)根据上述反应可判断出SO 、Cl 、Br 三种物质氧化性由强到弱的顺序是
2 2 2
________________________________。
【解析】海水淡化可得到NaCl,电解熔融的NaCl可得到Na和Cl ,利用生成的
2
Cl 氧化浓缩海水中的Br-得到Br ,发生的离子反应为Cl +2Br- Br +2Cl-,然后
2 2 2 2
通入空气吹出Br ,再用SO 水溶液吸收Br ,发生反应Br +SO +2H O
2 2 2 2 2 2
H SO +2HBr,该反应中氧化剂为Br ,还原剂为SO ,反应中每生成2 mol HBr,则消
2 4 2 2耗1 mol SO ,最后再向含HBr的溶液中通入适量Cl ,蒸馏即可得到Br 。通过上
2 2 2
述过程中的反应可判断出三种物质的氧化性由强到弱的顺序为Cl >Br >SO 。
2 2 2
答案:(1)Cl +2Br- 2Cl-+Br
2 2
(2)Br +SO +2H O H SO +2HBr Br 1
2 2 2 2 4 2
(3)Cl >Br >SO
2 2 2
一、选择题(本题包括1小题,共8分)
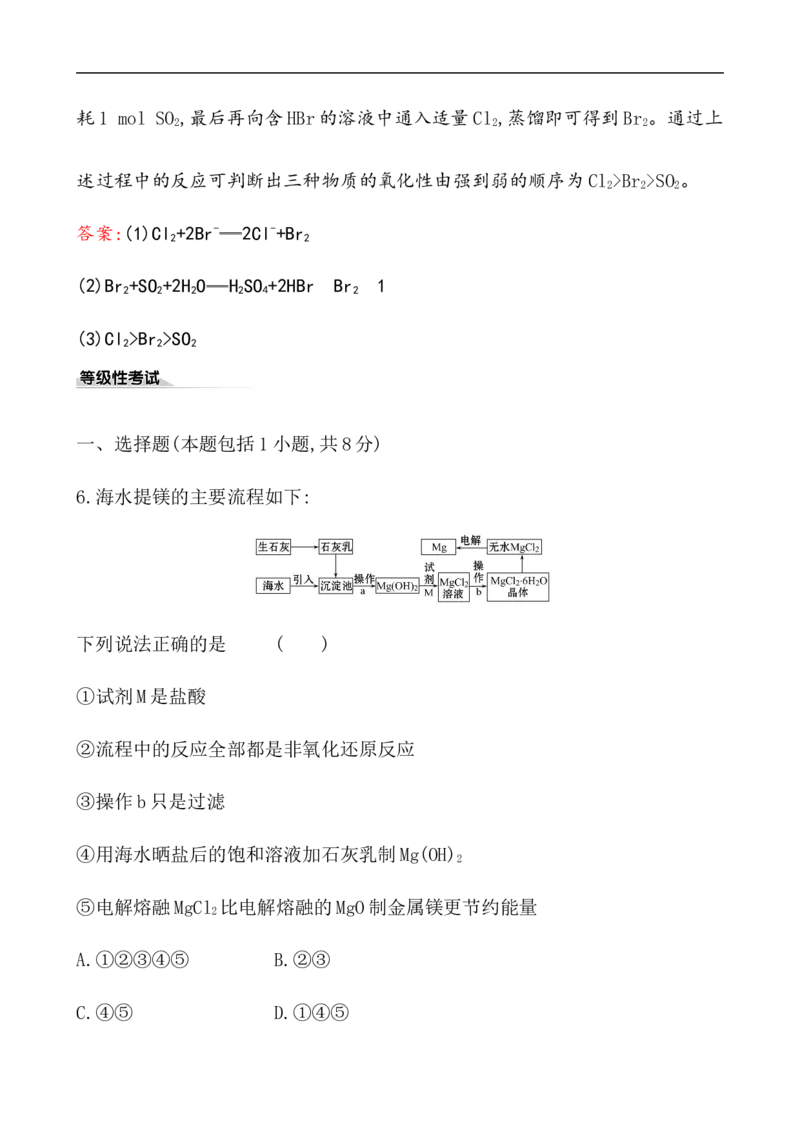
6.海水提镁的主要流程如下:
下列说法正确的是 ( )
①试剂M是盐酸
②流程中的反应全部都是非氧化还原反应
③操作b只是过滤
④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)
2
⑤电解熔融MgCl 比电解熔融的MgO制金属镁更节约能量
2
A.①②③④⑤ B.②③
C.④⑤ D.①④⑤【解析】选D。电解无水氯化镁的反应属于氧化还原反应,因此②是错误的。③
操作b应是蒸发、结晶、过滤,因此③是错误的。
二、非选择题(本题包括1小题,共12分)
7.钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO )是目前最好的白色颜料。
2
制备TiO 和Ti的原料是钛铁矿,我国的钛铁矿储量居世界首位。用含Fe O 的钛
2 2 3
铁矿(主要成分为FeTiO )制备TiO 流程如下:
3 2
(1)步骤①加Fe的目的是 _________________________________; 步骤②冷却的
目的是 __________________。
(2)上述制备TiO 的过程中,可以利用的副产物是________________;考虑成本
2
和废物综合利用因素,废液中应加入________________处理。
(3)由金红石(TiO )制取单质钛(Ti),涉及的步骤为
2
反应TiCl +2Mg 2MgCl +Ti在Ar气氛中进行的理由是 _____________。
4 2【解析】(1)分析框图知,铁最终转化成副产品绿矾,所以要将+3价Fe转化为+2
价Fe,降温减小FeSO 的溶解度,有利于绿矾结晶。
4
(2)水浸后发生的离子反应为TiO2++2H O H TiO ↓+2H+,废液主要呈酸性,所以
2 2 3
应加入CaO、CaCO 或碱。
3
(3)反应后Ti和Mg易与空气中O 、N 等反应,故应在Ar气氛中进行。
2 2
答案:(1)将Fe3+还原为Fe2+ 析出绿矾(FeSO ·7H O)
4 2
(2)绿矾(FeSO ·7H O) 生石灰(或碳酸钙、废碱)
4 2
(3)防止高温下镁或钛与O 、N 等反应
2 2