文档内容
第 2 课时 烷烃的性质
[核心素养发展目标] 1.了解烷烃的主要物理性质和化学性质,培养“变化观念与平衡思
想”的素养。2.熟练掌握甲烷的主要性质,提高“证据推理与模型认知”能力。3.认识取代
反应的概念及特点,培养“微观探析及变化观念”。
1.烷烃的物理性质
相似性 递变性(随分子中碳原子数增加)
熔、沸点 较低 逐渐升高
密度 比水小 逐渐增大
气态→液态→固态,常温常压下分子中碳原子数n≤4的
状态
烷烃为气态(常温常压下,新戊烷为气态)
溶解性 难溶于水,易溶于汽油等有机溶剂
2.化学性质
(1)稳定性:通常条件下与强酸、强碱或高锰酸钾等强氧化剂不反应。
(2)可燃性:烷烃都能燃烧。
CH 燃烧方程式:CH + 2O ――→ CO + 2H O
4 4 2 2 2
C H 燃烧方程式:C H + 5O ――→ 3CO + 4H O
3 8 3 8 2 2 2
链状烷烃燃烧通式:C H + O ――→ n CO + ( n + 1)H O
n 2n+2 2 2 2
(3)取代反应
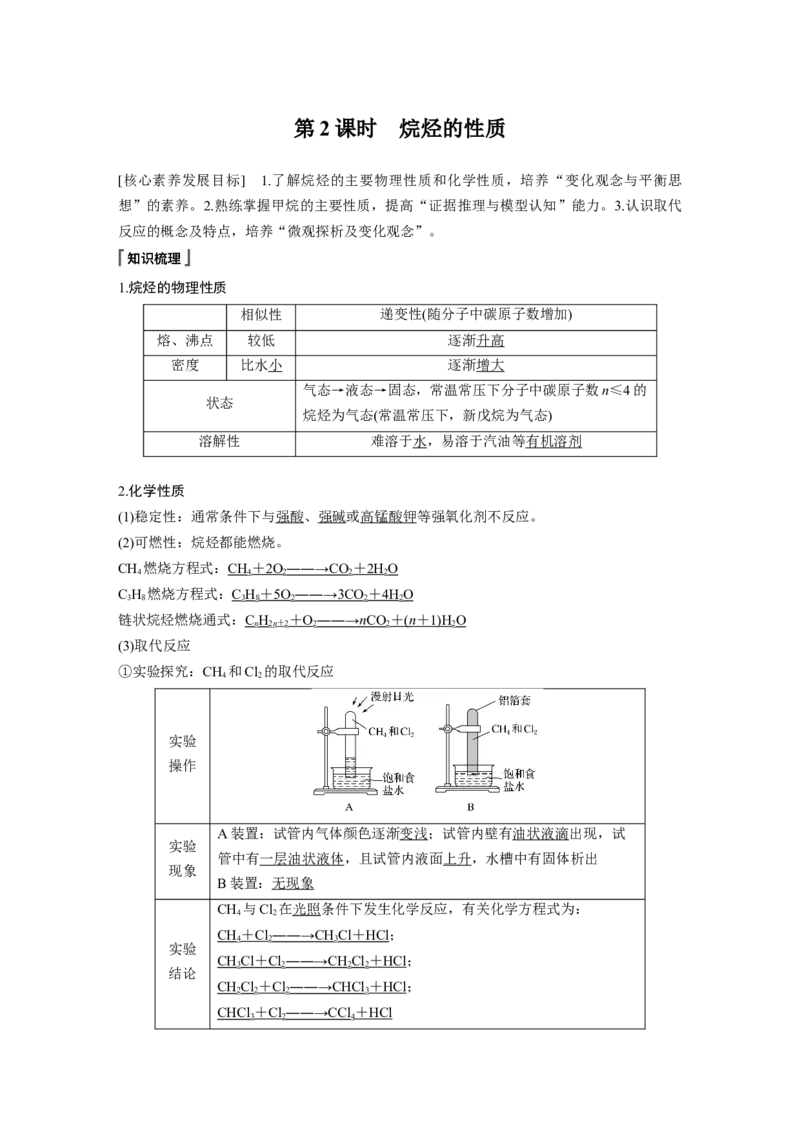
①实验探究:CH 和Cl 的取代反应
4 2
实验
操作
A装置:试管内气体颜色逐渐变浅;试管内壁有油状液滴出现,试
实验
管中有一层油状液体,且试管内液面上升,水槽中有固体析出
现象
B装置:无现象
CH 与Cl 在光照条件下发生化学反应,有关化学方程式为:
4 2
CH + C l ――→ CH Cl + HCl ;
4 2 3
实验
CH Cl + Cl ――→ CH Cl + HC l;
3 2 2 2
结论
CHCl + C l ――→ CHCl + HC l;
2 2 2 3
CHCl + C l ――→ CCl + HC l
3 2 4②甲烷的四种氯代产物的性质。
a.水溶性:CHCl、CHCl、CHCl 、CCl 均不溶于水。
3 2 2 3 4
b.状态:常温下除CHCl是气体,其余三种均为油状液体。
3
③取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应。
(4)分解反应:烷烃在较高的温度下会发生分解。
如: ――→ +
C16H34 C8H18 C8H16
(1)C H 的熔、沸点比CH 的熔、沸点高( √ )
4 10 4
(2)常温常压下,C H、C H 和C H 都呈液态( × )
3 8 4 10 6 14
提示 常温常压下,分子中碳原子数n≤4的烷烃为气态,故C H 为液态。
6 14
(3)烷烃的密度都小于水的密度( √ )
(4)乙烷也可以和氯气在光照条件下,发生取代反应( √ )
(5)CH 和Cl 按体积比1∶1混合,发生取代反应生成的产物只有两种( × )
4 2
提示 CH 和Cl 发生取代反应生成物除CHCl和HCl外,还有CHCl、CHCl 、CCl 。
4 2 3 2 2 3 4
1.CH 和Cl 发生取代反应中,产物的物质的量最多的是什么?如1 mol CH 和Cl 发生取代
4 2 4 2
反应,生成的氯代物的物质的量相等,则消耗的氯气为多少摩尔?
提示 产物中最多的为HCl,根据取代反应的特点,每取代一个氢原子,则消耗一个氯气分
子,故生成1 mol CH Cl、CHCl 、CHCl 、CCl 所消耗的氯气为 1 mol、2 mol、3 mol、4
3 2 2 3 4
mol,则1 mol CH 和Cl 反应生成等物质的量的氯代物消耗的氯气为0.25×(1+2+3+4) mol
4 2
=2.5 mol。
2.乙烷和甲烷性质相似,乙烷和氯气按体积比 1∶1混合,光照条件下能生成纯净的一氯乙烷
吗?
提示 不能,因为烷烃和氯气的反应是连锁反应,故乙烷分子中的氢原子是被氯原子逐步取
代,故产物是一氯乙烷到六氯乙烷和HCl的混合物,不能得到纯净的一氯乙烷。
烷烃(以甲烷为例)发生取代反应的有关规律
(1)反应条件:反应条件为光照,其光照为漫射光,强光直射易发生爆炸。
(2)反应物:反应物为卤素单质,如甲烷与氯水、溴水不反应,但可以与氯气、溴蒸气发生
取代反应。
(3)反应产物:虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不同,但
甲烷与氯气反应生成的产物都是CHCl、CHCl 、CHCl 和CCl 四种有机物与HCl形成的混
3 2 2 3 4
合物。反应产物中HCl的物质的量最多。
(4)反应特点①连锁反应
甲烷分子中的氢原子被氯原子逐步取代,第一步反应一旦开始,后续反应立即进行,且各步
反应可同时进行。即当n(CH)∶n(Cl )=1∶1时,并不只发生反应CH +Cl――→CHCl+
4 2 4 2 3
HCl,其他反应也在进行。
②数量关系
CH 与Cl 发生取代反应时,每有1 mol H被取代,则消耗1 mol Cl ,同时生成1 mol HCl,
4 2 2
即n(Cl )=n(H)=n(HCl)。1 mol CH 与Cl 发生取代反应,最多消耗4 mol Cl 。
2 4 2 2
1.(2019·济南月考)下列关于烷烃性质的叙述正确的是( )
A.烷烃的沸点随碳原子数增加而逐渐降低
B.烷烃易被酸性高锰酸钾溶液氧化
C.在光照条件下,烷烃易与溴水发生取代反应
D.烷烃的卤代反应很难得到纯净的产物
答案 D
解析 烷烃的沸点一般随碳原子数增加而逐渐升高,A项错误;烷烃通常情况下性质稳定,
不与酸性高锰酸钾溶液反应,B项错误;在光照条件下,烷烃只能与纯净的卤素单质发生取
代反应,不与溴水反应,C项错误;由于卤素原子取代烷烃分子中氢原子的位置和个数难以
控制,故很难得到纯净的产物,D项正确。
2.几种烷烃的沸点如下:
烷烃 甲烷 乙烷 丁烷 戊烷
沸点/℃ -162 -89 -1 36
根据以上数据推断丙烷的沸点可能是( )
A.约-40 ℃ B.低于-162 ℃
C.低于-89 ℃ D.高于36 ℃
答案 A
解析 随着碳原子数的增加,烷烃的沸点逐渐升高,丙烷的沸点应介于乙烷和丁烷的沸点之
间。
3.若甲烷与氯气以物质的量之比 1∶3 混合,在光照下得到的有机产物:① CHCl,
3
②CHCl,③CHCl ,④CCl ,其中正确的是( )
2 2 3 4
A.只有① B.只有③
C.①②③的混合物 D.①②③④的混合物
答案 D
解析 CH 和Cl 的取代反应为连锁反应,无论两者的物质的量之比为多少,其产物都是
4 2
HCl和CHCl、CHCl、CHCl 、CCl 的混合物,故选D。
3 2 2 3 44.(2018·上海静安区高一检测)将体积比为1∶4的甲烷与氯气混合于一集气瓶中,加盖后置
于光亮处,下列有关此实验的现象和结论叙述不正确的是( )
A.产物中只有四氯化碳分子是正四面体结构
B.瓶中气体的黄绿色逐渐变浅,瓶内壁有油状液滴形成
C.若日光直射,可能发生爆炸
D.生成物只有CCl 、HCl
4
答案 D
解析 A项,CCl 与CH 结构一样,为正四面体,正确。B项,CH 与Cl 反应消耗Cl ,所
4 4 4 2 2
以黄绿色逐渐变浅,反应生成的CHCl 、CHCl 、CCl 都是油状液体,正确。C项,若日光
2 2 3 4
直射,反应剧烈,放出大量的热,气体体积膨胀,可能发生爆炸,正确。D项,CH 与Cl
4 2
反应,生成CHCl、CHCl、CHCl 、CCl 和HCl,错误。
3 2 2 3 4
课时对点练
A组 基础对点练
题组一 烷烃的性质
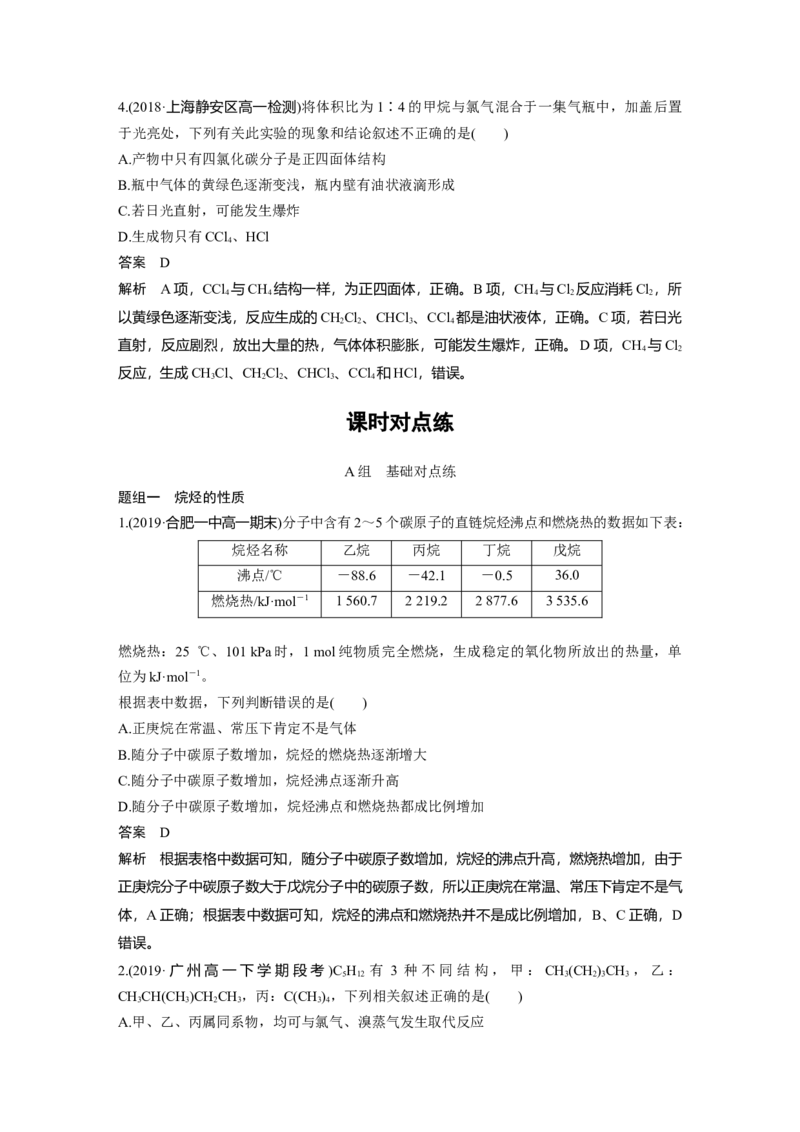
1.(2019·合肥一中高一期末)分子中含有2~5个碳原子的直链烷烃沸点和燃烧热的数据如下表:
烷烃名称 乙烷 丙烷 丁烷 戊烷
沸点/℃ -88.6 -42.1 -0.5 36.0
燃烧热/kJ·mol-1 1 560.7 2 219.2 2 877.6 3 535.6
燃烧热:25 ℃、101 kPa时,1 mol纯物质完全燃烧,生成稳定的氧化物所放出的热量,单
位为kJ·mol-1。
根据表中数据,下列判断错误的是( )
A.正庚烷在常温、常压下肯定不是气体
B.随分子中碳原子数增加,烷烃的燃烧热逐渐增大
C.随分子中碳原子数增加,烷烃沸点逐渐升高
D.随分子中碳原子数增加,烷烃沸点和燃烧热都成比例增加
答案 D
解析 根据表格中数据可知,随分子中碳原子数增加,烷烃的沸点升高,燃烧热增加,由于
正庚烷分子中碳原子数大于戊烷分子中的碳原子数,所以正庚烷在常温、常压下肯定不是气
体,A正确;根据表中数据可知,烷烃的沸点和燃烧热并不是成比例增加,B、C正确,D
错误。
2.(2019·广州高一下学期段考 )C H 有 3 种不同结构,甲:CH(CH)CH ,乙:
5 12 3 2 3 3
CHCH(CH )CHCH,丙:C(CH),下列相关叙述正确的是( )
3 3 2 3 3 4
A.甲、乙、丙属同系物,均可与氯气、溴蒸气发生取代反应B.C H 表示一种纯净物
5 12
C.甲、乙、丙中,丙的沸点最低
D.丙有4种不同沸点的一氯取代物
答案 C
解析 甲、乙、丙的结构不同,分子式相同,互为同分异构体,A错误;C H 有3种同分
5 12
异构体,所以不能表示纯净物,B错误;同分异构体中,支链越多,沸点越低,丙分子中支
链最多,所以沸点最低,C正确;丙分子中4个甲基上的氢原子是等效的,所以只有1种一
氯代物,D错误。
题组二 取代反应的理解及判断
3.(2018·山东烟台一中高一期末)下列有关甲烷的取代反应的叙述正确的是( )
A.甲烷与氯气以物质的量之比为1∶4混合时只生成CCl
4
B.甲烷与氯气反应生成的产物中CHCl的量最多
3
C.甲烷与氯气的取代反应生成的产物为混合物
D.1 mol甲烷生成CHCl 最多消耗1 mol氯气
2 2
答案 C
解析 甲烷与氯气发生取代反应生成的有机物为CHCl、CHCl 、CHCl 和CCl ,故得不到
3 2 2 3 4
纯净的CHCl,A错误,C正确;甲烷与氯气的反应中每取代 1 mol氢原子,消耗1 mol氯
3
气,生成1 mol HCl,故产物中HCl的量最多,B错误;1 mol甲烷生成CHCl 最多消耗2
2 2
mol氯气,D错误。
4.下列反应属于取代反应的是( )
①Mg+HSO ===MgSO +H↑
2 4 4 2
②NaOH+CHCOOH===CHCOONa+HO
3 3 2
③CHCH+2Br ――→CHBrCHBr+2HBr
3 3 2 2 2
④CHCl+Br ――→CHBrCl +HBr
2 2 2 2
A.②③ B.①③ C.②④ D.③④
答案 D
解析 反应①为置换反应;反应②属于复分解反应;反应③中CHCH 的2个H原子分别被
3 3
2个Br原子替代,该反应为取代反应,反应④中CHCl 中的一个H原子被一个Br原子替代
2 2
也为取代反应,故选D。
5.常温下,把体积相同的甲烷和氯气充入一个无色的集气瓶中,光照一段时间后,发现气体
的黄绿色变浅,集气瓶内壁上有油状液滴,此时集气瓶中最多含有气体物质的种数是( )
A.5种 B.6种 C.4种 D.3种
答案 C
解析 产物是气体的有CHCl、HCl,没有完全反应的CH 和Cl 也为气体,所以集气瓶中
3 4 2
最多含有4种气体,故选项C正确。题组三 烷烃燃烧及烃分子判定
6.某气态烷烃的体积是20 mL,完全燃烧时,正好消耗同温、同压下的氧气100 mL,该烷烃
的化学式是( )
A.C H B.C H
2 6 3 8
C.C H D.C H
4 10 5 12
答案 B
解析 根据题意,气态烃和消耗氧气的物质的量之比为1∶5,根据烃的燃烧通式:CH+(x
x y
+)O ――→xCO+HO,知x+=5。C H 中,x+=3.5,A错误;C H 中,x+=5,B正确;
2 2 2 2 6 3 8
C H 中,x+=6.5,C错误;C H 中,x+=8,D错误。
4 10 5 12
7.两种气态烃以一定比例混合,在105 ℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复
到原状态,所得气体总体积仍是10 L,下列混合烃中不符合此条件的是( )
A.CH、C H B.CH 、C H
4 2 4 4 3 8
C.C H、C H D.C H、C H
2 4 3 4 2 2 3 6
答案 B
解析 题述反应前后气体的体积不变,烃类物质完全燃烧的通式为 CH +(x
x y
+)O ――→xCO +HO,因为105 ℃时,生成的HO是气体,则1+(x+)=x+,解得y=
2 2 2 2
4,即氢原子平均数为4的混合烃符合题意,而CH 、C H 无论按什么比例混合,均不能使
4 3 8
氢原子平均数为4;C H 、C H 只有在体积比1∶1混合时H原子平均数才为4,CH 、C H
2 2 3 6 4 2 4
及C H、C H 以任意比混合时H原子平均数均为4。
2 4 3 4
8.(1)完全燃烧0.1 mol某烃,燃烧产物依次通过浓硫酸、浓碱溶液,实验结束后,称得浓硫
酸质量增加9 g,浓碱溶液质量增加17.6 g。该烃的化学式为________,并写出其所有可能
的 结 构 简 式 :
________________________________________________________________________。
(2)某链状烷烃的相对分子质量为128,该烷烃的化学式为________。
(3)在120 ℃和101 kPa的条件下,某气态烃和一定质量的氧气混合,点燃,完全反应后再
恢复到原来的温度时,气体体积不变,则该烃分子内的氢原子个数________(填字母)。
A.小于4 B.大于4
C.等于4 D.无法判断
答案 (1)C H CH—CH—CH—CH、 (2)C H (3)C
4 10 3 2 2 3 9 20
解析 (1)浓硫酸的作用是吸收HO,浓硫酸增加的质量为HO的质量,根据氢元素守恒,
2 2
烃中n(H)=×2=1 mol;浓碱溶液吸收的是CO ,浓碱溶液增加的质量为CO 的质量,根据
2 2
碳元素守恒,烃中n(C)==0.4 mol,因此1 mol该烃中含C的物质的量为4 mol,含H的物
质的量为10 mol,即该烃的分子式为C H ,其同分异构体为正丁烷和异丁烷,相应的结构
4 10简式分别是CH—CH—CH—CH、 。
3 2 2 3
(2)根据链状烷烃的通式C H ,相对分子质量为128,即14n+2=128,解得n=9,故该
n 2n+2
烷烃的分子式为C H 。
9 20
(3)烃燃烧的通式:CH+(x+)O ――→xCO +HO,温度高于100 ℃时,水以气态形式存
x y 2 2 2
在,反应前后气体体积不变,即 1+x+=x+,解得y=4,即该烃分子内的氢原子个数为
4。
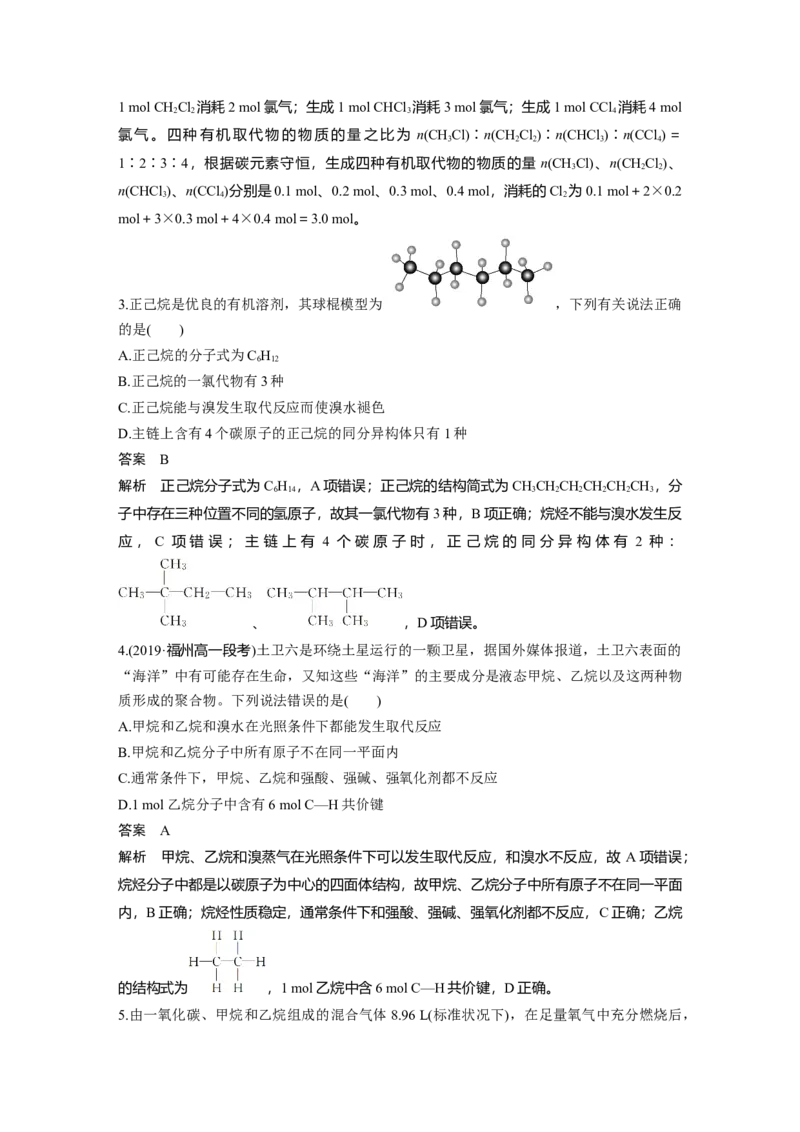
9.(2019·上海高一期中)某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。
请填写下列空白:
[实验一]用如图所示装置,收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一
段水柱,认为有氯化氢生成。
(1)该反应的反应类型为_____________________________________________________。
(2)该反应的化学方程式为(只写第一步)_________________________________________。
(3)水槽中盛放的液体应为________(填字母)。
A.水 B.饱和石灰水
C.饱和食盐水 D.饱和NaHCO 溶液
3
(4)该实验的实验现象为_______________、______________、试管壁上出现油状液滴。
(5)该油状液滴中含有的有机产物共有________种。
[实验二]收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO 溶液,看到有白色沉
3
淀生成,认为甲烷与氯气反应有氯化氢生成。
(6)你认为该实验设计得出的结论是否正确:_______________________________________;
若不正确,理由是________________________________________________________。
[实验三]步骤一:收集半试管氯气,加入10 mL蒸馏水,充分振荡,采用DIS系统的pH传
感器测溶液的pH(下同),测得pH=3.26;
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,
加入10 mL蒸馏水,充分振荡,测得pH=1.00。
(7)判断该反应中有氯化氢生成的依据是_____________________________________。
答案 (1)取代反应
(2)CH +Cl――→CHCl+HCl
4 2 3
(3)C
(4)量筒内液面上升 黄绿色逐渐变浅(5)3
(6)错误 氯气中滴加AgNO 溶液也会产生白色沉淀
3
(7)步骤二测得的pH比步骤一测得的pH低
解析 (1)甲烷与氯气在光照条件下发生取代反应。
(2)甲烷和氯气发生取代反应的第一步化学方程式为CH+Cl――→CHCl+HCl。
4 2 3
(3)因为氯气可溶于水,且能与水发生反应,因此水槽中不能盛放 HO,A错误;氯气与饱
2
和石灰水发生反应,水槽中不能盛放饱和石灰水,B错误;饱和食盐水可抑制氯气的溶解,
且饱和食盐水能吸收甲烷与氯气反应生成的HCl,使量筒中气体压强减小,量筒中的液面上
升,C正确;氯气与饱和NaHCO 溶液发生反应,且有杂质气体CO 产生,D错误。
3 2
(4)甲烷与氯气发生反应消耗氯气,故量筒内黄绿色变浅,因为生成物中 CHCl 、CHCl 、
2 2 3
CCl 为液体,量筒内壁上出现油状液滴,且HCl溶于饱和食盐水,造成量筒中气体压强减
4
小,即量筒中液面上升。
(5)甲烷与氯气反应的有机产物为CHCl、CHCl 、CHCl 、CCl ,其中CHCl为气态,另外
3 2 2 3 4 3
3种为液态,因此油状液滴中含有的有机物为CHCl、CHCl 、CCl ,共3种。
2 2 3 4
(6)氯气能与AgNO 溶液中的水反应,产生Cl-,与Ag+结合产生白色沉淀,因此该实验得
3
出的结论错误。
(7)根据实验,步骤二测得的pH小于步骤一测得的pH,说明c(H+)增大,即甲烷与氯气反应
产生了HCl。
B组 综合强化练
1.(2019·济宁一中高一月考)下列性质不属于甲烷性质的是( )
A.完全燃烧时生成二氧化碳和水
B.常温常压下能溶于水
C.光照下能与卤素单质发生取代反应
D.通常情况下,与强酸、强碱和强氧化剂不反应
答案 B
解析 常温常压下,甲烷是一种极难溶于水的气体;甲烷的化学性质稳定,与强酸、强碱、
强氧化剂等都不反应,但甲烷可燃,完全燃烧时生成二氧化碳和水,在光照条件下能与卤素
单质发生取代反应,B项符合题意。
2.(2018·江苏常州期中)在光照条件下,CH 与Cl 能发生取代反应。若1 mol CH 与Cl 反应,
4 2 4 2
待 反 应 完 成 后 测 得 四 种 有 机 取 代 物 的 物 质 的 量 之 比 为
n(CHCl)∶n(CHCl)∶n(CHCl )∶n(CCl )=1∶2∶3∶4,则消耗Cl 的物质的量为( )
3 2 2 3 4 2
A.1.0 mol B.2.0 mol
C.3.0 mol D.4.0 mol
答案 C
解析 在光照条件下,CH 与Cl 发生取代反应时,生成1 mol CH Cl消耗1 mol氯气;生成
4 2 31 mol CH Cl 消耗2 mol氯气;生成1 mol CHCl 消耗3 mol氯气;生成1 mol CCl 消耗4 mol
2 2 3 4
氯气。四种有机取代物的物质的量之比为 n(CHCl)∶n(CHCl)∶n(CHCl )∶n(CCl )=
3 2 2 3 4
1∶2∶3∶4,根据碳元素守恒,生成四种有机取代物的物质的量 n(CHCl)、n(CHCl)、
3 2 2
n(CHCl )、n(CCl )分别是0.1 mol、0.2 mol、0.3 mol、0.4 mol,消耗的Cl 为0.1 mol+2×0.2
3 4 2
mol+3×0.3 mol+4×0.4 mol=3.0 mol。
3.正己烷是优良的有机溶剂,其球棍模型为 ,下列有关说法正确
的是( )
A.正己烷的分子式为C H
6 12
B.正己烷的一氯代物有3种
C.正己烷能与溴发生取代反应而使溴水褪色
D.主链上含有4个碳原子的正己烷的同分异构体只有1种
答案 B
解析 正己烷分子式为C H ,A项错误;正己烷的结构简式为CHCHCHCHCHCH ,分
6 14 3 2 2 2 2 3
子中存在三种位置不同的氢原子,故其一氯代物有3种,B项正确;烷烃不能与溴水发生反
应 , C 项 错 误 ; 主 链 上 有 4 个 碳 原 子 时 , 正 己 烷 的 同 分 异 构 体 有 2 种 :
、 ,D项错误。
4.(2019·福州高一段考)土卫六是环绕土星运行的一颗卫星,据国外媒体报道,土卫六表面的
“海洋”中有可能存在生命,又知这些“海洋”的主要成分是液态甲烷、乙烷以及这两种物
质形成的聚合物。下列说法错误的是( )
A.甲烷和乙烷和溴水在光照条件下都能发生取代反应
B.甲烷和乙烷分子中所有原子不在同一平面内
C.通常条件下,甲烷、乙烷和强酸、强碱、强氧化剂都不反应
D.1 mol乙烷分子中含有6 mol C—H共价键
答案 A
解析 甲烷、乙烷和溴蒸气在光照条件下可以发生取代反应,和溴水不反应,故 A项错误;
烷烃分子中都是以碳原子为中心的四面体结构,故甲烷、乙烷分子中所有原子不在同一平面
内,B正确;烷烃性质稳定,通常条件下和强酸、强碱、强氧化剂都不反应,C正确;乙烷
的结构式为 ,1 mol乙烷中含6 mol C—H共价键,D正确。
5.由一氧化碳、甲烷和乙烷组成的混合气体8.96 L(标准状况下),在足量氧气中充分燃烧后,生成的气体先通过足量浓硫酸,再通过足量氢氧化钠溶液,测知氢氧化钠溶液质量增加26.4
g,则原混合气体中乙烷的物质的量( )
A.等于0.1 mol
B.大于或等于0.2 mol,小于0.3 mol
C.等于0.2 mol
D.大于0.1 mol,小于0.3 mol
答案 C
解析 混合气体的物质的量为=0.4 mol,浓硫酸吸收水、NaOH溶液吸收二氧化碳,故NaOH
溶液增加的26.4 g为二氧化碳的质量,二氧化碳的物质的量为=0.6 mol。设一氧化碳、甲烷
的总物质的量为x mol,乙烷的物质的量为y mol,则x mol+y mol=0.4 mol,x mol+2y
mol=0.6 mol,解得x=y=0.2,则原混合气体中乙烷的物质的量为0.2 mol,C正确。
6.(2018·河南平顶山月考)下列烷烃在光照下与氯气发生取代反应,生成的一氯代烃只有一种
的是( )
A.CHCHCHCH B.CH CH(CH )
3 2 2 3 3 3 2
C.CH C(CH) D.(CH)CHCH CH
3 3 3 3 2 2 3
答案 C
解析 此题是同分异构体的一种考查形式,解题关键是清楚每一种烷烃中有几种等效氢。同
一个碳上的氢为等效氢,对称碳上的氢为等效氢,同一个碳所连甲基上的氢为等效氢。等效
氢被取代得到的物质为同种物质。A、B项中有2种氢,C项中有1种氢,D项中有4种氢,
故C项符合题意。
7.“可燃冰”是天然气与水作用形成的晶体物质,主要存在于冻土层和海底大陆架中,其结
构如图所示,请回答下列问题:
(1)下列有关“可燃冰”的说法不正确的是________(填字母)。
A.“可燃冰”是混合物
B.“可燃冰”释放的甲烷为烷烃
C.“可燃冰”将成为人类的后续能源
D.甲烷和溴蒸气在光照条件下可发生取代反应,生成的一溴甲烷为正四面体结构
(2)下图是某同学利用日常用品注射器设计的简易实验装置。加热分离出可燃冰中的甲烷,
将10 mL甲烷注入甲管中,同温、同压下向乙管中注入 50 mL Cl ,将乙管中气体推入甲管,
2
用日光照射甲管一段时间,气体在甲管中反应。①下列是某同学预测的实验现象,其中正确的是______(填字母)。
A.气体最终变为无色
B.实验过程中,甲管活塞向内移动
C.甲管内壁有油状液滴产生
D.产生火花
②甲管中发生的化学反应类型为___________________________________________。
③反应后,甲管中剩余气体最好用________(填字母)吸收。
A.水 B.氢氧化钠溶液
C.硝酸银溶液 D.饱和食盐水
答案 (1)AD
(2)①BC ②取代反应 ③B
解析 (1)CH 和HO结合形成可燃冰,为纯净物,故A错误;“可燃冰”不稳定,可释放
4 2
出甲烷,甲烷属于烷烃,B正确;可燃冰释放出的甲烷是一种清洁能源,将成为人类的后续
能源,C正确;甲烷和溴蒸气生成的一溴甲烷结构为四面体,但不为正四面体,D错误。
(2)在光照下,甲烷与氯气发生多步取代反应:CH +Cl――→CHCl+HCl,CHCl+
4 2 3 3
Cl――→CHCl +HCl,CHCl +Cl――→CHCl +HCl,CHCl +Cl――→CCl +HCl。①
2 2 2 2 2 2 3 3 2 4
理论上,甲烷与氯气体积比为1∶4时二者恰好完全反应,而该针管里氯气与甲烷体积比为
5∶1>4∶1,说明氯气过量,最终气体中仍有氯气。该反应进行缓慢,不会产生火花。产物
中只有氯化氢和一氯甲烷为气体,其他为油状液体,所以气体的总物质的量减小,内部压强
减小,甲管活塞向内移动。②甲烷分子中的四个氢原子可被氯原子逐一取代,故甲管中发生
的是取代反应。③剩余气体中含有氯气和氯化氢,最好用氢氧化钠溶液吸收。
8.如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1∶4)的混合气体,假定
氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气混合气体的装置放置在有光亮的地方,
让混合气体缓慢地反应一段时间。
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:
__________________
______________________________________________________。
(2)若题目中甲烷与氯气体积之比为1∶1,则得到的产物为________(填字母,下同)。
A.CHCl HCl
3
B.CCl HCl
4
C.CH Cl CHCl
3 2 2
D.CHCl CHCl CHCl CCl HCl
3 2 2 3 4(3)经过几个小时的反应后,U形管右端的水柱变化是________。
A.升高 B.降低
C.不变 D.无法确定
答案 (1)CH +4Cl――→CCl +4HCl (2)D (3)B
4 2 4
解析 (1)因Cl 足量,若充分反应,则CH 中的四个H原子可完全被取代,生成CCl 和
2 4 4
HCl:CH+4Cl――→CCl +4HCl。
4 2 4
(2)甲烷与氯气的取代反应,是四步反应同时发生,故得到四种氯代产物和HCl。
(3)甲烷和氯气在光照的条件下发生取代反应生成油状液滴,U形管左侧生成的氯化氢气体
易溶于水。压强减小,U形管右端液面下降,左端液面上升。