文档内容
[复习目标] 1.掌握常见物质、离子的检验与鉴别。2.掌握简单实验方案的设计与评价。
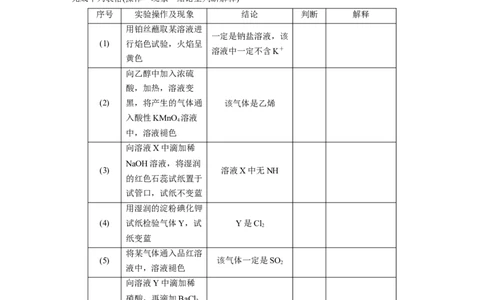
完成下列表格(操作—现象—结论型判断解释)
序号 实验操作及现象 结论 判断 解释
用铂丝蘸取某溶液进
一定是钠盐溶液,该
(1) 行焰色试验,火焰呈
溶液中一定不含K+
黄色
向乙醇中加入浓硫
酸,加热,溶液变
(2) 黑,将产生的气体通 该气体是乙烯
入酸性KMnO 溶液
4
中,溶液褪色
向溶液X中滴加稀
NaOH溶液,将湿润
(3) 溶液X中无NH
的红色石蕊试纸置于
试管口,试纸不变蓝
用湿润的淀粉碘化钾
(4) 试纸检验气体Y,试 Y是Cl
2
纸变蓝
将某气体通入品红溶
(5) 该气体一定是SO
2
液中,溶液褪色
向溶液Y中滴加稀
硝酸,再滴加BaCl
2
(6) Y中一定含有SO
溶液,有白色沉淀生
成
往CH===CHCHO
2
该有机物中含有碳碳
(7) 中滴入酸性KMnO
4
双键
溶液,溶液褪色
蘸有浓氨水的玻璃棒
(8) 靠近溶液X有白烟 X一定是浓盐酸
产生向某溶液中滴加
KSCN溶液,溶液不 该溶液中一定含Fe2
(9)
变色,滴加氯水后溶 +
液显红色
将SO 气体通入
2
(10) Ba(NO ) 溶液中,生 该沉淀一定是BaSO
3 2 3
成白色沉淀
将SO 气体通入
2
(11) BaCl 溶液中,无明 SO 和BaCl 不反应
2 2 2
显现象
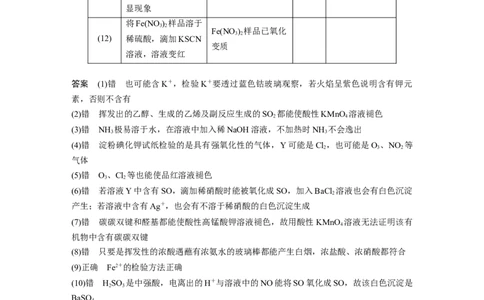
将Fe(NO ) 样品溶于
3 2
Fe(NO ) 样品已氧化
3 2
(12) 稀硫酸,滴加KSCN
变质
溶液,溶液变红
答案 (1)错 也可能含K+,检验K+要透过蓝色钴玻璃观察,若火焰呈紫色说明含有钾元
素,否则不含有
(2)错 挥发出的乙醇、生成的乙烯及副反应生成的SO 都能使酸性KMnO 溶液褪色
2 4
(3)错 NH 极易溶于水,在溶液中加入稀NaOH溶液,不加热时NH 不会逸出
3 3
(4)错 淀粉碘化钾试纸检验的是具有强氧化性的气体,Y可能是Cl ,也可能是O 、NO 等
2 3 2
气体
(5)错 O、Cl 等也能使品红溶液褪色
3 2
(6)错 若溶液Y中含有SO,滴加稀硝酸时能被氧化成SO,加入BaCl 溶液也会有白色沉淀
2
产生;若溶液中含有Ag+,也会有不溶于稀硝酸的白色沉淀生成
(7)错 碳碳双键和醛基都能使酸性高锰酸钾溶液褪色,故用酸性KMnO 溶液无法证明该有
4
机物中含有碳碳双键
(8)错 只要是挥发性的浓酸遇蘸有浓氨水的玻璃棒都能产生白烟,浓盐酸、浓硝酸都符合
(9)正确 Fe2+的检验方法正确
(10)错 HSO 是中强酸,电离出的H+与溶液中的NO能将SO氧化成SO,故该白色沉淀是
2 3
BaSO
4
(11)正确 HSO 是中强酸,而HCl是强酸,不能由中强酸制强酸
2 3
(12)错 在Fe(NO ) 中加入稀硫酸后,Fe2+能被H+、NO(两者同时存在相当于HNO)氧化成
3 2 3
Fe3+而干扰实验
1.常见气体的检验
气体 检验方法或思路
O 使带火星的木条复燃
2NO 在空气中立即变成红棕色
点燃时火焰呈淡蓝色,燃烧产物可使澄清石灰水变浑浊;或将气体通过灼
CO
热的CuO,CuO由黑色变成红色,且气体产物可使澄清石灰水变浑浊
无色无味的气体且能使澄清石灰水变浑浊,继续通入又可变澄清;使燃着
CO
2
的木条熄灭
无色有刺激性气味的气体且能使品红溶液褪色,加热后又恢复红色;使酸
SO
2
性高锰酸钾溶液褪色
通入水中得到无色溶液并产生气泡,液面上方有红棕色气体产生,水溶液
NO
2
显酸性;使湿润的淀粉-KI试纸变蓝
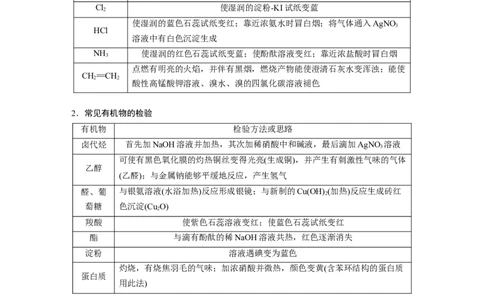
Cl 使湿润的淀粉-KI试纸变蓝
2
使湿润的蓝色石蕊试纸变红;靠近浓氨水时冒白烟;将气体通入AgNO
3
HCl
溶液中有白色沉淀生成
NH 使湿润的红色石蕊试纸变蓝;使酚酞溶液变红;靠近浓盐酸时冒白烟
3
点燃有明亮的火焰,并伴有黑烟,燃烧产物能使澄清石灰水变浑浊;能使
CH==CH
2 2
酸性高锰酸钾溶液、溴水、溴的四氯化碳溶液褪色
2.常见有机物的检验
有机物 检验方法或思路
卤代烃 首先加NaOH溶液并加热,其次加稀硝酸中和碱液,最后滴加AgNO 溶液
3
可使有黑色氧化膜的灼热铜丝变得光亮(生成铜),并产生有刺激性气味的气体
乙醇
(乙醛);与金属钠能够平缓地反应,产生氢气
醛、葡 与银氨溶液(水浴加热)反应形成银镜;与新制的Cu(OH) (加热)反应生成砖红
2
萄糖 色沉淀(Cu O)
2
羧酸 使紫色石蕊溶液变红;使蓝色石蕊试纸变红
酯 与滴有酚酞的稀NaOH溶液共热,红色逐渐消失
淀粉 溶液遇碘变为蓝色
灼烧,有烧焦羽毛的气味;加浓硝酸并微热,颜色变黄(含苯环结构的蛋白质
蛋白质
用此法)
角度一 物质的检验
1.(2020·天津,6)检验下列物质所选用的试剂正确的是( )
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
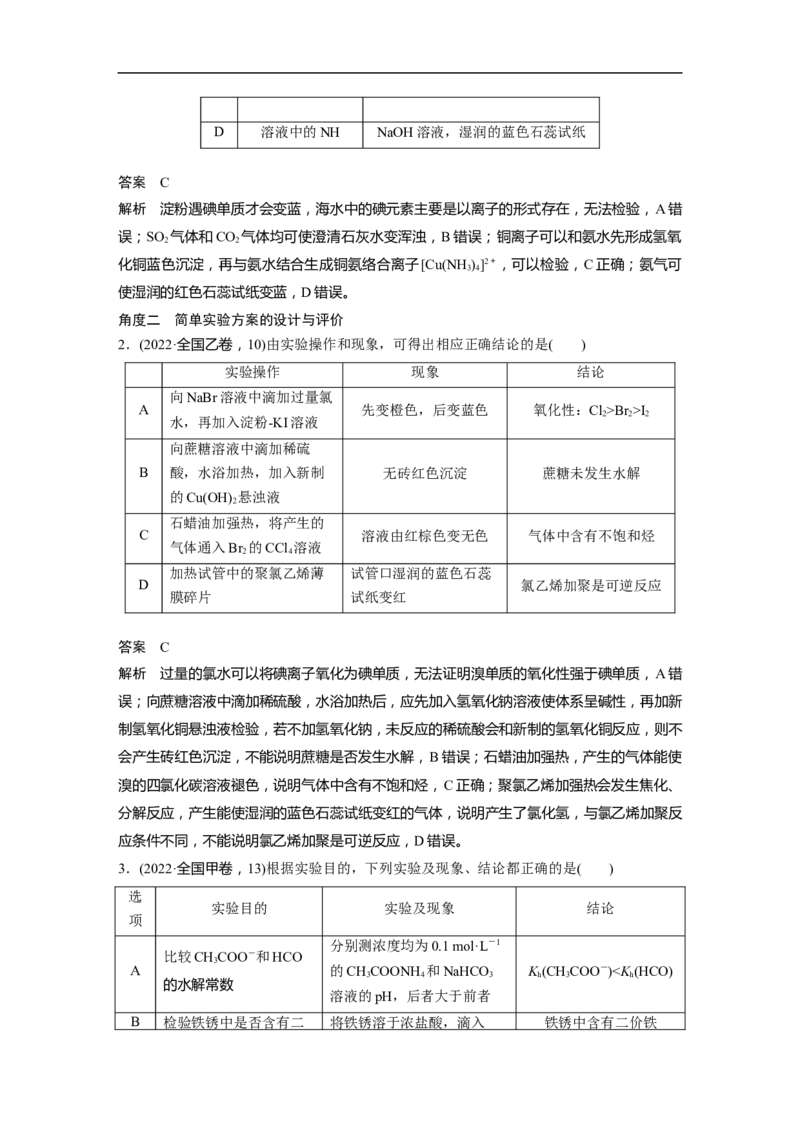
C 溶液中的Cu2+ 氨水D 溶液中的NH NaOH溶液,湿润的蓝色石蕊试纸
答案 C
解析 淀粉遇碘单质才会变蓝,海水中的碘元素主要是以离子的形式存在,无法检验,A错
误;SO 气体和CO 气体均可使澄清石灰水变浑浊,B错误;铜离子可以和氨水先形成氢氧
2 2
化铜蓝色沉淀,再与氨水结合生成铜氨络合离子[Cu(NH )]2+,可以检验,C正确;氨气可
3 4
使湿润的红色石蕊试纸变蓝,D错误。
角度二 简单实验方案的设计与评价
2.(2022·全国乙卷,10)由实验操作和现象,可得出相应正确结论的是( )
实验操作 现象 结论
向NaBr溶液中滴加过量氯
A 先变橙色,后变蓝色 氧化性:Cl>Br >I
2 2 2
水,再加入淀粉-KI溶液
向蔗糖溶液中滴加稀硫
B 酸,水浴加热,加入新制 无砖红色沉淀 蔗糖未发生水解
的Cu(OH) 悬浊液
2
石蜡油加强热,将产生的
C 溶液由红棕色变无色 气体中含有不饱和烃
气体通入Br 的CCl 溶液
2 4
加热试管中的聚氯乙烯薄 试管口湿润的蓝色石蕊
D 氯乙烯加聚是可逆反应
膜碎片 试纸变红
答案 C
解析 过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质,A错
误;向蔗糖溶液中滴加稀硫酸,水浴加热后,应先加入氢氧化钠溶液使体系呈碱性,再加新
制氢氧化铜悬浊液检验,若不加氢氧化钠,未反应的稀硫酸会和新制的氢氧化铜反应,则不
会产生砖红色沉淀,不能说明蔗糖是否发生水解,B错误;石蜡油加强热,产生的气体能使
溴的四氯化碳溶液褪色,说明气体中含有不饱和烃,C正确;聚氯乙烯加强热会发生焦化、
分解反应,产生能使湿润的蓝色石蕊试纸变红的气体,说明产生了氯化氢,与氯乙烯加聚反
应条件不同,不能说明氯乙烯加聚是可逆反应,D错误。
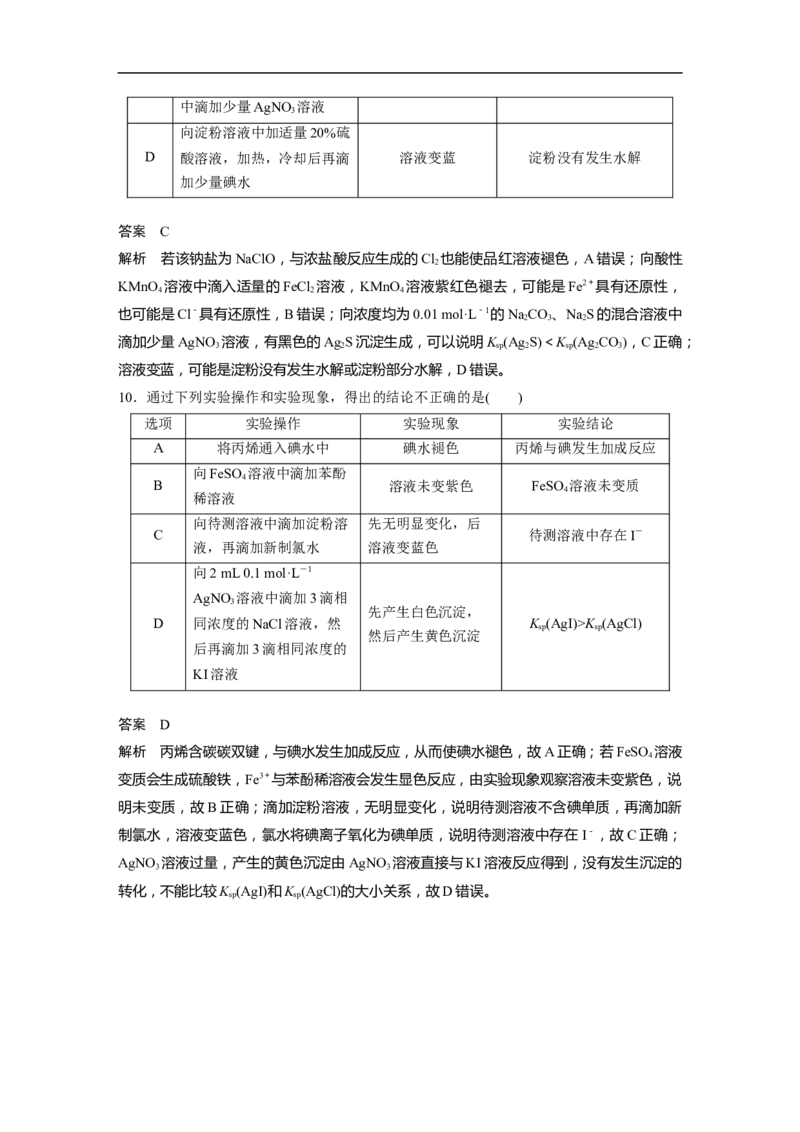
3.(2022·全国甲卷,13)根据实验目的,下列实验及现象、结论都正确的是( )
选
实验目的 实验及现象 结论
项
分别测浓度均为0.1 mol·L-1
比较CHCOO-和HCO
3
A 的CHCOONH 和NaHCO K (CHCOO-)K (AgCl)
sp sp
然后产生黄色沉淀
后再滴加3滴相同浓度的
KI溶液
答案 D
解析 丙烯含碳碳双键,与碘水发生加成反应,从而使碘水褪色,故A正确;若FeSO 溶液
4
变质会生成硫酸铁,Fe3+与苯酚稀溶液会发生显色反应,由实验现象观察溶液未变紫色,说
明未变质,故B正确;滴加淀粉溶液,无明显变化,说明待测溶液不含碘单质,再滴加新
制氯水,溶液变蓝色,氯水将碘离子氧化为碘单质,说明待测溶液中存在 I-,故C正确;
AgNO 溶液过量,产生的黄色沉淀由AgNO 溶液直接与KI溶液反应得到,没有发生沉淀的
3 3
转化,不能比较K (AgI)和K (AgCl)的大小关系,故D错误。
sp sp