文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题12
1.常温下,下列各组离子在指定环境中能大量共存的是
A. 能使石蕊试液变红的溶液:NH、K+、I-、CrO
B. 在FeCl 溶液中:Na+、Mg2+、SCN-、SO
3
C. 水电离出的c(H+)=1×10-10的溶液中:Na+、K+、NO SO
、
D. c(OH-)<mol·L-1的溶液中:Ca2+、NH、AlO、Cl-
2. 25℃,下列指定条件下离子能够大量共存的是
A.酸性条件下,Fe3+可以大量存在的体系:NO SO NH、Br-
、 2 、
B.pOH=12的溶液[pOH=lgc(OH-)]:Fe2+、NH、Br-、Cl-
C.等浓度醋酸溶液和醋酸钠溶液等体积混合时:Cl-、HCO NH、ClO-
、
D.惰性电极电解时,一开始就能产生氧气的溶液:SO HCO Na+、OH-
、 、
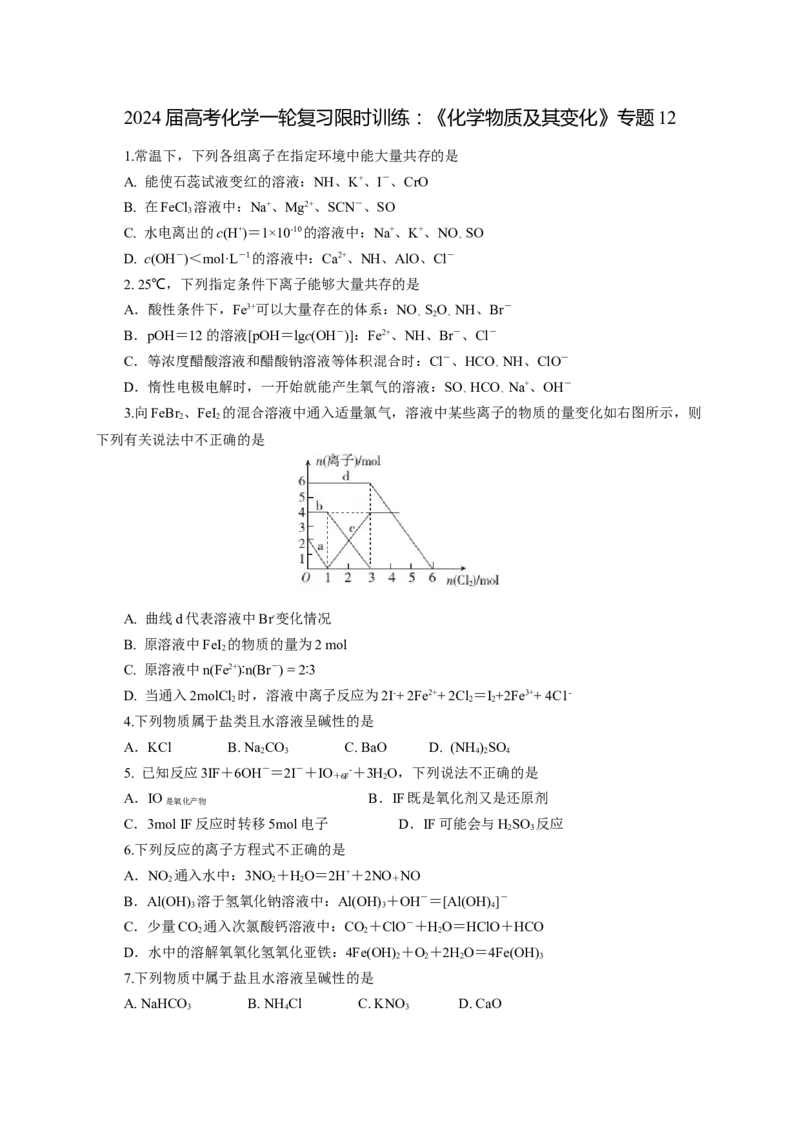
3.向FeBr 、FeI 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如右图所示,则
2 2
下列有关说法中不正确的是
A. 曲线d代表溶液中Br-变化情况
B. 原溶液中FeI 的物质的量为2 mol
2
C. 原溶液中n(Fe2+)∶n(Br-) = 2∶3
D. 当通入2molCl 时,溶液中离子反应为2I-+ 2Fe2++ 2Cl =I+2Fe3++ 4C1-
2 2 2
4.下列物质属于盐类且水溶液呈碱性的是
A.KCl B. Na CO C. BaO D. (NH )SO
2 3 4 2 4
5. 已知反应3IF+6OH-=2I-+IO -+3HO,下列说法不正确的是
+6F 2
A.IO B.IF既是氧化剂又是还原剂
是氧化产物
C.3mol IF反应时转移5mol电子 D.IF可能会与HSO 反应
2 3
6.下列反应的离子方程式不正确的是
A.NO 通入水中:3NO +HO=2H++2NO NO
2 2 2 +
B.Al(OH) 溶于氢氧化钠溶液中:Al(OH) +OH-=[Al(OH) ]-
3 3 4
C.少量CO 通入次氯酸钙溶液中:CO+ClO-+HO=HClO+HCO
2 2 2
D.水中的溶解氧氧化氢氧化亚铁:4Fe(OH) +O+2HO=4Fe(OH)
2 2 2 3
7.下列物质中属于盐且水溶液呈碱性的是
A. NaHCO B. NH Cl C. KNO D. CaO
3 4 38.KNO 和NH Cl混合加热可发生反应2KNO+2NH Cl===2N↑+O↑+2KCl+4HO,下列说
3 4 3 4 2 2 2
法正确的是
A. 还原产物是N 和O
2 2
B. 实验室加热可用氯化铵制备NH
3
C. KNO 既是氧化剂又是还原剂
3
D. 每生成1 mol N ,反应总共转移6 mol电子
2
9.下列反应的方程式不正确的是
A. 将碳酸氢钙溶液与过量的澄清石灰水混合:HCO Ca2++OH-=CaCO ↓+HO
+ 3 2
B. 将稀硫酸加入硫代硫酸钠溶液:SO SO+4H+=2SO ↑+S↓+2HO
2 + 2 2
C. CuSO 溶液与闪锌矿(ZnS)反应生成铜蓝(CuS):Cu2+(aq)+ZnS(s)=Zn+(aq)+CuS(s)
4
D. 向银氨溶液中滴加乙醛,水浴加热,析出光亮银镜:CHCHO+
3
2Ag(NH)OH===CHCOONH+2Ag↓+3NH +HO
3 2 3 4 3 2
10. 含有下列各组离子的溶液中,通入(或加入)过量的某种物质后仍能太量共存的是
A. 通入SO 气体,H+、Ba2+、Fe3+、NO
2
B. 通入NH 气体,Mg2+、K+、Cl-、NH
3
C. 通入CO 气体,H+、NH、Ba2+、Cl-
2
D. 加入AlCl 溶液,K+、Na+、I-、S2-
3
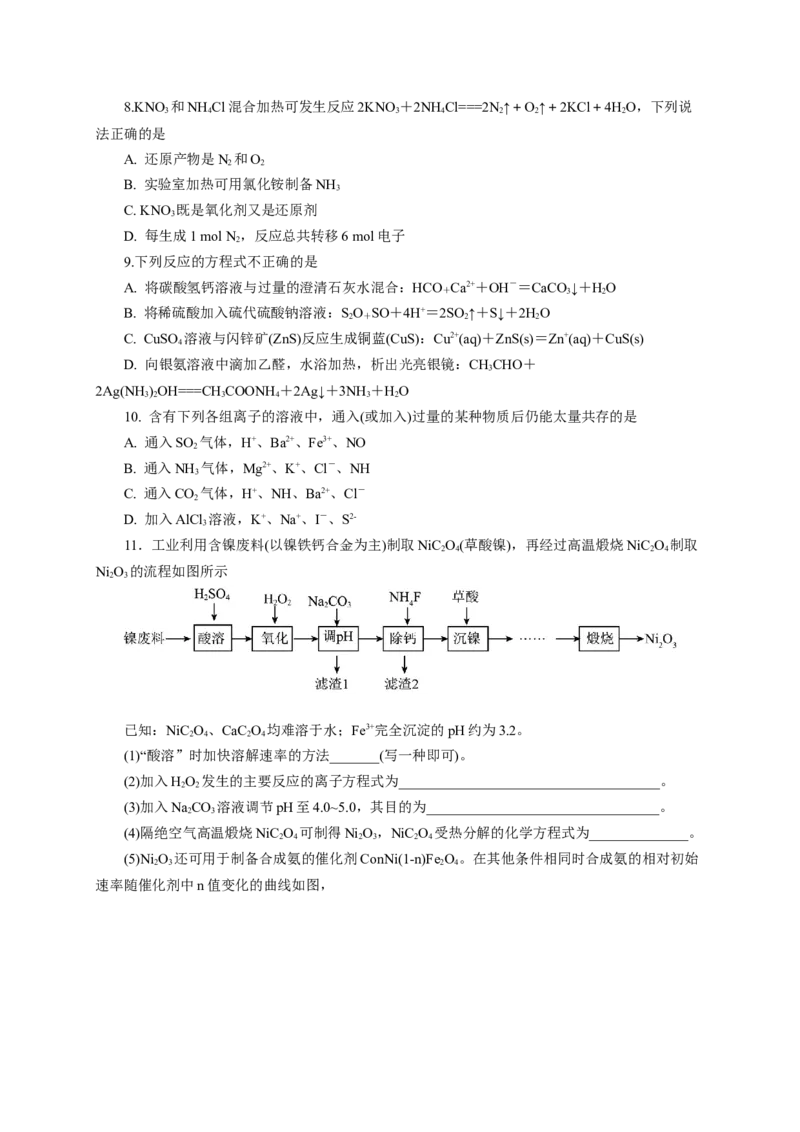
11.工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),再经过高温煅烧NiC O 制取
2 4 2 4
Ni O 的流程如图所示
2 3
已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH约为3.2。
2 4 2 4
(1)“酸溶”时加快溶解速率的方法_______(写一种即可)。
(2)加入HO 发生的主要反应的离子方程式为_____________________________________。
2 2
(3)加入NaCO 溶液调节pH至4.0~5.0,其目的为_________________________________。
2 3
(4)隔绝空气高温煅烧NiC O 可制得Ni O,NiC O 受热分解的化学方程式为______________。
2 4 2 3 2 4
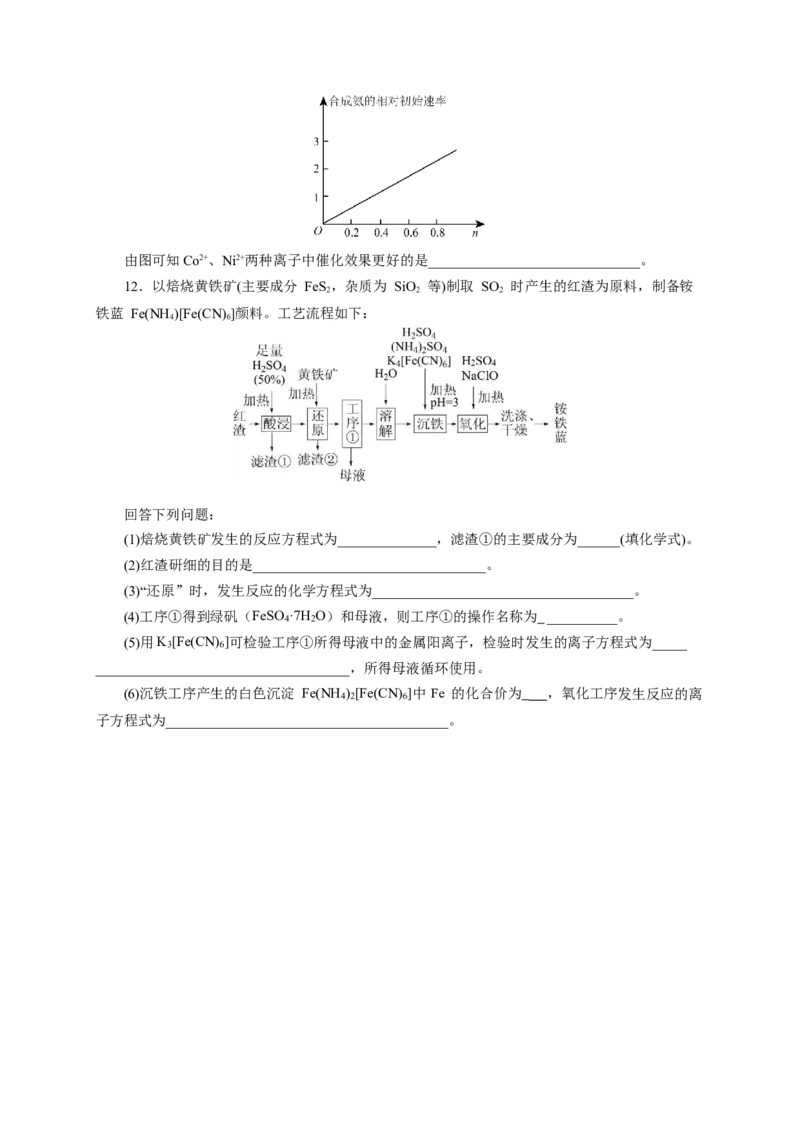
(5)NiO 还可用于制备合成氨的催化剂ConNi(1-n)Fe O。在其他条件相同时合成氨的相对初始
2 3 2 4
速率随催化剂中n值变化的曲线如图,由图可知Co2+、Ni2+两种离子中催化效果更好的是______________________________。
12.以焙烧黄铁矿(主要成分 FeS,杂质为 SiO 等)制取 SO 时产生的红渣为原料,制备铵
2 2 2
铁蓝 Fe(NH )[Fe(CN) ]颜料。工艺流程如下:
4 6
回答下列问题:
(1)焙烧黄铁矿发生的反应方程式为______________,滤渣①的主要成分为______(填化学式)。
(2)红渣研细的目的是_________________________________。
(3)“还原”时,发生反应的化学方程式为_____________________________________。
(4)工序①得到绿矾(FeSO
4
·7H
2
O)和母液,则工序①的操作名称为 __________。
(5)用K
3
[Fe(CN)
6
]可检验工序①所得母液中的金属阳离子,检验时发生的离子方程式为_____
____________________________________,所得母液循环使用。
(6)沉铁工序产生的白色沉淀 Fe(NH ) [Fe(CN) ]中 Fe 的化合价为 ,氧化工序发生反应的离
4 2 6
子方程式为________________________________________。