文档内容
第 54 讲 盐类的水解
[复习目标] 1.了解盐类水解的原理及一般规律。2.了解影响盐类水解程度的主要因素。3.了
解盐类水解的应用。4.能利用水解常数(K )进行相关计算。
h
考点一 盐类水解原理及规律
1.定义
在水溶液中,盐电离出来的离子与 水电离出来的 H + 或 OH - 结合生成弱电解质 的反应。
2.盐类水解的结果
使溶液中水的电离平衡向正反应方向移动,使溶液中c(H+)和c(OH-)发生变化,促进了水的
电离。
3.特点
(1)可逆:盐类的水解是可逆反应。
(2)吸热:盐类的水解可看作是酸碱中和反应的逆反应。
(3)微弱:盐类的水解程度很微弱。
4.盐类水解的规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。
盐的类型 实例 是否水解 水解的离子 溶液的酸碱性
强酸强碱盐 NaCl、NaNO 否 中性
3
强酸弱碱盐 NH Cl、Cu(NO ) 是 NH 、 Cu 2 + 酸性
4 3 2
强碱弱酸盐 CHCOONa、NaCO 是 CHCOO-、CO 碱性
3 2 3 3
5.水解反应的离子方程式的书写
(1)盐类水解的离子方程式一般用“”连接,且一般不标“↑”“↓”等状态符号。
(2)多元弱酸盐:分步书写,以第一步为主。
(3)多元弱碱盐:水解反应的离子方程式一步完成。
(4)阴、阳离子相互促进的水解
①若水解程度不大,用“”表示。
②相互促进的水解程度较大的,书写时用“===”“↑”“↓”。
应用举例
写出下列盐溶液中水解的离子方程式。
(1)NH Cl:NH+HONH ·H O+H+。
4 2 3 2(2)Na CO:CO+HOHCO+OH-、HCO+HOHCO+OH-。
2 3 2 2 2 3
(3)FeCl :Fe3++3HOFe(OH) +3H+。
3 2 3
(4)CH COONH:CHCOO-+NH+HOCHCOOH+NH ·H O。
3 4 3 2 3 3 2
(5)AlS:2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑。
2 3 2 3 2
(6)AlCl 溶液和NaHCO 溶液混合:Al3++3HCO===Al(OH) ↓+3CO↑。
3 3 3 2
1.盐溶液显酸碱性,一定是由水解引起的( )
2.溶液呈中性的盐一定是强酸、强碱生成的盐( )
3.pH相同的盐酸和氯化铵溶液中由水电离出的c(H+)相同( )
4.盐类加入水中,水的电离一定被促进( )
答案 1.× 2.× 3.× 4.×
一、盐类水解的实质及规律
1.根据相关物质的电离常数(25 ℃),回答下列问题:
CHCOOH K=1.8×10-5,HCN K=4.9×10-10,HCO K =4.3×10-7 K =5.6×10-
3 a a 2 3 a1 a2
11
(1)相同物质的量浓度的①CHCOONa、②NaCO 、③NaHCO 、④NaCN溶液,pH由大到
3 2 3 3
小的顺序: ② > ④ > ③ > ① ,水的电离程度由大到小的顺序: ② > ④ > ③ > ① 。
(2)相同pH的①CHCOONa,②NaCO,③NaHCO ,④NaCN溶液,物质的量浓度由大到
3 2 3 3
小的顺序: ① > ③ > ④ > ② 。
(3)NaCN溶液中,c(Na+)、c(CN-)、c(HCN)由大到小的顺序: c (Na + ) > c (CN - ) > c (HCN) 。
2.室温下,0.1 mol·L-1的NH CN溶液的pH等于9.32,据此,下列说法错误的是( )
4
A.上述溶液能使甲基橙试剂变黄色
B.室温下,NH ·H O是比HCN更弱的电解质
3 2
C.上述溶液中CN-的水解程度大于NH的水解程度
D.室温下,0.1 mol·L-1 NaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度
答案 B
解析 室温下,溶液呈碱性,能使甲基橙试剂变黄色,故A正确;HCN和NH ·H O均是弱
3 2
电解质,溶液呈碱性,说明CN-的水解程度大于NH的水解程度,由越弱越水解知NH ·H O
3 2
是比HCN强的电解质,故B错误、C正确;CN-、NH相互促进水解,所以 0.1 mol·L-1
NaCN溶液中,CN-的水解程度小于同浓度下NH CN溶液中CN-的水解程度,故D正确。
4
3.已知常温下三种物质的电离常数:CHCOOH(K =1.8×10-5),NH ·H O(K =1.8×10-
3 a 3 2 b
5),HCO(K =4.5×10-7),则CHCOONH 溶液显________性(填“酸”“碱”或“中”,
2 3 a1 3 4
下同),NH HCO 溶液显________性。
4 3答案 中 碱
二、水解产物判断与方程式的书写
4.下列离子方程式不正确的是( )
A.明矾用于净水:Al3++3HOAl(OH) (胶体)+3H+
2 3
B.泡沫灭火器灭火:Al3++3HCO===Al(OH) ↓+3CO↑
3 2
C.用纯碱清洗油污:CO+HOHCO+OH-
2
D.浓硫化钠溶液具有臭味:S2-+2HO===HS↑+2OH-
2 2
答案 D
解析 硫化钠分步水解,生成的硫化氢具有臭味,离子方程式必须分步书写、没有气体符号、
应使用可逆符号,D项错误。
5.(2022·济南模拟)物质与水发生的复分解反应称为水解反应。例如:MgN +
3 2
6HO===3Mg(OH) ↓+2NH ↑。在一定条件下,BrCl、CuCl 、MgC 和KP均可以发生水
2 2 3 2 2 3 3
解。根据上述观点,下列说法不正确的是( )
A.BrCl的水解产物是HBrO和HCl
B.KP的水解产物是KOH和HPO
3 3 4
C.MgC 的水解产物是Mg(OH) 和C H
2 3 2 3 4
D.CuCl 的水解产物是Cu(OH) 和HCl
2 2
答案 B
解析 BrCl中Cl为-1价,Br为+1价,所以BrCl的水解产物是HBrO和HCl,故A正确;
KP中P为-3价,水解生成PH ,即KP的水解产物是KOH和PH ,不生成HPO ,故B
3 3 3 3 3 4
错误;MgC 中Mg为+2价,C为-价,则水解产物是Mg(OH) 和C H ,故C正确;CuCl
2 3 2 3 4 2
中Cu为+2价,Cl为-1价,水解产物是Cu(OH) 和HCl,故D正确。
2
考点二 盐类水解的影响因素及应用
1.影响盐类水解的因素
(1)内因:形成盐的弱酸或弱碱越弱,其对应的弱酸根离子或弱碱阳离子的水解程度越大,
溶液的碱性或酸性越强。
如水解程度:NaCO>NaSO ,NaCO>NaHCO 。
2 3 2 3 2 3 3
(2)外因:盐类水解平衡同电离平衡一样,当温度、浓度等条件改变时,会引起水解平衡的
移动,从而影响盐类水解的程度。其中浓度的影响通常包括:加水稀释、加入适量的酸或碱
及能与酸或碱反应的盐等。
应用举例
以FeCl 水解为例:Fe3++3HOFe(OH) +3H+,分析外界条件对水解平衡的影响。
3 2 3条件 平衡移动方向 H+数 pH 现象
升温 向右 增多 减小 颜色变深
通HCl 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
生成红褐色沉
加NaHCO 向右 减少 增大
3
淀,放出气体
2.盐类水解在生产生活中的应用
(1)水解产物性质的应用
①纯碱溶液不能保存在玻璃塞的试剂瓶中的原因:溶液中碳酸根离子水解:CO+
HOHCO+OH-,使溶液显碱性,会与玻璃中成分SiO 反应。
2 2
②明矾净水的原理:明矾溶液中的铝离子水解:Al3++3HOAl(OH) (胶体)+3H+,
2 3
Al(OH) 胶体能吸附水中的悬浮物,起到净水作用。
3
③ZnCl 溶液可作焊接时的除锈剂的原因: Zn 2 + 水解使溶液显酸性,能溶解铁锈 。
2
(2)促进盐类水解的应用举例
①热的纯碱溶液去油污效果好,原因是碳酸钠的水解为吸热反应,升高温度水解平衡向右移
动,溶液的碱性增强,去污效果增强。
②铵态氮肥与草木灰不得混用的理由: 铵态氮肥中的 NH 水解显酸性,草木灰中的 CO 水解
显碱性,相互促进,使氨气逸出降低肥效。
③加MgO除去MgCl 溶液中的Fe3+杂质的原理:Fe3++3HOFe(OH) +3H+,MgO+2H+
2 2 3
===Mg2++HO,使Fe3+水解平衡向右移动,从而转化为Fe(OH) 沉淀除去,且不引入新的杂
2 3
质。
④泡沫灭火器反应原理:NaHCO 与Al (SO ) 饱和溶液发生相互促进的水解反应:Al3++
3 2 4 3
3HCO===Al(OH) ↓+3CO↑。
3 2
(3)抑制盐类水解的应用举例
①在配制FeCl 、AlCl 、SnCl 等溶液时为抑制水解,常先将盐溶于少量浓盐酸中,再加蒸
3 3 2
馏水稀释到所需浓度。
②用MgCl ·6H O晶体得到纯的无水 MgCl 操作方法及理由是 在干燥的 HC l 气流中加热
2 2 2
MgCl ·6H O ,可以得到无水 MgCl , HC l 气流能抑制 MgC l 的水解,且带走 MgC l ·6H O 因
2 2 2 2 2 2
受热产生的水蒸气。
1.稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强( )
2.水解平衡右移,盐的离子的水解程度一定增大( )
3.用NaS溶液与AlCl 溶液混合可以制备Al S( )
2 3 2 3
4.水解相互促进的离子在同一溶液中一定不能共存( )
答案 1.× 2.× 3.× 4.×一、外界因素对盐类水解的影响
1.下列说法正确的是( )
A.稀释0.1 mol·L-1 Na CO 溶液,溶液的pH增大
2 3
B.水解反应NH+HONH ·H O+H+达到平衡后,升高温度平衡逆向移动
2 3 2
C.加热0.1 mol·L-1 Na CO 溶液,CO的水解程度增大
2 3
D.向NaCO 溶液中加入少量Ca(OH) 固体,CO水解程度减小,溶液的pH减小
2 3 2
答案 C
解析 CO+HOHCO+OH-,稀释时平衡右移,但c(OH-)减小,pH减小,A项错误;
2
水解反应是吸热反应,升温平衡正向移动,B项错误;CO+HOHCO+OH-,加入少量
2
Ca(OH) 固体,CO与Ca2+生成沉淀,平衡左移,CO水解程度减小,c(OH-)增大,pH增大
2
D项错误。
2.常温下,下列各组微粒在指定溶液中因水解反应而不能大量共存的是( )
A.纯碱溶液:K+、SO、OH-、Cl-
B.含有大量AlO的溶液中:Na+、K+、HCO、NO
C.NH、Na+、CHCOO-、NO
3
D.中性溶液中:K+、Al3+、Cl-、SO
答案 D
解析 B项,AlO+HCO+HO===Al(OH) ↓+CO,不是因水解反应而不能共存;C项,
2 3
NH与CHCOO-虽然发生相互促进的水解反应,但促进程度很小,能大量共存;D项,Al3+
3
水解呈酸性,因而在中性溶液中不能大量存在。
3.(2022·广东模拟)关于下列实验的说法不正确的是( )
D.混合液中
B.溶液的pH减小
A.CHCOO-的 C.NHCl可促进 c(CHCOO-)和
3 4 3
是CHCOO-水解
3
水解程度增大 CHCOO-的水解 c(CHCOOH)之
3 3
平衡移动的结果
和大于c(Na+)
答案 B
解析 加热醋酸钠溶液促进CHCOO-的水解,使溶液的碱性增强,pH增大,故B错误。
3
二、盐溶液蒸干所得产物的判断
4.在空气中加热蒸干并灼烧下列盐溶液,将所得产物填入表格中。盐溶液 产物
Ca(HCO )/NaHCO
3 2 3
NH Cl
4
NaSO
2 3
FeCl /AlCl
2 3
Al (SO )/Fe (SO )/CuSO
2 4 3 2 4 3 4
NaAlO /Na CO
2 2 3
答案 CaO/Na CO 无 NaSO Fe O/Al O Al (SO )/Fe (SO )/CuSO NaAlO /Na CO
2 3 2 4 2 3 2 3 2 4 3 2 4 3 4 2 2 3
三、水解原理在除杂中的应用
5.物质的提纯(水解除杂,括号内为杂质)
Mg2+(Fe3+)加入 MgO 或 Mg(OH) ,Cu2+(Fe3+)加入 CuO 或 Cu(OH) 或 C u (OH) CO。
2 2 2 2 3
6.(2022·山东师范大学附中模拟)实验室以含锌废液(主要成分为ZnSO ,含少量的Fe2+、Mn2
4
+)为原料制备ZnCO ·2Zn(OH) 的实验流程如下:
3 2
下列说法正确的是( )
A.过二硫酸钠(Na SO)中硫元素的化合价为+7价
2 2 8
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO
C.调节pH时试剂X可以选用Zn、ZnO、ZnCO 等物质
3
D.沉锌时的离子方程式为3Zn2++6HCO===ZnCO ·2Zn(OH) ↓+5CO↑+HO
3 2 2 2
答案 D
解析 过二硫酸钠中含有过氧键,分子中硫元素的化合价为+6价,A错误;氧化除锰后的
溶液中存在的离子为Na+、Zn2+、Fe3+、SO,B错误;溶液中铁离子能与锌反应生成硫酸亚
铁和硫酸锌,所以调节溶液pH时试剂X不能选用锌,C错误;沉锌时发生的反应为溶液中
锌离子与碳酸氢根离子反应生成ZnCO ·2Zn(OH) 沉淀、二氧化碳和水,D正确。
3 2
答题规范(7) 利用平衡移动原理解释问题
(1)解答此类题的思维过程
①找出存在的平衡体系(即可逆反应或可逆过程)
②找出影响平衡的条件③判断平衡移动的方向
④分析平衡移动的结果及移动结果与所解答问题的联系
(2)答题模板
……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)。
1.为探究盐类水解是一个吸热过程,请用NaCO 溶液和其他必要试剂,设计一个简单的实
2 3
验方案:______________________________________________________________________。
答案 取NaCO 溶液,滴加酚酞溶液呈红色,然后分成两份,加热其中一份,若红色变深,
2 3
则盐类水解吸热
2.常温下,0.1 mol·L-1 NaHCO 溶液的pH大于8,则溶液中c(H CO)>(填“>”“=”或
3 2 3
“<”)c(CO),原因是HCOCO+H+,HCO+HOHCO +OH-,pH大于8则HCO
2 2 3
的水解程度大于电离程度(用离子方程式和必要的文字说明)。
3.把AlCl 溶液蒸干灼烧,最后得到的主要固体是什么?为什么?如何操作溶质不变?(用
3
化学方程式表示并配以必要的文字说明)。
答案 Al O ;在AlCl 溶液中存在着如下平衡:AlCl +3HOAl(OH) +3HCl,加热时水
2 3 3 3 2 3
解平衡右移,HCl浓度增大,蒸干时HCl挥发,使平衡进一步向右移动得到Al(OH) ,在灼
3
烧时发生反应:2Al(OH) =====Al O +3HO,因此最后得到的固体是Al O ;在HCl气流中
3 2 3 2 2 3
加热蒸发溶质不变。
4.Mg粉可溶解在NH Cl溶液中,分析其原因。
4
答案 在NH Cl溶液中存在水解平衡:NH+HONH ·H O+H+,加入Mg,Mg与H+反
4 2 3 2
应放出H,使溶液中c(H+)降低,平衡向右移动,使Mg粉不断溶解。
2
1.(2022·海南,13改编)NaClO溶液具有漂白能力,已知25 ℃时,K(HClO)=4.0×10-8。
a
下列关于NaClO溶液说法正确的是( )
A.0.01 mol·L-1溶液中,c(ClO-)>0.01 mol·L-1
B.长期露置在空气中,释放Cl,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO-+HO===HSO+HClO
2 2 2
D.25 ℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO-)=c(Na+)
答案 D
解析 NaClO溶液中ClO-会水解,故0.01 mol·L-1 NaClO溶液中c(ClO-)<0.01 mol·L-1,
A错误;NaClO溶液长期露置在空气中容易和CO 发生反应而失效,其反应为NaClO+CO
2 2
+HO===NaHCO +HClO,HClO再分解为HCl和O ,不会释放Cl ,B错误;将过量的
2 3 2 2
SO 通入NaClO溶液中,SO 被氧化:SO +ClO-+HO===Cl-+SO+2H+,C错误;25
2 2 2 2
℃,pH=7.0的NaClO和HClO的混合溶液中,存在电荷守恒:c(ClO-)+c(OH-)=c(H+)+c(Na+),c(H+)=c(OH-)则c(ClO-)=c(Na+),K (ClO-)===2.5×10-7,即ClO-的水解程
h
度大于HClO的电离程度,c(HClO)>c(ClO-),所以c(HClO)>c(ClO-)=c(Na+),D正确。
2.(2021·广东,8)鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用GHCl表示)。已
知GHCl水溶液呈酸性,下列叙述正确的是( )
A.0.001 mol·L-1 GHCl水溶液的pH=3
B.0.001 mol·L-1 GHCl水溶液加水稀释,pH升高
C.GHCl在水中的电离方程式为GHCl===G+HCl
D.GHCl水溶液中:c(OH-)+c(Cl-)=c(GH+)+ c(G)
答案 B
解析 GHCl为强酸弱碱盐,电离出的GH+会发生水解,但水解较为微弱,因此0.001 mol·L-
1 GHCl水溶液的pH>3,故A错误;稀释GHCl溶液时,GH+的水解程度将增大,根据勒夏
特列原理可知溶液中c(H+)将减小,溶液pH将升高,故B正确;GHCl为强酸弱碱盐,在水
中的电离方程式为GHCl===GH++Cl-,故C错误;根据电荷守恒可知,GHCl溶液中c(OH
-)+c(Cl-)=c(H+)+c(GH+),故D错误。
3.(2019·北京,12)实验测得0.5 mol·L-1CHCOONa溶液、0.5 mol·L-1CuSO 溶液以及HO
3 4 2
的pH随温度变化的曲线如图所示。下列说法正确的是( )
A.随温度升高,纯水中c(H+)>c(OH-)
B.随温度升高,CHCOONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO-、Cu2+水
3 4 3
解平衡移动方向不同
答案 C
解析 任何温度时,纯水中 H+浓度与 OH-浓度始终相等,A 项错误;随温度升高,
CHCOONa水解程度增大,溶液中c(OH-)增大,且温度升高,水的电离程度增大,c(OH-)
3
也增大,B项错误;温度升高,水的电离程度增大,c(H+)增大,又CuSO 水解使溶液显酸
4
性,温度升高,水解平衡正向移动,故 c(H+)增大,C项正确;温度升高,能使电离平衡和
水解平衡均正向移动,而CHCOONa溶液随温度升高pH降低的原因是水的电离程度增大得
3
多,而CuSO 溶液随温度升高pH降低的原因是Cu2+水解程度增大得多,D项错误。
4
4.(2022·湖南,13)为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为
3 3 2 30.1 mol·L-1)。
实验 操作与现象
① 在5 mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色
3
在5 mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加
3 2 3
②
K[Fe(CN) ]溶液,产生蓝色沉淀
3 6
在5 mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分
2 3 3
③ 成两份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产
3 6
生红褐色沉淀
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO对Fe3+的水解反应无影响,但对还原反应有影响
答案 D
解析 铁离子的水解反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,
生成较多的氢氧化铁,从而使溶液显红褐色,故A正确;在5 mL FeCl 溶液中滴加2滴同浓
3
度的NaSO 溶液,根据现象分析可知,Fe3+既发生了水解反应,生成红褐色的氢氧化铁,
2 3
又被亚硫酸根离子还原,生成亚铁离子,加入铁氰化钾溶液后,生成蓝色沉淀,故B正确;
实验③中在5 mL Na SO 溶液中滴加2滴同浓度的FeCl 溶液,根据溶液变红褐色,说明
2 3 3
Fe3+发生水解反应,滴加K[Fe(CN) ]无蓝色沉淀产生,说明没有发生还原反应,故C正确;
3 6
结合实验①、③可知,SO对Fe3+的水解反应有影响,故D错误。
课时精练
1.《本草纲目》中对白矾之用有如下叙述:“吐利风热之痰涎,取其酸苦涌泄也;治诸血
痛,脱肛……取其酸涩而收也……”下列说法正确的是( )
A.治血痛的原因是利用了胶体的吸附作用
B.白矾溶于水后微粒浓度排序:c(H O)>c(SO)>c(Al3+)>c(K+)>c(H+)>c(OH-)
2
C.白矾和氯化铁均可用作水处理剂,均可以杀菌消毒
D.白矾常在油条中作膨化剂的原理是Al3++3HCO===Al(OH) ↓+3CO↑
3 2
答案 D
解析 Al3+水解生成氢氧化铝胶体,治血痛的原因是利用了胶体的聚沉,故A错误;白矾是
硫酸铝钾晶体[KAl(SO)·12H O],其水溶液因铝离子水解而显酸性,铝离子减少,微粒浓度
4 2 2
排序:c(H O)>c(SO)>c(K+)>c(Al3+)>c(H+)>c(OH-),故B错误。
22.根据表中信息,判断0.10 mol·L-1的下列各物质的溶液pH最大的是( )
酸 电离常数(常温下)
CHCOOH K=1.75×10-5
3 a
HCO K =4.5×10-7,K =4.7×10-11
2 3 a1 a2
HS K =1.1×10-7,K =1.3×10-13
2 a1 a2
A.CHCOONa B.NaCO
3 2 3
C.NaHCO D.NaS
3 2
答案 D
解析 根据表格中的酸的电离常数可知,酸性:CHCOOH>H CO>H S>HCO>HS-,根据越
3 2 3 2
弱越水解的规律可知,水解能力:S2->CO>HS->HCO>CHCOO-,故D正确。
3
3.生活中处处有化学,下列有关说法正确的是( )
A.天然弱碱性水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子
B.焊接时用NH Cl溶液除锈与盐类水解无关
4
C.生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理
D.在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐褪去
2 3 2
答案 D
解析 A项,Mg2+水解呈酸性,Ca2+不发生水解反应,错误;B项,氯化铵是强酸弱碱盐,
NH水解使溶液显酸性,因此能溶解铁锈,错误;C项,惰性电极电解食盐水的生成物是氢
气、氢氧化钠与氯气,氯气与氢氧化钠溶液反应可以制备消毒液,与水解无关,错误;D项,
碳酸钠溶液中存在水解平衡:CO+HOHCO+OH-,加入氯化钡溶液后生成碳酸钡沉淀,
2
降低了CO的浓度,水解平衡逆向移动,溶液的碱性降低,所以红色逐渐褪去,正确。
4.(2022·常德模拟)下列应用与盐类水解有关的是( )
①用FeCl 作净水剂
3
②为保存FeCl 溶液,要在溶液中加少量盐酸
3
③实验室配制AlCl 溶液时,应先把AlCl 固体溶解在较浓的盐酸中,然后加水稀释
3 3
④NH Cl与ZnCl 溶液可用作焊接中的除锈剂
4 2
⑤实验室盛放NaCO 溶液的试剂瓶应用橡胶塞,而不用玻璃塞
2 3
⑥长期施用(NH )SO ,土壤酸性增强
4 2 4
A.①④⑥ B.②⑤⑥
C.③⑤⑥ D.全有关
答案 D
解析 ①FeCl 能水解,生成的Fe(OH) 胶体可吸附水中的杂质;②在FeCl 溶液中加入少量
3 3 3
盐酸,能抑制Fe3+的水解;③AlCl 水解生成Al(OH) 和HCl,先将AlCl 固体溶解在较浓的
3 3 3
盐酸中可以抑制Al3+的水解;④NH Cl、ZnCl 水解使溶液呈酸性,能溶解金属氧化物,可
4 2用作除锈剂;⑤ NaCO 水解使溶液呈碱性,会与玻璃中的主要成分 SiO 发生反应;
2 3 2
⑥(NH )SO 水解使溶液呈酸性,长期施用(NH )SO ,可使土壤酸性增强。
4 2 4 4 2 4
5.(2021·广东1月适应性测试,9)叠氮酸(HN )与NaOH溶液反应生成NaN 。已知NaN 溶
3 3 3
液呈碱性,下列叙述正确的是( )
A.0.01 mol·L-1 HN 溶液的pH=2
3
B.HN 溶液的pH随温度升高而减小
3
C.NaN 的电离方程式:NaN ===Na++3N
3 3
D.0.01 mol·L-1 NaN 溶液中:c(H+)+c(Na+)=c(N)+c(HN )
3 3
答案 B
解析 NaN 溶液呈碱性,说明HN 为弱酸,故0.01 mol·L-1 HN 溶液的pH>2,A错误;
3 3 3
HN 为弱酸,电离方程式为HN H++N,电离是吸热过程,升高温度促进 HN 的电离,
3 3 3
c(H+)增大, pH减小,B正确;NaN 是强电解质,电离方程式为 NaN === Na++N,C错
3 3
误;在0.01 mol·L-1 NaN 溶液中存在元素质量守恒:c(Na+)=c(N)+c(HN ),D错误。
3 3
6.下列实验操作不能达到实验目的的是( )
选项 实验目的 实验操作
A 实验室配制FeCl 水溶液 将FeCl 溶于少量浓盐酸中,再加水稀释
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
将0.1 mol·L-1 MgSO 溶液滴入NaOH溶
4
证明Cu(OH) 的溶度积比
2
C 液至不再有沉淀产生,再滴加0.1 mol·L-1
Mg(OH) 的小
2
CuSO 溶液
4
D 除去MgCl 酸性溶液中的Fe3+ 加入过量MgO充分搅拌,过滤
2
答案 B
解析 将MgCl 溶液加热蒸干时,镁离子的水解正向移动,加热可使HCl挥发,蒸干、灼烧
2
得到MgO,B项符合题意。
7.(2022·上海静安模拟)有机弱碱甲胺(CHNH )的碱性略强于氨水,也能与盐酸反应生成盐
3 2
酸盐(用CHNH Cl表示)。下列叙述正确的是( )
3 3
A.CHNH Cl水溶液中:c(Cl-)=c(CHNH)
3 3 3
B.0.01 mol·L-1 CHNH Cl水溶液的pH=2
3 3
C.CHNH Cl在水中的电离方程式为CHNH ClCHNH + H++Cl-
3 3 3 3 3 2
D.0.1 mol·L-1 CHNH Cl水溶液加少量水稀释,pH将增大
3 3
答案 D
解析 CHNH Cl水溶液中,CHNH发生水解,故c(Cl-) >c(CHNH),A错误;0.01 mol·L-1
3 3 3 3
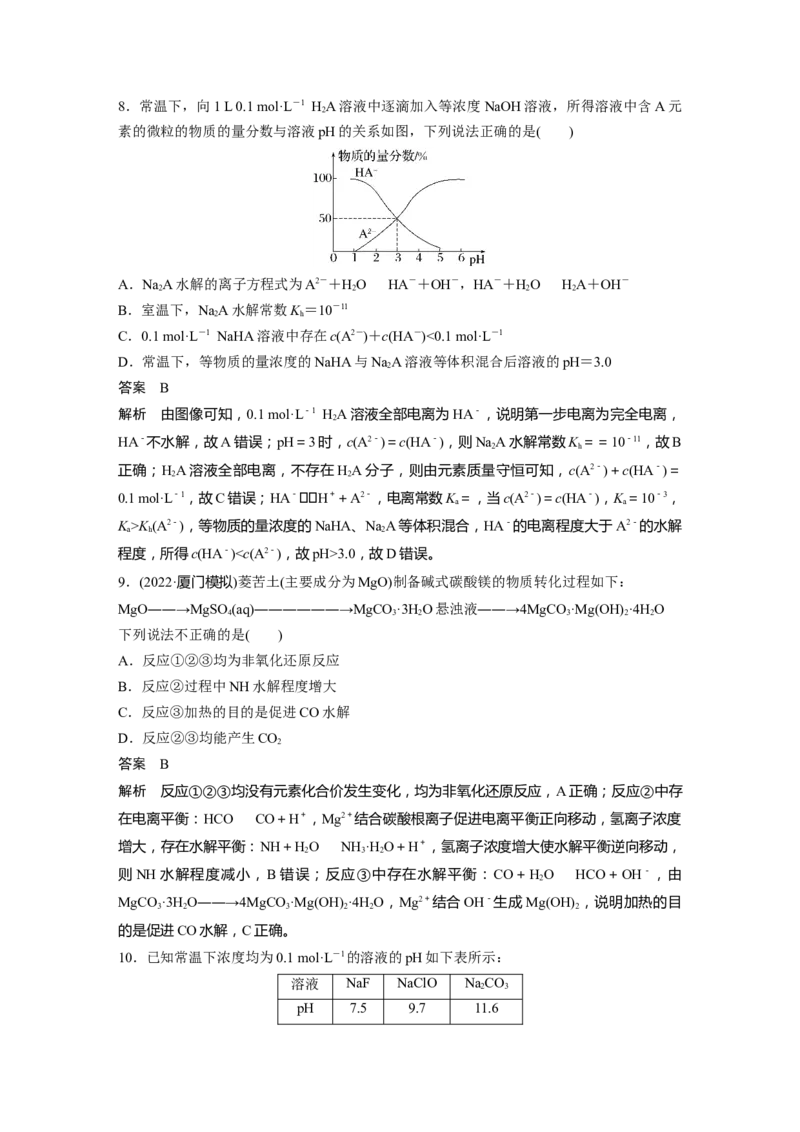
CHNH Cl水溶液中由于CHNH的水解,使溶液显酸性,但水解是微弱的,2K (A2-),等物质的量浓度的NaHA、NaA等体积混合,HA-的电离程度大于A2-的水解
a h 2
程度,所得c(HA-)3.0,故D错误。
9.(2022·厦门模拟)菱苦土(主要成分为MgO)制备碱式碳酸镁的物质转化过程如下:
MgO――→MgSO (aq)――――――→MgCO ·3H O悬浊液――→4MgCO ·Mg(OH) ·4H O
4 3 2 3 2 2
下列说法不正确的是( )
A.反应①②③均为非氧化还原反应
B.反应②过程中NH水解程度增大
C.反应③加热的目的是促进CO水解
D.反应②③均能产生CO
2
答案 B
解析 反应①②③均没有元素化合价发生变化,均为非氧化还原反应,A正确;反应②中存
在电离平衡:HCOCO+H+,Mg2+结合碳酸根离子促进电离平衡正向移动,氢离子浓度
增大,存在水解平衡:NH+HONH ·H O+H+,氢离子浓度增大使水解平衡逆向移动,
2 3 2
则NH水解程度减小,B错误;反应③中存在水解平衡:CO+HOHCO+OH-,由
2
MgCO ·3H O――→4MgCO ·Mg(OH) ·4H O,Mg2+结合OH-生成Mg(OH) ,说明加热的目
3 2 3 2 2 2
的是促进CO水解,C正确。
10.已知常温下浓度均为0.1 mol·L-1的溶液的pH如下表所示:
溶液 NaF NaClO NaCO
2 3
pH 7.5 9.7 11.6下列有关说法正确的是( )
A.根据上表得出三种酸的电离平衡常数:HF>HClO>HCO(一级电离平衡常数)
2 3
B.加热0.1 mol·L-1 NaClO溶液,其pH将小于9.7
C.pH=2的HF溶液与pH=12的NaOH溶液以等体积混合,则有c(Na+)=c(F-)>c(H+)=
c(OH-)
D.0.1 mol·L-1 Na CO 溶液中:c(OH-)-c(H+)=c(HCO)+2c(H CO)
2 3 2 3
答案 D
解析 相同温度下,相同浓度的钠盐溶液中,弱酸酸根离子水解程度越大其溶液pH越大。
根据表中数据可知,离子水解程度:F-<ClO-<CO,则酸的电离平衡常数:HF>HClO>
HCO,A项错误;盐类水解是吸热反应,升高温度促进盐类水解,故加热NaClO溶液,ClO
-水解程度增大,溶液的碱性增强,pH增大,B项错误;常温下,NaF溶液的pH=7.5>7,
说明NaF是强碱弱酸盐,则HF是弱酸,pH=2的HF浓度大于pH=12的NaOH溶液浓度,
二者等体积混合,HF有剩余,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒得c(Na+)<c(F
-),酸的电离程度较小,则溶液中离子浓度 c(F-)>c(Na+)>c(H+)>c(OH-),C项错误;根
据元素质量守恒得2[c(CO)+c(HCO)+c(H CO)]=c(Na+),根据电荷守恒得c(H+)+c(Na+)
2 3
=c(OH-)+c(HCO)+2c(CO),故c(OH-)-c(H+)=c(HCO)+2c(H CO),D项正确。
2 3
11.(2022·上海静安模拟)(1)常温下,浓度均为0.1 mol·L-1的六种溶液pH如下:
溶质 NaClO NaCO NaHCO NaSiO NaSO NaHSO
2 3 3 2 3 2 3 3
pH 10.3 11.6 9.7 12.3 10.0 4.0
常温下,相同物质的量浓度的下列稀溶液,其酸性由强到弱的顺序是________(填字母) 。
a.HCO b.HSO c.HSiO
2 3 2 3 2 3
六种溶液中,水的电离程度最小的是__________(填化学式)。
(2)用离子方程式说明NaCO 溶液pH>7的原因:________________________________。
2 3
(3) 欲 增 大 氯 水 中 次 氯 酸 的 浓 度 , 可 向 氯 水 中 加 入 上 表 中 的 物 质 是
______________________(填化学式),
用化学平衡移动的原理解释其原因:_______________________________________________。
答案 (1)bac NaHSO
3
(2)CO+HOHCO+OH-、HCO+HOHCO+OH-
2 2 2 3
(3)NaHCO (或NaClO) 因为Cl +HOH++Cl-+HClO,加入NaHCO (或NaClO)可消耗
3 2 2 3
H+,平衡向正反应方向移动,从而使溶液中次氯酸的浓度增大
解析 (1)NaHCO 溶液显碱性,则HCO的水解程度大于其电离程度,NaHSO 溶液显酸性,
3 3
则HSO的电离程度大于其水解程度,故HSO 酸性比HCO 的酸性强,等浓度的NaSiO 溶
2 3 2 3 2 3
液的碱性比NaHCO 的碱性强,弱酸越弱,其对应的酸根离子水解程度越大,其对应的强碱
3弱酸盐碱性越强,故碳酸的酸性比硅酸的酸性强,故常温下,相同物质的量浓度的稀溶液,
其酸性由强到弱的顺序是bac。六种溶液中,NaClO、NaCO 、NaHCO 、NaSiO 、NaSO
2 3 3 2 3 2 3
的溶液显碱性,均发生水解,促进水的电离,而NaHSO 溶液显酸性,HSO的电离程度大于
3
其水解程度,抑制水的电离,则水的电离程度最小的是NaHSO 溶液。
3
12.(1)铈(Ce)是地壳中含量最高的稀土元素,是宝贵的战略资源,在加热条件下CeCl 易发
3
生水解,无水CeCl 可用加热CeCl ·6H O和NH Cl固体混合物的方法来制备,其中NH Cl
3 3 2 4 4
的作用是__________________________________________________________。
(2)将 0.5 mol·L-1的 NaClO 溶液加热蒸干灼烧最后所得的固体是________,原因是
________________________________________________________________________。
(3)用离子方程式表示NaCN溶液呈碱性的原因:______________________________。
答案 (1)分解出HCl气体,抑制CeCl 的水解
3
(2)NaCl NaClO 水解的化学方程式为 NaClO+HONaOH+HClO,2HClO=====2HCl+
2
O↑,HCl+NaOH===NaCl+HO,最终得到NaCl
2 2
(3)CN-+HOHCN+OH-
2
13.(1)常温下,用NaOH溶液吸收SO 得到pH=9的NaSO 溶液,吸收过程中水的电离平
2 2 3
衡________(填“向左”“向右”或“不”)移动。试计算溶液中=________(常温下HSO 的
2 3
电离平衡常数K =1.0×10-2,K =6.0×10-8)。
a1 a2
(2)已知常温下,HCN的电离平衡常数K=6.2×10-10。
a
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显____________(填“酸”“碱”
或“中”)性,c(CN-)________(填“>”“<”或“=”)c(HCN)。该溶液中各离子浓度由
大到小的顺序为________________________________________________________。
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1 KCN溶液等体积混合后恰好得到中性溶液,
则c=__________(保留小数点后4位)。
答案 (1)向右 60
(2)①碱 < c(Na+)>c(CN-)>c(OH-)>c(H+) ②0.616 2
解析 (1)SO+HOHSO+OH-
2
K ===
h
所以===60。
(2)①常温下,NaCN的水解常数K ==≈1.61×10-5,K >K,故CN-的水解能力强于HCN
h h a
的电离能力,由于NaCN与HCN的物质的量相等,故水解产生的c(OH-)大于电离生成的
c(H+),混合溶液显碱性,且c(CN-)<c(HCN)。②当溶液显中性时,由电荷守恒知溶液中
c(K+)=c(CN-)+c(Cl-),由元素质量守恒得c(HCN)=c(K+)-c(CN-)=c(Cl-)=0.5c mol·L-
1,由CN-+HOHCN+OH-得K ===1.61×10-5,解得c≈0.616 2。
2 h