文档内容
2024 年高考化学临考押题卷 01
(考试时间:75分钟 试卷满分:100分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1. “定州花瓷瓯,颜色天下白”。定窑烧制的白瓷胎质洁白细腻,釉色匀净,薄而坚硬,素有“白如
玉、薄如纸、声如磬”的美誉,下列物质材质与之相同的是
A B C D
黄花梨四撞提盒 女史箴图 曾侯乙青铜编钟 青花山水长形瓷枕
2.下列物质的性质与用途对应关系错误的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造晶体管、集成电路等
B.蛋白质遇酶能发生水解,用加酶洗衣粉洗涤真丝织品可快速去污
C.血液中 平衡体系能缓解外来酸碱的影响,可以平衡人体的pH
D.金属电子从激发态跃迁回基态时,释放能量而呈现各种颜色,常制作烟花
3.下列装置正确,且能达到实验目的的是
A.甲装置:用 制取无水
B.乙装置:鉴别纯碱与小苏打
C.丙装置:铁制品表面镀铜
D.丁装置:验证某补铁口服液(含维生素C)中存在
4.酸性高锰酸钾氧化HO 的离子方程式为
2 2
。与该反应有关的说法正确的是
A.HO 的球棍模型为
2 2B.O 的电子式为:
2
C.基态Mn2+价电子的轨道表示式为
D.标准状况下收集到56LO 时,最多消耗
2
5.高中生应德智体美劳全面发展。下列劳动项目与所述的化学知识没有关联的是
劳动项目 化学知识
A 烹饪活动:向沸汤中加入蛋液做蛋花汤 加热使蛋白质变性
B 烘焙活动:碳酸钠可以用来调节面团的酸度 NaCO 能与酸反应
2 3
C 家务活动:擦干已洗净铁锅表面的水,以防生锈 铁与水蒸气反应生成Fe O
3 4
D 学农活动:施肥时铵态氮肥和草木灰不能同时使用 与 在一定条件反应
6.下列叙述正确的是
A.盐酸和氨水均可使Cu(OH) 溶解
2
B.Na和Fe均能与HO反应生成碱
2
C.NH 和SO 均可使红色石蕊试纸变蓝
3 2
D.SiO 和Fe O 均能与C反应生成CO
2 2 3 2
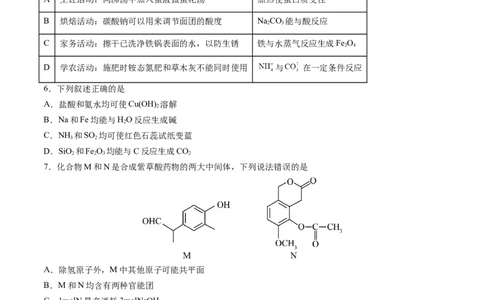
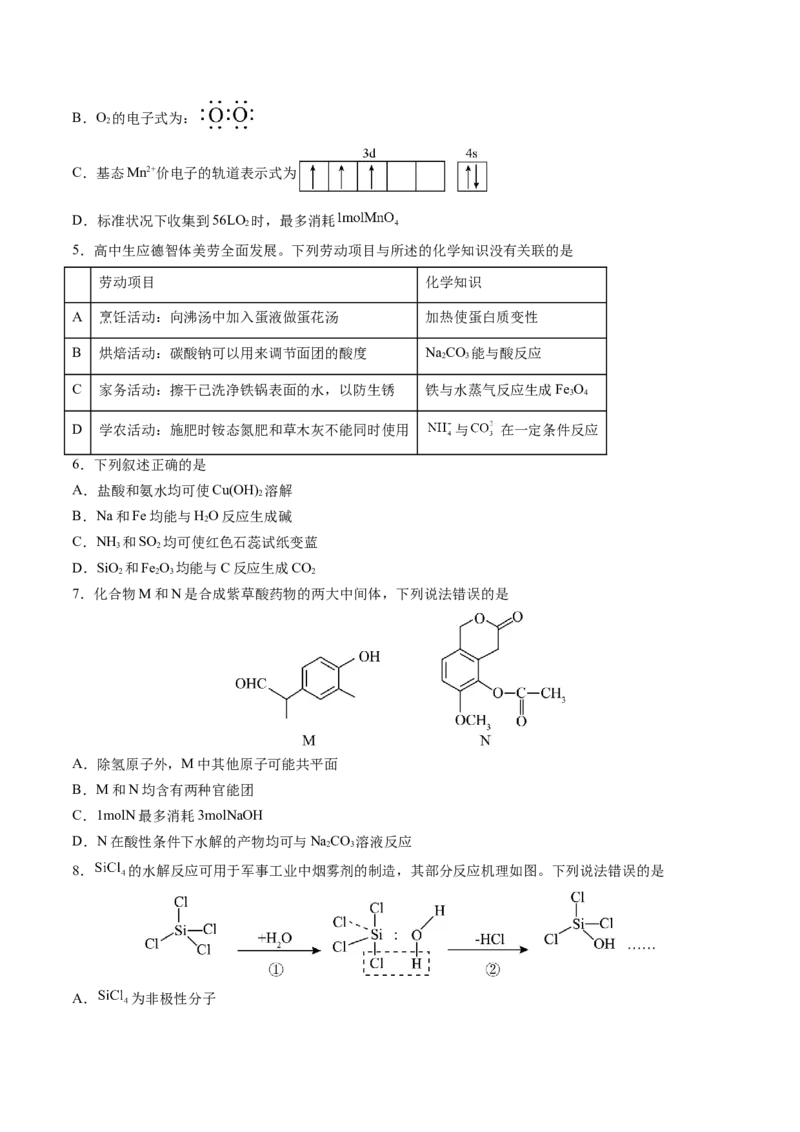
7.化合物M和N是合成紫草酸药物的两大中间体,下列说法错误的是
A.除氢原子外,M中其他原子可能共平面
B.M和N均含有两种官能团
C.1molN最多消耗3molNaOH
D.N在酸性条件下水解的产物均可与NaCO 溶液反应
2 3
8. 的水解反应可用于军事工业中烟雾剂的制造,其部分反应机理如图。下列说法错误的是
A. 为非极性分子B.电负性:O>Cl>H>Si
C.沸点: 大于
D.过程①中Si的 杂化轨道接纳O的孤电子对形成配位键
9.X、Y、Z、W是原子序数依次增大的4种短周期元素,由这4种元素组成的常见物质转化关系如图所
示(反应条件略去),已知m是单质,Q是由三种元素组成的盐。下列推断错误的是
A.元素电负性: B.Q可能是酸式盐
C.物质沸点: D.b、c、e、f都是极性分子
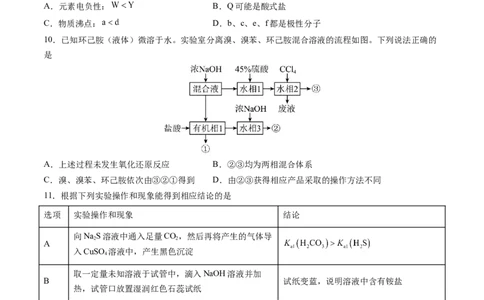
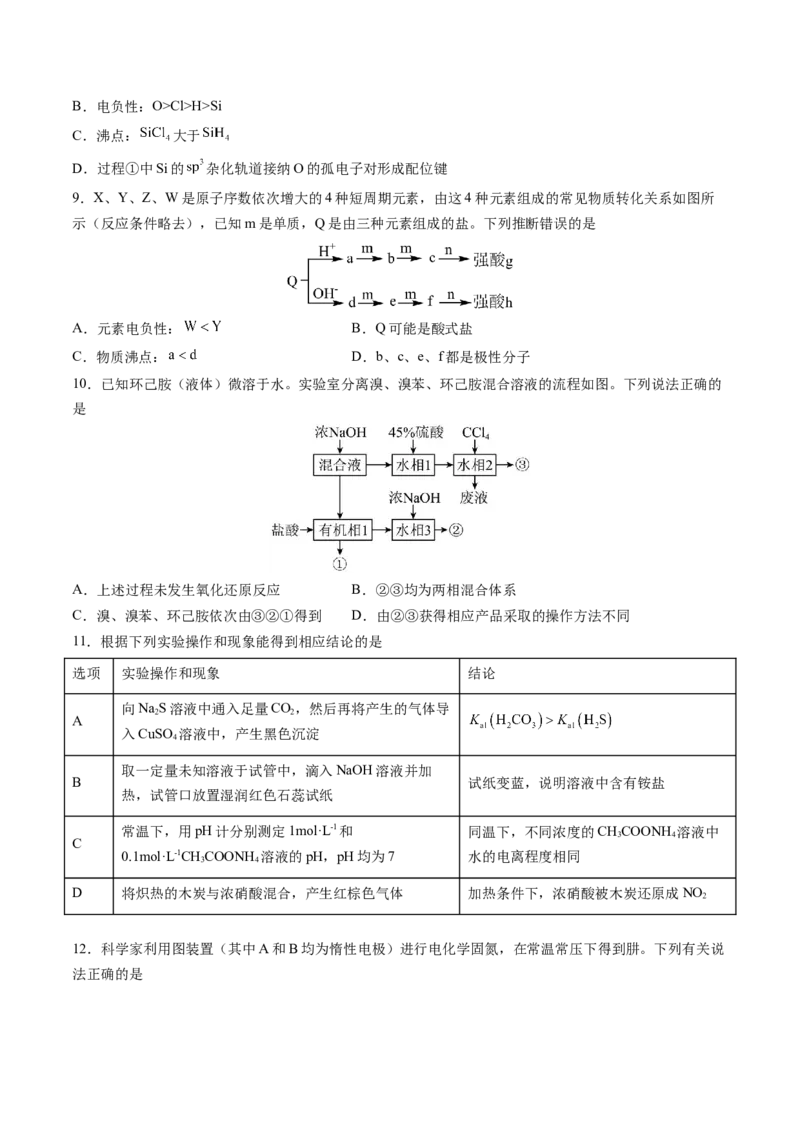
10.已知环己胺(液体)微溶于水。实验室分离溴、溴苯、环己胺混合溶液的流程如图。下列说法正确的
是
A.上述过程未发生氧化还原反应 B.②③均为两相混合体系
C.溴、溴苯、环己胺依次由③②①得到 D.由②③获得相应产品采取的操作方法不同
11.根据下列实验操作和现象能得到相应结论的是
选项 实验操作和现象 结论
向NaS溶液中通入足量CO,然后再将产生的气体导
2 2
A
入CuSO 溶液中,产生黑色沉淀
4
取一定量未知溶液于试管中,滴入NaOH溶液并加
B 试纸变蓝,说明溶液中含有铵盐
热,试管口放置湿润红色石蕊试纸
常温下,用pH计分别测定1mol·L-1和 同温下,不同浓度的CHCOONH 溶液中
3 4
C
0.1mol·L-1CHCOONH 溶液的pH,pH均为7 水的电离程度相同
3 4
D 将炽热的木炭与浓硝酸混合,产生红棕色气体 加热条件下,浓硝酸被木炭还原成NO
2
12.科学家利用图装置(其中A和B均为惰性电极)进行电化学固氮,在常温常压下得到肼。下列有关说
法正确的是A.电极B为阴极
B.H+穿过质子交换膜向B电极一侧移动
C.A电极的反应式为:
D.相同条件下,A电极每消耗22.4LN ,B电极理论上生成22.4LO
2 2
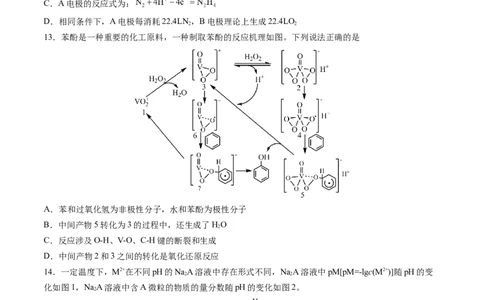
13.苯酚是一种重要的化工原料,一种制取苯酚的反应机理如图。下列说法正确的是
A.苯和过氧化氢为非极性分子,水和苯酚为极性分子
B.中间产物5转化为3的过程中,还生成了HO
2
C.反应涉及O-H、V-O、C-H键的断裂和生成
D.中间产物2和3之间的转化是氧化还原反应
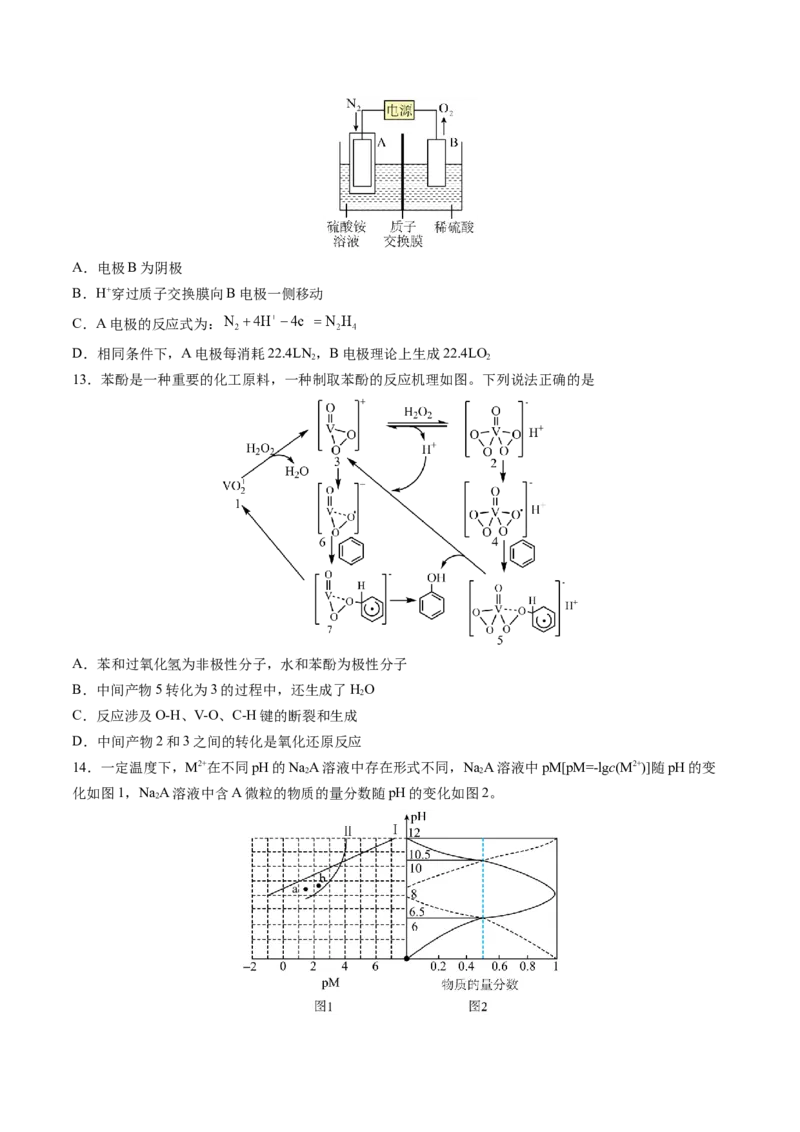
14.一定温度下,M2+在不同pH的NaA溶液中存在形式不同,NaA溶液中pM[pM=-lgc(M2+)]随pH的变
2 2
化如图1,NaA溶液中含A微粒的物质的量分数随pH的变化如图2。
2已知①MA,M(OH) 均为难溶物;②初始c(Na A)=0.2mol/L。
2 2
下列说法错误的是
A.c(A2-)=c(H A)时,pH=8.5
2
B.初始状态a点发生反应:A2-+M2+=MA↓
C.I曲线上的点满足c(M2+)·c2(OH-)=K [M(OH) ]
sp 2
D.初始状态的b点,平衡后溶液中存在c(A2-)+c(HA-)+c(H A)=0.2mol/L
2
二、非选择题:本题共4小题,共58分。
15.(14分)某废旧三元锂离子电池正极材料的主要成分是 还有少量有机粘结剂和铝
箔基底等,下图是处理电池正极材料回收锂、钴、镍、锰的一种流程。回答下列问题:
已知:①常温下,碳酸锂微溶于水,碳酸氢锂易溶于水。
中Ni和Co元素的化合价均为+2价。
③焙烧时 没有发生变化,焙烧还原时Li元素转化为
④常温时,氢氧化铝。
(1) 中Mn元素的化合价为 。
(2)为提高焙烧效率,可采取的措施有 (填写一种方法),焙烧的目的是 。
(3)除杂时发生反应的离子方程式为 (任写一个)。
(4)焙烧还原时发生反应的化学方程式为 。
(5)水浸时,通入CO 的目的是 。
2
(6)若废旧的锂离子电池拆解后先使用酸溶解,最终也可以得到, 等物质,在
酸浸中若Al3+浓度为0.1mol/L,则常温时pH> (结果保留两位小数)才能够形成氢氧化铝沉淀。
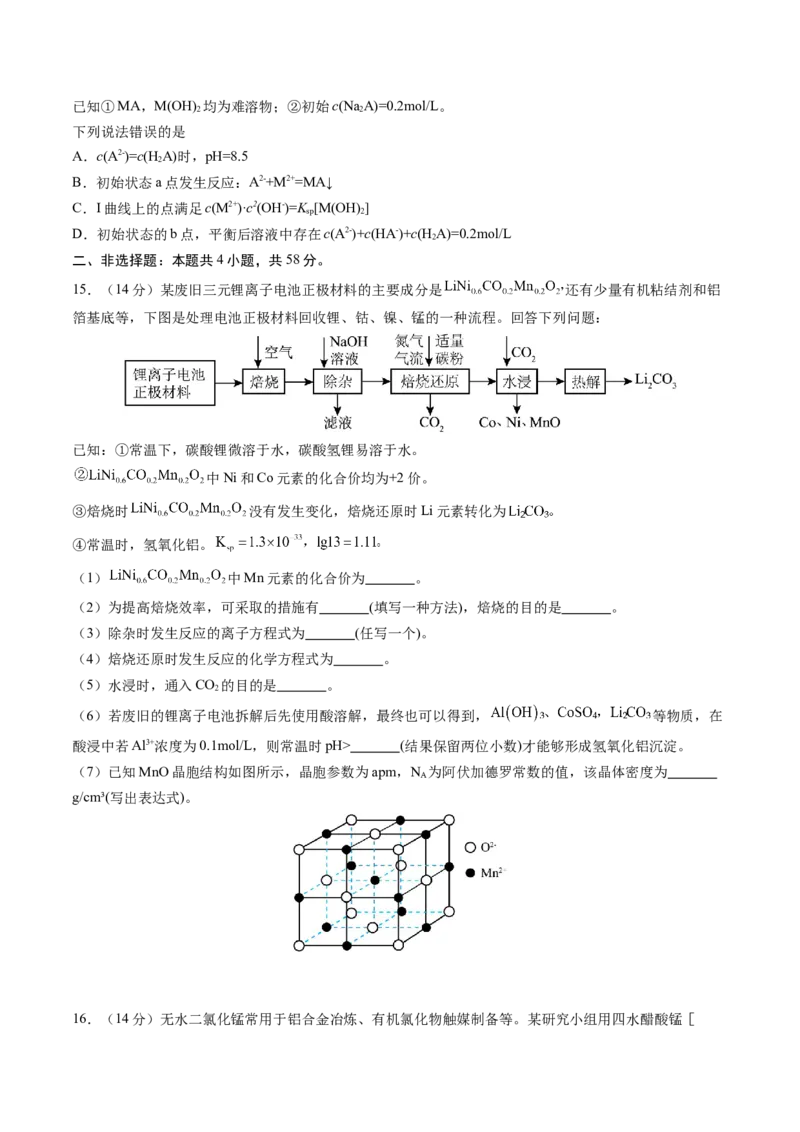
(7)已知MnO晶胞结构如图所示,晶胞参数为apm,N 为阿伏加德罗常数的值,该晶体密度为
A
g/cm³(写出表达式)。
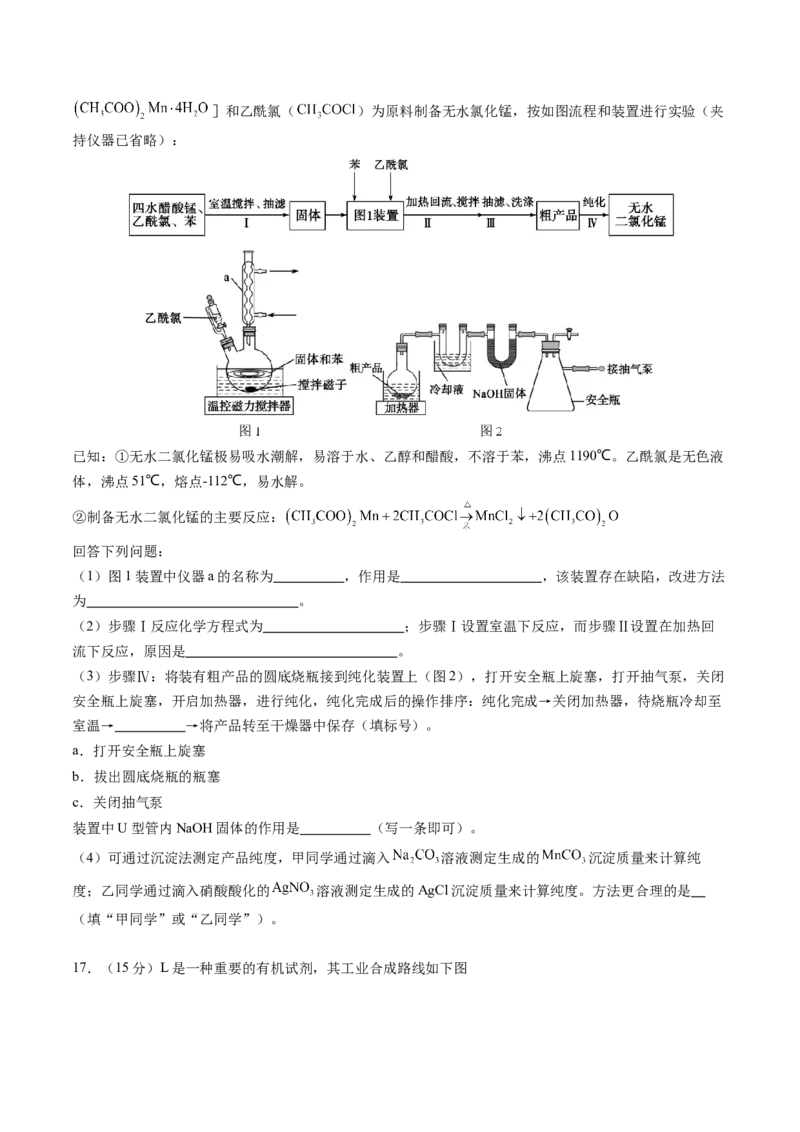
16.(14分)无水二氯化锰常用于铝合金冶炼、有机氯化物触媒制备等。某研究小组用四水醋酸锰[]和乙酰氯( )为原料制备无水氯化锰,按如图流程和装置进行实验(夹
持仪器已省略):
已知:①无水二氯化锰极易吸水潮解,易溶于水、乙醇和醋酸,不溶于苯,沸点1190℃。乙酰氯是无色液
体,沸点51℃,熔点-112℃,易水解。
②制备无水二氯化锰的主要反应:
回答下列问题:
(1)图1装置中仪器a的名称为 ,作用是 ,该装置存在缺陷,改进方法
为 。
(2)步骤Ⅰ反应化学方程式为 ;步骤Ⅰ设置室温下反应,而步骤Ⅱ设置在加热回
流下反应,原因是 。
(3)步骤Ⅳ:将装有粗产品的圆底烧瓶接到纯化装置上(图2),打开安全瓶上旋塞,打开抽气泵,关闭
安全瓶上旋塞,开启加热器,进行纯化,纯化完成后的操作排序:纯化完成→关闭加热器,待烧瓶冷却至
室温→ →将产品转至干燥器中保存(填标号)。
a.打开安全瓶上旋塞
b.拔出圆底烧瓶的瓶塞
c.关闭抽气泵
装置中U型管内NaOH固体的作用是 (写一条即可)。
(4)可通过沉淀法测定产品纯度,甲同学通过滴入 溶液测定生成的 沉淀质量来计算纯
度;乙同学通过滴入硝酸酸化的 溶液测定生成的AgCl沉淀质量来计算纯度。方法更合理的是
(填“甲同学”或“乙同学”)。
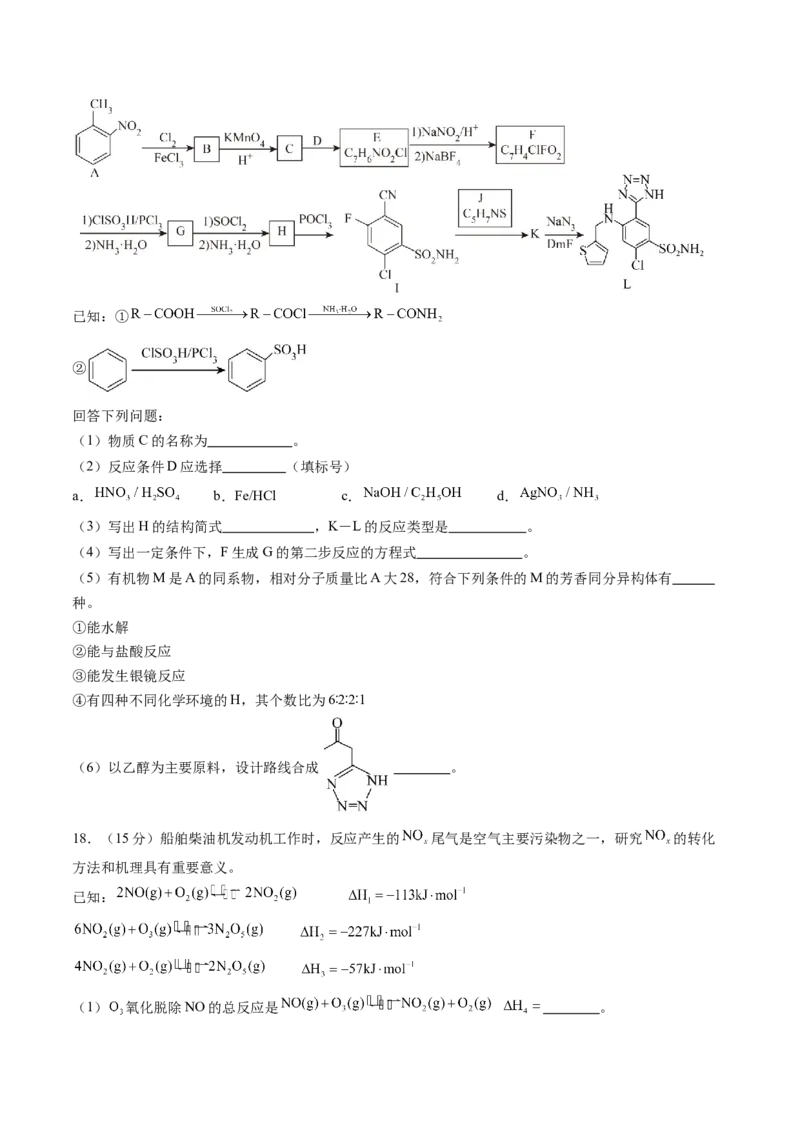
17.(15分)L是一种重要的有机试剂,其工业合成路线如下图已知:①
②
回答下列问题:
(1)物质C的名称为 。
(2)反应条件D应选择 (填标号)
a. b.Fe/HCl c. d.
(3)写出H的结构简式 ,K-L的反应类型是 。
(4)写出一定条件下,F生成G的第二步反应的方程式 。
(5)有机物M是A的同系物,相对分子质量比A大28,符合下列条件的M的芳香同分异构体有
种。
①能水解
②能与盐酸反应
③能发生银镜反应
④有四种不同化学环境的H,其个数比为6∶2∶2∶1
(6)以乙醇为主要原料,设计路线合成 。
18.(15分)船舶柴油机发动机工作时,反应产生的 尾气是空气主要污染物之一,研究 的转化
方法和机理具有重要意义。
已知:
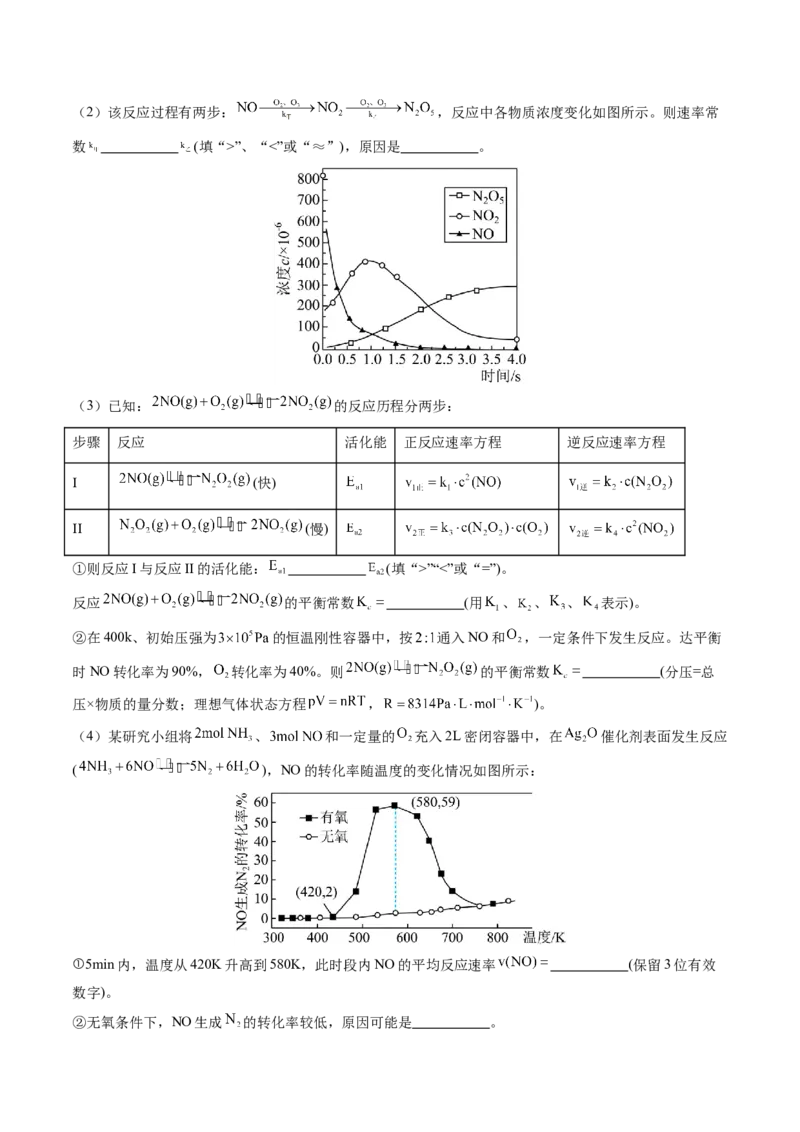
(1) 氧化脱除NO的总反应是 。(2)该反应过程有两步: ,反应中各物质浓度变化如图所示。则速率常
数 (填“>”、“<”或“≈”),原因是 。
(3)已知: 的反应历程分两步:
步骤 反应 活化能 正反应速率方程 逆反应速率方程
I (快)
II (慢)
①则反应I与反应II的活化能: (填“>”“<”或“=”)。
反应 的平衡常数 (用 、 、 、 表示)。
②在400k、初始压强为 的恒温刚性容器中,按 通入NO和 ,一定条件下发生反应。达平衡
时NO转化率为90%, 转化率为40%。则 的平衡常数 (分压=总
压×物质的量分数;理想气体状态方程 , )。
(4)某研究小组将 、 和一定量的 充入2L密闭容器中,在 催化剂表面发生反应
( ),NO的转化率随温度的变化情况如图所示:
①5min内,温度从420K升高到580K,此时段内NO的平均反应速率 (保留3位有效
数字)。
②无氧条件下,NO生成 的转化率较低,原因可能是 。