文档内容
2025届高三化学一轮专题复习讲义(11)
专题三 基本理论
3-4 化学平衡(一)(1课时,共2课时)
【复习目标】
1.了解化学反应速率的概念和定量表示方法,能正确计算平衡转化率(α)。
2.了解温度、浓度、压强和催化剂等对化学反应速率的影响,能用相关理论解释其一般规律。
3.掌握化学平衡状态的特征。
【重点突破】
1.化学反应速率的调控在生活、生产和科学研究领域中的重要作用。
2.可逆反应是否达到平衡状态的判断方法。
【真题再现】
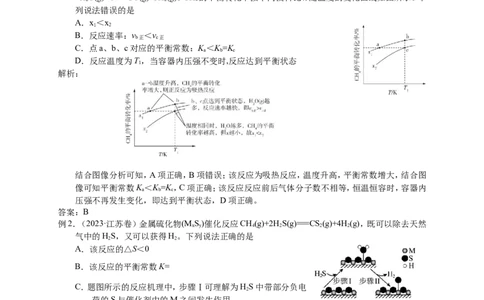
例1.(2023·湖南卷)向一恒容密闭容器中加入1molCH 和一定量的HO,发生反应:CH(g)
4 2 4
+H O(g) CO(g)+3H (g)。CH 的平衡转化率按不同投料比χ 随温度的变化曲线如图所示。下
2 2 4
列说法错误的是
A.x<x
1 2
B.反应速率:v <v
b正 c正
C.点a、b、c对应的平衡常数:K<K =K
a b c
D.反应温度为T,当容器内压强不变时,反应达到平衡状态
1
解析:
结合图像分析可知,A项正确,B项错误;该反应为吸热反应,温度升高,平衡常数增大,结合图
像可知平衡常数K<K =K,C项正确;该反应反应前后气体分子数不相等,恒温恒容时,容器内
a b c
压强不再发生变化,即达到平衡状态,D项正确。
答案:B
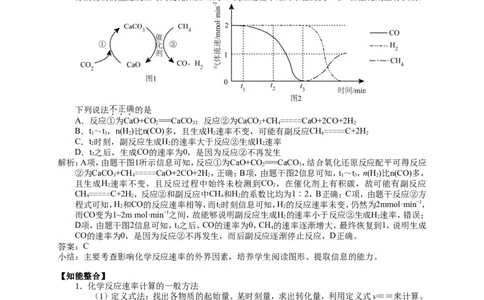
例2.(2023·江苏卷)金属硫化物(MS)催化反应CH(g)+2H S(g)===CS(g)+4H (g),既可以除去天然
x y 4 2 2 2
气中的HS,又可以获得H。下列说法正确的是
2 2
A.该反应的△S<0
B.该反应的平衡常数K=
C.题图所示的反应机理中,步骤Ⅰ可理解为HS中带部分负电
2
荷的S与催化剂中的M之间发生作用
D.该反应中每消耗1mol HS,转移电子的数目约为2×6.02×1023
2
解析:A项,左侧反应物气体计量数之和为3,右侧生成物气体计量数之和为5,△S>0,错误;B项,
由方程形式知,K= ,错误;C项,由题图知,经过步骤Ⅰ后,HS中带部分负电荷的S与催化剂中
2
的M之间形成了作用力,正确;D项,由方程式知,消耗1mol HS同时生成2 mol H ,转移
2 2
4mole-,数目为4×6.02×1023,错误。
答案:C
例3.(2022·江苏卷)用尿素水解生成的NH 催化还原NO,是柴油机车辆尾气净化的主要方法。反应
3
为4NH (g)+O(g)+4NO(g) 4N(g)+6HO(g),下列说法正确的是
3 2 2 2
A.上述反应△S<0
B.上述反应平衡常数C.上述反应中消耗1mol NH ,转移电子的数目为2×6.02×1023
3
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
解析:A项,由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,错误;
B项,由方程式可知,反应平衡常数 ,正确;C项,由方程式可知,反应
每消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数目为3mol×4×
×6.02×1023=3×6.02×1023,错误;D项,实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,
柴油机车辆排放的氨气对空气污染程度增大,错误。
答案: B
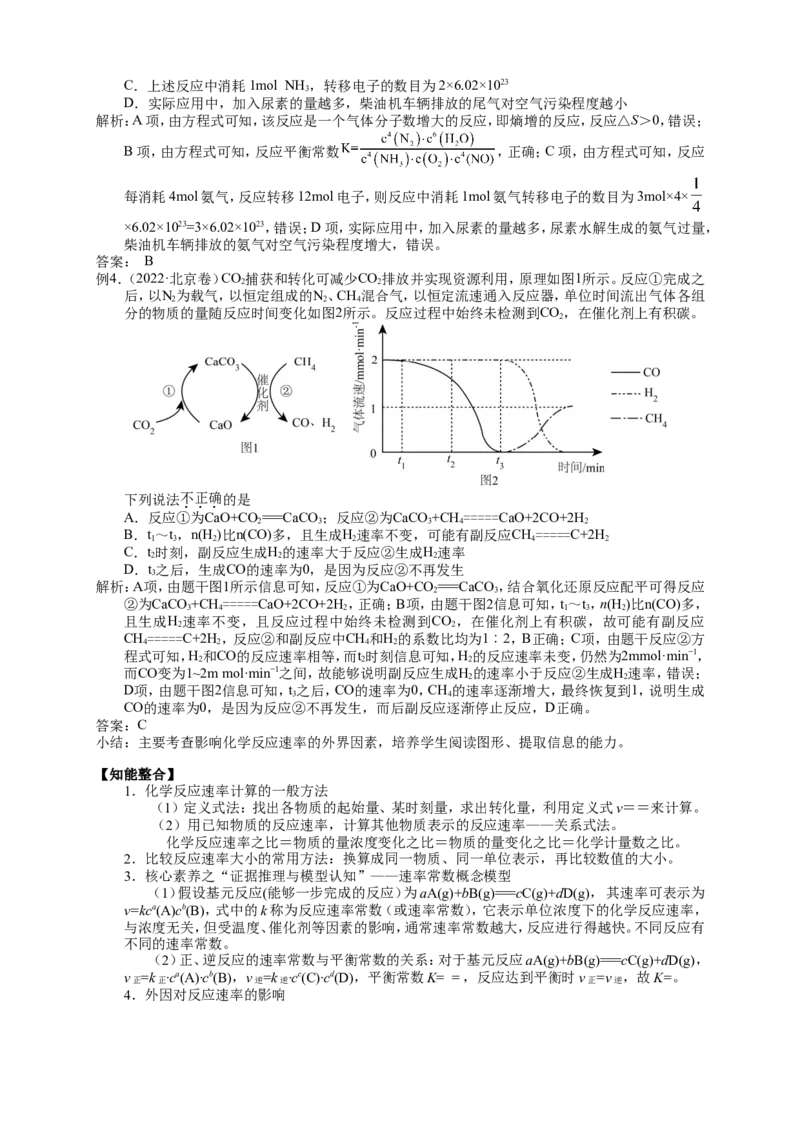
例4.(2022·北京卷)CO捕获和转化可减少CO排放并实现资源利用,原理如图1所示。反应①完成之
2 2
后,以N为载气,以恒定组成的N、CH混合气,以恒定流速通入反应器,单位时间流出气体各组
2 2 4
分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2
下列说法不正确的是
A.反应①为CaO+CO===CaCO ;反应②为CaCO +CH=====CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H速率不变,可能有副反应CH=====C+2H
1 3 2 2 4 2
C.t时刻,副反应生成H的速率大于反应②生成H速率
2 2 2
D.t之后,生成CO的速率为0,是因为反应②不再发生
3
解析:A项,由题干图1所示信息可知,反应①为CaO+CO===CaCO ,结合氧化还原反应配平可得反应
2 3
②为CaCO +CH=====CaO+2CO+2H,正确;B项,由题干图2信息可知,t~t,n(H )比n(CO)多,
3 4 2 1 3 2
且生成H 速率不变,且反应过程中始终未检测到CO ,在催化剂上有积碳,故可能有副反应
2 2
CH=====C+2H,反应②和副反应中CH和H的系数比均为1︰2,B正确;C项,由题干反应②方
4 2 4 2
程式可知,H和CO的反应速率相等,而t时刻信息可知,H的反应速率未变,仍然为2mmol·min−1,
2 2 2
而CO变为1~2m mol·min−1之间,故能够说明副反应生成H的速率小于反应②生成H速率,错误;
2 2
D项,由题干图2信息可知,t之后,CO的速率为0,CH的速率逐渐增大,最终恢复到1,说明生成
3 4
CO的速率为0,是因为反应②不再发生,而后副反应逐渐停止反应,D正确。
答案:C
小结:主要考查影响化学反应速率的外界因素,培养学生阅读图形、提取信息的能力。
【知能整合】
1.化学反应速率计算的一般方法
(1)定义式法:找出各物质的起始量、某时刻量,求出转化量,利用定义式v==来计算。
(2)用已知物质的反应速率,计算其他物质表示的反应速率——关系式法。
化学反应速率之比=物质的量浓度变化之比=物质的量变化之比=化学计量数之比。
2.比较反应速率大小的常用方法:换算成同一物质、同一单位表示,再比较数值的大小。
3.核心素养之“证据推理与模型认知”——速率常数概念模型
(1)假设基元反应(能够一步完成的反应)为aA(g)+bB(g)===cC(g)+dD(g), 其速率可表示为
v=kca(A)cb(B),式中的k称为反应速率常数(或速率常数),它表示单位浓度下的化学反应速率,
与浓度无关,但受温度、催化剂等因素的影响,通常速率常数越大,反应进行得越快。不同反应有
不同的速率常数。
(2)正、逆反应的速率常数与平衡常数的关系:对于基元反应aA(g)+bB(g)===cC(g)+dD(g),
v =k ·ca(A)·cb(B),v =k ·cc(C)·cd(D),平衡常数K= = ,反应达到平衡时v =v ,故K=。
正 正 逆 逆 正 逆
4.外因对反应速率的影响5.判断化学平衡状态的两种方法
(1)动态标志:v =v ≠0:
正 逆
①同种物质:同一物质的生成速率等于消耗速率。
②不同物质:必须标明是“异向”的反应速率关系。如aA+bB===cC+dD,=时,反应
达到平衡状态。
(2)静态标志:各种“量”不变:
①各物质的质量、物质的量或浓度不变。
②各物质的百分含量(物质的量分数、质量分数等)不变。
③温度、压强(化学反应方程式两边气体体积不相等)或颜色(某组分有颜色)不变。
【体系再构】
【随堂反馈】
基础训练
1.X(g)+3Y(g) 2Z(g) ΔH=-akJ·mol-1。一定条件下,将1 molX和3 molY通入2L的恒容密闭容
器,反应10 min,测得Y的物质的量为2.4 mol。下列说法正确的是
A.10 min内,Y的平均反应速率为0.03 mol·L-1·s-1
B.10 min内,消耗0.2 molX,生成0.4 molZ
C.第10 min时,X的反应速率为0.01 mol·L-1·min-1
D.10 min内,X和Y反应放出的热量为a kJ
2.在1 L 恒温恒容的密闭容器中投入一定量NO,发生反应:
2 5
反应1:NO(g) == N O(g)+ 1/2O(g) 反应2:NO(g) 2NO (g)
2 5 2 4 2 2 4 2
现有下列情况:①混合气体的密度保持不变;②气体压强保持不变;③ 保持不变;④气
体的平均摩尔质量保持不变; ⑤O 的物质的量保持不变;⑥v (N O)︰v (NO )=1︰2。
2 正 2 4 逆 2
能表明反应2一定达到平衡状态的是
A.②③④⑥ B.①②③⑥ C.①③⑤⑥ D.②③④⑤
3.已知反应2NO(g)+2H(g) N(g)+2HO(g) ΔH=-752 kJ/mol的反应机理如下:
2 2 2
①2NO(g) NO(g) (快)
2 2
②N O(g)+H(g) NO(g)+HO(g) (慢)
2 2 2 2 2
③NO(g)+H(g) N(g)+HO(g) (快)
2 2 2 2
下列有关说法错误的是
A.①的逆反应速率大于②的正反应速率
B.②中NO 与H 的碰撞仅部分有效
2 2 2
C.NO 和NO是该反应的催化剂
2 2 2
D.总反应中逆反应的活化能比正反应的活化能大
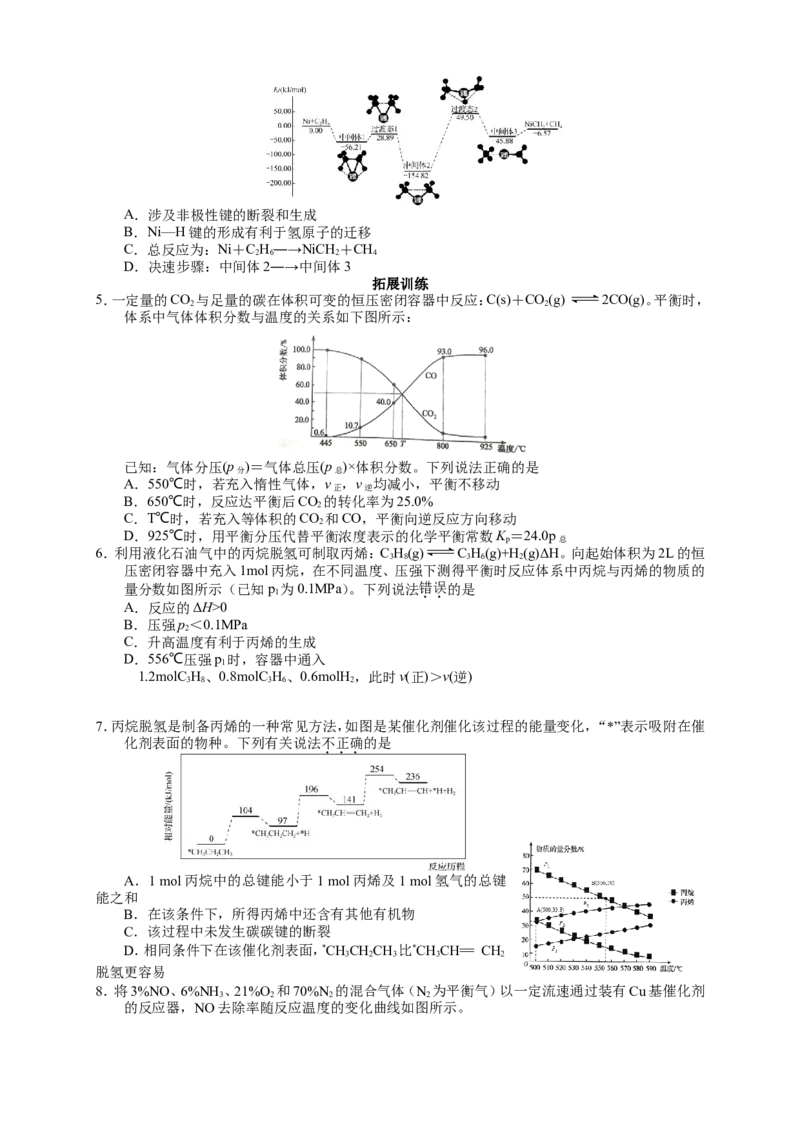
4.Ni可活化C H 放出CH,其反应历程如图所示。下列关于活化历程的说法错误的是
2 6 4A.涉及非极性键的断裂和生成
B.Ni—H键的形成有利于氢原子的迁移
C.总反应为:Ni+C H―→NiCH+CH
2 6 2 4
D.决速步骤:中间体2―→中间体3
拓展训练
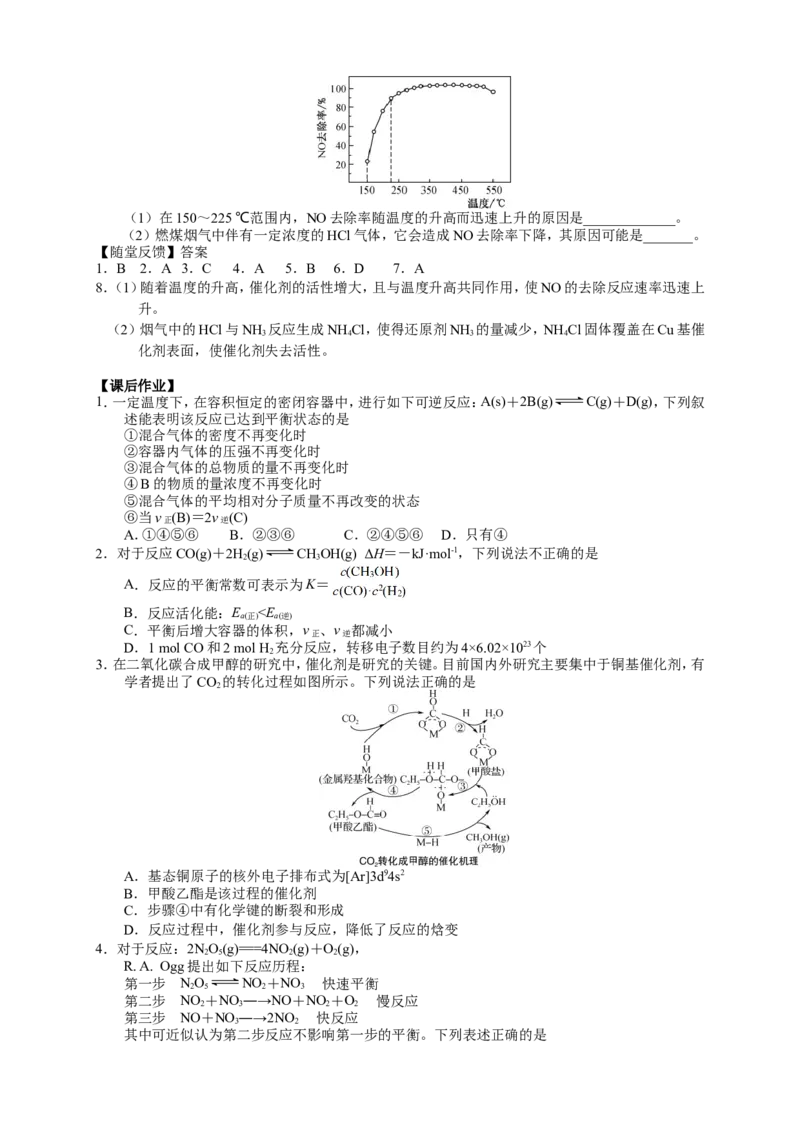
5.一定量的CO 与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO(g) 2CO(g)。平衡时,
2 2
体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(p )=气体总压(p )×体积分数。下列说法正确的是
分 总
A.550℃时,若充入惰性气体,v ,v 均减小,平衡不移动
正 逆
B.650℃时,反应达平衡后CO 的转化率为25.0%
2
C.T℃时,若充入等体积的CO 和CO,平衡向逆反应方向移动
2
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =24.0p
p 总
6.利用液化石油气中的丙烷脱氢可制取丙烯:C H(g) C H(g)+H(g)ΔH。向起始体积为2L的恒
3 8 3 6 2
压密闭容器中充入1mol丙烷,在不同温度、压强下测得平衡时反应体系中丙烷与丙烯的物质的
量分数如图所示(已知p 为0.1MPa)。下列说法错误的是
1
A.反应的ΔH>0
B.压强p<0.1MPa
2
C.升高温度有利于丙烯的生成
D.556℃压强p 时,容器中通入
1
1.2molC H、0.8molC H、0.6molH,此时v(正)>v(逆)
3 8 3 6 2
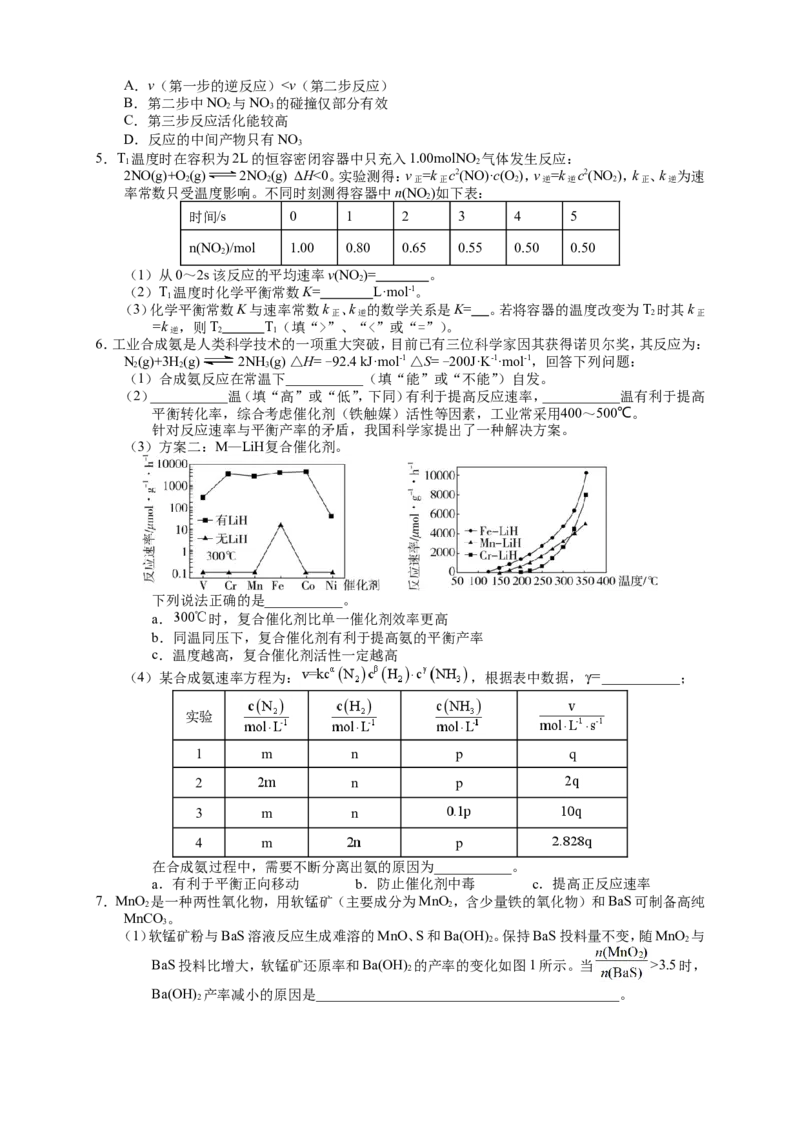
7.丙烷脱氢是制备丙烯的一种常见方法,如图是某催化剂催化该过程的能量变化,“*”表示吸附在催
化剂表面的物种。下列有关说法不正确的是
A.1 mol丙烷中的总键能小于1 mol丙烯及1 mol氢气的总键
能之和
B.在该条件下,所得丙烯中还含有其他有机物
C.该过程中未发生碳碳键的断裂
D.相同条件下在该催化剂表面,*CHCHCH 比*CHCH== CH
3 2 3 3 2
脱氢更容易
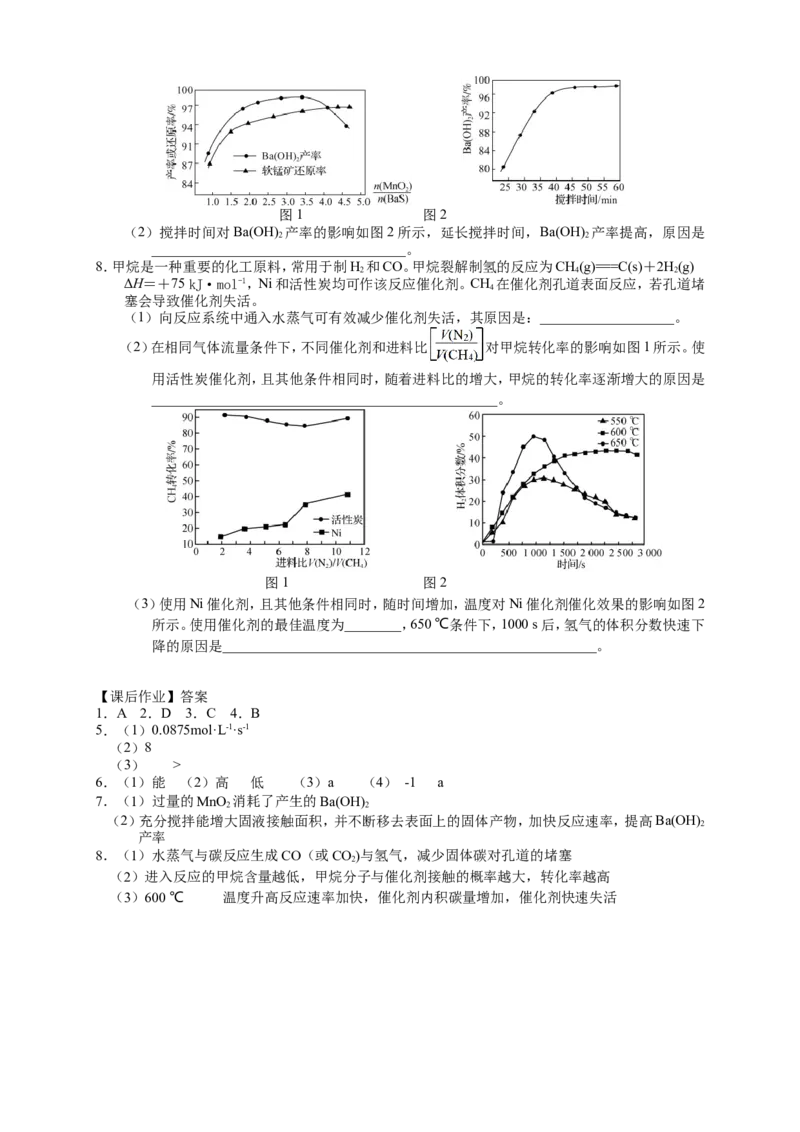
8.将3%NO、6%NH 、21%O 和70%N 的混合气体(N 为平衡气)以一定流速通过装有Cu基催化剂
3 2 2 2
的反应器,NO去除率随反应温度的变化曲线如图所示。(1)在150~225 ℃范围内,NO去除率随温度的升高而迅速上升的原因是_____________。
(2)燃煤烟气中伴有一定浓度的HCl气体,它会造成NO去除率下降,其原因可能是_______。
【随堂反馈】答案
1.B 2.A 3.C 4.A 5.B 6.D 7.A
8.(1)随着温度的升高,催化剂的活性增大,且与温度升高共同作用,使NO的去除反应速率迅速上
升。
(2)烟气中的HCl与NH 反应生成NH Cl,使得还原剂NH 的量减少,NH Cl固体覆盖在Cu基催
3 4 3 4
化剂表面,使催化剂失去活性。
【课后作业】
1.一定温度下,在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),下列叙
述能表明该反应已达到平衡状态的是
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当v (B)=2v (C)
正 逆
A.①④⑤⑥ B.②③⑥ C.②④⑤⑥ D.只有④
2.对于反应CO(g)+2H(g) CHOH(g) ΔH=-kJ·mol-1,下列说法不正确的是
2 3
A.反应的平衡常数可表示为K=
B.反应活化能:E ”、“<”或“=”)。
逆 2 1
6.工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为:
N(g)+3H (g) 2NH(g) △H= -92.4 kJ·mol-1 △S= -200J·K-1·mol-1,回答下列问题:
2 2 3
(1)合成氨反应在常温下___________(填“能”或“不能”)自发。
(2)___________温(填“高”或“低”,下同)有利于提高反应速率,___________温有利于提高
平衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用400~500℃。
针对反应速率与平衡产率的矛盾,我国科学家提出了一种解决方案。
(3)方案二:M—LiH复合催化剂。
下列说法正确的是___________。
a. 时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(4)某合成氨速率方程为: ,根据表中数据, ___________;
实验
1 m n p q
2 n p
3 m n
4 m p
在合成氨过程中,需要不断分离出氨的原因为___________。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
7.MnO 是一种两性氧化物,用软锰矿(主要成分为MnO ,含少量铁的氧化物)和BaS可制备高纯
2 2
MnCO 。
3
(1)软锰矿粉与BaS溶液反应生成难溶的MnO、S和Ba(OH) 。保持BaS投料量不变,随MnO 与
2 2
BaS投料比增大,软锰矿还原率和Ba(OH) 的产率的变化如图1所示。当 >3.5时,
2
Ba(OH) 产率减小的原因是___________________________________________。
2图1 图2
(2)搅拌时间对Ba(OH) 产率的影响如图2所示,延长搅拌时间,Ba(OH) 产率提高,原因是
2 2
____________________________________。
8.甲烷是一种重要的化工原料,常用于制H 和CO。甲烷裂解制氢的反应为CH(g)===C(s)+2H(g)
2 4 2
ΔH=+75 kJ·mol-1,Ni和活性炭均可作该反应催化剂。CH 在催化剂孔道表面反应,若孔道堵
4
塞会导致催化剂失活。
(1)向反应系统中通入水蒸气可有效减少催化剂失活,其原因是:___________________。
(2)在相同气体流量条件下,不同催化剂和进料比 对甲烷转化率的影响如图1所示。使
用活性炭催化剂,且其他条件相同时,随着进料比的增大,甲烷的转化率逐渐增大的原因是
_________________________________________________。
图1 图2
(3)使用Ni催化剂,且其他条件相同时,随时间增加,温度对Ni催化剂催化效果的影响如图2
所示。使用催化剂的最佳温度为________,650 ℃条件下,1000 s后,氢气的体积分数快速下
降的原因是_____________________________________________________。
【课后作业】答案
1.A 2.D 3.C 4.B
5.(1)0.0875mol·L-1·s-1
(2)8
(3) >
6.(1)能 (2)高 低 (3)a (4) -1 a
7.(1)过量的MnO 消耗了产生的Ba(OH)
2 2
(2)充分搅拌能增大固液接触面积,并不断移去表面上的固体产物,加快反应速率,提高Ba(OH)
2
产率
8.(1)水蒸气与碳反应生成CO(或CO)与氢气,减少固体碳对孔道的堵塞
2
(2)进入反应的甲烷含量越低,甲烷分子与催化剂接触的概率越大,转化率越高
(3)600 ℃ 温度升高反应速率加快,催化剂内积碳量增加,催化剂快速失活