文档内容
课时检测(四十七) 离子交换膜在电池中的应用
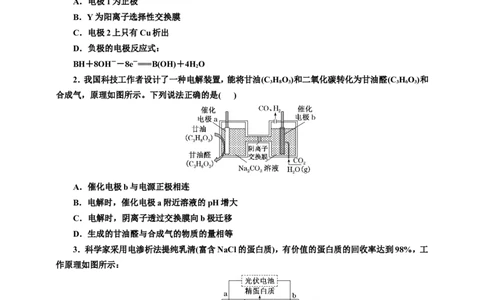
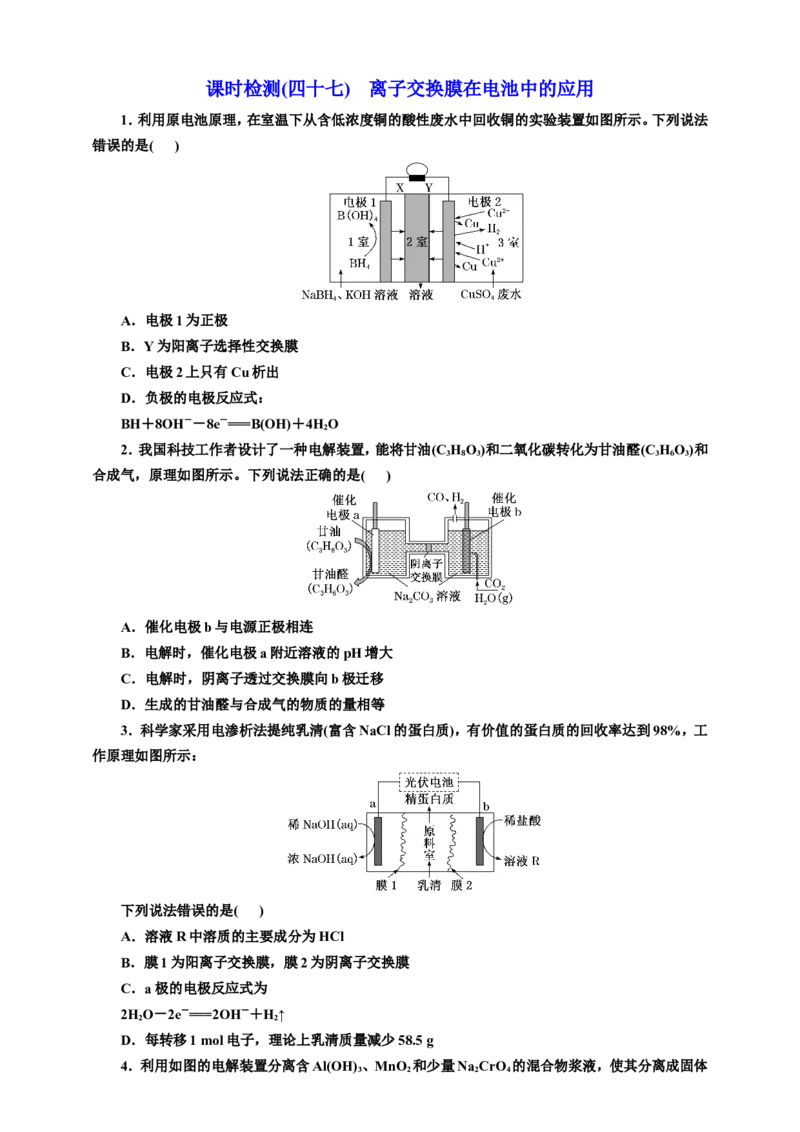
1.利用原电池原理,在室温下从含低浓度铜的酸性废水中回收铜的实验装置如图所示。下列说法
错误的是( )
A.电极1为正极
B.Y为阳离子选择性交换膜
C.电极2上只有Cu析出
D.负极的电极反应式:
BH+8OH--8e-===B(OH)+4HO
2
2.我国科技工作者设计了一种电解装置,能将甘油(C HO)和二氧化碳转化为甘油醛(C HO)和
3 8 3 3 6 3
合成气,原理如图所示。下列说法正确的是( )
A.催化电极b与电源正极相连
B.电解时,催化电极a附近溶液的pH增大
C.电解时,阴离子透过交换膜向b极迁移
D.生成的甘油醛与合成气的物质的量相等
3.科学家采用电渗析法提纯乳清(富含NaCl的蛋白质),有价值的蛋白质的回收率达到98%,工
作原理如图所示:
下列说法错误的是( )
A.溶液R中溶质的主要成分为HCl
B.膜1为阳离子交换膜,膜2为阴离子交换膜
C.a极的电极反应式为
2HO-2e-===2OH-+H↑
2 2
D.每转移1 mol电子,理论上乳清质量减少58.5 g
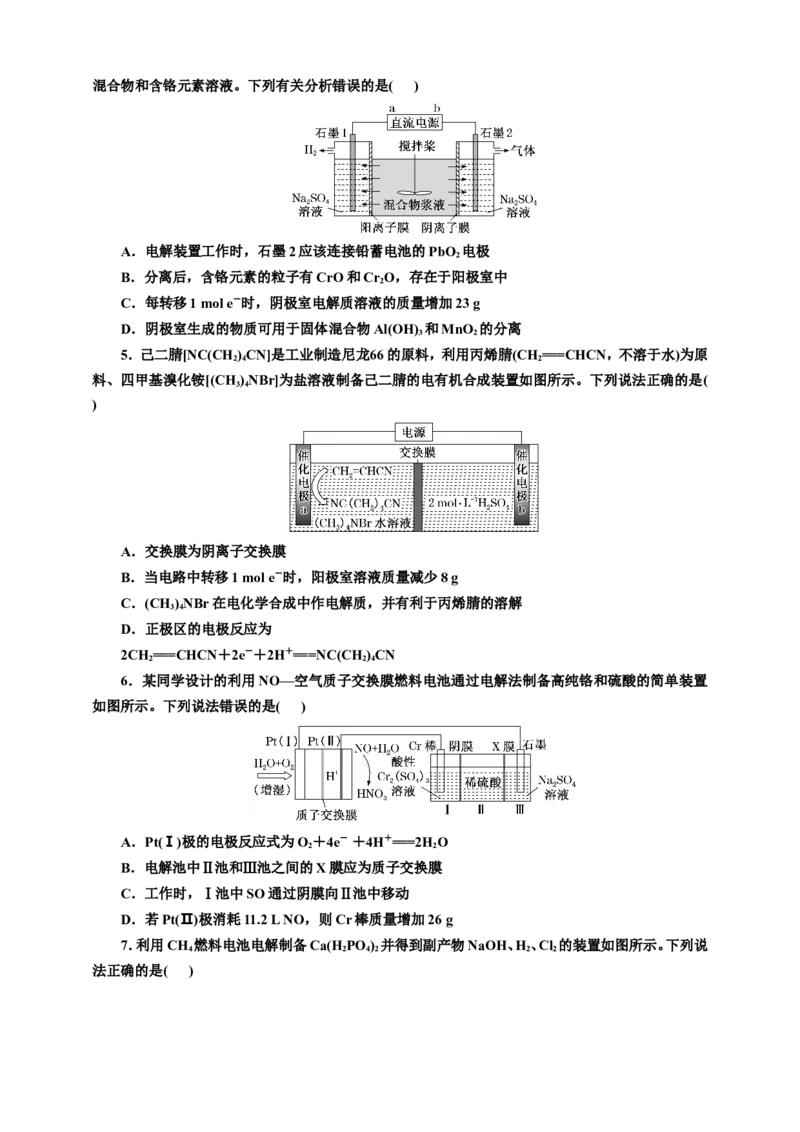
4.利用如图的电解装置分离含Al(OH) 、MnO 和少量Na CrO 的混合物浆液,使其分离成固体
3 2 2 4混合物和含铬元素溶液。下列有关分析错误的是( )
A.电解装置工作时,石墨2应该连接铅蓄电池的PbO 电极
2
B.分离后,含铬元素的粒子有CrO和CrO,存在于阳极室中
2
C.每转移1 mol e-时,阴极室电解质溶液的质量增加23 g
D.阴极室生成的物质可用于固体混合物Al(OH) 和MnO 的分离
3 2
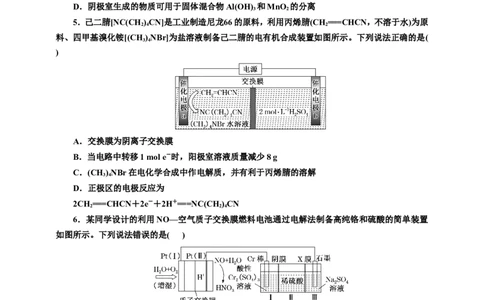
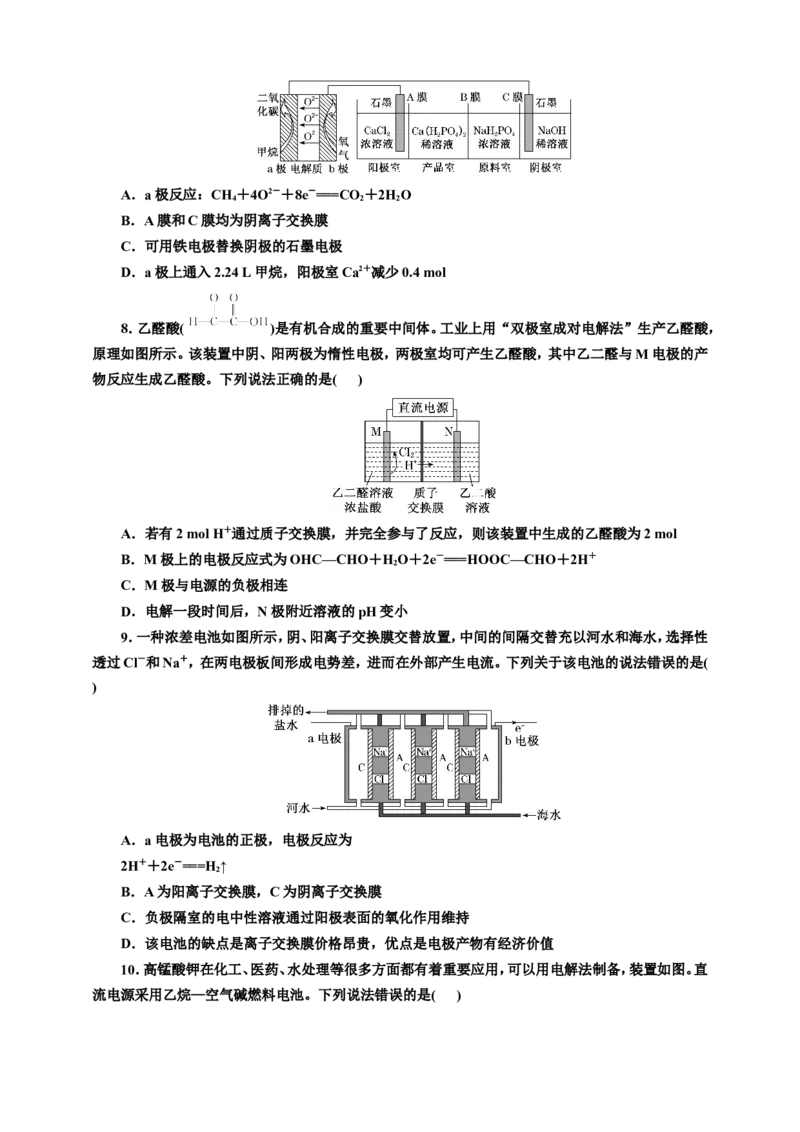
5.己二腈[NC(CH )CN]是工业制造尼龙66的原料,利用丙烯腈(CH===CHCN,不溶于水)为原
2 4 2
料、四甲基溴化铵[(CH)NBr]为盐溶液制备己二腈的电有机合成装置如图所示。下列说法正确的是(
3 4
)
A.交换膜为阴离子交换膜
B.当电路中转移1 mol e-时,阳极室溶液质量减少8 g
C.(CH)NBr在电化学合成中作电解质,并有利于丙烯腈的溶解
3 4
D.正极区的电极反应为
2CH ===CHCN+2e-+2H+===NC(CH )CN
2 2 4
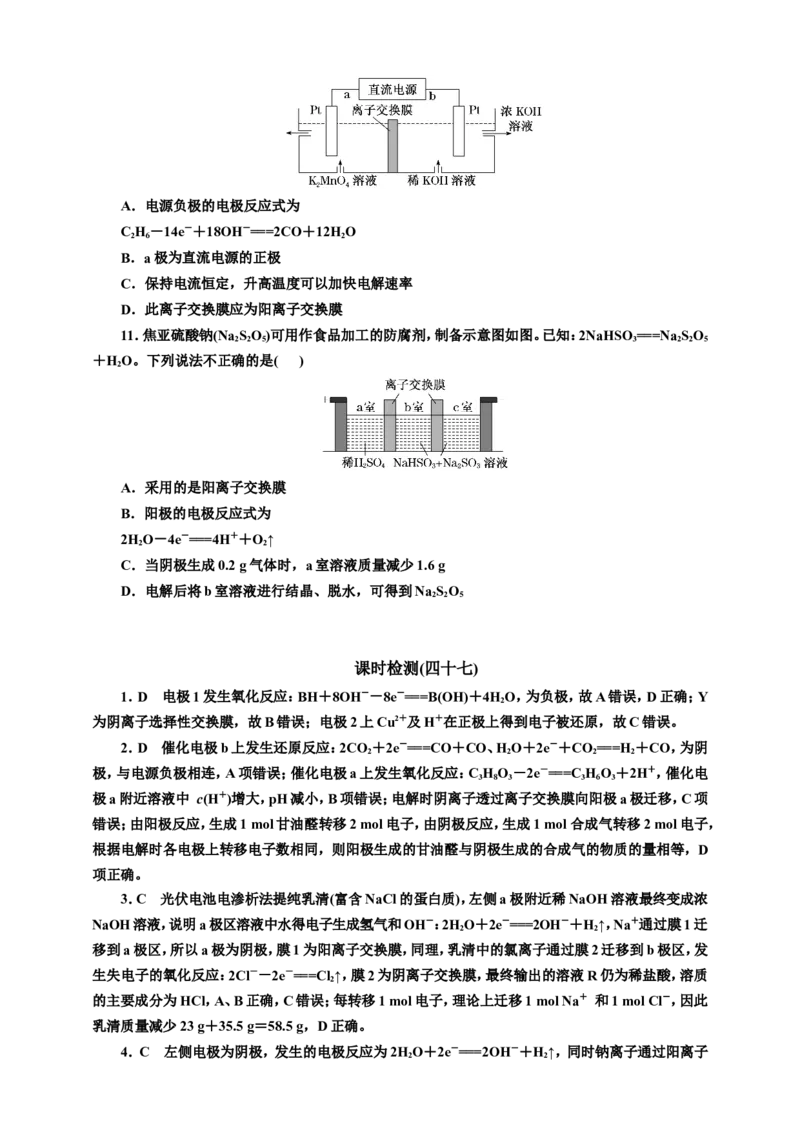
6.某同学设计的利用NO—空气质子交换膜燃料电池通过电解法制备高纯铬和硫酸的简单装置
如图所示。下列说法错误的是( )
A.Pt(Ⅰ)极的电极反应式为O+4e- +4H+===2H O
2 2
B.电解池中Ⅱ池和Ⅲ池之间的X膜应为质子交换膜
C.工作时,Ⅰ池中SO通过阴膜向Ⅱ池中移动
D.若Pt(Ⅱ)极消耗11.2 L NO,则Cr棒质量增加26 g
7.利用CH 燃料电池电解制备Ca(HPO) 并得到副产物NaOH、H、Cl 的装置如图所示。下列说
4 2 4 2 2 2
法正确的是( )A.a极反应:CH +4O2-+8e-===CO+2HO
4 2 2
B.A膜和C膜均为阴离子交换膜
C.可用铁电极替换阴极的石墨电极
D.a极上通入2.24 L甲烷,阳极室Ca2+减少0.4 mol
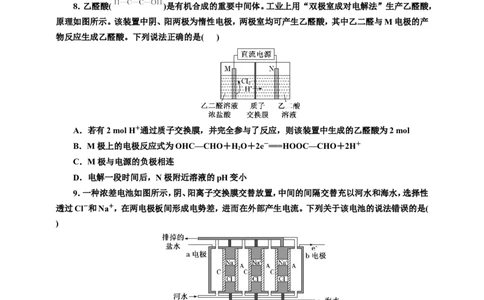
8.乙醛酸( )是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,
原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产
物反应生成乙醛酸。下列说法正确的是( )
A.若有2 mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为2 mol
B.M极上的电极反应式为OHC—CHO+HO+2e-===HOOC—CHO+2H+
2
C.M极与电源的负极相连
D.电解一段时间后,N极附近溶液的pH变小
9.一种浓差电池如图所示,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性
透过Cl-和Na+,在两电极板间形成电势差,进而在外部产生电流。下列关于该电池的说法错误的是(
)
A.a电极为电池的正极,电极反应为
2H++2e-===H ↑
2
B.A为阳离子交换膜,C为阴离子交换膜
C.负极隔室的电中性溶液通过阳极表面的氧化作用维持
D.该电池的缺点是离子交换膜价格昂贵,优点是电极产物有经济价值
10.高锰酸钾在化工、医药、水处理等很多方面都有着重要应用,可以用电解法制备,装置如图。直
流电源采用乙烷—空气碱燃料电池。下列说法错误的是( )A.电源负极的电极反应式为
CH-14e-+18OH-===2CO+12HO
2 6 2
B.a极为直流电源的正极
C.保持电流恒定,升高温度可以加快电解速率
D.此离子交换膜应为阳离子交换膜
11.焦亚硫酸钠(Na SO)可用作食品加工的防腐剂,制备示意图如图。已知:2NaHSO ===Na SO
2 2 5 3 2 2 5
+HO。下列说法不正确的是( )
2
A.采用的是阳离子交换膜
B.阳极的电极反应式为
2HO-4e-===4H++O↑
2 2
C.当阴极生成0.2 g气体时,a室溶液质量减少1.6 g
D.电解后将b室溶液进行结晶、脱水,可得到Na SO
2 2 5
课时检测(四十七)
1.D 电极1发生氧化反应:BH+8OH--8e-===B(OH)+4HO,为负极,故A错误,D正确;Y
2
为阴离子选择性交换膜,故B错误;电极2上Cu2+及H+在正极上得到电子被还原,故C错误。
2.D 催化电极b上发生还原反应:2CO +2e-===CO+CO、HO+2e-+CO ===H +CO,为阴
2 2 2 2
极,与电源负极相连,A项错误;催化电极a上发生氧化反应:CHO-2e-===C HO+2H+,催化电
3 8 3 3 6 3
极a附近溶液中 c(H+)增大,pH减小,B项错误;电解时阴离子透过离子交换膜向阳极a极迁移,C项
错误;由阳极反应,生成1 mol甘油醛转移2 mol电子,由阴极反应,生成1 mol 合成气转移2 mol电子,
根据电解时各电极上转移电子数相同,则阳极生成的甘油醛与阴极生成的合成气的物质的量相等,D
项正确。
3.C 光伏电池电渗析法提纯乳清(富含NaCl的蛋白质),左侧a极附近稀NaOH溶液最终变成浓
NaOH溶液,说明a极区溶液中水得电子生成氢气和OH-:2HO+2e-===2OH-+H↑,Na+通过膜1迁
2 2
移到a极区,所以a极为阴极,膜1为阳离子交换膜,同理,乳清中的氯离子通过膜2迁移到b极区,发
生失电子的氧化反应:2Cl--2e-===Cl↑,膜2为阴离子交换膜,最终输出的溶液R仍为稀盐酸,溶质
2
的主要成分为HCl,A、B正确,C错误;每转移1 mol电子,理论上迁移1 mol Na+ 和1 mol Cl-,因此
乳清质量减少23 g+35.5 g=58.5 g,D正确。
4.C 左侧电极为阴极,发生的电极反应为2HO+2e-===2OH-+H↑,同时钠离子通过阳离子
2 2膜进入阴极室,每转移1 mol e-,生成0.5 mol H ,同时有1 mol Na+进入阴极室,故阴极室电解质溶液
2
的质量增加23 g-1 g=22 g,C错误;右侧电极为阳极,铅蓄电池的PbO 电极为正极,故石墨2应该
2
连接铅蓄电池的PbO 电极,A正确;含铬元素的粒子有CrO和CrO,阴离子向阳极移动,分离后,存
2 2
在于阳极室中,B正确;阴极室生成的物质为氢氧化钠,氢氧化铝可溶于强碱氢氧化钠而二氧化锰不溶,
故可用于固体混合物Al(OH) 和MnO 的分离,D正确。
3 2
5.C 催化电极a:CH ===CHCN→NC(CH )CN,发生还原反应,为阴极,电极反应式为
2 2 4
2CH ===CHCN+2e-+2H+===NC(CH )CN,D错误;催化电极b为阳极,电极反应式为2HO-4e-
2 2 4 2
===O ↑+4H+,生成的氢离子由阳极区进入阴极区,故交换膜为阳离子交换膜,A错误;当电路中转移
2
1 mol e-时,阳极室生成氧气0.25 mol,质量为8 g,同时有1 mol H+进入阴极区,故溶液质量减少9 g,
B错误;丙烯腈为有机物,不溶于水,(CH)NBr在电化学合成中作电解质,并有利于丙烯腈的溶解,C
3 4
正确。
6.D Pt(Ⅱ)极:NO→HNO ,发生氧化反应,为负极,故Pt(Ⅰ)极为正极,电极反应式为O+4e-
3 2
+4H+===2H O,A选项正确;石墨电极为阳极,电极反应式为2HO-4e-===O ↑+4H+,生成的H+
2 2 2
通过X膜进入Ⅱ池中形成硫酸,故X膜为质子交换膜,B选项正确;工作时,Ⅰ池中SO通过阴膜向Ⅱ
池中移动形成硫酸,C选项正确;未标明气体所处环境的温度与压强,无法计算,D选项错误。
7.C a极为负极,负极上甲烷发生氧化反应,电极反应式为CH +4O2--8e-===CO+2HO,A
4 2 2
错误;利用CH 燃料电池电解制备Ca(HPO) 并得到副产物NaOH、H、Cl ,可知阳极室的电极反应
4 2 4 2 2 2
式为2Cl--2e-===Cl↑,则阳极室内钙离子向产品室移动,A膜为阳离子交换膜,阴极室的电极反应
2
式为2HO+2e-===2OH-+H↑,则原料室内钠离子向阴极室移动,C膜为阳离子交换膜,B错误;阴
2 2
极电极不参与反应,可用铁电极替换阴极的石墨电极,C正确;a极上通入 2.24 L甲烷,没有注明在标
准状况下,无法计算钙离子减少的物质的量,D错误。
8.A 有2 mol H+通过质子交换膜时,电池中转移2 mol电子,阴极的电极反应式为HOOC—
COOH+2H++2e-===HOOC—CHO+HO,阳极区的反应有2Cl--2e-===Cl↑、OHC—CHO+Cl
2 2 2
+HO===HOOC—CHO+2Cl- +2H+,两极各生成1 mol乙醛酸,共生成2 mol 乙醛酸,故A正确;
2
M极为电解池的阳极,氯离子在阳极上失电子发生氧化反应生成氯气,电极反应式为 2Cl--2e-
===Cl↑,然后氯气将乙二醛氧化为乙醛酸:OHC—CHO+Cl +HO===HOOC—CHO+2Cl- +2H
2 2 2
+,故B错误;M极为电解池的阳极,与电源的正极相连,故C错误;N极为电解池的阴极,若有2 mol
H+通过质子交换膜进入阴极室,则电池中转移2 mol电子,阴极的电极反应式为HOOC—COOH+
2H++2e-===HOOC—CHO+HO,消耗的H+与迁移过来的H+的物质的量相等,但乙二酸中羧基减
2
少了,N极附近溶液的pH不会减小,只会变大,故D错误。
9.B 由题图中电子的移动方向可以判断a电极为电池的正极,b电极为电池的负极,正极电极反
应为2H++2e-===H ↑,A正确;Na+向a电极方向移动,Cl-向b电极方向移动,故A为阴离子交换膜,
2
C为阳离子交换膜,B错误;通过负极表面的氧化作用,维持负极隔室溶液的电中性,C正确;离子交换
膜价格昂贵,但两极产物氢气、氯气是工业制盐酸等的原料,D正确。
10.C 电源负极上乙烷在碱性条件下失电子生成碳酸根离子,电极反应式为CH-14e-+18OH-
2 6
===2CO+12H O,A正确;左侧Pt电极为阳极,则a极为直流电源的正极,B正确;电解时保持电流恒
2
定,即单位时间内转移的电子数恒定,则消耗的反应物与产生的生成物的量恒定,也就是反应速率恒
定,与温度无关,C错误;右侧稀氢氧化钾溶液变为浓氢氧化钾溶液,右侧Pt电极为阴极,电极反应为
2HO+2e-===H ↑+2OH-,钾离子通过离子交换膜移向右侧,故该离子交换膜为阳离子交换膜,D正
2 2确。
11.C a室为阳极室,发生电极反应:2HO-4e-===4H++O↑,氧气从a室逸出,氢离子向b室
2 2
移动,则a室溶液减少的质量为水的质量,阴极发生还原反应,电极反应为2HO+2e-===H ↑+2OH
2 2
-,当生成0.2 g即0.1 mol氢气时,转移电子0.2 mol,根据电子守恒,a室消耗水的物质的量为 0.1 mol
,质量为0.1 mol×18 g·mol-1=1.8 g,故A、B正确,C错误;电解后在b室得到NaHSO 溶液,NaHSO
3 3
溶液经结晶脱水可得到Na SO,故D正确。
2 2 5