文档内容
课时检测(四十五) 电解池、金属的腐蚀与防护的基本知能评价
1.(2022·广东等级考)以熔融盐为电解液,以含Cu、Mg和Si等的铝合金废料为阳极进行电解,实
现Al的再生。该过程中( )
A.阴极发生的反应为Mg-2e-===Mg2+
B.阴极上Al被氧化
C.在电解槽底部产生含Cu的阳极泥
D.阳极和阴极的质量变化相等
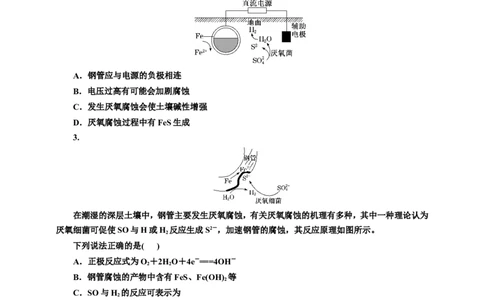
2.地下管道表面附着的硫酸盐会促进钢铁发生厌氧腐蚀,为减少腐蚀的发生,可使钢管与外接电
源相连,使其表面形成致密的FeO。下列说法错误的是( )
3 4
A.钢管应与电源的负极相连
B.电压过高有可能会加剧腐蚀
C.发生厌氧腐蚀会使土壤碱性增强
D.厌氧腐蚀过程中有FeS生成
3.
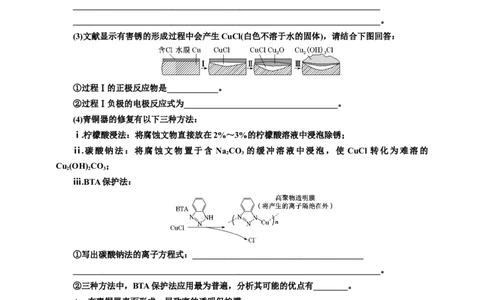
在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其中一种理论认为
厌氧细菌可促使SO与H或H 反应生成S2-,加速钢管的腐蚀,其反应原理如图所示。
2
下列说法正确的是( )
A.正极反应式为O+2HO+4e-===4OH-
2 2
B.钢管腐蚀的产物中含有FeS、Fe(OH) 等
2
C.SO与H 的反应可表示为
2
4H+SO-8e-=====S2-+4HO
2 2
D.向钢中加入Cu制成的合金可减缓钢管的腐蚀
4.关于下列装置分析正确的是( )
A.装置甲中阳极上析出红色物质B.若开始阶段两极质量相同,电流表中通过0.1 mol 电子时,装置甲中两极质量差为3.2 g
C.若装置乙通电一段时间后,撤去直流电源,电流表指针一定仍然偏转
D.可以将装置乙中的铜片更换为锌片制成镀锌铁
5.(2023·宁波一模)铝的冶炼在工业上通常采用电解Al O 的方法,装置示意图如图。研究表明,电
2 3
解AlCl NaCl熔融盐也可得到Al,熔融盐中铝元素主要存在形式为AlCl和Al Cl。下列说法不正确的
3 2
是( )
A.电解Al O 装置中B电极为阴极,发生还原反应
2 3
B.电解Al O 过程中碳素电极虽为惰性电极,但生产中会有损耗,需定期更换
2 3
C.电解AlCl NaCl时阴极反应式可表示为4Al Cl+3e-===Al+7AlCl
3 2
D.电解AlCl NaCl时AlCl从阳极流向阴极
3
6.厌氧性硫酸盐还原菌(SRB)是导致金属微生物腐蚀最为普遍的菌种,腐蚀过程如图所示。下列
说法正确的是( )
A.正极的电极反应式为8H++8e-===8H·(吸附)、SO+8H·(吸附)=====S2-+4HO
2
B.正极区溶液的pH变小
C.生成 1 mol FeS,转移6 mol电子
D.若引入新细菌,一定会加速金属的腐蚀
7.我国科学家利用电解法在常温常压下实现了氨的合成,该装置工作时阴极区的微观示意图如
下,其中电解液为溶解有三氟甲磺酸锂和乙醇的惰性有机溶剂。下列说法错误的是( )
A.三氟甲磺酸锂的作用是增强导电性
B.选择性透过膜允许N、NH 和HO通过
2 3 2
C.该装置用Au作催化剂,目的是降低N 的活化能
2
D.生成NH 的电极反应为
3
N+6CHOH+6e-===2NH+6CHO-
2 2 5 3 2 5
8.“修旧如旧”是文物保护的主旨。《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。
(1)查阅高中教材得知铜锈为Cu (OH) CO ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青
2 2 3
铜器的艺术价值。参与形成铜绿的物质有Cu和______________。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu (OH) CO 和Cu (OH) Cl。考
2 2 3 2 3
古学家将铜锈分为无害锈和有害锈,结构如图所示:
Cu (OH) CO 和Cu (OH) Cl分别属于无害锈和有害锈,请解释原因:_________
2 2 3 2 3
________________________________________________________________________
________________________________________________________________________。
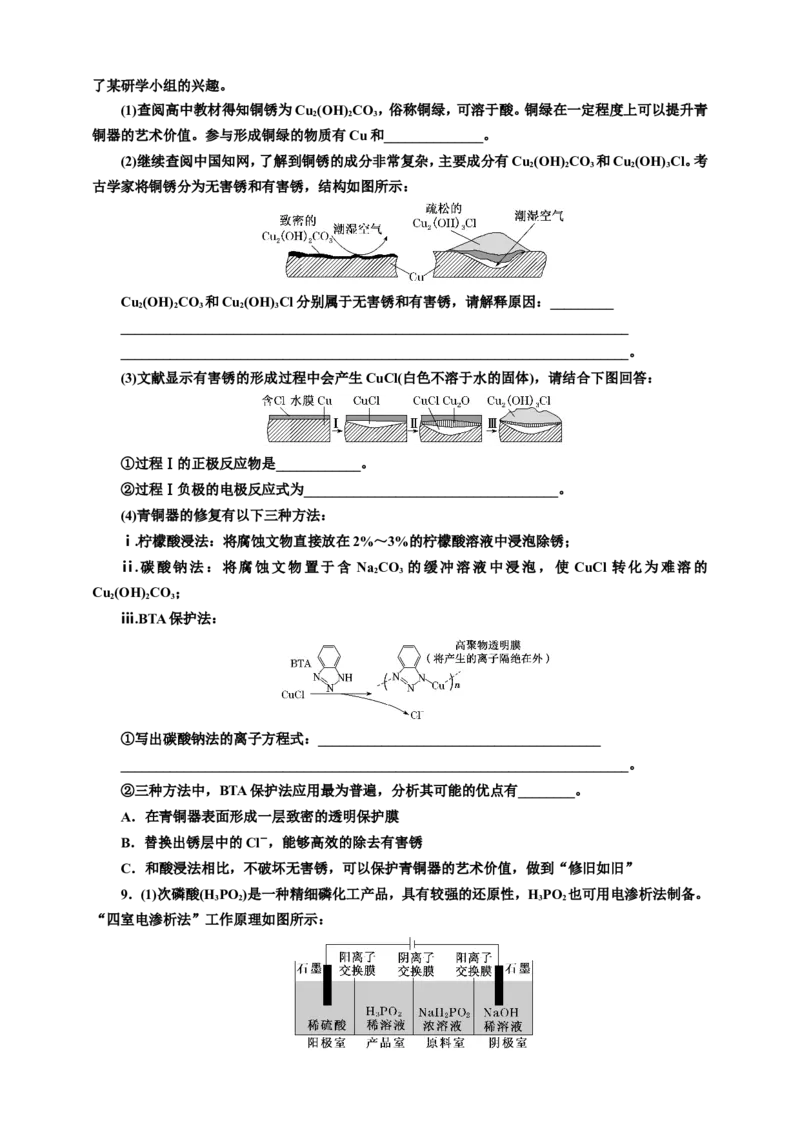
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
①过程Ⅰ的正极反应物是____________。
②过程Ⅰ负极的电极反应式为____________________________________。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%~3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含 Na CO 的缓冲溶液中浸泡,使 CuCl 转化为难溶的
2 3
Cu (OH) CO ;
2 2 3
ⅲ.BTA保护法:
①写出碳酸钠法的离子方程式:________________________________________
________________________________________________________________________。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有________。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
9.(1)次磷酸(H PO)是一种精细磷化工产品,具有较强的还原性,HPO 也可用电渗析法制备。
3 2 3 2
“四室电渗析法”工作原理如图所示:写出阳极的电极反应式:____________________________________________,
分析产品室可得到HPO 的原因:_______________________________________
3 2
________________________________________________________________________。
(2)利用如图所示装置电解制备NCl (氯的化合价为+1价),其原理是NH Cl+2HCl=====NCl +
3 4 3
3H↑ , b 电 极 接 电 源 的 ______( 填 “ 正 ” 或 “ 负 ” ) 极 , 阳 极 反 应 式 为
2
________________________________________________________________________。
(3)用NaOH溶液吸收烟气中的SO ,将所得的Na SO 溶液进行电解,可循环再生NaOH,同时得
2 2 3
到HSO ,其原理如图所示(电极材料为石墨):
2 4
图中 a 电极接电源的________(填“正”或“负”)极,SO 放电的电极反应式为
________________________________________________________________________,
从C口流出的物质是________,电解过程中,阴极区碱性明显增强,用平衡移动原理解释原因:
________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
课时检测(四十五)
1.C 阴极发生得电子的还原反应:Al3++3e-===Al,A、B错误;阳极材料中Cu和Si不参与氧化
反应,在电解槽底部可形成阳极泥,C正确;因为阳极除了铝参与电子转移,镁也参与了电子转移,且
还会形成阳极泥,而阴极只有铝离子得电子生成铝单质,根据电子转移数守恒及元素质量守恒可知,
阳极与阴极的质量变化不相等,D错误。
2.A 钢管表面形成FeO,失去电子,作为阳极,应与电源的正极相连,故A错误;电压过高,内
3 4
层金属可能会继续失电子被氧化,加剧腐蚀,故B正确;厌氧腐蚀中氢离子浓度减小,氢氧根离子浓度
增大,土壤碱性增强,故C正确;铁失电子生成Fe2+,与S2-生成FeS,故D正确。
3.B 在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,则正极反应式为2HO+2e-===H ↑+2OH
2 2
-,负极反应式为Fe-2e-===Fe2+,厌氧细菌可促使SO与H或H 反应生成S2-,S2-及正极上生成的
2
OH-与Fe2+可分别反应生成 FeS、Fe(OH) ,A错误,B正确;SO与H 的反应可表示为 4H +
2 2 2
SO=====S2-+4HO,C错误;向钢中加入铜发生电化学腐蚀时,铜作正极,Fe作负极,可加速钢管的
2腐蚀,D错误。
4.B 装置甲为电解池,右端石墨电极为阳极,氯离子发生氧化反应生成氯气,左端石墨电极为阴
极,铜离子发生还原反应生成铜单质,当转移0.1 mol电子时,左端石墨电极生成3.2 g铜单质,右端石
墨电极无固体析出,两极质量差为3.2 g,A错误、B正确;装置乙为电镀池,阳极电极反应式为Cu-2e
-===Cu2+,阴极电极反应式为Cu2++2e-===Cu,电解池工作一段时间后,铁表面会镀上一层铜,撤去
直流电源后无法形成原电池,电流表指针不会偏转,C错误;装置乙中,将铜片更换为锌片后,阳极的
电极反应式为Zn-2e-===Zn2+,氧化性:Zn2+