文档内容
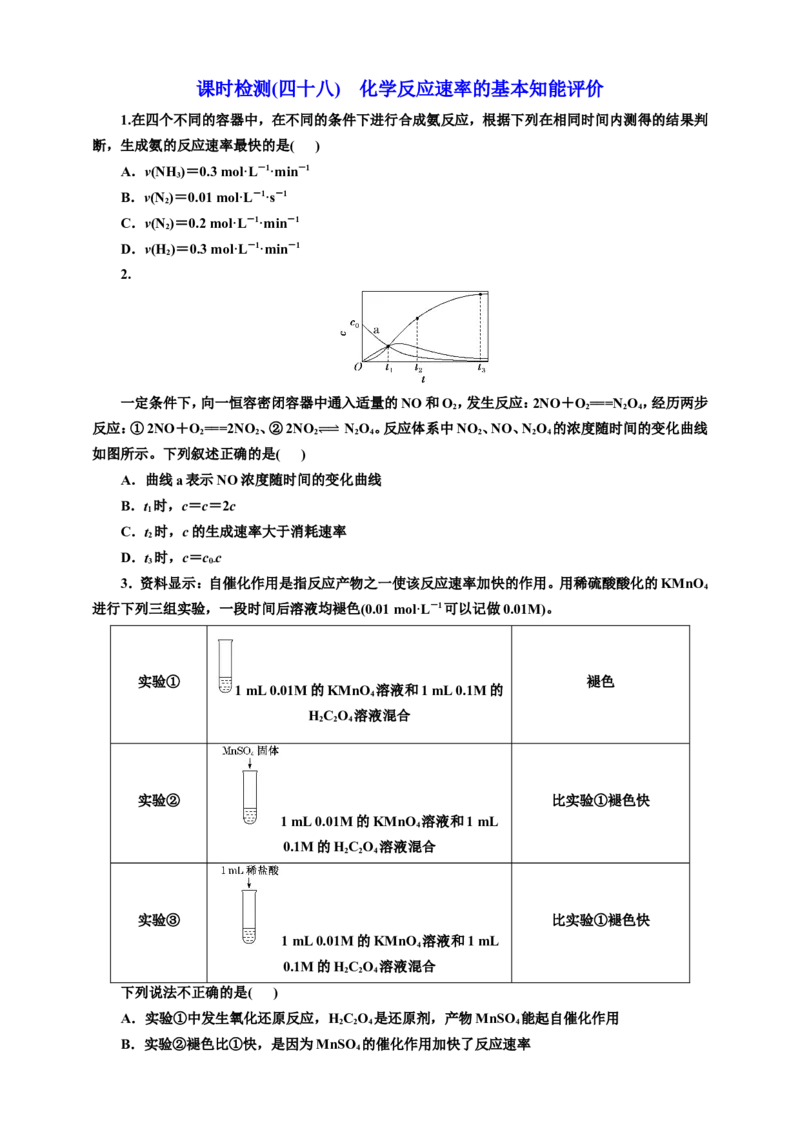
课时检测(四十八) 化学反应速率的基本知能评价
1.在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判
断,生成氨的反应速率最快的是( )
A.v(NH)=0.3 mol·L-1·min-1
3
B.v(N )=0.01 mol·L-1·s-1
2
C.v(N )=0.2 mol·L-1·min-1
2
D.v(H )=0.3 mol·L-1·min-1
2
2.
一定条件下,向一恒容密闭容器中通入适量的NO和O,发生反应:2NO+O===N O,经历两步
2 2 2 4
反应:①2NO+O===2NO、②2NO NO。反应体系中NO 、NO、NO 的浓度随时间的变化曲线
2 2 2 2 4 2 2 4
如图所示。下列叙述正确的是( )
⥫⥬
A.曲线a表示NO浓度随时间的变化曲线
B.t 时,c=c=2c
1
C.t 时,c的生成速率大于消耗速率
2
D.t 时,c=c c
3 0-
3.资料显示:自催化作用是指反应产物之一使该反应速率加快的作用。用稀硫酸酸化的KMnO
4
进行下列三组实验,一段时间后溶液均褪色(0.01 mol·L-1可以记做0.01M)。
实验① 褪色
1 mL 0.01M的KMnO 溶液和1 mL 0.1M的
4
HCO 溶液混合
2 2 4
实验② 比实验①褪色快
1 mL 0.01M的KMnO 溶液和1 mL
4
0.1M的HCO 溶液混合
2 2 4
实验③ 比实验①褪色快
1 mL 0.01M的KMnO 溶液和1 mL
4
0.1M的HCO 溶液混合
2 2 4
下列说法不正确的是( )
A.实验①中发生氧化还原反应,HCO 是还原剂,产物MnSO 能起自催化作用
2 2 4 4
B.实验②褪色比①快,是因为MnSO 的催化作用加快了反应速率
4C.实验③褪色比①快,是因为Cl-的催化作用加快了反应速率
D.若用1 mL 0.2M的HCO 做实验①,推测比实验①褪色快
2 2 4
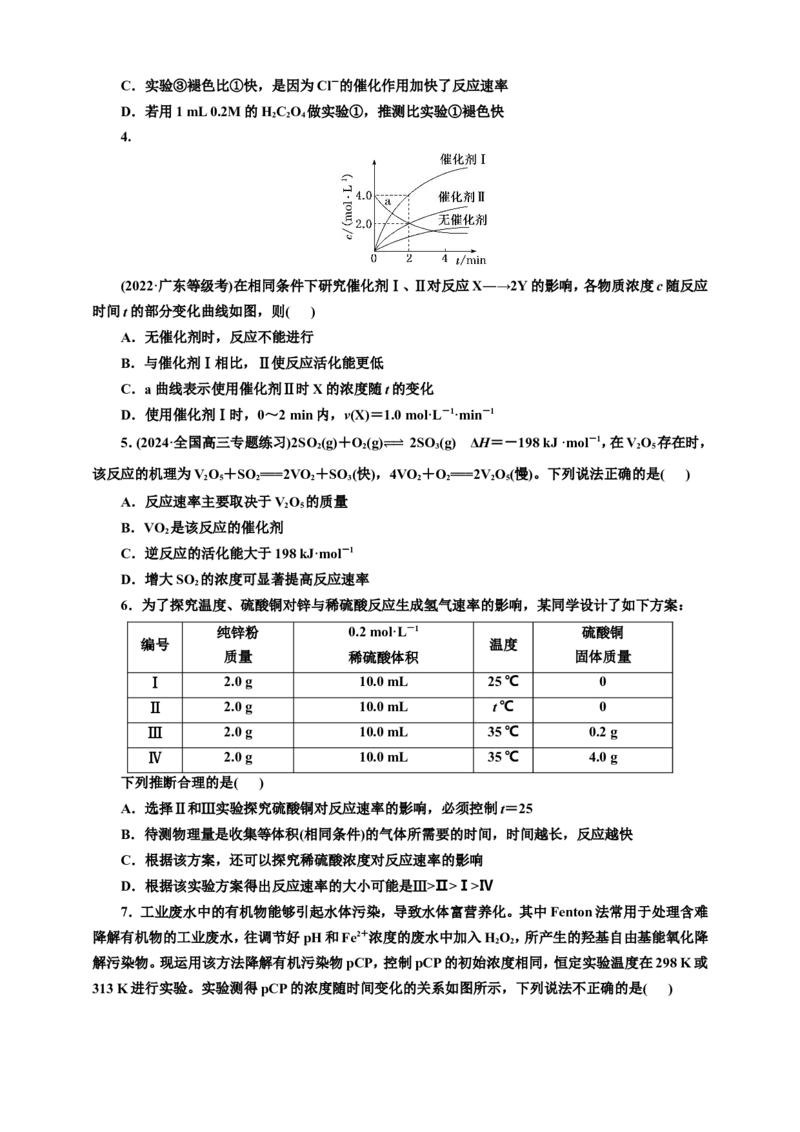
4.
(2022·广东等级考)在相同条件下研究催化剂Ⅰ、Ⅱ对反应X―→2Y的影响,各物质浓度c随反应
时间t的部分变化曲线如图,则( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1
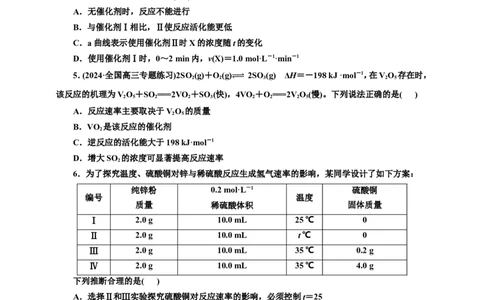
5.(2024·全国高三专题练习)2SO (g)+O(g) 2SO (g) ΔH=-198 kJ ·mol-1,在VO 存在时,
2 2 3 2 5
该反应的机理为VO+SO ===2VO+SO (快),⥫4⥬VO+O===2V O(慢)。下列说法正确的是( )
2 5 2 2 3 2 2 2 5
A.反应速率主要取决于VO 的质量
2 5
B.VO 是该反应的催化剂
2
C.逆反应的活化能大于198 kJ·mol-1
D.增大SO 的浓度可显著提高反应速率
2
6.为了探究温度、硫酸铜对锌与稀硫酸反应生成氢气速率的影响,某同学设计了如下方案:
纯锌粉 0.2 mol·L-1 硫酸铜
编号 温度
质量 稀硫酸体积 固体质量
Ⅰ 2.0 g 10.0 mL 25 ℃ 0
Ⅱ 2.0 g 10.0 mL t ℃ 0
Ⅲ 2.0 g 10.0 mL 35 ℃ 0.2 g
Ⅳ 2.0 g 10.0 mL 35 ℃ 4.0 g
下列推断合理的是( )
A.选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,必须控制t=25
B.待测物理量是收集等体积(相同条件)的气体所需要的时间,时间越长,反应越快
C.根据该方案,还可以探究稀硫酸浓度对反应速率的影响
D.根据该实验方案得出反应速率的大小可能是Ⅲ>Ⅱ>Ⅰ>Ⅳ
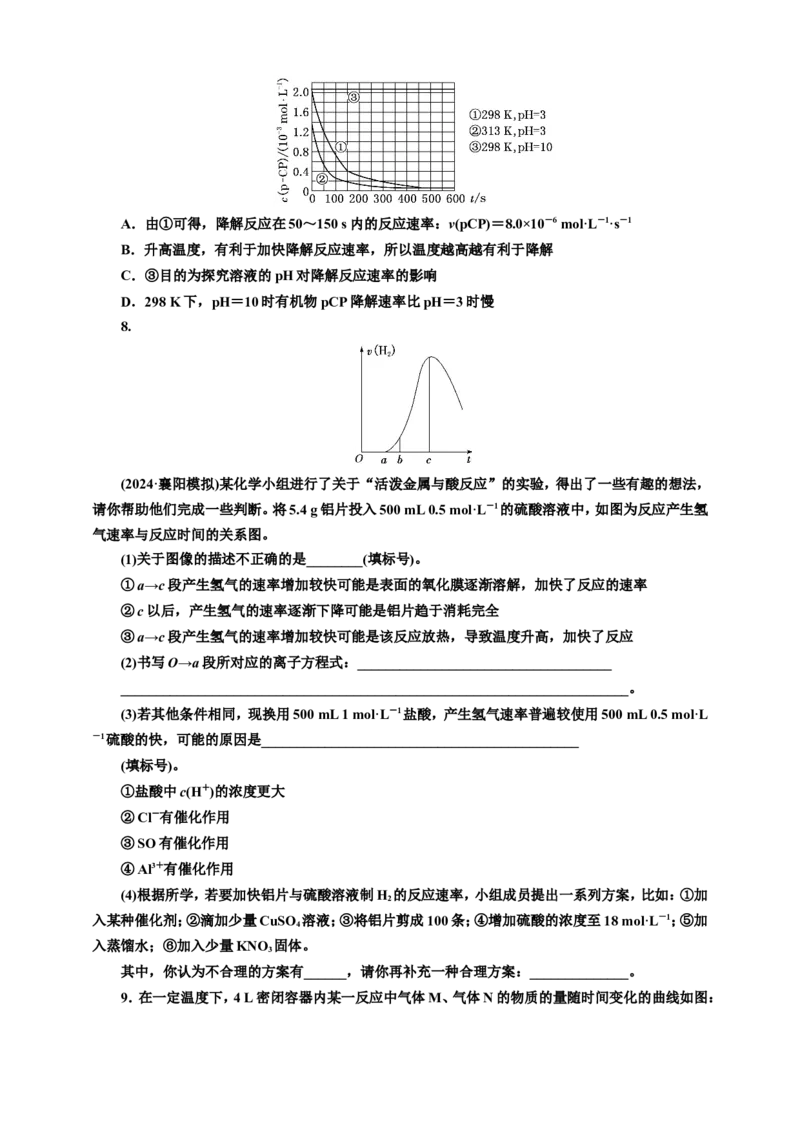
7.工业废水中的有机物能够引起水体污染,导致水体富营养化。其中Fenton法常用于处理含难
降解有机物的工业废水,往调节好pH和Fe2+浓度的废水中加入HO,所产生的羟基自由基能氧化降
2 2
解污染物。现运用该方法降解有机污染物pCP,控制pCP的初始浓度相同,恒定实验温度在298 K或
313 K进行实验。实验测得pCP的浓度随时间变化的关系如图所示,下列说法不正确的是( )A.由①可得,降解反应在50~150 s内的反应速率:v(pCP)=8.0×10-6 mol·L-1·s-1
B.升高温度,有利于加快降解反应速率,所以温度越高越有利于降解
C.③目的为探究溶液的pH对降解反应速率的影响
D.298 K下,pH=10时有机物pCP降解速率比pH=3时慢
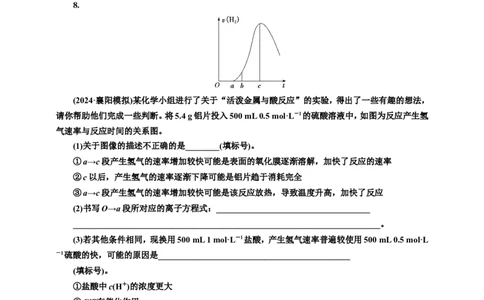
8.
(2024·襄阳模拟)某化学小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,
请你帮助他们完成一些判断。将5.4 g铝片投入500 mL 0.5 mol·L-1的硫酸溶液中,如图为反应产生氢
气速率与反应时间的关系图。
(1)关于图像的描述不正确的是________(填标号)。
①a→c段产生氢气的速率增加较快可能是表面的氧化膜逐渐溶解,加快了反应的速率
②c以后,产生氢气的速率逐渐下降可能是铝片趋于消耗完全
③a→c段产生氢气的速率增加较快可能是该反应放热,导致温度升高,加快了反应
(2)书写O→a段所对应的离子方程式:____________________________________
________________________________________________________________________。
(3)若其他条件相同,现换用500 mL 1 mol·L-1盐酸,产生氢气速率普遍较使用500 mL 0.5 mol·L
-1硫酸的快,可能的原因是_____________________________________________
(填标号)。
①盐酸中c(H+)的浓度更大
②Cl-有催化作用
③SO有催化作用
④Al3+有催化作用
(4)根据所学,若要加快铝片与硫酸溶液制H 的反应速率,小组成员提出一系列方案,比如:①加
2
入某种催化剂;②滴加少量CuSO 溶液;③将铝片剪成100条;④增加硫酸的浓度至18 mol·L-1;⑤加
4
入蒸馏水;⑥加入少量KNO 固体。
3
其中,你认为不合理的方案有______,请你再补充一种合理方案:______________。
9.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:(1)比较t 时刻,正逆反应速率大小:v ________v (填“>”“=”或“<”)。
2 正 逆
(2)若t=2 min,计算反应开始至t 时刻用M的浓度变化表示的平均反应速率为______。
2 2
(3)t 时刻化学反应达到平衡,反应物的转化率为________。
3
(4)如果升高温度,则v ________(填“增大”“减小”或“不变”)。
逆
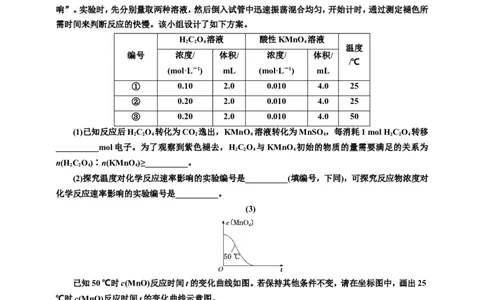
10.某小组利用HCO 溶液和酸性KMnO 溶液反应来探究“外界条件对化学反应速率的影
2 2 4 4
响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所
需时间来判断反应的快慢。该小组设计了如下方案。
HCO 溶液 酸性KMnO 溶液
2 2 4 4
温度
编号 浓度/ 体积/ 浓度/ 体积/
/℃
(mol·L-1) mL (mol·L-1) mL
① 0.10 2.0 0.010 4.0 25
② 0.20 2.0 0.010 4.0 25
③ 0.20 2.0 0.010 4.0 50
(1)已知反应后HCO 转化为CO 逸出,KMnO 溶液转化为MnSO ,每消耗1 mol H CO 转移
2 2 4 2 4 4 2 2 4
__________mol电子。为了观察到紫色褪去,HCO 与KMnO 初始的物质的量需要满足的关系为
2 2 4 4
n(H CO)∶n(KMnO )≥__________。
2 2 4 4
(2)探究温度对化学反应速率影响的实验编号是__________(填编号,下同),可探究反应物浓度对
化学反应速率影响的实验编号是__________。
(3)
已知50 ℃时c(MnO)反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25
℃时c(MnO)反应时间t的变化曲线示意图。
课时检测(四十八)
1.B 如果都用氢气表示反应速率,则根据方程式N+3H 2NH 以及反应速率之比是相应的化学
2 2 3
计量数之比,可知四个选项的反应速率分别是[mol·L-1·min⥫-⥬1]0.45、1.8、0.6、0.3,所以反应速率最快的
是选项B。
2.A NO 是中间产物,其浓度先增大后减小,曲线a代表NO,A项正确;根据题图可知,t 时,
2 1
NO、NO 、NO 的浓度相等,B项错误;t 时,NO 的浓度在减小,说明其生成速率小于消耗速率,C项
2 2 4 2 2
错误;根据题图可知,t 时,NO完全消耗,根据氮元素守恒,则c+2c=c,D项错误。
3 03.C 碳元素的化合价升高,且锰离子可作催化剂,则实验①中发生氧化还原反应,HCO 是还
2 2 4
原剂,故A正确;催化剂可加快反应速率,则实验②褪色比①快,是因为 MnSO 的催化作用加快了反
4
应速率,故B正确;高锰酸钾可氧化氯离子,则实验③褪色比①快,与催化作用无关,故C错误;增大
浓度,反应速率加快,则用1 mL 0.2M的HCO 做实验①,推测比实验①褪色快,故D正确。
2 2 4
4.D 由题图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也能进行,故A错
误;由题图可知,催化剂Ⅰ比催化剂Ⅱ催化效果好,说明催化剂Ⅰ使反应活化能更低,反应更快,故B
错误;由题图可知,使用催化剂Ⅱ时,在0~2 min内Y的浓度变化了2.0 mol·L-1,而a曲线表示的X
的浓度变化了2.0 mol·L-1,二者变化量之比不等于化学计量数之比,所以a曲线表示使用催化剂Ⅰ时
X浓度随时间t的变化,故C错误;使用催化剂Ⅰ时,在0~2 min内,Y的浓度变化了4.0 mol·L-1,则
v(X)=v(Y)==×=1.0 mol·L-1·min-1,故D正确。
5.C 由反应机理可得,VO 是该反应的催化剂,反应速率与催化剂VO 的质量有一定关系,但
2 5 2 5
主要取决于催化剂VO 的表面积,选项A错误;由反应机理可得,VO 是该反应的催化剂,VO 是该
2 5 2 5 2
反应的中间产物,选项B错误;ΔH=正反应的活化能-逆反应的活化能=-198 kJ·mol-1,所以逆反
应的活化能大于198 kJ·mol-1,选项C正确;使用催化剂可以显著提高反应速率,增大SO 的浓度可以
2
提高反应速率(不是显著提高),选项D错误。
6.D 若选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,Ⅱ的温度必须控制在35 ℃,A错误;收
集相同条件下等体积的气体所需的时间越长,则反应速率越慢,B错误;各组实验中稀硫酸的浓度均相
同,故无法探究稀硫酸浓度对反应速率的影响,C错误;实验Ⅱ的温度为35 ℃,则反应速率:Ⅱ>Ⅰ,实
验Ⅲ中锌与置换出的铜及稀硫酸构成原电池,使Ⅲ的反应速率比Ⅱ的快,实验Ⅳ中CuSO 用量过多,
4
置换出的铜可能覆盖在锌表面而阻止反应的进行,从而使Zn与HSO 反应速率大大减小,故四个反
2 4
应的反应速率的大小关系可能为Ⅲ>Ⅱ>Ⅰ>Ⅳ,D正确。
7.B 根据图像可知,曲线①中50 s时的浓度为1.2×10-3 mol·L-1,150 s时浓度为0.4×10-3 mol·L
-1,则50~150 s内的平均反应速率为 v(pCP)===8.0×10-6 mol·L-1·s-1,A正确;升高温度,有利于
加快降解反应速率,但温度过高时,过氧化氢不稳定易分解而导致降解反应速率减小,B错误;③目的
为探究溶液的pH对降解反应速率的影响,通过图像曲线变化可知,当pH=10时,随着时间的变化,
其浓度基本不变,即反应速率趋向于零,C正确;根据曲线③可以得出,该反应在pH=10的溶液中基
本停止,故在298 K下,pH=10时有机物pCP降解速率比pH=3时慢,D正确。
8.解析:(1)在反应的后期,由于硫酸的浓度逐渐降低,导致反应速率逐渐降低。铝是固体,其质量
多少不能影响反应速率,所以②是错误的。(2)铝是活泼的金属,极易被氧化生成一层致密的氧化膜,所
以开始没有氢气产生,是因为硫酸和氧化铝反应导致的,方程式为Al O+6H+===2Al3++3HO。(3)
2 3 2
根据浓度可知氢离子的浓度是相同的,所以①不正确;反应中都生成铝离子,④不正确;由于酸中阴离
子是不同的,盐酸反应快,这说明Cl- 有催化作用,或者是SO有阻化作用,③不正确,②正确。(4)一
般增大反应物的浓度、升高温度、加入催化剂、形成原电池、增大反应物的接触面积等都能加快反应速
率。浓硫酸和铝不能产生氢气,④不正确;⑤是稀释降低氢离子浓度,反应速率降低;在酸性溶液中,硝
酸钾能和铝反应,但产生的气体是NO,而不是氢气,⑥不正确。
答案:(1)② (2)AlO+6H+===2Al3++3HO (3)②
2 3 2
(4)④⑤⑥ 升高温度(或适当增加HSO 浓度)(任填一种)
2 4
9.解析:(1)t 时刻,反应物逐渐减少,生成物逐渐增多,反应未达到平衡且正向进行,v >v 。(2)v
2 正 逆
===0.25 mol·L-1·min-1。(3)t 时刻化学反应达到平衡,剩余2 mol N,转化率为×100%=75%。(4)升
3高温度,反应速率增大。
答案:(1)> (2)0.25 mol·L-1·min-1 (3)75% (4)增大
10.解析:(1)H CO 中碳的化合价是+3价,CO 中碳的化合价为+4价,故每消耗1 mol H CO
2 2 4 2 2 2 4
转移2 mol 电子,配平反应的化学方程式为 2KMnO +5HCO +3HSO ===K SO +2MnSO +
4 2 2 4 2 4 2 4 4
10CO ↑+8HO,为保证KMnO 完全反应,需要满足c(H CO)∶c(KMnO )≥2.5。(2)探究温度对反应
2 2 4 2 2 4 4
速率的影响,则浓度必然相同,则为实验②和③;同理探究浓度对反应速率的影响的实验是①和②。(3)
温度降低,化学反应速率减小,故KMnO 褪色时间延长,故作图时要同时体现25 ℃ MnO浓度降低
4
比50 ℃时MnO的浓度降低缓慢和反应完全时间比50 ℃时“拖后”。
答案:(1)2 2.5 (2)②和③ ①和②
(3)
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\4\\24YLCXHXⅡ6-8.TIF" \*
MERGEFORMATINET