文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练04 14道选择题+主观有机题
完卷时间:40分钟
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 A C C D A C B B A D B C C B
一、选择题(只有1个正确选项)
1.化学与生产生活密切相关。下列说法错误的是
A.用CaSO 来减轻盐碱地(含NaCO)的碱性,利用了CaSO 溶于水显酸性
4 2 3 4
B.波尔多液(含有CuSO)含有重金属离子,可用作植物体表面的杀菌剂
4
C.O、Cl的某些单质或两元素之间形成的某种化合物均可作水的消毒剂
D.实验室中,温度计不慎被打破,散落的水银应用硫粉处理后收集
【答案】A
【解析】A.盐碱地(含较多NaCl、NaCO )的碱性是由 离子的水解引起的,加入CaSO
2 3 4
后,发生沉淀转化:能将NaCO 中的 沉淀为CaCO 沉淀,从而降低盐碱地的碱性,而
2 3 3
不是由于CaSO 溶于水显酸性所致,A错误;B.波尔多液是利用胆矾与熟石灰、水按照一
4
定比例混合得到的混合物,其中含有重金属阳离子Cu2+,Cu2+能够使细菌的蛋白质发生变性
而失去生理活性,从而抑制病原菌孢子萌发或菌丝生长,故可用作植物体表面的杀菌剂,B
正确;C.O、Cl、ClO 都具有强氧化性,能够使细菌、病毒蛋白质氧化变性而失去其生理
3 2 2
活性,故均可作水的消毒剂,C正确;D.Hg具有挥发性,容易被人吸收导致中毒,其能够
与S在室温下反应产生HS,因此实验室中,若温度计不慎被打破,其中散落的水银应用硫
2
粉处理后收集,防止空气污染导致人中毒事件的发生,D正确;故合理选项是A。
2.工业上制备硝酸的关键反应为 ,下列有关化学用语错误
的是
A. 的电子式为 B.基态O的电子排布式为C. 的 模型为 D. 属于极性分子
【答案】C
【解析】A. 为共价化合物,电子式为 ,A正确;B.氧为8号元素,基
态O的电子排布式为 ,B正确;C.HO分子中中心O原子价层电子对数为2+
2
=4, 模型为四面体形,C错误;D. 分子中正负电荷重心不重合,属于极性分
子,D正确;故选C。
3.设 为阿伏加德罗常数的值。下列说法正确的是
A.1mol 含有的共价键数为
B.1L 溶液中含有 总数为
C.标准状况下,11.2L 含有的电子数大于
D.向 盐酸溶液中通氨气至中性, 的数目大于
【答案】C
【解析】A.根据NH 的结构可知,1mol的NH 中含有共价键的数目为 , A选项错误;
2 4 2 4
B.氢硫酸是弱酸,电离程度小,1L 溶液中含有 总数远小于 ,B选
项错误;C.1个水分子含10个电子,标准状况下,11.2L 不是气体、其物质的量远大
于0.5mol,则含有的电子数大于 ,C选项正确;D.溶液体积不知道,不能计算铵离子
数目,D选项错误;答案选C。
4.下列实验操作及所选实验装置均正确的是A.海带提碘实验中使用装置甲将海带灼烧成灰
B.配制NaOH溶液过程中使用装置乙将NaOH固体溶解
C.用NaOH溶液分离乙醇和乙酸乙酯的混合物使用装置丙
D. 标准溶液滴定亚铁盐实验,滴定结束时如图丁所示读数
【答案】D
【解析】A.海带提碘实验中使用坩埚将海带灼烧成灰,A错误;B.容量瓶不能用于溶解
和稀释,只能配制一定物质的量浓度的溶液,应先在烧杯中溶解NaOH固体,冷却至室温后
再转移至容量瓶,B错误;C.用NaOH溶液会使乙酸乙酯水解,应用饱和碳酸钠溶液,C错
误;D.酸性高锰酸钾用酸式滴定管,读数时视线与凹液面相平,D正确;故选D。
5.下列化学反应与方程式不相符的是
A.向银氨溶液中加入过量盐酸:
B. 溶液中加入 产生沉淀:
C.将二氧化硫通入氢硫酸中产生黄色沉淀:
D.乙醇与 酸性溶液反应:
【答案】A
【解析】A.银氨溶液中存在[Ag(NH) ] +,银氨溶液滴加盐酸,生成氯化银沉淀,离子方
3 2
程式为:[Ag(NH) ] ++OH-+3H++Cl-=AgCl↓+2 +2HO,故A错误;B.FeSO 溶液中加入
3 2 2 4
HO 产生氢氧化铁沉淀,其反应的离子方程式为:2Fe2++HO+4HO═2Fe(OH)↓+4H+,故B
2 2 2 2 2 3
正确;C.将二氧化硫通入氢硫酸中产生黄色沉淀,化学方程式为:2HS+SO=3S↓+2HO,
2 2 2
故C正确;D.乙醇被酸性重铬酸钾氧化为乙酸、铬离子和水,离子方程式为:
,故D正确;故选:A。
6.某种双核钴配合物阳离子的结构如图。X的第一电离能在第二周期主族元素中位居第二,
Y的核外电子只有一种运动状态,Z的一种同素异形体是极性分子。下列说法错误的是A.简单氢化物的稳定性:Z>X
B.电负性:Z>X>Y
C.Co位于元素周期表ds区,在该阳离子中呈+2价
D.从结构推测该配合物阳离子不稳定,且具有一定的氧化性
【答案】C
【分析】X的第一电离能在第二周期主族元素中位居第二,X为N,Y的核外电子只有一种
运动状态,Y为H;Z的一种同素异形体是极性分子,即Z为O,O 为极性分子。
3
【解析】A.非金属性:Z(O)>X(N),因此简单氢化物的稳定性:Z>X,故A正确;B.
同周期元素,从左往右电负性逐渐增大,同族元素,从上到下电负性逐渐减小,即电负性:
Z(O)>X(N)>Y(H),故B正确;C.Co位于元素周期表d区,故C错误;D.该配合物
阳离子存在过氧键,因此不稳定,且具有一定的氧化性,故D正确;故选C。
7.利用硼烷独特温和的化学选择性可还原羧酸﹐其机理如下:
下列说法错误的是
A.过程①的进行与硼原子的缺电子有关
B.整个过程中硼的杂化方式不发生改变
C.过程⑥的反应类型属于取代反应
D.根据上述机理猜测硼烷还可还原酯基
【答案】B
【解析】A.过程①的进行与硼原子的缺电子有关,B提供空轨道,O提供孤电子对,形成
配位键,A正确;B.反应①得到的产物中硼原子为sp3杂化,而BH 中硼原子属于sp2杂化,
3
则整个过程中的杂化方式发生改变,B错误;C.过程⑥是R-CHOBH 与HO发生取代反应生
2 2 2
成RCHOH和BH(OH),反应类型属于取代反应,C正确;D.根据上述机理,硼烷作用于碳
2 2
氧双键,则猜测硼烷还可还原酯基,D正确;答案选B。
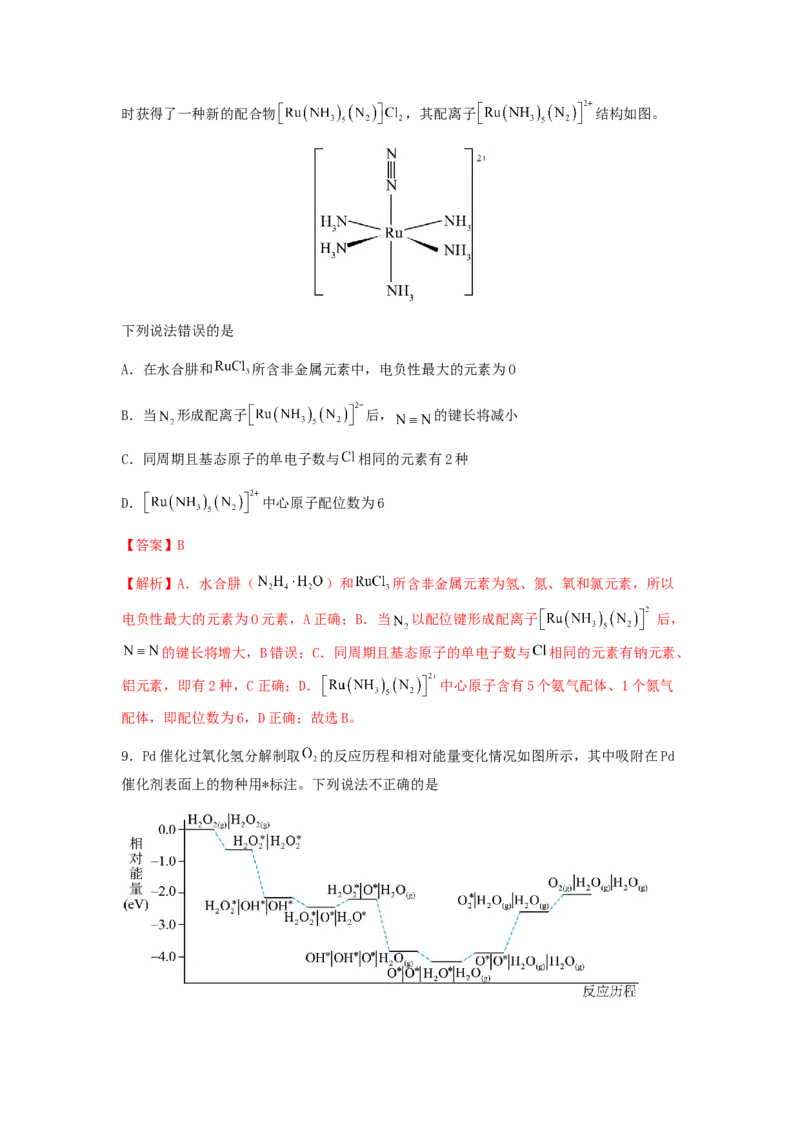
8.过渡元素钉(Ru)及其化合物用途广泛。利用水合肼( )还原时获得了一种新的配合物 ,其配离子 结构如图。
下列说法错误的是
A.在水合肼和 所含非金属元素中,电负性最大的元素为O
B.当 形成配离子 后, 的键长将减小
C.同周期且基态原子的单电子数与 相同的元素有2种
D. 中心原子配位数为6
【答案】B
【解析】A.水合肼( )和 所含非金属元素为氢、氮、氧和氯元素,所以
电负性最大的元素为O元素,A正确;B.当 以配位键形成配离子 后,
的键长将增大,B错误;C.同周期且基态原子的单电子数与 相同的元素有钠元素、
铝元素,即有2种,C正确;D. 中心原子含有5个氨气配体、1个氮气
配体,即配位数为6,D正确;故选B。
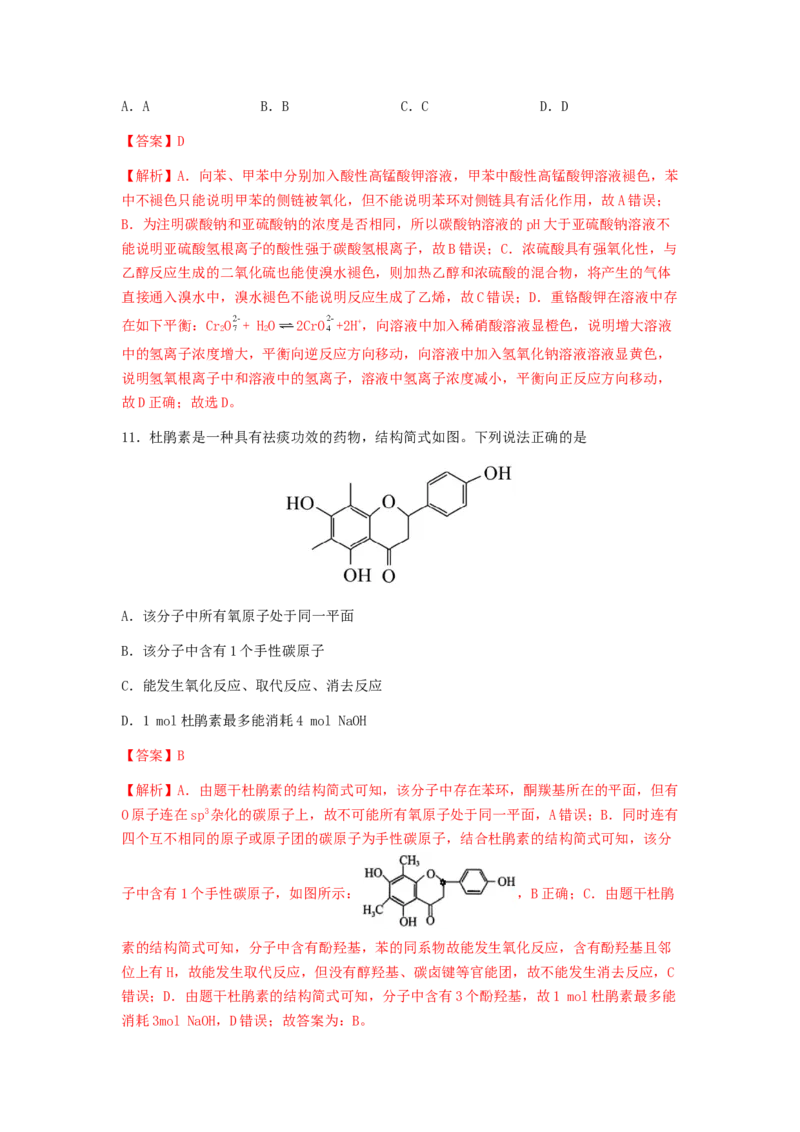
9.Pd催化过氧化氢分解制取 的反应历程和相对能量变化情况如图所示,其中吸附在Pd
催化剂表面上的物种用*标注。下列说法不正确的是A.该反应历程中所有步骤均是放热过程
B. 的总键能大于 的总键能
C.催化剂Pd降低了 分解反应的活化能,加快了 的分解速率
D.整个催化分解过程中既有极性键的断裂和形成,也有非极性键的断裂和形成
【答案】A
【解析】A.从图知,该反应历程中,有一些步骤是吸热过程(相对能量升高),也有一些步
骤是放热过程(相对能量降低),A符合题意;B.从图中可知总反应为放热反应,即 =反
应物总键能-生成物总键能<0,则生成物总键能大于反应物总键能, 的
总键能大于 的总键能,B不符合题意;C.Pd为催化剂,能降低该分解反应
的活化能,加快分解速率,C不符合题意;D.Pd催化过氧化氢分解制取 的方程式:
,整个催化分解过程中既有极性键H-O键的断裂和形成,也有非极性
键O-O键的断裂和O=O键的形成,D不符合题意;故选A。
10.下列各实验操作、现象及对应结论都正确的是
选
实验操作 现象 对应结论
项
向苯、甲苯中分别加入酸性高锰酸 甲苯中酸性高锰酸钾溶 苯环对侧链具有
A
钾溶液 液褪色,苯中不褪色 活化作用
大小:
25℃时,用 试纸测 溶 酸性强弱:
B
液和 溶液的
加热乙醇和浓硫酸的混合物,将产
C 溴水褪色 反应生成了乙烯
生的气体直接通入溴水中
①②两支试管中均盛有
溶液,向①
对该反应
试管①中溶液显橙色,
D 中加入数滴 溶液, 的化学平衡产生
试管②中溶液显黄色
影响
向②中加入数滴 溶
液,冷却后观察现象A.A B.B C.C D.D
【答案】D
【解析】A.向苯、甲苯中分别加入酸性高锰酸钾溶液,甲苯中酸性高锰酸钾溶液褪色,苯
中不褪色只能说明甲苯的侧链被氧化,但不能说明苯环对侧链具有活化作用,故A错误;
B.为注明碳酸钠和亚硫酸钠的浓度是否相同,所以碳酸钠溶液的pH大于亚硫酸钠溶液不
能说明亚硫酸氢根离子的酸性强于碳酸氢根离子,故B错误;C.浓硫酸具有强氧化性,与
乙醇反应生成的二氧化硫也能使溴水褪色,则加热乙醇和浓硫酸的混合物,将产生的气体
直接通入溴水中,溴水褪色不能说明反应生成了乙烯,故C错误;D.重铬酸钾在溶液中存
在如下平衡:CrO + HO 2CrO +2H+,向溶液中加入稀硝酸溶液显橙色,说明增大溶液
2 2
中的氢离子浓度增大,平衡向逆反应方向移动,向溶液中加入氢氧化钠溶液溶液显黄色,
说明氢氧根离子中和溶液中的氢离子,溶液中氢离子浓度减小,平衡向正反应方向移动,
故D正确;故选D。
11.杜鹃素是一种具有祛痰功效的药物,结构简式如图。下列说法正确的是
A.该分子中所有氧原子处于同一平面
B.该分子中含有1个手性碳原子
C.能发生氧化反应、取代反应、消去反应
D.1 mol杜鹃素最多能消耗4 mol NaOH
【答案】B
【解析】A.由题干杜鹃素的结构简式可知,该分子中存在苯环,酮羰基所在的平面,但有
O原子连在sp3杂化的碳原子上,故不可能所有氧原子处于同一平面,A错误;B.同时连有
四个互不相同的原子或原子团的碳原子为手性碳原子,结合杜鹃素的结构简式可知,该分
子中含有1个手性碳原子,如图所示: ,B正确;C.由题干杜鹃
素的结构简式可知,分子中含有酚羟基,苯的同系物故能发生氧化反应,含有酚羟基且邻
位上有H,故能发生取代反应,但没有醇羟基、碳卤键等官能团,故不能发生消去反应,C
错误;D.由题干杜鹃素的结构简式可知,分子中含有3个酚羟基,故1 mol杜鹃素最多能
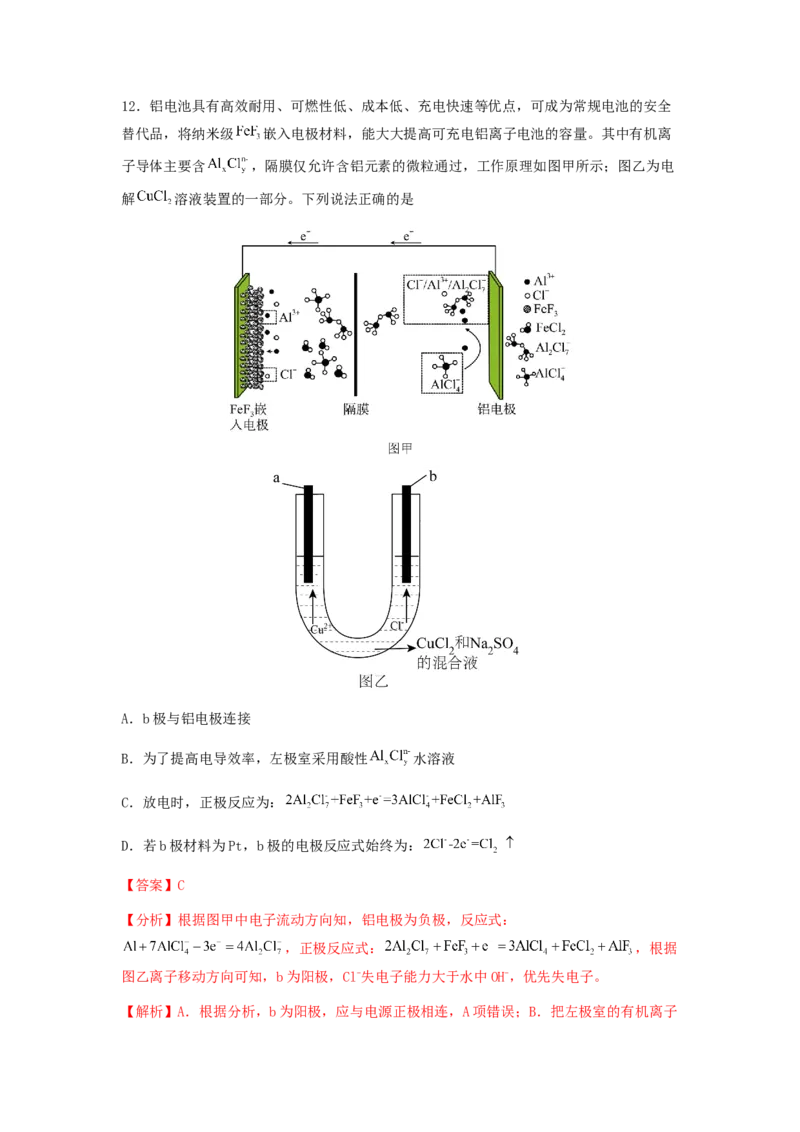
消耗3mol NaOH,D错误;故答案为:B。12.铝电池具有高效耐用、可燃性低、成本低、充电快速等优点,可成为常规电池的安全
替代品,将纳米级 嵌入电极材料,能大大提高可充电铝离子电池的容量。其中有机离
子导体主要含 ,隔膜仅允许含铝元素的微粒通过,工作原理如图甲所示;图乙为电
解 溶液装置的一部分。下列说法正确的是
A.b极与铝电极连接
B.为了提高电导效率,左极室采用酸性 水溶液
C.放电时,正极反应为:
D.若b极材料为Pt,b极的电极反应式始终为:
【答案】C
【分析】根据图甲中电子流动方向知,铝电极为负极,反应式:
,正极反应式: ,根据
图乙离子移动方向可知,b为阳极,Cl-失电子能力大于水中OH-,优先失电子。
【解析】A.根据分析,b为阳极,应与电源正极相连,A项错误;B.把左极室的有机离子导体改成水溶液后,会使左极室溶液中的离子总浓度减小,导致电导效率下降,B项错误;
C.根据分析,原电池正极反应为 ,C项正确;D.
若b极材料为Pt,b极先发生的电极反应为 ,当 放电完毕后,水发生
放电反应,D项错误。答案选C。
13.一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的
投影图如下所示(晶胞边长为apm,晶胞高为cpm, 为阿伏加德罗常数的值)。
下列说法正确的是
A.该物质的化学式为 B.硼原子间最近距离为
C. 的配位数为12 D.该物质的摩尔体积为
【答案】C
【解析】A.结合投影图可知,晶体结构中实线部分为1个晶胞, Mg个数为4×
=1,有2个B位于晶胞体内,化学式为 ,A错误;B.晶胞沿c轴的投影图中硼原子
位于正三角形的中心,硼原子间的最近距离,应为 ,B错误;C.由晶胞图可知,6
个B距底面中心的Mg距离相同,底面的Mg为2个晶胞共有,即距Mg最近的B有12个,即
Mg的配位数为12,故C正确;D.该物质的摩尔体积为 ,D错误;
故选C。
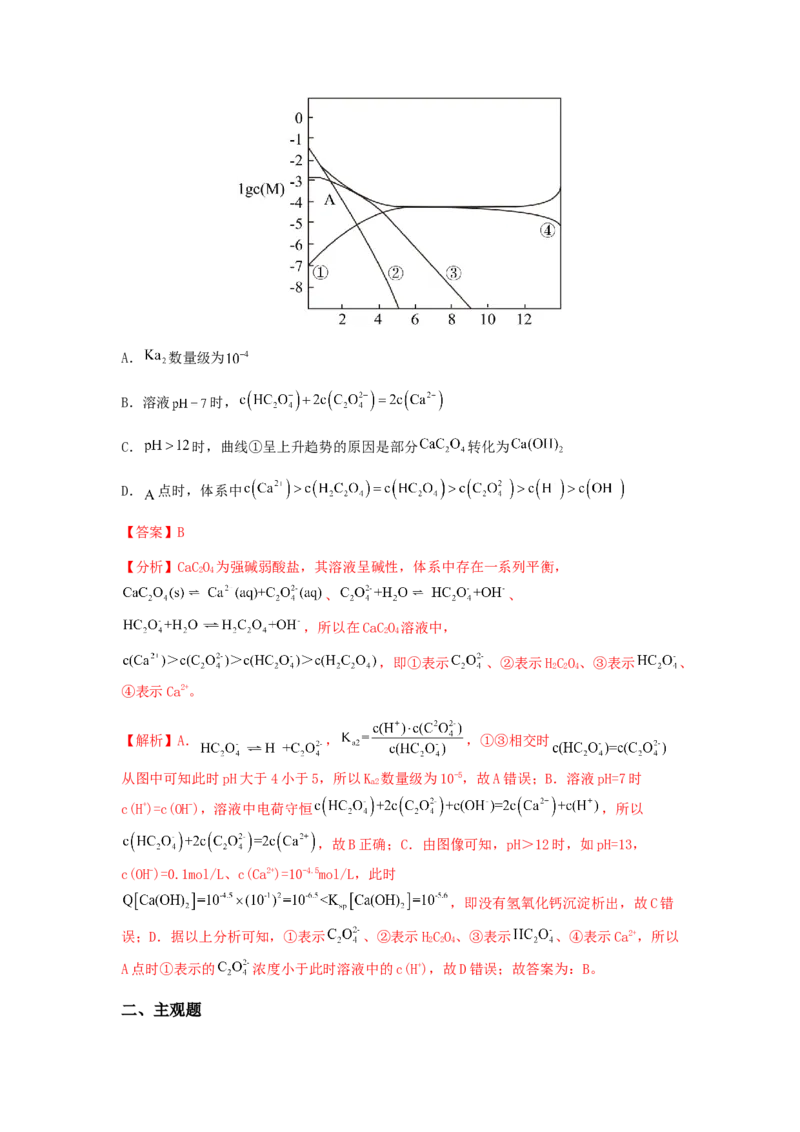
14.菠萝“扎嘴”的原因之一是菠萝中含有一种难溶于水的草酸钙针晶。常温下,草酸钙
在不同 下体系中 与 关系如图所示( 代表 ),已
知 。下列有关说法正确的是A. 数量级为
B.溶液 时,
C. 时,曲线①呈上升趋势的原因是部分 转化为
D. 点时,体系中
【答案】B
【分析】CaCO 为强碱弱酸盐,其溶液呈碱性,体系中存在一系列平衡,
2 4
、 、
,所以在CaCO 溶液中,
2 4
,即①表示 、②表示HCO、③表示 、
2 2 4
④表示Ca2+。
【解析】A. , ,①③相交时
从图中可知此时pH大于4小于5,所以K 数量级为10-5,故A错误;B.溶液pH=7时
a2
c(H+)=c(OH-),溶液中电荷守恒 ,所以
,故B正确;C.由图像可知,pH>12时,如pH=13,
c(OH-)=0.1mol/L、c(Ca2+)=10-4.5mol/L,此时
,即没有氢氧化钙沉淀析出,故C错
误;D.据以上分析可知,①表示 、②表示HCO、③表示 、④表示Ca2+,所以
2 2 4
A点时①表示的 浓度小于此时溶液中的c(H+),故D错误;故答案为:B。
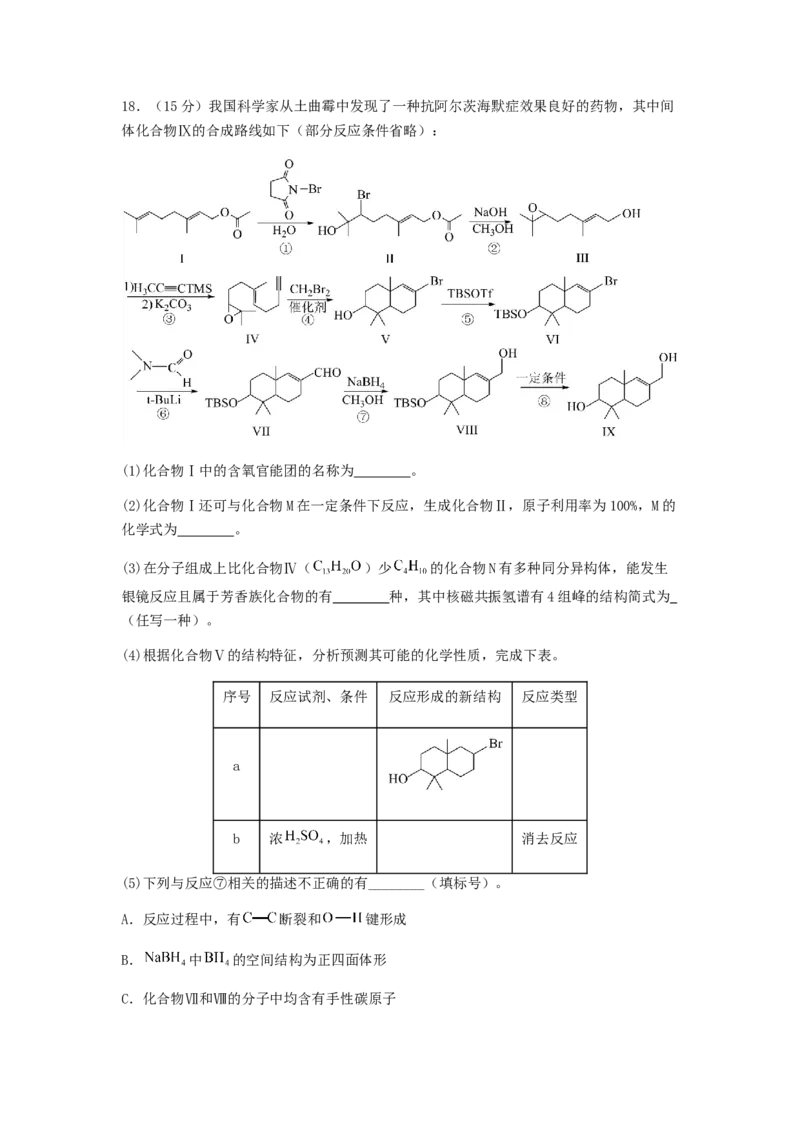
二、主观题18.(15分)我国科学家从土曲霉中发现了一种抗阿尔茨海默症效果良好的药物,其中间
体化合物Ⅸ的合成路线如下(部分反应条件省略):
(1)化合物Ⅰ中的含氧官能团的名称为 。
(2)化合物Ⅰ还可与化合物M在一定条件下反应,生成化合物Ⅱ,原子利用率为100%,M的
化学式为 。
(3)在分子组成上比化合物Ⅳ( )少 的化合物N有多种同分异构体,能发生
银镜反应且属于芳香族化合物的有 种,其中核磁共振氢谱有4组峰的结构简式为
(任写一种)。
(4)根据化合物Ⅴ的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a
b 浓 ,加热 消去反应
(5)下列与反应⑦相关的描述不正确的有________(填标号)。
A.反应过程中,有 断裂和 键形成
B. 中 的空间结构为正四面体形
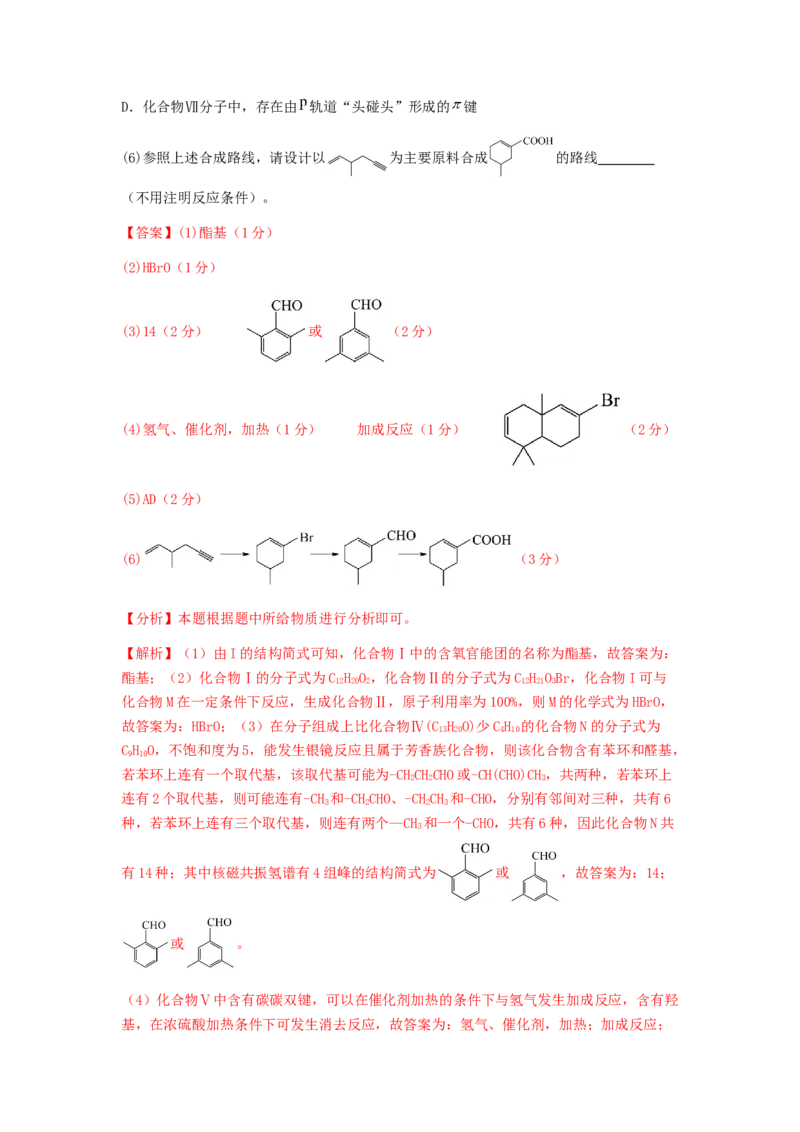
C.化合物Ⅶ和Ⅷ的分子中均含有手性碳原子D.化合物Ⅶ分子中,存在由 轨道“头碰头”形成的 键
(6)参照上述合成路线,请设计以 为主要原料合成 的路线
(不用注明反应条件)。
【答案】(1)酯基(1分)
(2)HBrO(1分)
(3)14(2分) 或 (2分)
(4)氢气、催化剂,加热(1分) 加成反应(1分) (2分)
(5)AD(2分)
(6) (3分)
【分析】本题根据题中所给物质进行分析即可。
【解析】(1)由I的结构简式可知,化合物Ⅰ中的含氧官能团的名称为酯基,故答案为:
酯基;(2)化合物Ⅰ的分子式为C H O,化合物Ⅱ的分子式为C H OBr,化合物I可与
12 20 2 12 21 3
化合物M在一定条件下反应,生成化合物Ⅱ,原子利用率为100%,则M的化学式为HBrO,
故答案为:HBrO;(3)在分子组成上比化合物Ⅳ(C H O)少CH 的化合物N的分子式为
13 20 4 10
CH O,不饱和度为5,能发生银镜反应且属于芳香族化合物,则该化合物含有苯环和醛基,
9 10
若苯环上连有一个取代基,该取代基可能为-CHCHCHO或-CH(CHO)CH,共两种,若苯环上
2 2 3
连有2个取代基,则可能连有-CH 和-CHCHO、-CHCH 和-CHO,分别有邻间对三种,共有6
3 2 2 3
种,若苯环上连有三个取代基,则连有两个—CH 和一个-CHO,共有6种,因此化合物N共
3
有14种;其中核磁共振氢谱有4组峰的结构简式为 或 ,故答案为:14;
或 。
(4)化合物Ⅴ中含有碳碳双键,可以在催化剂加热的条件下与氢气发生加成反应,含有羟
基,在浓硫酸加热条件下可发生消去反应,故答案为:氢气、催化剂,加热;加成反应;。
(5)A.观察化合物Ⅶ和Ⅷ的结构可知,反应过程中有C=O断裂和O-H、C-H键形成,故A
错误;B. 中心原子的价电子对数为 ,孤电子对数为0,因此 的
空间结构为正四面体形,故B正确;C.手性碳原子指连有四个不同的原子或原子团的碳原
子,化合物VII和VIII的分子中均含有手性碳原子,故C正确;D.“头碰头”形成σ键,
“肩并肩”形成π键,故D错误;故答案为:AD。
(6)参照上述流程可得以 为主要原料合成的路线为:
,故答案为:
。