文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练06 14道选择题+主观实验题
完卷时间:40分钟
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案
一、选择题(只有1个正确选项)
1.中国地大物博,化学与全国各地丰富的资源息息相关,下列说法错误的是
A.江西景德镇又名瓷都,陶瓷属于硅酸盐材料 B.辽宁鞍山又名钢都,钢属于合金
C.云南个旧又名锡都,灰锡属于金属晶体 D.四川自贡又名盐都,氯化钠属于电解质
2.下列描述不正确的是
A.1869年俄国化学家门捷列夫根据相对原子质量从小到大的顺序制作了第一张元素周期
表
B.1922年德国化学家施陶丁格提出了“聚合反应是大量小分子以化学键相互结合形成大
分子的过程”假说,为建立高分子科学奠定了基础
C.葡萄糖在水溶液中存在链状和环状结构之间的平衡,从链状到环状发生了加成反应
D.核酸检测是诊断新冠肺炎的重要依据,核酸是生物体遗传信息的载体,通过红外光谱仪
可检测其结构中存在单键、双键、氢键等化学键
3.反应 用于制备火箭推进剂 。下列说法正确的
A. 含有非极性键 B. 中 的化合价为“ ”
C. 的电子式: D. 的球棍模型:
4.设 为阿伏加德罗常数的值。下列说法正确的是
A. 的硫酸溶液中,含氢离子数目为
B.在常温常压下,11.2LCO 分子中含氧原子数目小于
2
C.21g 分子中含σ键数目一定是
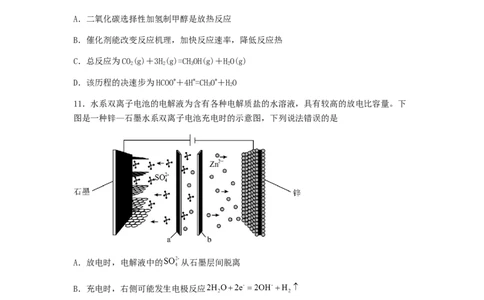
D.在 中,每生成3mol ,转移的电子数为5.用下列实验装置和方法进行相应实验,能达到实验目的的是
A.可用装置①测量反应产生气体的体积 B.可用装置②分离NHCl和NaCl
4
C.可用装置③除去甲烷中混有的乙烯 D.可用装置④证明氯化银溶解度大于硫化银
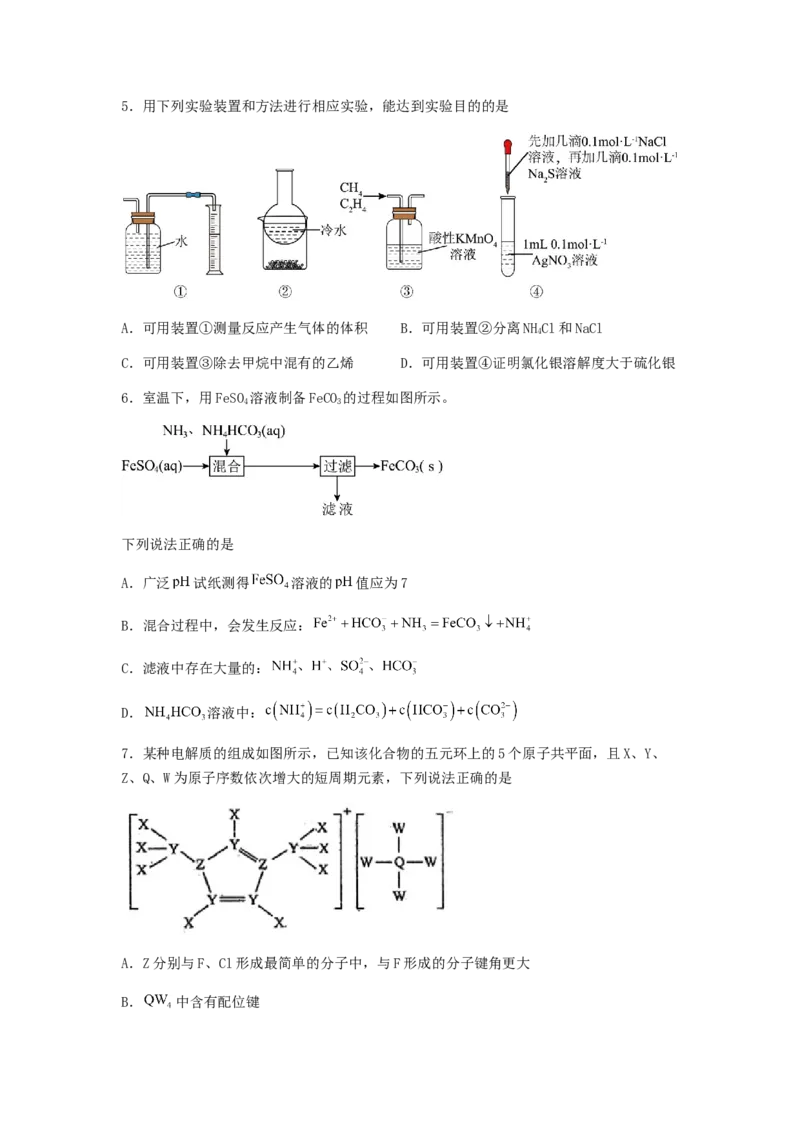
6.室温下,用FeSO 溶液制备FeCO 的过程如图所示。
4 3
下列说法正确的是
A.广泛 试纸测得 溶液的 值应为7
B.混合过程中,会发生反应:
C.滤液中存在大量的:
D. 溶液中:
7.某种电解质的组成如图所示,已知该化合物的五元环上的5个原子共平面,且X、Y、
Z、Q、W为原子序数依次增大的短周期元素,下列说法正确的是
A.Z分别与F、Cl形成最简单的分子中,与F形成的分子键角更大
B. 中含有配位键C.冰的分子间氢键
D.在该物质中Z有 , 的两种杂化方式
8.某有机物具有广谱抗菌活性,结构简式如图。下列有光该化合物说法错误的是
A.存在顺反异构体
B.可与 发生显色反应
C.1mol该有机物最多与4molNaOH反应
D.与足量 加成后的产物分子中含有6个手性碳原子
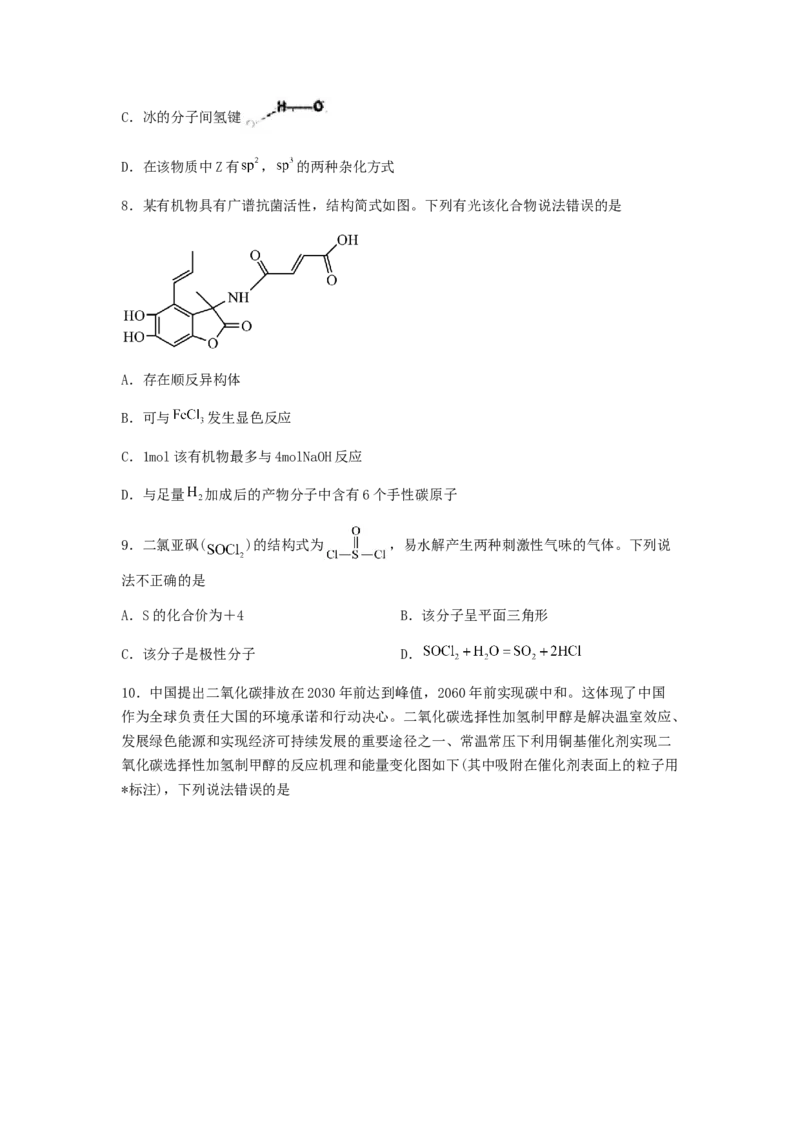
9.二氯亚砜( )的结构式为 ,易水解产生两种刺激性气味的气体。下列说
法不正确的是
A.S的化合价为+4 B.该分子呈平面三角形
C.该分子是极性分子 D.
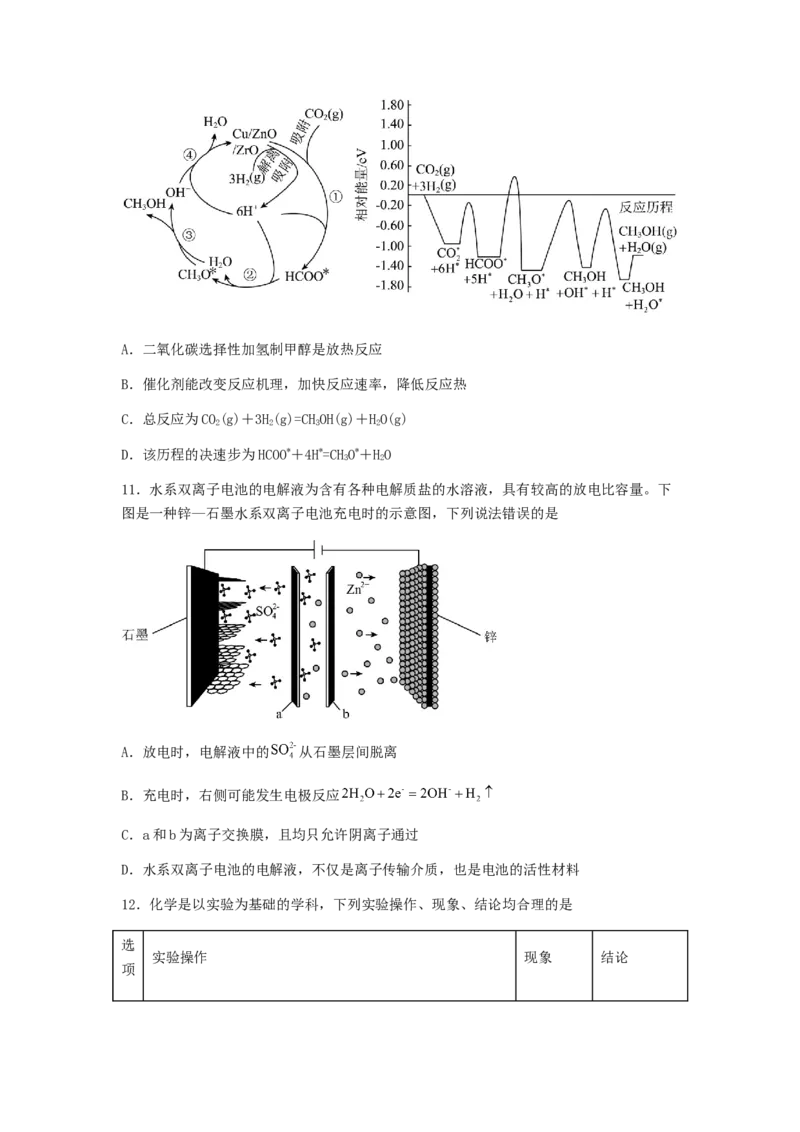
10.中国提出二氧化碳排放在2030年前达到峰值,2060年前实现碳中和。这体现了中国
作为全球负责任大国的环境承诺和行动决心。二氧化碳选择性加氢制甲醇是解决温室效应、
发展绿色能源和实现经济可持续发展的重要途径之一、常温常压下利用铜基催化剂实现二
氧化碳选择性加氢制甲醇的反应机理和能量变化图如下(其中吸附在催化剂表面上的粒子用
*标注),下列说法错误的是A.二氧化碳选择性加氢制甲醇是放热反应
B.催化剂能改变反应机理,加快反应速率,降低反应热
C.总反应为CO(g)+3H(g)=CHOH(g)+HO(g)
2 2 3 2
D.该历程的决速步为HCOO*+4H*=CHO*+HO
3 2
11.水系双离子电池的电解液为含有各种电解质盐的水溶液,具有较高的放电比容量。下
图是一种锌—石墨水系双离子电池充电时的示意图,下列说法错误的是
A.放电时,电解液中的 从石墨层间脱离
B.充电时,右侧可能发生电极反应
C.a和b为离子交换膜,且均只允许阴离子通过
D.水系双离子电池的电解液,不仅是离子传输介质,也是电池的活性材料
12.化学是以实验为基础的学科,下列实验操作、现象、结论均合理的是
选
实验操作 现象 结论
项样
观察到溶
A 将 样品溶于稀 ,滴加KSCN溶液
品已氧化变
液变红
质
将乙醇和浓硫酸混合溶液加热至170℃,将产生的气体通
B 溴水褪色 有乙烯生成
入溴水中
取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧 溶液未变 淀粉已经完
C
化钠溶液中和酸,再加少量碘水 蓝 全水解
结合氢
产生白色
D 向盛有 溶液的试管中滴加碳酸氢钠溶液 离子的能力
沉淀
比 强
A.A B.B C.C D.D
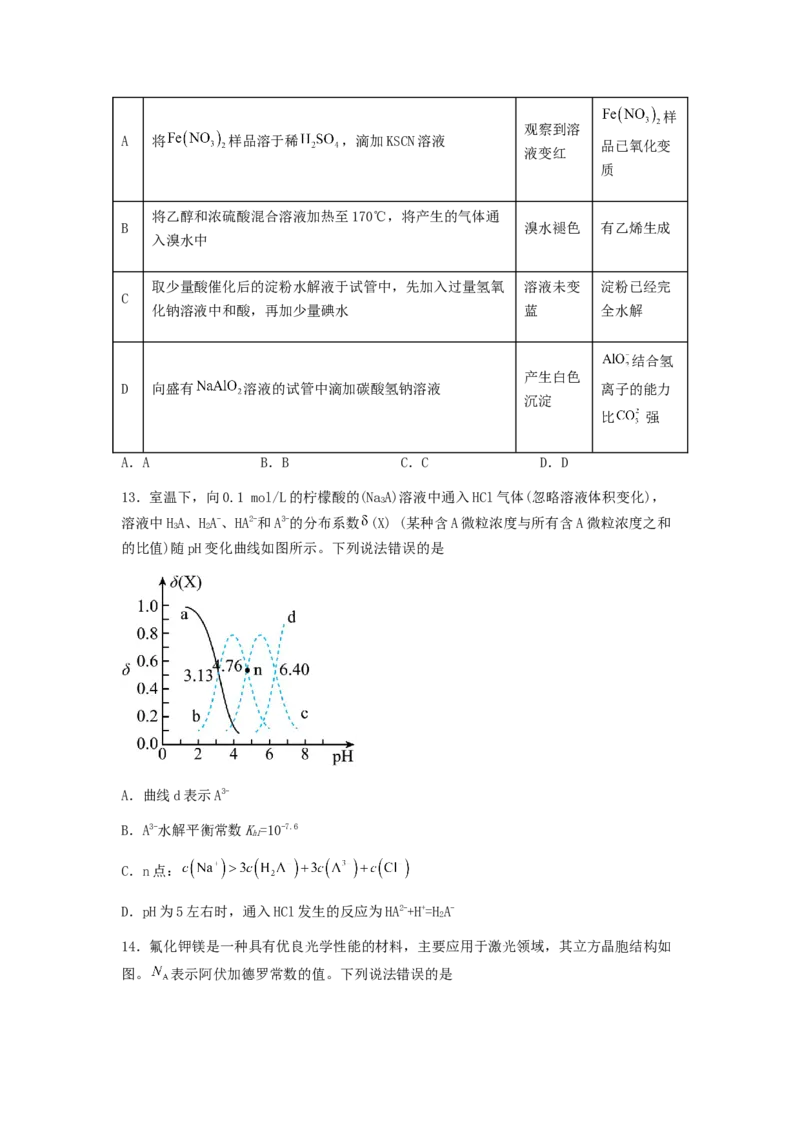
13.室温下,向0.1 mol/L的柠檬酸的(NaA)溶液中通入HCl气体(忽略溶液体积变化),
3
溶液中HA、HA-、HA2-和A3-的分布系数 (X) (某种含A微粒浓度与所有含A微粒浓度之和
3 2
的比值)随pH变化曲线如图所示。下列说法错误的是
A.曲线d表示A3-
B.A3-水解平衡常数K=10-7.6
h1
C.n点:
D.pH为5左右时,通入HCl发生的反应为HA2-+H+=HA-
2
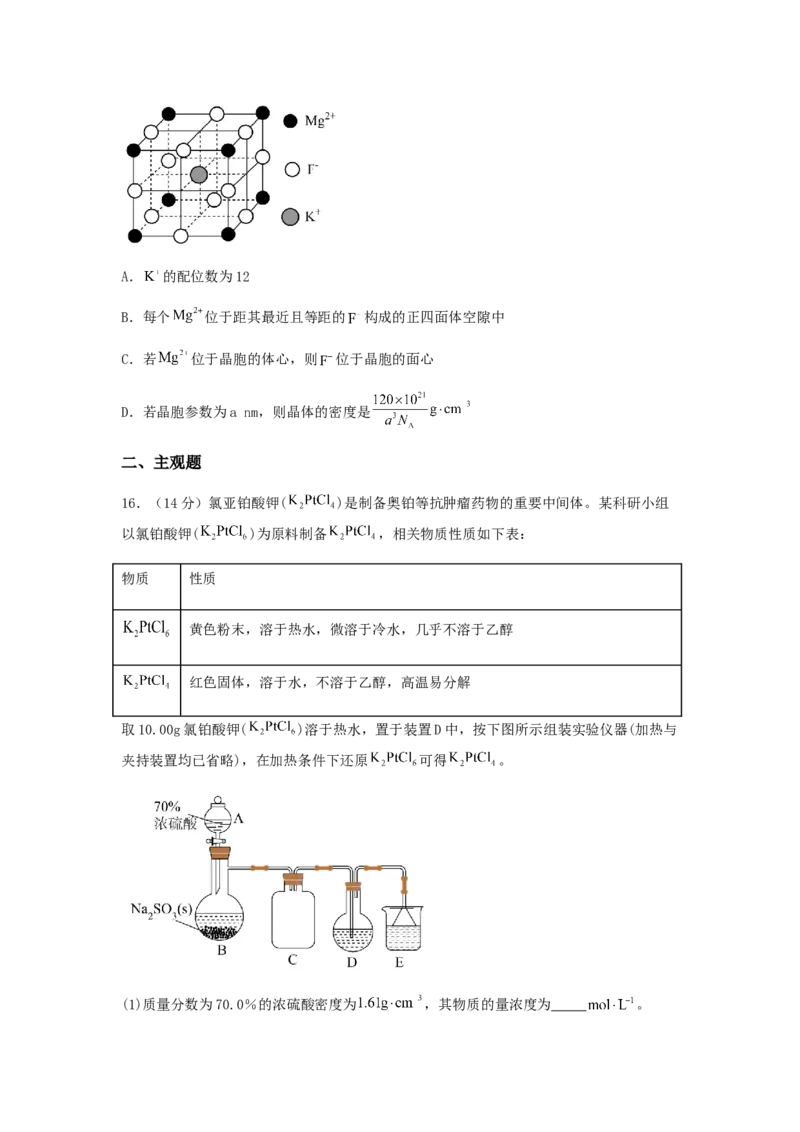
14.氟化钾镁是一种具有优良光学性能的材料,主要应用于激光领域,其立方晶胞结构如
图。 表示阿伏加德罗常数的值。下列说法错误的是A. 的配位数为12
B.每个 位于距其最近且等距的 构成的正四面体空隙中
C.若 位于晶胞的体心,则 位于晶胞的面心
D.若晶胞参数为a nm,则晶体的密度是
二、主观题
16.(14分)氯亚铂酸钾( )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组
以氯铂酸钾( )为原料制备 ,相关物质性质如下表:
物质 性质
黄色粉末,溶于热水,微溶于冷水,几乎不溶于乙醇
红色固体,溶于水,不溶于乙醇,高温易分解
取10.00g氯铂酸钾( )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与
夹持装置均已省略),在加热条件下还原 可得 。
(1)质量分数为70.0%的浓硫酸密度为 ,其物质的量浓度为 。(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为 。
(3)仪器B的名称为 ,装置C的作用是 。
(4)装置D中反应的化学方程式为 ,装置E中的试剂可选用 (填序号)。
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色
固体6.25g。
①加入无水乙醇的目的是 。
② 的产率为 (结果保留三位有效数字)。