文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练08 14道选择题+主观有机题
完卷时间:40分钟
答案速查
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B C C C B C B B D B D C D C
一、选择题(只有1个正确选项)
1.化学与生活、科技、社会发展息息相关。下列有关说法不正确的是
A.卡塔尔世界杯球馆屋顶采用了折叠式PTFE(聚四氟乙烯)板材,该板材属于合成高分子
材料
B.乙醇、过氧化氢、次氯酸钠等消毒剂均能将病毒氧化而达到消毒的目的
C.砖瓦是用黏土烧制而成,黏土主要成分为含水的铝硅酸盐
D.高铁酸钾(KFeO)在水处理过程中涉及的变化过程有:胶体聚沉、盐类水解、氧化还原
2 4
反应等
【答案】B
【解析】A.聚四氟乙烯属于合成高分子材料,A正确;B.乙醇使蛋白质变性,不能将病
毒氧化,过氧化氢和次氯酸钠能将病毒氧化而达到消毒的目的,B错误;C.砖瓦是传统硅
酸盐材料,由黏土烧制而成,黏土的主要成分为含水的铝硅酸盐,C正确;D.高铁酸钾发
生氧化还原反应变为Fe3+,Fe3+水解得到氢氧化铁胶体,胶体吸附水中悬浮颗粒发生胶体聚
沉,从而达到水处理的目的,D正确;故选B。
2.某有机物结构简式如图所示。下列关于该有机物的说法错误的是
A.分子式为
B.该物质没有手性碳原子C.1mol该物质最多能与6mol 反应
D.该物质既能与NaOH溶液反应,又能与盐酸反应
【答案】C
【分析】根据结构式可知,分子式为C H FNO,手性碳为与四个各不相同原子或基团相连
16 18 3 3
的碳原子,该有机物没有手性碳,其中苯环、羰基、碳碳双键都会与H 反应,有羧基和
2
,可以与NaOH溶液反应,又能与盐酸反应,据此回答。
【解析】A.由结构简式可知,分子式为 ,A正确;B.该物质没有手性碳原子,
B正确;C.苯环、酮羰基、碳碳双键能与氢气发生加成反应,羖基不能,1mol该物质最多
能与5mol 反应,C错误;D.该物质含有羧基,具有弱酸性,能与NaOH溶液反应,含有
,具有碱性,能与盐酸反应,D正确。故选C。
3.给定条件下,下列物质间的转化均能实现的是
A.
B.NaCl
C.
D.
【答案】C
【解析】A. 与过量的SO 反应,生成 ,A错误;B .NaCl与 不反
2
应,侯氏制碱法是先在饱和食盐水中通入氨气再通入CO,B错误;C.Fe与水蒸气反应生
2
成四氧化三铁,与稀硝酸反应生成硝酸铁,C正确;D.蔗糖无醛基,不能与氢氧化铜在加
热条件下生成氧化亚铜,D错误;故选C。
4.下列有关化学用语表示正确的是
A.HClO的电子式:
B.O 的分子结构空间模型:
3C.基态As原子的电子排布式:[Ar]3d104s24p3
D.反式聚异戊二烯的结构简式:
【答案】C
【解析】A.HClO的电子式: ,A错误;B.O 的分子结构空间模型:
3
,B错误;C.基态As原子的电子排布式:[Ar]3d104s24p3,C正确;D.反
式聚异戊二烯的结构简式: ,D错误; 故选C。
5.在指定的条件下,一定能大量共存的离子组是
A.无色溶液。
B.碱性条件:
C.水电离出的 的溶液:
D.制作印刷电路板的腐蚀液:
【答案】B
【解析】A. 有颜色,不能在无色溶液中大量存在,且氢离子与碳酸根离子也不能大
量共存,A不选;B.碱性条件下, 不发生反应,能大量共存,B选;
C.水电离出的 的溶液可能呈酸性也可能呈碱性, 不能在碱性条件
下大量存在,C不选;D.印刷电路板的腐蚀液中含有Fe2+, 会和Fe2+发生氧化还
原反应,不能大量共存,D不选;故选B。
6.化学处处呈现美。下列有关说法正确的是
A. 分子呈现完美对称,为V形结构
B.NaCl焰色试验为黄色,与氯原子的电子跃迁有关
C.冰雪融化时需要破坏氢键和范德华力
D.镁条燃烧发出耀眼的白光,只将化学能转化为光能
【答案】C【解析】A. 分子中中心原子碳原子价层电子对为 ,为sp杂化,呈直线
形结构,呈现完美对称, 故A错误;B. 焰色试验为黄色,Na+离子的核外电子从能
量高的状态跃迁到能量较低的状态,以光的形式将能量释放出来,故B错误;C.水分子间
存在范德华力和氢键,冰雪融化时,需要破坏范德华力和氢键,故C正确;D.Mg在空气
中燃烧时发出耀眼的白光,化学能一部分转化为光能,一部分转化为热能,故D错误;故
答案选C。
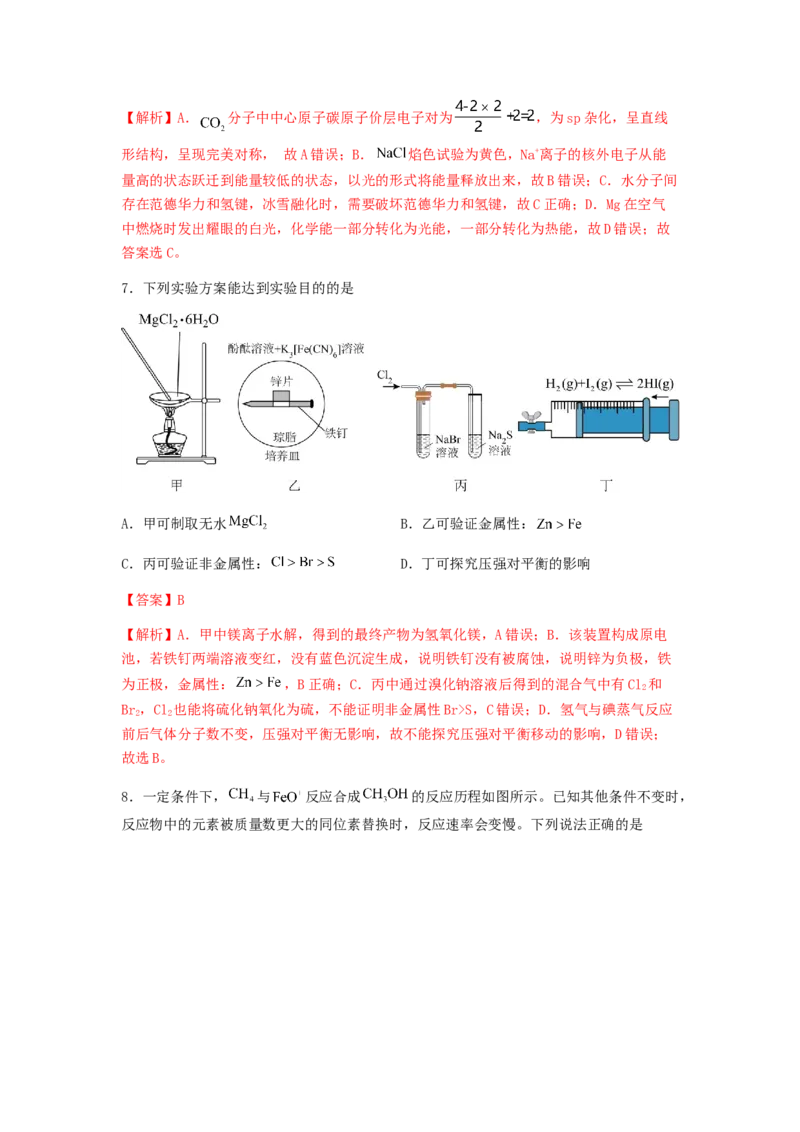
7.下列实验方案能达到实验目的的是
A.甲可制取无水 B.乙可验证金属性:
C.丙可验证非金属性: D.丁可探究压强对平衡的影响
【答案】B
【解析】A.甲中镁离子水解,得到的最终产物为氢氧化镁,A错误;B.该装置构成原电
池,若铁钉两端溶液变红,没有蓝色沉淀生成,说明铁钉没有被腐蚀,说明锌为负极,铁
为正极,金属性: ,B正确;C.丙中通过溴化钠溶液后得到的混合气中有Cl 和
2
Br,Cl 也能将硫化钠氧化为硫,不能证明非金属性Br>S,C错误;D.氢气与碘蒸气反应
2 2
前后气体分子数不变,压强对平衡无影响,故不能探究压强对平衡移动的影响,D错误;
故选B。
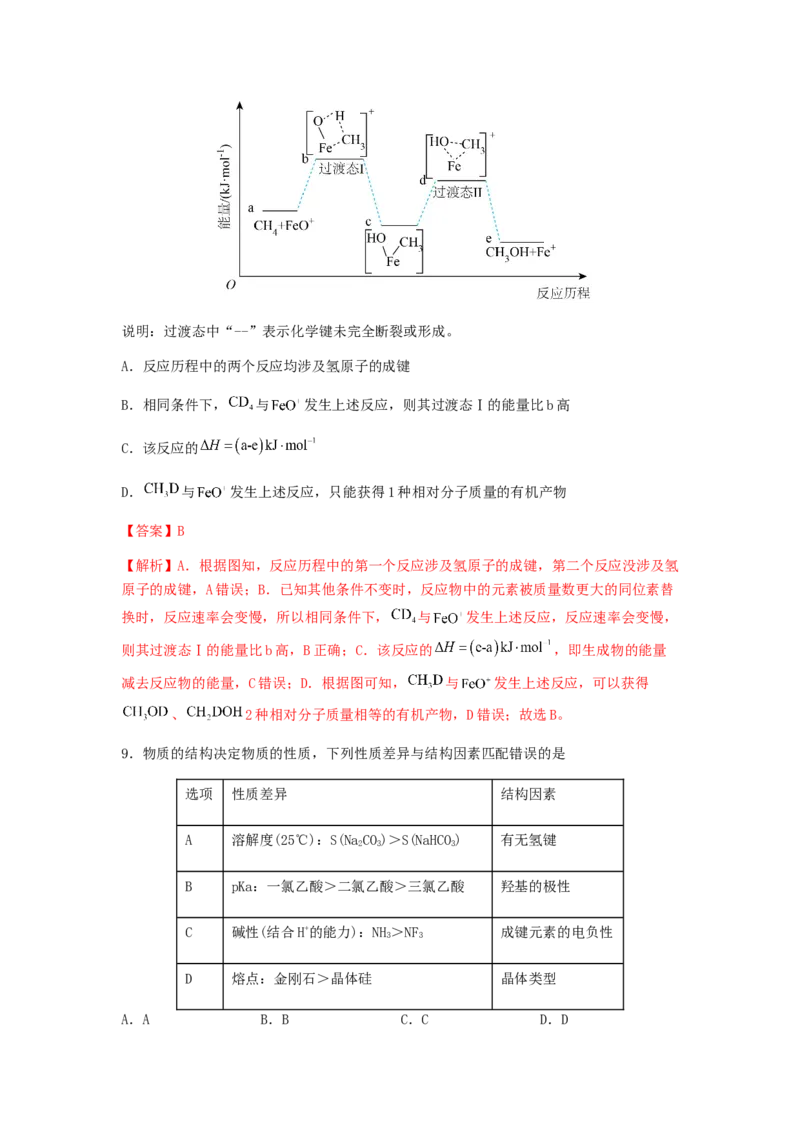
8.一定条件下, 与 反应合成 的反应历程如图所示。已知其他条件不变时,
反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。下列说法正确的是说明:过渡态中“--”表示化学键未完全断裂或形成。
A.反应历程中的两个反应均涉及氢原子的成键
B.相同条件下, 与 发生上述反应,则其过渡态Ⅰ的能量比b高
C.该反应的
D. 与 发生上述反应,只能获得1种相对分子质量的有机产物
【答案】B
【解析】A.根据图知,反应历程中的第一个反应涉及氢原子的成键,第二个反应没涉及氢
原子的成键,A错误;B.已知其他条件不变时,反应物中的元素被质量数更大的同位素替
换时,反应速率会变慢,所以相同条件下, 与 发生上述反应,反应速率会变慢,
则其过渡态Ⅰ的能量比b高,B正确;C.该反应的 ,即生成物的能量
减去反应物的能量,C错误;D.根据图可知, 与 发生上述反应,可以获得
、 2种相对分子质量相等的有机产物,D错误;故选B。
9.物质的结构决定物质的性质,下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 溶解度(25℃):S(NaCO)>S(NaHCO) 有无氢键
2 3 3
B pKa:一氯乙酸>二氯乙酸>三氯乙酸 羟基的极性
C 碱性(结合H+的能力):NH>NF 成键元素的电负性
3 3
D 熔点:金刚石>晶体硅 晶体类型
A.A B.B C.C D.D【答案】D
【解析】A.在室温25℃时,NaCO 易溶于水,NaHCO 能溶于水,这是由于NaCO 的阴离子
2 3 3 2 3
能够与HO分子之间形成氢键,导致物质更易溶于水,而 与HO分子之间不能形
2 2
成氢键,故物质的溶解度:S(NaCO)>S(NaHCO),A正确;B.三种物质都是CHCOOH的甲
2 3 3 3
基—CH 上的H原子分别Cl原子取代产生的物质,由于Cl的电负性较大,导致羧酸分子中
3
羟基的极性增强,分子中含有的Cl原子越多,羧酸分子中羟基的极性就越强,则根据极性:
—CCl>—CHCl>—CClH,使羧基-COOH上羟基-OH的H+电离能力逐渐减弱,因此酸性:
3 2 2
CCl—COOH>CHCl—COOH>CHCl—COOH,弱酸的酸性越强,其电离平衡常数Ka就越大,
3 2 2
则其pKa就越小,故pKa:一氯乙酸>二氯乙酸>三氯乙酸,B正确;C.由于电负性:F>
N>H,导致N原子周围电子云密度:NH>NF,N原子周围电子云密度越大,其结合H+能力
3 3
就越强,物质的碱性就越强,故(结合H+的能力):NH>NF,C正确;D.金刚石、晶体硅
3 3
都属于共价晶体,原子之间以共价键结合形成立体网状结构。由于原子半径:C<Si,键长:
C-C<Si-Si,晶体中共价键键长越短,其断裂消耗的能量就越高,物质的熔点就越高,所
以熔点:金刚石>晶体硅,D错误;故合理选项是D。
10.实验室合成并提纯山梨酸乙酯(密度 ,沸点195.5℃)的过程如下图所示。
下列说法正确的是
A.操作①控温110℃,目的是除去生成的水
B.操作③可以通过观察气泡现象控制试剂a的用量
C.操作③④均应收集下层液体
D.操作②⑤可用玻璃棒轻轻拨散固体,以加快过滤速率
【答案】B
【分析】山梨酸和乙醇在浓硫酸、110℃条件下发生酯化反应生成山梨酸乙酯,产物混合物
过滤后滤液中加入试剂a为碳酸氢钠,用于中和多余的山梨酸,再用水洗涤分液,在有机
层中加入少量无水硫酸镁吸收多余的水分,再进行过滤得到滤液,滤液进行蒸馏得到山梨
酸乙酯。
【解析】A.操作①控制温度为110℃,加热可以加快反应的进行,同时温度又不至于过高
导致乙醇大量挥发,且山梨酸乙酯的沸点高于110℃可减少山梨酸乙酯的挥发,A错误;
B.操作③加入的是碳酸氢钠溶液,用于除去多余的山梨酸,碳酸氢钠与山梨酸反应生成二
氧化碳气体,可观察气泡现象控制碳酸氢钠溶液的用量,B正确;C.操作③④最后得到含
有山梨酸乙酯的有机层,山梨酸乙酯密度小于水,因此应该收集上层的液体,C错误;D.
过滤时玻璃棒的作用为引流,不能用其拨散固体,防止捣破滤纸,D错误;故答案选B。11.草酸晶体(H
2
C
2
O 4⋅2H
2
O)用途广泛,易溶于水,其制备及纯度测定实验如下。
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温
至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝
酸与98%硫酸),主要反应为 。严格
控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶
体 。
Ⅱ.纯度测定
称取制得的草酸晶体 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO 标
4
准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列说
法正确的是
A.65%浓硝酸( )的物质的量浓度约为13.6mol·L-1
B.草酸晶体的产率为
C.配制的草酸溶液物质的量浓度为0.025cVmol·L-1
D.草酸晶体的纯度为
【答案】D
【解析】A.65%浓硝酸( )的物质的量浓度约为
,故A错误;B. , ,则草酸晶体的产率
为 ,故B错误;C.根据得失电子守恒有5HCO~2KMnO,则配制的草
2 2 4 4
酸溶液物质的量浓度为 ,故C错误;D.据C解析草酸溶液
的物质的量浓度,则草酸晶体的纯度为,故D正确;故选D。
12.利用一种电解质溶液浓度不同引起电势差的装置称为“浓差电池”,其原理是高浓度
溶液向低浓度溶液扩散而引发的一类电池。某浓差电池的模拟装置如图所示。已知:两电
极银的质量均为300g。下列叙述正确的是
A. 电极为负极,发生氧化反应
B. 由右侧向左侧迁移
C.电池停止工作时两电极的质量差为432g
D.电池放电时将化学能全部转化成电能
【答案】C
【分析】浓差电池通过改变电解质溶液浓度实现放电,当浓度相等时停止放电。阴离子交
换膜只允许阴离子通过,所以只能通过电极反应改变电解质溶液浓度,左侧电解质溶液浓
度减小,右侧电解质溶液浓度增大, 极上析出Ag, 极上银溶解,由此推知,
为正极,Ag(2)为负极。
【解析】A.根据分析知, 为正极,Ag(2)为负极,A错误;B.为了维持电荷守恒,
左侧电解质溶液中 向右侧迁移,B错误;C.当两电极所在电解质溶液浓度相等时达到
平衡,停止放电,停止放电时 mol⋅L ,即只转移2 mol电子,负极:
,正极: ,起始时,两电极的质量相等,停止放电时,正极增
加2 mol Ag(216g),负极减少2 mol Ag(216g),两电极的质量差为432 g,C正确;D.电
池放电时将化学能主要转化成电能,还有热能等,D错误;故选C。
13.钴氧化物和 按照适量的比例高温煅烧可得到钴蓝,钴蓝可用于青花瓷的颜料。
钴蓝晶体结构是由图1中Ⅰ型和Ⅱ型两种小立方体平移所得。图2是钴蓝的晶胞,已知钴
原子位于晶胞的顶角和面心。下列说法中错误的是A.钴蓝晶胞中 原子个数比为
B.Co原子间最短的距离为
C.图2所示字母中,Ⅰ型小立方体分别是
D.钴蓝晶体的密度为
【答案】D
【解析】A.Ⅰ型立体结构中Co位于顶点和体心,原子数是4× +1;O位于晶胞内,原子
数是4;Ⅱ型小立方体中Co位于顶点,原子数是4× ;O位于晶胞内,原子数是4;Al位
于晶胞内,原子数是4;该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,所以1个晶胞含
有Co原子数是8、O原子数是32、Al原子数是16,钴蓝晶体中三种原子个数比N(Co):
N(Al):N(O)=8:16:32= 1:2:4,故A正确;B.由图可知, 原子间最短的距离为面对
角线的一半,则该距离为: ,故B正确;C.根据晶胞中Ⅰ型立体结构、Ⅱ型小立
方体关系,图2中Ⅰ型小立方体位于图2中上层ac对角线的位置、下层f位置,故分别是
a、c、f,故C正确;D.由A分析可知,图2所示晶胞质量为
,晶胞体积为 ,所以密度为
,故D错误;故答案选D。
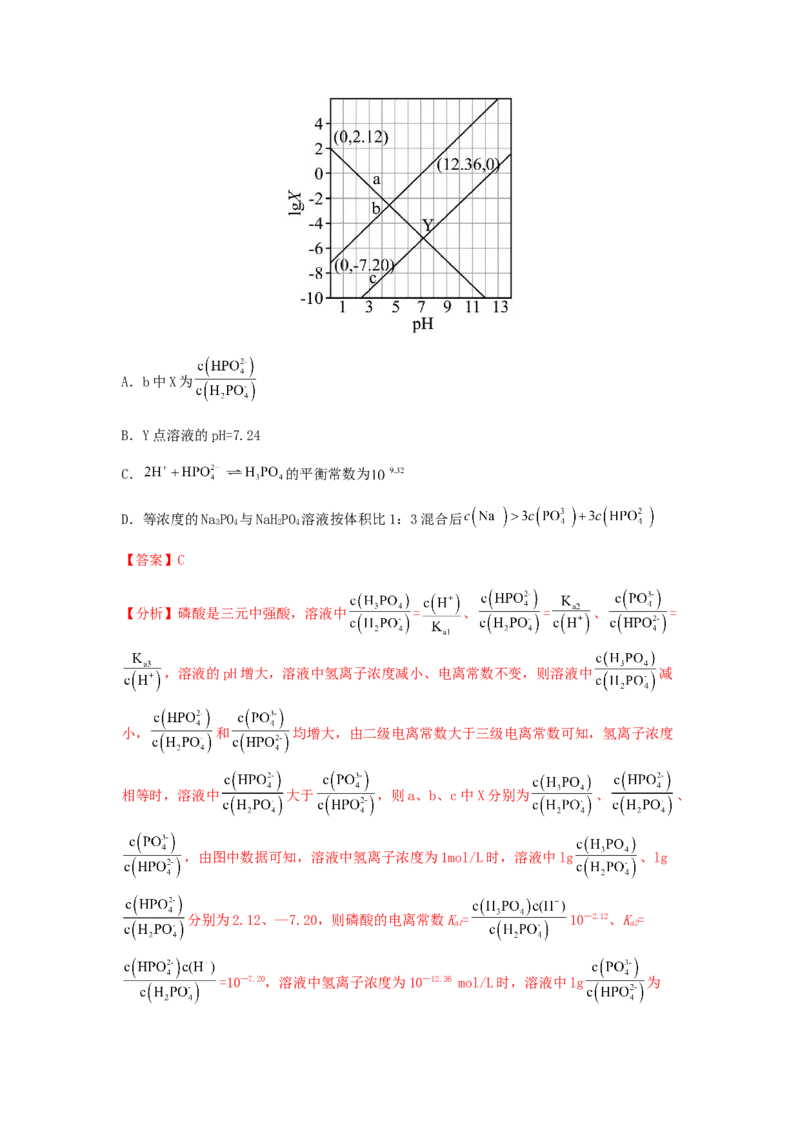
14.常温下,用一定浓度的NaOH溶液滴定某浓度的磷酸溶液,所得溶液的pH与lgX的关
系如图所示,X表示 、 或 ,下列说法错误的是A.b中X为
B.Y点溶液的pH=7.24
C. 的平衡常数为
D.等浓度的NaPO 与NaHPO 溶液按体积比1:3混合后
3 4 2 4
【答案】C
【分析】磷酸是三元中强酸,溶液中 = 、 = 、 =
,溶液的pH增大,溶液中氢离子浓度减小、电离常数不变,则溶液中 减
小, 和 均增大,由二级电离常数大于三级电离常数可知,氢离子浓度
相等时,溶液中 大于 ,则a、b、c中X分别为 、 、
,由图中数据可知,溶液中氢离子浓度为1mol/L时,溶液中lg 、lg
分别为2.12、—7.20,则磷酸的电离常数K= 10—2.12、K=
a1 a2
=10—7.20,溶液中氢离子浓度为10—12.36 mol/L时,溶液中lg 为0,K= =10—12.36。
a3
【解析】A.由分析可知,a、b、c中X分别为 、 、 ,故A
正确;B.由图可知,Y点溶液中 = ,由分析可知,溶液中 =
,则溶液中氢离子浓度为 mol/L = mol/L= 10-7.24mol/L,所
以溶液pH为7.24,故B正确;C.由方程式可知,反应的平衡常数K= =
= = =109.32,故C错误;D.等浓度的
磷酸钠溶液与磷酸二氢钠溶液按体积比1:3混合恰好反应生成等浓度的磷酸氢钠与磷酸二
氢钠混合溶液,由物料守恒 可知,
溶液中 ,故D正确;故选C。
二、主观题
18.(15分)有机物G是合成中草药活性成分Psoralidin的中间体,其合成路线如下:
已知:酯分子中的α-碳原子上的氢比较活泼,使酯与酯之间能发生缩合反应:
回答下列问题:
(1)化合物A的名称为 ;C中官能团的名称为 。(2)结合已有知识,写出E→F的方程式: ;该反应类型为 。
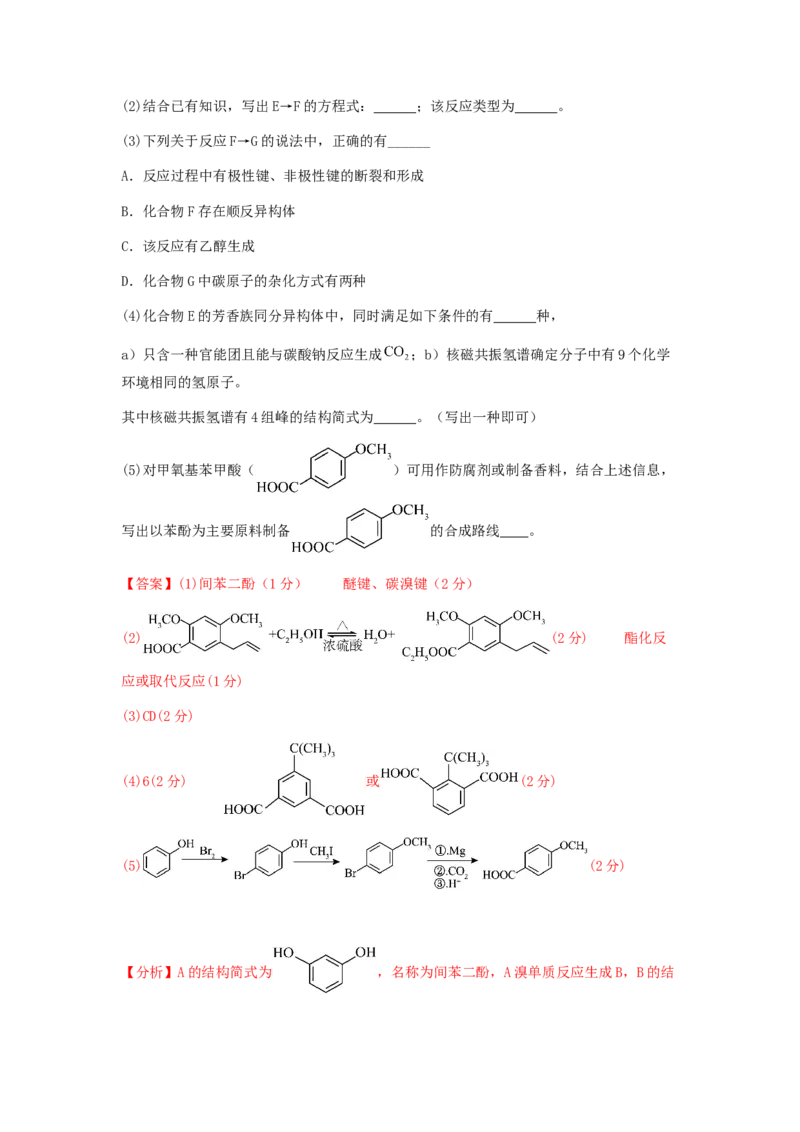
(3)下列关于反应F→G的说法中,正确的有______
A.反应过程中有极性键、非极性键的断裂和形成
B.化合物F存在顺反异构体
C.该反应有乙醇生成
D.化合物G中碳原子的杂化方式有两种
(4)化合物E的芳香族同分异构体中,同时满足如下条件的有 种,
a)只含一种官能团且能与碳酸钠反应生成 ;b)核磁共振氢谱确定分子中有9个化学
环境相同的氢原子。
其中核磁共振氢谱有4组峰的结构简式为 。(写出一种即可)
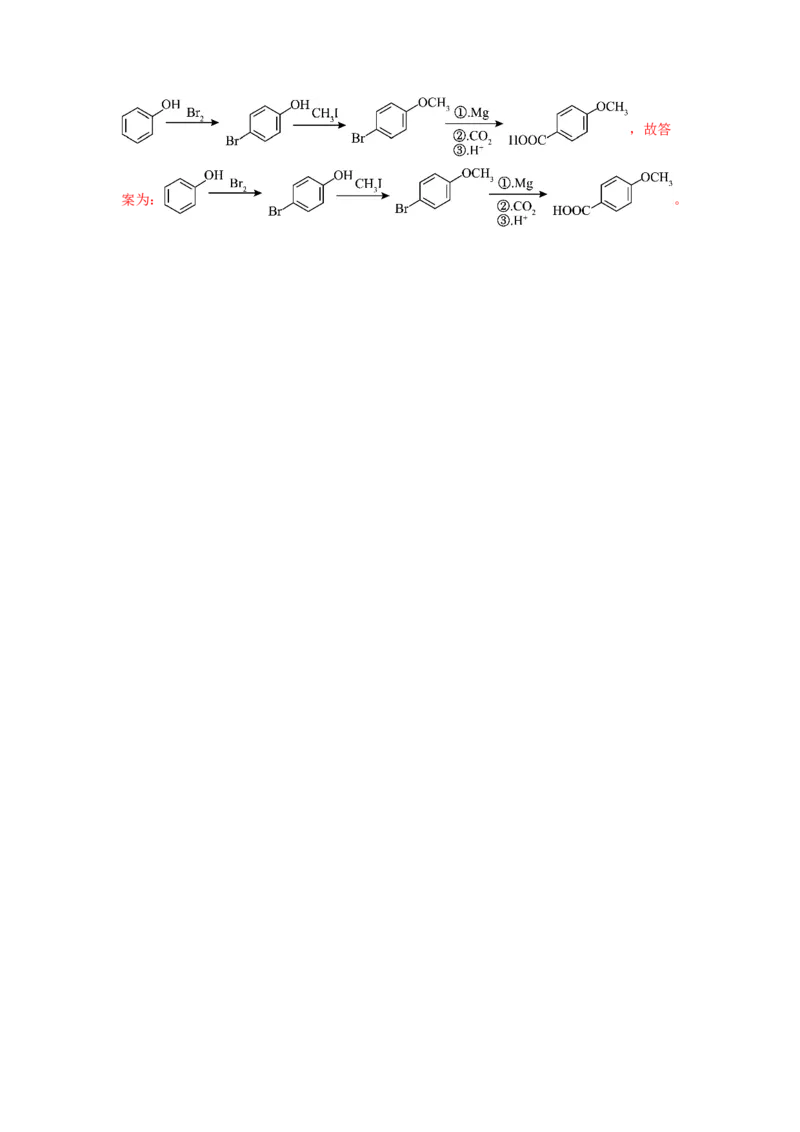
(5)对甲氧基苯甲酸( )可用作防腐剂或制备香料,结合上述信息,
写出以苯酚为主要原料制备 的合成路线 。
【答案】(1)间苯二酚(1分) 醚键、碳溴键(2分)
(2) (2分) 酯化反
应或取代反应(1分)
(3)CD(2分)
(4)6(2分) 或 (2分)
(5) (2分)
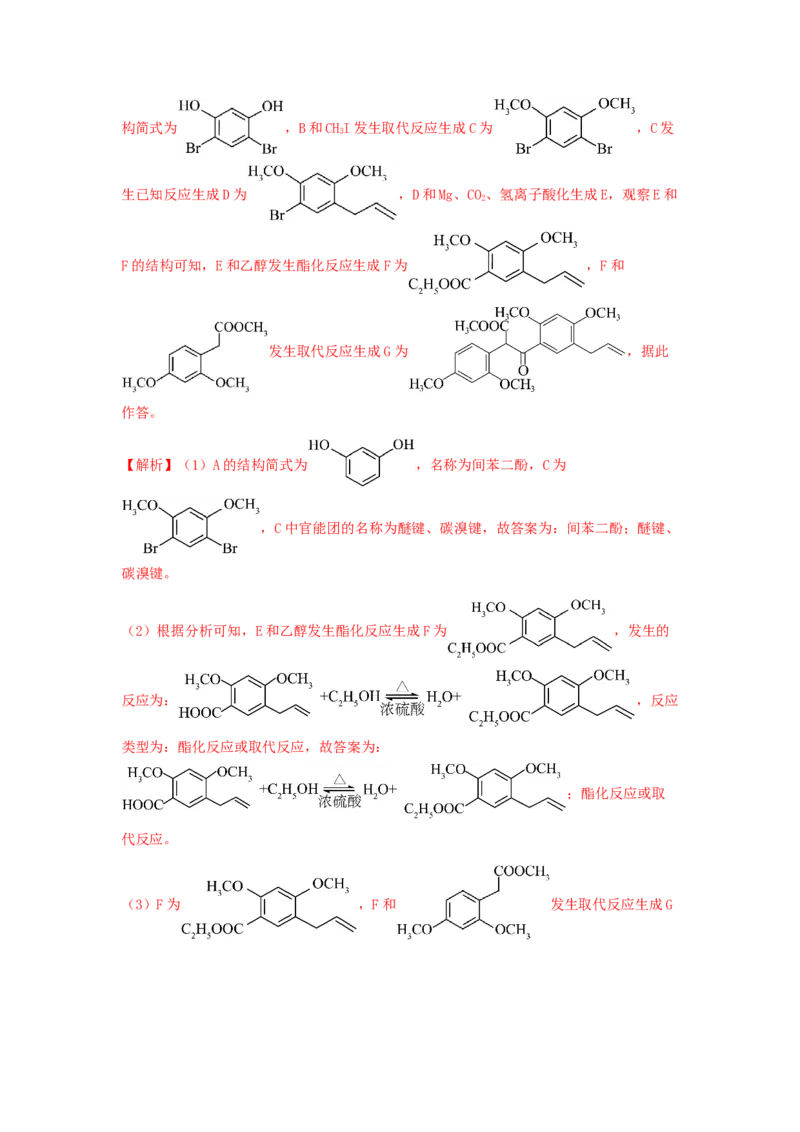
【分析】A的结构简式为 ,名称为间苯二酚,A溴单质反应生成B,B的结构简式为 ,B和CHI发生取代反应生成C为 ,C发
3
生已知反应生成D为 ,D和Mg、CO、氢离子酸化生成E,观察E和
2
F的结构可知,E和乙醇发生酯化反应生成F为 ,F和
发生取代反应生成G为 ,据此
作答。
【解析】(1)A的结构简式为 ,名称为间苯二酚,C为
,C中官能团的名称为醚键、碳溴键,故答案为:间苯二酚;醚键、
碳溴键。
(2)根据分析可知,E和乙醇发生酯化反应生成F为 ,发生的
反应为: ,反应
类型为:酯化反应或取代反应,故答案为:
;酯化反应或取
代反应。
(3)F为 ,F和 发生取代反应生成G为 ,可知:
A.反应过程中只有极性键断裂和形成,故A错误;B.F为 ,
碳碳双键两端有一端存在2个H原子,不存在顺反异构,故B错误;C.
和 在CHONa的作用下生成
2 5
,发生已知信息中的反应,反应中有乙醇产生,故C正确;
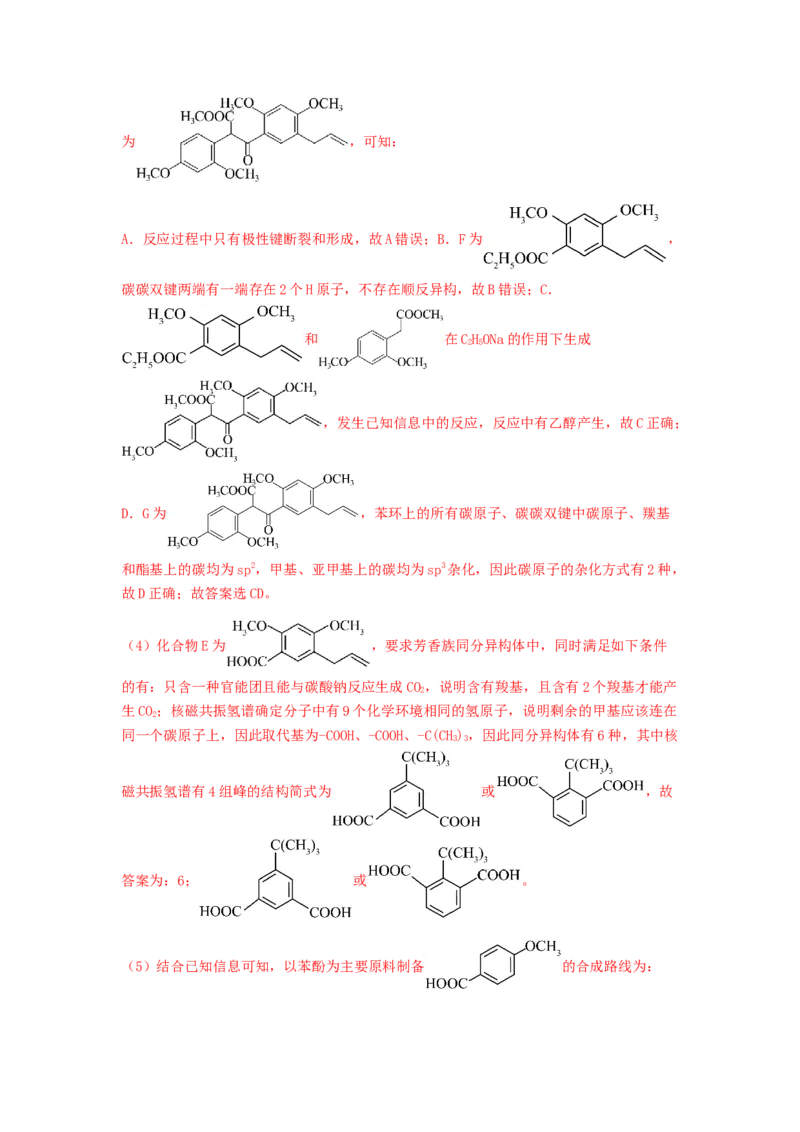
D.G为 ,苯环上的所有碳原子、碳碳双键中碳原子、羰基
和酯基上的碳均为sp2,甲基、亚甲基上的碳均为sp3杂化,因此碳原子的杂化方式有2种,
故D正确;故答案选CD。
(4)化合物E为 ,要求芳香族同分异构体中,同时满足如下条件
的有:只含一种官能团且能与碳酸钠反应生成CO,说明含有羧基,且含有2个羧基才能产
2
生CO;核磁共振氢谱确定分子中有9个化学环境相同的氢原子,说明剩余的甲基应该连在
2
同一个碳原子上,因此取代基为-COOH、-COOH、-C(CH),因此同分异构体有6种,其中核
3 3
磁共振氢谱有4组峰的结构简式为 或 ,故
答案为:6; 或 。
(5)结合已知信息可知,以苯酚为主要原料制备 的合成路线为:,故答
案为: 。