文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练09 14道选择题+主观流程题
完卷时间:40分钟
答案速查
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C D C A C D A D C D D D C D
一、选择题(共42分,只有1个正确选项)
1.化学推动着社会的进步和人类的发展。下列说法不正确的是
A.“煤制烯现代化成套技术开发及应用”中煤的气化属于化学变化
B.热压氮化硅具有高强度、低密度、耐高温等优点,是可用于制造汽车发动机的新型耐高
温结构材料
C.质检机构从某品牌液态奶中检测出违禁添加物丙二醇,丙二醇是乙醇的同系物
D.“嫦娥五号”采集的月壤样本中含有 , 与 互为同位素
【答案】C
【解析】A.煤的气化是煤形成 、CO等气体的过程,有新物质生成,是化学变化,故A
正确;B. 具有高强度、低密度、耐高温等优点,是可用于制造汽车发动机的新型耐
高温结构材料,故B正确;C.一个丙二醇分子中含有2个羟基,一个乙醇分子中含有1个
羟基,两者不属于同系物,故C错误;D.质子数相同,中子数不同的同种元素的不同核素
互称为同位素, 、 两者互为同位素,故D正确;本题选C。
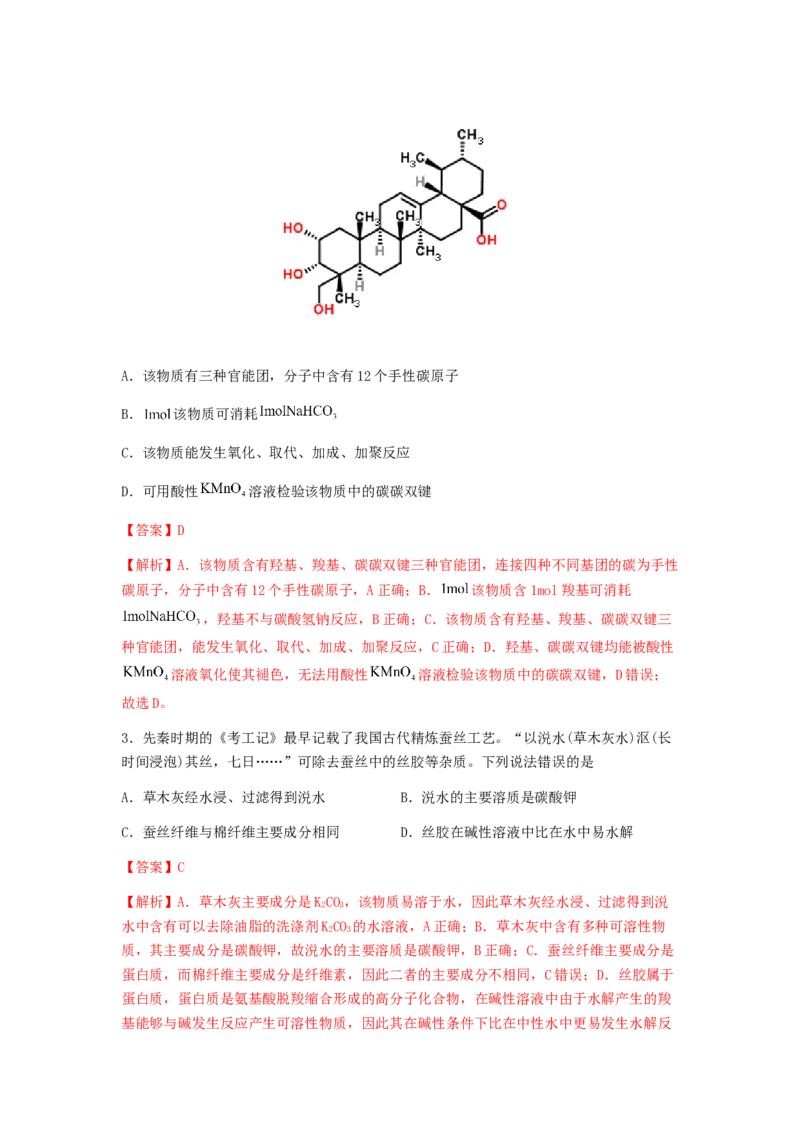
2.去羟加利果酸具有抗炎作用,它对LPS诱导的内毒性休克具有保护作用,其结构简式如
图所示。下列有关该物质的说法错误的是A.该物质有三种官能团,分子中含有12个手性碳原子
B. 该物质可消耗
C.该物质能发生氧化、取代、加成、加聚反应
D.可用酸性 溶液检验该物质中的碳碳双键
【答案】D
【解析】A.该物质含有羟基、羧基、碳碳双键三种官能团,连接四种不同基团的碳为手性
碳原子,分子中含有12个手性碳原子,A正确;B. 该物质含1mol羧基可消耗
,羟基不与碳酸氢钠反应,B正确;C.该物质含有羟基、羧基、碳碳双键三
种官能团,能发生氧化、取代、加成、加聚反应,C正确;D.羟基、碳碳双键均能被酸性
溶液氧化使其褪色,无法用酸性 溶液检验该物质中的碳碳双键,D错误;
故选D。
3.先秦时期的《考工记》最早记载了我国古代精炼蚕丝工艺。“以涚水(草木灰水)沤(长
时间浸泡)其丝,七日……”可除去蚕丝中的丝胶等杂质。下列说法错误的是
A.草木灰经水浸、过滤得到涚水 B.涚水的主要溶质是碳酸钾
C.蚕丝纤维与棉纤维主要成分相同 D.丝胶在碱性溶液中比在水中易水解
【答案】C
【解析】A.草木灰主要成分是KCO,该物质易溶于水,因此草木灰经水浸、过滤得到涚
2 3
水中含有可以去除油脂的洗涤剂KCO 的水溶液,A正确;B.草木灰中含有多种可溶性物
2 3
质,其主要成分是碳酸钾,故涚水的主要溶质是碳酸钾,B正确;C.蚕丝纤维主要成分是
蛋白质,而棉纤维主要成分是纤维素,因此二者的主要成分不相同,C错误;D.丝胶属于
蛋白质,蛋白质是氨基酸脱羧缩合形成的高分子化合物,在碱性溶液中由于水解产生的羧
基能够与碱发生反应产生可溶性物质,因此其在碱性条件下比在中性水中更易发生水解反应,D正确;故合理选项是C。
4.常温下,下列各组离子在指定溶液中能大量共存的是
A. 溶液: 、 、
B. 稀硫酸: 、 、
C. 溶液: 、 、
D. 溶液: 、 、
【答案】A
【解析】A. 溶液: 、 、 不会发生化学反应,可以大量共存,
A正确;B. 稀硫酸存在情况下,硝酸根具有强氧化性,会氧化碘离子为碘单质,
不能大量共存,B错误;C.碳酸氢根离子会与铝离子发生双水解生成氢氧化铝和二氧化碳,
不能大量共存,C错误;D.铁离子会与 发生反应生成Fe( ),不能大量共存,D
3
错误;故选A。
5.2024年春节过后,健康塑形成为人们热议的话题。化学也再次显示了其在生活中的重
要作用,以下有关说法正确的是
A.对于需要减重的人群,应减少脂肪摄入,但应保证必需的蛋白质摄入,蛋白质将在人体
内通过氧化反应转化成氨基酸
B.糖类是重要的供能物质,糖类包含单糖、二糖、多糖等,二糖、多糖属于非还原糖
C.运动也是健康塑形的重要手段,人在运动时会大量出汗,汗液中含有尿素,尿素(
)属于酰胺类有机物
D.人的体型除了与生活习惯有关,与遗传也关系密切,而核酸就是生物的遗传物质,核酸
包含DNA与RNA,一切生物都既有DNA又有RNA
【答案】C
【解析】A.蛋白质将在人体内通过水解反应转化成氨基酸,故A错误;B.麦芽糖是能发
生水解反应生成葡萄糖的二糖,麦芽糖是能发生银镜反应的还原糖,故B错误;C.由结构
简式可知,尿素分子的官能团为酰胺基,所以尿素属于酰胺类有机物,故C正确;D.大多
数生物体的遗传物质是DNA,少数生物体的遗传物质是RNA,一种病毒只含一种核酸DNA或
RNA,不会既有DNA又有RNA,故D错误;故选C。
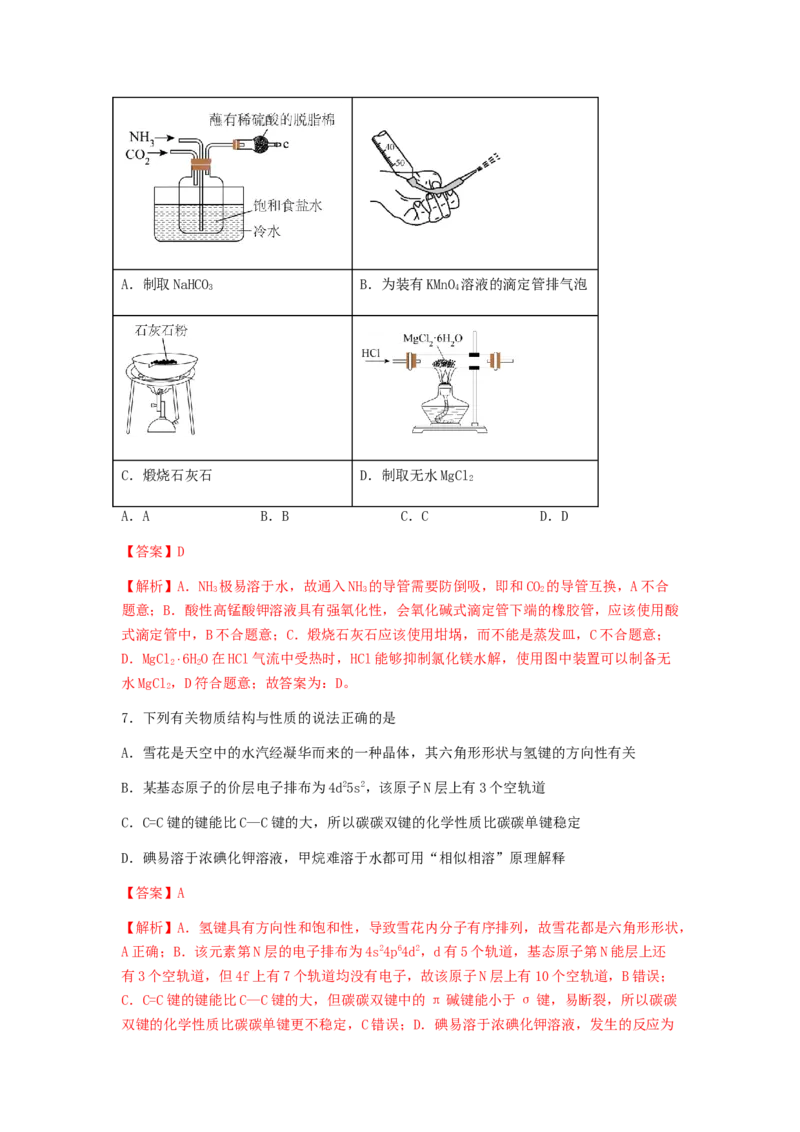
6.用下列实验装置进行相应实验,其中装置正确且能达到实验目的的是A.制取NaHCO B.为装有KMnO 溶液的滴定管排气泡
3 4
C.煅烧石灰石 D.制取无水MgCl
2
A.A B.B C.C D.D
【答案】D
【解析】A.NH 极易溶于水,故通入NH 的导管需要防倒吸,即和CO 的导管互换,A不合
3 3 2
题意;B.酸性高锰酸钾溶液具有强氧化性,会氧化碱式滴定管下端的橡胶管,应该使用酸
式滴定管中,B不合题意;C.煅烧石灰石应该使用坩埚,而不能是蒸发皿,C不合题意;
D.MgCl 2⋅6H
2
O在HCl气流中受热时,HCl能够抑制氯化镁水解,使用图中装置可以制备无
水MgCl,D符合题意;故答案为:D。
2
7.下列有关物质结构与性质的说法正确的是
A.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关
B.某基态原子的价层电子排布为4d25s2,该原子N层上有3个空轨道
C.C=C键的键能比C—C键的大,所以碳碳双键的化学性质比碳碳单键稳定
D.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
【答案】A
【解析】A.氢键具有方向性和饱和性,导致雪花内分子有序排列,故雪花都是六角形形状,
A正确;B.该元素第N层的电子排布为4s24p64d2,d有5个轨道,基态原子第N能层上还
有3个空轨道,但4f上有7个轨道均没有电子,故该原子N层上有10个空轨道,B错误;
C.C=C键的键能比C—C键的大,但碳碳双键中的π碱键能小于σ键,易断裂,所以碳碳
双键的化学性质比碳碳单键更不稳定,C错误;D.碘易溶于浓碘化钾溶液,发生的反应为I+I- ,与相似相溶原理无关,甲烷是非极性分子,HO是极性分子,故CH 难溶于水
2 2 4
可用“相似相溶”原理解释,D错误;故选A。
8.关于反应2CuS+14HNO=2CuSO+2Cu(NO)+5NO↑+5NO↑+7HO,下列说法不正确的是
2 3 4 3 2 2 2
A.HNO 在反应中体现氧化性和酸性
3
B.CuSO 和Cu(NO) 都是氧化产物
4 3 2
C.0.2mol CuS参加反应,转移电子2mol
2
D.随着产物中NO和NO 比例的改变,CuSO 和Cu(NO) 的比例也发生相应的改变
2 4 3 2
【答案】D
【解析】A.反应中N元素化合价从+5价降低到+2价,被还原,HNO 作氧化剂,体现了氧
3
化性;生成物有Cu(NO),还体现了HNO 的酸性,A正确;B.反应中Cu元素化合价由+1
3 2 3
价升高到+2价,S元素化合价从-2价升高到0价,硫酸铜和硝酸铜都是氧化产物,B正确;
C.CuS作还原剂,Cu元素化合价由+1价升高到+2价,S元素化合价从-2价升高到0价,
2
0.2molCuS参与反应,转移2mol电子,C正确;D.根据原子守恒,每1molCuS参与反应,
2 2
S守恒则硫酸铜1mol,Cu守恒则硝酸铜1mol,硫酸铜与硝酸铜的比例一直是1:1,D错误;
答案选D。
9.已知 的立方晶胞如图所示,其晶胞参数为a pm。下列说法正确的是
A.与 距离最近的 数目为4
B. 晶体中 与 之间的最近距离为
C. 晶体的密度为
D.晶胞中 围成的立方体棱长为 pm
【答案】C
【分析】由图知,该晶胞中,黑球在面心和顶点,共有4个,白球在晶胞内,共有8个,故黑球为 ,白球为 ,据此回答。
【解析】A.与 距离最近的 数目为8,A错误;B. 晶体中 与 之间的最近
距离为体对角线的四分之一,故最近距离为 ,B错误;C. 晶体的密度为
,C正确;D.晶胞中 围成的立方体
的体对角线为 ,故棱长为 pm,D错误;故选C。
10.某实验小组在探究 性质时,做了如下实验:
实验Ⅰ:向NaCl溶液中加入 溶液,溶液呈绿色。
实验Ⅱ:向 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生
绿色沉淀。
实验Ⅲ:向 溶液中加入适量氨水,溶液变为深蓝色。
实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入 溶液,产生蓝色沉淀。
资料显示: 为黄色, 为绿色不溶物。
下列说法错误的是
A.实验Ⅰ: 在NaCl溶液中部分转化为
B.实验Ⅱ:Mg消耗了溶液中的 从而产生了
C.实验Ⅲ:有 生成
D.实验Ⅳ:获得的蓝色沉淀为
【答案】D
【解析】A.向NaCl溶液中加入 溶液后溶液呈绿色,是 在NaCl溶液中部分转
化为 ,A正确;B. 为绿色不溶物,实验Ⅱ:产生大量气泡同时溶
液中产生绿色沉淀,Mg消耗了溶液中的 从而产生了 ,B正确;C.实验Ⅲ
溶液变为深蓝色是因为有 生成,C正确;D.实验Ⅳ产生蓝色沉淀为
,D错误;故答案为:D。11. 是合成某种全氮阴离子配合物所需的中间体。其中,
X、Y、Z、W为原子序数依次增大的短周期主族元素,X元素基态原子的电子只有一种自旋
取向,Y与Z是同周期相邻非金属元素,且Y的第一电离能大于Z。下列说法正确的是
A.简单氢化物的沸点:Y>Z
B.简单离子的半径:W>Z>Y>X
C.该中间体所含的大π键为
D. 分子的VSEPR模型名称为四面体
【答案】D
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X元素基态原子的电子只有
一种自旋取向,所以X为H元素;Y与Z是同周期相邻非金属元素,且Y的第一电离能大于
Z,所以Y为VA族元素、Z为VIA族元素,则Y为N元素,Z为O元素;根据X为H、Z为O
以及 可知W为+2价金属元素,即W为Mg元素。
【解析】A.Y和Z的简单氢化物分别为NH、HO,沸点HO>NH,故A错误;B.N3-、O2-、
3 2 2 3
Mg2+的电子层结构相同,电子层结构相同的微粒,核电荷数越大、半径越小,H+的半径在四
种中最小,所以简单离子的半径:N3-> O2-> Mg2+>H+,故B错误;C.该中间体中N-含有大
5
π键,大π键表示为 ,故C错误;D.HO的中心原子O原子含有4个价层电子对、 2
2
对孤电子对,所以其VSEPR模型名称为四面体,故D正确;故答案为:D。
12.已知在有机化合物中,吸电子基团(吸引电子云密度靠近)能力:
,推电子基团(排斥电子云密度偏离)能力:
,一般来说,体系越缺电子,酸性越强;体系
越富电子,碱性越强。下列说法错误的是
A.与Na反应的容易程度:
B.羟基的活性:CHOH>HO
6 5 2
C.酸性:
D.碱性: >
【答案】D
【解析】A.吸电子能力 ,因此 中C-H比 中C-H键更易断裂,则 比 更易与钠反应,A正确;B.苯环的吸电子能力强于H,故
羟基的活性:CHOH>HO,B正确;C.-Cl为吸电子基团, 中Cl原子数多,吸
6 5 2
电子能力强,导致-COOH更易电离,故酸性 ,C正确;D.甲基
为推电子基团,故 中六元环的电子云密度大,碱性强,D错误;故选:
D。
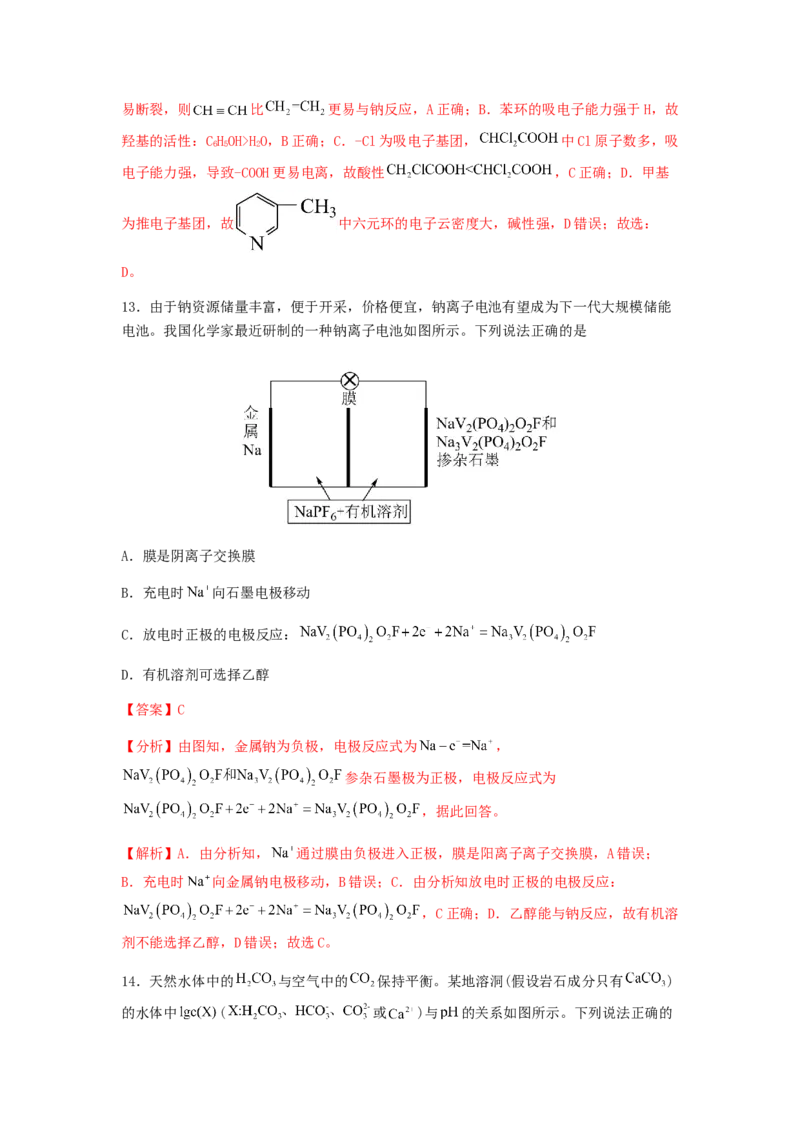
13.由于钠资源储量丰富,便于开采,价格便宜,钠离子电池有望成为下一代大规模储能
电池。我国化学家最近研制的一种钠离子电池如图所示。下列说法正确的是
A.膜是阴离子交换膜
B.充电时 向石墨电极移动
C.放电时正极的电极反应:
D.有机溶剂可选择乙醇
【答案】C
【分析】由图知,金属钠为负极,电极反应式为 ,
参杂石墨极为正极,电极反应式为
,据此回答。
【解析】A.由分析知, 通过膜由负极进入正极,膜是阳离子离子交换膜,A错误;
B.充电时 向金属钠电极移动,B错误;C.由分析知放电时正极的电极反应:
,C正确;D.乙醇能与钠反应,故有机溶
剂不能选择乙醇,D错误;故选C。
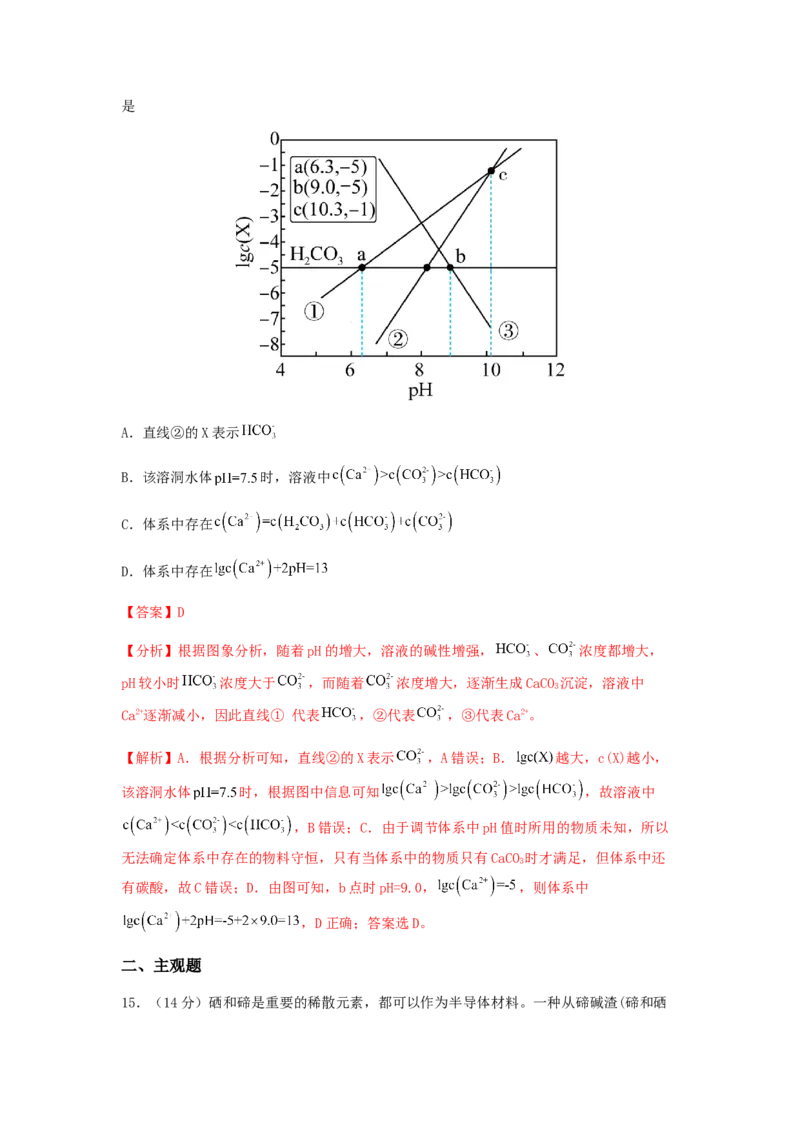
14.天然水体中的 与空气中的 保持平衡。某地溶洞(假设岩石成分只有 )
的水体中 ( 或 )与 的关系如图所示。下列说法正确的是
A.直线②的X表示
B.该溶洞水体 时,溶液中
C.体系中存在
D.体系中存在
【答案】D
【分析】根据图象分析,随着pH的增大,溶液的碱性增强, 、 浓度都增大,
pH较小时 浓度大于 ,而随着 浓度增大,逐渐生成CaCO 沉淀,溶液中
3
Ca2+逐渐减小,因此直线① 代表 ,②代表 ,③代表Ca2+。
【解析】A.根据分析可知,直线②的X表示 ,A错误;B. 越大,c(X)越小,
该溶洞水体 时,根据图中信息可知 ,故溶液中
,B错误;C.由于调节体系中pH值时所用的物质未知,所以
无法确定体系中存在的物料守恒,只有当体系中的物质只有CaCO 时才满足,但体系中还
3
有碳酸,故C错误;D.由图可知,b点时pH=9.0, ,则体系中
,D正确;答案选D。
二、主观题
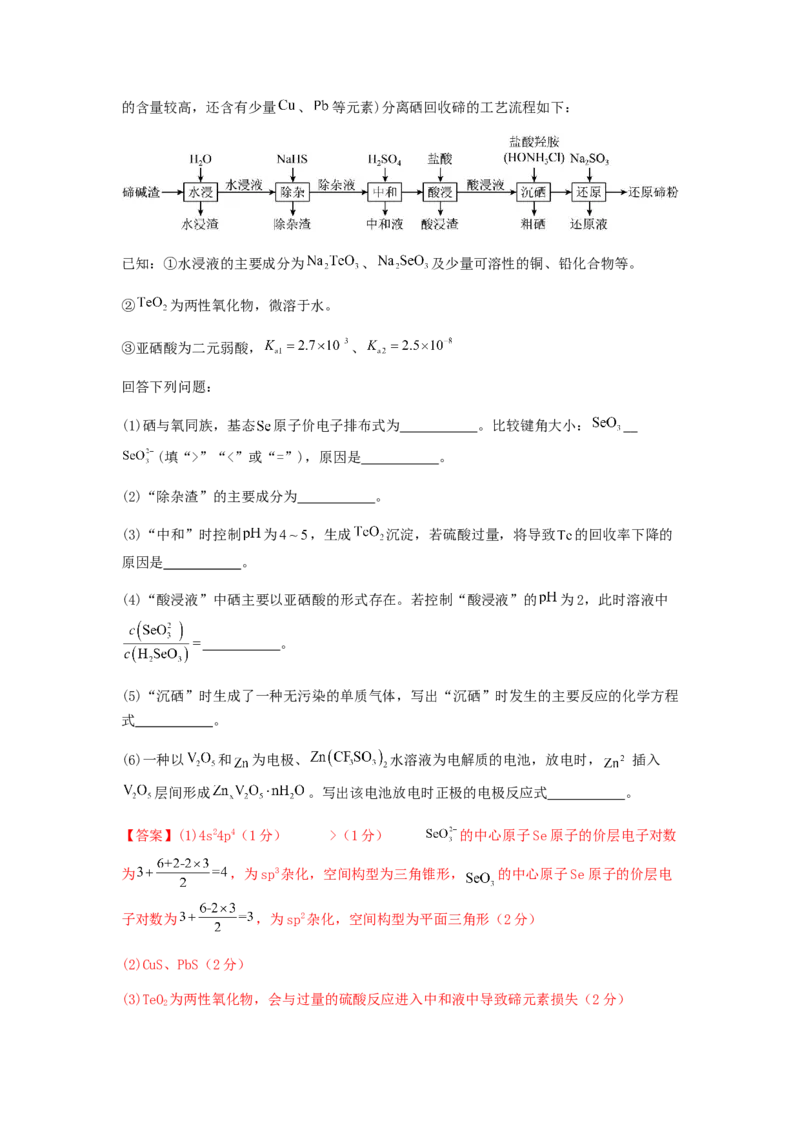
15.(14分)硒和碲是重要的稀散元素,都可以作为半导体材料。一种从碲碱渣(碲和硒的含量较高,还含有少量 、 等元素)分离硒回收碲的工艺流程如下:
已知:①水浸液的主要成分为 、 及少量可溶性的铜、铅化合物等。
② 为两性氧化物,微溶于水。
③亚硒酸为二元弱酸, 、
回答下列问题:
(1)硒与氧同族,基态 原子价电子排布式为 。比较键角大小:
(填“>”“<”或“=”),原因是 。
(2)“除杂渣”的主要成分为 。
(3)“中和”时控制 为 ,生成 沉淀,若硫酸过量,将导致 的回收率下降的
原因是 。
(4)“酸浸液”中硒主要以亚硒酸的形式存在。若控制“酸浸液”的 为2,此时溶液中
。
(5)“沉硒”时生成了一种无污染的单质气体,写出“沉硒”时发生的主要反应的化学方程
式 。
(6)一种以 和 为电极、 水溶液为电解质的电池,放电时, 插入
层间形成 。写出该电池放电时正极的电极反应式 。
【答案】(1)4s24p4(1分) >(1分) 的中心原子Se原子的价层电子对数
为 ,为sp3杂化,空间构型为三角锥形, 的中心原子Se原子的价层电
子对数为 ,为sp2杂化,空间构型为平面三角形(2分)
(2)CuS、PbS(2分)
(3)TeO 为两性氧化物,会与过量的硫酸反应进入中和液中导致碲元素损失(2分)
2(4) (2分)
(5) (2分)
(6) (2分)
【分析】碲碱渣加水水浸得到水浸渣和水浸液,水浸液的主要成分为 、
及少量可溶性的铜、铅化合物等,加入NaHS除杂,得到除杂渣,除杂渣主要成分为CuS、
PbS,除杂液加入硫酸中和得到中和固体物质,固体物质用盐酸酸浸得到酸浸渣和酸浸液,
酸浸液加入盐酸羟胺沉硒得到粗硒,溶液再加入亚硫酸钠还原得到还原液和还原碲粉;
【解析】(1)基态硒是第四周期ⅥA族元素,主族元素价电子数等于最外层电子数,所以
基态硒原子的价电子排布式为4s24p4 ; 的中心原子Se原子的价层电子对数为
,为sp3杂化,空间构型为三角锥形, 的中心原子Se原子的价层电子
对数为 ,为sp2杂化,空间构型为平面三角形,则键角大小: > ;
(2)由分析可知,“除杂渣”的主要成分为CuS、PbS;
(3) 为两性氧化物,微溶于水,“中和”时控制 为 ,生成 沉淀,若硫
酸过量,TeO 为两性氧化物,会与过量的硫酸反应进入中和液中导致碲元素损失,导致Te
2
的回收率下降;
(4) ;
(5)沉硒”时酸浸液加入盐酸羟胺沉硒得到粗硒,生成了一种无污染的单质气体,则为氮
气,发生的主要反应的化学方程式为 ;
(6)锌为活泼金属,放电时负极锌失去电子发生氧化反应生成锌离子: ;
为正极,得到电子发生还原反应生成 ,反应为:
。