文档内容
专练 22 化学工艺流程题
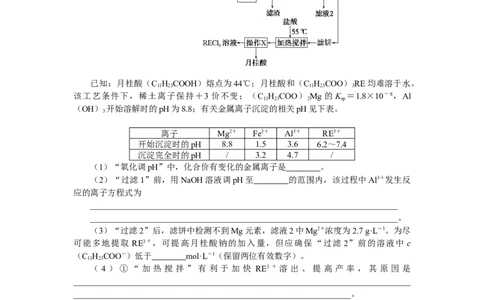
1.[2022·广东卷]稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方
特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺
如下:
已知:月桂酸(C H COOH)熔点为44℃;月桂酸和(C H COO) RE均难溶于水。
11 23 11 23 3
该工艺条件下,稀土离子保持+3 价不变;(C H COO) Mg 的 K =1.8×10-8,Al
11 23 2 sp
(OH) 开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
3
离子 Mg2+ Fe3+ Al3+ RE3+
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是 。
(2)“过滤1”前,用NaOH溶液调pH至 的范围内,该过程中Al3+发生反
应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(3)“过滤2”后,滤饼中检测不到Mg元素,滤液2中Mg2+浓度为2.7 g·L-1。为尽
可能多地提取 RE3+,可提高月桂酸钠的加入量,但应确保“过滤 2”前的溶液中 c
(C H COO-)低于 mol·L-1(保留两位有效数字)。
11 23
( 4 ) ① “ 加 热 搅 拌 ” 有 利 于 加 快 RE3 + 溶 出 、 提 高 产 率 , 其 原 因 是
_______________________________________________________________________________
_________________________________________________________________。
②“操作X”的过程为:先 ,再固液分离。
(5)该工艺中,可再生循环利用的物质有 (写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y。
3
①还原YCl 和PtCl 熔融盐制备Pt Y时,生成1 mol Pt Y转移 mol电子。
3 4 3 3
②Pt Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 O 的还原,发生的
3 2
电极反应为 。
2.[2021·湖南卷]碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原
料制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤Ⅰ.Na CO 的制备
2 3步骤Ⅱ.产品中NaHCO 含量测定
3
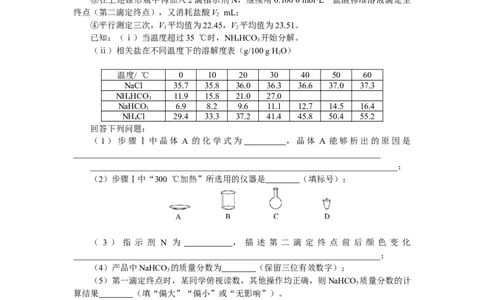
①称取产品2.500 g,用蒸馏水溶解,定容于250 mL 容量瓶中;
②移取25.00 mL上述溶液于锥形瓶,加入2滴指示剂M,用0.100 0 mol·L-1盐酸标准
溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸V mL;
1
③在上述锥形瓶中再加入2滴指示剂N,继续用0.100 0 mol·L-1盐酸标准溶液滴定至
终点(第二滴定终点),又消耗盐酸V mL;
2
④平行测定三次,V 平均值为22.45,V 平均值为23.51。
1 2
已知:(ⅰ)当温度超过35 ℃时,NH HCO 开始分解。
4 3
(ⅱ)相关盐在不同温度下的溶解度表(g/100 g H O)
2
温度/ ℃ 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
回答下列问题:
(1)步骤Ⅰ中晶体 A 的化学式为 ,晶体 A 能够析出的原因是
________________________________________________________________________
________________________________________________________________________;
(2)步骤Ⅰ中“300 ℃加热”所选用的仪器是 (填标号);
( 3 ) 指 示 剂 N 为 , 描 述 第 二 滴 定 终 点 前 后 颜 色 变 化
________________________________________________________________________;
(4)产品中NaHCO 的质量分数为 (保留三位有效数字);
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO 质量分数的计
3
算结果 (填“偏大”“偏小”或“无影响”)。
3.[2021·广东卷]对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝
(Al)、钼(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25 ℃时,HCO 的K =4.5×10-7,K =4.7×10-11;K (BaMoO )=3.5×10
2 3 a1 a2 sp 4
-8;K (BaCO )=2.6×10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO的形态存在。
sp 3(1)“焙烧”中,有NaMoO 生成,其中Mo元素的化合价为 。
2 4
(2)“沉铝”中,生成的沉淀X为 。
(3)“沉钼”中,pH为7.0。
①生成BaMoO 的离子方程式为
4
________________________________________________________________________
________________________________________________________________________。
②若条件控制不当,BaCO 也会沉淀。为避免BaMoO 中混入BaCO 沉淀,溶液中c∶c
3 4 3
= (列出算式)时,应停止加入BaCl 溶液。
2
(4)①滤液Ⅲ中,主要存在的钠盐有NaCl和Y,Y为 。
②往滤液Ⅲ中添加适量NaCl固体后,通入足量 (填化学式)气体,再通
入足量CO,可析出Y。
2
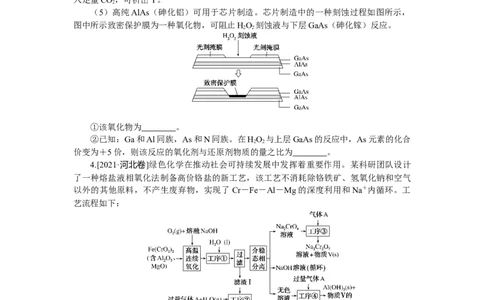
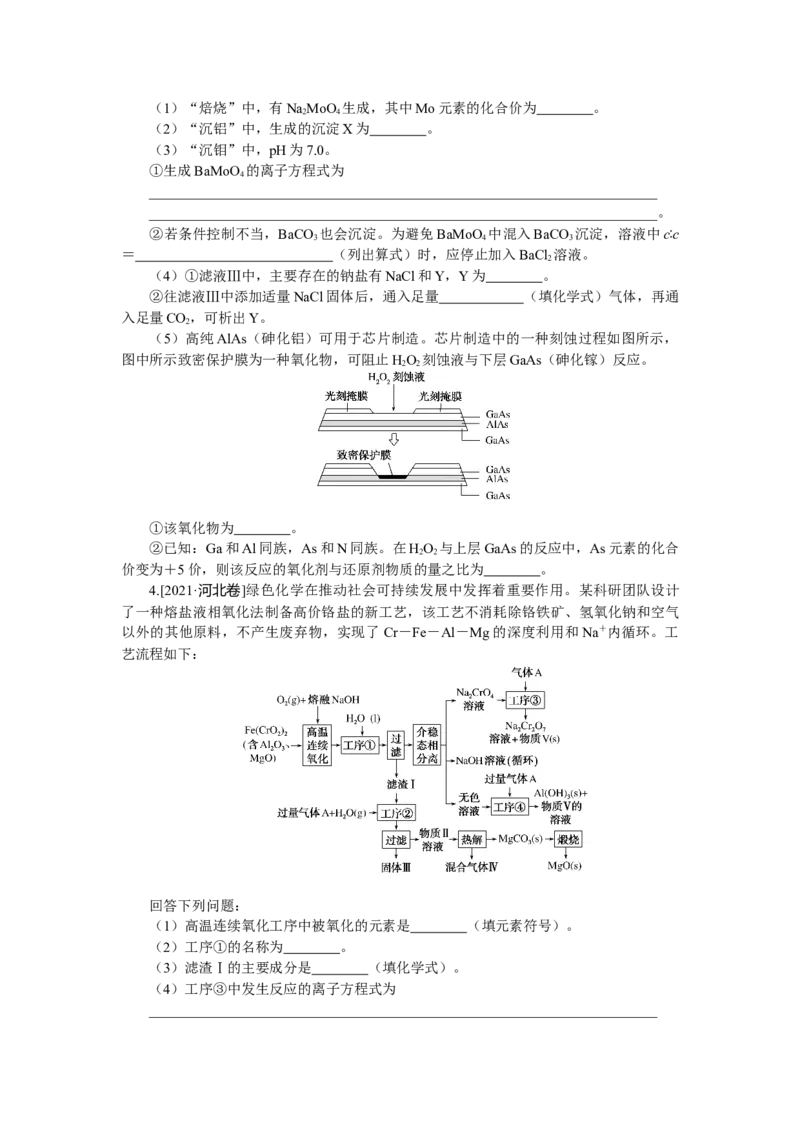
(5)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,
图中所示致密保护膜为一种氧化物,可阻止HO 刻蚀液与下层GaAs(砷化镓)反应。
2 2
①该氧化物为 。
②已知:Ga和Al同族,As和N同族。在HO 与上层GaAs的反应中,As元素的化合
2 2
价变为+5价,则该反应的氧化剂与还原剂物质的量之比为 。
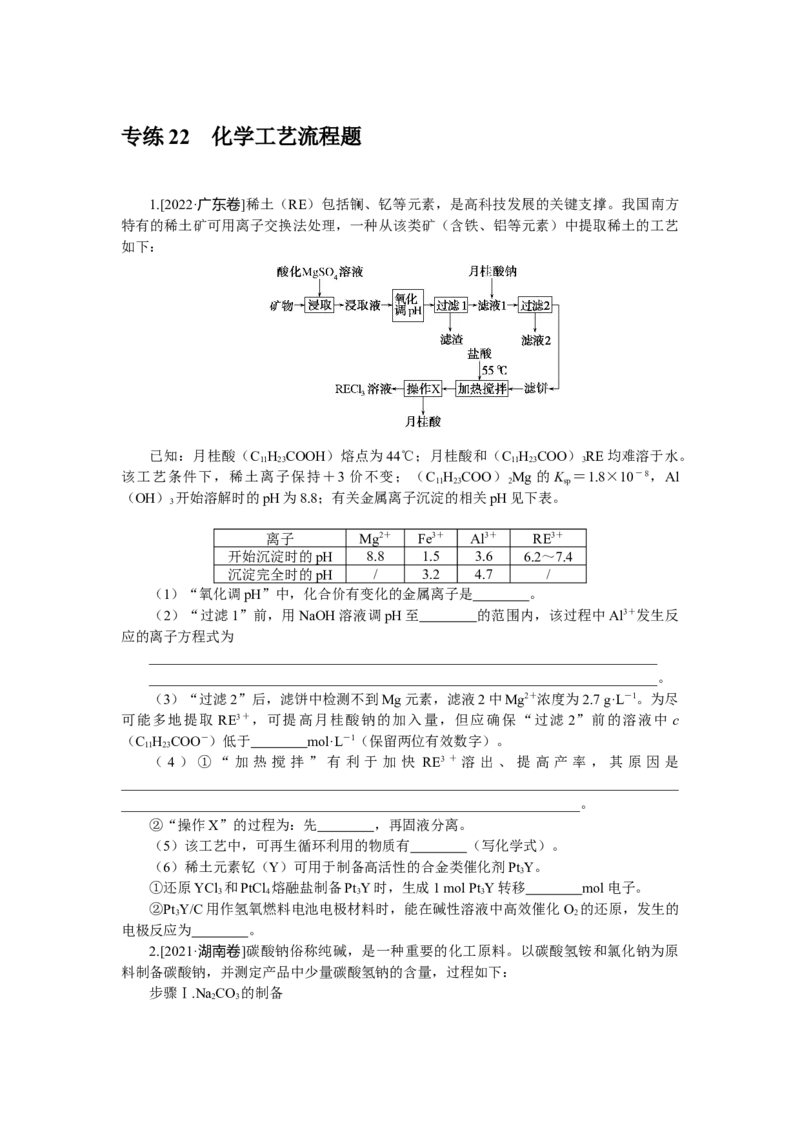
4.[2021·河北卷]绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计
了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气
以外的其他原料,不产生废弃物,实现了Cr-Fe-Al-Mg的深度利用和Na+内循环。工
艺流程如下:
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是 (填元素符号)。
(2)工序①的名称为 。
(3)滤渣Ⅰ的主要成分是 (填化学式)。
(4)工序③中发生反应的离子方程式为
________________________________________________________________________________________________________________________________________________。
(5)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式
为 ,可代替NaOH的化学试剂还有 (填化学式)。
(6)热解工序产生的混合气体最适宜返回工序 (填“①”“②”“③”或
“④”)参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为 。{通常认为溶液
中离子浓度小于10-5 mol·L-1为沉淀完全:Al(OH)
3
+OH- ⇌Al(OH) K=100.63;K
w
=10-14,K [Al(OH)]=10-33}
sp 3