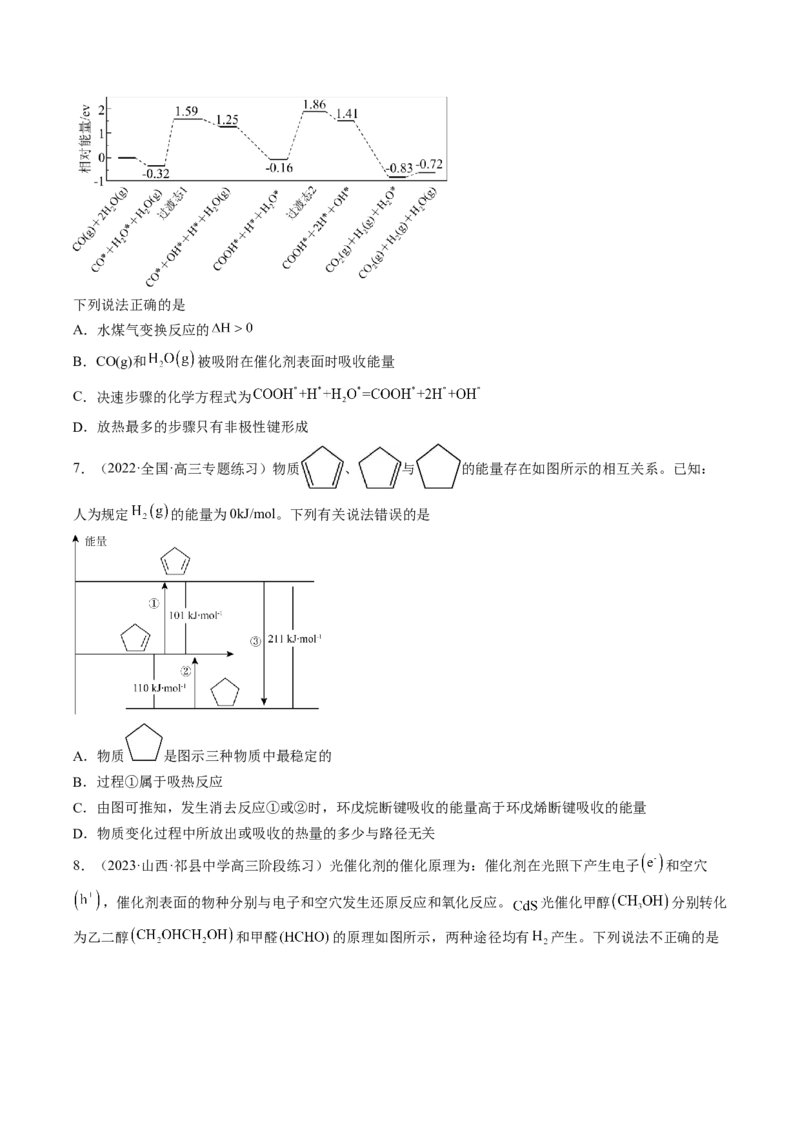文档内容
专项 12 化学能与热能 能量转化历程图
该专题分为三个板块
【1】知识点梳理
【2】真题模拟演练
【3】专项练习
【1】知识点梳理
一、ΔH的求解方式
1、ΔH=H(生成物)-H(反应物)
2、ΔH=∑E(反应物键能)-∑E(生成物键能)
3、盖斯定律
二、热化学方程式中的注意事项
(1)未标明反应物或生成物的状态而造成错误。
(2)反应热的符号使用不正确,即吸热反应未标出“+”号,放热反应未标出“-”号,从而导致错误。
(3)漏写ΔH的单位,或者将ΔH的单位写为kJ,从而造成错误。
(4)反应热的数值与方程式的计量数不对应而造成错误。
(5)对燃烧热、中和热的概念理解不到位,忽略其标准是1 mol可燃物或生成1 mol H O(l)而造成错误。
2
三、键长、能量、稳定性的关系
键长越长,键能越小,物质能量越大,越不稳定
键长越短,键能越大,物质能量越小,越稳定
【2】真题模拟演练
例1. (2021·东城区模拟)如图所示为某基元反应过程的能量变化(E1、E2、E3均大于0)。下列说法正确的是
( )
A.该反应的正反应为吸热反应
B.E+E 为该反应的活化能
1 3
C.图中对应的该反应的焓变ΔH=-E
2
D.NO 和CO分子发生有效碰撞才能形成过渡状态分子
2
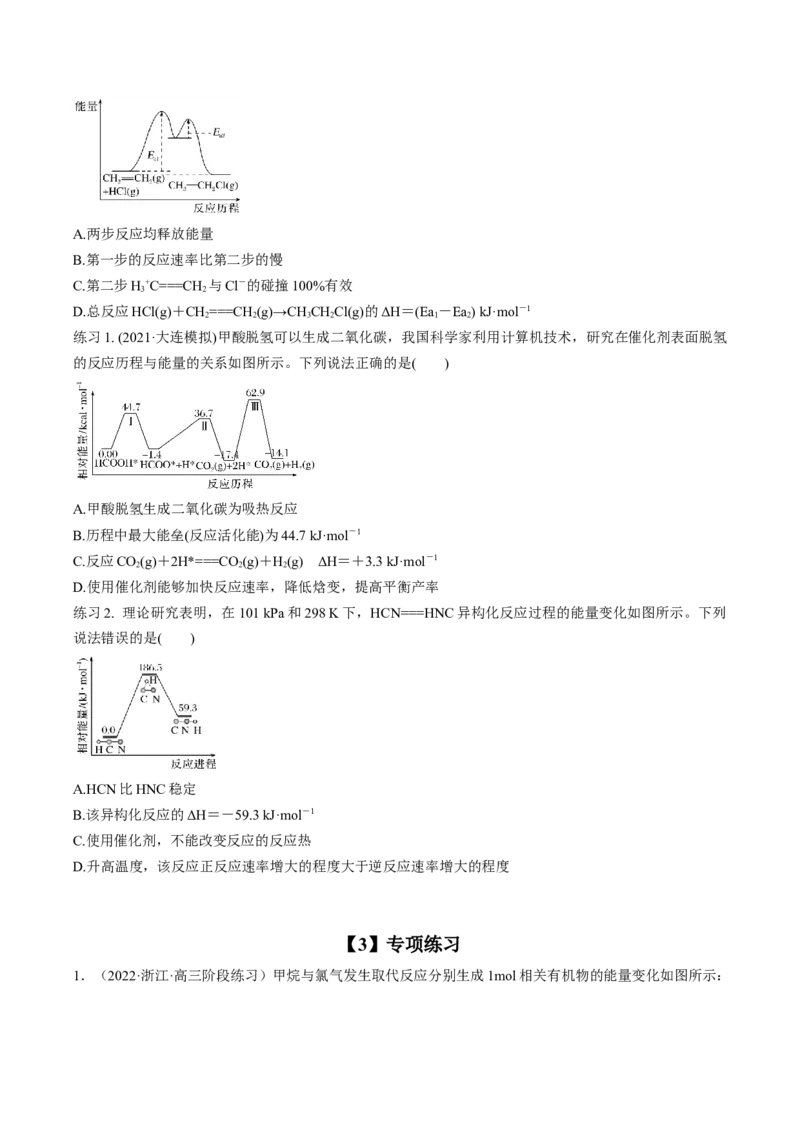
例2. (2021·厦门模拟)CH===CH 与HCl的加成反应由第一步HCl+CH===CH →H+C===CH +Cl-和第二
2 2 2 2 3 2
步H+C===CH +Cl-→CH—CHCl组成,能量与反应历程如图所示。下列说法正确的是( )
3 2 3 2A.两步反应均释放能量
B.第一步的反应速率比第二步的慢
C.第二步H+C===CH 与Cl-的碰撞100%有效
3 2
D.总反应HCl(g)+CH===CH (g)→CH CHCl(g)的ΔH=(Ea -Ea) kJ·mol-1
2 2 3 2 1 2
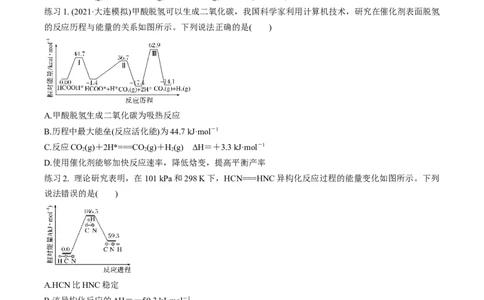
练习1. (2021·大连模拟)甲酸脱氢可以生成二氧化碳,我国科学家利用计算机技术,研究在催化剂表面脱氢
的反应历程与能量的关系如图所示。下列说法正确的是( )
A.甲酸脱氢生成二氧化碳为吸热反应
B.历程中最大能垒(反应活化能)为44.7 kJ·mol-1
C.反应CO(g)+2H*===CO(g)+H(g) ΔH=+3.3 kJ·mol-1
2 2 2
D.使用催化剂能够加快反应速率,降低焓变,提高平衡产率
练习2. 理论研究表明,在101 kPa和298 K下,HCN===HNC异构化反应过程的能量变化如图所示。下列
说法错误的是( )
A.HCN比HNC稳定
B.该异构化反应的ΔH=-59.3 kJ·mol-1
C.使用催化剂,不能改变反应的反应热
D.升高温度,该反应正反应速率增大的程度大于逆反应速率增大的程度
【3】专项练习
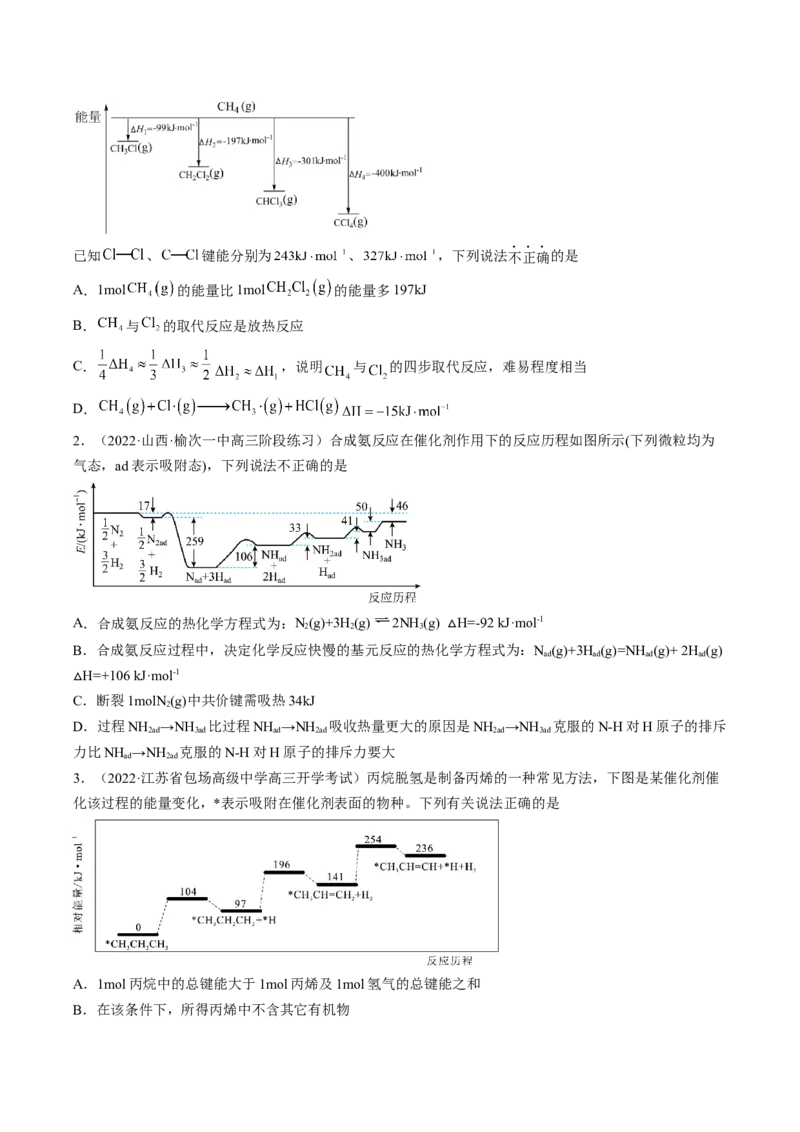
1.(2022·浙江·高三阶段练习)甲烷与氯气发生取代反应分别生成1mol相关有机物的能量变化如图所示:已知 、 键能分别为 、 ,下列说法不正确的是
A.1mol 的能量比1mol 的能量多197kJ
B. 与 的取代反应是放热反应
C. ,说明 与 的四步取代反应,难易程度相当
D.
2.(2022·山西·榆次一中高三阶段练习)合成氨反应在催化剂作用下的反应历程如图所示(下列微粒均为
气态,ad表示吸附态),下列说法不正确的是
A.合成氨反应的热化学方程式为:N(g)+3H(g) 2NH (g) H=-92 kJ·mol-1
2 2 3
B.合成氨反应过程中,决定化学反应快慢的基元反应的热化 △ 学方程式为:N ad (g)+3H ad (g)=NH ad (g)+ 2H ad (g)
H=+106 kJ·mol-1
C.断裂1molN (g)中共价键需吸热34kJ
△ 2
D.过程NH →NH 比过程NH →NH 吸收热量更大的原因是NH →NH 克服的N-H对H原子的排斥
2ad 3ad ad 2ad 2ad 3ad
力比NH →NH 克服的N-H对H原子的排斥力要大
ad 2ad
3.(2022·江苏省包场高级中学高三开学考试)丙烷脱氢是制备丙烯的一种常见方法,下图是某催化剂催
化该过程的能量变化,*表示吸附在催化剂表面的物种。下列有关说法正确的是
A.1mol丙烷中的总键能大于1mol丙烯及1mol氢气的总键能之和
B.在该条件下,所得丙烯中不含其它有机物C.该过程中发生了碳碳键的断裂与形成
D.相同条件下在该催化剂表面, 比 脱氢更困难
4.(2022·全国·高三专题练习)已知化合物A与HO在一定条件下反应生成化合物B与 ,其反应
2
历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
A.中间体I2比中间体I1更稳定
B.该历程中的反应③为该反应的决速步
C.平衡状态时,升温使反应正向移动
D.使用更高效的催化剂可降低反应所需的活化能和反应热
5.(2022·重庆巴蜀中学高三阶段练习)卤代烃在有机合成中发挥着重要桥梁作用,研究卤代烃的反应历
程十分有意义。 发生水解反应的历程如图所示:
说明:①E表示方框中物质的总能量(单位:kJ/mol),TS表示过渡态。
②相关化学键键能: 为351kJ/mol。
下列说法错误的是
A.水解反应过程中中心碳原子的杂化轨道类型发生变化
B. 水解总反应的 可表示为
C.若 ,则决定速率步骤的化学方程式为
D.若 ,C—Br键能为426kJ/mol
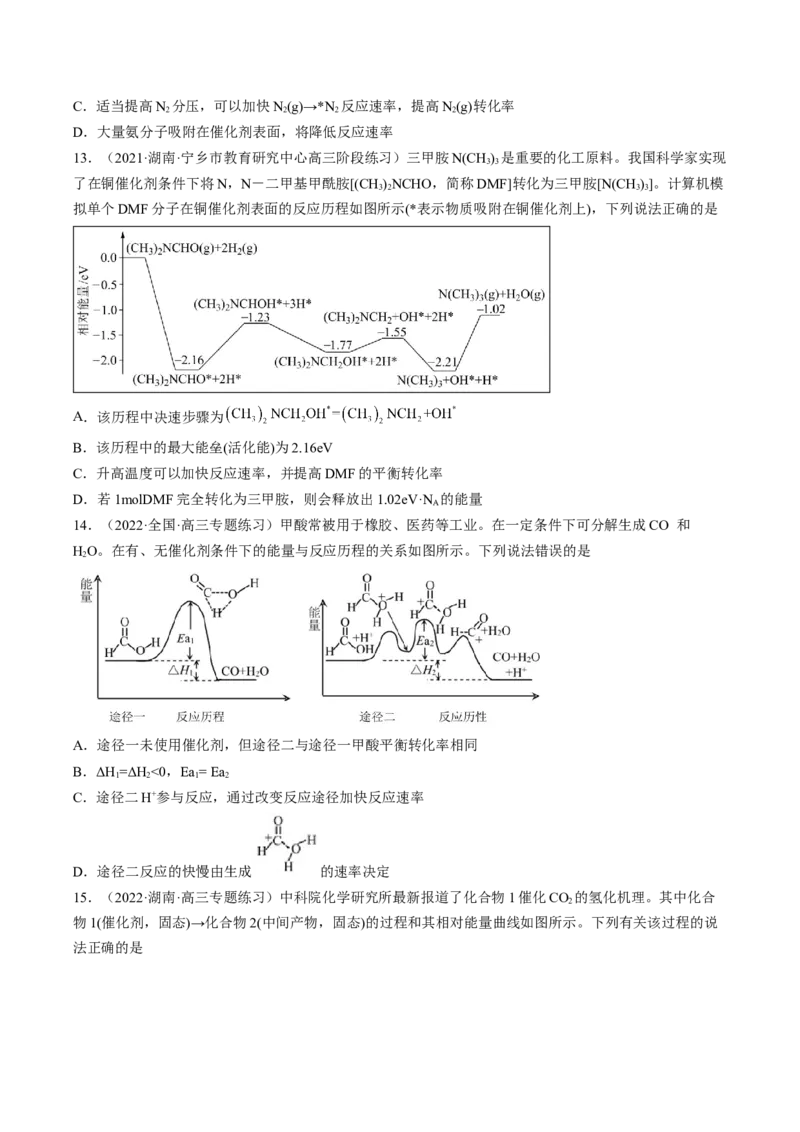
6.(2022·河南·高三阶段练习)水煤气变换反应 在金催化剂表面上的历
程如下图所示(吸附在金催化剂表面上的物种用*标注)。下列说法正确的是
A.水煤气变换反应的
B.CO(g)和 被吸附在催化剂表面时吸收能量
C.决速步骤的化学方程式为
D.放热最多的步骤只有非极性键形成
7.(2022·全国·高三专题练习)物质 、 与 的能量存在如图所示的相互关系。已知:
人为规定 的能量为0kJ/mol。下列有关说法错误的是
A.物质 是图示三种物质中最稳定的
B.过程①属于吸热反应
C.由图可推知,发生消去反应①或②时,环戊烷断键吸收的能量高于环戊烯断键吸收的能量
D.物质变化过程中所放出或吸收的热量的多少与路径无关
8.(2023·山西·祁县中学高三阶段练习)光催化剂的催化原理为:催化剂在光照下产生电子 和空穴
,催化剂表面的物种分别与电子和空穴发生还原反应和氧化反应。 光催化甲醇 分别转化
为乙二醇 和甲醛 的原理如图所示,两种途径均有 产生。下列说法不正确的是A. 和 均为反应的中间体
B. 从催化剂表面脱附需吸收能量
C.途径1中产生 的原理为
D.途径1和途径2中 断裂的化学键相同
9.(2022·全国·高三专题练习)丙烷卤代反应的部分反应机理(以Cl 为例)如下:
2
I.Cl(g)→2Cl·(g)
2
II.CHCHCH(g)+Cl·(g)→ (g)+HCl(g)
3 2 3
III. (g)+Cl (g)→CH CHClCH (g)+Cl·(g)
2 3 3
其中,II步反应为决速步骤,能量随反应进程的变化如图,下列说法不正确的是
A.氯代时I步反应的ΔH大于溴代时
B.稳定性: 小于
C.丙烷中不同基团上碳氢键断裂吸收的能量不同
D.丙烷氯代产物中 与溴代产物中 近似相等
10.(2022·全国·高三专题练习)苯与 的催化反应历程如图所示。关于该反应历程,下列说法正确的是A.苯与 的催化反应为放热反应
B.该反应历程,苯与 的催化反应可生成溴苯、邻二溴苯
C.苯与 的催化反应决速步伴随着极性键的断裂与形成
D.从反应速率角度,苯与Br ,的催化反应主反应为取代反应,原因是该反应活化能更低
2
11.(2022·全国·高三专题练习)下图是不饱和烃加氢时能量变化示意图(E代表反应物具有的总能量),具
体数据如下:
反应
(1)如果 与 以物质的量 反应,其主要产物是X。
(2)如果 与 的醇溶液共热后,主要产物是Y,另一副产物是Z。
下列推断正确的是A.不饱和烃加氢的反应的 B.Y是
C.X是 D.
12.(2022·江苏·启东中学模拟预测)我国科研人员研究发现合成氨的反应历程有多种,其中有一种反应
历程如图所示(吸附在催化剂表面的物质用*表示)。下列说法错误的是
A.N 生成NH 是通过多步还原反应生成的
2 3
B.过程Ⅰ和Ⅲ中能量的变化不相同C.适当提高N 分压,可以加快N(g)→*N 反应速率,提高N(g)转化率
2 2 2 2
D.大量氨分子吸附在催化剂表面,将降低反应速率
13.(2021·湖南·宁乡市教育研究中心高三阶段练习)三甲胺N(CH ) 是重要的化工原料。我国科学家实现
3 3
了在铜催化剂条件下将N,N-二甲基甲酰胺[(CH )NCHO,简称DMF]转化为三甲胺[N(CH )]。计算机模
3 2 3 3
拟单个DMF分子在铜催化剂表面的反应历程如图所示(*表示物质吸附在铜催化剂上),下列说法正确的是
A.该历程中决速步骤为
B.该历程中的最大能垒(活化能)为2.16eV
C.升高温度可以加快反应速率,并提高DMF的平衡转化率
D.若1molDMF完全转化为三甲胺,则会释放出1.02eV·N 的能量
A
14.(2022·全国·高三专题练习)甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成CO 和
HO。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
2
A.途径一未使用催化剂,但途径二与途径一甲酸平衡转化率相同
B.ΔH=ΔH <0,Ea= Ea
1 2 1 2
C.途径二H+参与反应,通过改变反应途径加快反应速率
D.途径二反应的快慢由生成 的速率决定
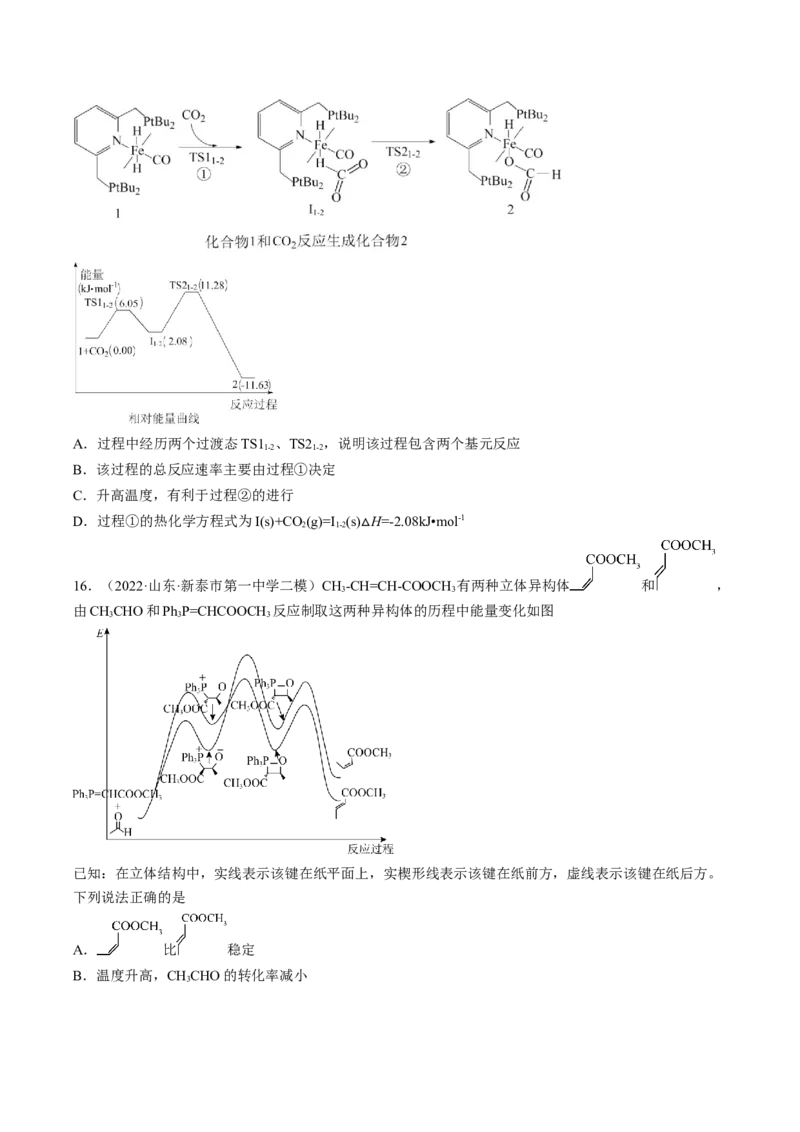
15.(2022·湖南·高三专题练习)中科院化学研究所最新报道了化合物1催化CO 的氢化机理。其中化合
2
物1(催化剂,固态)→化合物2(中间产物,固态)的过程和其相对能量曲线如图所示。下列有关该过程的说
法正确的是A.过程中经历两个过渡态TS1 、TS2 ,说明该过程包含两个基元反应
1-2 1-2
B.该过程的总反应速率主要由过程①决定
C.升高温度,有利于过程②的进行
D.过程①的热化学方程式为I(s)+CO (g)=I (s) H=-2.08kJ•mol-1
2 1-2
△
16.(2022·山东·新泰市第一中学二模)CH-CH=CH-COOCH 有两种立体异构体 和 ,
3 3
由CHCHO和Ph P=CHCOOCH 反应制取这两种异构体的历程中能量变化如图
3 3 3
已知:在立体结构中,实线表示该键在纸平面上,实楔形线表示该键在纸前方,虚线表示该键在纸后方。
下列说法正确的是
A. 比 稳定
B.温度升高,CHCHO的转化率减小
3C.生成 的过程中,速率最快的是由 生成 的反应
D.两个反应历程中,中间产物相同
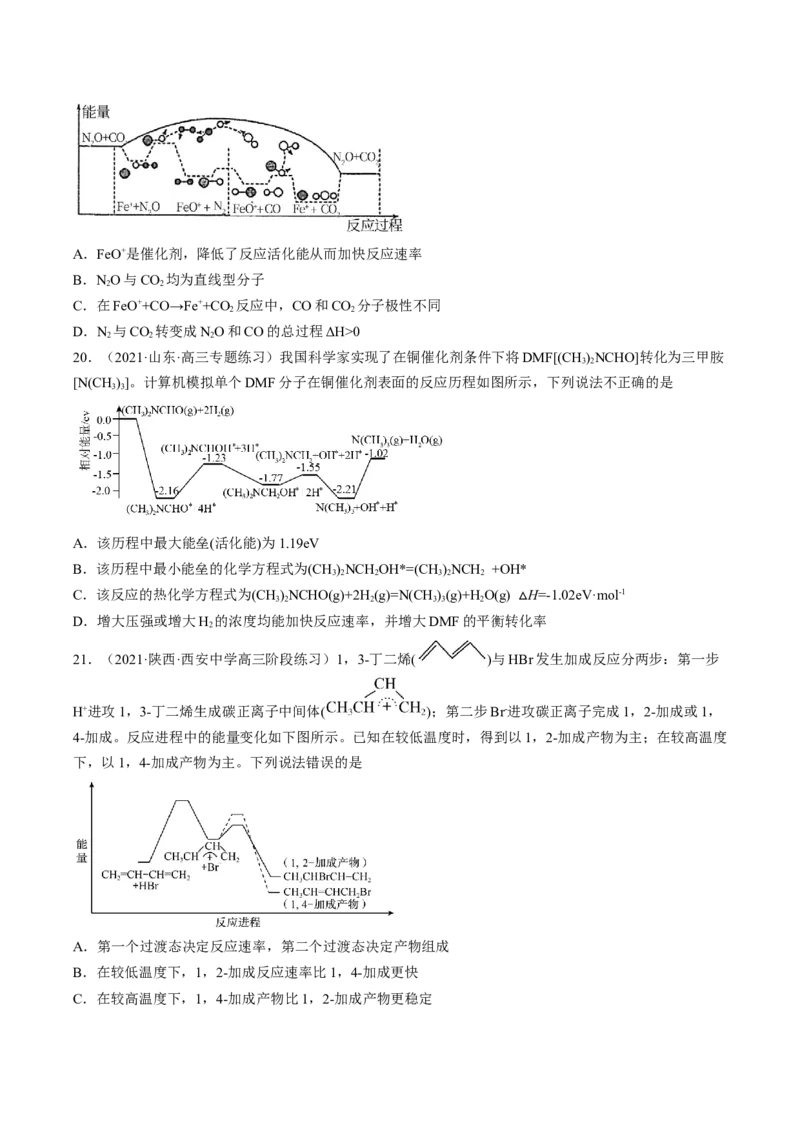
17.(2022·全国·高三专题练习)相同温度和压强下,关于反应的 ,下列判断正确的是
A. B.
C. D.
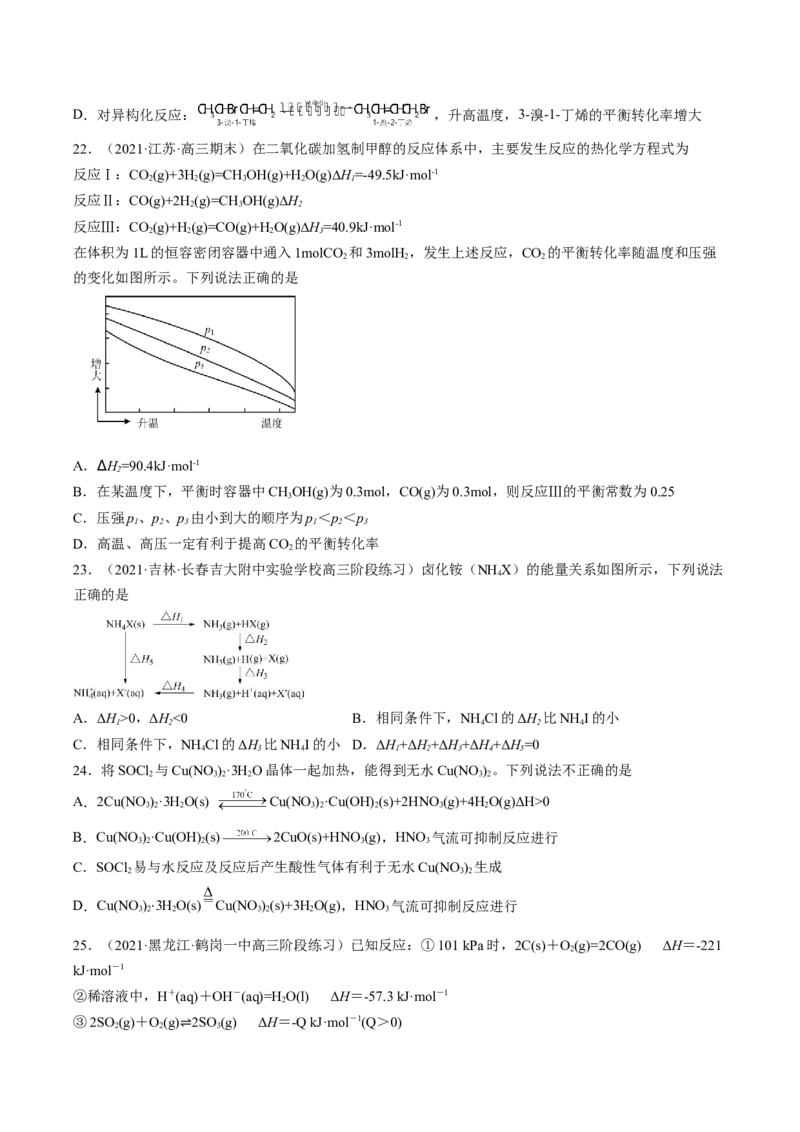
18.苯乙烷 与Cl 在光照条件下发生一氯取代,生成两种一取代物的速率如图1,反应基
2
本历程如图Ⅱ,下列说法不正确的是
A.反应①②③的 H>0,反应④⑤⑥的 H<0
B.光照条件下,得到等物质的量的(A)和(B)时,生成(A)时需要能量更少
△ △
C.使用恰当的催化剂,可以使反应②的程度减小,反应③的程度增大
D.在相同条件下,由 分别制备等物质的量的 和 , H相
等
△
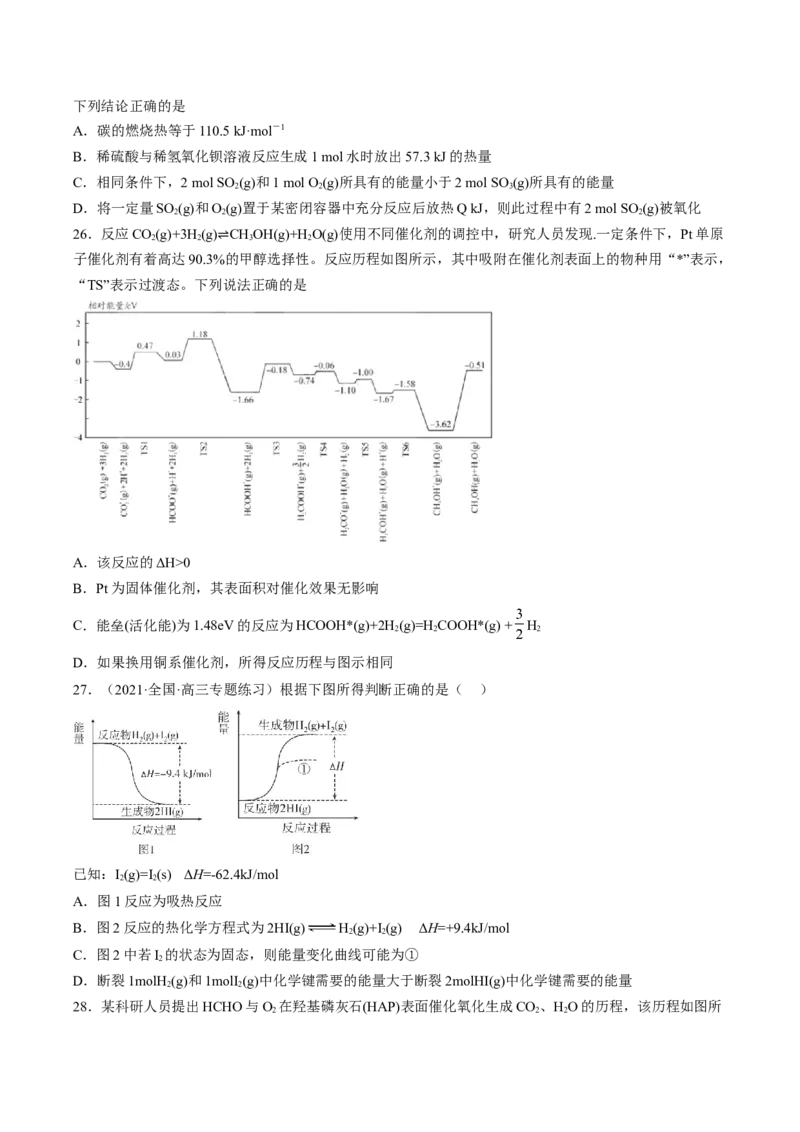
19.(2021·辽宁·沈阳二中高三阶段练习)研究表明NO与CO在Fe+作用下发生反应的能量变化及反应过
2
程如图所示,下列说法错误的是A.FeO+是催化剂,降低了反应活化能从而加快反应速率
B.NO与CO 均为直线型分子
2 2
C.在FeO++CO→Fe++CO 反应中,CO和CO 分子极性不同
2 2
D.N 与CO 转变成NO和CO的总过程ΔH>0
2 2 2
20.(2021·山东·高三专题练习)我国科学家实现了在铜催化剂条件下将DMF[(CH )NCHO]转化为三甲胺
3 2
[N(CH )]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法不正确的是
3 3
A.该历程中最大能垒(活化能)为1.19eV
B.该历程中最小能垒的化学方程式为(CH)NCH OH*=(CH )NCH +OH*
3 2 2 3 2 2
C.该反应的热化学方程式为(CH)NCHO(g)+2H(g)=N(CH )(g)+HO(g) H=-1.02eV·mol-1
3 2 2 3 3 2
D.增大压强或增大H 的浓度均能加快反应速率,并增大DMF的平衡转化率
2 △
21.(2021·陕西·西安中学高三阶段练习)1,3-丁二烯( )与HBr发生加成反应分两步:第一步
H+进攻1,3-丁二烯生成碳正离子中间体( );第二步Br-进攻碳正离子完成1,2-加成或1,
4-加成。反应进程中的能量变化如下图所示。已知在较低温度时,得到以1,2-加成产物为主;在较高温度
下,以1,4-加成产物为主。下列说法错误的是
A.第一个过渡态决定反应速率,第二个过渡态决定产物组成
B.在较低温度下,1,2-加成反应速率比1,4-加成更快
C.在较高温度下,1,4-加成产物比1,2-加成产物更稳定D.对异构化反应: ,升高温度,3-溴-1-丁烯的平衡转化率增大
22.(2021·江苏·高三期末)在二氧化碳加氢制甲醇的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO(g)+3H(g)=CH OH(g)+H O(g)∆H=-49.5kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO(g)+2H(g)=CH OH(g)∆H
2 3 2
反应Ⅲ:CO(g)+H(g)=CO(g)+HO(g)∆H=40.9kJ·mol-1
2 2 2 3
在体积为1L的恒容密闭容器中通入1molCO 和3molH ,发生上述反应,CO 的平衡转化率随温度和压强
2 2 2
的变化如图所示。下列说法正确的是
A.∆H=90.4kJ·mol-1
2
B.在某温度下,平衡时容器中CHOH(g)为0.3mol,CO(g)为0.3mol,则反应Ⅲ的平衡常数为0.25
3
C.压强p、p、p 由小到大的顺序为p<p<p
1 2 3 1 2 3
D.高温、高压一定有利于提高CO 的平衡转化率
2
23.(2021·吉林·长春吉大附中实验学校高三阶段练习)卤化铵(NH X)的能量关系如图所示,下列说法
4
正确的是
A.ΔH>0,ΔH<0 B.相同条件下,NH Cl的ΔH 比NH I的小
1 2 4 2 4
C.相同条件下,NH Cl的ΔH 比NH I的小 D.ΔH+ΔH+ΔH+ΔH+ΔH=0
4 3 4 1 2 3 4 5
24.将SOCl 与Cu(NO )·3H O晶体一起加热,能得到无水Cu(NO )。下列说法不正确的是
2 3 2 2 3 2
A.2Cu(NO )·3H O(s) Cu(NO )·Cu(OH) (s)+2HNO(g)+4HO(g)ΔH>0
3 2 2 3 2 2 3 2
B.Cu(NO )·Cu(OH) (s) 2CuO(s)+HNO (g),HNO 气流可抑制反应进行
3 2 2 3 3
C.SOCl 易与水反应及反应后产生酸性气体有利于无水Cu(NO ) 生成
2 3 2
D.Cu(NO ) 3HO(s) Cu(NO )(s)+3HO(g),HNO 气流可抑制反应进行
3 2 2 3 2 2 3
⋅
25.(2021·黑龙江·鹤岗一中高三阶段练习)已知反应:①101 kPa时,2C(s)+O(g)=2CO(g) ΔH=-221
2
kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H O(l) ΔH=-57.3 kJ·mol-1
2
③2SO (g)+O(g) 2SO (g) ΔH=-Q kJ·mol-1(Q>0)
2 2 3
⇌下列结论正确的是
A.碳的燃烧热等于110.5 kJ·mol-1
B.稀硫酸与稀氢氧化钡溶液反应生成1 mol水时放出57.3 kJ的热量
C.相同条件下,2 mol SO (g)和1 mol O (g)所具有的能量小于2 mol SO (g)所具有的能量
2 2 3
D.将一定量SO (g)和O(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO (g)被氧化
2 2 2
26.反应CO(g)+3H(g) CHOH(g)+H O(g)使用不同催化剂的调控中,研究人员发现.一定条件下,Pt单原
2 2 3 2
子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,
⇌
“TS”表示过渡态。下列说法正确的是
A.该反应的ΔH>0
B.Pt为固体催化剂,其表面积对催化效果无影响
C.能垒(活化能)为1.48eV的反应为HCOOH*(g)+2H (g)=HCOOH*(g) + H
2 2 2
D.如果换用铜系催化剂,所得反应历程与图示相同
27.(2021·全国·高三专题练习)根据下图所得判断正确的是( )
已知:I(g)=I (s) ΔH=-62.4kJ/mol
2 2
A.图1反应为吸热反应
B.图2反应的热化学方程式为2HI(g) H(g)+I (g) ΔH=+9.4kJ/mol
2 2
C.图2中若I 的状态为固态,则能量变化曲线可能为①
2
D.断裂1molH (g)和1molI (g)中化学键需要的能量大于断裂2molHI(g)中化学键需要的能量
2 2
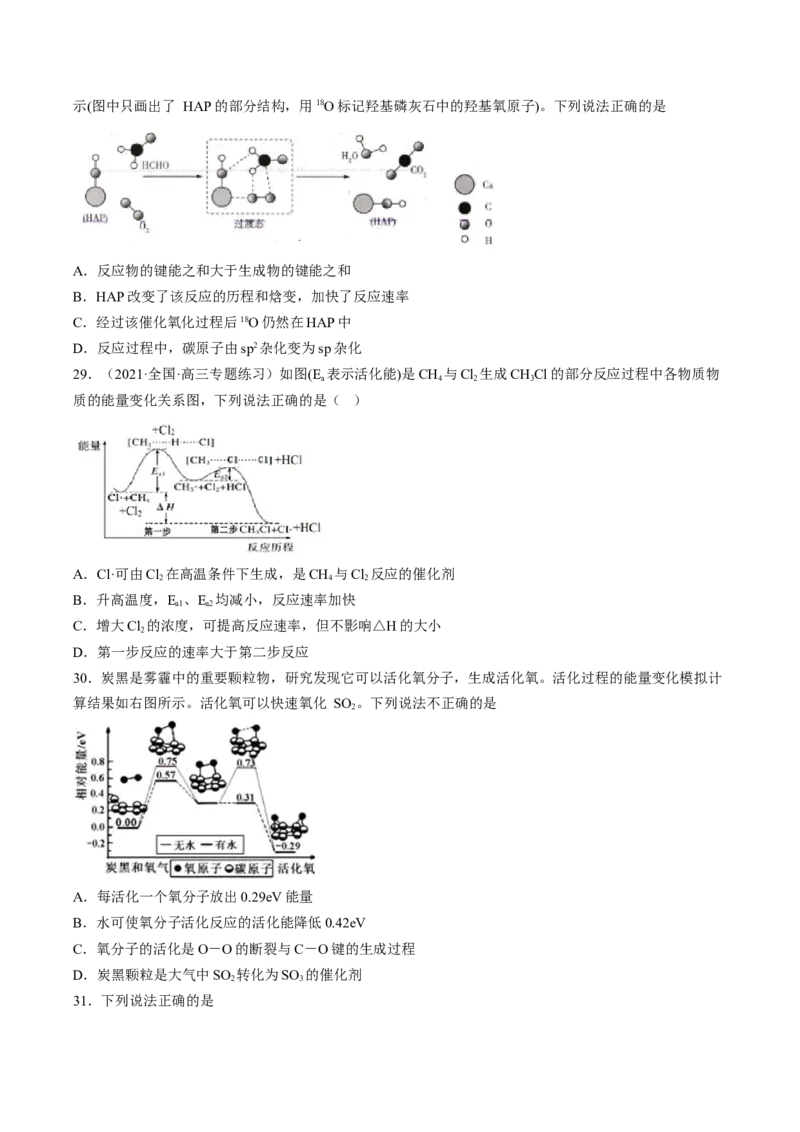
28.某科研人员提出HCHO与O 在羟基磷灰石(HAP)表面催化氧化生成CO、HO的历程,该历程如图所
2 2 2示(图中只画出了 HAP的部分结构,用18O标记羟基磷灰石中的羟基氧原子)。下列说法正确的是
A.反应物的键能之和大于生成物的键能之和
B.HAP改变了该反应的历程和焓变,加快了反应速率
C.经过该催化氧化过程后18O仍然在HAP中
D.反应过程中,碳原子由sp2杂化变为sp杂化
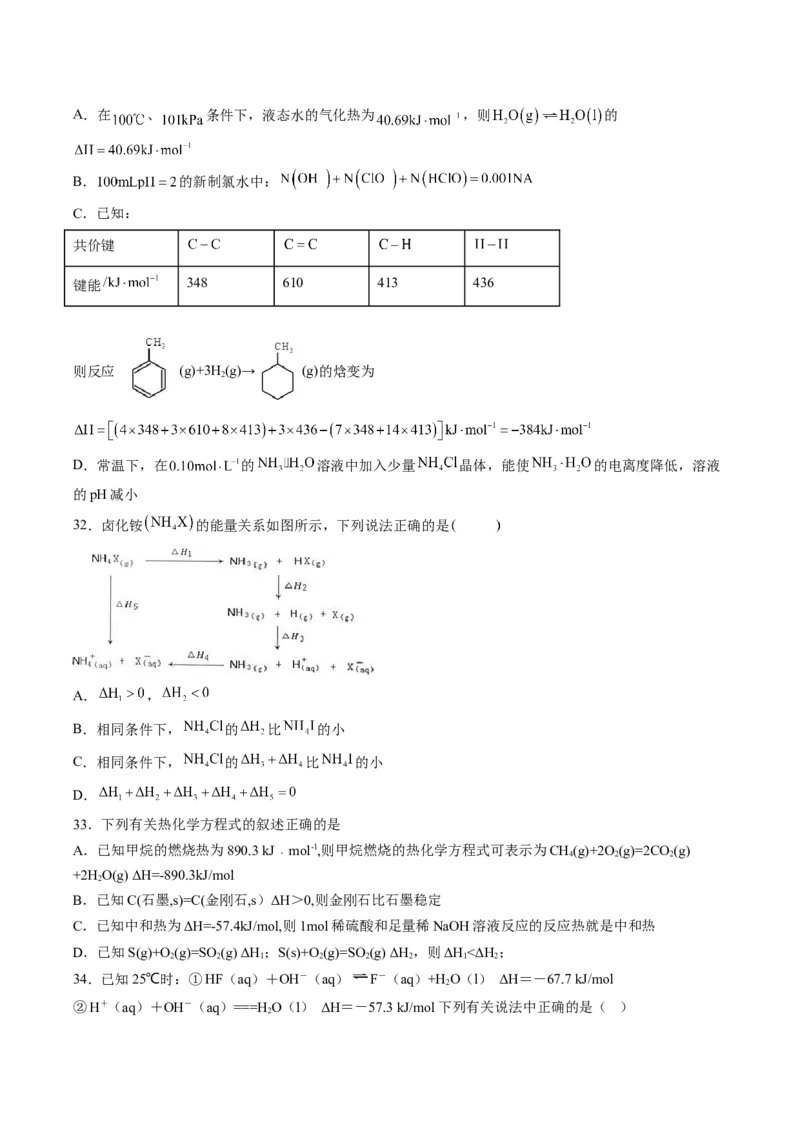
29.(2021·全国·高三专题练习)如图(E 表示活化能)是CH 与Cl 生成CHCl的部分反应过程中各物质物
a 4 2 3
质的能量变化关系图,下列说法正确的是( )
A.Cl·可由Cl 在高温条件下生成,是CH 与Cl 反应的催化剂
2 4 2
B.升高温度,E 、E 均减小,反应速率加快
a1 a2
C.增大Cl 的浓度,可提高反应速率,但不影响△H的大小
2
D.第一步反应的速率大于第二步反应
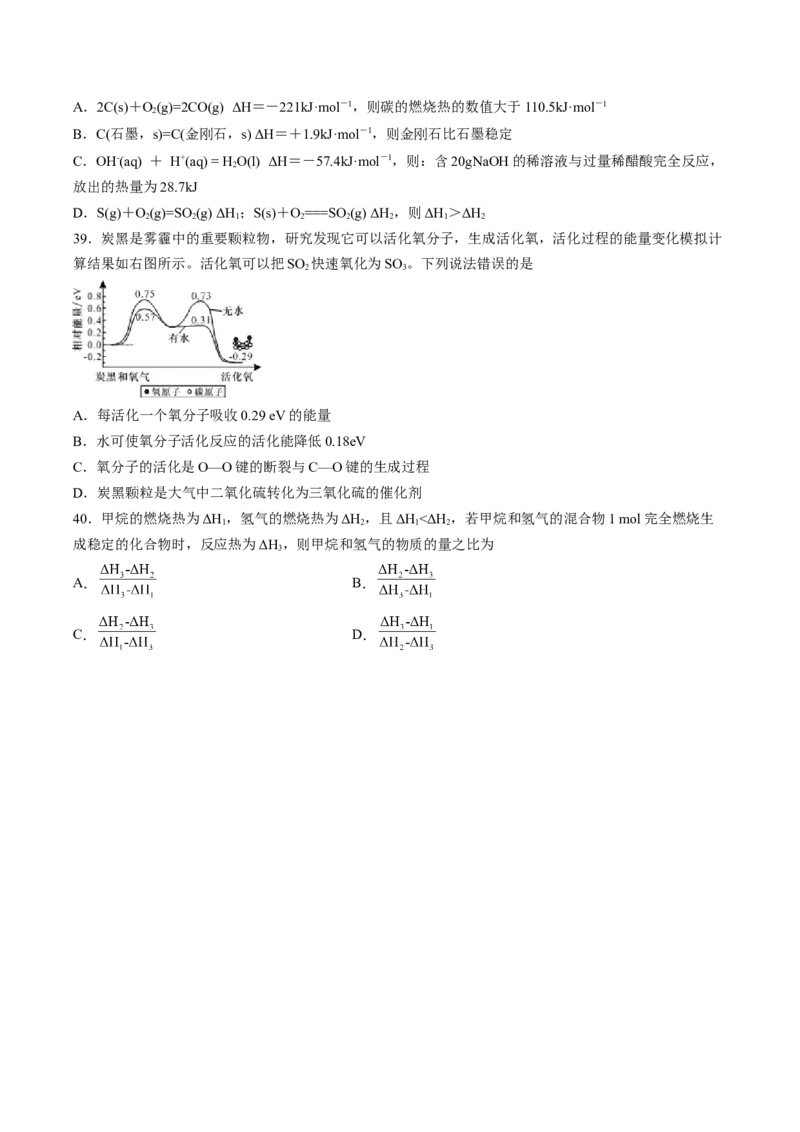
30.炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。活化过程的能量变化模拟计
算结果如右图所示。活化氧可以快速氧化 SO 。下列说法不正确的是
2
A.每活化一个氧分子放出0.29eV能量
B.水可使氧分子活化反应的活化能降低0.42eV
C.氧分子的活化是O-O的断裂与C-O键的生成过程
D.炭黑颗粒是大气中SO 转化为SO 的催化剂
2 3
31.下列说法正确的是A.在 、 条件下,液态水的气化热为 ,则 的
B. 的新制氯水中:
C.已知:
共价键
键能 348 610 413 436
则反应 (g)+3H(g)→ (g)的焓变为
2
D.常温下,在 的 溶液中加入少量 晶体,能使 的电离度降低,溶液
的pH减小
32.卤化铵 的能量关系如图所示,下列说法正确的是
A. ,
B.相同条件下, 的 比 的小
C.相同条件下, 的 比 的小
D.
33.下列有关热化学方程式的叙述正确的是
A.已知甲烷的燃烧热为890.3 kJ﹒mol-1,则甲烷燃烧的热化学方程式可表示为CH(g)+2O(g)=2CO (g)
4 2 2
+2H O(g) ΔH=-890.3kJ/mol
2
B.已知C(石墨,s)=C(金刚石,s)ΔH>0,则金刚石比石墨稳定
C.已知中和热为ΔH=-57.4kJ/mol,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热
D.已知S(g)+O(g)=SO(g) ΔH ;S(s)+O (g)=SO(g) ΔH ,则ΔH<ΔH ;
2 2 1 2 2 2 1 2
34.已知25℃时:①HF(aq)+OH-(aq) F-(aq)+H O(l) ΔH=-67.7 kJ/mol
2
②H+(aq)+OH-(aq)===HO(l) ΔH=-57.3 kJ/mol下列有关说法中正确的是( )
2A.HF电离:HF(aq) H+(aq)+F-(aq) H=+10.4KJ/mol
B.水解消耗0.1 mol F-时,吸收的热量为6.77 k△J
C.中和热均为57.3 kJ/mol
D.含1 mol HF、1 mol NaOH的两种溶液混合后放出的热量为67.7 kJ
35.甲烷与氯气在光照条件下取代反应的部分反应历程和能量变化如下:
第一步:Cl(g)→2Cl(g) H= +242.7kJ/mol
2 1
第二步:CH(g)+Cl(g)→CH (g)+HCl(g) H= +7.5 kJ/mol
4 △ 3 2
第三步:CH(g)+Cl (g)→CH Cl(g)+Cl(g) H= -112.9 kJ/mol(其中CH 表示甲基,Cl表示氯原子)
3 2 3 △ 3 3
下列说法不正确的是( )
△
A.甲烷与氯气在光照下发生反应的过程中会生成少量的乙烷
B.CH(g)+Cl (g)→CH Cl(g)+HCl(g) H= -105.4 kJ/mol
4 2 3
C.形成1mol CHCl(g)中C-Cl键放出的能量比拆开1mol Cl (g)中Cl-Cl键吸收的能量多
3 △ 2
D.若是CH 与Br 发生取代反应,则第二步反应的△H<+7.5kJ/mol
4 2
36.在25 ℃、1.01×105 Pa下,将22 g CO 通入750 mL 1mol/LNaOH溶液中充分反应,测得反应放出x kJ
2
热量。在该条件下,1 mol CO 通入1mol/L NaOH溶液2 L中充分反应放出y kJ热量。则CO 与NaOH溶
2 2
液反应生成NaHCO 的热化学方程式是
3
A.CO(g)+NaOH(aq)=NaHCO (aq) ΔH=-(2y-x) kJ·mol−1
2 3
B.CO(g)+NaOH(aq)=NaHCO (aq) ΔH=-(2x-y) kJ·mol−1
2 3
C.CO(g)+NaOH(aq)=NaHCO (aq) ΔH=-(4x-y) kJ·mol−1
2 3
D.2CO(g)+NaOH(l)=NaHCO (l) ΔH=-(8x-2y) kJ·mol−1
2 3
37.(2021·全国·高三专题练习)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应
系统原理。
下列说法不正确的是( )
A.通过计算,可知系统(Ⅰ)制备氢气的热化学方程式为:HO(l)= H (g)+1/2O (g) ΔH = 286 kJ· mol-1
2 2 2
B.通过计算,可知系统(Ⅱ)制备氢气的热化学方程式为:HS(g)=H(g)+S(s) ΔH =20kJ·mol-1
2 2
C.若反应H(g)+1/2O (g)=HO(g) ΔH = -a kJ · mol-1 , 则a>286
2 2 2
D.制得等量H 所需能量较少的是热化学硫碘循环硫化氢分解法
2
38.(2021·全国·高三专题练习)下列推论正确的是A.2C(s)+O(g)=2CO(g) ΔH=-221kJ·mol-1,则碳的燃烧热的数值大于110.5kJ·mol-1
2
B.C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1,则金刚石比石墨稳定
C.OH-(aq) + H+(aq) = H O(l) ΔH=-57.4kJ·mol-1,则:含20gNaOH的稀溶液与过量稀醋酸完全反应,
2
放出的热量为28.7kJ
D.S(g)+O(g)=SO(g) ΔH ;S(s)+O===SO(g) ΔH ,则ΔH>ΔH
2 2 1 2 2 2 1 2
39.炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计
算结果如右图所示。活化氧可以把SO 快速氧化为SO 。下列说法错误的是
2 3
A.每活化一个氧分子吸收0.29 eV的能量
B.水可使氧分子活化反应的活化能降低0.18eV
C.氧分子的活化是O—O键的断裂与C—O键的生成过程
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
40.甲烷的燃烧热为ΔH,氢气的燃烧热为ΔH,且ΔH<ΔH ,若甲烷和氢气的混合物1 mol完全燃烧生
1 2 1 2
成稳定的化合物时,反应热为ΔH,则甲烷和氢气的物质的量之比为
3
A. B.
C. D.