文档内容
专项训练 物质含量的测定
一、单选题
1.某小组设计实验测定胆矾( )纯度(杂质不参与反应):称取 胆矾样品
溶于蒸馏水,加入足量KI溶液,充分反应后,过滤。把滤液配制成250mL溶液,准
确量取配制溶液25.00mL于锥形瓶中,滴加2滴溶液X,用 溶液滴定
至终点,消耗滴定液Vml。涉及有关反应如下: ,
。下列叙述正确的是
A.X为甲基橙溶液
B.滴加 溶液时选择滴定管如图所示
C.滴定管装液之前最后一步操作是水洗
D.胆矾纯度为
2.下图是为测定过氧化钠样品(只含NaCO 杂质)纯度而设计的装置,气球Q弹性良
2 3
好。
下列说法正确的是
A.Q中反应的离子方程式为 +2H+=H O+CO↑,2 +4H+=2H O+O↑
2 2 2 2
B.测量气体体积时应先关闭K、K,打开K,反应完毕后再缓缓打开K
1 2 3 1
C.没有导管a稀硫酸不易滴下来,而且会导致测量气体的体积偏大
资料收集整理【淘宝店铺:向阳百分百】D.若操作正确,量筒I、Ⅱ分别收集xmL、ymL水,则NaO 的质量分数为
2 2
3.现有2.0g含NaO杂质的NaO 样品,用如图的实验装置测定NaO 试样的纯度,
2 2 2 2 2
(可供选用的反应物只有CaCO 固体、盐酸、硫酸和蒸馏水)。下列说法错误的是
3
A.装置A中液体试剂为盐酸
B.装置B的作用是除去挥发出的HCl气体
C.若去掉装置E会导致所测NaO 试样的纯度高
2 2
D.若反应结束后由气体体积计算得气体质量为0.32g,则NaO 试样的纯度为39%
2 2
4.经处理后的工业废水中含有少量的苯酚,实验室测定其含量的步骤如下:
Ⅰ.取VmLamol•L-1KBrO 溶液,加入稍过量的KBr溶液并用HSO 酸化;
1 3 2 4
Ⅱ.向Ⅰ所得溶液中加入VmL废水,充分反应后再加入稍过量的KI溶液;
2
Ⅲ.用bmol•L-1NaSO 标准溶液滴定Ⅱ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴
2 2 3
定至终点,共消耗VmLNa SO 溶液。
3 2 2 3
已知:①废水中不含干扰测定的物质;
② +3Br → ↓+3HBr;
2
③I +Na SO=2NaI+Na SO,NaSO 溶液和NaSO 溶液均为无色。
2 2 2 3 2 4 6 2 2 3 2 4 6
下列说法正确的是
A.步骤Ⅰ中被氧化与被还原的溴元素质量之比为5:1 B.步骤Ⅱ中Br 与苯酚发
2
生加成反应
C.步骤Ⅲ中滴定至终点时溶液变为蓝色 D.废水中苯酚的含量为
g•L-1
5.三氧化二铟 具有优良的气体传感性。以 为原料制备三氧化二铟的工艺
资料收集整理【淘宝店铺:向阳百分百】如下:
已知:①In的+3价强酸盐易水解;
②加热2使纯净物M的失重率(失重率 )为 。
下列说法错误的是
A.不能用稀盐酸替代热水 B. 的性质与 有相似之
处
C.加热1和加热2的温度可能不相同 D.纯净物M中铟的质量分数为
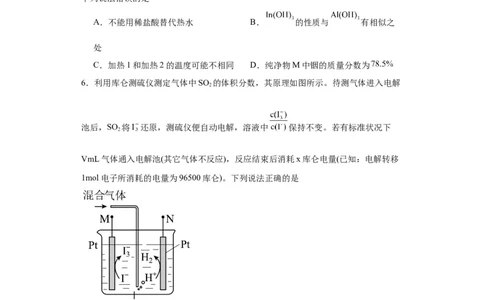
6.利用库仑测硫仪测定气体中SO 的体积分数,其原理如图所示。待测气体进入电解
2
池后,SO 将I 还原,测硫仪便自动电解,溶液中 保持不变。若有标准状况下
2
VmL气体通入电解池(其它气体不反应),反应结束后消耗x库仑电量(已知:电解转移
1mol电子所消耗的电量为96500库仑)。下列说法正确的是
A.M接电源的负极 B.阳极反应式为2H++2e-=H ↑
2
C.反应结束后溶液的pH增大 D.混合气体中SO 的体积分数为
2
×100%
7.铁是人体必需的微量元素之一,某小组设计实验测定菠菜中铁的含量(mg/100g,即
每100g菠菜中铁元素的质量),实验过程如图:
I.配制溶液
资料收集整理【淘宝店铺:向阳百分百】II.测定含量
下
列说法正确的是
A.灼烧时用到的主要仪器有:蒸发皿、三脚架、泥三角、酒精灯
B.该菠菜中铁的含量为2800cVmg/100g
C.取少量待测液滴加KSCN溶液,溶液变为红色则含有Fe2+
D.配制100mL待测液时,若仰视容量瓶上的刻度线,浓度偏高
8. 是一种常用的补血剂,在空气中易变质。某同学通过如下实验测定该
补血剂中 的含量:先称取 样品,用煮沸冷却的蒸馏水配制成
溶液;再量取 溶液于锥形瓶中,逐滴滴入 的
溶液,反应完全后,共消耗 溶液(不考虑空气对反应的影响)。
下列说法错误的是
A.该反应的离子方程式为
B.该样品中 的含量为21.875%
C.配制溶液时需用到的玻璃仪器仅有烧杯、漏斗、量筒、玻璃棒和 容量瓶
D.用煮沸冷却的蒸馏水配制溶液的目的是除去溶解在水中的氧气
9.某探究小组利用下列装置测定空气中 的含量,空气流速为 ,假定空气
中的 可被溶液充分吸收,实验结束时,测定耗时b min。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.多孔玻璃球泡起到增大气体与溶液的接触面积的作用
B.为了提高实验的准确性,空气的流速越快越好
C.当观察到装置内溶液恰好变蓝色时,停止通入空气
D.该空气样品中 的含量是
10.钢铁制品经常要进行烤蓝处理,即在铁制品的表面生成一层致密的 。某化
学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
Ⅰ.把一定量烤蓝铁片加工成均匀粉末;
Ⅱ.取一定量的粉末,放入 的盐酸中,二者恰好完全反应,生成
(标况) ,再向溶液中滴入KSCN溶液,无现象。
已知:①不考虑空气对反应的影响;②杂质不参与反应。
下列说法错误的是
A.由实验可知,反应后所得的溶液中一定无
B.样品中氧元素的物质的量为
C.样品中铁元素的含量约为70%
D.若将生成的 恰好全部与灼热的氧化铜反应,最多可得到 铜单质
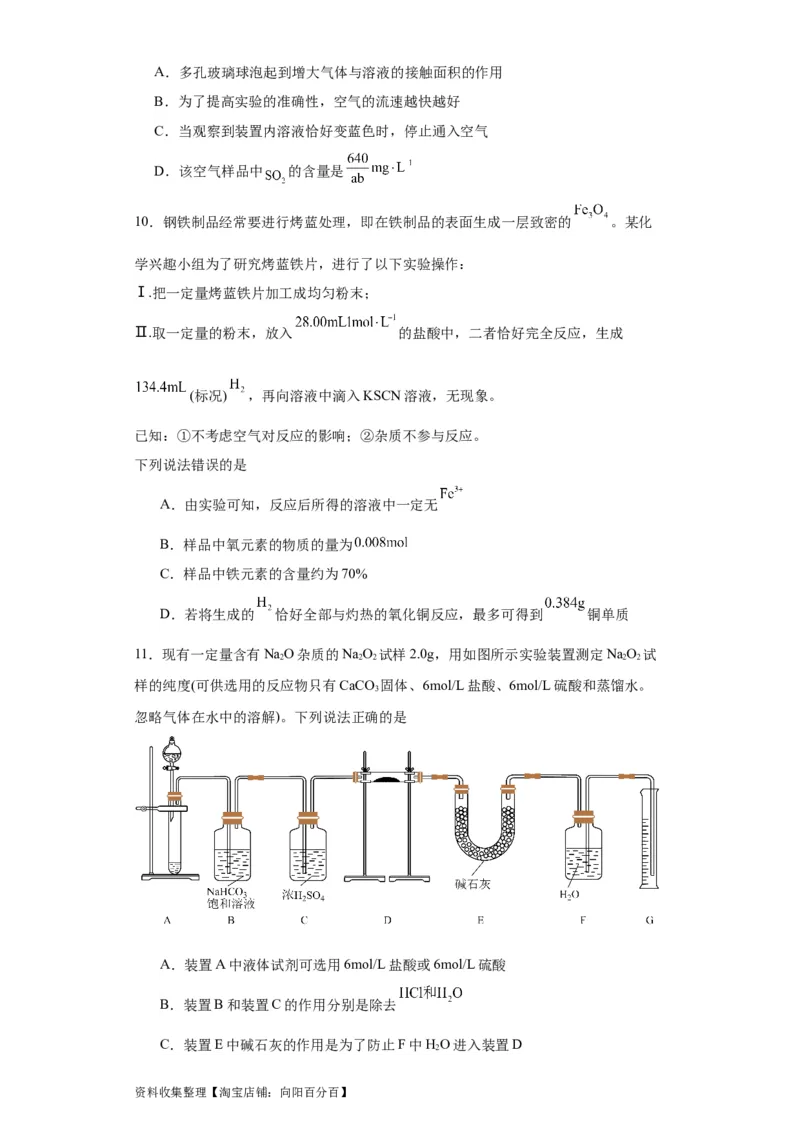
11.现有一定量含有NaO杂质的NaO 试样2.0g,用如图所示实验装置测定NaO 试
2 2 2 2 2
样的纯度(可供选用的反应物只有CaCO 固体、6mol/L盐酸、6mol/L硫酸和蒸馏水。
3
忽略气体在水中的溶解)。下列说法正确的是
A.装置A中液体试剂可选用6mol/L盐酸或6mol/L硫酸
B.装置B和装置C的作用分别是除去
C.装置E中碱石灰的作用是为了防止F中HO进入装置D
2
资料收集整理【淘宝店铺:向阳百分百】D.实验结束后经过变换生成0.01mol O ,则NaO 样品的纯度为70%
2 2 2
12.某学生用NaHCO 和KHCO 组成的某混合物进行实验,测得如下数据(盐酸的物质
3 3
的量浓度相等),下列分析推理不正确的是
50mL盐酸 50mL盐酸 50mL盐酸
m(混合物) 9.2g 15.7g 27.6g
V(CO )(标况) 2.24L 3.36L 3.36L
2
A.盐酸的物质的量浓度为3.0mol·L-1
B.根据表中数据不能计算出混合物中NaHCO 的质量分数
3
C.加入混合物9.2g时盐酸过量
D.15.7g混合物未与盐酸完全反应
13.煤燃烧释放出的气体中主要含 、 、 、 、 ,可采用库仑测硫仪
快速检测出煤中硫的含量。其原理示意图如图所示。检测前,电解质溶液中 保持
定值时,电解池不工作。将待测气体通入电解池后, 溶解并将 还原,测硫仪便
立即工作使 又恢复到原定值,测定结束,通过测定电解消耗的电量可以求得煤中
含硫量。已知:电路中转移 时所消耗的电量为96500库仑。下列说法正确的是
A.测硫仪工作时阴极电极反应式为
资料收集整理【淘宝店铺:向阳百分百】B. 在电解池中发生反应的离子方程式为
C.煤样为 ,电解消耗的电量为x库仑,煤样中硫的质量分数为
D.电解过程中需控制电解质溶液 ,当 时,混合气体中的 能将 氧化
为 ,使测得煤中含硫量偏高
14.草酸合铁(Ⅲ)酸钾晶体 易溶于水,难溶于乙醇,110℃可
完全失去结晶水,是制备某些铁触媒的主要原料。实验室通过下列步骤测定其组成:
步骤1:准确称取两份质量均为0.4910g的草酸合铁酸钾样品。
步骤2:一份在 氛围下保持110℃加热至恒重,称得残留固体质量为0.4370g。
步骤3:另一份完全溶于水后,让其通过装有某阴离子交换树脂的交换柱
,用蒸馏水冲洗交换柱,收集
交换出的 ,以 为指示剂,用 的 溶液滴定至终点,消耗
溶液20.00mL。通过计算确定草酸合铁酸钾晶体的化学式为
A. B.
C. D.
15.世界卫生组织(WHO)和中国卫健委公认二氧化氯(ClO )为新时代绿色消毒剂。常温
2
下,ClO 气体与Cl 具有相似的颜色与气味,易溶于水,在水中的溶解度是Cl 的5~8
2 2 2
倍。ClO 对热、震动、撞击和摩擦相当敏感,极易分解发生爆炸。ClO 几乎不与冷水
2 2
反应,遇热水则会分解。经研究表明,ClO 反应释放出的原子氧可以氧化色素,所以
2
ClO 也是优良的漂白剂。工业上可采用SO 与氯酸钠在酸性条件下反应制取ClO ,并
2 2 2
生成NaHSO。相信在不久的将来,ClO 将广泛应用到杀菌消毒领域。某兴趣小组取
4 2
NaClO 样品质量6.0g,通过反应吸收得250mLClO 溶液,取出25.00mL,加入
3 2
42.00mL0.500mol•L﹣1Fe2+充分反应,过量Fe2+再用0.0500mol•L﹣1KCr O 标准溶液发生
2 2 7
反应,恰好反应时消耗KCr O 溶液20.00mL。反应原理如下:
2 2 7
4H++ClO +5Fe2+═Cl﹣+5Fe3++2H O
2 2
资料收集整理【淘宝店铺:向阳百分百】14H++ +6Fe2+═2Cr3++6Fe3++7H O
2
若以“ ”作为衡量ClO 产率,则ClO 的“产率”为
2 2
A.33.75% B.47.25% C.50.75% D.67.50%
16.现有2.5g含 杂质的 样品,用如图的实验装置测定 试样的纯度
(可供选用的反应物只有 固体、盐酸、硫酸和蒸馏水)、下列说法错误的是
A.装置A中液体试剂为盐酸
B.装置B的作用是除去HCl
C.若去掉装置E会导致所测 试样的纯度偏低
D.若反应结束后由气体体积计算得气体质量为0.32g,则 试样的纯度为
62.4%
二、多选题
17.“铬鞣制法”可以使皮革变的柔软和耐用,为检测皮革中 的含量,可以采取
碘量法测定,过程如下:
①高温熔融:
②酸化:
③加碘化钾滴定: 、
若皮革样品质量为 ,滴定过程共消耗 的 。下列说法正确的
是
资料收集整理【淘宝店铺:向阳百分百】A.反应①中氧化剂与还原剂的物质的量比为5∶1
B. 元素参与了3个氧化还原过程
C.实验过程中,所得 与 的物质的量比可能大于5∶2
D.皮革中 的含量为
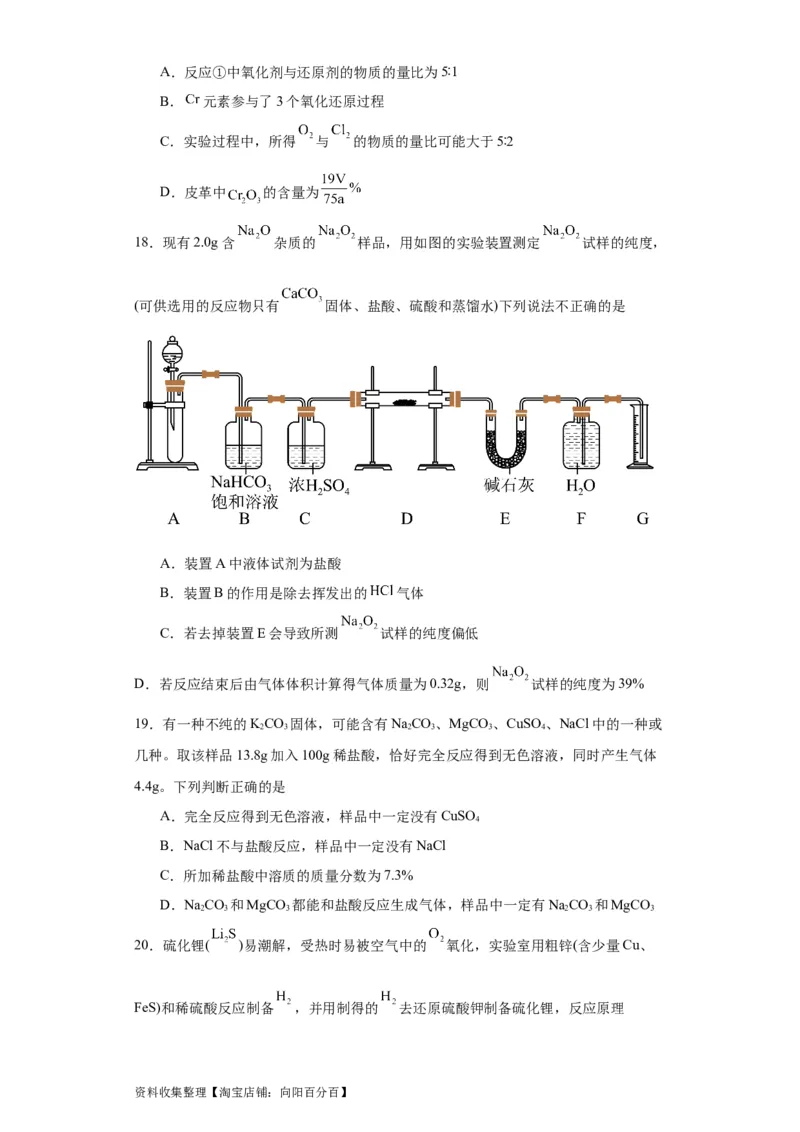
18.现有2.0g含 杂质的 样品,用如图的实验装置测定 试样的纯度,
(可供选用的反应物只有 固体、盐酸、硫酸和蒸馏水)下列说法不正确的是
A.装置A中液体试剂为盐酸
B.装置B的作用是除去挥发出的 气体
C.若去掉装置E会导致所测 试样的纯度偏低
D.若反应结束后由气体体积计算得气体质量为0.32g,则 试样的纯度为39%
19.有一种不纯的KCO 固体,可能含有NaCO、MgCO 、CuSO 、NaCl中的一种或
2 3 2 3 3 4
几种。取该样品13.8g加入100g稀盐酸,恰好完全反应得到无色溶液,同时产生气体
4.4g。下列判断正确的是
A.完全反应得到无色溶液,样品中一定没有CuSO
4
B.NaCl不与盐酸反应,样品中一定没有NaCl
C.所加稀盐酸中溶质的质量分数为7.3%
D.NaCO 和MgCO 都能和盐酸反应生成气体,样品中一定有NaCO 和MgCO
2 3 3 2 3 3
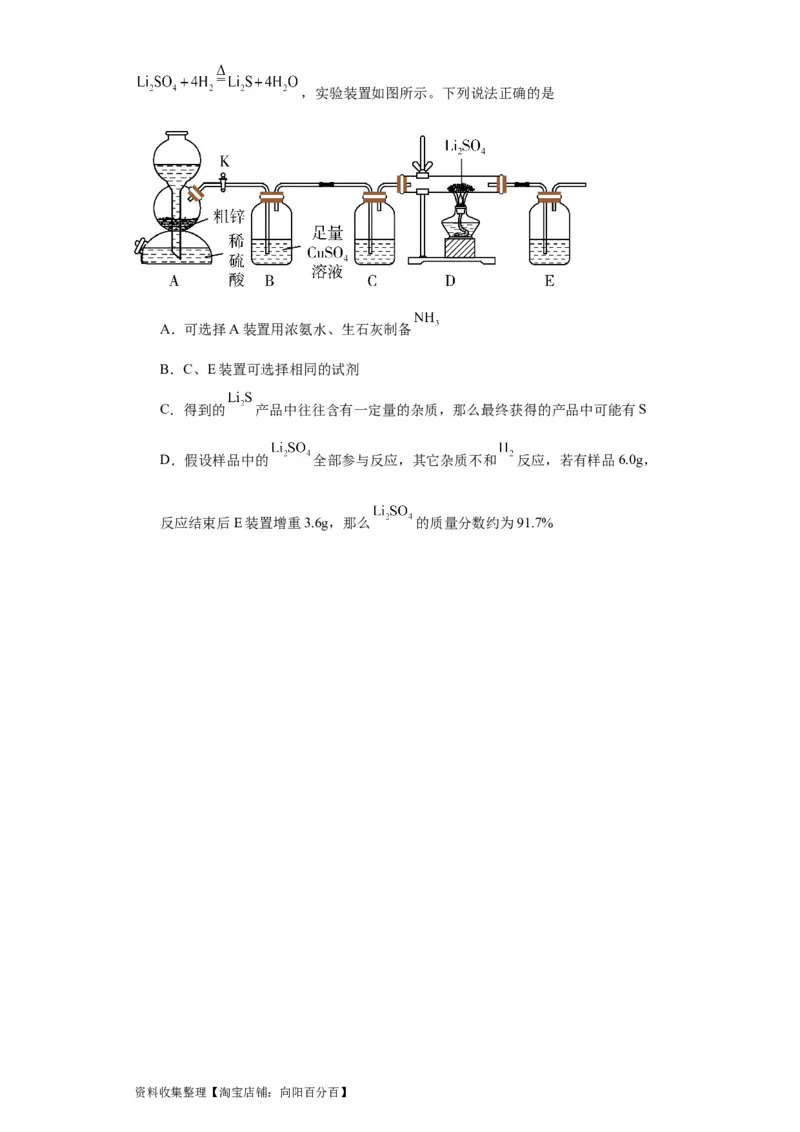
20.硫化锂( )易潮解,受热时易被空气中的 氧化,实验室用粗锌(含少量Cu、
FeS)和稀硫酸反应制备 ,并用制得的 去还原硫酸钾制备硫化锂,反应原理
资料收集整理【淘宝店铺:向阳百分百】,实验装置如图所示。下列说法正确的是
A.可选择A装置用浓氨水、生石灰制备
B.C、E装置可选择相同的试剂
C.得到的 产品中往往含有一定量的杂质,那么最终获得的产品中可能有S
D.假设样品中的 全部参与反应,其它杂质不和 反应,若有样品6.0g,
反应结束后E装置增重3.6g,那么 的质量分数约为91.7%
资料收集整理【淘宝店铺:向阳百分百】