文档内容
专项训练 金属的腐蚀与防护
一、单选题
1.下列有关金属腐蚀的说法不正确的是
A.镀层破损的白铁皮(镀锌)比马口铁(镀锡)更易被腐蚀
B.海水中钢铁水闸与外加直流电源的负极相连可减缓其腐蚀
C.用氯化铁溶液腐蚀铜板制作印刷电路板
D.铝片经过浓硫酸处理后表面生成致密的氧化膜可保护铝
2.下列有关说法正确的是
A.在潮湿的空气中,白铁皮(镀锌)镀层受损后,比受损前更容易生锈
B.对于反应 ,增大反应容器体积,达到平衡时,
减小
C.反应 达到平衡后,升高温度,反应速率
和 的平衡转化率均增大
D.恒温恒容下,反应 ,当气体密度不变时,可判断
反应达到了平衡
3.下列现象与电化学腐蚀无关的是
A.铜锌合金(黄铜)不易被腐蚀
B.银质物品久置表面变黑
C.附有银制配件的铁制品其接触处易生锈
D.铁锅炒菜后未洗净擦干容易生锈
4.带有铁铆钉的铜板若暴露在空气中,铁很快就会被腐蚀成铁锈,如图是铜板电化学
腐蚀示意图。下列说法错误的是
A.铜板表面被潮湿空气或雨水浸润,空气中的 、 溶解其中,形成电解质
资料收集整理【淘宝店铺:向阳百分百】溶液,组成原电池,加速了铁的腐蚀
B.铜作正极
C.理论上,每转移1 mol电子,有2 mol Fe被氧化
D.该腐蚀反应是自发的
5.下列实验方案能达到实验目的的是
选
A B C D
项
实
验
方
案
实
验 验证CuSO 4 对 用铁氰化钾溶液验
HO 分解反应有 进行喷泉实验 验证非金属性:Cl>C>Si 证牺牲阳极的阴极
2 2
目
催化作用 保护法
的
A.A B.B C.C D.D
【答案】B
【详解】A.加 溶液的试管同时也加热了,其反应速率加快,不能证明是
的催化作用,A项错误;
B.虽然烧杯里是蒸馏水,但引发喷泉的操作是挤入胶头滴管中的NaOH溶液, 溶
于NaOH使烧瓶内压强减小,引起喷泉,B项正确;
C.验证非金属性的强弱,应比较元素最高价氧化物的水化物的酸性,盐酸应改为高氯
酸,C项错误;
D.图示装置是外接电流的阴极保护法而不是牺牲阳极的阴极保护法,D项错误;
答案选B。
6.下列实验能达到目的的是
实验目的 实验方法或操作
酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温
A 测定中和反应的反应热
度
探究浓度对化学反应速率 量取同体积不同浓度的NaClO溶液,分别加入等体积等浓度
B
的影响 的 溶液,对比现象
资料收集整理【淘宝店铺:向阳百分百】将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中。一段
检验牺牲阳极法对钢铁防
C
腐的效果 时间后,取溶液加入 溶液无蓝色沉淀生成
除去碱式滴定管胶管内的
D 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出
气泡
A.A B.B C.C D.D
7.下列有关金属的电化学腐蚀与防护正确的是
A.纯铁比生铁易生锈
B.镀锌铁皮的镀层破损后,铁皮会加速腐蚀
C.钢铁设施在河水中的腐蚀速率比海水中的快
D.钢铁护栏涂刷多彩防锈漆,原理是钢铁与潮湿的空气隔绝可防止腐蚀
8.下列叙述错误的是
A.工业电解饱和食盐水时,阴极区获得烧碱溶液和氢气
B.电解精炼铜时外电路通过2mol ,阳极质量减少64g
C.碱性或中性条件下钢铁发生吸氧腐蚀时,正极反应为
D.工业上用石墨电极电解熔融 冶炼铝时,阳极因被氧气氧化需定期更换
9.下列有关化学实验的方案设计、现象和结论,都正确的是
选
目的 方案设计 现象和结论
项
判断C元素和S 常温下,测定等物质的量浓度 若 溶液pH比 溶
A 元素的非金属性
的 和 溶液的pH
液的大,则非金属性:S>C
强弱
取 20%的麦芽糖溶液于
试管中,加入适量稀 后
探究麦芽糖是否 若生成砖红色沉淀,则麦芽糖
B 水浴加热 ,冷却后先加足
发生水解 已水解
量 溶液,再加入适量新
制 悬浊液并加热煮沸
用饱和食盐水和琼脂粉配制琼
脂溶液并倒入两个培养皿中, 裹有锌皮的铁钉周围出现红
证实金属防腐措
各滴加几滴酚酞和铁氰化钾溶 色,缠有铜丝的铁钉周围出现
C 施中牺牲阳极法
液,将裹有锌皮和缠有铜丝的 红色和蓝色,说明活泼性强的
的有效性
两个铁钉分别放入培养皿,观 锌保护了铁
察现象
取 1-溴丙烷和 饱和
检验1-溴丙烷消 氢氧化钾乙醇溶液,均匀加 若高锰酸钾溶液褪色,则有丙
D
去产物中的丙烯 热,将产生的气体通入 稀 烯生成
酸性高锰酸钾溶液中
A.A B.B C.C D.D
资料收集整理【淘宝店铺:向阳百分百】10.实验是化学的最高法庭。下列所示装置或操作能达到实验目的的是
A B C D
检验 有碳 乙醚萃取碘水得到 验证铁钉的吸氧腐
配制 溶液
碳双键 的乙醚溶液 蚀
A.A B.B C.C D.D
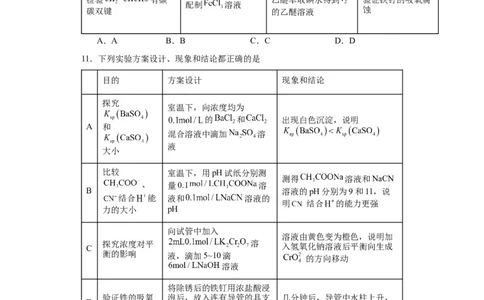
11.下列实验方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
探究
室温下,向浓度均为
的 和 出现白色沉淀,说明
A 和
混合溶液中滴加 溶
液
大小
比较 室温下,用pH试纸分别测
测得 溶液和NaCN
、 量0.1 溶
B 溶液的pH分别为9和11,说
结合 能 液和 溶液的
明 结合 的能力更强
力的大小 pH
向试管中加入
溶液由黄色变为橙色,说明加
C 探究浓度对平 溶 入氢氧化钠溶液后平衡向生成
衡的影响 液,滴加5~10滴
的方向移动
溶液
将除锈后的铁钉用浓盐酸浸
验证铁的吸氧 泡后,放入连有导管的具支 几分钟后,导管中水柱上升,
D
腐蚀 试管中,塞上橡胶塞,将导 说明铁发生了吸氧腐蚀
管末端浸入水中
A.A B.B C.C D.D
12.用下图所示的实验装置,按下列实验设计不能完成的实验是
资料收集整理【淘宝店铺:向阳百分百】选
实验目的 实验设计
项
A 减缓铁的腐蚀 X为石墨棒,溶液含 ,开关K置于A处
B 模拟铁的吸氧腐蚀 X为锌棒,溶液含 ,开关K置于B处
X为铜棒,溶液含 ,开关K
C 在铁棒上镀铜
置于A处
比较铁和铜的金属活动
D X为铜棒,溶液含 ,开关K置于B处
性强弱
A.A B.B C.C D.D
13.在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其
中一种理论为厌氧细菌可促使 与 反应生成 ,加速钢管的腐蚀,其反应原理
如图所示。下列说法正确的是
A.正极的电极反应式为
B. 与 的反应可表示为
C.钢管腐蚀的直接产物中只有
D.在钢管表面镀锌或铜可减缓钢管的腐蚀,即使镀层破损后仍对钢管有保护作用
14.某同学利用下图所示装置探究金属的腐蚀与防护条件。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.①区 电极上产生气泡, 电极附近滴加 溶液后出现蓝色,
被腐蚀
B.②区 电极上产生气泡, 电极附近滴加 溶液后出现蓝色,
被腐蚀
C.③区 电极的电极反应式为 , 电极附近滴加
溶液后未出现蓝色, 被保护
D.④区 电极的电极反应式为 , 电极附近滴加
溶液后出现蓝色, 被腐蚀
15.含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝
化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正
确的是
A.阳极保护法中受保护的金属外接电源的负极
B.电流密度越大,金属受保护程度越好
C.CFD区,金属受到保护
D.外接电势越高,对金属保护性越有效
16.厌氧性硫酸盐还原菌(SRB)是导致铁腐蚀的一种菌种,其腐蚀原理的图解如图
所示。下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.负极产生的Fe2+向正极移动
B. 在SRB细菌作用下发生的电极反应为 +8e-+4HO S2-+8OH-
2
C.总反应的化学方程式为4Fe+ +4HO FeS+3Fe(OH)+2OH-
2 2
D.若引入新的菌种,则一定会加速金属的腐蚀
二、多选题
17.一定条件下,碳钢腐蚀与溶液pH的关系如下表。下列说法错误的是
pH 2 4 6 6.5 8 13.5 14
腐蚀快慢 较快 慢 较快
主要产物 Fe2+ Fe O Fe O FeO
3 4 2 3
A.当pH<4时,碳钢主要发生析氢腐蚀
B.当614时,正极反应为O+4H++4e-=2H O
2 2
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
三、填空题
18.研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。某化学社团欲进行
以下研究,回答相关问题:
(1)利用下图研究氧气的浓度对铁腐蚀速率的影响。插入海水中的铁棒(含碳量为10.8%)
越靠近下端腐蚀就越 (填“轻微”、“严重”)。
资料收集整理【淘宝店铺:向阳百分百】(2)利用下图研究电解质的酸碱性对铁腐蚀速率的影响。起始时两管内液面相平,均在
恒温条件下研究。若溶液X是1mol/L的盐酸,一段时间后发现U形管内液面左低右高,
则铁丝的腐蚀过程属于 (填“吸氧腐蚀”或“析氢腐蚀”)。
(3)利用下图装置研究铁的防腐过程:
①能最大程度地减缓铁棒腐蚀的方案是闭合 (填“ ”、“ ”或“
”)。
②若闭合 ,石墨电极附近的pH将 (填“变大”、“变小”或“不变”)。
19.电化学的发展对人类文明的进步起到了推动作用。
研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(1)如图1中的铁棒为纯铁,则其腐蚀过程属于 腐蚀。
(2)如图1中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越 (选填
“轻微”、“严重”)。该实验说明 因素会影响铁的腐蚀速率。腐蚀时正极的
资料收集整理【淘宝店铺:向阳百分百】电极反应式为 。(已知:海水pH约为8.1)
(3)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化
情况。
(已知:起始时两管内液面相平,实验过程中铁丝始终不接触溶液,选填“左高右低”、
“左低右高”或“几乎不变”)
浓盐
溶液X 浓硫酸 稀硫酸
酸
液面情况
该组实验目的:研究 、 等因素对铁的腐蚀过程产生影响。
(4)用图3所示装置研究铁的防腐蚀过程:
①K、K、K 只关闭一个,则铁腐蚀的速度最快的是只闭合 (填“K”、“K”或
1 2 3 1 2
“K”下同)。
3
②为减缓铁的腐蚀,应只闭合 ,该防护法称为 。
③只闭合K,石墨电极附近的pH将 (填“变大”、“变小”或“不变”)。
3
(5)图4为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
资料收集整理【淘宝店铺:向阳百分百】①腐蚀过程中,负极是 (填“a”、“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
Cu (OH) Cl。青铜器发生电化腐蚀并最终生成Cu (OH) Cl的总离子方程式为 。
2 3 2 3
20.某化学兴趣小组对电化学问题进行了实验探究。
Ⅰ.利用如图所示装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表
面有气泡产生。
(1)写出负极的电极反应式: 。
(2)某学生认为,铁电极可能参与反应,并对产物作出假设:
假设1:铁参与反应,被氧化生成Fe2+;
假设2:铁参与反应,被氧化生成Fe3+;
假设3: 。
(3)为了探究假设1、2,他采取如下操作:
①取0.01 mol/L FeCl 溶液2 mL于试管中,加入过量铁粉;
3
②取操作①试管的上层清液加入2滴K[Fe(CN)]溶液,生成蓝色沉淀;
3 6
③取少量正极附近溶液加入2滴K[Fe(CN)]溶液,未见蓝色沉淀生成;
3 6
④取少量正极附近溶液加入2滴KSCN溶液,未见溶液变红。
据②、③、④现象得出的结论是 。
(4)该实验原理可应用于防护钢铁腐蚀,请再举一例防护钢铁腐蚀的措施
。
资料收集整理【淘宝店铺:向阳百分百】资料收集整理【淘宝店铺:向阳百分百】