文档内容
专题06 水溶液中的离子平衡
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.关于25℃时,体积相同的盐酸与醋酸两种溶液,下列说法正确的是
A.若浓度相同,中和所需的NaOH物质的量不一定相同
B.若浓度相同,溶液中c(OH-)前者小于后者
C.若pH相等,则[CHCOO-]>[Cl-]
3
D.若pH相等,分别与NaOH反应呈中性后,n(CHCOO-)①>②>④
B.浓度均为 的 溶液与 溶液,溶液中阴、阳离子的总浓度前者大于后者
C. 为一元酸,在 水溶液中存在:
D. 的 溶液中,
3.广安市某中学的化学课外兴趣小组,利用手持技术,进行了酸碱中和滴定实验: 25°C时,向
10.00mL 0.10mol/LCH COOH溶液中,逐滴加入0.10mol/L NaOH溶液,通过pH传感器,在电脑上得到了pH
3
变化曲线如图所示。下列说法正确的是
A.25°C时,CHCOOH的电离平衡常数Ka=1.0 ×10-6
3B.b点表示的溶液中c(Na+) < c(CHCOO-)
3
C.a点表示的溶液中2c(Na+)=c(CH COO-)+c(CH COOH)
3 3
D.a、b两点所示的溶液中水的电离程度较大的是a点
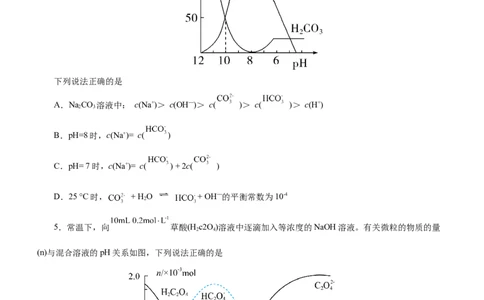
4.25°C时,向某NaCO 溶液中加入稀盐酸,溶液中含碳微粒的物质的量分数(φ)随溶液pH变化的部分
2 3
情况如图所示。
下列说法正确的是
A.NaCO 溶液中: c(Na+)> c(OH—)> c( )> c( )> c(H+)
2 3
B.pH=8时,c(Na+)= c( )
C.pH= 7时,c(Na+)= c( ) + 2c( )
D.25 °C时, + H O + OH—的平衡常数为10-4
2
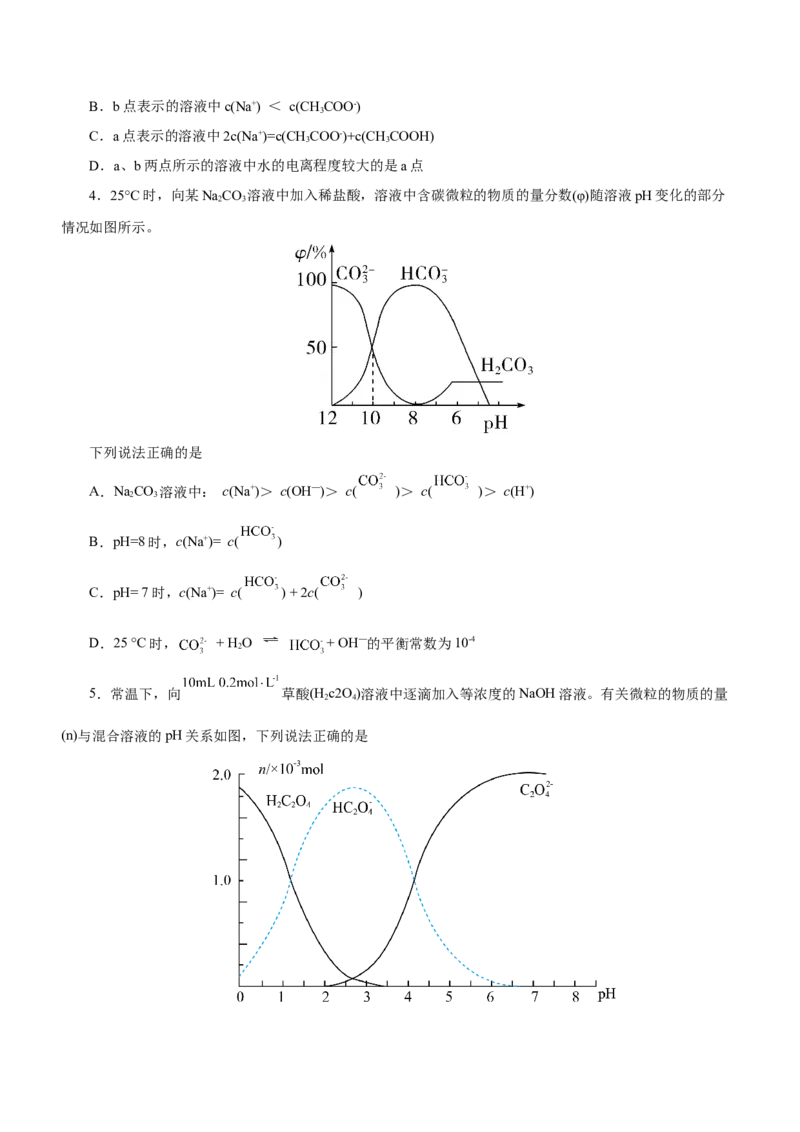
5.常温下,向 草酸(H c2O)溶液中逐滴加入等浓度的NaOH溶液。有关微粒的物质的量
2 4
(n)与混合溶液的pH关系如图,下列说法正确的是A.
B.当 时溶液中存在:
C.当 时溶液中存在:
D.当 时溶液中存在:
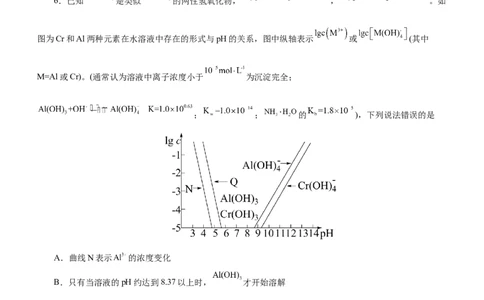
6.已知 是类似 的两性氢氧化物, , 。如
图为Cr和Al两种元素在水溶液中存在的形式与pH的关系,图中纵轴表示 或 (其中
M=Al或Cr)。(通常认为溶液中离子浓度小于 为沉淀完全;
; ; 的 ),下列说法错误的是
A.曲线N表示 的浓度变化
B.只有当溶液的pH约达到8.37以上时, 才开始溶解
C.在 和 共沉淀的体系中
D.向 的 溶液中滴加1moL/L的氨水,先产生白色胶状沉淀,继续滴加过量氨水会引
起部分沉淀的溶解
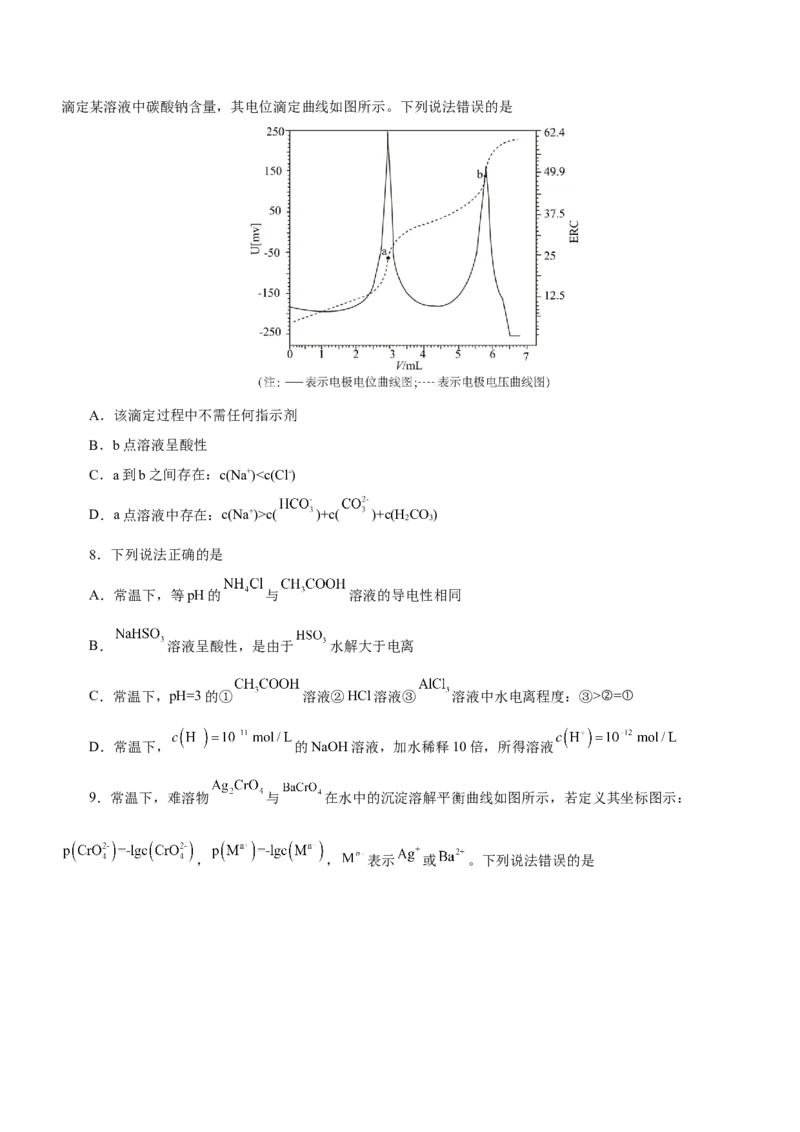
7.电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量
点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。现利用盐酸滴定某溶液中碳酸钠含量,其电位滴定曲线如图所示。下列说法错误的是
A.该滴定过程中不需任何指示剂
B.b点溶液呈酸性
C.a到b之间存在:c(Na+)c( )+c( )+c(H CO)
2 3
8.下列说法正确的是
A.常温下,等pH的 与 溶液的导电性相同
B. 溶液呈酸性,是由于 水解大于电离
C.常温下,pH=3的① 溶液②HCl溶液③ 溶液中水电离程度:③>②=①
D.常温下, 的NaOH溶液,加水稀释10倍,所得溶液
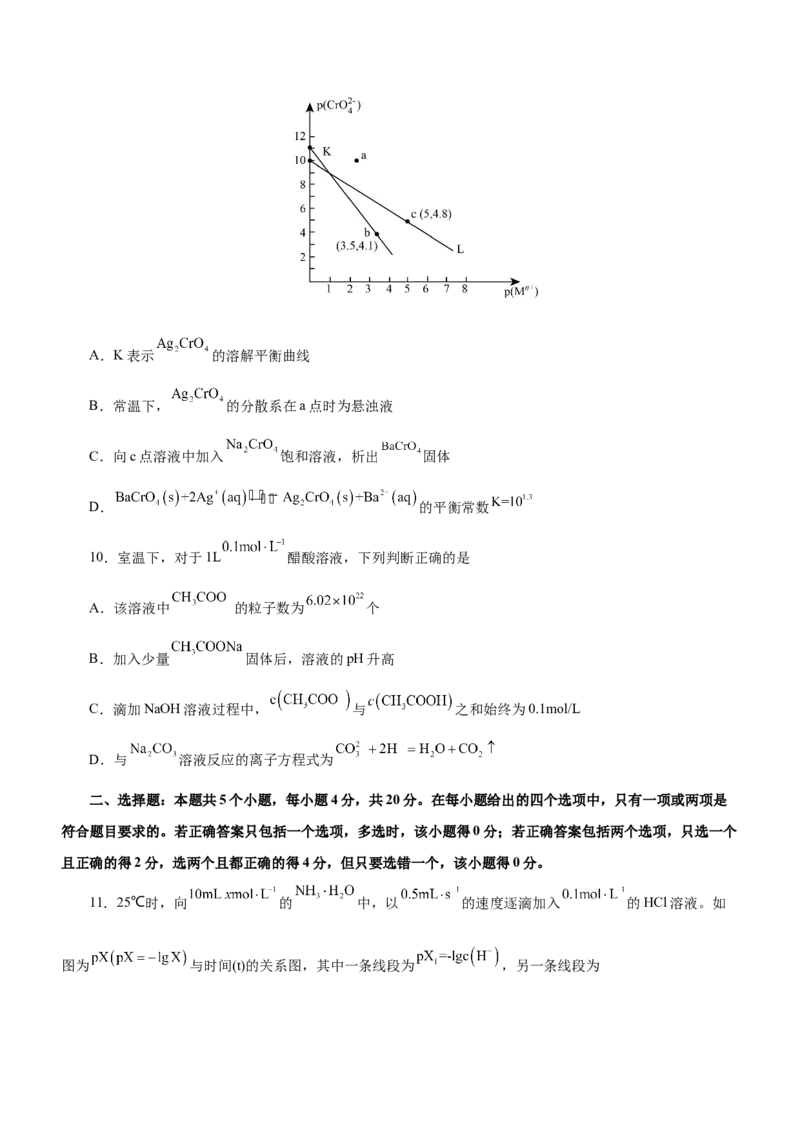
9.常温下,难溶物 与 在水中的沉淀溶解平衡曲线如图所示,若定义其坐标图示:
, , 表示 或 。下列说法错误的是A.K表示 的溶解平衡曲线
B.常温下, 的分散系在a点时为悬浊液
C.向c点溶液中加入 饱和溶液,析出 固体
D. 的平衡常数
10.室温下,对于1L 醋酸溶液,下列判断正确的是
A.该溶液中 的粒子数为 个
B.加入少量 固体后,溶液的pH升高
C.滴加NaOH溶液过程中, 与 之和始终为0.1mol/L
D.与 溶液反应的离子方程式为
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.25℃时,向 的 中,以 的速度逐滴加入 的HCl溶液。如
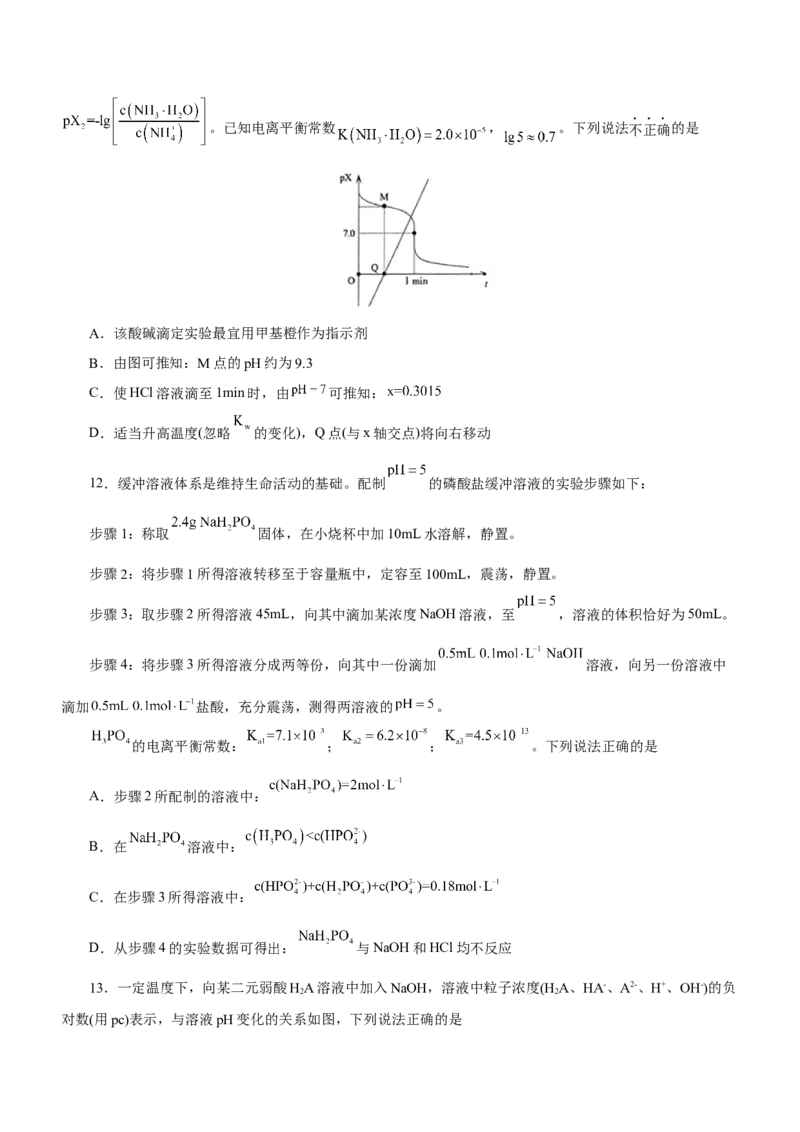
图为 与时间(t)的关系图,其中一条线段为 ,另一条线段为。已知电离平衡常数 , 。下列说法不正确的是
A.该酸碱滴定实验最宜用甲基橙作为指示剂
B.由图可推知:M点的pH约为9.3
C.使HCl溶液滴至1min时,由 可推知:
D.适当升高温度(忽略 的变化),Q点(与x轴交点)将向右移动
12.缓冲溶液体系是维持生命活动的基础。配制 的磷酸盐缓冲溶液的实验步骤如下:
步骤1:称取 固体,在小烧杯中加10mL水溶解,静置。
步骤2:将步骤1所得溶液转移至于容量瓶中,定容至100mL,震荡,静置。
步骤3:取步骤2所得溶液45mL,向其中滴加某浓度NaOH溶液,至 ,溶液的体积恰好为50mL。
步骤4:将步骤3所得溶液分成两等份,向其中一份滴加 溶液,向另一份溶液中
滴加 盐酸,充分震荡,测得两溶液的 。
的电离平衡常数: ; ; 。下列说法正确的是
A.步骤2所配制的溶液中:
B.在 溶液中:
C.在步骤3所得溶液中:
D.从步骤4的实验数据可得出: 与NaOH和HCl均不反应
13.一定温度下,向某二元弱酸HA溶液中加入NaOH,溶液中粒子浓度(H A、HA-、A2-、H+、OH-)的负
2 2
对数(用pc)表示,与溶液pH变化的关系如图,下列说法正确的是A.曲线c是代表HA-浓度的负对数 B.0.01mol/LH A的溶液,Ka 的数量级为10-4
2 2
C.Z点溶液中c(Na+)>2c(A2-)+2c(OH-) D.X点对应的pH= - (lgK +lgK )
a1 a2
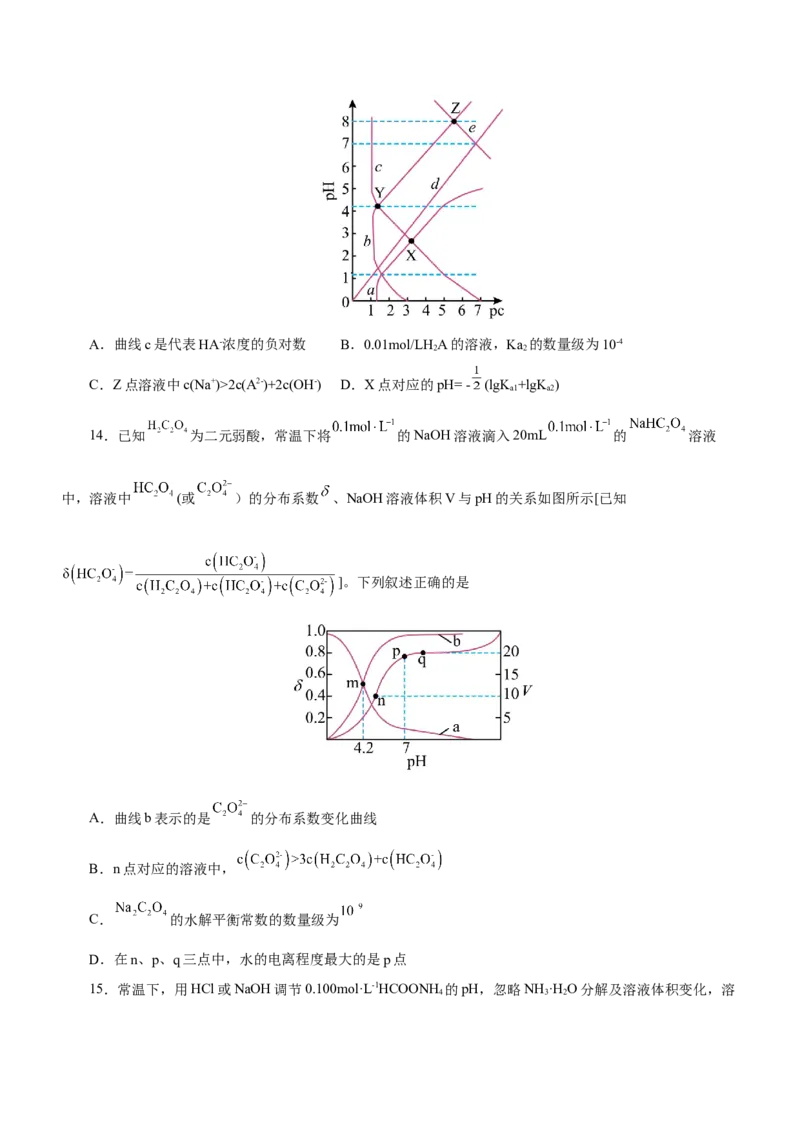
14.已知 为二元弱酸,常温下将 的NaOH溶液滴入20mL 的 溶液
中,溶液中 (或 )的分布系数 、NaOH溶液体积V与pH的关系如图所示[已知
]。下列叙述正确的是
A.曲线b表示的是 的分布系数变化曲线
B.n点对应的溶液中,
C. 的水解平衡常数的数量级为
D.在n、p、q三点中,水的电离程度最大的是p点
15.常温下,用HCl或NaOH调节0.100mol·L-1HCOONH 的pH,忽略NH ·H O分解及溶液体积变化,溶
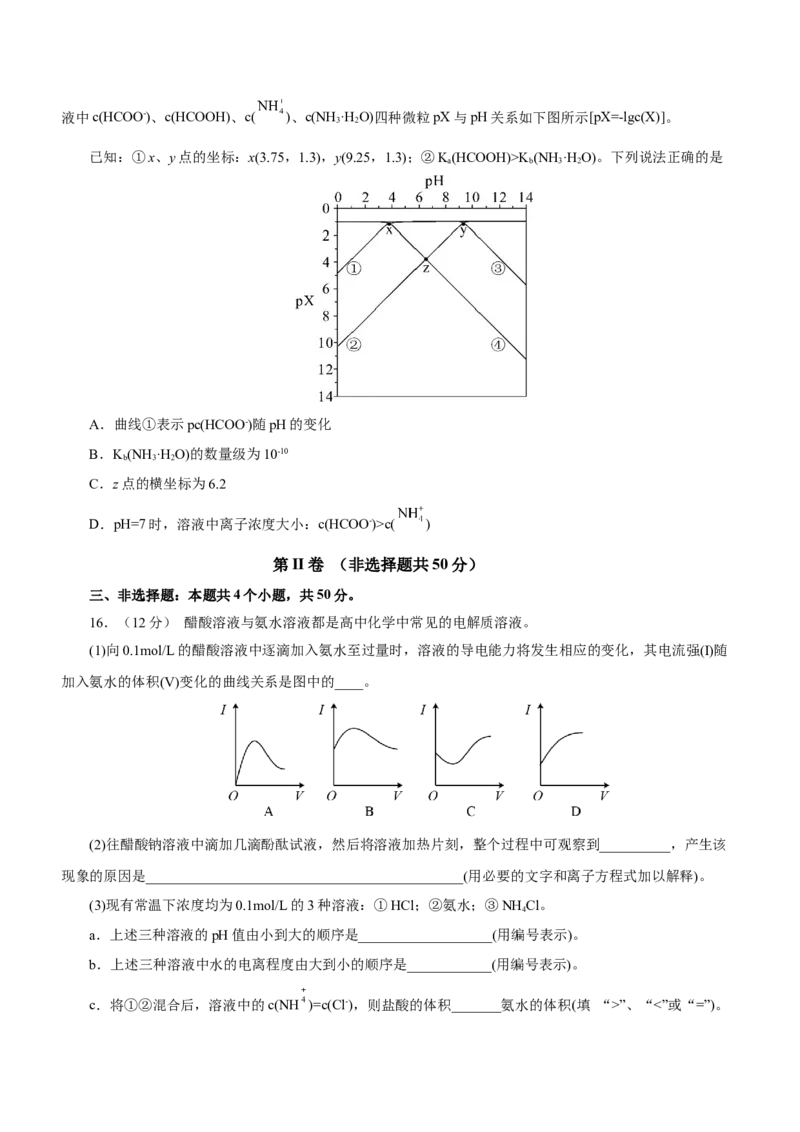
4 3 2液中c(HCOO-)、c(HCOOH)、c( )、c(NH ·H O)四种微粒pX与pH关系如下图所示[pX=-lgc(X)]。
3 2
已知:①x、y点的坐标:x(3.75,1.3),y(9.25,1.3);②K(HCOOH)>K (NH ·H O)。下列说法正确的是
a b 3 2
A.曲线①表示pc(HCOO-)随pH的变化
B.K(NH ·H O)的数量级为10-10
b 3 2
C.z点的横坐标为6.2
D.pH=7时,溶液中离子浓度大小:c(HCOO-)>c( )
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(12分) 醋酸溶液与氨水溶液都是高中化学中常见的电解质溶液。
(1)向0.1mol/L的醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强(I)随
加入氨水的体积(V)变化的曲线关系是图中的____。
(2)往醋酸钠溶液中滴加几滴酚酞试液,然后将溶液加热片刻,整个过程中可观察到__________,产生该
现象的原因是_____________________________________________(用必要的文字和离子方程式加以解释)。
(3)现有常温下浓度均为0.1mol/L的3种溶液:①HCl;②氨水;③NH Cl。
4
a.上述三种溶液的pH值由小到大的顺序是___________________(用编号表示)。
b.上述三种溶液中水的电离程度由大到小的顺序是____________(用编号表示)。
c.将①②混合后,溶液中的c(NH )=c(Cl-),则盐酸的体积_______氨水的体积(填 “>”、“<”或“=”)。(4)下列有关(NH )SO 溶液的说法正确的是____。
4 2 4
A.电离方程式:(NH )SO =2NH +SO
4 2 4
B.水解离子方程式:NH +H O=NH ·H O+H+
2 3 2
C.离子浓度关系:c(NH )+c(H+)=c(SO )+c(OH-)
D.微粒浓度大小:c(NH )>c(SO )>c(H+)>c(NH·H O)>c(OH-)
3 2
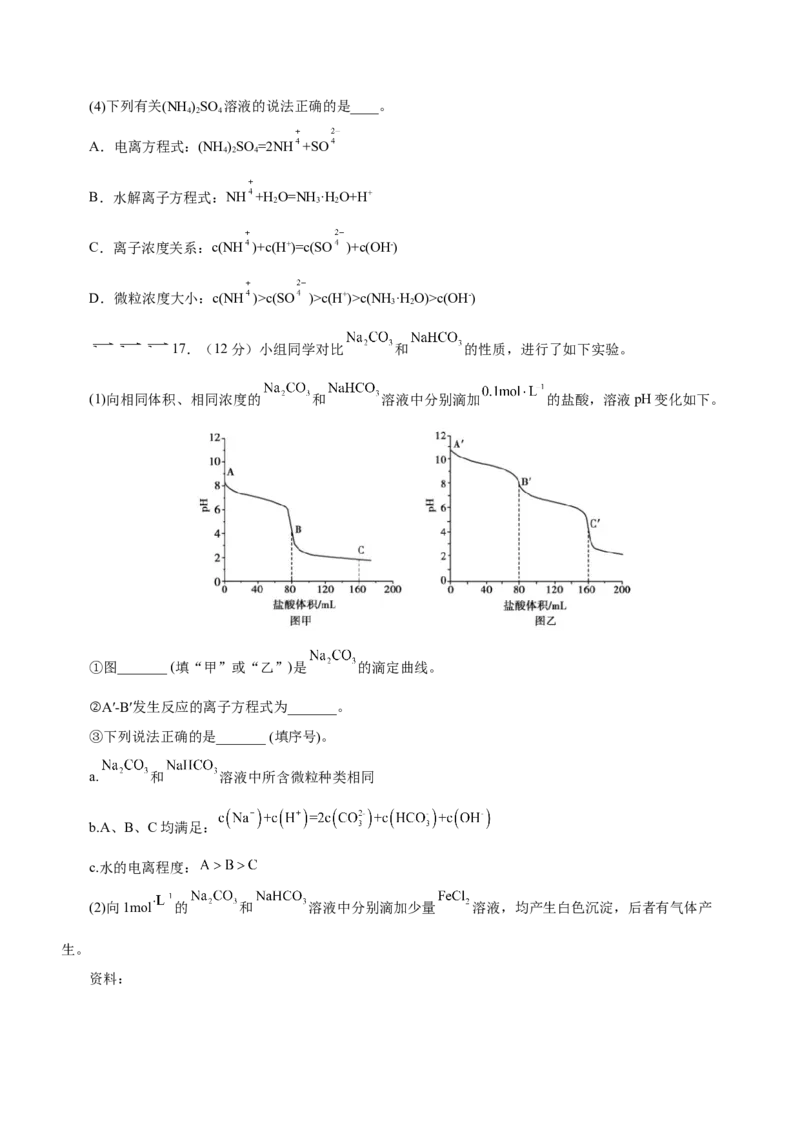
17.(12分)小组同学对比 和 的性质,进行了如下实验。
(1)向相同体积、相同浓度的 和 溶液中分别滴加 的盐酸,溶液pH变化如下。
①图_______ (填“甲”或“乙”)是 的滴定曲线。
②A′-B′发生反应的离子方程式为_______。
③下列说法正确的是_______ (填序号)。
a. 和 溶液中所含微粒种类相同
b.A、B、C均满足:
c.水的电离程度:
(2)向1mol 的 和 溶液中分别滴加少量 溶液,均产生白色沉淀,后者有气体产
生。
资料:i.1mol 的 溶液中, ,
ii.25℃时, ,
①补全 与 反应的离子方程式:
②通过计算说明 与 反应产生的沉淀为 而不是 _______。
18.(14分)某实验小组利用虚拟感应器技术探究1 mol⋅L 的碳酸钠溶液滴定10.00 mL 1 的盐酸
溶液过程中离子浓度变化。已知:25℃时, 的 , ; 。回答下列问
题:
(1)碳酸钠溶液的 ______ 。
(2)用浓盐酸配制滴定实验需要的1 的盐酸溶液80mL,需要的玻璃仪器除玻璃棒、烧杯、胶头滴管
外,还需要____________。配制完成后,需用_______量取10.00 mL 1 的盐酸溶液于锥形瓶中。
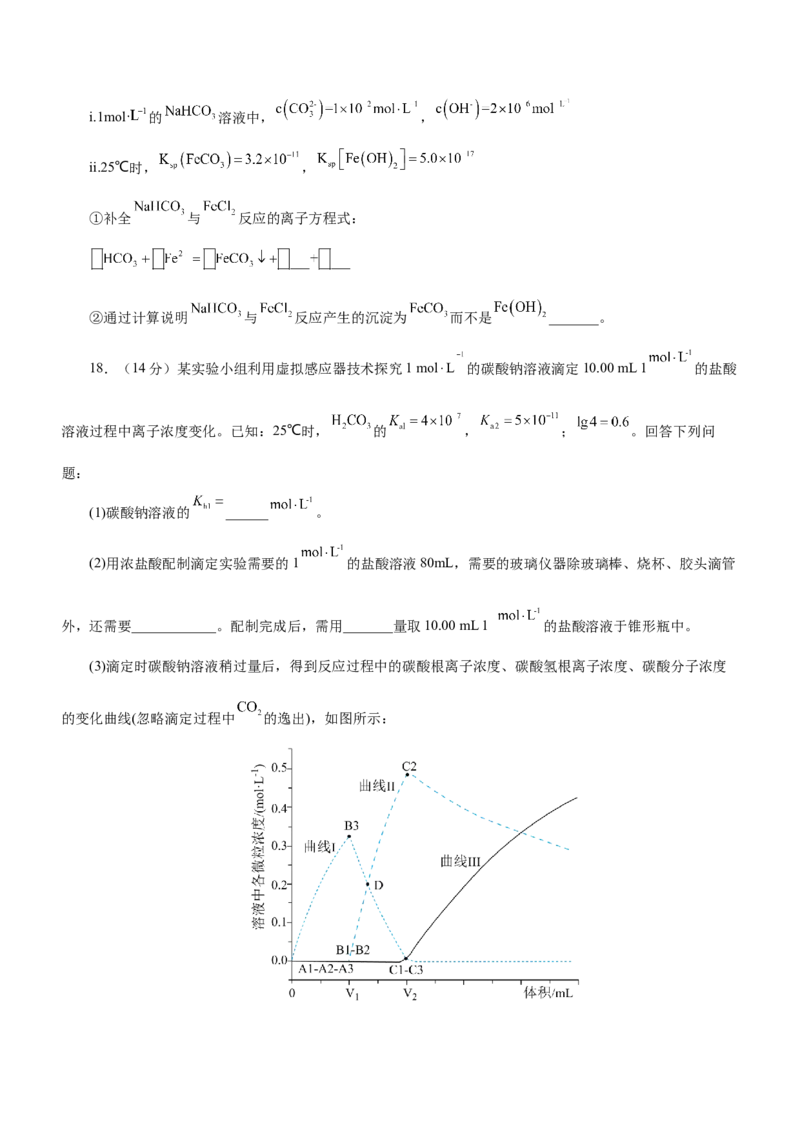
(3)滴定时碳酸钠溶液稍过量后,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度
的变化曲线(忽略滴定过程中 的逸出),如图所示:①由分析可知, ______mL,曲线Ⅱ是______浓度变化曲线。
②图中B3和c2溶液中水的电离程度较大的是______,D点 ______。
19.(12分)室温下,依次进行如下实验:
①取一定量冰醋酸,配制成100mL0.1mol/L醋酸溶液
②取20mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
③继续滴加a mL0.1mol/L稀盐酸,至溶液的pH=7;
④再取10mL①中所配溶液,加入20mL0.1mol/LNaOH溶液;
⑤向①中剩余醋酸溶液中逐滴加入0.1mol/L氨水至过量,用电导率传感器实时测量该过程中溶液的电导
率(溶液导电性越强,电导率越大)。
(1)用化学用语解释醋酸溶液pH<7的原因:_______,另外配制100mL与①中醋酸溶液等pH的盐酸,分
别取10mL上述两种溶液,各加入10mL蒸馏水,稀释后醋酸溶液的pH_______盐酸(>、=或<)。
(2)②中反应后的溶液中离子浓度由大到小的顺序为_______(用离子符号表示即可)。
(3)a___20mL(>、=或<,下同);③中反应后的溶液: ____ 。
(4)④中反应后的溶液中各微粒浓度存在如下关系: _____ ____
_____mol/L。
(5)请你预测⑤中滴入氨水过程中电导率的变化情况:_______。