文档内容
专题 07 化学反应中的能量变化及反应机理
1.(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
能量/
249 218 39 10 0 0 136 242
kJmol-1
HO(g)+HO(g)=H O (g) H O 214kJmol-1 H
可根据 2 2 计算出 2 2中氧氧单键的键能为 。下列说法不正确的是A. 2
的键能为436kJmol-1
O H O
B. 2的键能大于 2 2中氧氧单键的键能的两倍
HOOⅠ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A说法
正确;
B.进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相同,B
说法不正确;
C.进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这两步反应分别
是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;
D.由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为
P+Z,因此,Z没有表现出催化作用,D说法正确;
综上所述,本题选AD。
3.(2021·山东)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如
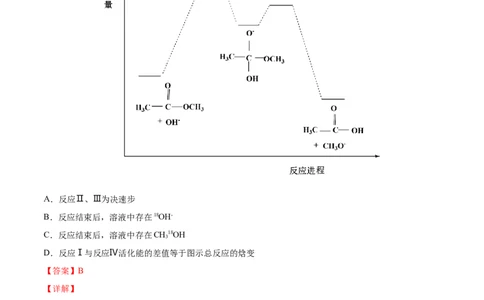
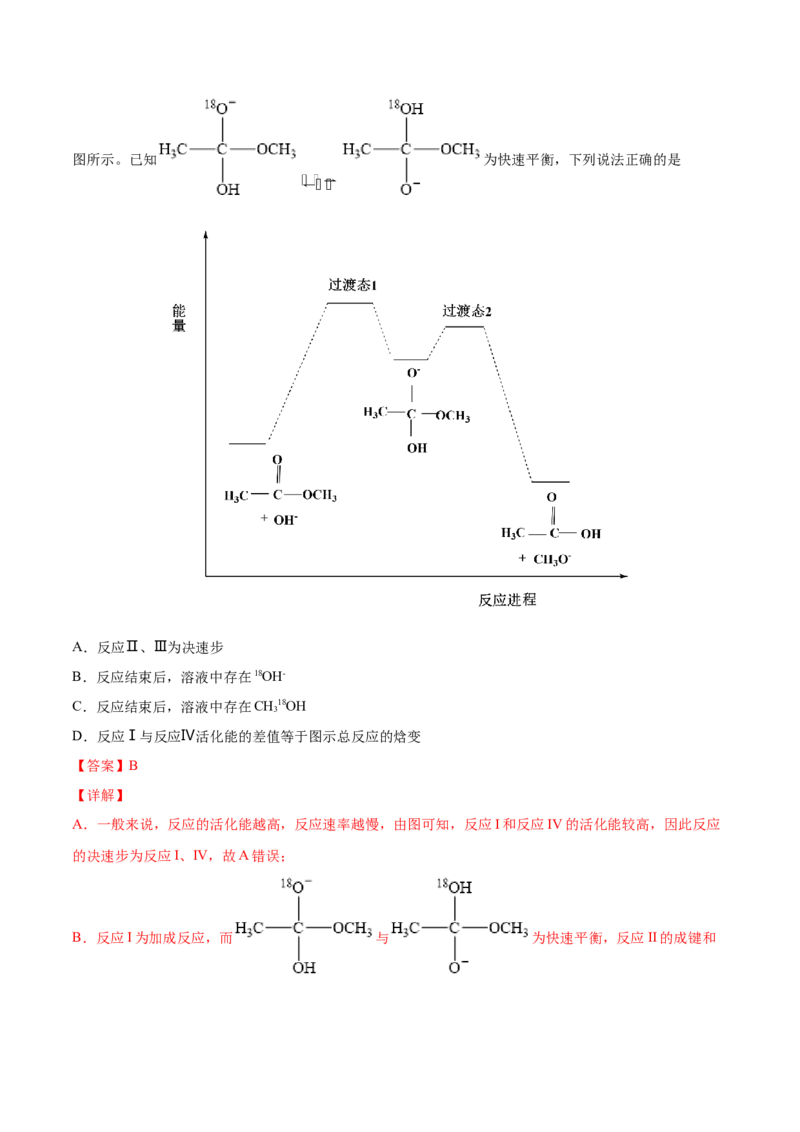
3图所示。已知 为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【详解】
A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较高,因此反应
的决速步为反应I、IV,故A错误;
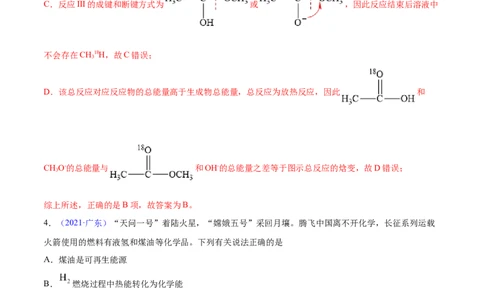
B.反应I为加成反应,而 与 为快速平衡,反应II的成键和断键方式为 或 ,后者能生成18OH-,因此反应结束后,溶液
中存在18OH-,故B正确;
C.反应III的成键和断键方式为 或 ,因此反应结束后溶液中
不会存在CH18H,故C错误;
3
D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因此 和
CHO-的总能量与 和OH-的总能量之差等于图示总反应的焓变,故D错误;
3
综上所述,正确的是B项,故答案为B。
4.(2021·广东)“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列运载
火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是
A.煤油是可再生能源
B. 燃烧过程中热能转化为化学能
C.火星陨石中的 质量数为20
D.月壤中的 与地球上的 互为同位素
【答案】C
【解析】A.煤油来源于石油,属于不可再生能源,故A错误;
B.氢气的燃烧过程放出热量,将化学能变为热能,故B错误;
C.元素符号左上角数字为质量数,所以火星陨石中的 20Ne 质量数为20,故C正确;D.同位素须为同种元素,3He 和 3H的质子数不同,不可能为同位素关系,故D错误;故选C。
5.(2021·浙江)相同温度和压强下,关于反应的 ,下列判断正确的是
A. B.
C. D.
【答案】C
【分析】一般的烯烃与氢气发生的加成反应为放热反应,但是,由于苯环结构的特殊性决定了苯环结构的
稳定性,苯与氢气发生加成反应生成1,3-环己二烯时,破坏了苯环结构的稳定性,因此该反应为吸热反
应。
【解析】A.环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此, ,
A不正确;
B.苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,其与氢气完全
加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即
,B不正确;
C.环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放反应, ,由于1mol 1,3-
环己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量更多,其 ;苯与
氢气发生加成反应生成1,3-环己二烯的反应为吸热反应( ),根据盖斯定律可知,苯与氢气完全
加成的反应热 ,因此 ,C正确;
D.根据盖斯定律可知,苯与氢气完全加成的反应热 ,因此 ,D不正确。
综上所述,本题选C。6.(2021·浙江)已知共价键的键能与热化学方程式信息如下表:
共价键 H-H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
【答案】D
【分析】根据ΔH=反应物的键能总和-生成物的键能总和计算。
【解析】反应的ΔH=2(H-H)+(O-O)-4(H-O);-482kJ/mol=2×436kJ/mol+(O-O)-4×463kJ/mol,解得O-O键的
键能为498kJ/mol,2个氧原子结合生成氧气的过程需要释放能量,因此2O(g)=O (g)的ΔH=-498kJ/mol。
2
7.(2021·湖南)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量的变化情
况如图所示:
下
列说法错误的是
A.该过程的总反应为
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】D【详解】
A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然后又结合氢离
子转化为氢气,所以化学方程式为HCOOH CO↑+H ↑,故A正确;
2 2
B.若氢离子浓度过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制
加酸的电离,使甲酸根浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减
慢,故B正确;
C.由反应机理可知,Fe在反应过程中,化学键数目发生变化,则化合价也发生变化,故C正确;
D.由反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,故D错误;
故选D。
8.[2020浙江7月选考]关于下列 的判断正确的是( )
A. B. C. D.
【答案】B
【解析】
碳酸氢根的电离属于吸热过程,则CO (aq)+H+(aq)=HCO (aq)为放热反应,所以△H<0;
1
CO (aq)+H O(l) HCO (aq)+OHˉ(aq)为碳酸根的水解离子方程式,CO 的水解反应为吸热反应,所
2以△H>0;
2
OHˉ(aq)+H+(aq)=H O(l)表示强酸和强碱的中和反应,为放热反应,所以△H<0;
2 3
醋酸与强碱的中和反应为放热反应,所以△H<0;
4
但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应过程放出的热量小于强酸和强碱反
应放出的热量,则△H>△H;
4 3
综上所述,只有△H<△H 正确,故答案为B。
1 2
9.[2020天津卷]理论研究表明,在101kPa和298K下, 异构化反应过程的能量变化
如图所示。下列说法错误的是
A.HCN比HNC稳定
B.该异构化反应的
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【答案】D
【解析】
A.根据图中信息得到HCN能量比HNC能量低,再根据能量越低越稳定,因此HCN比HNC稳定,故A
正确;
B.根据焓变等于生成物总能量减去反应物总能量,因此该异构化反应的
,故B正确;
C.根据图中信息得出该反应是吸热反应,因此正反应的活化能大于逆反应的活化能,故C正确;
D.使用催化剂,不能改变反应的反应热,只改变反应路径,反应热只与反应物和生成物的总能量有关,
故D错误。
综上所述,答案为D。