文档内容
专题08 元素及其化合物
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共70分)
一、选择题:本题共10个小题,每小题4分,共40分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.我国在材料的开发和应用方面取得了举世嘱目的成就。下列属于金属材料的是
A.港珠澳大桥使用的 B.高速列车外壳使 C.“中国天眼”使 D.卫星芯片使用
混凝土 用的硬铝 用的碳化硅 的高纯硅
2.将铜丝插入浓硝酸中进行如图(a~c是浸有相应试剂的棉花)所示的探究实验,下列分析正确的是
A.Cu与浓硝酸反应,硝酸只表现出酸性,产生红棕色气体
B.a处可观察到棉花变红后褪色
C.b处观察到棉花变蓝,说明 具有还原性
D.c处NaOH能与产生的气体发生复分解反应
3.下列有关陈述I和II均正确且有因果关系的是
选项 陈述I 陈述II
A 回收铁制品常用纯碱溶液去油污 可与强酸反应
B 葡萄酒中添加少量 有漂白性
C 干冰可用于人工降雨 性质稳定D 往轮船外壳镶嵌Zn块可防腐蚀 Zn的金属性强于Fe
4.“铁肥”(主要含 )常用于解决植物叶面变黄问题,通过溶于水配制成溶液喷施在叶面上。
下列有关“铁肥”说法错误的是
A.“铁肥”易因保存不当被空气氧化变质
B.可用 溶液检验“铁肥”中的
C.为保证“铁肥”的效果,可向配制后的溶液中加入少量铁粉
D.可用KSCN溶液检验“铁肥”是否完全失效
5.2022年6月5日,我国“神舟十四号”载人飞船在酒泉卫星发射中心成功发射,完成空间站的“T”字
形布局。下列说法错误的是
A.氧化铝陶瓷可作为火箭腹部的隔热瓦,说明氧化铝耐高温,熔点高
B.飞船上的蒙皮采用的铝合金是混合物
C.CCGA器件所用芯片的主要成分是硅单质
D.操纵棒杆体采用的高强度的碳纤维属于有机高分子材料
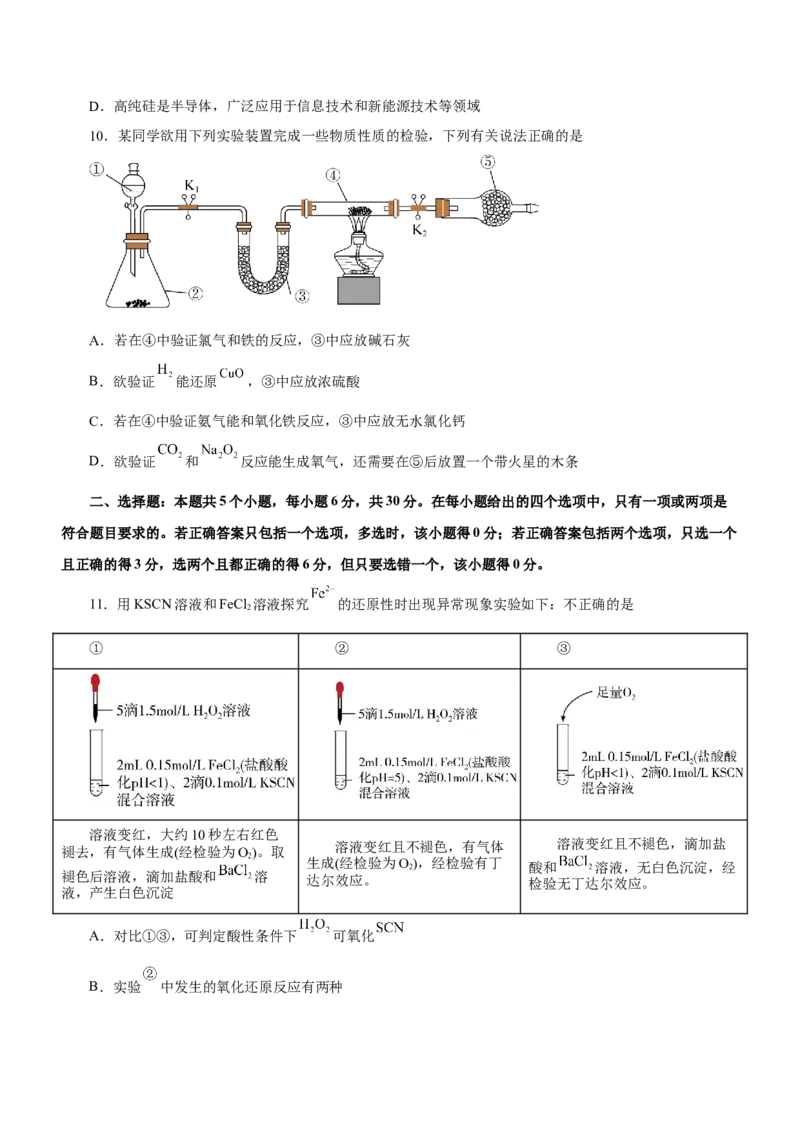
6.将浓盐酸加到 中进行如图(a~c均为浸有相应试液的棉花)所示的探究实验,反应一段时间后,
下列分析正确的是
A.a处变黄色,说明 具有还原性
B.b处变橙色,说明非金属性C.c处红色逐渐变浅,说明 具有漂白性
D.浓盐酸与 反应,只体现HCl的酸性
7.氢氧化铈[Ce(OH) ]是一种重要的稀土氢氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末
4
(含SiO、Fe O、CeO),某课题组以此粉末为原料回收铈,设计实验流程如下:
2 2 3 2
下列说法错误的是( )
A.滤渣A中主要含有SiO、CeO
2 2
B.过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒
C.过程②中发生反应的离子方程式为CeO+HO+3H+===Ce3++2HO+O↑
2 2 2 2 2
D.过程④中消耗 11.2 L O(已折合成标准状况),转移电子数为2×6.02×1023
2
8.某化学学习小组利用如图装置来制备无水AlCl 或NaH(已知:AlCl 、NaH遇水都能迅速发生反应)。下
3 3
列说法错误的是( )
A.制备无水AlCl :装置①中的试剂可能是高锰酸钾
3
B.点燃④处酒精灯之前需排尽装置中的空气
C.装置③中的试剂为浓硫酸
D.制备无水AlCl 和NaH时球形干燥管中碱石灰的作用完全相同
3
9.下列关于物质的性质及用途,说法不正确的是
A.氯化铁溶液具有氧化性,可用于蚀刻铜制品
B.二氧化碳不支持燃烧,故泡沬灭火器可用于金属钠着火后灭火
C.浓硫酸难挥发,可用于实验室制备盐酸D.高纯硅是半导体,广泛应用于信息技术和新能源技术等领域
10.某同学欲用下列实验装置完成一些物质性质的检验,下列有关说法正确的是
A.若在④中验证氯气和铁的反应,③中应放碱石灰
B.欲验证 能还原 ,③中应放浓硫酸
C.若在④中验证氨气能和氧化铁反应,③中应放无水氯化钙
D.欲验证 和 反应能生成氧气,还需要在⑤后放置一个带火星的木条
二、选择题:本题共5个小题,每小题6分,共30分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得3分,选两个且都正确的得6分,但只要选错一个,该小题得0分。
11.用KSCN溶液和FeCl 溶液探究 的还原性时出现异常现象实验如下:不正确的是
2
① ② ③
溶液变红,大约10秒左右红色
溶液变红且不褪色,有气体 溶液变红且不褪色,滴加盐
褪去,有气体生成(经检验为O)。取
2
生成(经检验为O
2
),经检验有丁
酸和 溶液,无白色沉淀,经
褪色后溶液,滴加盐酸和 溶 达尔效应。 检验无丁达尔效应。
液,产生白色沉淀
A.对比①③,可判定酸性条件下 可氧化
B.实验 中发生的氧化还原反应有两种C.②中红色溶液中含有 胶体
D.③中发生的氧化还原反应为:
12.某实验小组通过下图所示实验探究 与水的反应。已知: ;
。下列分析正确的是
A.实验②中 的主要作用是降低了水中 的溶解度
B.⑤酸性 溶液足量,则④⑤产生 的总量与②产生 的量相等
C.实验④证明了同温下
D.实验②⑤均可证明实验①中有复分解反应发生
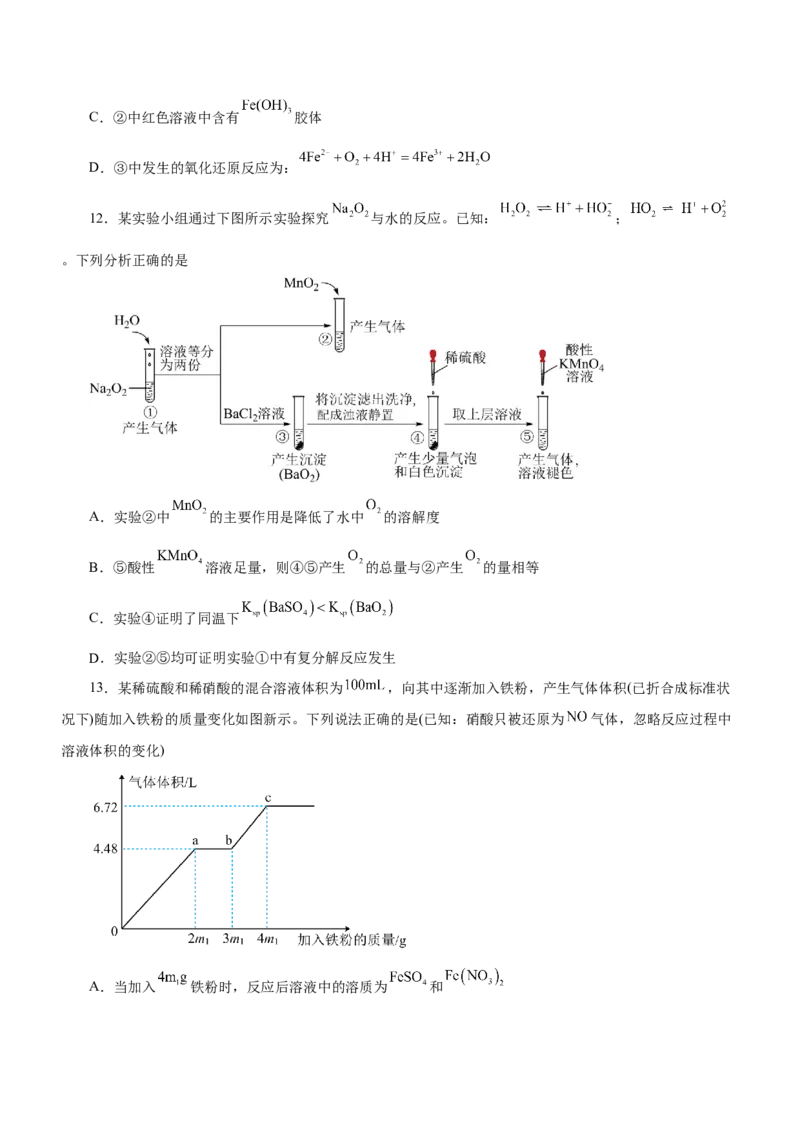
13.某稀硫酸和稀硝酸的混合溶液体积为 ,向其中逐渐加入铁粉,产生气体体积(已折合成标准状
况下)随加入铁粉的质量变化如图新示。下列说法正确的是(已知:硝酸只被还原为 气体,忽略反应过程中
溶液体积的变化)
A.当加入 铁粉时,反应后溶液中的溶质为 和B.混合溶液中 的物质的量浓度为
C.转移电子的物质的量之比
D. 该混合溶液最多能溶解 铜粉
14.向 、 的混合液中加入一定量的铁粉,充分反应后仍有固体存在。则下列判断正确的是
A.加入 溶液一定不变红色 B.溶液中不一定含有
C.溶液中一定含有 D.剩余固体中不一定含有
15.有一包白色粉末,可能含有NaCl、NaI、Mg(OH) 、NaSO 中的一种或几种,为鉴定其成分,取少量
2 2 3
样品进行以下实验:
(1)溶于足量水中,得到无色透明溶液,但仍有部分固体末溶解。
(2)取①的上层清液,滴加少量新制氯水,再加入CCl ,振荡,静置,CCl 层呈无色。
4 4
(3)取②反应后的上层清液,滴加BaCl 溶液,有白色沉淀生成。
2
(4)另取②反应后的上层清液,加入过量的AgNO 溶液和稀硝酸,有白色沉淀生成。
3
有关白色粉末成分的推断正确的是
A.白色粉末中一定含有Mg(OH) 、NaSO 和NaCl,一定不含有NaI
2 2 3
B.白色粉末中一定含有Mg(OH) 、NaSO ,一定不含有NaI,可能含有NaCl
2 2 3
C.白色粉末中一定含有Mg(OH) 、NaSO ,可能含有NaCl和NaI
2 2 3
D.白色粉末中一定含有Mg(OH) ,可能含有NaSO 、NaCl,一定不含有NaI
2 2 3
第II卷 (非选择题共30分)
三、非选择题:本题共2个小题,共30分。
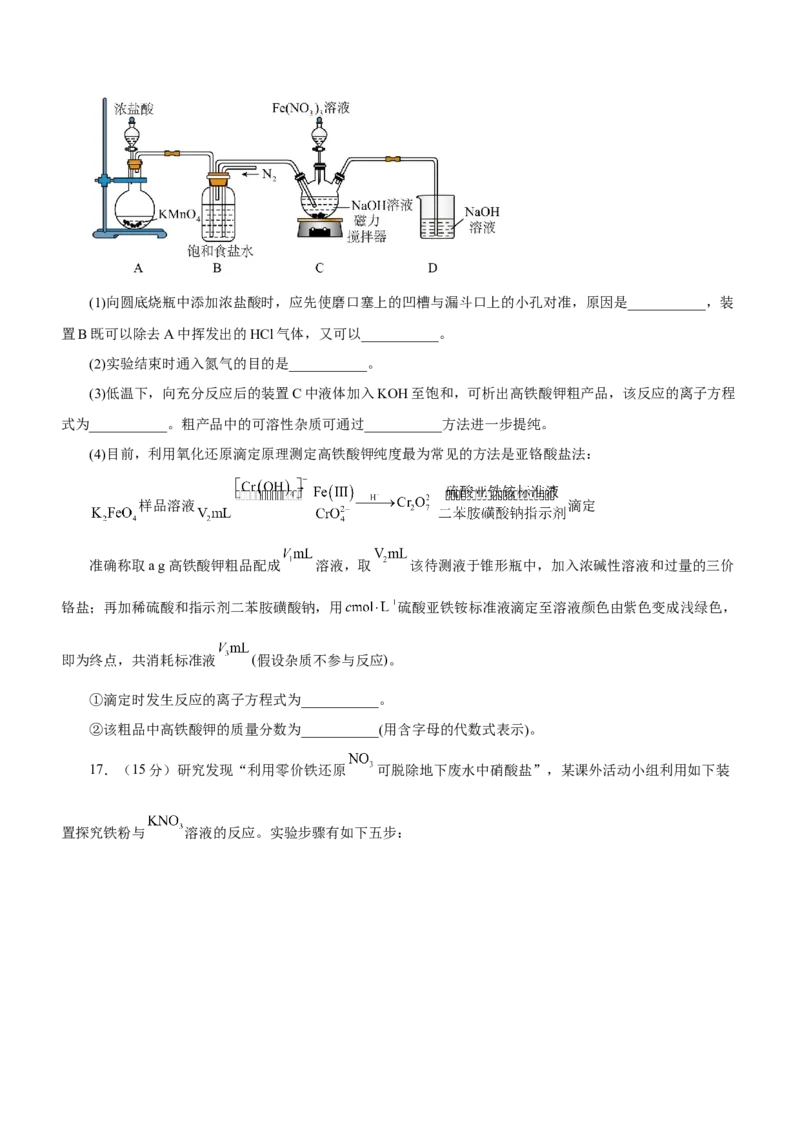
16.(15分) 高铁酸钾 是一种新型非氯高效消毒净水剂,集氧化、消毒、吸附、絮凝、去污等
多种功能为一体,是新型、高效、安全、多功能的水处理剂。如图是以三价铁盐作为铁源、次氯酸盐作为强氧
化剂制备高铁酸钾的装置图(部分夹持装置略)。回答下列问题:(1)向圆底烧瓶中添加浓盐酸时,应先使磨口塞上的凹槽与漏斗口上的小孔对准,原因是___________,装
置B既可以除去A中挥发出的HCl气体,又可以___________。
(2)实验结束时通入氮气的目的是___________。
(3)低温下,向充分反应后的装置C中液体加入KOH至饱和,可析出高铁酸钾粗产品,该反应的离子方程
式为___________。粗产品中的可溶性杂质可通过___________方法进一步提纯。
(4)目前,利用氧化还原滴定原理测定高铁酸钾纯度最为常见的方法是亚铬酸盐法:
样品溶液 滴定
准确称取a g高铁酸钾粗品配成 溶液,取 该待测液于锥形瓶中,加入浓碱性溶液和过量的三价
铬盐;再加稀硫酸和指示剂二苯胺磺酸钠,用 硫酸亚铁铵标准液滴定至溶液颜色由紫色变成浅绿色,
即为终点,共消耗标准液 (假设杂质不参与反应)。
①滴定时发生反应的离子方程式为___________。
②该粗品中高铁酸钾的质量分数为___________(用含字母的代数式表示)。
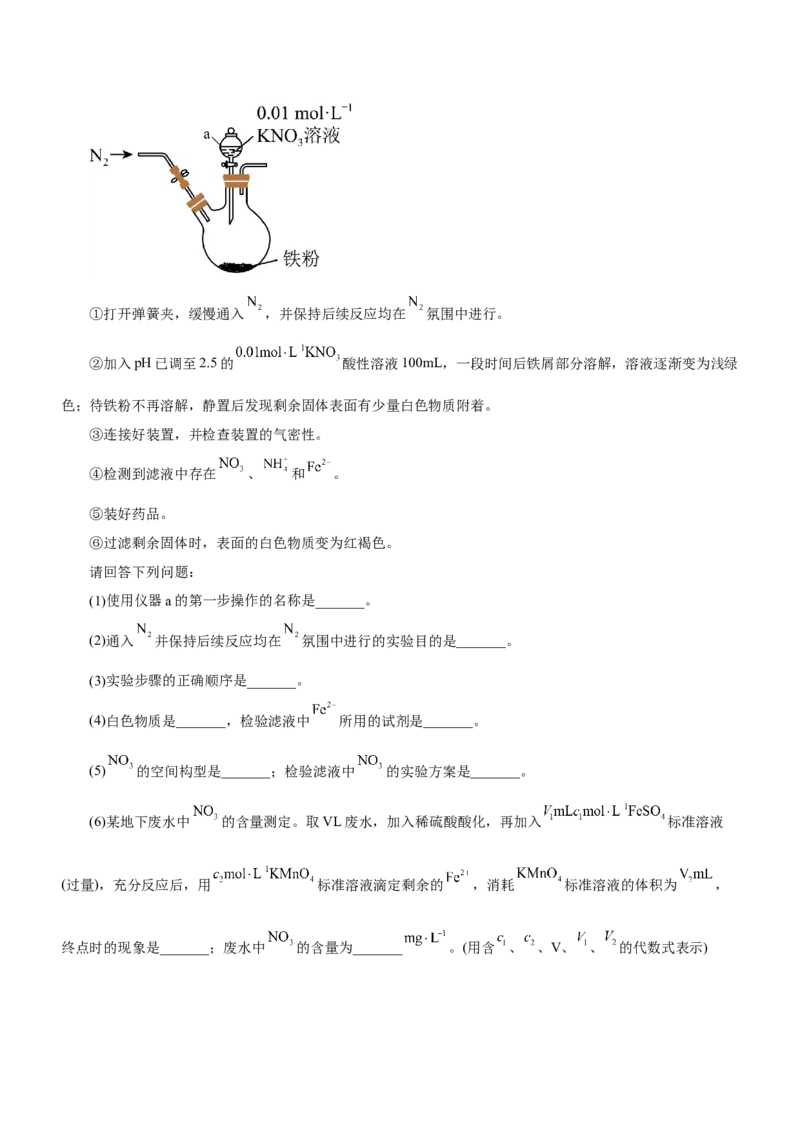
17.(15分)研究发现“利用零价铁还原 可脱除地下废水中硝酸盐”,某课外活动小组利用如下装
置探究铁粉与 溶液的反应。实验步骤有如下五步:①打开弹簧夹,缓慢通入 ,并保持后续反应均在 氛围中进行。
②加入pH已调至2.5的 酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿
色;待铁粉不再溶解,静置后发现剩余固体表面有少量白色物质附着。
③连接好装置,并检查装置的气密性。
④检测到滤液中存在 、 和 。
⑤装好药品。
⑥过滤剩余固体时,表面的白色物质变为红褐色。
请回答下列问题:
(1)使用仪器a的第一步操作的名称是_______。
(2)通入 并保持后续反应均在 氛围中进行的实验目的是_______。
(3)实验步骤的正确顺序是_______。
(4)白色物质是_______,检验滤液中 所用的试剂是_______。
(5) 的空间构型是_______;检验滤液中 的实验方案是_______。
(6)某地下废水中 的含量测定。取VL废水,加入稀硫酸酸化,再加入 标准溶液
(过量),充分反应后,用 标准溶液滴定剩余的 ,消耗 标准溶液的体积为 ,
终点时的现象是_______;废水中 的含量为_______ 。(用含 、 、V、 、 的代数式表示)