文档内容
专题 09 化学反应速率与化学平衡
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共70分)
一、选择题:本题共10个小题,每小题4分,共40分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.下列事实不能用勒夏特列原理解释的是
A.工业上SO 和O 在常压下生成SO
2 2 3
B.加热蒸干AlCl 溶液不能得到无水AlCl
3 3
C.用浓氨水和氢氧化钠制取氨气
D.水中的c(H+)比0.1mol·L-1 NaOH溶液中的大
2.下列有关NO与O 生成NO 的反应的说法正确的是
2 2
A.该反应在任意温度下都可自发进行
B.该反应达到平衡时,2v(O ) =v(NO)
2 正 逆
C.及时移出部分生成的NO 可加快NO的反应速率
2
D.当反应中消耗22.4 LNO时,转移的电子数约为
3.一定温度下,向2.0L恒容密闭容器中充入 ,发生反应 ,
反应过程中测得的有关数据见下表:
0 2 4 6 8
0 0.30 0.39 0.40 0.40
下列说法正确的是A.0~2s,用CO表示的平均反应速率为
B.若达平衡后缩小容器体积,重新达到平衡前,
C.其他条件不变,若改用更高效的催化剂,2~6s时测得的数据均会增大
D.其他条件不变,改为在恒容绝热密闭容器中进行该反应,化学平衡常数不变
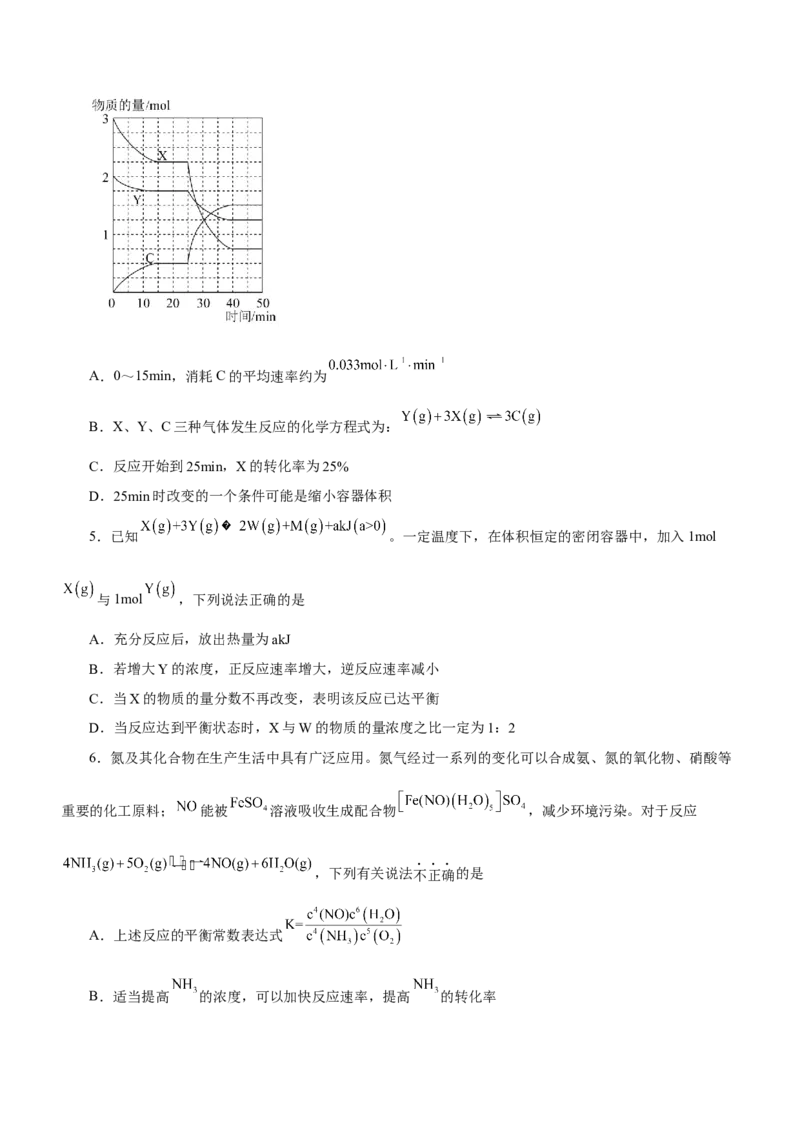
4.在一定条件下的1L密闭容器中,X、Y、C三种气体的物质的量随时间的变化如图所示。下列说法不
正确的是A.0~15min,消耗C的平均速率约为
B.X、Y、C三种气体发生反应的化学方程式为:
C.反应开始到25min,X的转化率为25%
D.25min时改变的一个条件可能是缩小容器体积
5.已知 。一定温度下,在体积恒定的密闭容器中,加入1mol
与1mol ,下列说法正确的是
A.充分反应后,放出热量为akJ
B.若增大Y的浓度,正反应速率增大,逆反应速率减小
C.当X的物质的量分数不再改变,表明该反应已达平衡
D.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
6.氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等
重要的化工原料; 能被 溶液吸收生成配合物 ,减少环境污染。对于反应
,下列有关说法不正确的是
A.上述反应的平衡常数表达式
B.适当提高 的浓度,可以加快反应速率,提高 的转化率C. 断裂同时有 断裂,说明达该条件下的平衡状态
D.其它条件不变,加入高效的催化剂能提高单位体积内的活化分子百分数
7.在 下,向 的恒容密闭容器里按 充入气体A,B,发生反应:
。 时达到平衡,测得部分数据如表所示:
物质及状态
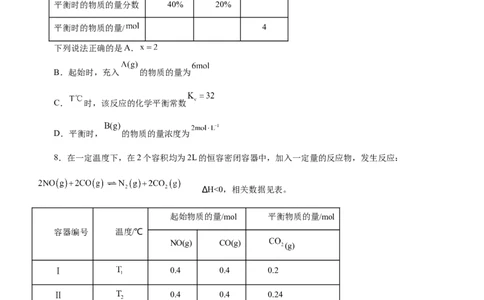
平衡时的物质的量分数 40% 20%
平衡时的物质的量/ 4
下列说法正确的是A.
B.起始时,充入 的物质的量为
C. 时,该反应的化学平衡常数
D.平衡时, 的物质的量浓度为
8.在一定温度下,在2个容积均为2L的恒容密闭容器中,加入一定量的反应物,发生反应:
∆H<0,相关数据见表。
起始物质的量/mol 平衡物质的量/mol
容器编号 温度/℃
NO(g) CO(g)
(g)
Ⅰ 0.4 0.4 0.2
Ⅱ 0.4 0.4 0.24
下列说法不正确的是A.
B.Ⅰ中反应达到平衡时,CO的转化率为50%
C.达到平衡所需要的时间:Ⅱ<Ⅰ
D.对于Ⅰ,平衡后向容器中再充入0.4mol CO和0.2mol ,平衡正向移动
9.一定温度下,在V = 1L的恒容容器中,反应2NO(g) = 2N (g) + O(g)的部分实验数据如下:
2 2 2反应时间
/ min 0 10 20 30 40 50 60 70 80 90 100
c(NO) /
2
mol·L-1 0.10 0.09 0.08 0.07 0.06 0.05 0.04 0.03 0.02 0.01 0.00
下列说法不正确的是
A.其它条件一定时,NO的分解速率与其浓度无关
2
B.0~100min内,以O 表示的平均反应速率为5×10-4mol∙L-1∙min-1
2
C.若某时刻NO的转化率为50%,则此时容器内压强为初始压强的1.25倍
2
D.若保持体积不变,NO初始浓度改为0.20mol/L,则反应30min时其转化率仍为30%
2
10.某小组同学进行了如下实验:
① 溶液和 溶液各1mL混合得到红色溶液a,均分溶液a置于b、c
两支试管中;
②向b中滴加3滴饱和 溶液,溶液颜色加深;
③再向上述b溶液中滴加3滴 溶液,溶液颜色变浅且出现浑浊;
④向c中逐渐滴加 溶液2mL,过程中溶液颜色先变深后变浅。
下列分析不正确的是
A.实验②中增大 浓度使平衡 正向移动
B.实验③中发生反应:
C.实验③和④中溶液颜色变浅的原因相同
D.实验②、③、④均可说明浓度改变对平衡移动的影响
二、选择题:本题共5个小题,每小题6分,共30分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得3分,选两个且都正确的得6分,但只要选错一个,该小题得0分。
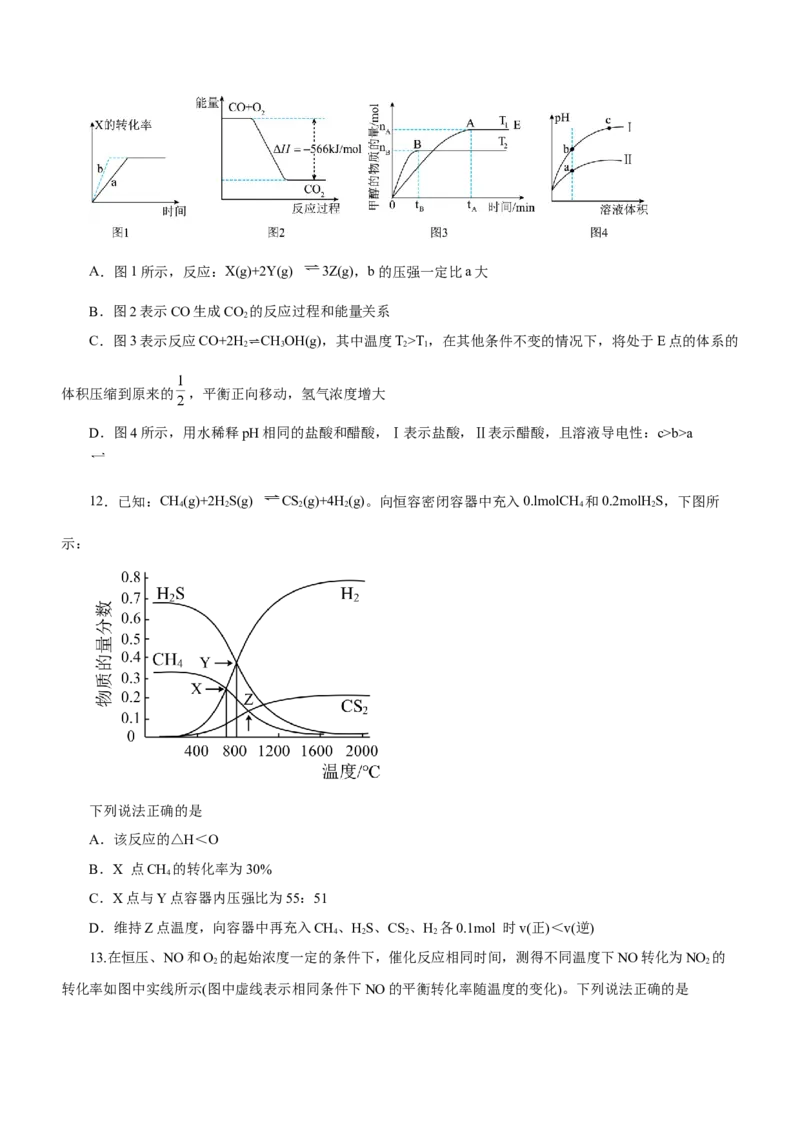
11.如图所示与对应的叙述一定正确的是A.图1所示,反应:X(g)+2Y(g) 3Z(g),b的压强一定比a大
B.图2表示CO生成CO 的反应过程和能量关系
2
C.图3表示反应CO+2H 2⇌CH
3
OH(g),其中温度T
2
>T
1
,在其他条件不变的情况下,将处于E点的体系的
体积压缩到原来的 ,平衡正向移动,氢气浓度增大
D.图4所示,用水稀释pH相同的盐酸和醋酸,Ⅰ表示盐酸,Ⅱ表示醋酸,且溶液导电性:c>b>a
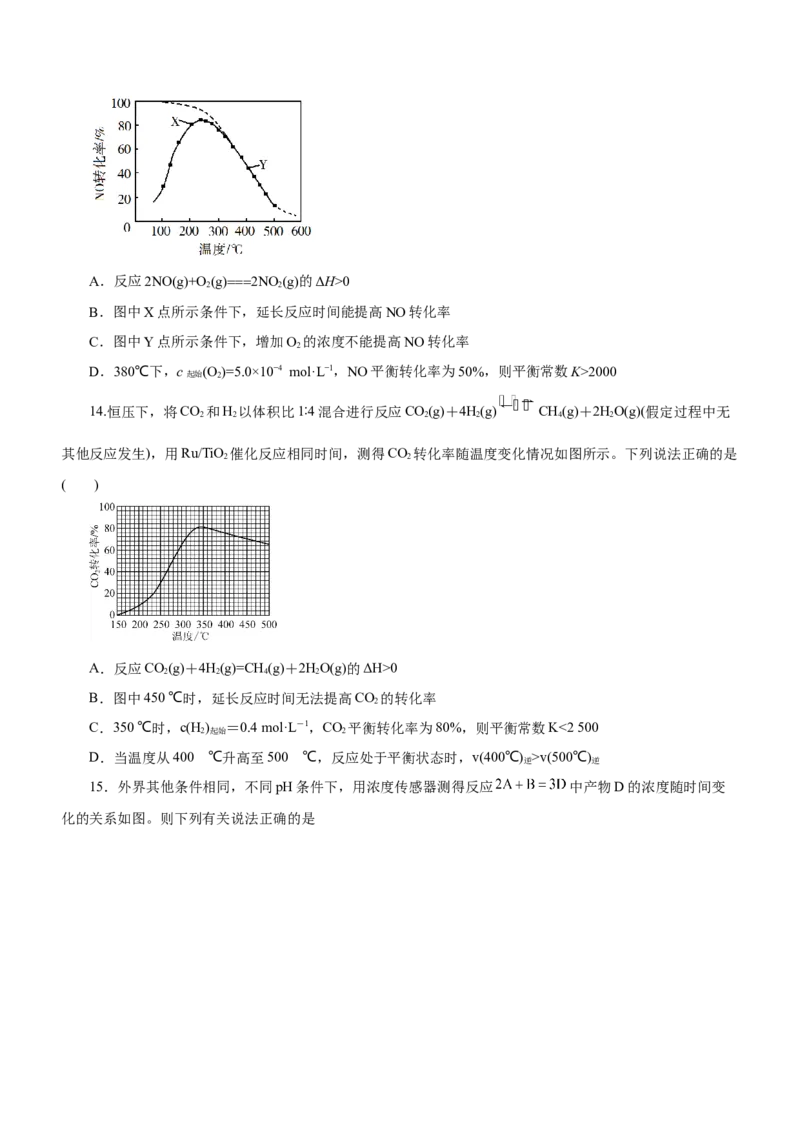
12.已知:CH(g)+2HS(g) CS(g)+4H(g)。向恒容密闭容器中充入0.lmolCH 和0.2molHS,下图所
4 2 2 2 4 2
示:
下列说法正确的是
A.该反应的△H<O
B.X 点CH 的转化率为30%
4
C.X点与Y点容器内压强比为55:51
D.维持Z点温度,向容器中再充入CH、HS、CS、H 各0.1mol 时v(正)<v(逆)
4 2 2 2
13.在恒压、NO和O 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO 的
2 2
转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是A.反应2NO(g)+O (g)===2NO (g)的ΔH>0
2 2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O 的浓度不能提高NO转化率
2
D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
14.恒压下,将CO 和H 以体积比1∶4混合进行反应CO(g)+4H(g) CH(g)+2HO(g)(假定过程中无
2 2 2 2 4 2
其他反应发生),用Ru/TiO 催化反应相同时间,测得CO 转化率随温度变化情况如图所示。下列说法正确的是
2 2
( )
A.反应CO(g)+4H(g)=CH (g)+2HO(g)的ΔH>0
2 2 4 2
B.图中450 ℃时,延长反应时间无法提高CO 的转化率
2
C.350 ℃时,c(H) =0.4 mol·L-1,CO 平衡转化率为80%,则平衡常数K<2 500
2 起始 2
D.当温度从400 ℃升高至500 ℃,反应处于平衡状态时,v(400℃) >v(500℃)
逆 逆
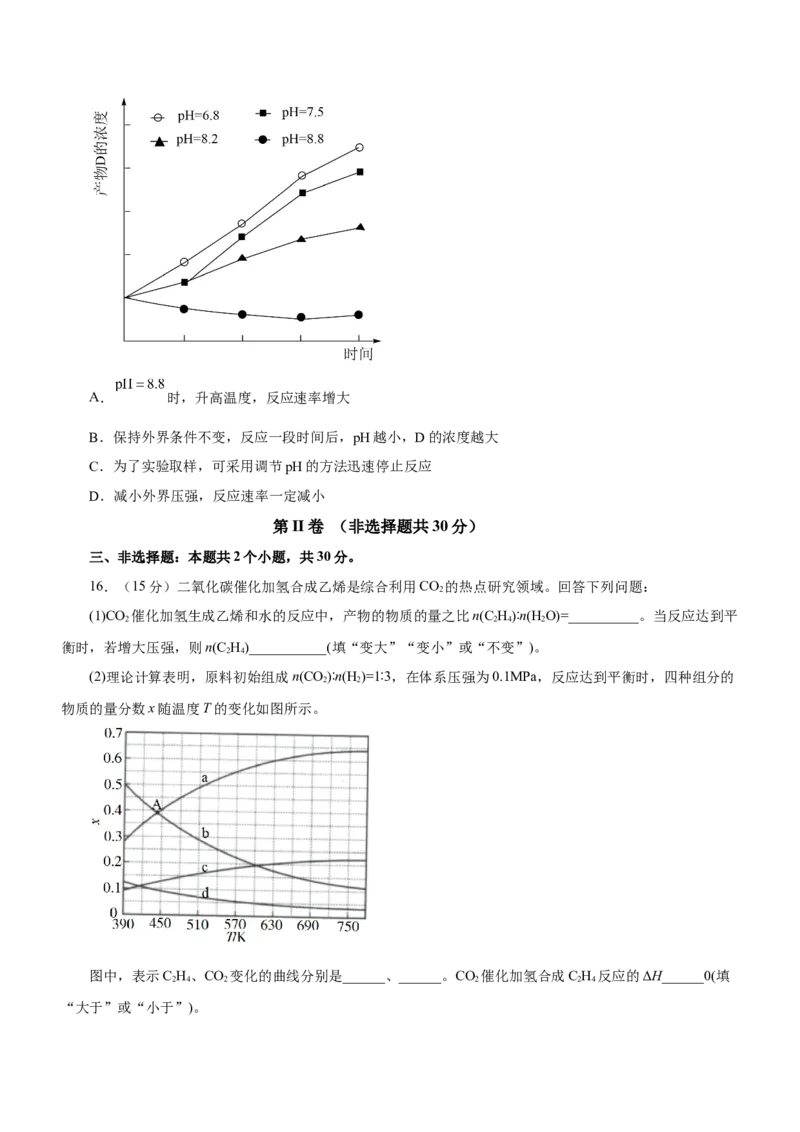
15.外界其他条件相同,不同pH条件下,用浓度传感器测得反应 中产物D的浓度随时间变
化的关系如图。则下列有关说法正确的是A. 时,升高温度,反应速率增大
B.保持外界条件不变,反应一段时间后,pH越小,D的浓度越大
C.为了实验取样,可采用调节pH的方法迅速停止反应
D.减小外界压强,反应速率一定减小
第II卷 (非选择题共30分)
三、非选择题:本题共2个小题,共30分。
16.(15分)二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答下列问题:
2
(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C H)∶n(H O)=__________。当反应达到平
2 2 4 2
衡时,若增大压强,则n(C H)___________(填“变大”“变小”或“不变”)。
2 4
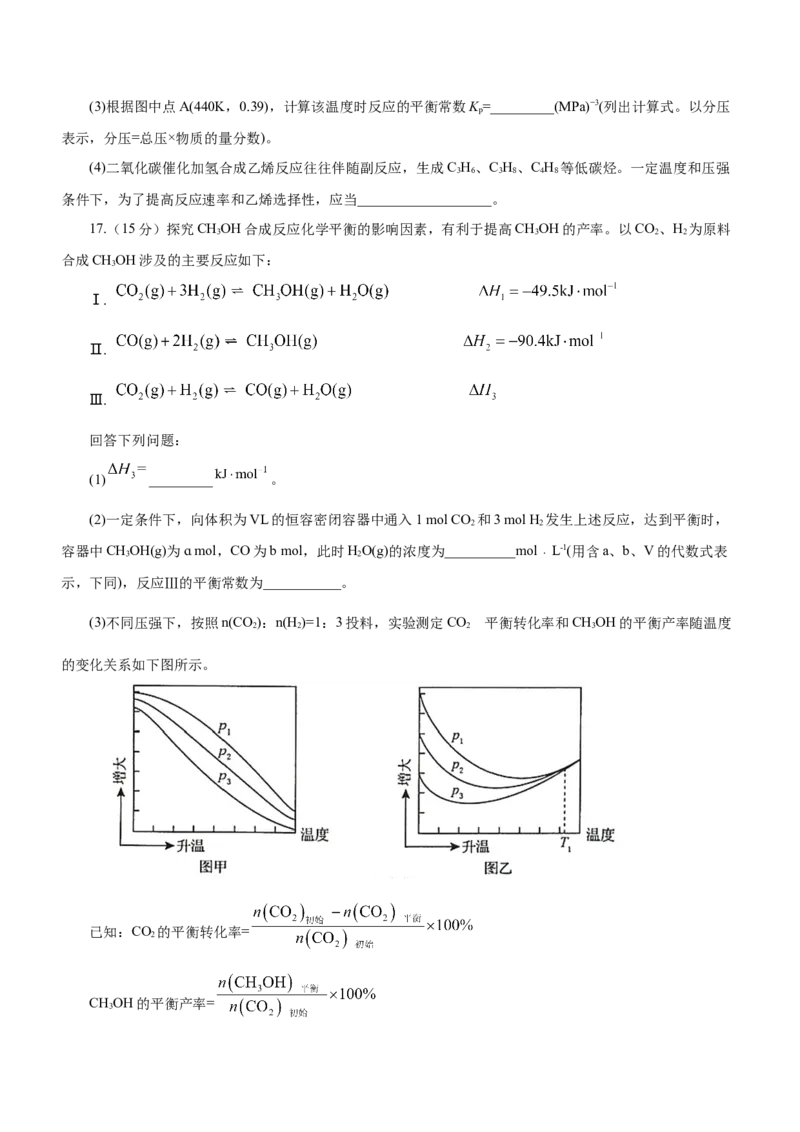
(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分的
2 2
物质的量分数x随温度T的变化如图所示。
图中,表示C H、CO 变化的曲线分别是______、______。CO 催化加氢合成C H 反应的ΔH______0(填
2 4 2 2 2 4
“大于”或“小于”)。(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数K =_________(MPa)−3(列出计算式。以分压
p
表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C H、C H、C H 等低碳烃。一定温度和压强
3 6 3 8 4 8
条件下,为了提高反应速率和乙烯选择性,应当___________________。
17.(15分)探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以CO、H 为原料
3 3 2 2
合成CHOH涉及的主要反应如下:
3
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1) _________ 。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO 和3 mol H 发生上述反应,达到平衡时,
2 2
容器中CHOH(g)为ɑ mol,CO为b mol,此时HO(g)的浓度为__________mol﹒L-1(用含a、b、V的代数式表
3 2
示,下同),反应Ⅲ的平衡常数为___________。
的
(3)不同压强下,按照n(CO):n(H )=1:3投料,实验测定CO 平衡转化率和CHOH的平衡产率随温度
2 2 2 3
的变化关系如下图所示。
已知:CO 的平衡转化率=
2
CHOH的平衡产率=
3其中纵坐标表示CO 平衡转化率的是图___________(填“甲”或“乙”);压强p、p、p 由大到小的顺序
2 1 2 3
为___________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________。
1
(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为_________(填标号)。
2 3
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压