文档内容
专题 09 化学反应速率与化学平衡
1.将4份等量的铝片分别加到足量的下列溶液中充分反应后,产生氢气量最快的是
A. 溶液 B. 溶液
C. 溶液 D. 溶液
【答案】C
【解析】铝和稀硝酸反应生成NO,不会放出氢气,铝和醋酸、硫酸、盐酸反应实质是和氢离子反应,氢
离子浓度越大放出氢气越快,硫酸是二元强酸,盐酸是一元强酸,醋酸是一元弱酸,相同浓度的三种酸开始时
氢离子浓度由大到小的顺序为:硫酸>盐酸>醋酸,所以铝和相同浓度的醋酸、硫酸、盐酸,放出氢气最快的
是硫酸,答案选C。
2.下列生产中,不涉及勒夏特列原理的是
A.合成氨 B.饱和氨盐水中通 制碳酸氢钠
C. 和 制 D.侯氏制碱法处理母液
【答案】C
【解析】合成氨反应为可逆反应,生产中一定涉及勒夏特列原理,故A不符合题意;饱和氨盐水中存在
着氨水的电离平衡,则饱和氨盐水中通二氧化碳制碳酸氢钠一定涉及勒夏特列原理,故B不符合题意;氢气
与氯气制氯化氢的反应不是可逆反应,氯化氢的生产中不一定涉及勒夏特列原理,故C符合题意;侯氏制碱
法的母液中存在铵根离子和碳酸氢根离子的水解平衡,向母液中加碱溶液,碳酸氢根离子和铵根离子均能与氢
氧根离子反应,则侯氏制碱法处理母液时一定涉及勒夏特列原理,故D不符合题意;故选C。
3.反应A(g)+3B(g) 2C(g) 达到平衡后,将反应体系的温度降低,下列叙述中正确的是
A.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率和逆反应速率都减小,平衡向正反应方向移动
D.正反应速率和逆反应速率都减小,平衡向逆反应方向移动
【答案】C【解析】反应A(g)+3B(g) 2C(g)的焓变 ,即该反应正向放热,反应达到平衡后,降低温度,正逆
反应速率都将减小,降低温度,平衡将向放热反应移动,即平衡向正反应方向移动,故答案为C。
4.以 、 和 为原料,制备 和氯化亚砜( )的原理为:
。下列说法正确的是
A.反应平衡常数
B. 键断裂的同时有 键形成,说明反应到达该条件下的平衡状态
C.使用催化剂可以同时降低正反应和逆反应的活化能
D.上述反应中消耗 的 ,转移电子数为
【答案】C
【解析】反应中 为固体,由化学方程式可知,反应平衡常数 ,A错误;
1mol 键断裂的同时有 键形成,描述的都是正反应,不能说明反应到达该条件下的平衡状
态,B错误;催化剂改变反应历程,加快反应速率;使用催化剂可以同时降低正反应和逆反应的活化能,C正
确;没有标况,不能计算转移的电子数,D错误;故选C。
5.对某一可逆反应来说,升高温度的作用是
A.提高反应物的平衡转化率 B.改变平衡混合物的组成
C.降低反应物和生成物的键能 D.加快正反应速率,减慢逆反应速率
【答案】B
【解析】升高温度,平衡不一定正向移动,若为吸热反应,升温平衡逆向移动,反应物的平衡转化率减
小,故A错误;化学反应一定伴随能量的变化,可能为放热反应,也可能为吸热反应,升温平衡可能正向移
动,也可能逆向移动,故升高温度能改变平衡混合物的组成,故B正确;反应物和生成物的键能不随温度的
改变而改变,故C错误;升高温度,正、逆反应速率均增大,故D错误;故选B。
6.氯气、氯盐、次氯盐[ ]、二氧化氯在生产生活中具有广泛应用。Deacon曾提出在催化
剂作用下,通过氧气直接氧化氯化氢成功制备氯气。该反应具有一定的可逆性,热化学方程式可表示:
;二氧化氯(ClO )为新型绿色消毒
2剂,沸点为9.9℃,可溶于水,有毒,浓度较高时易发生爆炸。用浓盐酸和NaClO 反应可制得ClO 关于
3 2.
Deacon提出的制Cl 的反应,下列有关说法正确的是
2
A.该反应的
B.每生成22.4LCl (已折算成标准状况),放出58kJ的热量
2
C.升高温度,核反应v (逆)增大,v (正)减小,平衡向逆反应方向移动
D.断裂4molH—Cl键的同时,有4molH—O键生成,说明该反应达到平衡状态
【答案】B
【解析】反应为气体分子数减小的反应,为熵减反应 ,A错误;由热化学方程式可知,每生成
22.4LCl (已折算成标准状况,为1mol),放出116kJ÷2=58kJ的热量,B正确;升高温度,正逆反应速率均会变
2
大,C错误;断裂4molH—Cl键的同时,有4molH—O键生成,描述的都是正反应,不能说明该反应达到平衡
状态,D错误;故选B。
7.利用合成气(CO和 )在催化剂作用下合成甲醇: (Q>0),反应体系
中CO的平衡转化率α(CO)与温度、压强的关系如图所示。下列说法错误的是
A.升高温度,平衡常数减小
B.
C.在不同温度、压强下进行该反应,α(CO)不可能相等
D.若 ,则合成气中
【答案】C
【分析】反应为放热反应,升高温度平衡逆向移动,平衡常数减小;反应为气体分子数减小的反应,相同条件下,增大压强,平衡正向移动,CO的平衡转化率增大,故 ;
【解析】由分析可知,升高温度平衡逆向移动,平衡常数减小,A正确; 由分析可知,增大压强,平衡
正向移动,CO的平衡转化率增大,故 ,B正确;温度、压强均会改变平衡移动,由图可知,不同温
度、压强下进行该反应,α(CO)可能相等,C错误;若 ,则反应中投料比等于反应的系数比,故
合成气中 ,D正确;故选C。
9.甲烷水蒸气催化重整是制备高纯氢的方法之一,反应为CH
4
(g)+H
2
O(g)⇌CO(g)+3H
2
(g)。在不同温度下,
向a、b两个恒温恒容的密闭容器中均通入1.1mol CH (g)和1.1mol H O(g),测得容器a中CO物质的量、容器b
4 2
中H 物质的量随时间的变化曲线如图所示(已知容器a、b的体积为2L)。下列说法正确的是 ( )
2
A.该反应为放热反应
B.两容器达到平衡时,b容器中CO的体积分数大于a容器
C.a容器前4min用CH 表示的平均反应速率为0.125mol/(L∙min)
4
D.a容器达到平衡后,再充入1.1mol CH (g)和1molCO(g),此时v <v
4 正 逆
【答案】C
【解析】已知在a、b两个恒温、恒容的密闭容器中,充入相同量的甲烷和水,生成氢气的计量数是CO
的3倍,结合图像可知,b为H(g)的图像,其转化为CO(g)时,物质的量为0.6mol;a为CO(g)的图像,a达到
2
平衡所用的时间比b段,则a的温度高于b,升高温度,CO的物质的量增大,即平衡正向移动,故正反应为吸
热反应。分析可知,该反应为吸热反应,A说法错误;分析可知,b表示H(g)的图像,其转化为CO(g)时,达
2
到平衡时,物质的量为0.6mol,a容器中两容器达到平衡时,b容器中CO的体积分数小于a容器,B说法错误;根据图像,a容器前4min CO的物质的量为1.0mol,用CH 表示的平均反应速率为
4
=0.125mol/(L∙min),C说法正确;a容器达到平衡时,
再充入1.1mol CH (g)和1molCO(g),K= >Q= ,平衡正向移动,v >v ,D说法
4 c 正 逆
错误;答案为C。
10.利用现代传感技术探究压强对 2NO (g) NO(g)平衡移动的影响。在恒定温度和标准压强条件下,
2 2 4
往针筒中充入一定体积的 NO 气体后密封并保持活塞位置不变。分别在 t、t 时迅速移动活塞后并保持活塞
2 1 2
位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是( )
A.t 时移动活塞,使容器体积增大
1
B.在 B、E 两点,对应的正反应速率:v(B)>v(E)
C.图中除 A、C、F 点外,其他点均为平衡状态
D.在 E,F,H 三点中,H 点的气体平均相对分子质量最大
【答案】C
【解析】由图可知,t 时移动活塞,针筒内气体压强迅速减小,说明针筒的体积增大,故A正确;针筒
1
内气体压强越强越大,化学反应速率越大,由图可知,B点压强大于E点,则对应的正反应速率:v(B)>v(E),
故B正确;由图可知,除 A、C、F 点外,G点也没有达到平衡,故C错误;由质量守恒定律可知,E,F,H
三点中气体的质量相同,由图可知,t 时移动活塞,针筒内气体压强迅速增大,说明针筒的体积减小,增大
2压强,平衡向正反应方向移动,混合气体的物质的量减小,则E,F,H 三点中,H 点的气体物质的量最小,
平均相对分子质量最大,故D正确;故选C。
11.在 恒容密闭容器中充入气体 和 ,发生反应 ,所得实验数
据如表所示。下列说法正确的是 ( )
实验编号 温度/℃ 起始 起始 平衡
① 300
② 500
③ 500
A.上述反应的
B. 时测得①中 ,则 内
C.500℃时,该反应的平衡常数
D.实验③中反应达到平衡时, 的转化率小于20%
【答案】D
【解析】由实验①和实验②中数据可知,升高温度,平衡时C的物质的量减少,说明平衡逆向移动,则
正反应为放热反应, ,选项A错误;D是固体,故不能用D的浓度变化来表示反应速率,选项B错
误;
500℃时,由实验②可知反应 达到平衡状态时,c(C)= =0.04mol/L,
c(A)= =0.16mol/L,c(B)= =0.01mol/L,K= ,选项C
错误;实验②与实验③的温度相同,容器的容积相同,而实验③反应物的用量恰好是实验②的一半,即相当于
减压,减压使平衡向气体分子数增大的方向移动,所以实验③中反应达到平衡后,反应物的转化率小于实验
②(实验②中的平衡转化率为20%),选项D正确。答案选D。
12.温度为T 时,在容积为10 L的恒容密闭容器充入一定量的M (g)和N (g),发生反应
1。反应过程中的部分数据如表所示,下列说法正确的是( )
t/min 0 5 10
n(M)/ mol 6.0 4.0
n(N)/ mol 3.0 1.0
A.T 时该反应的化学平衡常数为0.64,则T>T
2 1 2
B.0-5 min内,用M表示的平均反应速率为0.4 mol∙L-1∙min-1
C.该反应在第8 min时v >v
逆 正
D.当M、N的转化率之比保持不变时,可判断该反应达到平衡状态
【答案】A
【解析】根据表格信息,可列三段式: ,再结
合10min时的数据可知温度为T 时,反应在5min时已达到平衡,在该温度下的平衡常数为:
1
,由此解答。该反应为吸热反应,升高温度,平衡正向进行,平衡常数增
大,已知T 时该反应的化学平衡常数为0.8,T 时该反应的化学平衡常数为0.64,故T>T,A正确;根据三
1 2 1 2
段式可知,0-5 min内,用M表示的平均反应速率为 ,B错误;根
据分析可知,反应在5min时达到平衡状态,故在第8 min时v =v ,C错误;根据反应方程式M、N的化学
逆 正
计量数之比可知,二者的转化率之比始终保持不变,是个定值,故D错误;答案选A。
13.工业上,用天然气处理废气中的 发生反应为
△H。某小组在刚性密闭容器充入lmol (g)和2mol (g)在不同温度下仅发生上述反应,测得
的浓度( )变化如下表所示。时间温度 0 5min 10min 15min 20min 25min
℃ 1.00 0.70 0.65 0.60 0.60 0.60
℃ 1.00 0.80 0.70 0.65 0.50 0.50
下列叙述错误的是
A.上述反应温度T:
B. ℃下,若开始加入催化剂,则平衡所用时间小于15min
C. ℃下,20min时充入少量 ,则 平衡转化率增大
D. ℃下,上述反应的平衡常数
【答案】D
【解析】观察表格数据,其他条件相同, ℃下, 浓度变化较快,速率较大,即温度较高;观察平
衡时 浓度知, ℃→ ℃时降低,平衡时 浓度减小,说明平衡向正反应方向移动,即正反应是放热
反应,降温时平衡常数增大,A项正确;加入催化剂,反应加快,缩短达到平衡的时间,B项正确;达到平衡
时充入 ,则平衡向正反应方向移动, 的平衡转化率增大,C项正确; ℃下平衡时,
, , ,代入数据可计算
,D项错误;故选D。
14.T℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图
1所示;若保持其他条件不变,温度分别为T 和T 时,Y的体积分数与时间的关系如图2所示。则下列结论正
1 2
确的是A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L·min)
B.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
【答案】B
【解析】根据图1所示可知反应进行的前3 min内,X的浓度减小了△c(X)=2.0 mol/L-1.4 mol/L=0.6
mol/L,则用X表示的化学反应速率v(X)= ,A错误;根据图示可知:在反应过程中
X、Y浓度减小,Z浓度增加,反应进行到3 min时三种物质都存在,且它们的浓度不再发生变化,说明该反
应是可逆反应,其中X、Y是反应物,Z是生成物,在前3 min内X、Y、Z三种物质的浓度变化分别是0.6
mol/L、0.2 mol/L、0.4 mol/L,三种物质的变化变化的比为3:1:2,故反应方程式可表示为3X(g)+Y(g)
2Z(g),B正确;在其它条件不变时,温度升高,化学反应速率加快,达到平衡所需时间缩短。根据图2可知温
度:T>T。升高温度,Y的体积分数减少,说明升高温度,化学平衡正向移动,导致反应的化学平衡常数K
2 1
增大,C错误;若改变反应条件,使反应进程如图3所示,反应达到平衡所需时间缩短,但各种物质的含量不
变,说明化学平衡不移动。由于反应3X(g)+Y(g) 2Z(g)是反应前后气体体积改变的反应,则改变的条件应该
是使用了催化剂,而不可能是增大体系的压强,D错误;故合理选项是B。
15.体积为1L的恒温恒容密闭容器中发生反应: ,A、B浓度随时间变化关系如下图所
示。下列说法不正确的是A.曲线X表示A的浓度随时间的变化
B.25~30min内用A表示的平均化学反应速率是
C.气体总压不随时间变化可以说明该反应达到平衡状态
D.反应进行至25min时,曲线发生变化的原因是增加A的浓度
【答案】B
【分析】10min内X变化量为0.6-0.2=0.4mol/L,Y的变化量为0.6-0.4=0.2mol/L, 根据
反应方程式 可知X为A,Y为B;
【解析】根据分析可知曲线X表示A的浓度随时间的变化,故A正确;25~30min内
, ,A表示的平均化学反应速率是
,故B错误;该反应是前后气体分子数变化的反应,当压强不变了可以说明该反应达到平衡
状态,故C正确;反应进行至25min时,曲线A瞬间增大,B是连续的点,所以发生变化的原因是增加A的
浓度,故D正确; 故答案为B。
16.向密闭容器中充入SCl、Cl 和SCl ,发生反应 ,SCl 与SCl 的初始
2 2 2 2 2 2 2
消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是A.a为v(SCl )随温度的变化曲线
2
B.该反应的ΔH<0
C.200℃下反应一段时间,SCl 的物质的量增多
2 2
D.反应达到平衡后向体系中充入氦气,平衡不移动
【答案】C
【解析】图中A、B点处于平衡状态,由方程式 可知,v(SCl )=2v(S Cl),
2 2 2
则a为v(SCl )随温度的变化曲线,b为v(S Cl) 随温度的变化曲线,故A正确;图中A、B点处于平衡状态,
2 2 2
继续升高温度,SCl 的消耗速率大于SCl 的消耗速率的二倍,则平衡逆向移动,从而得出正反应为放热反
2 2 2
应,ΔH<0,故B正确;200℃下,SCl 的消耗速率小于SCl 的消耗速率的两倍,反应还没有平衡,反应继续
2 2 2
正向进行,反应一段时间,SCl 的物质的量减小,故C错误; 是气体体积不
2 2
变的反应,反应达到平衡后向体系中充入氦气,反应物和生成物浓度不变,平衡不移动,故D正确;故选C。
1. (2022·辽宁卷)某温度下,在 恒容密闭容器中 发生反应 ,有关
数据如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
【答案】B
【解析】反应开始一段时间,随着时间的延长,反应物浓度逐渐减小,产物Z的平均生成速率逐渐减小,
则 内Z的平均生成速率大于 内的,故 时,Z的浓度大于 ,A正确;
时生成的Z的物质的量为 , 时生成的Z的物质的量为
,故反应在 时已达到平衡,设达到平衡时生了 ,列
三段式:
根据 ,得 ,则Y的平衡浓度为 ,Z的平衡浓度为 ,平衡常数
, 时Y的浓度为 ,Z的浓度为 ,加入 后Z
的浓度变为 , ,反应正向进行,故 ,B错误;
反应生成的Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,相同条件下,体积之比等
于物质的量之比, ,故Y的体积分数始终约为33.3%,C正确;由B项分析可知 时反应处于
平衡状态,此时生成Z为 ,则X的转化量为 ,初始X的物质的量为 ,剩余X的物质的量
为 ,D正确;故选B。2. (2021·广东卷)反应 经历两步:① ;② 。反应体系中X、Y、Z的浓度c随时间t
的变化曲线如图所示。下列说法不正确的是
A. a为c(X)随t的变化曲线 B. t 时,
1
C. t 时,Y的消耗速率大于生成速率 D. t 后,
2 3
【答案】D
【解析】由题中信息可知,反应X=2Z经历两步:① ;② 。因此,图中呈不断减小趋势的a
线为X的浓度c随时间t的变化曲线,呈不断增加趋势的线为Z的浓度c随时间t的变化曲线,先增加后减小
的线为Y的浓度c随时间t的变化曲线。X是唯一的反应物,随着反应的发生,其浓度不断减小,因此,由图
可知,a为c(X)随t的变化曲线,A正确;由图可知,分别代表3种不同物质的曲线相交于t 时刻,因此,t 时
1 1
,B正确;由图中信息可知,t 时刻以后,Y的浓度仍在不断减小,说明t 时刻反应两步仍在
2 2
向正反应方向发生,而且反应①生成Y的速率小于反应②消耗Y的速率,即t 时Y的消耗速率大于生成速
2
率,C正确;由图可知,t 时刻反应①完成,X完全转化为Y,若无反应②发生,则 ,由于反应②
3
的发生,t 时刻Y浓度的变化量为 ,变化量之比等于化学计量数之比,所以Z的浓度的变化
3
量为 ,这种关系在t 后仍成立, 因此,D不正确。综上所述,本题选D。
3
3. (2021·河北卷)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、k
1 1 2 2 1 2
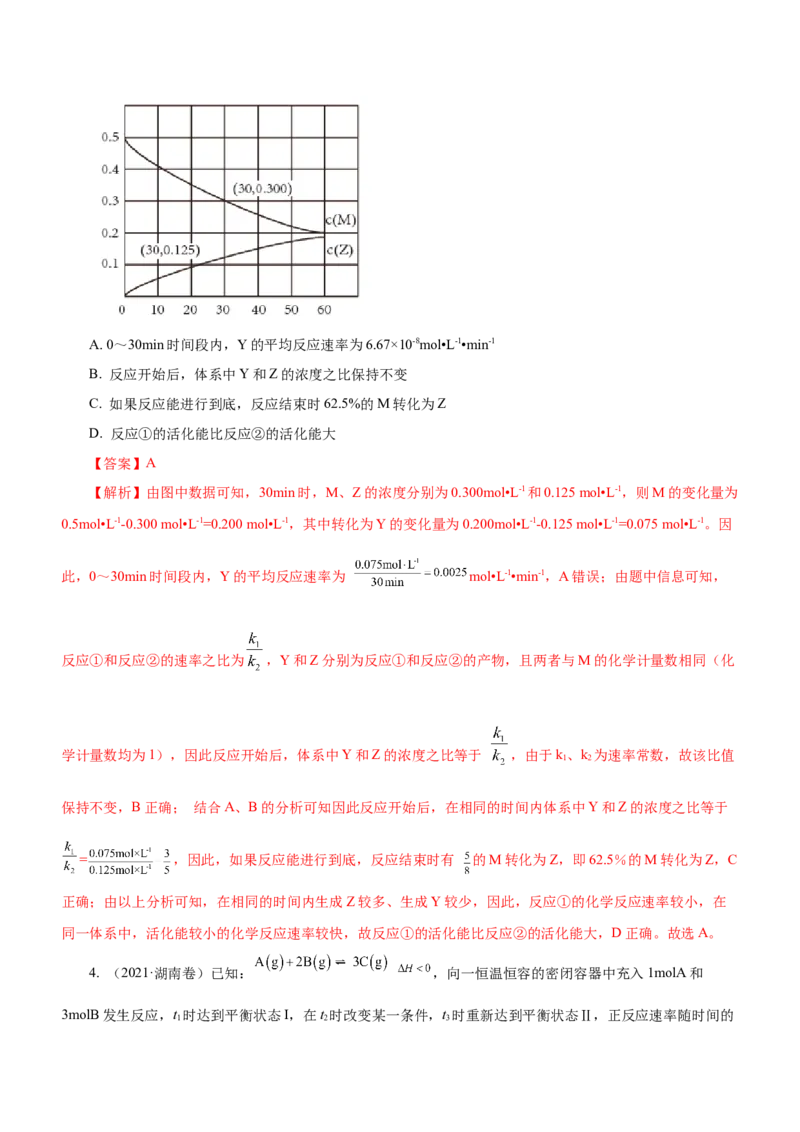
为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是( )A. 0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B. 反应开始后,体系中Y和Z的浓度之比保持不变
C. 如果反应能进行到底,反应结束时62.5%的M转化为Z
D. 反应①的活化能比反应②的活化能大
【答案】A
【解析】由图中数据可知,30min时,M、Z的浓度分别为0.300mol•L-1和0.125 mol•L-1,则M的变化量为
0.5mol•L-1-0.300 mol•L-1=0.200 mol•L-1,其中转化为Y的变化量为0.200mol•L-1-0.125 mol•L-1=0.075 mol•L-1。因
此,0~30min时间段内,Y的平均反应速率为 mol•L-1•min-1,A错误;由题中信息可知,
反应①和反应②的速率之比为 ,Y和Z分别为反应①和反应②的产物,且两者与M的化学计量数相同(化
学计量数均为1),因此反应开始后,体系中Y和Z的浓度之比等于 ,由于k、k 为速率常数,故该比值
1 2
保持不变,B正确; 结合A、B的分析可知因此反应开始后,在相同的时间内体系中Y和Z的浓度之比等于
= ,因此,如果反应能进行到底,反应结束时有 的M转化为Z,即62.5%的M转化为Z,C
正确;由以上分析可知,在相同的时间内生成Z较多、生成Y较少,因此,反应①的化学反应速率较小,在
同一体系中,活化能较小的化学反应速率较快,故反应①的活化能比反应②的活化能大,D正确。故选A。
4. (2021·湖南卷)已知: ,向一恒温恒容的密闭容器中充入1molA和
3molB发生反应,t 时达到平衡状态I,在t 时改变某一条件,t 时重新达到平衡状态Ⅱ,正反应速率随时间的
1 2 3变化如图所示。下列说法正确的是( )
A. 容器内压强不变,表明反应达到平衡 B. T 时改变的条件:向容器中加入C
2
C. 平衡时A的体积分数 : D. 平衡常数K:
【答案】BC
【解析】根据图像可知,向恒温恒容密闭容器中充入1molA和3molB发生反应,反应时间从开始到t 阶
1
段,正反应速率不断减小,所以平衡向正反应方向移动,t-t 时间段,正反应速率不变,反应达到平衡状态,
1 2
t-t 时间段,改变条件使正反应速率逐渐增大,平衡向逆反应方向移动,t 以后反应达到新的平衡状态,据此
2 3 3
结合图像分析解答。容器内发生的反应为A(g)+2B(g) 3C(g),该反应是气体分子数不变的可逆反应,所以在
恒温恒容条件下,气体的压强始终保持不变,则容器内压强不变,不能说明反应达到平衡状态,A错误;根据
图像变化曲线可知,t t 过程中,t 时 瞬间不变,平衡过程中不断增大,则说明反应向逆反应方向移动,
2 3 2
且不是“突变”图像,属于“渐变”过程,所以排除温度与催化剂等影响因素,改变的条件为:向容器中加入
C,B正确;t-t 时间段,改变条件使正反应速率逐渐增大,平衡向逆反应方向移动,达到新的平衡状态后,
2 3
生成A的量增大,总的物质的量不变,所以A的体积分数 增大,即A的体积分数 : (II)> (I),C正
确;平衡常数K与温度有关,因该反应在恒温条件下进行,所以K保持不变,D错误。故选BC。
5.(2020·江苏卷)CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
在恒压、反应物起始物质的量比 条件下,CH 和CO 的平衡转化率随温度变化的
4 2
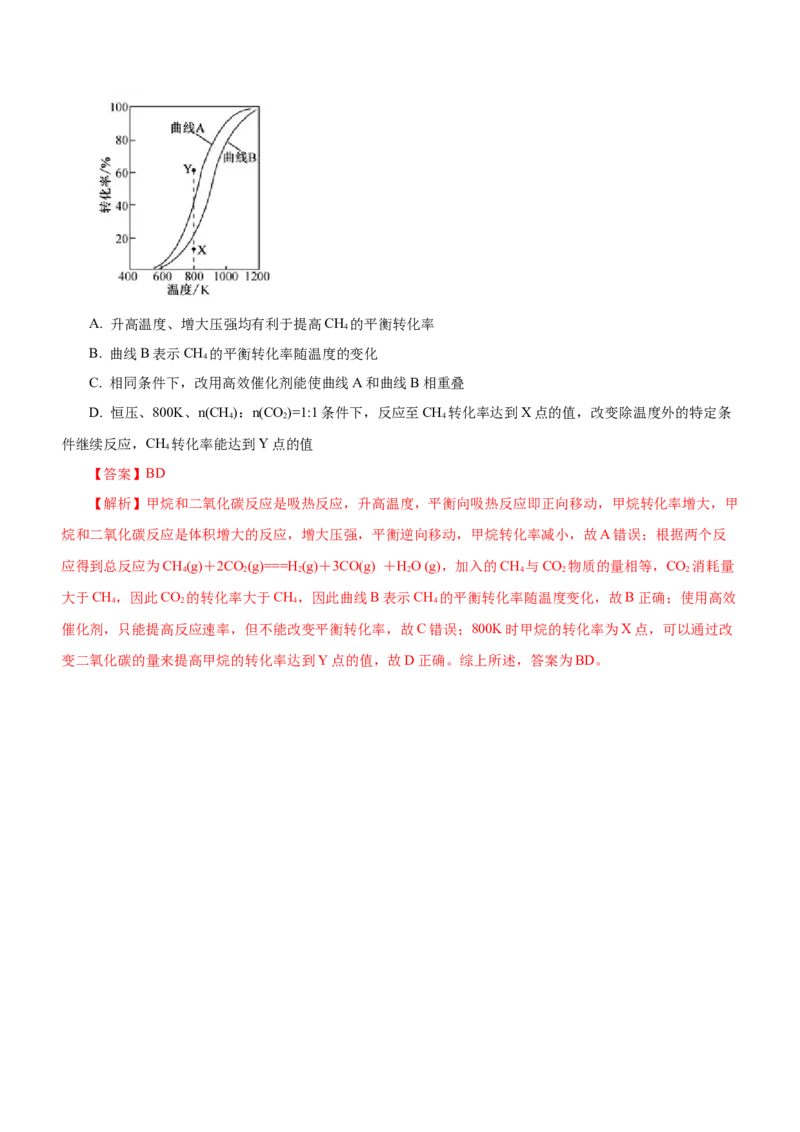
曲线如图所示。下列有关说法正确的是 ( )A. 升高温度、增大压强均有利于提高CH 的平衡转化率
4
B. 曲线B表示CH 的平衡转化率随温度的变化
4
C. 相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D. 恒压、800K、n(CH):n(CO)=1:1条件下,反应至CH 转化率达到X点的值,改变除温度外的特定条
4 2 4
件继续反应,CH 转化率能达到Y点的值
4
【答案】BD
【解析】甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应即正向移动,甲烷转化率增大,甲
烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,故A错误;根据两个反
应得到总反应为CH(g)+2CO(g)===H(g)+3CO(g) +HO (g),加入的CH 与CO 物质的量相等,CO 消耗量
4 2 2 2 4 2 2
大于CH,因此CO 的转化率大于CH,因此曲线B表示CH 的平衡转化率随温度变化,故B正确;使用高效
4 2 4 4
催化剂,只能提高反应速率,但不能改变平衡转化率,故C错误;800K时甲烷的转化率为X点,可以通过改
变二氧化碳的量来提高甲烷的转化率达到Y点的值,故D正确。综上所述,答案为BD。