文档内容
专题 10 化学反应机理与历程
一、选择题(本题包括35小题,每小题2分,共70分,每小题只有一个选项符合题意)
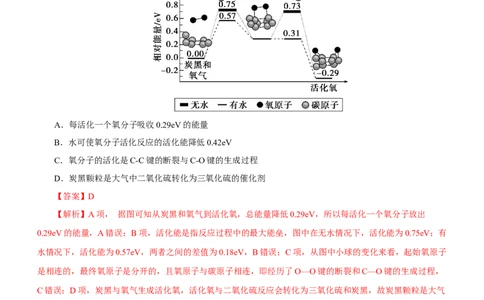
1.(2023·河南省新安县第一高级中学高三质检)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,
生成活化氧。活化过程的能量变化模拟计算结果如图所示。活化氧可以快速氧化二氧化硫。下列说法正确的是
( )
A.每活化一个氧分子吸收0.29eV的能量
B.水可使氧分子活化反应的活化能降低0.42eV
C.氧分子的活化是C-C键的断裂与C-O键的生成过程
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
【答案】D
【解析】A项, 据图可知从炭黑和氧气到活化氧,总能量降低0.29eV,所以每活化一个氧分子放出
0.29eV的能量,A错误;B项,活化能是指反应过程中的最大能垒,图中在无水情况下,活化能为0.75eV;有
水情况下,活化能为0.57eV,两者之间的差值为0.18eV,B错误;C项,从图中小球的变化来看,起始氧原子
是相连的,最终氧原子是分开的,且氧原子与碳原子相连,即经历了O—O键的断裂和C—O键的生成过程,
C错误;D项,炭黑与氧气生成活化氧,活化氧与二氧化硫反应会转化为三氧化硫和炭黑,故炭黑颗粒是大气
中二氧化硫转化为三氧化硫的催化剂,D正确;故选D。
2.利用铜-铈氧化物(xCuO·yCeO),Ce是活泼金属催化氧化除去H 中少量CO的可能机理如图所示。下
2 2
列说法正确的是( )A.反应(i)中Cu、Ce化合价均升高
B.铜的价电子排布为3d104s1,位于元素周期表d区
C.若用18O 参与反应,一段时间后,18O不可能现在铜–铈氧化物中
2
D.反应一段时间后催化剂活性下降,可能是CuO被还原成Cu所致
【答案】D
【解析】A项,反应(i)中CO作还原剂,[Ce-O-Cu]a+作氧化剂,转化为[Ce-□-Cu]a+,铜铈氧化物中Cu为+2
价、Ce为+4价,反应中Cu元素的化合价从+2变成+1,Ce元素的化合价从+4变成+3,化合价均降低,A错误;
B项,Cu为29号元素,价电子排布式为:3d104s1,位于元素周期表ds区,B错误;C项,由图可知,在反应
(ⅱ)中氧分子和催化剂铜-铈氧化物中的空位结合,反应后1个氧原子进入空位,故一段时间后,18O可能出现
在铜-铈氧化物中,C错误;D项,一氧化碳具有还原性,会把氧化铜还原为铜单质,反应一段时间后催化剂
活性下降,可能是CuO被还原成Cu所致,D正确;故选D。
3.(2023·江西省南昌二中高三模拟)氮及其化合物在工农业生产和生命活动中起着重要的作用,一种利用
电化学制备NH 的转化历程如图所示。下列说法错误的是( )
3
A.步骤Ⅱ发生的既是化合反应,也是氧化还原反应
B.步骤Ⅲ的化学方程式LiN+3HO=NH +3LiOH
3 2 3
C.该历程总反应为2N+6H O=4NH +3O
2 2 3 2D.由该历程说明N 的氧化性强于O
2 2
【答案】D
【解析】由图可知:步骤Ⅰ电解熔融的LiOH生成Li、水和氧气,步骤Ⅱ中Li和N 反应生成LiN,步骤
2 3
Ⅲ中LiN和水反应,生成LiOH和NH ,总反应为:2N+6H O=4NH +3O 。A项,步骤Ⅱ中Li和N 反应生成
3 3 2 2 3 2 2
LiN,既是化合反应,也是氧化还原反应,A正确;B项,步骤ⅢLiN和水反应,生成LiOH和NH ,化学方
3 3 3
程式LiN+3HO=NH +3LiOH,B正确;C项,由图象可知:反应物为氮气和水,产物为氨气和氧气,LiOH为
3 2 3
催化剂,由电子守恒和原子守恒可得总反应为:2N+6H O=4NH +3O ,C正确;D项,该反应历程中步骤Ⅰ是
2 2 3 2
通过电解发生,不能说明N 的氧化性强于O,D错误;故选D。
2 2
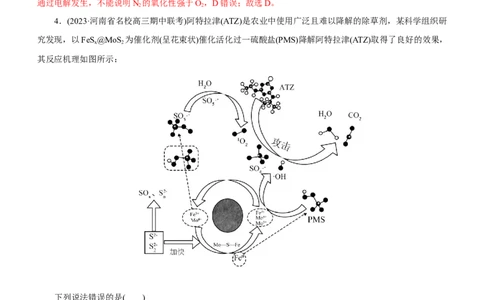
4.(2023·河南省名校高三期中联考)阿特拉津(ATZ)是农业中使用广泛且难以降解的除草剂,某科学组织研
究发现,以FeS@MoS 为催化剂(呈花束状)催化活化过一硫酸盐(PMS)降解阿特拉津(ATZ)取得了良好的效果,
x 2
其反应机理如图所示:
下列说法错误的是( )
A.PMS对应的酸为HSO ,该酸含有过氧键
2 5
B.生成SO ·-的途径之一为2SO ·-=2SO·-+1O
4 5 4 2
C.流程中直接氧化ATZ的微粒只有1O
2
D.S2-、 以及Fe0可以促进Fe2+再生
【答案】C
【解析】A项,由图可知,过一硫酸根离子为HSO -,对应的酸为HSO ,该酸可以看成是H-O-O-H中一
3 2 5个氢原子被-SO H代替的产物,所以含有过氧键,A正确;B项,图示有两种途径生成SO ·−,其中一种为
3 4
2SO ·−=2SO·−+1O,B正确;C项,据图可知,流程中直接氧化ATZ的微粒还有SO ·−、·OH,C错误;D项,
5 4 2 4
S2-、S2-以及Fe0具有还原性,可以还原Fe3+促进Fe2+再生,D正确;故选C。
2
5.(2023·福建省宁德市高三区域性学业质量检测)硼氢化钠(NaBH )被称为“万能还原剂”,能与水反应产
4
生H,NaBH 在催化剂钌( Ru)表面与水反应的历程如图所示:
2 4 44
下列说法不正确的是( )
A.元素钌( Ru)位于第5周期Ⅷ族
44
B.若将NaBH 中的H用D代替,反应后生成的气体中含有H、HD和D
4 2 2
C.过程③中产生1mol H,转移电子物质的量为2mol
2
D.NaBH 与水反应的离子方程式为:BH-+4H O=B(OH) -+4H ↑
4 4 2 4 2
【答案】C
【解析】根据硼氢化钠(NaBH )在催化剂作用下与水反应获取氢气的微观过程图可知,BH-和HO生成
4 4 2
B(OH) -和H,离子反应方程式为:BH-+4H O=B(OH) -+4H ↑。A项,元素钌( Ru)为44号元素,位于第五周
4 2 4 2 4 2 44
期第VIII族,A正确;B项,若用D代替H,生成的氢气原子重新组合,所以生成的氢气有H、HD、D,B
2 2
正确;C项,过程③中产生1mol H,反应为HB(OH)+H O=HB(OH)2+H ↑,转移电子物质的量为1mol,C不
2 2 2 2
正确;D项,根据上述分析,反应的离子方程式为:BH-+4H O=B(OH) -+4H ↑,D正确;故选C。
4 2 4 2
6.(2022·浙江省浙南名校高三联考)在催化剂作用下,HCOOH分解生成CO 和H 可能的反应机理如图所
2 2
示,研究发现:其他条件不变时,可以用HCOOK溶液代替HCOOH获得H。下列说法不正确的是( )
2A.HCOOD催化释氢反应除生成CO 外,还生成HD
2
B.A、B、C均为该反应过程中的中间产物
C.用HCOOK溶液代替HCOOH可以提高释放氢气的速率和氢气的纯度
D.催化剂催化过程中发生了共价键的断裂和形成
【答案】B
【解析】A项,根据图示可得HCOOH中的两个H结合产生H,则HCOOD除生成CO 外,还生成HD,
2 2
A正确;B项,由图示可得HCOOH分解经历了三步历程,物质A是先消耗再生成,属于催化剂,物质B、C
物质开始没有,先发生反应产生,然后又消耗,属于中间产物,B错误;C项,HCOOK是强电解质更容易产
生HCOO-和K+,更快的产生KH,KH与水反应生成H 和KOH,KOH可吸收掉CO,使生成的氢气纯度更高,
2 2
C正确;D项,根据图示可知:在催化剂催化过程中发生了共价键的断裂和形成,D正确;故选B。
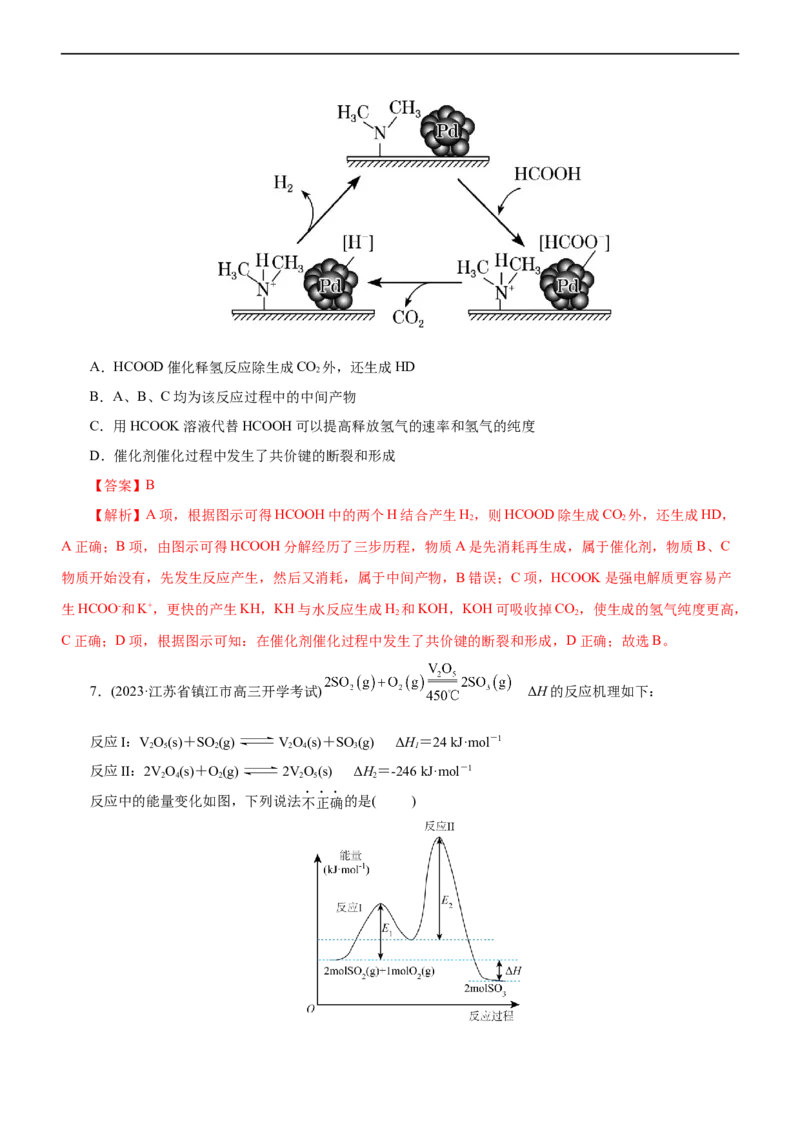
7.(2023·江苏省镇江市高三开学考试) ΔH的反应机理如下:
反应I:VO(s)+SO (g) VO(s)+SO (g) ΔH=24 kJ·mol-1
2 5 2 2 4 3 1
反应II:2VO(s)+O(g) 2VO(s) ΔH=-246 kJ·mol-1
2 4 2 2 5 2
反应中的能量变化如图,下列说法不正确的是( )A.ΔH=-198kJ·mol-1 B.反应I的ΔS>0
C.通入过量空气,可提高SO 的平衡转化率 D.反应速率由反应I决定
2
【答案】D
【解析】A项,由盖斯定律知,ΔH =2ΔH +ΔH = ,A正
1 2
确;B项,反应I可以发生,则ΔG=ΔH-TΔS<0(又因为反应的ΔH>0),故ΔS>0,B正确;C项,通入过量
空气,氧气浓度增大,平衡向正反应方向移动,二氧化硫的转化率增大,C正确;D项,反应的活化能越大,
反应速率越慢,从图上可以看出反应II的活化能大于反应I的活化能,故反应速率由反应II决定,D错误;故
选D。
8.(2023·甘肃省永昌县高三第一次模拟考试)我国学者利用催化剂催化丙烷氧化脱氢的历程如图(吸附在催
化剂表面的物质用标注)。下列说法正确的是( )
A.反应历程中第一步化学反应为决速步骤
B.催化剂改变了丙烷氧化脱氢的焓变(ΔH)
C.过渡态物质的稳定性:过渡态2小于过渡态1
D.吸附过程为吸热过程
【答案】A
【解析】A项,化学反应的决速步骤是慢反应,而活化能越大,反应的速率越慢,由图可知能垒(活化能)
最大的是C H*到过渡态I的能量,故第一步化学反应为决速步骤,A正确;B项,催化剂不能改反应的焓变
3 8
(ΔH),B错误;C项,物质具有的能量越低越稳定,故过渡态2更稳定,C错误;D项,由图可知吸附过程为
放热过程,D错误;故选A。
9.(2022·河南·宝丰县第一高级中学高三阶段练习)在亚纳米金属钯(Pd)团簇作用下,过氧化氢可以直接将
苯高效催化转化为苯酚,催化剂中掺杂碱金属离子可改变催化能力,反应历程如图(*表示吸附态,TS表示过
渡态),下列说法错误的是( )A.苯与HO 反应生成苯酚是放热反应
2 2
B.反应历程中,存在反应 +O*→
C.使用Pd-Na+催化剂后,每一步的产物均比使用Pd催化剂更稳定
D.其他条件相同时,使用掺杂Na+的催化剂,单位时间内可得更多苯酚产品
【答案】C
【解析】A项,由反应历程可知,苯酚和水的总能量低于HO 和苯的总能量,苯与HO 反应生成苯酚是
2 2 2 2
放热反应,A正确;B项,反应历程中存在 +H O+O* +H O,,即 +O*
2 2
,B正确;C项,第一步和第二步中使用Pd-Na+催化剂产物能量更高,不稳定,C错误;D项,使用Pd-
Na+催化剂后,每一步的活化能均比使用催化剂Pd低,反应速率加快,单位时间内可生成更多苯酚,D正确;
故选C。
10.(2023·湖南省益阳市高三质量检测)研究CHI与氯自由基(用Cl 表示)的反应有助于保护臭氧层。已知
3
CHI与Cl 反应有4条可能的反应路径,如图所示。图中TS表示过渡态∗,IM表示中间体。下列说法中正确的
3
是( ) ∗A.相同条件下,路径①的反应速率最快
B.路径④属于放热反应
C.路径②CHI*+Cl*= CH*+ICl是基元反应
3 3
D.过渡态中最稳定的是TS1,产物最稳定的是路径④的
【答案】B
【解析】A项,相同条件下,路径①的活化能最大,反应速率最慢,A不正确;B项,路径④的生成物总
能量小于反应物总能量,属于放热反应,B正确;C项,基元反应是指反应物一步直接转化为产物的反应,从
图中可以看出,路径②中存在中间产物,则CHI*+Cl*= CH*+ICl不是基元反应,C错误;D项,过渡态中
3 3
TS1的能量最高,稳定性最差,D错误;故选B。
11.(2023·河北省曲阳县第一高级中学高三摸底考试)利用水煤气(CO、H)制备甲烷(CH)的热化学方程式
2 4
为CO(g)+3H(g) CH(g)+HO(g) H。如图为在钴催化剂表面上进行该反应的历程,其中吸附在钴催化
2 4 2
剂表面上的物种用*标注。 △下列说法正确的是( )
A.该反应的ΔH =-243.5kJ·mol-1
B.反应过程中发生极性键和非极性键的断裂与生成
C.决定反应速率快慢的反应为CO*+2H*+2H(g)=C*+O*+2H*+2H (g)
2 2
D.若使用更高效催化剂,则该反应的ΔH的绝对值将增大
【答案】C
【解析】A项,该反应的ΔH =-206.2kJ·mol-1,A错误;B项,反应过程中无非极性键的生成,B错误;C
项,由图可知,CO*+2H*+2H(g) →过渡态Ⅰ的能垒最大,是该反应的决速步骤,化学方程式为
2
CO*+2H*+2H(g)=C*+O*+2H*+2H (g),C正确;D项,催化剂不改变反应的ΔH,D错误;故选C。
2 2
12.(2022·重庆市南开中学高三模拟检测)苯和液溴反应进程中的能量变化如图所示。已知:
①断裂化学键所需要的能量( ):
413 276 194 366
②
③
下列叙述不正确的是( )
A.该反应的
B.第二步是该反应的决速步骤
C.该反应的原子利用率约为
D.可用 溶液除去产物溴苯中混有的Br
2
【答案】A【解析】A项,∆H=反应物的总键能-生成物的总键能,已知Br (l)= Br (g) ∆H=+30 kJ·mol-1、断裂1mol
2 2
Br (g)需要能量为194kJ,则断裂1mol Br (l)需要能量为224kJ,该反应苯上断裂C-H键、Br (l)断裂Br-Br键,
2 2 2
生成C-Br键和H-Br键,则∆H=(413+164)-( 276+366)=-95kJ/mol,故A错误;B项,第二步的正活化能比第一
步的大,活化能越大反应速率越慢,最慢的那一步是该反应的决速步骤,故B正确;C项,由
,期望产物是溴苯其质量为157g,生成物有溴苯和HBr,总质量为
157+81=238g,则原子利用率约为 ,故C正确;D项,溴可与氢氧化钠反应,而溴苯不反应,
可用于除杂,故D正确;故选A。
13.(2022·上海市敬业中学高三模拟)H (g)+2ICl(g)→2HCl(g)+I (g)能量曲线如图。描述正确的是( )
2 2
A.反应①为放热反应,反应②为吸热反应
B.若加入催化剂可降低反应热
C.热化学方程式为H(g)+2ICl(g)→2HCl(g)+I (g)-218kJ
2 2
D.若反应的生成物为2HCl(g)+I (s),则反应热数值将变大
2
【答案】D
【解析】由图可知,反应物总能量大于生成物总能量,为放热反应,活化能越小,反应速率越快,且反应
中H、I元素的化合价变化。A项,根据图象可知,反应①和反应②中反应物总能量都大于生成物,则反应①、
反应②均为放热反应,△H均小于零,故A错误;B项,若加入催化剂,只能改变反应速率,不能改变反应热,
故B错误;C项,反应①、反应②总的能量变化为218kJ,根据盖斯定律可知,反应①、反应②的焓变之和为
△H=-218kJ•mol-1,即H(g)+2ICl(g)→2HCl(g)+I (g)+218kJ•mol-1,故C错误;D项,根据图象可知,反应①和
2 2
反应②中反应物总能量都大于生成物,图中反应②即I(g)+2HCl(g)=I (s)+2HCl(g),所以I(g)+2HCl(g)的能量高
2 2 2
于 I(s)+2HCl(g)的总能量,则反应热数值将变大,故D正确;故选D。
2
14.(2022·北京市101中学三模)下图是计算机模拟的在催化剂表面上水煤气变化的反应历程。吸附在催化剂表面的物种用“*”标注。
下列说法正确的是( )
A.①表示CO和HO从催化剂表面脱离的过程
2
B.②和④中化学键变化相同,因此吸收的能量相同
C.由图可知CO (g)+H O (g) =CO (g)+H(g)为吸热反应
2 2 2
D.相同条件下,反应速率④>②
【答案】B
【解析】A项,由题干反应历程图信息可知,①表示CO和HO在催化剂表面吸附的过程,A错误;B项,
2
由题干反应历程图信息可知,②和④中化学键变化相同均为HO中的H-O键,因此吸收的能量相同,B正确;
2
C项,由题干反应历程图信息可知,反应CO (g)+H O (g) =CO (g)+H(g)中反应物CO和HO的总能量高于生成
2 2 2 2
物CO 和H 的总能量,故为放热反应,C错误;D项,由题干反应历程图信息可知,过程②需要的活化能
2 2
(1.59-(-0.32))=1.91eV低于反应④的活化能(1.86-(0.16))=2.02eV,相同条件下,活化能越大,反应速率越慢,故
反应速率④<②,D错误;故选B。
15.(2023·浙江省十校联盟高三10月月考)自由基是化学键断裂时产生的含未成对电子的中间体,活泼自
由基与氧气的反应一直是科研人员的关注点。HNO自由基与O 反应过程的能量变化如图所示,下列说法正确
2
的是( )A.反应物的键能总和大于生成物的键能总和
B.该历程中最大正反应的活化能E =186.19 kJ∙mol-1
正
C.两种产物中P 更稳定,相同条件下Z转化为产物的速率:v(P )<v(P )
2 1 2
D.使用催化剂能提高产物P 的平衡产率
2
【答案】B
【解析】A项,从图中可以看出,反应物的总能量高于生成物的总能量,则反应物的键能总和小于生成物
的键能总和,A不正确;B项,该历程中最大正反应的活化能E =205.11 kJ∙mol-1-18.92 kJ∙mol-1=186.19
正
kJ∙mol-1,B正确;C项,两种产物中P 的能量更低,更稳定,相同条件下Z转化为产物的活化能E(P )<
2 1
E(P ),则Z转化为产物的速率:v(P )>v(P ),C不正确;D项,使用催化剂能降低反应在的活化能,加快反应
2 1 2
速率,但不能提高产物P 的平衡产率,D不正确;故选B。
2
16.由X、Y转化为M的反应历程如图所示,下列说法错误的是
A.①→②的总过程放热 B. M是CHCOOH
3C.反应过程中形成C-H键 D.反应X+Y→M的原子利用率为100%
【答案】C
【解析】A中根据反应物和生成物的能量变化判断反应类型;B中根据有机物的球棍模型判断判断化学式;
C中利用反应物和生成物的变化判断形成的键;D中利用反应方程式进行判断。A项,根据图像中反应物的能
量变化由高到低判断该反应为放热反应,A 正确;B 项,根据图像中的 M 的球棍模型判断化学式为
CHCOOH,故B正确;C项,根据图像中X判断是甲烷,Y是二氧化碳,两者形成乙酸,形成的是碳碳键、
3
氧氢键,故C不正确;D项,根据原子守恒甲烷和二氧化碳1:1完全反应生成乙酸,故原子利用率100%,故
D正确;故选C。
17.CO 选择性加氢制甲醇是解决温室应、发展绿色能源和实现经济可持续发展的重要途径之一。下图是
2
CO 催化加氢的反应机理图(“*”表示微粒吸附在催化剂表面)。有关说法错误的是
2
A.状态②、④和⑥为反应的过渡态
B.状态A到状态B的变化不能说明H 断键变成氢原子要放出能量
2
C.状态①到③发生的反应方程式为:CO*+H=HCOO*
2
D.更改催化剂不会改变状态③到状态④的能量大小
【答案】D
【解析】A项,过渡态是指反应物体系转变成产物体系过程中,经过的能量最高状态,由图示可知,状态
②、④和⑥为反应的过渡态,A正确;B项,“*”表示微粒吸附在催化剂表面,因此状态A到状态B的变化中,
3H(g)→6H*不能说明H 断键变成氢原子要放出能量,B正确;C项,由图示可知,状态①到③发生的反应方
2 2
程式为:CO*+H=HCOO*,C正确;D项,催化剂能改变反应的活化能,从而改变化学反应速率,因此更改
2
催化剂会改变状态③到状态④的能量大小,D错误;故选D。
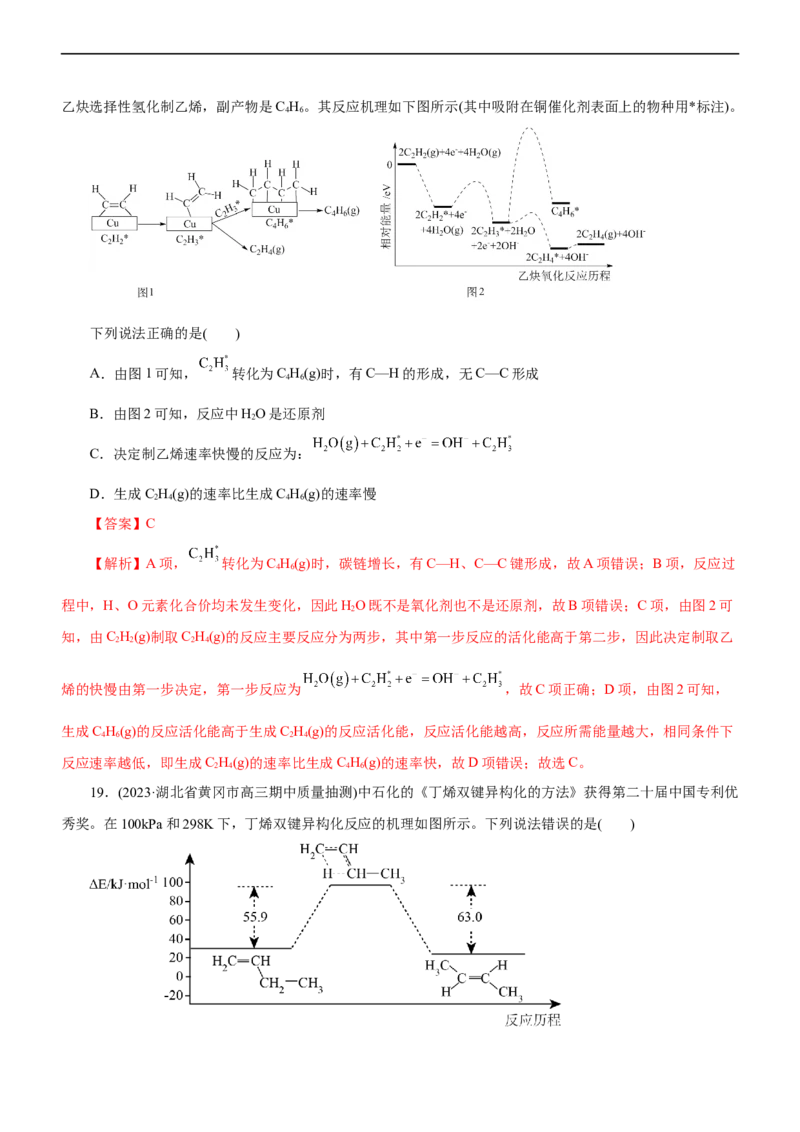
18.(2023·重庆市拔尖强基联盟联合高三检测)中国科学院于良等科学研究者实现了常温常压下利用铜催化乙炔选择性氢化制乙烯,副产物是C H。其反应机理如下图所示(其中吸附在铜催化剂表面上的物种用*标注)。
4 6
下列说法正确的是( )
A.由图1可知, 转化为C H(g)时,有C—H的形成,无C—C形成
4 6
B.由图2可知,反应中HO是还原剂
2
C.决定制乙烯速率快慢的反应为:
D.生成C H(g)的速率比生成C H(g)的速率慢
2 4 4 6
【答案】C
【解析】A项, 转化为C H(g)时,碳链增长,有C—H、C—C键形成,故A项错误;B项,反应过
4 6
程中,H、O元素化合价均未发生变化,因此HO既不是氧化剂也不是还原剂,故B项错误;C项,由图2可
2
知,由C H(g)制取C H(g)的反应主要反应分为两步,其中第一步反应的活化能高于第二步,因此决定制取乙
2 2 2 4
烯的快慢由第一步决定,第一步反应为 ,故C项正确;D项,由图2可知,
生成C H(g)的反应活化能高于生成C H(g)的反应活化能,反应活化能越高,反应所需能量越大,相同条件下
4 6 2 4
反应速率越低,即生成C H(g)的速率比生成C H(g)的速率快,故D项错误;故选C。
2 4 4 6
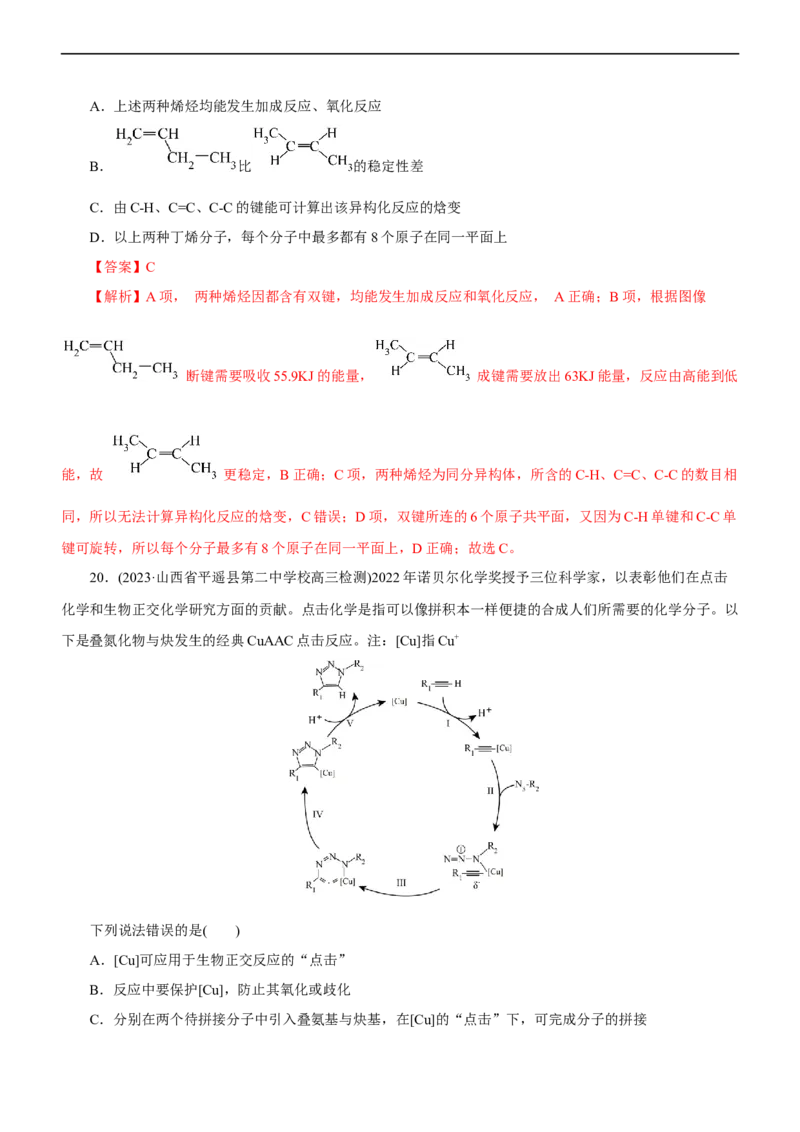
19.(2023·湖北省黄冈市高三期中质量抽测)中石化的《丁烯双键异构化的方法》获得第二十届中国专利优
秀奖。在100kPa和298K下,丁烯双键异构化反应的机理如图所示。下列说法错误的是( )A.上述两种烯烃均能发生加成反应、氧化反应
B. 比 的稳定性差
C.由C-H、C=C、C-C的键能可计算出该异构化反应的焓变
D.以上两种丁烯分子,每个分子中最多都有8个原子在同一平面上
【答案】C
【解析】A项, 两种烯烃因都含有双键,均能发生加成反应和氧化反应, A正确;B项,根据图像
断键需要吸收55.9KJ的能量, 成键需要放出63KJ能量,反应由高能到低
能,故 更稳定,B正确;C项,两种烯烃为同分异构体,所含的C-H、C=C、C-C的数目相
同,所以无法计算异构化反应的焓变,C错误;D项,双键所连的6个原子共平面,又因为C-H单键和C-C单
键可旋转,所以每个分子最多有8个原子在同一平面上,D正确;故选C。
20.(2023·山西省平遥县第二中学校高三检测)2022年诺贝尔化学奖授予三位科学家,以表彰他们在点击
化学和生物正交化学研究方面的贡献。点击化学是指可以像拼积本一样便捷的合成人们所需要的化学分子。以
下是叠氮化物与炔发生的经典CuAAC点击反应。注:[Cu]指Cu+
下列说法错误的是( )
A.[Cu]可应用于生物正交反应的“点击”
B.反应中要保护[Cu],防止其氧化或歧化
C.分别在两个待拼接分子中引入叠氨基与炔基,在[Cu]的“点击”下,可完成分子的拼接D.在反应历程中,存在共价键的断裂与离子键的生成
【答案】D
【解析】A项,根据题意,[Cu]可应用于生物正交反应的“点击”,A正确;B项,Cu+易被氧化和发生歧
化反应,反应中要保护[Cu],防止其氧化或歧化,B正确;C项,根据经典CuAAC点击反应历程,在[Cu]的
“点击”下,完成了叠氮化物与炔分子的拼接,C正确;D项,根据反应历程图,Cu+与炔分子反应使≡C-H
中的C-H键断裂以及后续反应中旧的共价键断裂和新的共价键生成,整个历程中无阴阳离子构成的离子化合
物,[Cu]与有机物以短线即共价键结合,则没有离子键的生成,D错误;故选D。
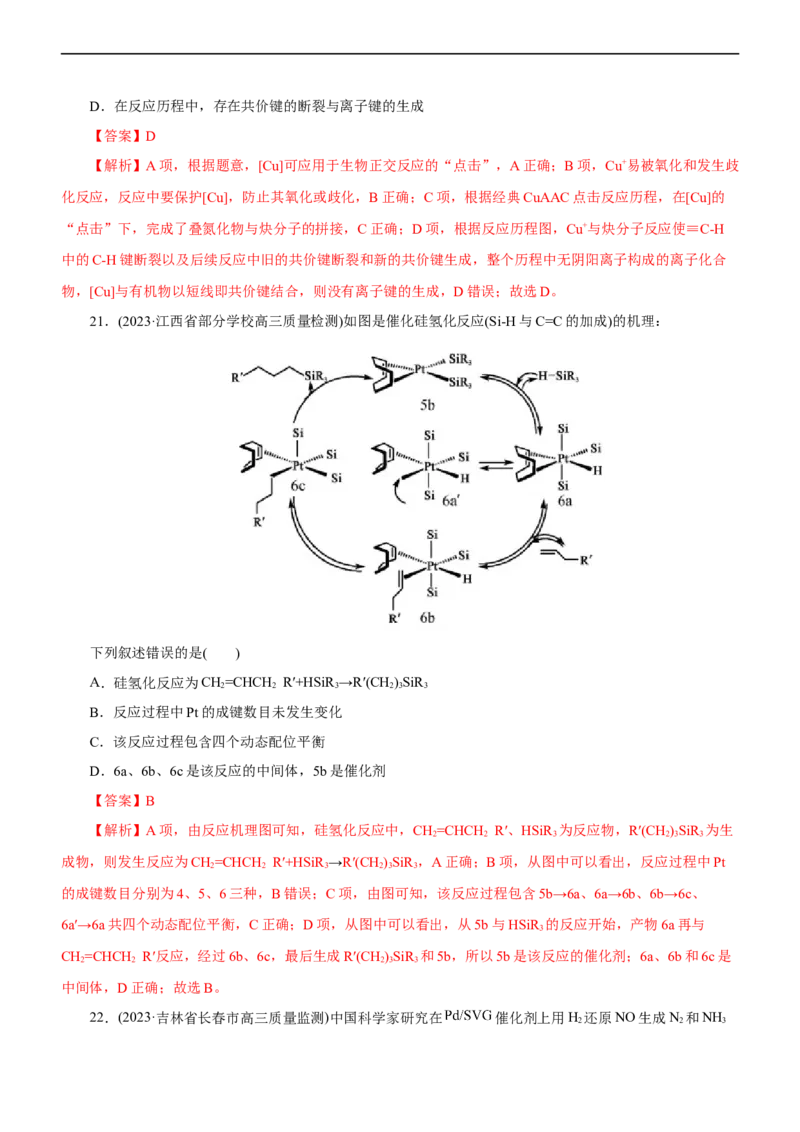
21.(2023·江西省部分学校高三质量检测)如图是催化硅氢化反应(Si-H与C=C的加成)的机理:
下列叙述错误的是( )
A.硅氢化反应为CH=CHCH R′+HSiR →R′(CH)SiR
2 2 3 2 3 3
B.反应过程中Pt的成键数目未发生变化
C.该反应过程包含四个动态配位平衡
D.6a、6b、6c是该反应的中间体,5b是催化剂
【答案】B
【解析】A项,由反应机理图可知,硅氢化反应中,CH=CHCH R′、HSiR 为反应物,R′(CH)SiR 为生
2 2 3 2 3 3
成物,则发生反应为CH=CHCH R′+HSiR →R′(CH)SiR ,A正确;B项,从图中可以看出,反应过程中Pt
2 2 3 2 3 3
的成键数目分别为4、5、6三种,B错误;C项,由图可知,该反应过程包含5b→6a、6a→6b、6b→6c、
6a′→6a共四个动态配位平衡,C正确;D项,从图中可以看出,从5b与HSiR 的反应开始,产物6a再与
3
CH=CHCH R′反应,经过6b、6c,最后生成R′(CH)SiR 和5b,所以5b是该反应的催化剂;6a、6b和6c是
2 2 2 3 3
中间体,D正确;故选B。
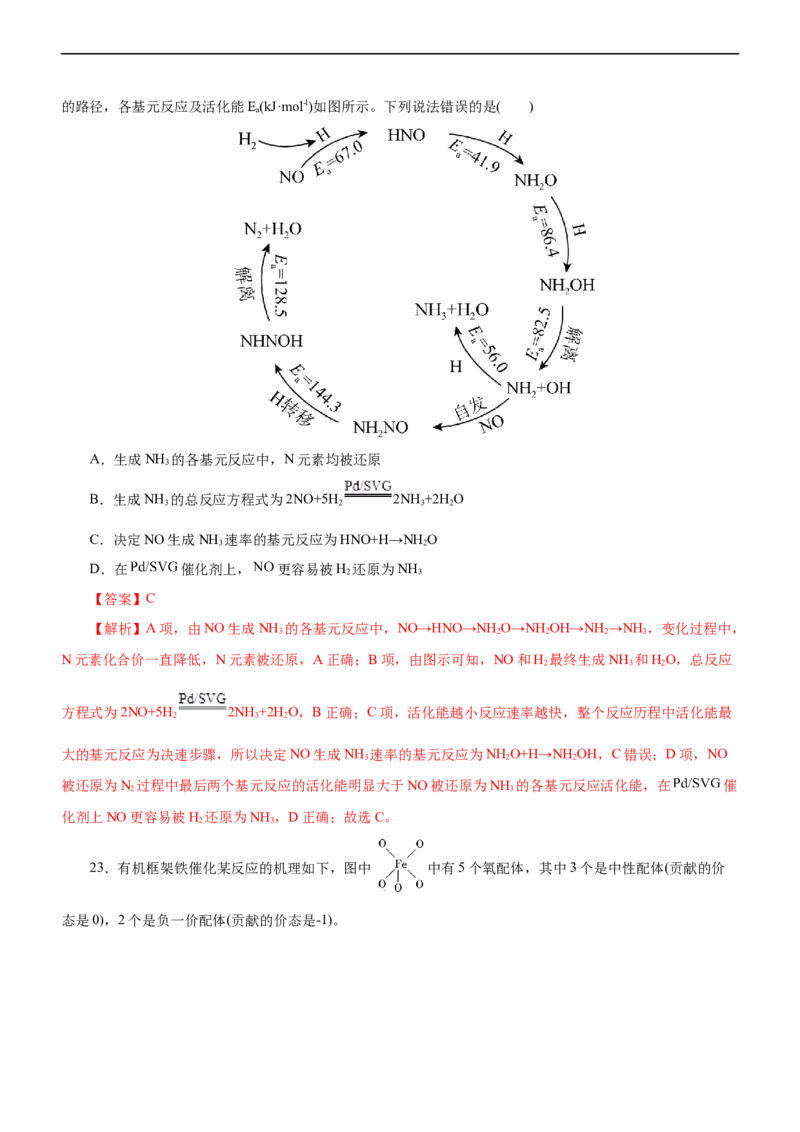
22.(2023·吉林省长春市高三质量监测)中国科学家研究在 催化剂上用H 还原NO生成N 和NH
2 2 3的路径,各基元反应及活化能E(kJ·mol-l)如图所示。下列说法错误的是( )
a
A.生成NH 的各基元反应中,N元素均被还原
3
B.生成NH 的总反应方程式为2NO+5H 2NH +2H O
3 2 3 2
C.决定NO生成NH 速率的基元反应为HNO+H→NH O
3 2
D.在 催化剂上, 更容易被H 还原为NH
2 3
【答案】C
【解析】A项,由NO生成NH 的各基元反应中,NO→HNO→NH O→NHOH→NH →NH ,变化过程中,
3 2 2 2 3
N元素化合价一直降低,N元素被还原,A正确;B项,由图示可知,NO和H 最终生成NH 和HO,总反应
2 3 2
方程式为2NO+5H 2NH +2H O,B正确;C项,活化能越小反应速率越快,整个反应历程中活化能最
2 3 2
大的基元反应为决速步骤,所以决定NO生成NH 速率的基元反应为NH O+H→NH OH,C错误;D项,NO
3 2 2
被还原为N 过程中最后两个基元反应的活化能明显大于NO被还原为NH 的各基元反应活化能,在 催
2 3
化剂上NO更容易被H 还原为NH ,D正确;故选C。
2 3
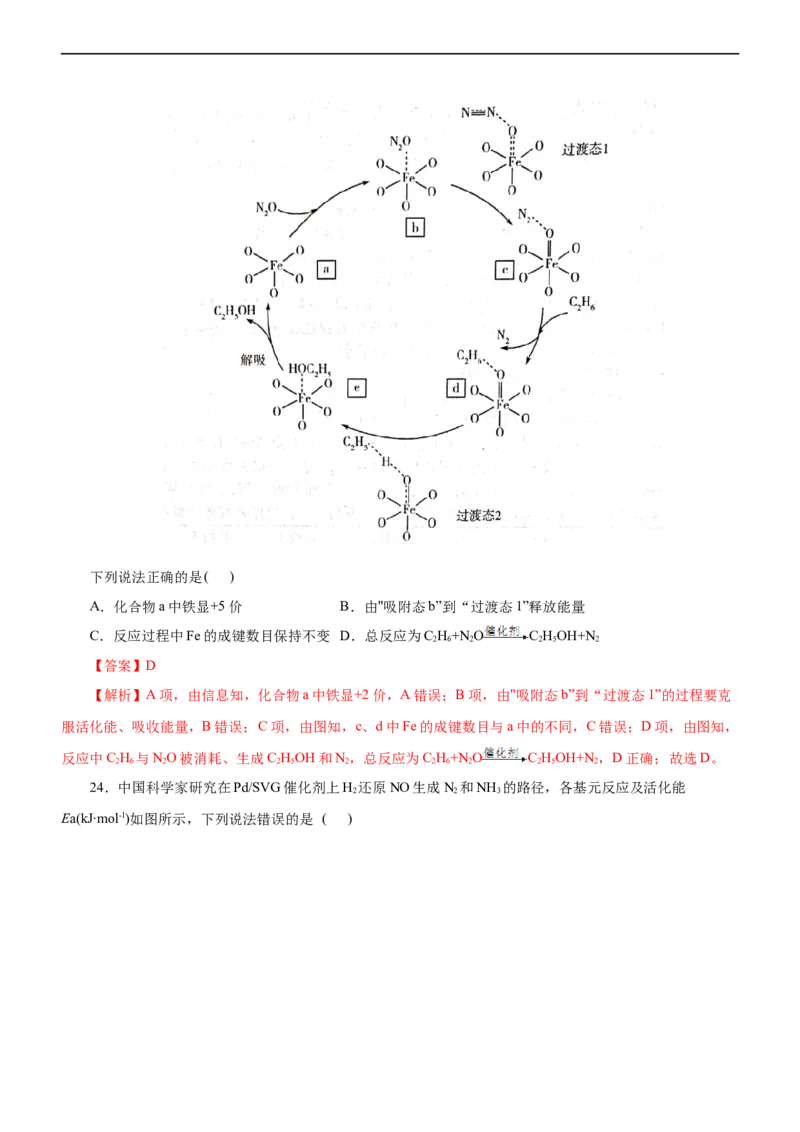
23.有机框架铁催化某反应的机理如下,图中 中有5个氧配体,其中3个是中性配体(贡献的价
态是0),2个是负一价配体(贡献的价态是-1)。下列说法正确的是( )
A.化合物a中铁显+5价 B.由"吸附态b”到“过渡态1”释放能量
C.反应过程中Fe的成键数目保持不变 D.总反应为C H+N O C HOH+N
2 6 2 2 5 2
【答案】D
【解析】A项,由信息知,化合物a中铁显+2价,A错误;B项,由"吸附态b”到“过渡态1”的过程要克
服活化能、吸收能量,B错误;C项,由图知,c、d中Fe的成键数目与a中的不同,C错误;D项,由图知,
反应中C H 与NO被消耗、生成C HOH和N,总反应为C H+N O C HOH+N ,D正确;故选D。
2 6 2 2 5 2 2 6 2 2 5 2
24.中国科学家研究在Pd/SVG催化剂上H 还原NO生成N 和NH 的路径,各基元反应及活化能
2 2 3
Ea(kJ∙mol-1)如图所示,下列说法错误的是 ( )A.生成NH 的各基元反应中,N元素均被还原
3
B.生成NH 的总反应方程式为 2NO+5H 2NH +2H O
3 2 3 2
C.在Pd/SVG催化剂上,NO更容易被H 还原为N
2 2
D.该过程中涉及极性键、非极性键的断裂和形成
【答案】C
【解析】A项,由图可知,生成氨气的各基元反应中,氮元素的化合价均降低被还原,故A正确;B项,
由图可知,生成氨气的总反应为在催化剂作用下,一氧化氮与氢气反应生成氨气和水,反应的化学方程式为
2NO+5H 2NH +2H O,故B正确;C项,由图可知,一氧化氮还原生成氮气的活化能大于还原生成
2 3 2
氨气的活化能,则在Pd/SVG催化剂的作用下,一氧化氮更容易生成氨气,故C错误;D项,由图可知,反应
中有氢氢非极性键和氮氧极性键发生断裂,有氮氮非极性键和氮氢、氢氧极性键的形成,故D正确;故选
C。
25.(2022·浙江省宁波市高三下学期模拟考试二模)Buchwald-Hartwig偶联反应(布赫瓦尔德-哈特维希反应)
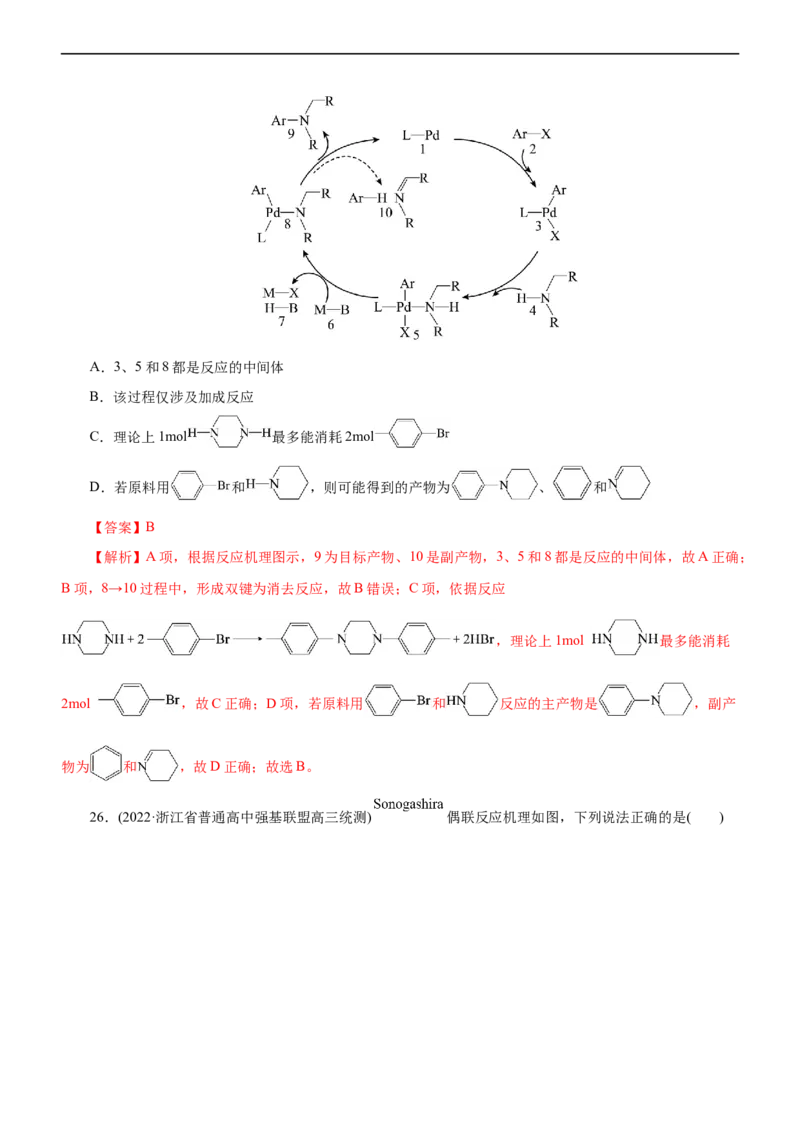
是合成芳胺的重要方法,反应机理如图(图中Ar表示芳香烃基,---表示为副反应)。下列说法不正确的是( )A.3、5和8都是反应的中间体
B.该过程仅涉及加成反应
C.理论上1mol 最多能消耗2mol
D.若原料用 和 ,则可能得到的产物为 、 和
【答案】B
【解析】A项,根据反应机理图示,9为目标产物、10是副产物,3、5和8都是反应的中间体,故A正确;
B项,8→10过程中,形成双键为消去反应,故B错误;C项,依据反应
,理论上1mol 最多能消耗
2mol ,故C正确;D项,若原料用 和 反应的主产物是 ,副产
物为 和 ,故D正确;故选B。
26.(2022·浙江省普通高中强基联盟高三统测) 偶联反应机理如图,下列说法正确的是( )A.若原料用苯乙炔和CH=CHBr,则产物是
2
B.R X变为 发生了氧化反应
1
C.该反应只用了一种催化剂LnPd
D.适量添加NaCO 有利于提高产率
2 3
【答案】D
【解析】由图知,在催化剂作用下, 。A项,苯环应和碳碳三键相连,
碳碳三键和碳碳双键应换一个位置,A错误;B项,LnPd中元素化合价升高、发生氧化反应,有机物发生了
还原反应,B错误;C项,由图知,CuX也参与循环、CuX也是催化剂,C错误;D项,由图知,在催化剂作
用下, , 能吸收HX,有利于反应向右进行、利于提高产率,D
正确;故选D。
27.(2022·浙江省绍兴市高三选考科目适应性考试二模)某实验小组设计一种固定CO 的方法,下列说法不
2
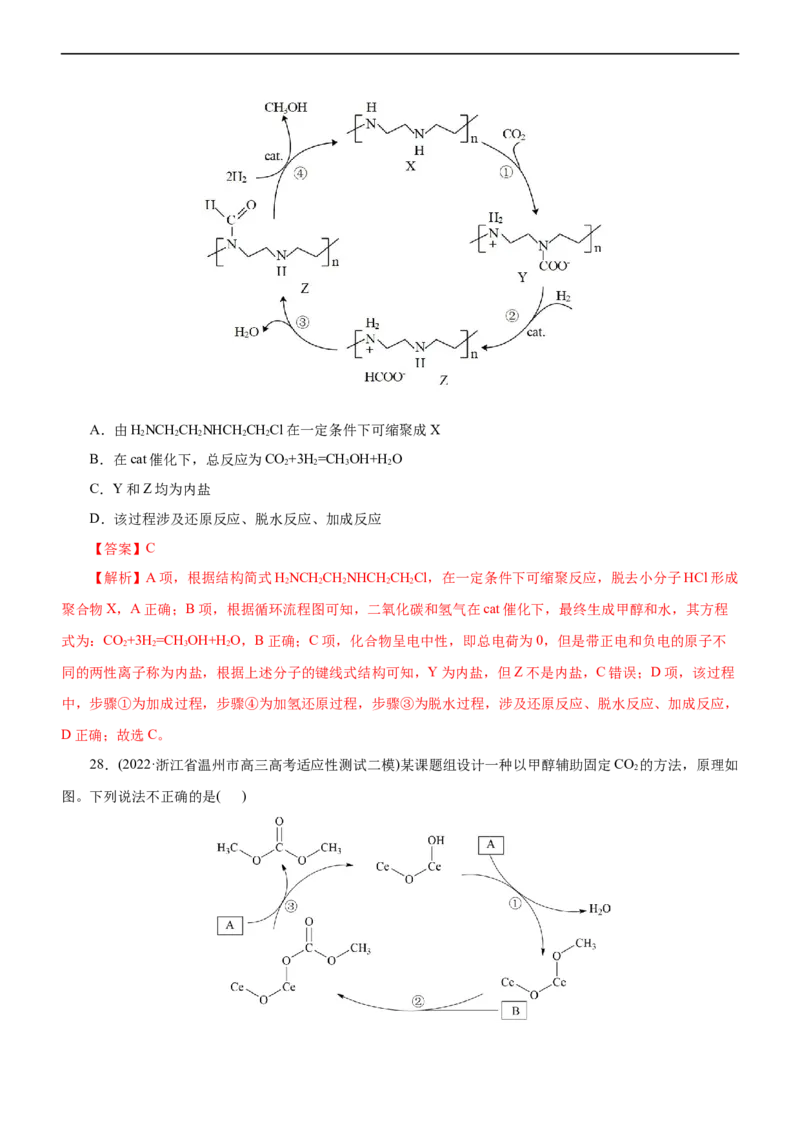
正确的是( )A.由HNCH CHNHCH CHCl在一定条件下可缩聚成X
2 2 2 2 2
B.在cat催化下,总反应为CO+3H =CH OH+H O
2 2 3 2
C.Y和Z均为内盐
D.该过程涉及还原反应、脱水反应、加成反应
【答案】C
【解析】A项,根据结构简式HNCH CHNHCH CHCl,在一定条件下可缩聚反应,脱去小分子HCl形成
2 2 2 2 2
聚合物X,A正确;B项,根据循环流程图可知,二氧化碳和氢气在cat催化下,最终生成甲醇和水,其方程
式为:CO+3H =CH OH+H O,B正确;C项,化合物呈电中性,即总电荷为0,但是带正电和负电的原子不
2 2 3 2
同的两性离子称为内盐,根据上述分子的键线式结构可知,Y为内盐,但Z不是内盐,C错误;D项,该过程
中,步骤①为加成过程,步骤④为加氢还原过程,步骤③为脱水过程,涉及还原反应、脱水反应、加成反应,
D正确;故选C。
28.(2022·浙江省温州市高三高考适应性测试二模)某课题组设计一种以甲醇辅助固定CO 的方法,原理如
2
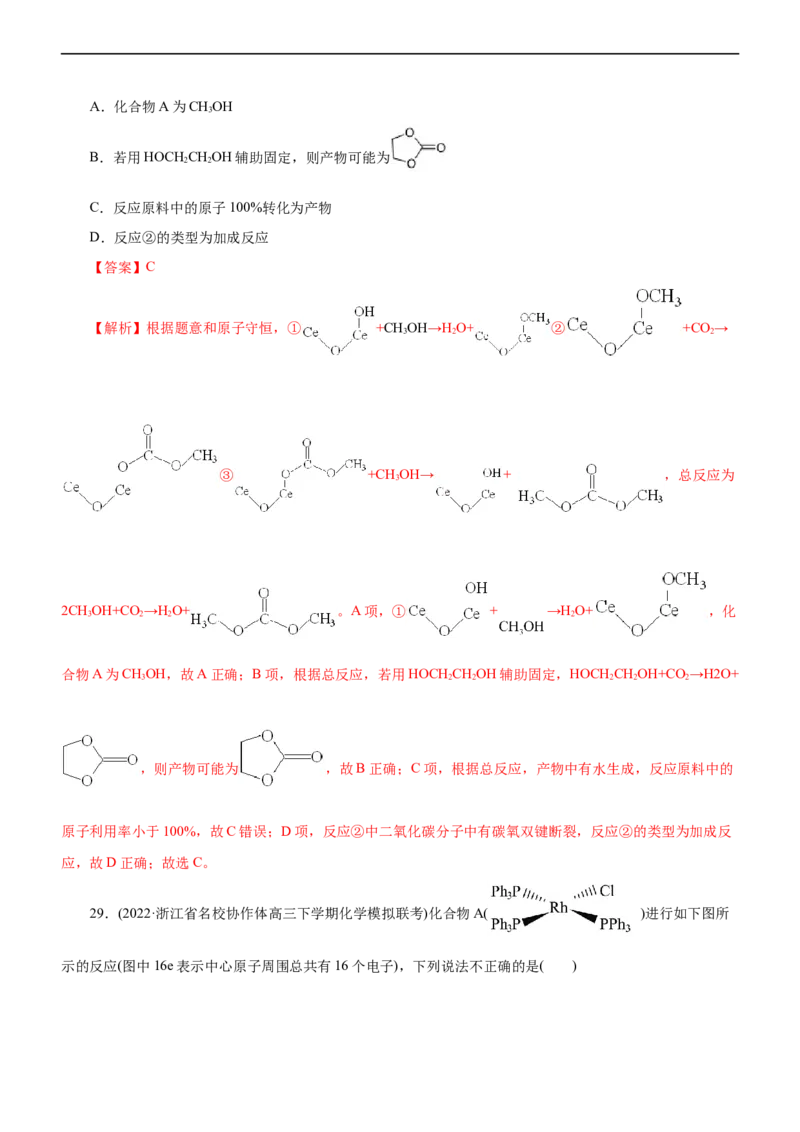
图。下列说法不正确的是( )A.化合物A为CHOH
3
B.若用HOCH CHOH辅助固定,则产物可能为
2 2
C.反应原料中的原子100%转化为产物
D.反应②的类型为加成反应
【答案】C
【解析】根据题意和原子守恒,① +CHOH→HO+ ② +CO →
3 2 2
③ +CH OH→ + ,总反应为
3
2CHOH+CO →HO+ 。A项,① + →HO+ ,化
3 2 2 2
合物A为CHOH,故A正确;B项,根据总反应,若用HOCH CHOH辅助固定,HOCH CHOH+CO →H2O+
3 2 2 2 2 2
,则产物可能为 ,故B正确;C项,根据总反应,产物中有水生成,反应原料中的
原子利用率小于100%,故C错误;D项,反应②中二氧化碳分子中有碳氧双键断裂,反应②的类型为加成反
应,故D正确;故选C。
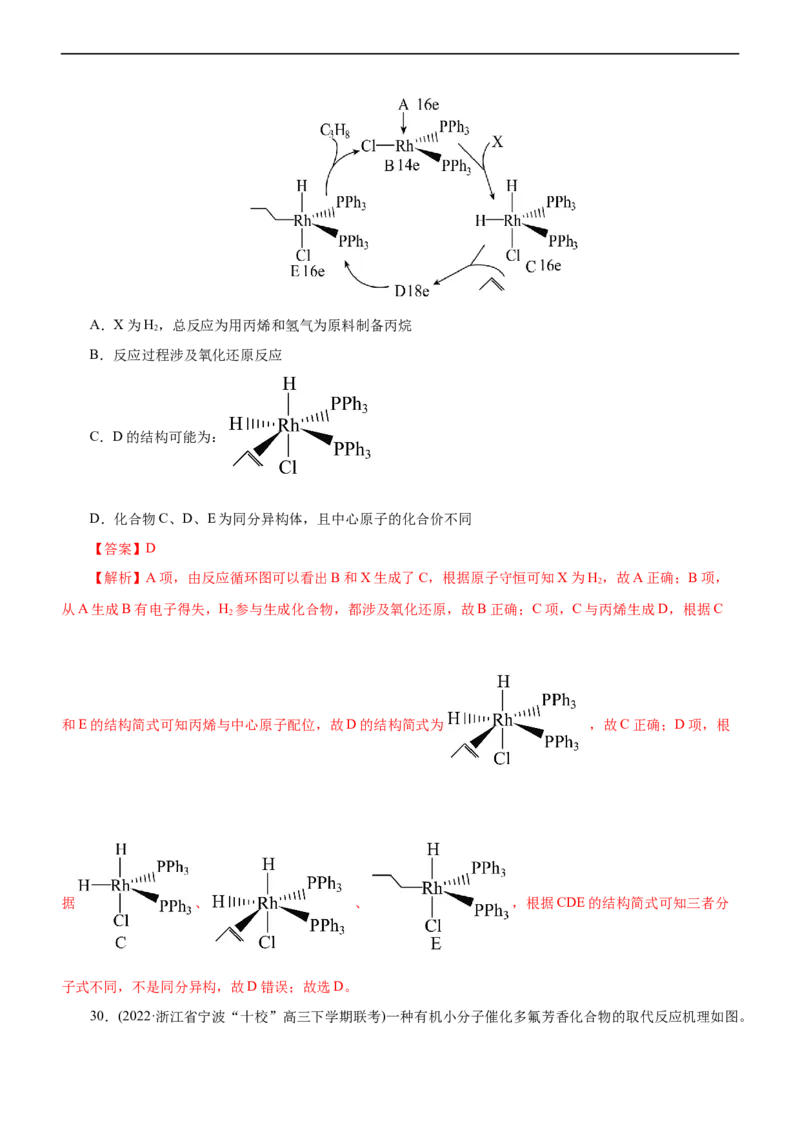
29.(2022·浙江省名校协作体高三下学期化学模拟联考)化合物A( )进行如下图所
示的反应(图中16e表示中心原子周围总共有16个电子),下列说法不正确的是( )A.X为H,总反应为用丙烯和氢气为原料制备丙烷
2
B.反应过程涉及氧化还原反应
C.D的结构可能为:
D.化合物C、D、E为同分异构体,且中心原子的化合价不同
【答案】D
【解析】A项,由反应循环图可以看出B和X生成了C,根据原子守恒可知X为H,故A正确;B项,
2
从A生成B有电子得失,H 参与生成化合物,都涉及氧化还原,故B正确;C项,C与丙烯生成D,根据C
2
和E的结构简式可知丙烯与中心原子配位,故D的结构简式为 ,故C正确;D项,根
据 、 、 ,根据CDE的结构简式可知三者分
子式不同,不是同分异构,故D错误;故选D。
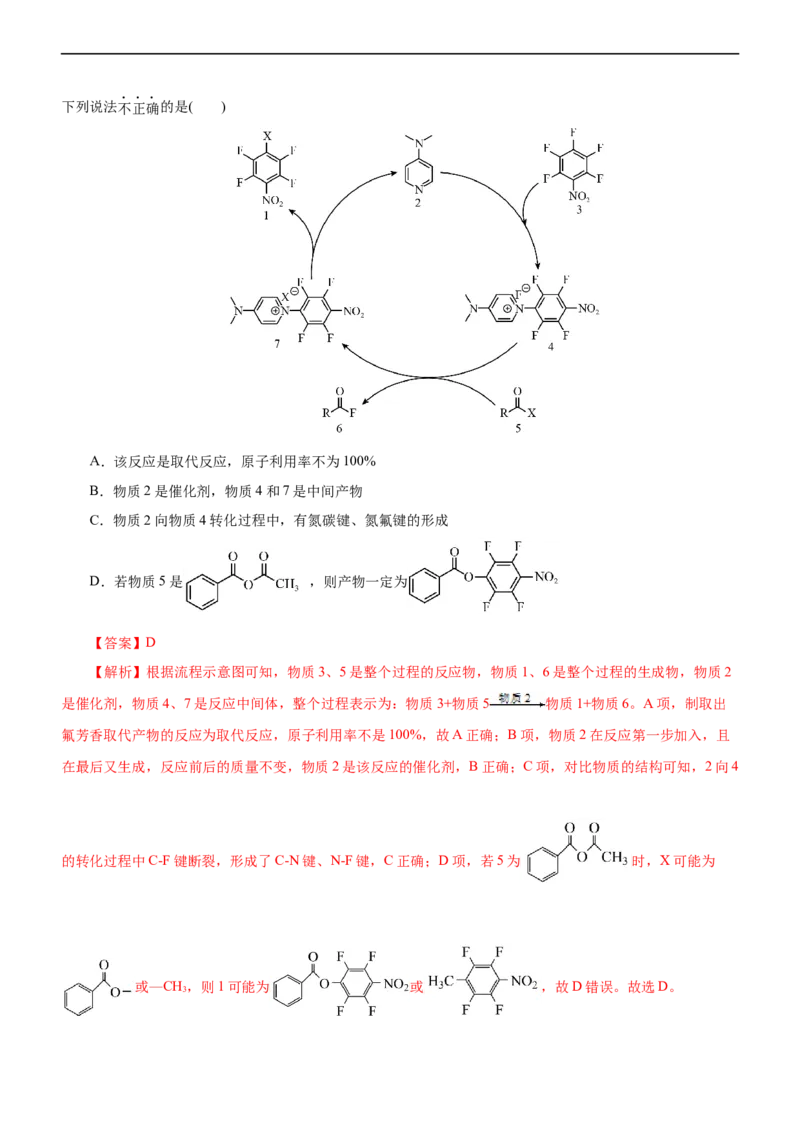
30.(2022·浙江省宁波“十校”高三下学期联考)一种有机小分子催化多氟芳香化合物的取代反应机理如图。下列说法不正确的是( )
A.该反应是取代反应,原子利用率不为100%
B.物质2是催化剂,物质4和7是中间产物
C.物质2向物质4转化过程中,有氮碳键、氮氟键的形成
D.若物质5是 ,则产物一定为
【答案】D
【解析】根据流程示意图可知,物质3、5是整个过程的反应物,物质1、6是整个过程的生成物,物质2
是催化剂,物质4、7是反应中间体,整个过程表示为:物质3+物质5 物质1+物质6。A项,制取出
氟芳香取代产物的反应为取代反应,原子利用率不是100%,故A正确;B项,物质2在反应第一步加入,且
在最后又生成,反应前后的质量不变,物质2是该反应的催化剂,B正确;C项,对比物质的结构可知,2向4
的转化过程中C-F键断裂,形成了C-N键、N-F键,C正确;D项,若5为 时,X可能为
或—CH,则1可能为 或 ,故D错误。故选D。
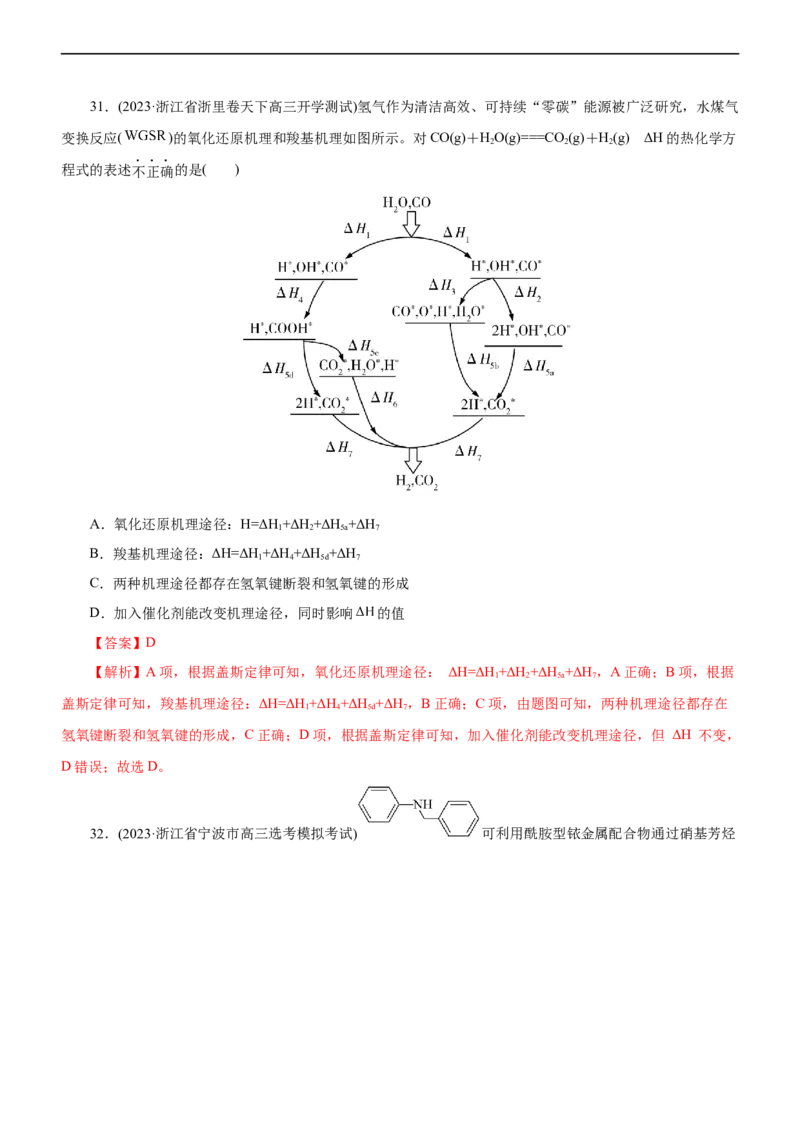
331.(2023·浙江省浙里卷天下高三开学测试)氢气作为清洁高效、可持续“零碳”能源被广泛研究,水煤气
变换反应( )的氧化还原机理和羧基机理如图所示。对CO(g)+HO(g)===CO (g)+H(g) ΔH的热化学方
2 2 2
程式的表述不正确的是( )
A.氧化还原机理途径:H=ΔH+ΔH +ΔH +ΔH
1 2 5a 7
B.羧基机理途径:ΔH=ΔH+ΔH +ΔH +ΔH
1 4 5d 7
C.两种机理途径都存在氢氧键断裂和氢氧键的形成
D.加入催化剂能改变机理途径,同时影响 的值
【答案】D
【解析】A项,根据盖斯定律可知,氧化还原机理途径: ΔH=ΔH+ΔH +ΔH +ΔH ,A正确;B项,根据
1 2 5a 7
盖斯定律可知,羧基机理途径:ΔH=ΔH+ΔH +ΔH +ΔH ,B正确;C项,由题图可知,两种机理途径都存在
1 4 5d 7
氢氧键断裂和氢氧键的形成,C正确;D项,根据盖斯定律可知,加入催化剂能改变机理途径,但 ΔH 不变,
D错误;故选D。
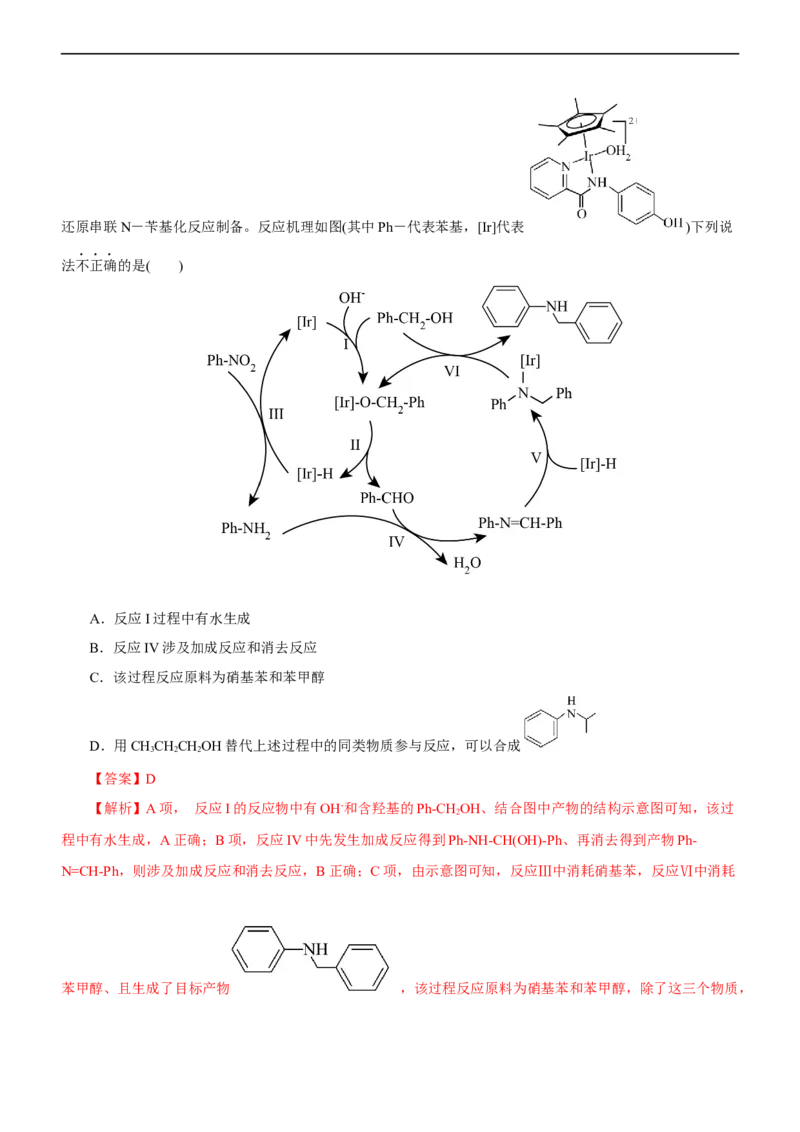
32.(2023·浙江省宁波市高三选考模拟考试) 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表 )下列说
法不正确的是( )
A.反应I过程中有水生成
B.反应IV涉及加成反应和消去反应
C.该过程反应原料为硝基苯和苯甲醇
D.用CHCHCHOH替代上述过程中的同类物质参与反应,可以合成
3 2 2
【答案】D
【解析】A项, 反应I的反应物中有OH-和含羟基的Ph-CH OH、结合图中产物的结构示意图可知,该过
2
程中有水生成,A正确;B项,反应IV中先发生加成反应得到Ph-NH-CH(OH)-Ph、再消去得到产物Ph-
N=CH-Ph,则涉及加成反应和消去反应,B正确;C项,由示意图可知,反应Ⅲ中消耗硝基苯,反应Ⅵ中消耗
苯甲醇、且生成了目标产物 ,该过程反应原料为硝基苯和苯甲醇,除了这三个物质,其余含苯环的有机物均为中间产物,C正确;D项,用CHCHCHOH替代上述过程中的同类物质参与反应,
3 2 2
可以合成 ,D不正确;故选D。
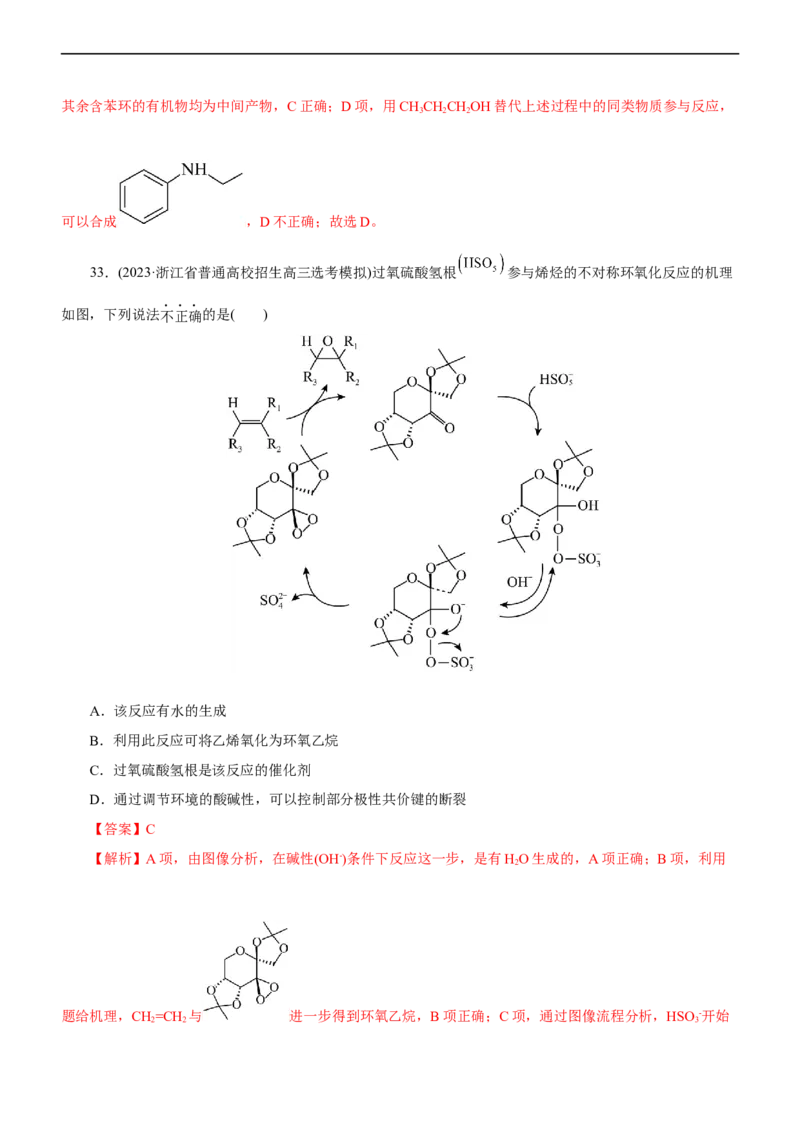
33.(2023·浙江省普通高校招生高三选考模拟)过氧硫酸氢根 参与烯烃的不对称环氧化反应的机理
如图,下列说法不正确的是( )
A.该反应有水的生成
B.利用此反应可将乙烯氧化为环氧乙烷
C.过氧硫酸氢根是该反应的催化剂
D.通过调节环境的酸碱性,可以控制部分极性共价键的断裂
【答案】C
【解析】A项,由图像分析,在碱性(OH-)条件下反应这一步,是有HO生成的,A项正确;B项,利用
2
题给机理,CH=CH 与 进一步得到环氧乙烷,B项正确;C项,通过图像流程分析,HSO -开始
2 2 3参与反应最终转为SO 2-,不是催化剂,C项错误;D项,通过分析 这个过程,可
4
知通过调节环境的碱性,使得有机物中的-OH间的极性共价键断裂,D项正确;故选C。
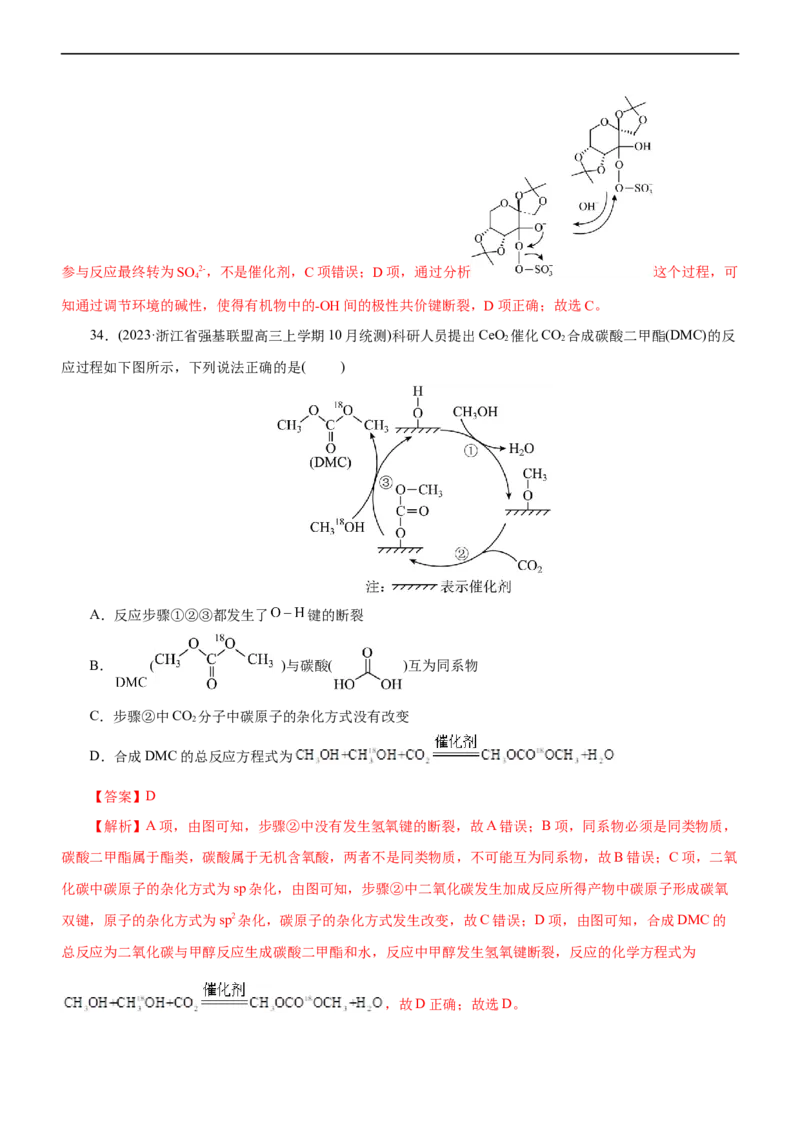
34.(2023·浙江省强基联盟高三上学期10月统测)科研人员提出CeO 催化CO 合成碳酸二甲酯(DMC)的反
2 2
应过程如下图所示,下列说法正确的是( )
A.反应步骤①②③都发生了 键的断裂
B. ( )与碳酸( )互为同系物
C.步骤②中CO 分子中碳原子的杂化方式没有改变
2
D.合成DMC的总反应方程式为
【答案】D
【解析】A项,由图可知,步骤②中没有发生氢氧键的断裂,故A错误;B项,同系物必须是同类物质,
碳酸二甲酯属于酯类,碳酸属于无机含氧酸,两者不是同类物质,不可能互为同系物,故B错误;C项,二氧
化碳中碳原子的杂化方式为sp杂化,由图可知,步骤②中二氧化碳发生加成反应所得产物中碳原子形成碳氧
双键,原子的杂化方式为sp2杂化,碳原子的杂化方式发生改变,故C错误;D项,由图可知,合成DMC的
总反应为二氧化碳与甲醇反应生成碳酸二甲酯和水,反应中甲醇发生氢氧键断裂,反应的化学方程式为
,故D正确;故选D。35.(2023·浙江省浙南名校联盟高三上学期第一次联考)以钒化合物作催化剂制备高纯度次氯酸的机理如图,
已知钒元素V最高化合价为+5价,N(His404)、 N(His496)为氨基酸,下列说法不正确的是( )
A.反应①④中,都形成配位键,都有氢氧键的断裂和形成
B.反应过程中,钒化合物甲是催化剂,乙、丙、丁、戊是中间产物
C.在该催化循环过程中,中心原子V的化合价和VSEPR模型发生了改变
D.此图钒化合物的每一次循环使无机物发生的净反应:HO+Cl-+H+=HOCl+H O
2 2 2
【答案】C
【解析】A项,反应①中HO 断裂H-O键,-OOH与V形成配位键,反应④HO断裂H-O键,-OH与V
2 2 2
形成配位键,故A正确;B项,反应过程中,化合物甲先和HO 反应,经过一系列反应又生成了甲,因此该
2 2
机理中化合物甲作催化剂,乙、丙、丁、戊是中间产物,故B正确;C项,反应过程中,中心原子V的共用电
子对与孤对电子数不变,则VSEPR模型不变,故C错误;D项,根据图中的转化关系得到制备机理的总反应
的方程式为:HO+Cl-+H+=HClO+H O,故D正确;故选C。
2 2 2
二、非选择题(本题包括4小题,共30分)
36.(12分)(2023·安徽省A10联盟高三阶段考试)H S、NO、SO 是有害气体,处理有害气体的工艺原理有
2 2
以下几种:
(1)一种脱除HS回收硫工艺的两个阶段主要反应分别如下:
2
第一阶段:2HS(g)+3O(g) 2SO (g)+2HO(g)
2 2 2 2
第二阶段:4HS(g)+2SO (g) 3S(g)+4HO(g)
2 2 2 2理论上,该工艺需控制第二阶段与第一阶段参加反应的HS的物质的量之比 _______,若
2
过小,导致的结果是_______。
(2)有氧条件下,NO在催化剂作用下可被NH 还原为N。
3 2
①在钒基催化剂作用下的脱硝反应机理如上图所示,该机理中体现氧化性的微粒有_______种。
②由上图可知,其总反应方程式为_______。
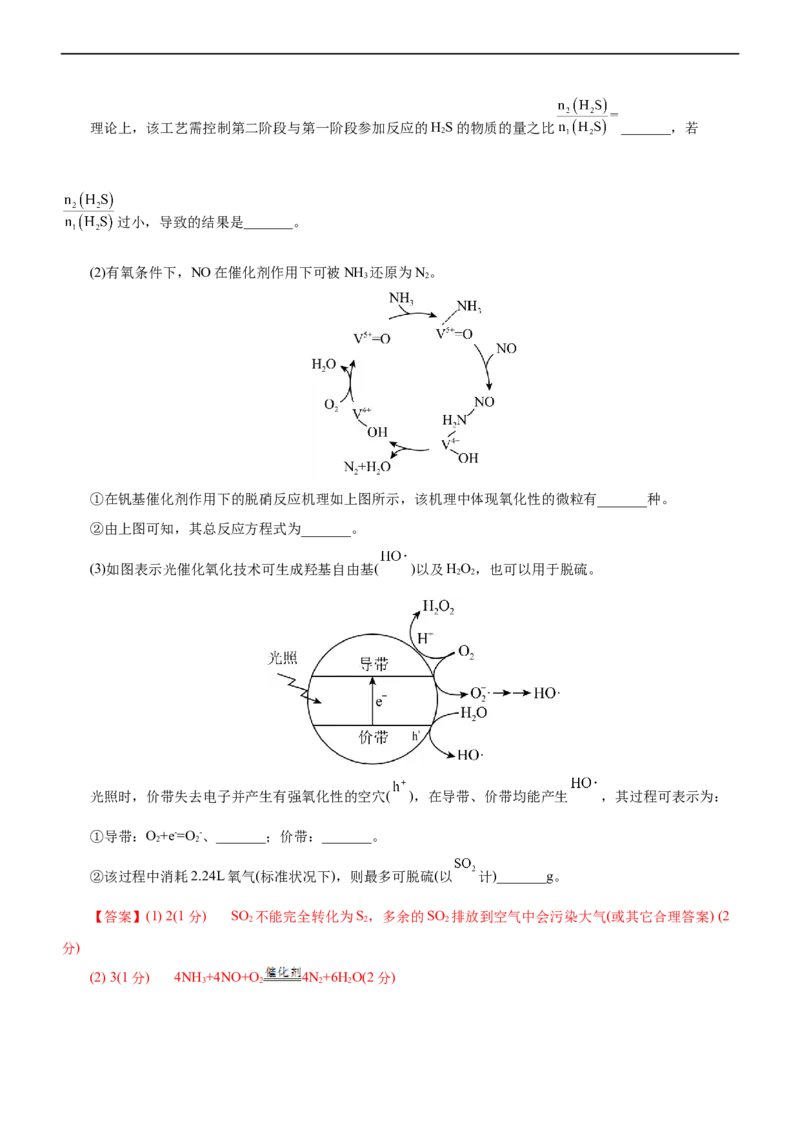
(3)如图表示光催化氧化技术可生成羟基自由基( )以及HO,也可以用于脱硫。
2 2
光照时,价带失去电子并产生有强氧化性的空穴( ),在导带、价带均能产生 ,其过程可表示为:
①导带:O+e-=O -、_______;价带:_______。
2 2
②该过程中消耗2.24L氧气(标准状况下),则最多可脱硫(以 计)_______g。
【答案】(1) 2(1分) SO 不能完全转化为S,多余的SO 排放到空气中会污染大气(或其它合理答案) (2
2 2 2
分)
(2) 3(1分) 4NH +4NO+O 4N+6H O(2分)
3 2 2 2(3) (2分) (2分) 12.8(2分)
【解析】(1)该工艺需要控制第二阶段参加反应的HS与SO 恰好完全反应,而SO 是在第一阶段由HS反
2 2 2 2
应产生的,则 ;由题意可知,若 过小,则第一阶段反应生成的SO 过多,在第二阶段反应
2
中SO 不能完全转化为S,多余的SO 排放到空气中会污染大气;(2)①氧化剂体现氧化性。
2 2 2
过程中, 做氧化剂,
过程中, 既是氧化剂又是还原剂,
过程中,O 做氧化剂,因此该机理中体现氧化性的微粒有3种;②根据反应机理,
2
NO、 和O 在钒基催化剂作用下反应生成N 和HO,其总反应方程式为 ;
2 2 2
(3)①导带产生 的过程是: 、 ,价带上产生 的过程是:
;②该过程中消耗2.24L氧气(标准状况下),则最多转移电子的物质的量为0.4mol,因此最
多可脱硫的质量为: 。
37.(10分)(2023·山东省日照市高三期中联考)利用生物浸出黄铜矿(主要成分CuFeS,含有少量SiO 杂质)
2 2
回收其中铁和铜的工艺流程如图:
回答下列问题:
(1)Cu2+的生物浸出原理如图:浸出温度不宜过高,其原因是_____,反应①的离子方程式为____。(2)浸渣的主要成分为____(填化学式),操作1的名称为____。
(3)分离Cu2+的原理如下:Cu2++2(HR)org (CuR )org+2H+。根据流程,反萃取加入的试剂应该为
2
_____(填化学式)。
(4)检验滤液2中是否存在Fe3+,可选用_____(填标号)。
A.KSCN溶液 B.K[Fe(CN) ]溶液 C.K[Fe(CN) ]溶液 D.KMnO 溶液
4 6 3 6 4
(5)“一系列操作”包括_____、洗涤、干燥。
【答案】(1) 温度过高细菌失活(1分) CuFeS+4Fe3+=5Fe2++2S+Cu2+(2分)
2
(2) SiO (1分) 萃取分液(1分) (3)H SO (1分) (4)AB(2分)
2 2 4
(5)蒸发浓缩、冷却结晶、过滤(2分)
【解析】黄铜矿生物浸出得到铜盐溶液,二氧化硅不反应进入滤渣,滤液加入有机萃取剂分液铜离子进入
有机相,反萃取得到硫酸铜溶液,最终转化为铜;水相加入铁得到二价铁溶液,经过蒸发浓缩、冷却结晶、过
滤、洗涤、干燥得到硫酸亚铁晶体。(1)Cu2+的生物浸出过程中细菌参与了反应,浸出温度不宜过高,其原因是
温度过高细菌失活;反应①为CuFeS 和Fe3+反应生成亚铁离子和硫、铜离子,离子方程式为
2
CuFeS+4Fe3+=5Fe2++2S+Cu2+;(2)黄铜矿中二氧化硅不反应,成为滤渣,故滤渣的主要成分为SiO,操作1得
2 2
到有机相和水相,为萃取分液过程;(3)根据流程反萃取得到硫酸铜溶液,则反萃取加入的试剂应该为稀硫酸
HSO ,加入硫酸氢离子浓度变大,Cu2++2(HR)org (CuR )org+2H+逆向进行生成硫酸铜溶液;(4)铁离子
2 4 2
和KSCN溶液反应溶液变为血红色、和K[Fe(CN) ]溶液反应生成蓝色沉淀,可以检验铁离子,故选AB;
4 6
(5)“一系列操作”得到硫酸亚铁晶体,操作为蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
38.(4分)利用污泥燃烧产生的还原性气体(NH 、CO等)也可还原烟气中的NO 。CO还原NO的反应历程
3 x
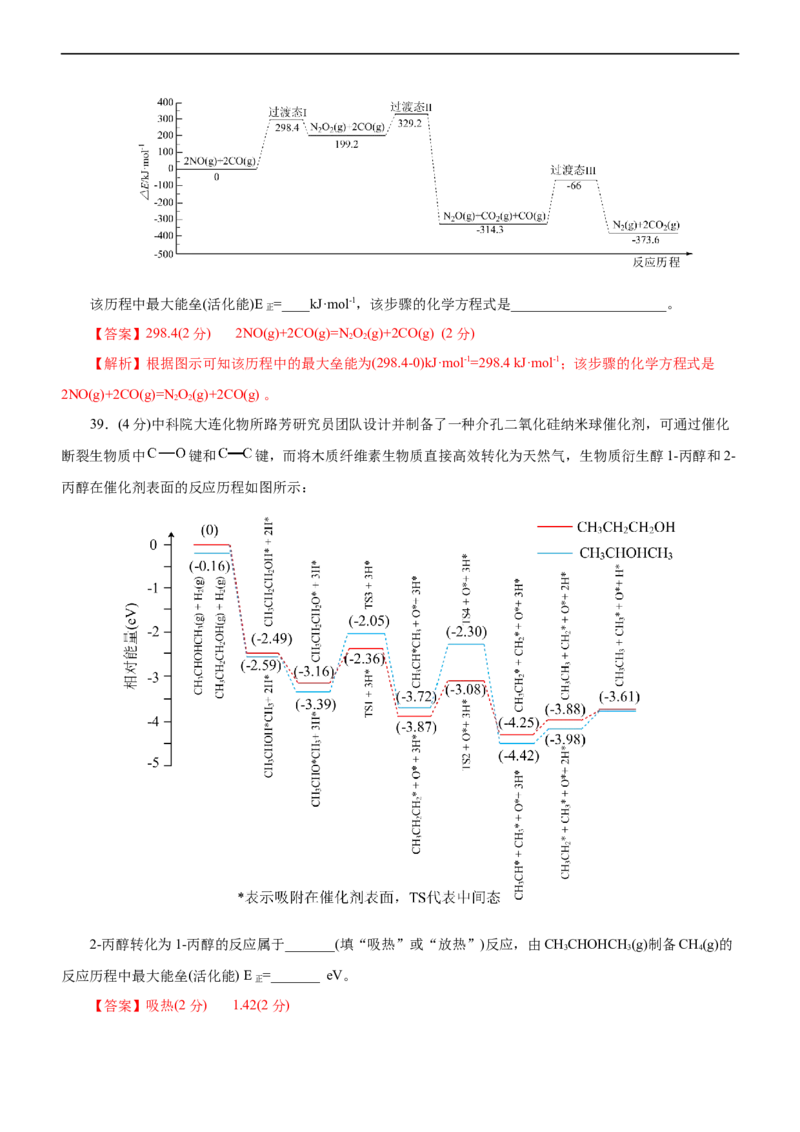
中相对能量变化如图:该历程中最大能垒(活化能)E =____kJ·mol-1,该步骤的化学方程式是______________________。
正
【答案】298.4(2分) 2NO(g)+2CO(g)=N O(g)+2CO(g) (2分)
2 2
【解析】根据图示可知该历程中的最大垒能为(298.4-0)kJ·mol-1=298.4 kJ·mol-1;该步骤的化学方程式是
2NO(g)+2CO(g)=N O(g)+2CO(g) 。
2 2
39.(4分)中科院大连化物所路芳研究员团队设计并制备了一种介孔二氧化硅纳米球催化剂,可通过催化
断裂生物质中 键和 键,而将木质纤维素生物质直接高效转化为天然气,生物质衍生醇1-丙醇和2-
丙醇在催化剂表面的反应历程如图所示:
2-丙醇转化为1-丙醇的反应属于_______(填“吸热”或“放热”)反应,由CHCHOHCH (g)制备CH(g)的
3 3 4
反应历程中最大能垒(活化能) E =_______ eV。
正
【答案】吸热(2分) 1.42(2分)【解析】由图可知,2-丙醇能量低于1-丙醇,故2-丙醇转化为1-丙醇的反应属于吸热反应;过渡态物质的
总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,图中峰值越小则活化能越小,结合图
像可知,由CHCHOHCH (g)制备CH(g)的反应历程中最大能垒(活化能)E =-2.30 eV -(-3.72 eV)=1.42 eV。
3 3 4 正