文档内容
专题 10 化学反应机理与历程
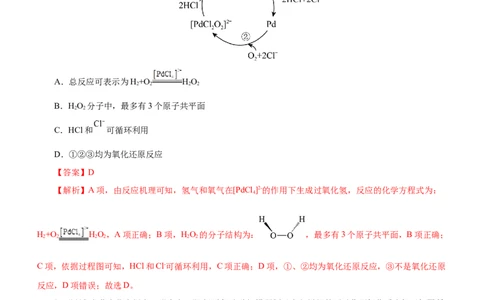
1.(2023·浙江省名校协作体高三开学考试)某种制备HO 的反应机理如图。下列说法不正确的是( )
2 2
A.总反应可表示为H+O HO
2 2 2 2
B.HO 分子中,最多有3个原子共平面
2 2
C.HCl和 可循环利用
D.①②③均为氧化还原反应
【答案】D
【解析】A项,由反应机理可知,氢气和氧气在[PdCl ]2-的作用下生成过氧化氢,反应的化学方程式为:
4
H+O HO,A项正确;B项,HO 的分子结构为: ,最多有3个原子共平面,B项正确;
2 2 2 2 2 2
C项,依据过程图可知,HCl和Cl-可循环利用,C项正确;D项,①、②均为氧化还原反应,③不是氧化还原
反应,D项错误;故选D。
2.(2023·湖北省华中师大一附中高三期中)过氧硫酸氢根(HSO -)参与烯烃的不对称环氧化反应机理如图所
3
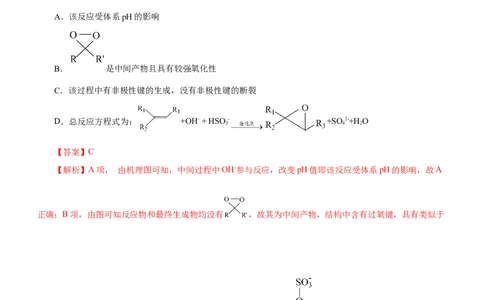
示,下列说法错误的是( )A.该反应受体系pH的影响
B. 是中间产物且具有较强氧化性
C.该过程中有非极性键的生成,没有非极性键的断裂
D.总反应方程式为: +OH- + HSO - +SO2-+H O
3 4 2
【答案】C
【解析】A项, 由机理图可知,中间过程中OH-参与反应,改变pH值即该反应受体系pH的影响,故A
正确;B项,由图可知反应物和最终生成物均没有 ,故其为中间产物,结构中含有过氧键,具有类似于
双氧水的强氧化性,故B正确;C项,如图中间产物 和 中均存在非极性键,整个过程中存
在非极性键断裂,故C错误;D项,由图可知该反应的反应物有: 、OH- 、 HSO ,生成物为:、SO 2-、HO,总反应方程式为: +OH- + HSO - +SO2-
4 2 3 4
+H O,故D正确;故选C。
2
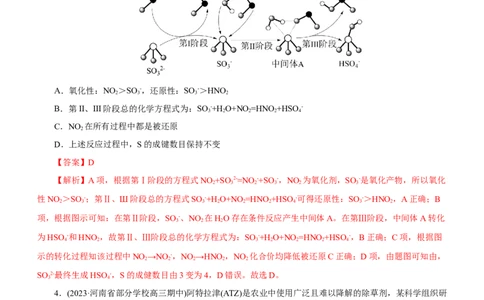
3.(2023·山西省吕梁·高三阶段练习)科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主
要过程示意图如图。下列说法错误的是( )
A.氧化性:NO >SO -,还原性:SO ->HNO
2 3 3 2
B.第II、III阶段总的化学方程式为:SO -+H O+NO =HNO +HSO -
3 2 2 2 4
C.NO 在所有过程中都是被还原
2
D.上述反应过程中,S的成键数目保持不变
【答案】D
【解析】A项,根据第Ⅰ阶段的方程式NO +SO2-=NO-+SO-,NO 为氧化剂,SO -是氧化产物,所以氧化
2 3 2 3 2 3
性NO >SO -;第Ⅱ、Ш阶段总的方程式SO -+H O+NO =HNO +HSO -可得还原性:SO ->HNO,A正确;B
2 3 3 2 2 2 4 3 2
项,根据图示可知:在第Ⅱ阶段,SO -、NO 在HO存在条件反应产生中间体A。在第Ⅲ阶段,中间体A转化
3 2 2
为HSO -和HNO,故第Ⅱ、Ⅲ阶段总的化学方程式为:SO -+H O+NO =HNO +HSO -,B正确;C项,根据图
4 2 3 2 2 2 4
示的转化过程知该过程中NO →NO -,NO →HNO,NO 化合价均降低被还原C正确;D项,由题图可知由,
2 2 2 2 2
SO 2-最终生成HSO -,S的成健数目由3变为4,D错误。故选D。
3 4
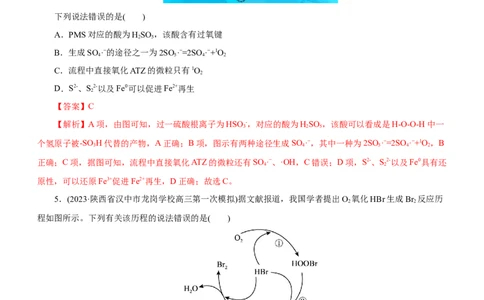
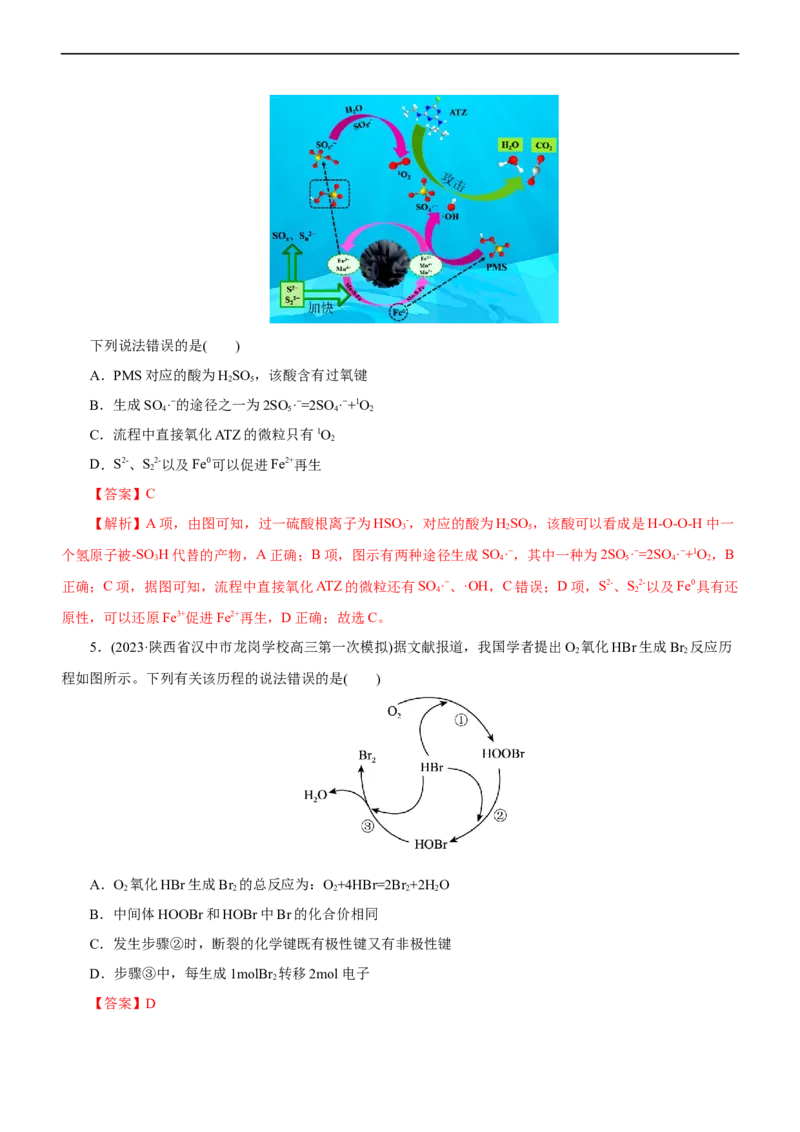
4.(2023·河南省部分学校高三期中)阿特拉津(ATZ)是农业中使用广泛且难以降解的除草剂,某科学组织研
究发现,以FeS@MoS 为催化剂(呈花束状)催化活化过一硫酸盐(PMS)降解阿特拉津(ATZ)取得了良好的效果,
x 2
其反应机理如图所示:下列说法错误的是( )
A.PMS对应的酸为HSO ,该酸含有过氧键
2 5
B.生成SO ·−的途径之一为2SO ·−=2SO·−+1O
4 5 4 2
C.流程中直接氧化ATZ的微粒只有1O
2
D.S2-、S2-以及Fe0可以促进Fe2+再生
2
【答案】C
【解析】A项,由图可知,过一硫酸根离子为HSO -,对应的酸为HSO ,该酸可以看成是H-O-O-H中一
3 2 5
个氢原子被-SO H代替的产物,A正确;B项,图示有两种途径生成SO ·−,其中一种为2SO ·−=2SO·−+1O,B
3 4 5 4 2
正确;C项,据图可知,流程中直接氧化ATZ的微粒还有SO ·−、·OH,C错误;D项,S2-、S2-以及Fe0具有还
4 2
原性,可以还原Fe3+促进Fe2+再生,D正确;故选C。
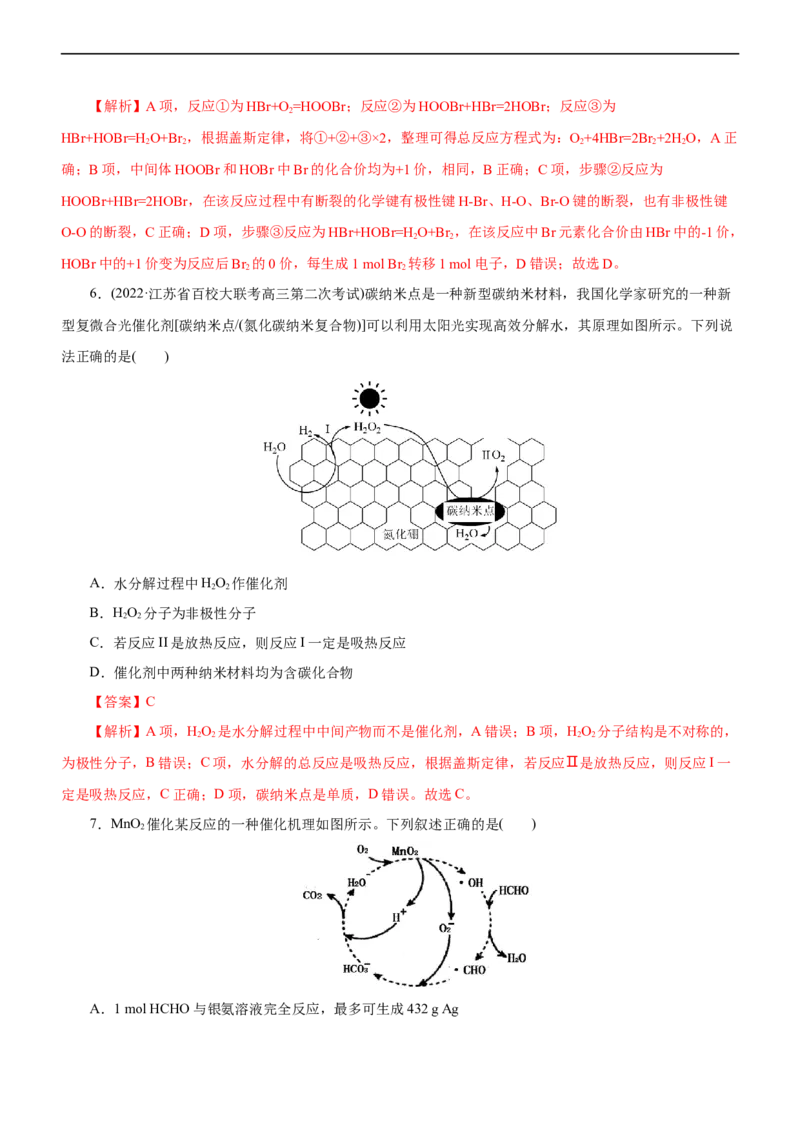
5.(2023·陕西省汉中市龙岗学校高三第一次模拟)据文献报道,我国学者提出O 氧化HBr生成Br 反应历
2 2
程如图所示。下列有关该历程的说法错误的是( )
A.O 氧化HBr生成Br 的总反应为:O+4HBr=2Br +2H O
2 2 2 2 2
B.中间体HOOBr和HOBr中Br的化合价相同
C.发生步骤②时,断裂的化学键既有极性键又有非极性键
D.步骤③中,每生成1molBr 转移2mol电子
2
【答案】D【解析】A项,反应①为HBr+O=HOOBr;反应②为HOOBr+HBr=2HOBr;反应③为
2
HBr+HOBr=H O+Br ,根据盖斯定律,将①+②+③×2,整理可得总反应方程式为:O+4HBr=2Br +2H O,A正
2 2 2 2 2
确;B项,中间体HOOBr和HOBr中Br的化合价均为+1价,相同,B正确;C项,步骤②反应为
HOOBr+HBr=2HOBr,在该反应过程中有断裂的化学键有极性键H-Br、H-O、Br-O键的断裂,也有非极性键
O-O的断裂,C正确;D项,步骤③反应为HBr+HOBr=H O+Br ,在该反应中Br元素化合价由HBr中的-1价,
2 2
HOBr中的+1价变为反应后Br 的0价,每生成1 mol Br 转移1 mol电子,D错误;故选D。
2 2
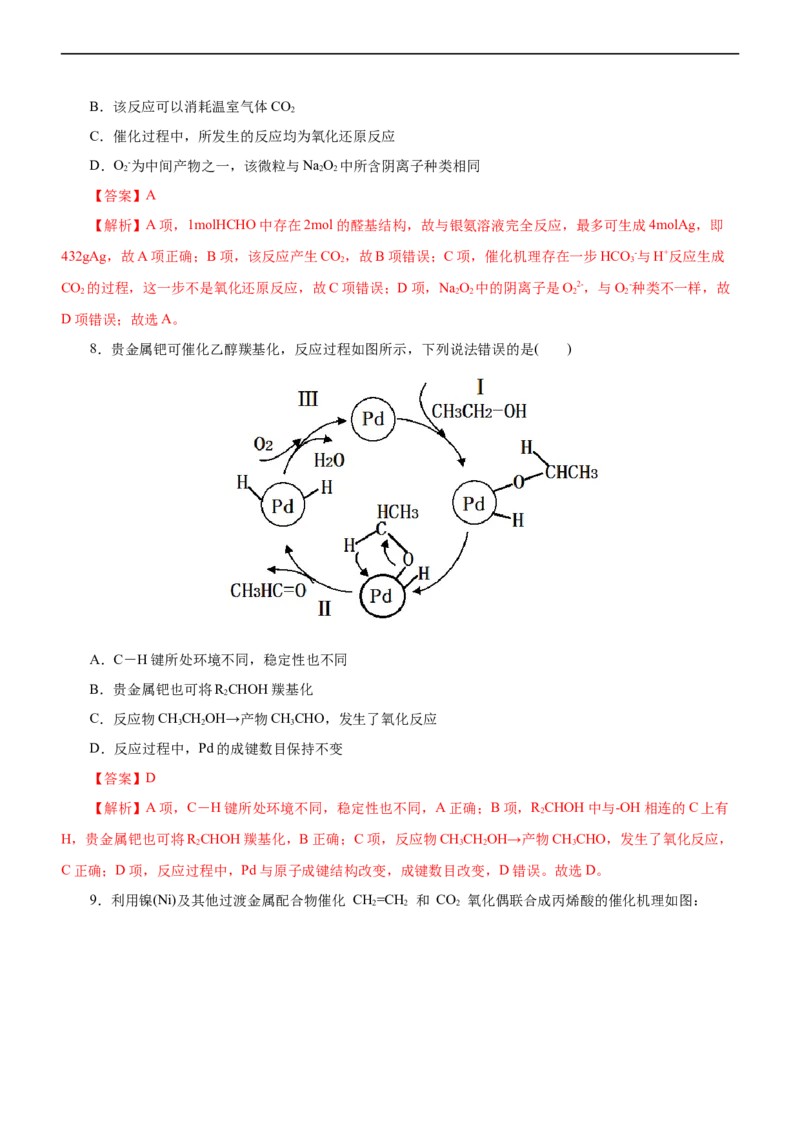
6.(2022·江苏省百校大联考高三第二次考试)碳纳米点是一种新型碳纳米材料,我国化学家研究的一种新
型复微合光催化剂[碳纳米点/(氮化碳纳米复合物)]可以利用太阳光实现高效分解水,其原理如图所示。下列说
法正确的是( )
A.水分解过程中HO 作催化剂
2 2
B.HO 分子为非极性分子
2 2
C.若反应II是放热反应,则反应I一定是吸热反应
D.催化剂中两种纳米材料均为含碳化合物
【答案】C
【解析】A项,HO 是水分解过程中中间产物而不是催化剂,A错误;B项,HO 分子结构是不对称的,
2 2 2 2
为极性分子,B错误;C项,水分解的总反应是吸热反应,根据盖斯定律,若反应Ⅱ是放热反应,则反应I一
定是吸热反应,C正确;D项,碳纳米点是单质,D错误。故选C。
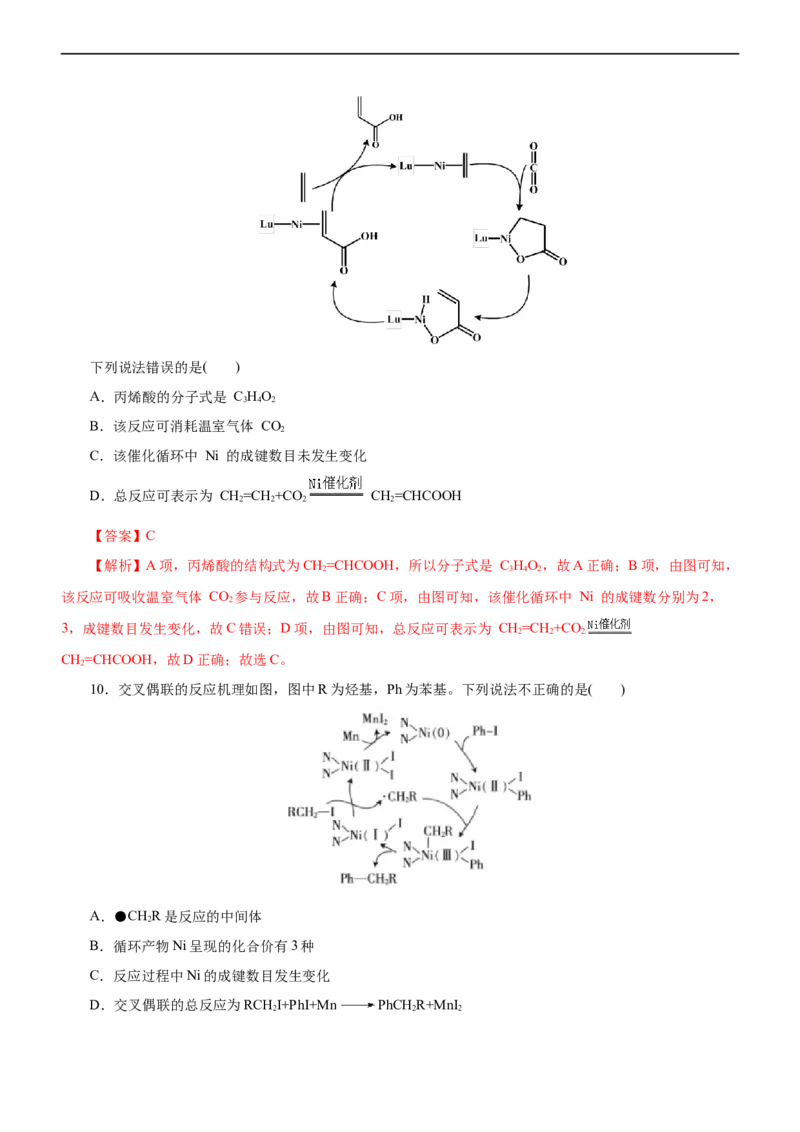
7.MnO 催化某反应的一种催化机理如图所示。下列叙述正确的是( )
2
A.1 mol HCHO与银氨溶液完全反应,最多可生成432 g AgB.该反应可以消耗温室气体CO
2
C.催化过程中,所发生的反应均为氧化还原反应
D.O-为中间产物之一,该微粒与NaO 中所含阴离子种类相同
2 2 2
【答案】A
【解析】A项,1molHCHO中存在2mol的醛基结构,故与银氨溶液完全反应,最多可生成4molAg,即
432gAg,故A项正确;B项,该反应产生CO,故B项错误;C项,催化机理存在一步HCO -与H+反应生成
2 3
CO 的过程,这一步不是氧化还原反应,故C项错误;D项,NaO 中的阴离子是O2-,与O-种类不一样,故
2 2 2 2 2
D项错误;故选A。
8.贵金属钯可催化乙醇羰基化,反应过程如图所示,下列说法错误的是( )
A.C-H键所处环境不同,稳定性也不同
B.贵金属钯也可将R CHOH羰基化
2
C.反应物CHCHOH→产物CHCHO,发生了氧化反应
3 2 3
D.反应过程中,Pd的成键数目保持不变
【答案】D
【解析】A项,C-H键所处环境不同,稳定性也不同,A正确;B项,R CHOH中与-OH相连的C上有
2
H,贵金属钯也可将R CHOH羰基化,B正确;C项,反应物CHCHOH→产物CHCHO,发生了氧化反应,
2 3 2 3
C正确;D项,反应过程中,Pd与原子成键结构改变,成键数目改变,D错误。故选D。
9.利用镍(Ni)及其他过渡金属配合物催化 CH=CH 和 CO 氧化偶联合成丙烯酸的催化机理如图:
2 2 2下列说法错误的是( )
A.丙烯酸的分子式是 C HO
3 4 2
B.该反应可消耗温室气体 CO
2
C.该催化循环中 Ni 的成键数目未发生变化
D.总反应可表示为 CH=CH +CO CH=CHCOOH
2 2 2 2
【答案】C
【解析】A项,丙烯酸的结构式为CH=CHCOOH,所以分子式是 C HO,故A正确;B项,由图可知,
2 3 4 2
该反应可吸收温室气体 CO 参与反应,故B正确;C项,由图可知,该催化循环中 Ni 的成键数分别为2,
2
3,成键数目发生变化,故C错误;D项,由图可知,总反应可表示为 CH=CH +CO
2 2 2
CH=CHCOOH,故D正确;故选C。
2
10.交叉偶联的反应机理如图,图中R为烃基,Ph为苯基。下列说法不正确的是( )
A.●CHR是反应的中间体
2
B.循环产物Ni呈现的化合价有3种
C.反应过程中Ni的成键数目发生变化
D.交叉偶联的总反应为RCHI+PhI+Mn PhCH R+MnI
2 2 2【答案】B
【解析】A项,根据交叉偶联的反应机理可知,●CHR是反应的中间体,故A正确;B项,由图可知,
2
Ni的化合价呈现0价、+1价、+2价、+3价四种,故B错误;C项,反应过程中Ni的成键数目有4、5、3、
2,发生变化,故C正确;D项,根据交叉偶联的反应机理可知,交叉偶联的总反应为RCHI+PhI+Mn
2
PhCH R+MnI 。故D正确;故选B。
2 2
11.利用 分子筛催化剂,NH 可脱除燃煤烟气中的NO和NO ,生成两种无毒物质,其反
3 2
应历程如图所示,下列说法正确的是( )
A.X和Y均是N
2
B.上述历程的总反应为:2NH +NO+NO 2N+3H O
3 2 2 2
C.阶段④中氮元素只被还原
D.NH 、NH +、HO中的质子数、电子数均相同
3 4 2
【答案】B
【解析】A项,图示反应可以生成X的反应[(NH )(NO )]2++NO=[(NH )(HNO)]++X+H+,原子守恒判断X
4 2 2 4 2
为N 和HO,故A错误;B项,由反应历程图可知,氨气、二氧化氮和一氧化氮是反应物,氮气与水是生成
2 2
物,所以总反应为:2NH +NO+NO 2N+3H O+3HO,故B正确;C项,阶段④中氮元素由[(NH )
3 2 2 2 2 4
(HNO)]+变成氮气,氮元素的化合价有升高有降低,氮元素既被氧化也被还原,故C错误;D项,NH 、
2 3
NH +、HO中的质子数分别为10、11、10;NH 、NH +、HO中的电子数为:10、10、10,所以质子数不同,
4 2 3 4 2
故D错误;故选B。
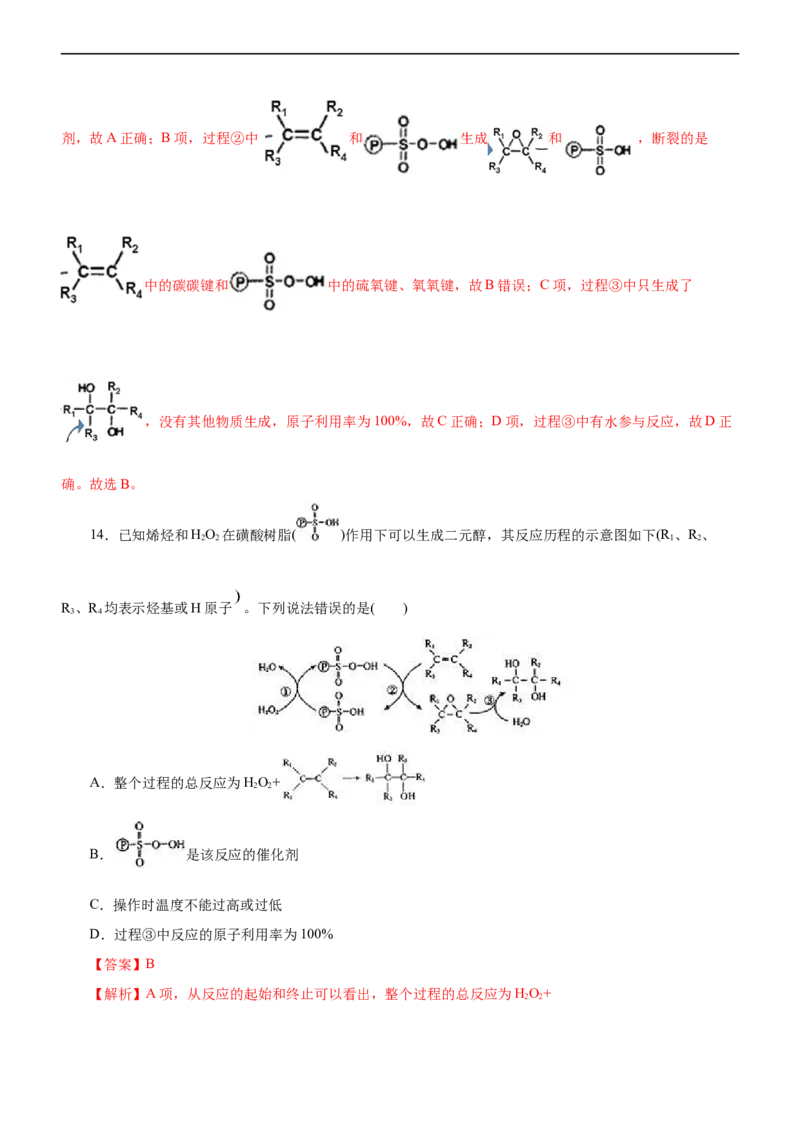
12.某科研人员提出HCHO与O 在羟基磷灰石(HAP)表面催化氧化生成CO、HO的历程示意图如下(图
2 2 2
中只画出了HAP的部分结构)。下列说法错误的是( )A.过渡态是该历程中能量最高的状态
B.HCHO在反应过程中,C-H键全部断裂
C.CO 分子中的氧原子全部来自O
2 2
D.该反应可表示为:HCHO+O CO+H O
2 2 2
【答案】C
【解析】A项,过渡态是指反应物体系转变成产物体系过程中,经过的能量最高状态,则过渡态是该历程
中能量最高的状态,故A正确;B项,由图示可知,HCHO在反应过程中,甲醛分子中的两个C-H键全部断
裂,故B正确;C项,根据图知,CO 分子中的氧原子一部分来自O,另一部分还来自于甲醛,故 C错误;
2 2
D项,该反应中反应物是甲醛和氧气,生成物是二氧化碳和水,HAP为催化剂,反应方程式为:HCHO+O
2
CO+H O,故D正确;故选C。
2 2
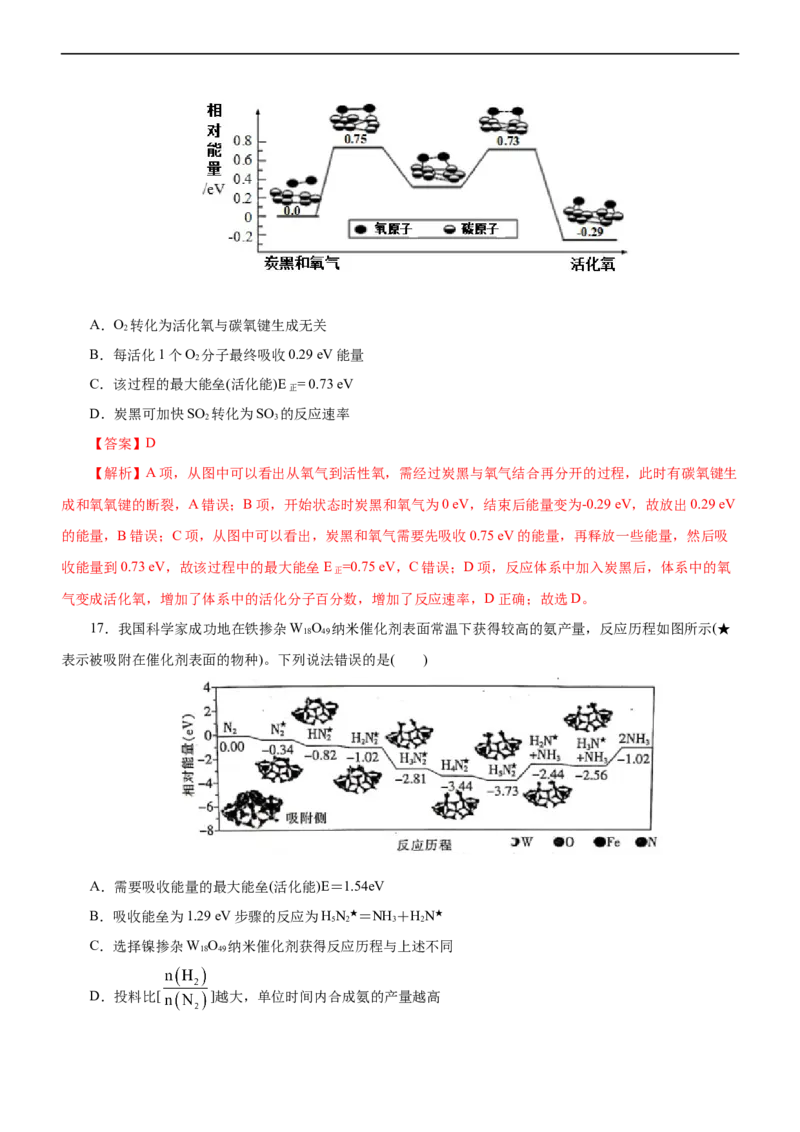
13.磺酸树脂催化下的烯烃二羟化反应历程的示意图如下:
(R 、R 、R 、R 均表示烃基或H原子。)
1 2 3 4
下列说法不正确的是( )
A.过程①中,HO 作氧化剂 B.过程②中,有碳碳键、碳氢键断裂
2 2
C.过程③中反应的原子利用率为100% D.在反应历程中,有水参与反应
【答案】B
【解析】A项,过程①中HO 中的氧元素由-1价降低到-2价得电子发生还原反应生成HO,HO 作氧化
2 2 2 2 2剂,故A正确;B项,过程②中 和 生成 和 ,断裂的是
中的碳碳键和 中的硫氧键、氧氧键,故B错误;C项,过程③中只生成了
,没有其他物质生成,原子利用率为100%,故C正确;D项,过程③中有水参与反应,故D正
确。故选B。
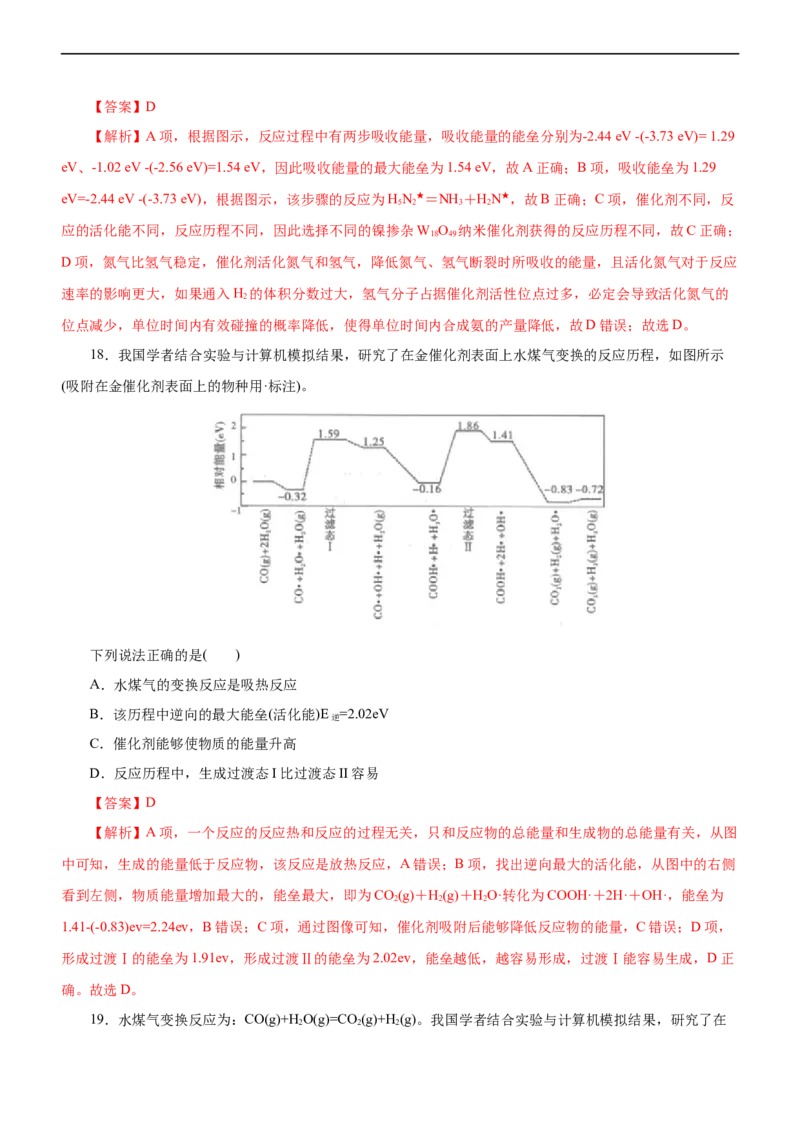
14.已知烯烃和HO 在磺酸树脂( )作用下可以生成二元醇,其反应历程的示意图如下(R 、R 、
2 2 1 2
R 、R 均表示烃基或H原子 。下列说法错误的是( )
3 4
A.整个过程的总反应为HO+
2 2
B. 是该反应的催化剂
C.操作时温度不能过高或过低
D.过程③中反应的原子利用率为100%
【答案】B
【解析】A项,从反应的起始和终止可以看出,整个过程的总反应为HO+
2 2,A正确;B项, 才是该反应的催化剂, 是该反应
中 的中间产物,最后又转为 ,B错误;C项,温度过高HO 分解,温度过低反应速率慢,
2 2
C正确;D项,过程③中产物为一种,没有其它物质生成,原料分子中的原子全部转化成所需要的产物,原子
利用率为100%,D正确;故选B。
15.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),
甲醇与水在铜催化剂上的反应机理和能量变化如图。
下列说法正确的是( )
A.反应过程只有C-H键断开
B.反应I的活化能为(c-a)kJ mol−1
C.总反应的热化学方程式为:CHOH(g)+H O(g)= CO (g)+3H(g) ΔH=(b-a)kJ mol−1
3 2 2 2 4
D.反应历程中,反应Ⅱ决定整个反应进程的快慢
【答案】C
【解析】A项,据图可知反应过程中甲醇中的O-H键也发生断裂,故A错误;B项,反应I的活化能为反
应物断键吸收的能量,即反应I过程中最大能量与a的差值,图中没有体现反应I过程中的最大能量,故B错
误;C项,焓变=生成物的能量-反应物能量,据图可知总反应的热化学方程式为:CHOH(g)+H O(g)= CO (g)
3 2 2
+3H (g) H=(b-a)kJ mol−1,故C正确;D项,据图可知反应I的活化能大于反应Ⅱ的活化能,活化能越
2 4
大反应越慢,慢反应决定整个反应的反应速率,所以反应I决定整个反应进程的快慢,故D错误;故选C。
16.已知活性氧可以把SO 快速氧化为SO ,根据计算机模拟结果,在炭黑表面上O 转化为活化氧的反应
2 3 2
历程与能量变化关系如图所示。下列说法正确的是( )A.O 转化为活化氧与碳氧键生成无关
2
B.每活化1个O 分子最终吸收0.29 eV能量
2
C.该过程的最大能垒(活化能)E = 0.73 eV
正
D.炭黑可加快SO 转化为SO 的反应速率
2 3
【答案】D
【解析】A项,从图中可以看出从氧气到活性氧,需经过炭黑与氧气结合再分开的过程,此时有碳氧键生
成和氧氧键的断裂,A错误;B项,开始状态时炭黑和氧气为0 eV,结束后能量变为-0.29 eV,故放出0.29 eV
的能量,B错误;C项,从图中可以看出,炭黑和氧气需要先吸收0.75 eV的能量,再释放一些能量,然后吸
收能量到0.73 eV,故该过程中的最大能垒E =0.75 eV,C错误;D项,反应体系中加入炭黑后,体系中的氧
正
气变成活化氧,增加了体系中的活化分子百分数,增加了反应速率,D正确;故选D。
17.我国科学家成功地在铁掺杂W O 纳米催化剂表面常温下获得较高的氨产量,反应历程如图所示(★
18 49
表示被吸附在催化剂表面的物种)。下列说法错误的是( )
A.需要吸收能量的最大能垒(活化能)E=1.54eV
B.吸收能垒为1.29 eV步骤的反应为HN★=NH +HN★
5 2 3 2
C.选择镍掺杂W O 纳米催化剂获得反应历程与上述不同
18 49
D.投料比[ ]越大,单位时间内合成氨的产量越高【答案】D
【解析】A项,根据图示,反应过程中有两步吸收能量,吸收能量的能垒分别为-2.44 eV -(-3.73 eV)= 1.29
eV、-1.02 eV -(-2.56 eV)=1.54 eV,因此吸收能量的最大能垒为1.54 eV,故A正确;B项,吸收能垒为1.29
eV=-2.44 eV -(-3.73 eV),根据图示,该步骤的反应为HN★=NH +HN★,故B正确;C项,催化剂不同,反
5 2 3 2
应的活化能不同,反应历程不同,因此选择不同的镍掺杂W O 纳米催化剂获得的反应历程不同,故C正确;
18 49
D项,氮气比氢气稳定,催化剂活化氮气和氢气,降低氮气、氢气断裂时所吸收的能量,且活化氮气对于反应
速率的影响更大,如果通入H 的体积分数过大,氢气分子占据催化剂活性位点过多,必定会导致活化氮气的
2
位点减少,单位时间内有效碰撞的概率降低,使得单位时间内合成氨的产量降低,故D错误;故选D。
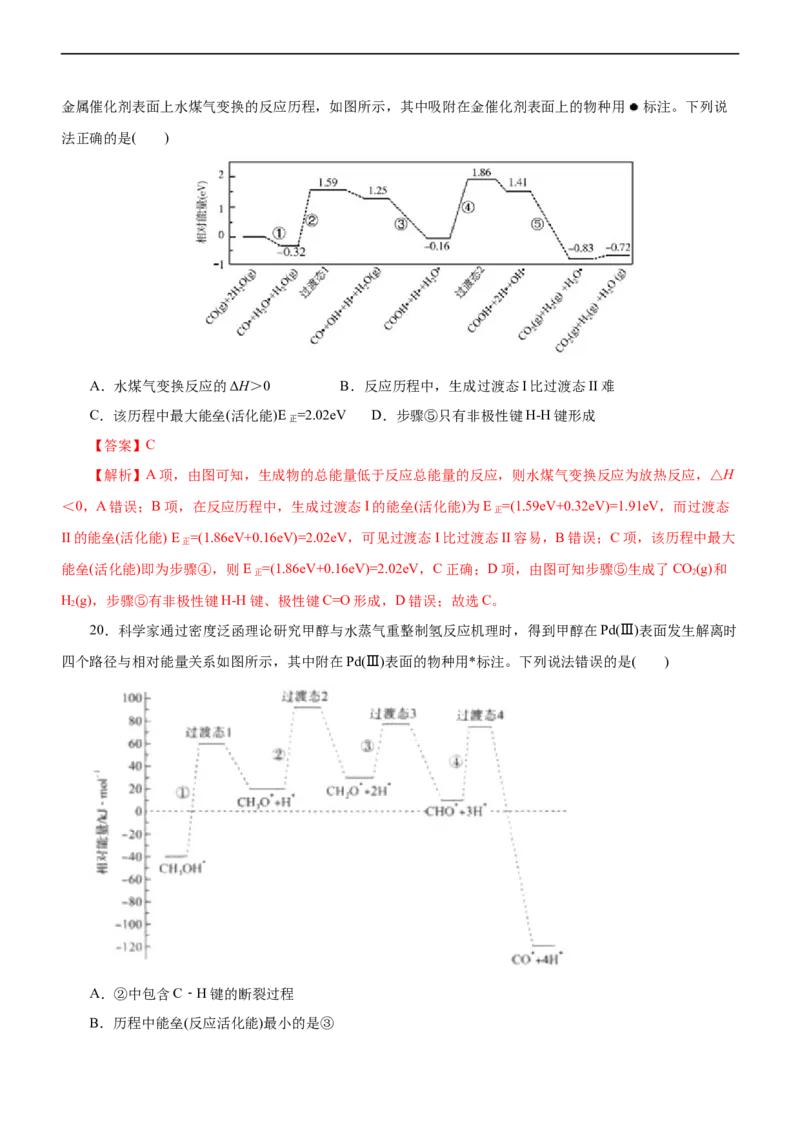
18.我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示
(吸附在金催化剂表面上的物种用·标注)。
下列说法正确的是( )
A.水煤气的变换反应是吸热反应
B.该历程中逆向的最大能垒(活化能)E =2.02eV
逆
C.催化剂能够使物质的能量升高
D.反应历程中,生成过渡态I比过渡态II容易
【答案】D
【解析】A项,一个反应的反应热和反应的过程无关,只和反应物的总能量和生成物的总能量有关,从图
中可知,生成的能量低于反应物,该反应是放热反应,A错误;B项,找出逆向最大的活化能,从图中的右侧
看到左侧,物质能量增加最大的,能垒最大,即为CO(g)+H(g)+HO·转化为COOH·+2H·+OH·,能垒为
2 2 2
1.41-(-0.83)ev=2.24ev,B错误;C项,通过图像可知,催化剂吸附后能够降低反应物的能量,C错误;D项,
形成过渡Ⅰ的能垒为1.91ev,形成过渡Ⅱ的能垒为2.02ev,能垒越低,越容易形成,过渡Ⅰ能容易生成,D正
确。故选D。
19.水煤气变换反应为:CO(g)+HO(g)=CO(g)+H(g)。我国学者结合实验与计算机模拟结果,研究了在
2 2 2金属催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。下列说
法正确的是( )
A.水煤气变换反应的ΔH>0 B.反应历程中,生成过渡态I比过渡态II难
C.该历程中最大能垒(活化能)E =2.02eV D.步骤⑤只有非极性键H-H键形成
正
【答案】C
【解析】A项,由图可知,生成物的总能量低于反应总能量的反应,则水煤气变换反应为放热反应,△H
<0,A错误;B项,在反应历程中,生成过渡态I的能垒(活化能)为E =(1.59eV+0.32eV)=1.91eV,而过渡态
正
II的能垒(活化能) E =(1.86eV+0.16eV)=2.02eV,可见过渡态I比过渡态II容易,B错误;C项,该历程中最大
正
能垒(活化能)即为步骤④,则E =(1.86eV+0.16eV)=2.02eV,C正确;D项,由图可知步骤⑤生成了CO(g)和
正 2
H(g),步骤⑤有非极性键H-H键、极性键C=O形成,D错误;故选C。
2
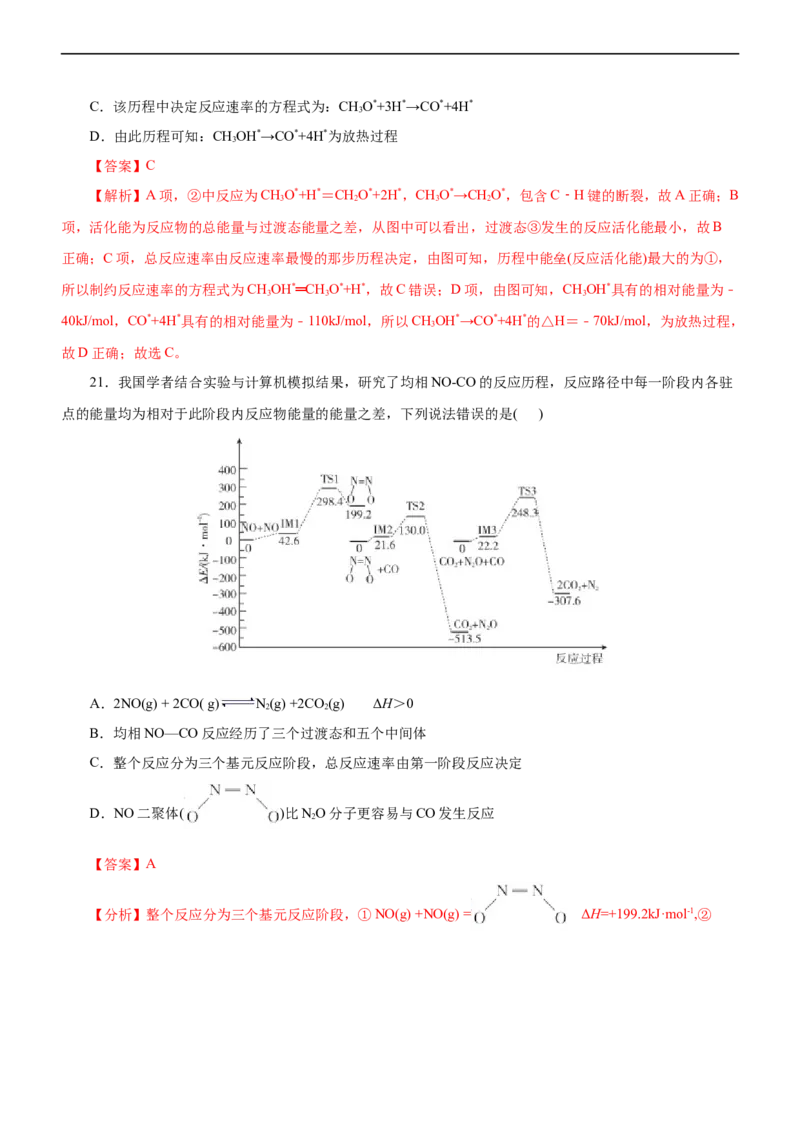
20.科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表面发生解离时
四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。下列说法错误的是( )
A.②中包含C﹣H键的断裂过程
B.历程中能垒(反应活化能)最小的是③C.该历程中决定反应速率的方程式为:CHO*+3H*→CO*+4H*
3
D.由此历程可知:CHOH*→CO*+4H*为放热过程
3
【答案】C
【解析】A项,②中反应为CHO*+H*=CHO*+2H*,CHO*→CHO*,包含C﹣H键的断裂,故A正确;B
3 2 3 2
项,活化能为反应物的总能量与过渡态能量之差,从图中可以看出,过渡态③发生的反应活化能最小,故B
正确;C项,总反应速率由反应速率最慢的那步历程决定,由图可知,历程中能垒(反应活化能)最大的为①,
所以制约反应速率的方程式为CHOH*═CH O*+H*,故C错误;D项,由图可知,CHOH*具有的相对能量为﹣
3 3 3
40kJ/mol,CO*+4H*具有的相对能量为﹣110kJ/mol,所以CHOH*→CO*+4H*的△H=﹣70kJ/mol,为放热过程,
3
故D正确;故选C。
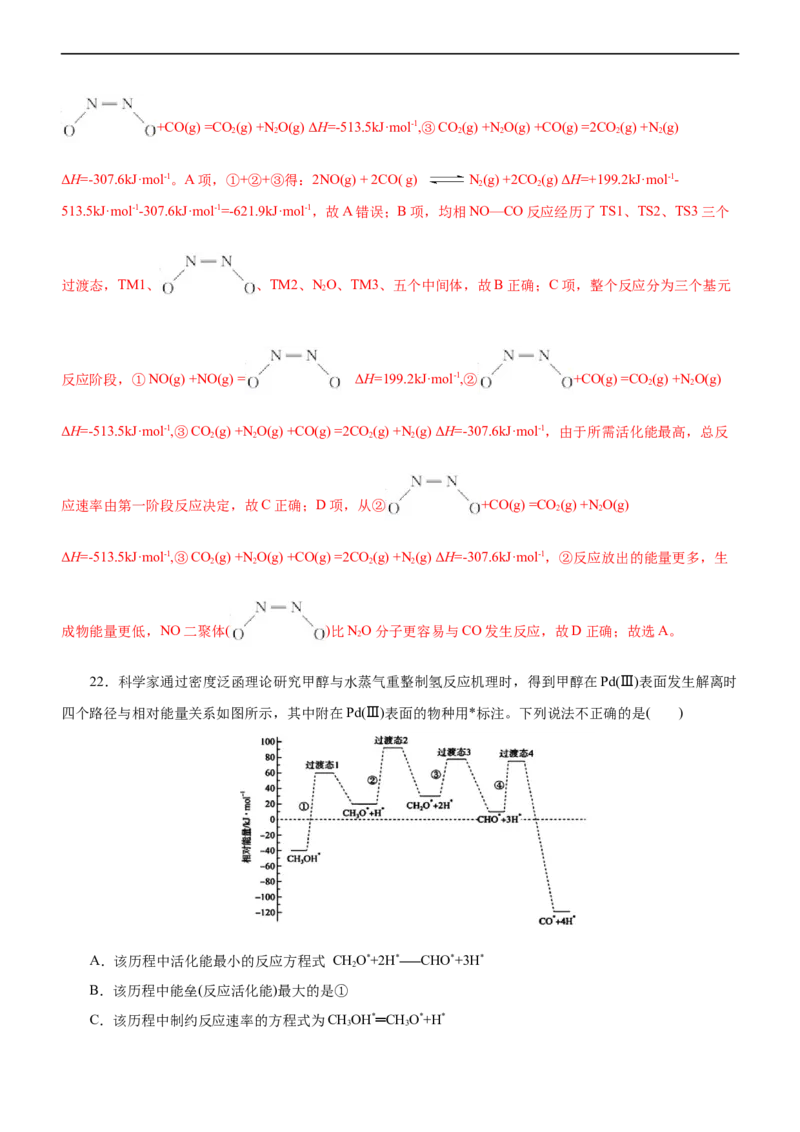
21.我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,反应路径中每一阶段内各驻
点的能量均为相对于此阶段内反应物能量的能量之差,下列说法错误的是( )
A.2NO(g) + 2CO( g) N(g) +2CO (g) ΔH>0
2 2
B.均相NO—CO反应经历了三个过渡态和五个中间体
C.整个反应分为三个基元反应阶段,总反应速率由第一阶段反应决定
D.NO二聚体( )比NO分子更容易与CO发生反应
2
【答案】A
【分析】整个反应分为三个基元反应阶段,①NO(g) +NO(g) = ΔH=+199.2kJ·mol-1,②+CO(g) =CO (g) +N O(g) ΔH=-513.5kJ·mol-1,③CO(g) +N O(g) +CO(g) =2CO (g) +N (g)
2 2 2 2 2 2
ΔH=-307.6kJ·mol-1。A项,①+②+③得:2NO(g) + 2CO( g) N(g) +2CO (g) ΔH=+199.2kJ·mol-1-
2 2
513.5kJ·mol-1-307.6kJ·mol-1=-621.9kJ·mol-1,故A错误;B项,均相NO—CO反应经历了TS1、TS2、TS3三个
过渡态,TM1、 、TM2、NO、TM3、五个中间体,故B正确;C项,整个反应分为三个基元
2
反应阶段,①NO(g) +NO(g) = ΔH=199.2kJ·mol-1,② +CO(g) =CO (g) +N O(g)
2 2
ΔH=-513.5kJ·mol-1,③CO(g) +N O(g) +CO(g) =2CO (g) +N (g) ΔH=-307.6kJ·mol-1,由于所需活化能最高,总反
2 2 2 2
应速率由第一阶段反应决定,故C正确;D项,从② +CO(g) =CO (g) +N O(g)
2 2
ΔH=-513.5kJ·mol-1,③CO(g) +N O(g) +CO(g) =2CO (g) +N (g) ΔH=-307.6kJ·mol-1,②反应放出的能量更多,生
2 2 2 2
成物能量更低,NO二聚体( )比NO分子更容易与CO发生反应,故D正确;故选A。
2
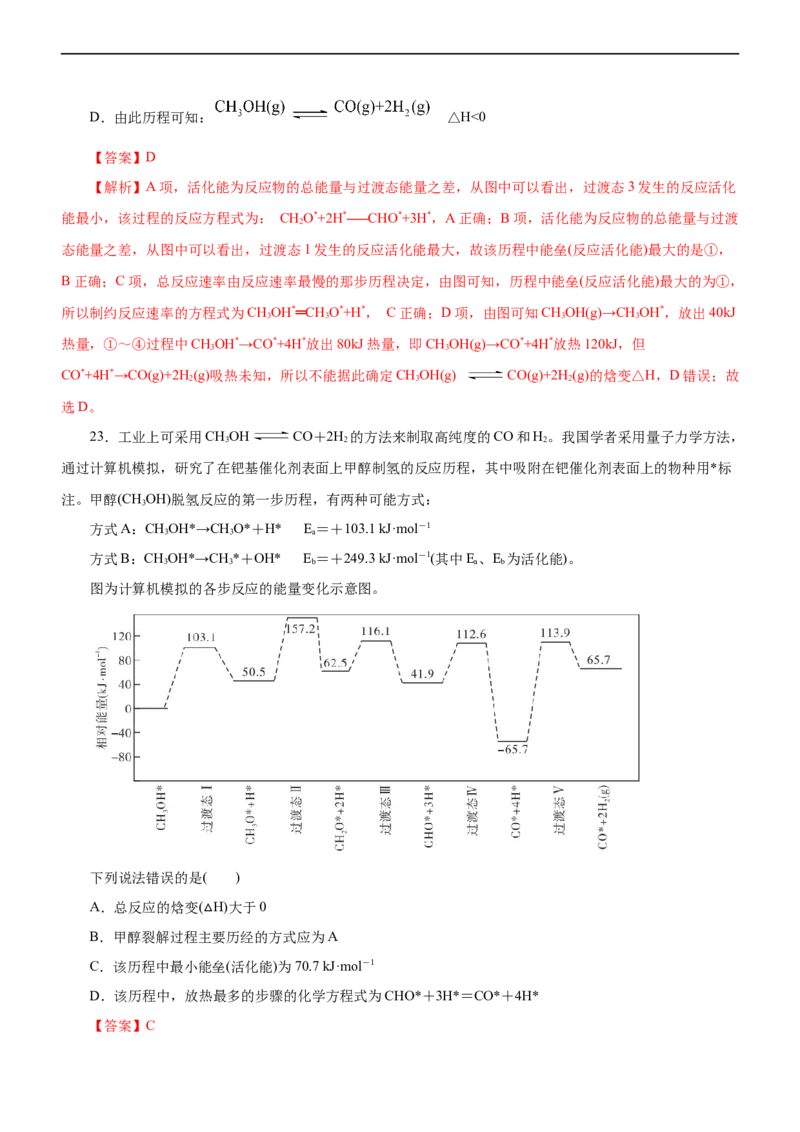
22.科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表面发生解离时
四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。下列说法不正确的是( )
A.该历程中活化能最小的反应方程式 CHO*+2H* CHO*+3H*
2
B.该历程中能垒(反应活化能)最大的是①
C.该历程中制约反应速率的方程式为CHOH*═CH O*+H*
3 3D.由此历程可知: △H<0
【答案】D
【解析】A项,活化能为反应物的总能量与过渡态能量之差,从图中可以看出,过渡态3发生的反应活化
能最小,该过程的反应方程式为: CHO*+2H* CHO*+3H*,A正确;B项,活化能为反应物的总能量与过渡
2
态能量之差,从图中可以看出,过渡态1发生的反应活化能最大,故该历程中能垒(反应活化能)最大的是①,
B正确;C项,总反应速率由反应速率最慢的那步历程决定,由图可知,历程中能垒(反应活化能)最大的为①,
所以制约反应速率的方程式为CHOH*═CH O*+H*, C正确;D项,由图可知CHOH(g)→CHOH*,放出40kJ
3 3 3 3
热量,①~④过程中CHOH*→CO*+4H*放出80kJ热量,即CHOH(g)→CO*+4H*放热120kJ,但
3 3
CO*+4H*→CO(g)+2H(g)吸热未知,所以不能据此确定CHOH(g) CO(g)+2H(g)的焓变△H,D错误;故
2 3 2
选D。
23.工业上可采用CHOH CO+2H 的方法来制取高纯度的CO和H。我国学者采用量子力学方法,
3 2 2
通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标
注。甲醇(CHOH)脱氢反应的第一步历程,有两种可能方式:
3
方式A:CHOH*→CH O*+H* E=+103.1 kJ·mol-1
3 3 a
方式B:CHOH*→CH *+OH* E =+249.3 kJ·mol-1(其中E、E 为活化能)。
3 3 b a b
图为计算机模拟的各步反应的能量变化示意图。
下列说法错误的是( )
A.总反应的焓变( H)大于0
B.甲醇裂解过程主△要历经的方式应为A
C.该历程中最小能垒(活化能)为70.7 kJ·mol-1
D.该历程中,放热最多的步骤的化学方程式为CHO*+3H*=CO*+4H*
【答案】C【解析】A项,由图可知,CHOH的能量低于CO和2H 的总能量,反应CHOH CO+2H 为吸热反应,
3 2 3 2
△H大于0,故A正确;B项,催化剂能降低反应的活化能,加快反应速率,方式A的活化能低,说明甲醇裂
解过程主要历经的方式应为A,故B正确;C项,由图可知,该历程中最小能垒(活化能)为(116.1-62.5) kJ·mol
-1=53.6 kJ·mol-1,故C错误;D 项,由图可知,反应CHO*+3H*=CO*+4H*反应物的能量高于生成物的能
量,且差别最大,是放热最多的步骤,故D正确;故选C。
24.HCOOH在Pd催化剂表面脱氢的反应机理、反应历程与能量的关系如图所示:
下列说法不正确的是( )
A.在Pd催化剂表面HCOOH脱氢反应的 H <0
B.在Pd催化剂表面离解O-H键比C-H键的活化能低
C.在历程Ⅰ~Ⅴ中,生成Ⅴ的反应速率最慢
D.用DCOOH或HCOOD代替HCOOH,得到的产物都有HD和CO
2
【答案】B
【解析】A项,由图可知,在Pd催化剂表面HCOOH脱氢反应为放热反应, H 小于0,故A正确;B
项,由图可知,在Pd催化剂表面离解O-H键的活化能较高,解离C-H键的活化能低,故B错误;C项,在
历程Ⅰ~Ⅴ中,生成Ⅴ的活化能最高,反应速率最慢,故C正确;D项,由图可知,HCOOH脱氢是生成氢气
和二氧化碳,所以用DCOOH或HCOOD代替HCOOH,得到的产物都有HD和CO,故D正确;故选B。
2
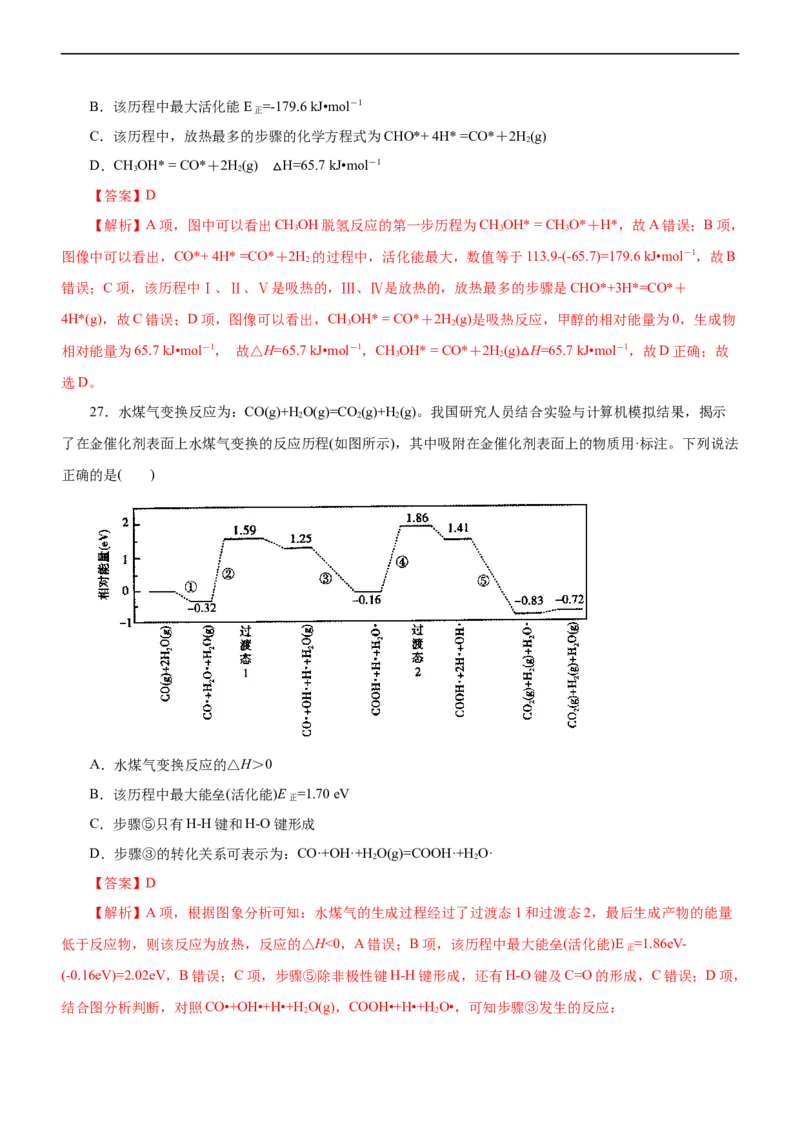
25.一种双功能结构催化剂能同时活化水和甲醇,用以解决氢气的高效存储和安全运输。下图是甲醇脱氢转化的反应历程( 表示过渡态)
下列说法不正确的是( )
A.CHOH的脱氢反应是分步进行的
3
B.甲醇脱氢反应历程的最大能垒(活化能)是0.95eV
C.甲醇脱氢反应中断裂了极性键和非极性键
D.该催化剂的研发为醇类重整产氢的工业应用提供了新思路
【答案】C
【解析】A项,读图知,CHOH的脱氢反应是分步进行的,故A正确;B项,能垒是发生某步反应需要
3
克服的能量,1.30-0.94=0.36、2.15-1.60=0.55,2.53-2.28=0.25、2.69-2.02=0.67、3.11-2.16=0.95,最大能垒(活化
能)是0.95eV,故B正确;C项,该历程为CHOH(g)=CO(g)+4H,没有非极性键断裂,故C错误;D项,该催化
3
剂的成功研发,对工业上的醇类重整产氢有重要的启示,对促进我国制氢工业的节能减排和氢能升级提供了新
思路,故D正确。故选C。
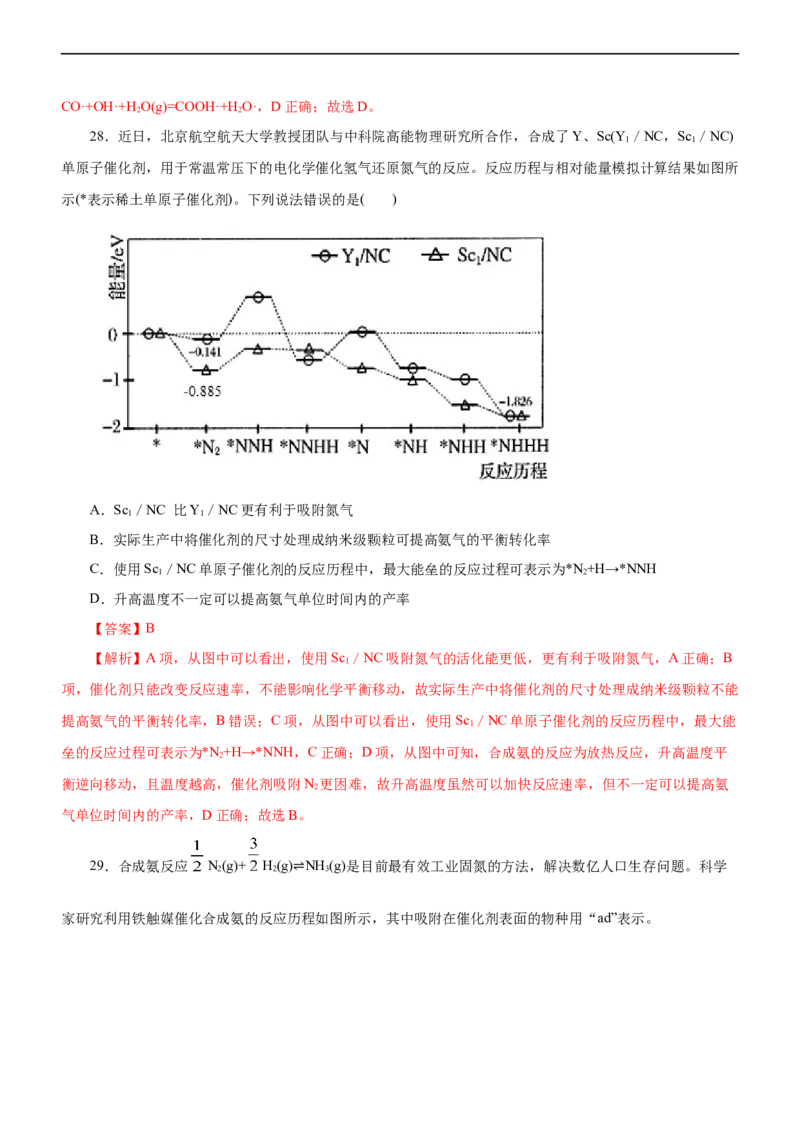
26.工业上可采用CHOH CO+2H 的方法来制取高纯度的CO和H。我国学者采用量子力学方法,
3 2 2
通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标
注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是( )
A.CHOH脱氢反应的第一步历程为CHOH* =CH*+OH*
3 3 3B.该历程中最大活化能E =-179.6 kJ•mol-1
正
C.该历程中,放热最多的步骤的化学方程式为CHO*+ 4H* =CO*+2H(g)
2
D.CHOH* = CO*+2H(g) H=65.7 kJ•mol-1
3 2
【答案】D △
【解析】A项,图中可以看出CHOH脱氢反应的第一步历程为CHOH* = CH O*+H*,故A错误;B项,
3 3 3
图像中可以看出,CO*+ 4H* =CO*+2H 的过程中,活化能最大,数值等于113.9-(-65.7)=179.6 kJ•mol-1,故B
2
错误;C项,该历程中Ⅰ、Ⅱ、Ⅴ是吸热的,Ⅲ、Ⅳ是放热的,放热最多的步骤是CHO*+3H*=CO*+
4H*(g),故C错误;D项,图像可以看出,CHOH* = CO*+2H(g)是吸热反应,甲醇的相对能量为0,生成物
3 2
相对能量为65.7 kJ•mol-1, 故△H=65.7 kJ•mol-1,CHOH* = CO*+2H(g) H=65.7 kJ•mol-1,故D正确;故
3 2
选D。 △
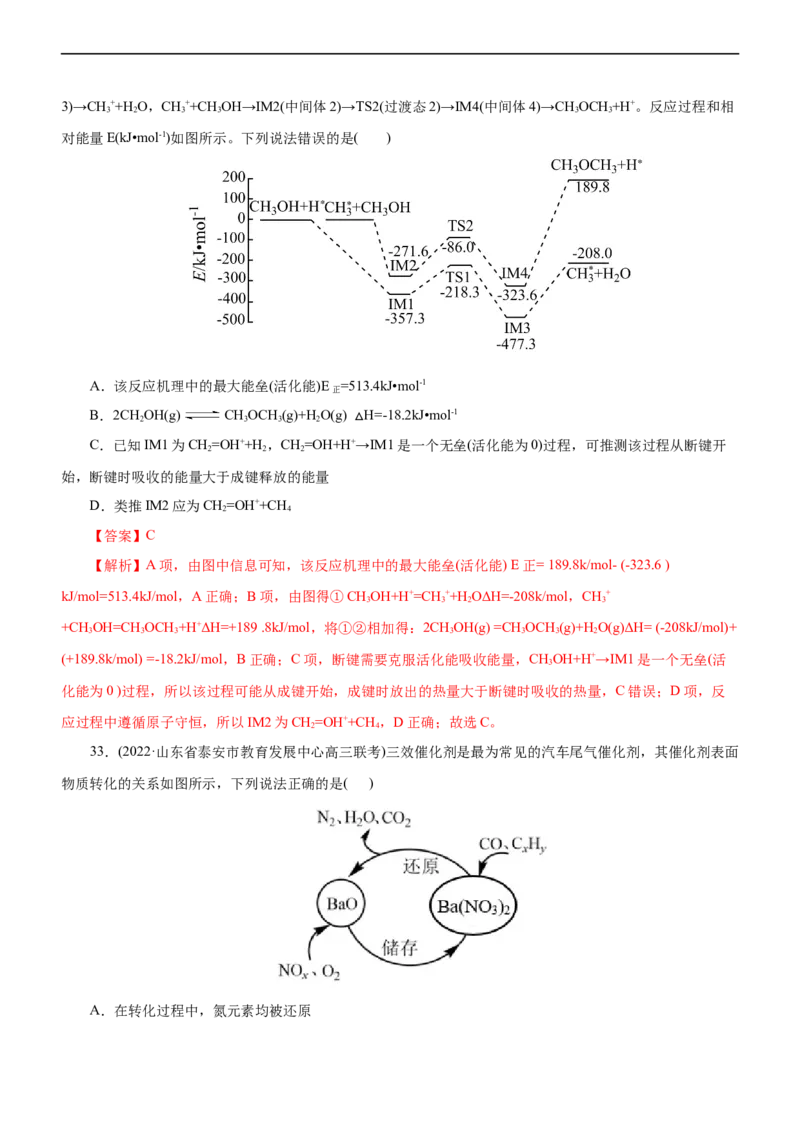
27.水煤气变换反应为:CO(g)+HO(g)=CO(g)+H(g)。我国研究人员结合实验与计算机模拟结果,揭示
2 2 2
了在金催化剂表面上水煤气变换的反应历程(如图所示),其中吸附在金催化剂表面上的物质用·标注。下列说法
正确的是( )
A.水煤气变换反应的△H>0
B.该历程中最大能垒(活化能)E =1.70 eV
正
C.步骤⑤只有H-H键和H-O键形成
D.步骤③的转化关系可表示为:CO·+OH·+H O(g)=COOH·+H O·
2 2
【答案】D
【解析】A项,根据图象分析可知:水煤气的生成过程经过了过渡态1和过渡态2,最后生成产物的能量
低于反应物,则该反应为放热,反应的△H<0,A错误;B项,该历程中最大能垒(活化能)E =1.86eV-
正
(-0.16eV)=2.02eV,B错误;C项,步骤⑤除非极性键H-H键形成,还有H-O键及C=O的形成,C错误;D项,
结合图分析判断,对照CO•+OH•+H•+H O(g),COOH•+H•+H O•,可知步骤③发生的反应:
2 2CO·+OH·+H O(g)=COOH·+H O·,D正确;故选D。
2 2
28.近日,北京航空航天大学教授团队与中科院高能物理研究所合作,合成了Y、Sc(Y /NC,Sc /NC)
1 1
单原子催化剂,用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所
示(*表示稀土单原子催化剂)。下列说法错误的是( )
A.Sc /NC 比Y/NC更有利于吸附氮气
1 1
B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氨气的平衡转化率
C.使用Sc /NC单原子催化剂的反应历程中,最大能垒的反应过程可表示为*N+H→*NNH
1 2
D.升高温度不一定可以提高氨气单位时间内的产率
【答案】B
【解析】A项,从图中可以看出,使用Sc /NC吸附氮气的活化能更低,更有利于吸附氮气,A正确;B
1
项,催化剂只能改变反应速率,不能影响化学平衡移动,故实际生产中将催化剂的尺寸处理成纳米级颗粒不能
提高氨气的平衡转化率,B错误;C项,从图中可以看出,使用Sc /NC单原子催化剂的反应历程中,最大能
1
垒的反应过程可表示为*N+H→*NNH,C正确;D项,从图中可知,合成氨的反应为放热反应,升高温度平
2
衡逆向移动,且温度越高,催化剂吸附N 更困难,故升高温度虽然可以加快反应速率,但不一定可以提高氨
2
气单位时间内的产率,D正确;故选B。
29.合成氨反应 N(g)+ H(g) NH (g)是目前最有效工业固氮的方法,解决数亿人口生存问题。科学
2 2 3
⇌
家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。下列说法错误的是( )
A.该合成氨反应的△H=-46 kJ/mol
B.活化能最大的一步反应的方程式为N +H =NH
ad ad ad
C.升高温度、增大压强均能提高原料的平衡转化率
D.加入催化剂能降低反应活化能,加快正反应速率
【答案】C
【解析】A项,合成氨反应中,反应物的总能量高于生成物的总能量,所以反应为放热反应,放热反应的
ΔH<0,故A正确;B项,从图中可以看出,活化能最大的一步反应是N +H =NH ,活化能高于106kJ/
ad ad ad
mol,故B正确;C项,合成氨反应是放热反应,升高温度,平衡逆向移动,降低原料的平衡转化率;合成氨
反应是气体体积减小的反应,增大压强,平衡正向移动,可以提高原料的平衡转化率,故C错误;D项,催化
剂能降低反应的活化能,加快正逆反应速率,故D正确;故选C。
30.我国科学家实现了在铜催化剂条件下将DMF[(CH )NCHO]转化为三甲胺[N(CH )]。计算机模拟单个
3 2 3 3
DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是( )
A.该历程中最小能垒的化学方程式为 (CH)NCH OH*=(CH)NCH +OH*
3 2 2 3 2 2
B.该历程中最大能垒(活化能)为2.16eV
C.该反应的热化学方程式为(CH)NCHO(g)+2H(g)=N(CH )(g)+HO(g) ΔH=-1.02ev•mol-1
3 2 2 3 3 2
D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率
【答案】A
【解析】从图中可以看出,在正向进行的三个反应中,其能垒分别为:-1.23-(-2.16)=0.93、-1.55-
(-1.77)=0.22、-1.02-(-2.21)=1.19。A项,从以上分析知,该历程中最小能垒为0.22,是由(CH)NCH OH*转化
3 2 2为(CH)NCH 的反应,化学方程式为 (CH)NCH OH*=(CH)NCH +OH*,A正确;B项,该历程中最大能
3 2 2 3 2 2 3 2 2
垒(活化能)为1.19eV,B不正确;C项,该反应的总反应是由(CH)NCHO(g)转化为N(CH )(g),但1.02ev•为
3 2 3 3
单个(CH)NCHO(g)反应时放出的热量,所以热化学方程式为(CH)NCHO(g)+2H(g)=N(CH )(g)+HO(g)
3 2 3 2 2 3 3 2
ΔH=-1.02N ev•mol-1,C不正确;D项,增大压强或升高温度均能加快反应速率,但升高温度平衡逆向移动,
A
不能增大DMF平衡转化率,D不正确;故选A。
31.研究表明NO (g)与CO(g)在 作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是(
2
)
A.未使用催化剂时,该反应的逆反应活化能为557.8
B.催化剂参与的两步反应均为放热反应
C.NO、CO、 夺取O的能力依次增大
2
D.总反应的热化学方程式为NO(g)+CO (g)=N (g)+CO (g) H=-358.9kJ·mol-1
2 2 2
【答案】C △
【详解】A项,根据历程,反应物总能量大于生成物的总能量,即该反应为放热反应,逆反应的活化能
358.9kJ·mol-1+198.9kJ·mol-1=557.8kJ·mol-1,故A正确;B项,由图可知,在Ir+催化下,两步反应能量均降
低,均为放热反应,故B正确;C项,从NO+Ir++CO到N+IrO++CO,说明Ir+夺取O的能量强于NO,
2 2 2
从N+IrO++CO到N+CO+Ir+,说明CO夺取O的能力强于IrO+,故C错误;D项,△H只与始态和终态
2 2 2
有关,与反应的途径无关,因此总反应的热化学方程式为NO(g)+CO(g)=N(g)+CO(g) H=-358.9kJ·mol-
2 2 2
1,故D正确;故选C。 △
32.(2022·辽宁省铁岭市六校高三联考)我国某科研团队通过计算机模拟技术提出在12—磷钨酸(固体强酸)
催化作用下甲醇气相脱水合成二甲醚的反应机理:CHOH+H+→IM1(中间体1)→TS1(过渡态1)→IM3(中间体
33)→CH++H O,CH++CH OH→IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CHOCH +H+。反应过程和相
3 2 3 3 3 3
对能量E(kJ•mol-1)如图所示。下列说法错误的是( )
A.该反应机理中的最大能垒(活化能)E =513.4kJ•mol-1
正
B.2CHOH(g) CHOCH (g)+HO(g) H=-18.2kJ•mol-1
2 3 3 2
C.已知IM1为CH
2
=OH++H
2
,CH
2
=OH+H+△→IM1是一个无垒(活化能为0)过程,可推测该过程从断键开
始,断键时吸收的能量大于成键释放的能量
D.类推IM2应为CH=OH++CH
2 4
【答案】C
【解析】A项,由图中信息可知,该反应机理中的最大能垒(活化能) E正= 189.8k/mol- (-323.6 )
kJ/mol=513.4kJ/mol,A正确;B项,由图得①CHOH+H+=CH ++H OΔH=-208k/mol,CH+
3 3 2 3
+CH OH=CH OCH +H+ΔH=+189 .8kJ/mol,将①②相加得:2CHOH(g) =CHOCH (g)+HO(g)ΔH= (-208kJ/mol)+
3 3 3 3 3 3 2
(+189.8k/mol) =-18.2kJ/mol,B正确;C项,断键需要克服活化能吸收能量,CHOH+H+→IM1是一个无垒(活
3
化能为0 )过程,所以该过程可能从成键开始,成键时放出的热量大于断键时吸收的热量,C错误;D项,反
应过程中遵循原子守恒,所以IM2为CH=OH++CH ,D正确;故选C。
2 4
33.(2022·山东省泰安市教育发展中心高三联考)三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面
物质转化的关系如图所示,下列说法正确的是( )
A.在转化过程中,氮元素均被还原B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1 mol N,转移0.5 mol电子
2
D.三效催化剂能有效实现汽车尾气中CO、C H、NO 三种成分的净化
x y x
【答案】D
【解析】A项,根据图示可知,NO 与BaO、O 转化成Ba(NO ) 的过程中,N元素化合价升高被氧化,故
x 2 3 2
A错误; B项,根据图示可知,BaO为催化剂,NO 与BaO、O 转化成Ba(NO ) 时,BaO参与储存N元素,
x 2 3 2
故B错误;C项,还原过程中生成0.1 mol N,转移电子的物质的量为0.1 mol×(5-0)×2=1 mol,故C错误;D
2
项,整个过程中,CO、C H、NO 转化成CO、HO、N,说明三效催化剂能有效实现汽车尾气中CO、
x y x 2 2 2
C H、NO 三种成分的净化,故D正确;故选D。
x y x
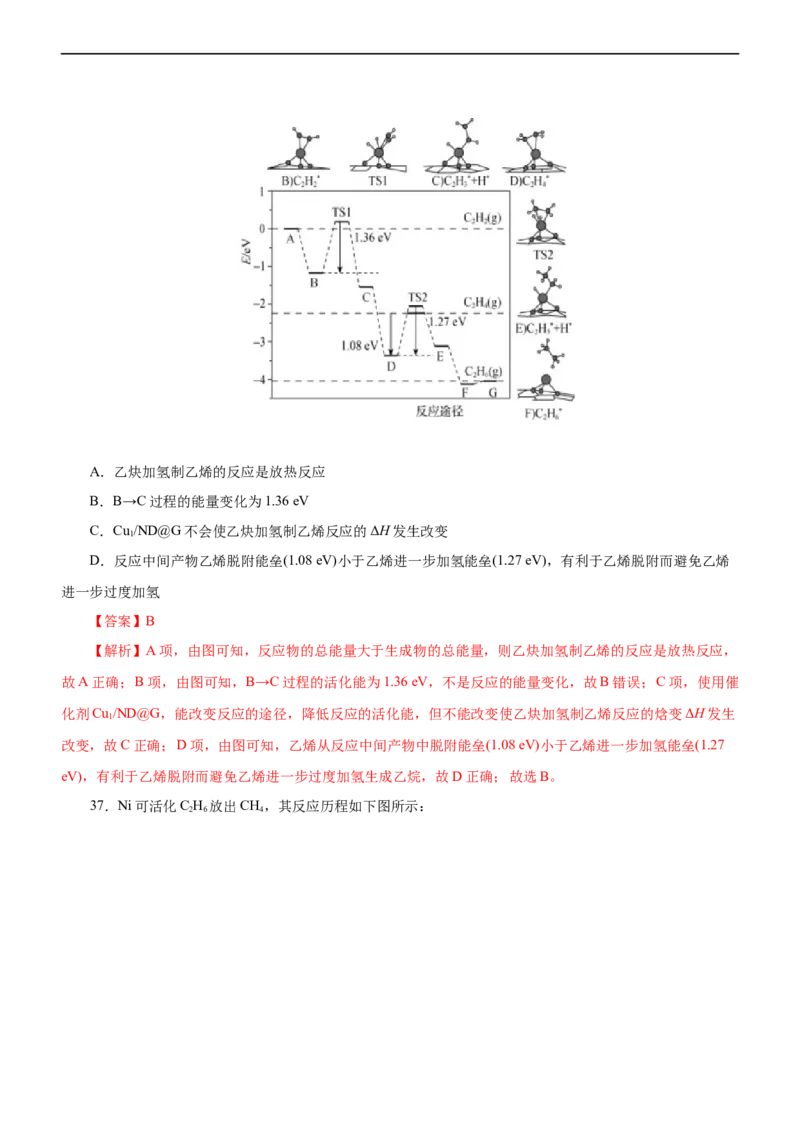
34.(2022·内蒙古新城一模)硫酸盐(含SO 2-、HSO -)气溶胶是PM2.5的成分之一、科研人员提出了雾霾微
4 4
粒中硫酸盐生成的三个阶段的转化机理,其主要过程如图所示,下列说法不正确的是( )
A.HNO、NO 、HO均只含有极性共价键
2 2 2
B.该过程中NO -为中间产物
2
C.总反应SO 2-+2NO+H O=HSO -+NO-+HNO
3 2 2 4 2 2
D.还原性SO ->HNO
3 2
【答案】B
【解析】A项,HNO 含有氮氧键、氧氢键,NO 含有氮氧键,HO含有氢氧键,三者都只含有极性共价
2 2 2
键,故A正确;B项,反应中第一个阶段是SO 2-+NO=SO-+NO-,第二个阶段是SO -+NO+H O=HSO -
3 2 3 2 3 2 2 4
+HNO ,两个阶段总反应SO 2-+2NO+H O=HSO -+NO-+HNO ,因此NO -为反应产物,不是中间产物,故B错
2 3 2 2 4 2 2 2
误;C项,根据B选项的分析的总反应为SO 2-+2NO+H O=HSO -+NO-+HNO ,故C正确;D项,根据第二个
3 2 2 4 2 2
阶段反应SO -+NO+H O=HSO -+HNO ,得到还原性SO ->HNO,故D正确。故选B。
3 2 2 4 2 3 2
35.最新研究表明,在多孔炭材料,上搭载活性组分催化氧化脱硫效果明显优于传统方法,其反应机理如
图所示,此时 在水中浓度为0.34g/100mL。下列有关说法正确的是( )A.温度过高不利于脱硫的效果 B.活性炭作用是降低反应物的总能量
C.该反应的总反应是吸热过程 D.该温度下, 的
【答案】A
【解析】A项,温度过高,HS和溶解氧的溶解度下降,不利于脱硫的效果,A项正确;B项,根据题目
2
信息,活性炭具有催化氧化效果,可降低反应的活化能,但不能降低反应物的总能量,B项错误;C项,由图
可知,该反应的总反应方程式为2HS+O=2H O+2S↓,反应的 ,反应能自发进行说明 ,
2 2 2
,则反应的 ,总反应为放热反应,C项错误;D项, 在水中浓度为0.34g/100mL,即
,由图可知 ,故 ,
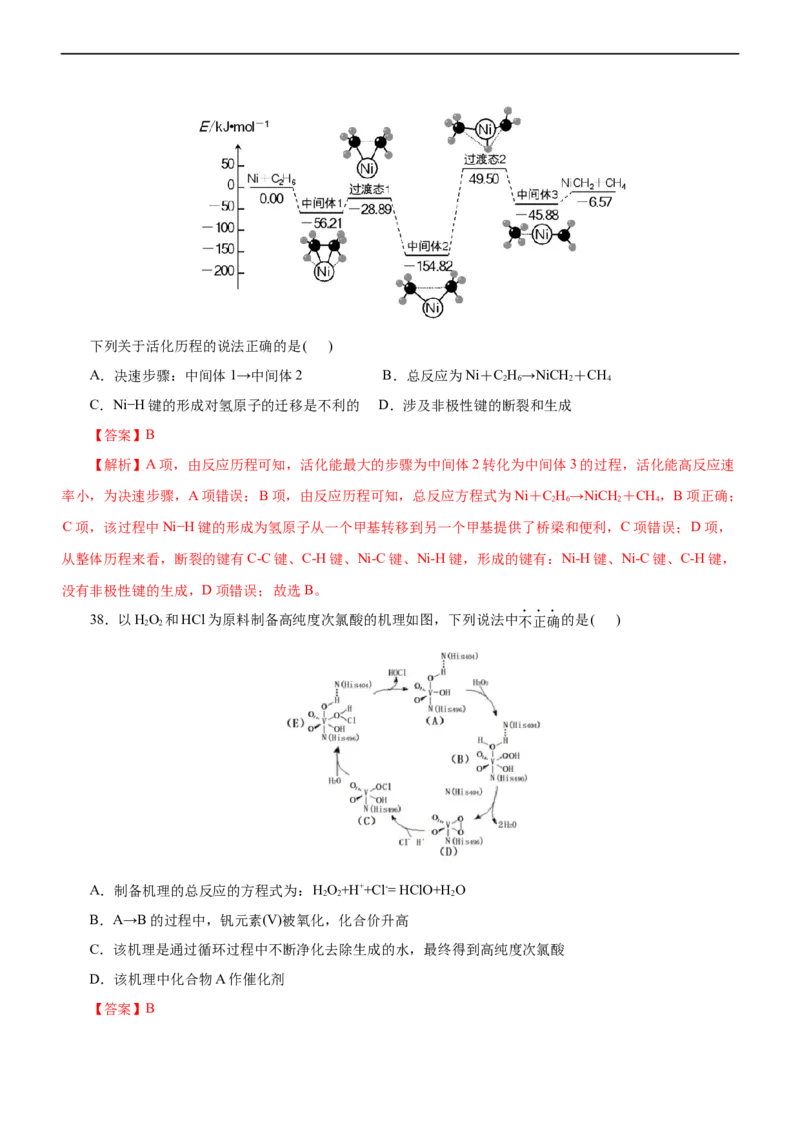
D项错误;故选A。 36.乙炔选择性加氢是工业上重要催化反应之一、原子级分散的Cu催化剂Cu /ND@G
1
在乙炔氢化反应中,可有效促进乙炔的活化和乙烯的脱附,过程如下图所示。下列说法错误的是( )A.乙炔加氢制乙烯的反应是放热反应
B.B→C过程的能量变化为1.36 eV
C.Cu /ND@G不会使乙炔加氢制乙烯反应的ΔH发生改变
1
D.反应中间产物乙烯脱附能垒(1.08 eV)小于乙烯进一步加氢能垒(1.27 eV),有利于乙烯脱附而避免乙烯
进一步过度加氢
【答案】B
【解析】A项,由图可知,反应物的总能量大于生成物的总能量,则乙炔加氢制乙烯的反应是放热反应,
故A正确;B项,由图可知,B→C过程的活化能为1.36 eV,不是反应的能量变化,故B错误;C项,使用催
化剂Cu /ND@G,能改变反应的途径,降低反应的活化能,但不能改变使乙炔加氢制乙烯反应的焓变ΔH发生
1
改变,故C正确;D项,由图可知,乙烯从反应中间产物中脱附能垒(1.08 eV)小于乙烯进一步加氢能垒(1.27
eV),有利于乙烯脱附而避免乙烯进一步过度加氢生成乙烷,故D正确;故选B。
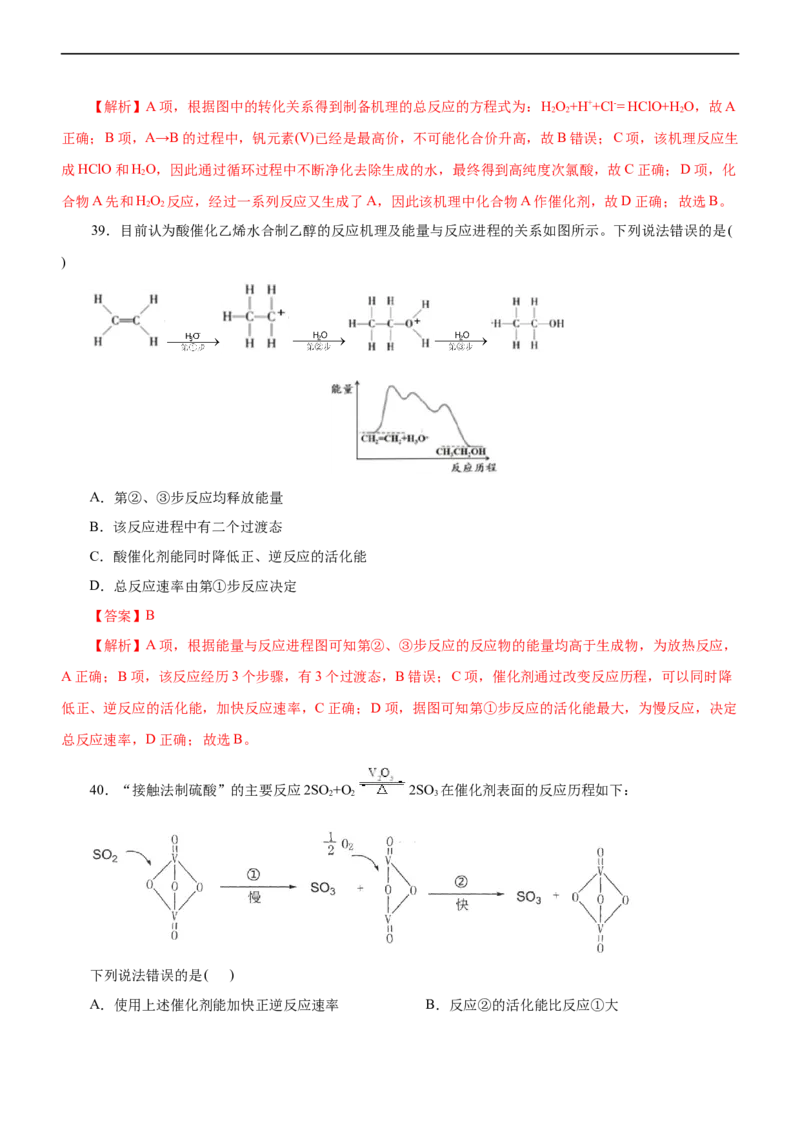
37.Ni可活化C H 放出CH,其反应历程如下图所示:
2 6 4下列关于活化历程的说法正确的是( )
A.决速步骤:中间体1→中间体2 B.总反应为Ni+C H→NiCH+CH
2 6 2 4
C.Ni−H键的形成对氢原子的迁移是不利的 D.涉及非极性键的断裂和生成
【答案】B
【解析】A项,由反应历程可知,活化能最大的步骤为中间体2转化为中间体3的过程,活化能高反应速
率小,为决速步骤,A项错误;B项,由反应历程可知,总反应方程式为Ni+C H→NiCH+CH,B项正确;
2 6 2 4
C项,该过程中Ni−H键的形成为氢原子从一个甲基转移到另一个甲基提供了桥梁和便利,C项错误;D项,
从整体历程来看,断裂的键有C-C键、C-H键、Ni-C键、Ni-H键,形成的键有:Ni-H键、Ni-C键、C-H键,
没有非极性键的生成,D项错误;故选B。
38.以HO 和HCl为原料制备高纯度次氯酸的机理如图,下列说法中不正确的是( )
2 2
A.制备机理的总反应的方程式为:HO+H++Cl-= HClO+HO
2 2 2
B.A→B的过程中,钒元素(V)被氧化,化合价升高
C.该机理是通过循环过程中不断净化去除生成的水,最终得到高纯度次氯酸
D.该机理中化合物A作催化剂
【答案】B【解析】A项,根据图中的转化关系得到制备机理的总反应的方程式为:HO+H++Cl-= HClO+HO,故A
2 2 2
正确;B项,A→B的过程中,钒元素(V)已经是最高价,不可能化合价升高,故B错误;C项,该机理反应生
成HClO和HO,因此通过循环过程中不断净化去除生成的水,最终得到高纯度次氯酸,故C正确;D项,化
2
合物A先和HO 反应,经过一系列反应又生成了A,因此该机理中化合物A作催化剂,故D正确;故选B。
2 2
39.目前认为酸催化乙烯水合制乙醇的反应机理及能量与反应进程的关系如图所示。下列说法错误的是(
)
A.第②、③步反应均释放能量
B.该反应进程中有二个过渡态
C.酸催化剂能同时降低正、逆反应的活化能
D.总反应速率由第①步反应决定
【答案】B
【解析】A项,根据能量与反应进程图可知第②、③步反应的反应物的能量均高于生成物,为放热反应,
A正确;B项,该反应经历3个步骤,有3个过渡态,B错误;C项,催化剂通过改变反应历程,可以同时降
低正、逆反应的活化能,加快反应速率,C正确;D项,据图可知第①步反应的活化能最大,为慢反应,决定
总反应速率,D正确;故选B。
40.“接触法制硫酸”的主要反应2SO +O 2SO 在催化剂表面的反应历程如下:
2 2 3
下列说法错误的是( )
A.使用上述催化剂能加快正逆反应速率 B.反应②的活化能比反应①大C.过程中既有V-O键的断裂,也有V-O键的形成 D.该反应的催化剂是VO
2 5
【答案】B
【解析】A项,催化剂能同等程度加快正逆反应速率,故A正确;B项,活化能越大反应越慢,反应②的
活化能比反应①小,故B错误;C项,反应①有V-O键的断裂,反应②有V-O键的形成,故C正确;D项,
根据图示, VO 是该反应的催化剂,故D正确;故选B。
2 5
1.(2023·浙江省山水联盟高三开学考试)我国科学家通过双功能催化剂催化水煤气变换反应:CO(g)
+H O(g) CO(g)+H(g) H<0,此时该反应总熵变记作△S。低温即可获得高转化率和高反应速率,反
2 2 2
应过程示意图如图: △
下列说法不正确的是( )
A.△H= H+ H+ H+ H
1 2 3 4
B.△S=△S
1
+ △S
2
+ △S
3
+ △S
4
C.状态△III→状△态△IV过△程的△S
3
<0,△H
3
<0
D.催化剂的使用使反应放出热量增多,温度升高导致反应速率加快
【答案】D
【解析】A项,根据盖斯定律,状态Ⅰ至Ⅴ之和等于总反应,则△H= H+ H+ H+ H,A正确;B项,
1 2 3 4
由A分析可知,△S= S+ S+ S+ S,B正确;C项,状态III→状态IV△反应△后微粒△数减△少,△S<0;总反
1 2 3 4 3
应为放热反应,状态Ⅰ△→状△态Ⅱ△、状△态Ⅱ→状态III、状态IV→状态V分别涉及断键、断键、脱离过程均为吸
热过程,则.状态III→状态IV为放热过程,△H<0,C正确;D项,催化剂的使用不会改变反应的焓变,D
3
错误;故选D。
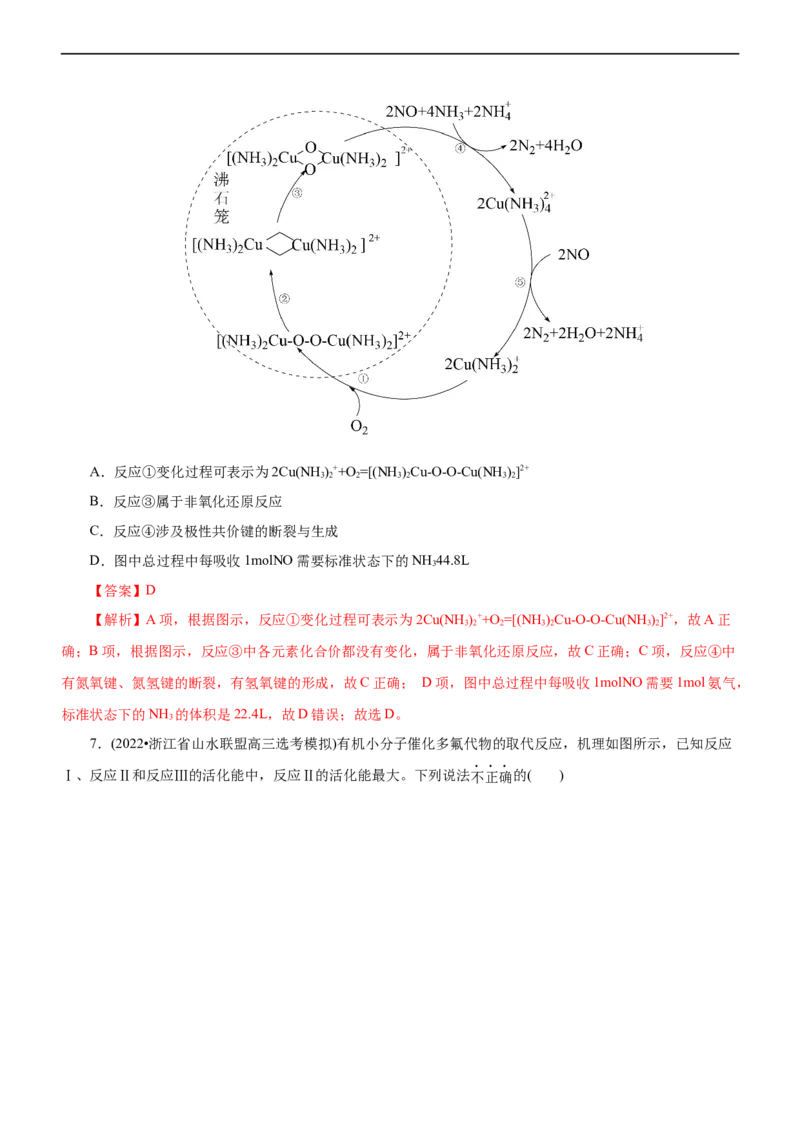
2.(2022·河南省重点中学高三模拟调研)利用烟气中SO 可回收废水中的 ,实现碘单质的再生,其反应
2
原理如下图所示下列说法错误的是( )
A.[(NH )C -O-O-C (NH )]4+中Co的化合价为+3价
3 5 O O 3 5
B.总反应离子方程式为:SO +O +2I-=I +SO2-
2 2 2 4
C.反应①~⑤中均有电子的转移
D.反应③中,每消耗1molO 会转移2mol电子
2
【答案】C
【解析】A项,[(NH )C -O-O-C (NH )]4+中含有过氧键,故氧元素显-1价,由化合价规则知A项正确;B
3 5 O O 3 5
项,由题干信息及工作原理图知,反应物有SO 、O、I-,生成物是I、SO 2-,B项正确;C项,过程②和⑤中
2 2 2 4
没有电子转移,C项错误;D项,反应③中O 得到电子后转化为过氧键,D项正确。故选C。
2
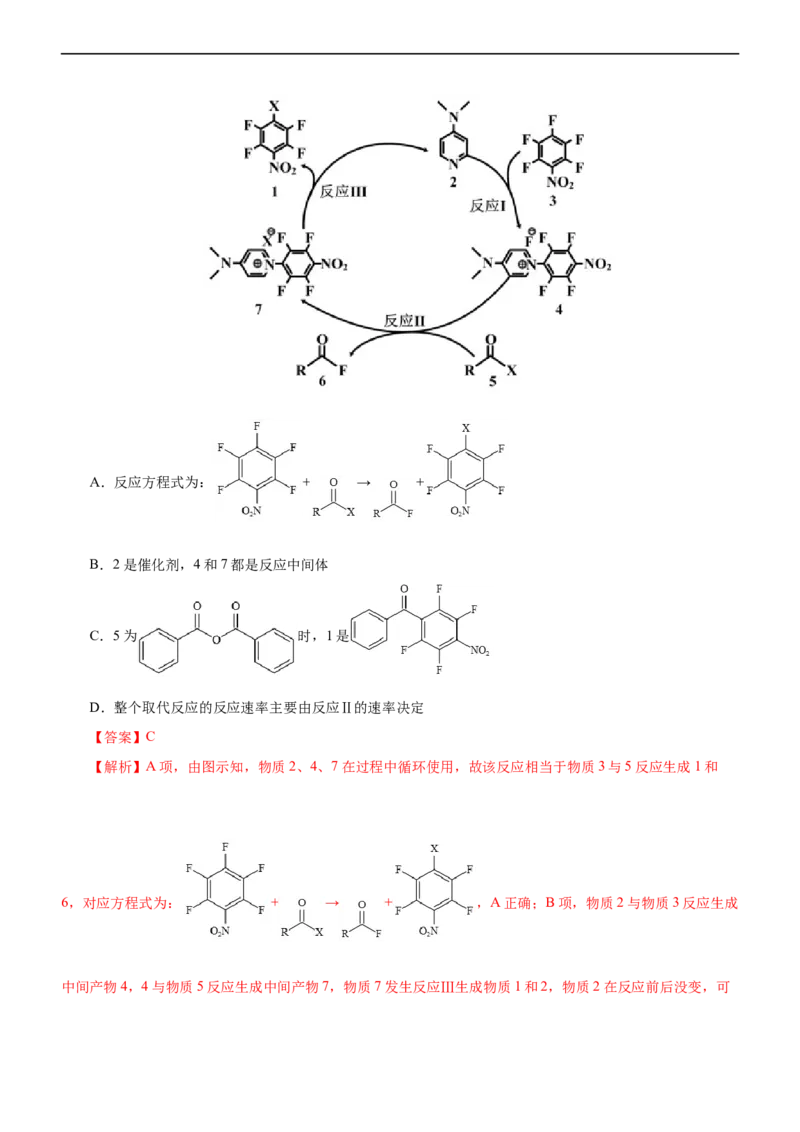
3.(2022·重庆市育才中学高三期中)让天更蓝、山更绿、水更清,化学在行动。利用Cu-ZSM-5分子筛催
化剂,NH 可脱除燃煤烟气中的NO和NO ,生成两种无毒物质,反应历程如图,下列说法错误的是( )
3 2
A.过程Ⅰ、Ⅱ发生的是非氧化还原反应
B.过程Ⅲ中X为N,它既是氧化产物,又是还原产物
2
C.过程Ⅳ中,每生成0.1molH+,转移的电子数为0.15N
A
D.上述历程的总反应为2NH +NO+NO 2N+3H O
3 2 2 2
【答案】C
【解析】A项,过程Ⅰ、Ⅱ中,元素化合价均没有发生变化,都是非氧化还原反应,故A正确;B项,过
程Ⅲ中生成X的离子方程式是[(NH )(NO )]2++NO=[(NH )(HNO)]++X+H++H O,根据元素守恒,X是 N,
4 2 2 4 2 2 2 2[(NH )(NO )]2+中N的化合价升高、NO中N的化合价降低,所以它既是氧化产物又是还原产物,故B正确;C
4 2 2
项,过程Ⅳ发生反应的离子方程式是[(NH )(HNO)]+=N +2H O+H+,N元素化合价由+3降低为0、由-3升高为
4 2 2 2 2
0,每生成1molH+转移3mol电子,所以每生成0.1molH+转移的电子数为0.3N ,故C错误;D项,根据图示
A
可知总反应为2NH +NO+NO 2N+3H O,故D正确;选C。
3 2 2 2
4.(2022·江西省赣州市十六县市十七校高三期中联考)工业上除去电石渣浆(含CaO)上清液中的S2-,并制
取石膏(CaSO•2H O)的常用流程如图:
4 2
常温下,饱和石灰水的物质的量浓度为0.002mol•L-1,下列说法不正确的是( )
A.Mn(OH) 在过程Ⅰ中作还原剂,SO2-在过程Ⅱ中是氧化产物
2 2 3
B.将10L上清液中的S2-直接被O 氧化为SO 2-(S2-浓度为480mg•L-1),理论上共需要0.3mol的O
2 4 2
C.由过程Ⅰ可知,O 的氧化性强于MnO 2-
2 3
D.常温下,56gCaO溶于水配成1L溶液,溶液中Ca2+的数目为N 个
A
【答案】D
【解析】A项,Mn(OH) 在过程I化合价升高,作还原剂,由流程可知过程Ⅱ中,反应的离子方程式为4
2
MnO 2-+2S2-+9H O═S O2-+4Mn(OH) ↓+10OH-,S元素化合价升高,则S2O32-是氧化产物,故A正确。B项,
3 2 2 3 2
将10L上清液中的S2-转化为SO 2- (S2-浓度为480mg•L-1),质量为480mg•L-1×10L=3800mg=4.8g,物质的量为
4
,根据得失电子守恒0.15mol×8=n(O )×4,n(O )=0.3mol,理论上共需要0.3mol的
2 2
O,故B正确;C项,过程I反应的离子方程式为2Mn(OH) +O +4OH-=2 MnO 2-+4H O,O元素化合价降低,
2 2 2 3 2
O 做氧化剂,MnO 2-是氧化产物,则O 的氧化性强于MnO 2-,故C正确;D项,常温下,饱和石灰水的物质
2 3 2 3
的量浓度为0.002mol•L-1,因此56gCaO溶于水配成1L溶液,是饱和溶液,因此1L溶液中Ca2+的数目为
0.002N 个,故D错误;故选D。
A
5.(2022·山东省临沂市高三期中联考)某种含铜的催化剂[Cu(OH)(NH )]+可用于汽车尾气脱氮,催化机理
3
如图所示。下列说法正确的是( )A.每一步骤只存在铜和氮元素之间的电子转移
B.该催化循环中Cu的成键数目没有发生变化
C.反应过程中存在非极性键的断裂和形成
D.总反应的化学方程式为4NH +2NO+2O 3N 6HO
3 2 2+ 2
【答案】C
【解析】A项,步骤存在铜、氧和氮元素之间的电子转移,故A错误;B项,[Cu(OH)(NH )]+中Cu的成
3
键数目为2,[Cu(OH)(NH )]+中Cu的成键数目为4,故B错误;C项,反应过程中有氧气参加反应,断裂氧氧
3
非极性键,有氮气生成,形成氮氮非极性键,故C正确;D项,根据图,加入2NH 、2NO、 O 生成2N、
3 2 2
3HO,该脱硝过程的总反应的化学方程式为4NH +4NO+O 4N 6HO,D说法错误。 故选C。
2 3 2 2+ 2
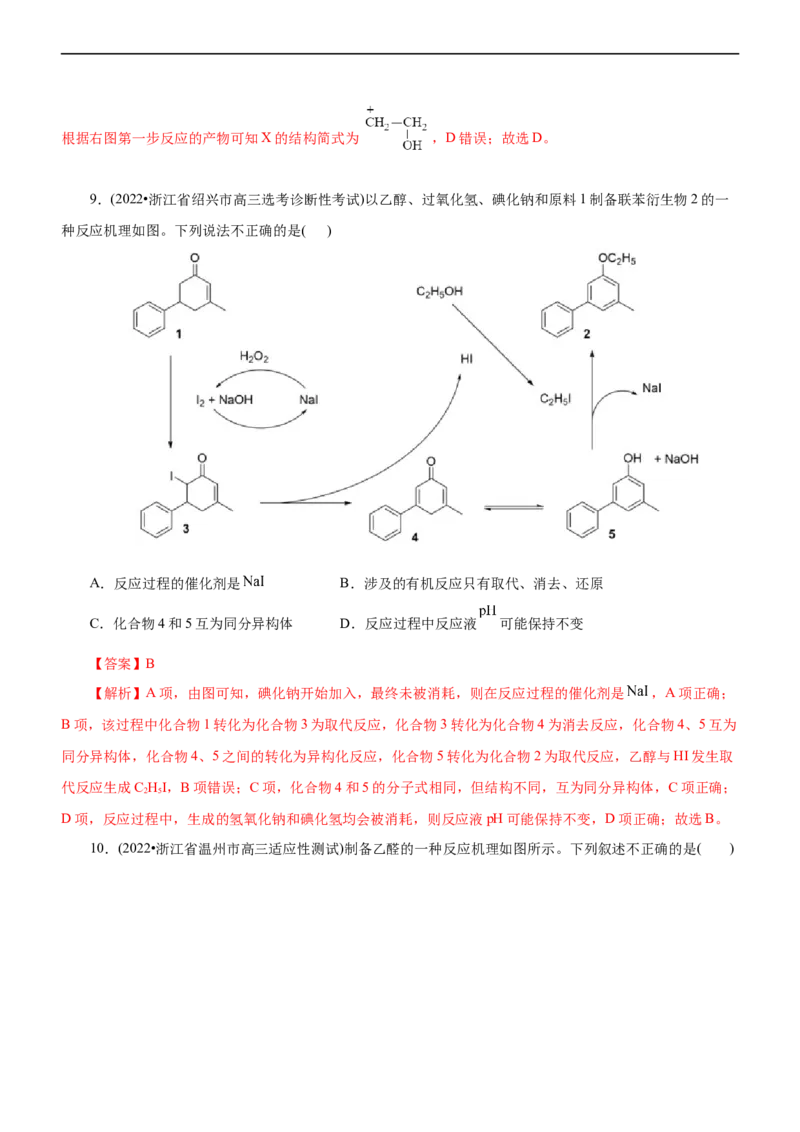
6.(2022·湖北省部分市州高三期末联合调研考试)氮氧化物(NO )是一类特殊的污染物,它本身会对生态系
x
统和人体健康造成危害。一种以沸石笼作为载体对氮氧化物进行催化还原的原理如图所示。下列叙述错误的是
( )A.反应①变化过程可表示为2Cu(NH )++O =[(NH )Cu-O-O-Cu(NH )]2+
3 2 2 3 2 3 2
B.反应③属于非氧化还原反应
C.反应④涉及极性共价键的断裂与生成
D.图中总过程中每吸收1molNO需要标准状态下的NH 44.8L
3
【答案】D
【解析】A项,根据图示,反应①变化过程可表示为2Cu(NH )++O =[(NH )Cu-O-O-Cu(NH )]2+,故A正
3 2 2 3 2 3 2
确;B项,根据图示,反应③中各元素化合价都没有变化,属于非氧化还原反应,故C正确;C项,反应④中
有氮氧键、氮氢键的断裂,有氢氧键的形成,故C正确; D项,图中总过程中每吸收1molNO需要1mol氨气,
标准状态下的NH 的体积是22.4L,故D错误;故选D。
3
7.(2022•浙江省山水联盟高三选考模拟)有机小分子催化多氟代物的取代反应,机理如图所示,已知反应
Ⅰ、反应Ⅱ和反应Ⅲ的活化能中,反应Ⅱ的活化能最大。下列说法不正确的( )A.反应方程式为: + → +
B.2是催化剂,4和7都是反应中间体
C.5为 时,1是
D.整个取代反应的反应速率主要由反应Ⅱ的速率决定
【答案】C
【解析】A项,由图示知,物质2、4、7在过程中循环使用,故该反应相当于物质3与5反应生成1和
6,对应方程式为: + → + ,A正确;B项,物质2与物质3反应生成
中间产物4,4与物质5反应生成中间产物7,物质7发生反应Ⅲ生成物质1和2,物质2在反应前后没变,可看作催化剂,4、7为中间产物,B正确;C项,若物质5为 ,即结构-X为
,则物质1为: ,C错误;D项,相同条件下,反应活化能越大,普
通分子变成活化分子越难,反应速率越慢,由于反应Ⅱ活化能最大,故整个过程的反应速率由反应Ⅱ速率决定,
D正确;故选C。
8.(2022•浙江省稽阳联谊学校高三联考)酸性条件下,环氧乙烷水合法制备乙二醇涉及的机理如下:
下列说法不正确的是( )
A.制备乙二醇的总反应为 +H O
2
B.环氧乙烷能与二氧化碳反应生成可降解的有机物
C.二甘醇的分子式是C H O
4 10 3
D.X的结构简式为
【答案】D
【解析】A项,根据左图可知,流程中加入的反应物为环氧乙烷和水,氢离子为催化剂,产物为乙二醇,
总反应为 +H O ,A正确;B项,根据生成乙二醇的机理可知,环氧乙烷可以和
2
二氧化碳发生类似的加成反应,得到含有酯基的有机物,酯基可以在碱性环境中彻底水解,B正确;C项,参
考生成乙二醇的机理,可知二甘醇的结构简式为HOCH CHOCH CHOH,分子式是C H O,C正确;D项,
2 2 2 2 4 10 3根据右图第一步反应的产物可知X的结构简式为 ,D错误;故选D。
9.(2022•浙江省绍兴市高三选考诊断性考试)以乙醇、过氧化氢、碘化钠和原料1制备联苯衍生物2的一
种反应机理如图。下列说法不正确的是( )
A.反应过程的催化剂是 B.涉及的有机反应只有取代、消去、还原
C.化合物4和5互为同分异构体 D.反应过程中反应液 可能保持不变
【答案】B
【解析】A项,由图可知,碘化钠开始加入,最终未被消耗,则在反应过程的催化剂是 ,A项正确;
B项,该过程中化合物1转化为化合物3为取代反应,化合物3转化为化合物4为消去反应,化合物4、5互为
同分异构体,化合物4、5之间的转化为异构化反应,化合物5转化为化合物2为取代反应,乙醇与HI发生取
代反应生成C HI,B项错误;C项,化合物4和5的分子式相同,但结构不同,互为同分异构体,C项正确;
2 5
D项,反应过程中,生成的氢氧化钠和碘化氢均会被消耗,则反应液pH可能保持不变,D项正确;故选B。
10.(2022•浙江省温州市高三适应性测试)制备乙醛的一种反应机理如图所示。下列叙述不正确的是( )A.反应过程涉及氧化反应
B.化合物2和化合物4互为同分异构体
C.可以用乙烯和氧气为原料制备乙醛
D.PdCl 需要转化为PdCl 2-才能催化反应的进行
2 4
【答案】B
【解析】A项,根据图示可知:在反应过程中发生反应:Cu+被O 氧化产生Cu2+,O 得到电子被还原产生
2 2
HO,该反应就是氧化还原反应,A正确;B项,化合物2和化合物4分子式不同,因此二者不是同分异构体,
2
B错误;C项,乙烯和氧气在一定条件下发生反应产生乙醛、水,故可以乙烯和氧气为原料制备乙醛,C正确
D项,根据图示可知:PdCl 需要转化为PdCl 2-,然后再催化反应的进行,D正确;故选B。
2 4
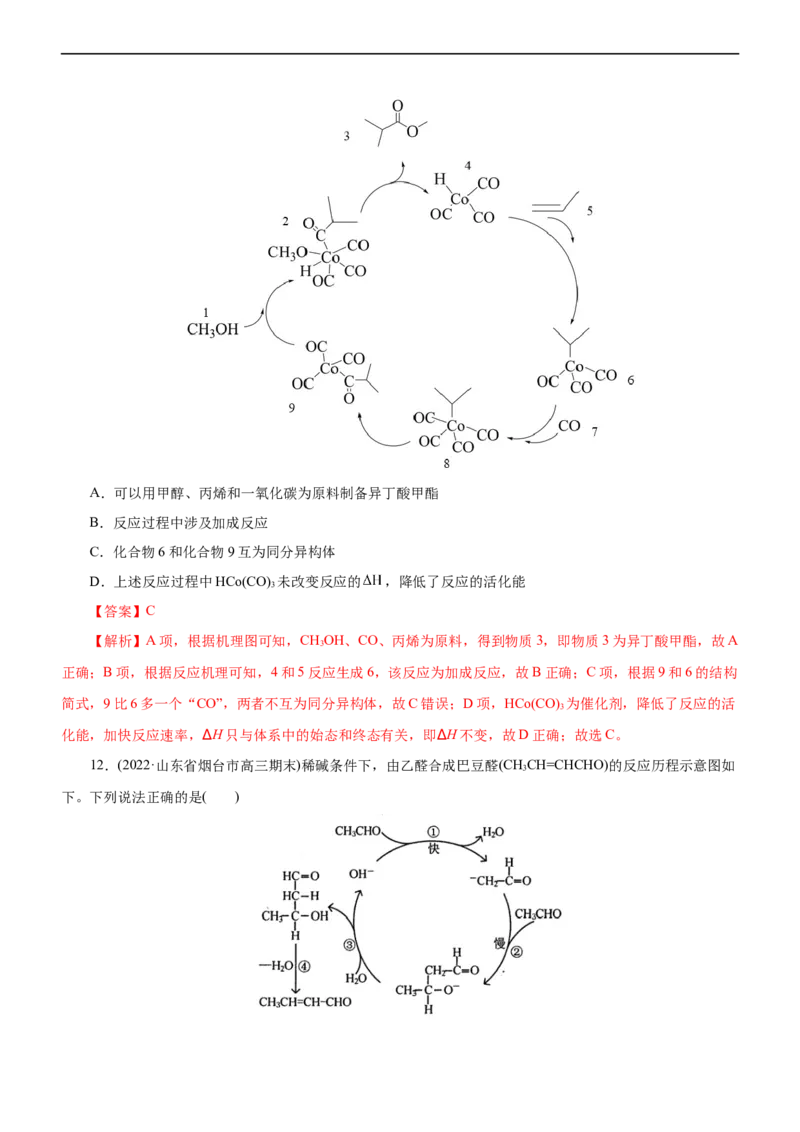
11.(2022•浙江省嘉兴市高三选考模拟测试)制备异丁酸甲酯的某种反应机理如图所示。下列说法不正确的
是( )A.可以用甲醇、丙烯和一氧化碳为原料制备异丁酸甲酯
B.反应过程中涉及加成反应
C.化合物6和化合物9互为同分异构体
D.上述反应过程中HCo(CO) 未改变反应的 ,降低了反应的活化能
3
【答案】C
【解析】A项,根据机理图可知,CHOH、CO、丙烯为原料,得到物质3,即物质3为异丁酸甲酯,故A
3
正确;B项,根据反应机理可知,4和5反应生成6,该反应为加成反应,故B正确;C项,根据9和6的结构
简式,9比6多一个“CO”,两者不互为同分异构体,故C错误;D项,HCo(CO) 为催化剂,降低了反应的活
3
化能,加快反应速率,∆H只与体系中的始态和终态有关,即∆H不变,故D正确;故选C。
12.(2022·山东省烟台市高三期末)稀碱条件下,由乙醛合成巴豆醛(CHCH=CHCHO)的反应历程示意图如
3
下。下列说法正确的是( )A.苯甲醛也能发生类似反应
B.反应①的活化能大于反应②的活化能
C.反应中,OH-、HO均为反应催化剂
2
D.由上述历程可知醛基 的酸性强于醇羟基
【答案】D
【解析】A项,苯甲醛无 ,不能发生类似反应,故A错误;B项,反应①较快,反应②较慢,反应越
慢活化能越大,故B错误;C项,由图中可知,OH-为反应的催化剂,HO为反应的中间产物,故C错误;D
2
项,由上述历程可知,CHCHO可制得 ,故可知醛基 的酸性强于醇羟基,故D正确;故选D。
3
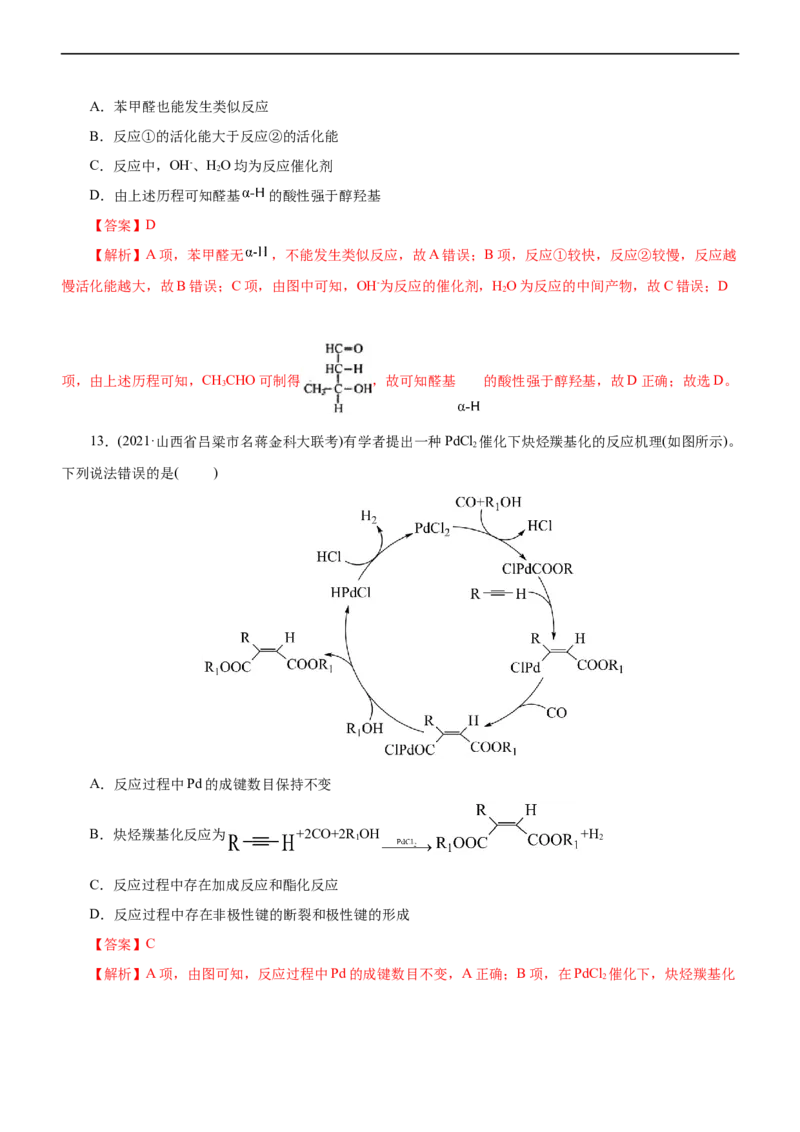
13.(2021·山西省吕粱市名蒋金科大联考)有学者提出一种PdCl 催化下炔烃羰基化的反应机理(如图所示)。
2
下列说法错误的是( )
A.反应过程中Pd的成键数目保持不变
B.炔烃羰基化反应为 +2CO+2R OH +H
1 2
C.反应过程中存在加成反应和酯化反应
D.反应过程中存在非极性键的断裂和极性键的形成
【答案】C
【解析】A项,由图可知,反应过程中Pd的成键数目不变,A正确;B项,在PdCl 催化下,炔烃羰基化
2反应为 +2CO+2R OH +H ,B正确;C项,反应过程中不存在酯化
1 2
反应,C错误;D项,反应过程中存在碳碳非极性键的断裂和氢氯键等极性键的形成,D正确。故选C。
14.(2022·安徽省九师联盟高三质量检测)甲烷-甲醇-碘甲烷热化学循环如图(图中各物质均为气态)所示。
下列说法错误的是( )
A.反应①的
B.①②③均发生氧化还原反应
C.反应③在高温下能自发进行,则其∆H<0,∆S<0
D.上述热化学循环实现了水的分解
【答案】C
【解析】A项,根据流程中反应可知,反应① ,A正确;B项,由循环图可知,
①②③均有化合价变化,发生氧化还原反应,B正确;C项,反应③的ΔS>0,C错误;D项,由反应①CH(g)
4
+HO(g) CO(g)+3H(g);②CO(g)+2H(g) CHOH(g);③2CHOH(g)+I(g) 2CHI(g)+
2 2 2 3 3 2 3
HO(g)+1/2O(g);④2CHI(g)+HO(g) CHOH(g)+I(g)+CH(g);四式相加得
2 2 3 2 3 2 4
,故为水的分解,D正确;故选C。
15.(2022·内蒙古新城·一模)硫酸盐(含SO 2-、HSO -)气溶胶是PM2.5的成分之一、科研人员提出了雾霾微
4 4
粒中硫酸盐生成的三个阶段的转化机理,其主要过程如图所示,下列说法不正确的是( )A.HNO、NO 、HO均只含有极性共价键
2 2 2
B.该过程中NO -为中间产物
2
C.总反应SO 2-+2NO+H O=HSO -+NO-+HNO
3 2 2 4 2 2
D.还原性SO ->HNO
3 2
【答案】B
【解析】A项,HNO 含有氮氧键、氧氢键,NO 含有氮氧键,HO含有氢氧键,三者都只含有极性共价
2 2 2
键,故A正确;B项,反应中第一个阶段是SO 2-+NO=SO-+NO-,第二个阶段是SO -+NO+H O=HSO -
3 2 3 2 3 2 2 4
+HNO ,两个阶段总反应SO 2-+2NO+H O=HSO -+NO-+HNO ,因此NO -为反应产物,不是中间产物,故B错
2 3 2 2 4 2 2 2
误;C项,根据B选项的分析的总反应为SO 2-+2NO+H O=HSO -+NO-+HNO ,故C正确;D项,根据第二个
3 2 2 4 2 2
阶段反应SO -+NO+H O=HSO -+HNO ,得到还原性SO ->HNO,故D正确。故选B。
3 2 2 4 2 3 2
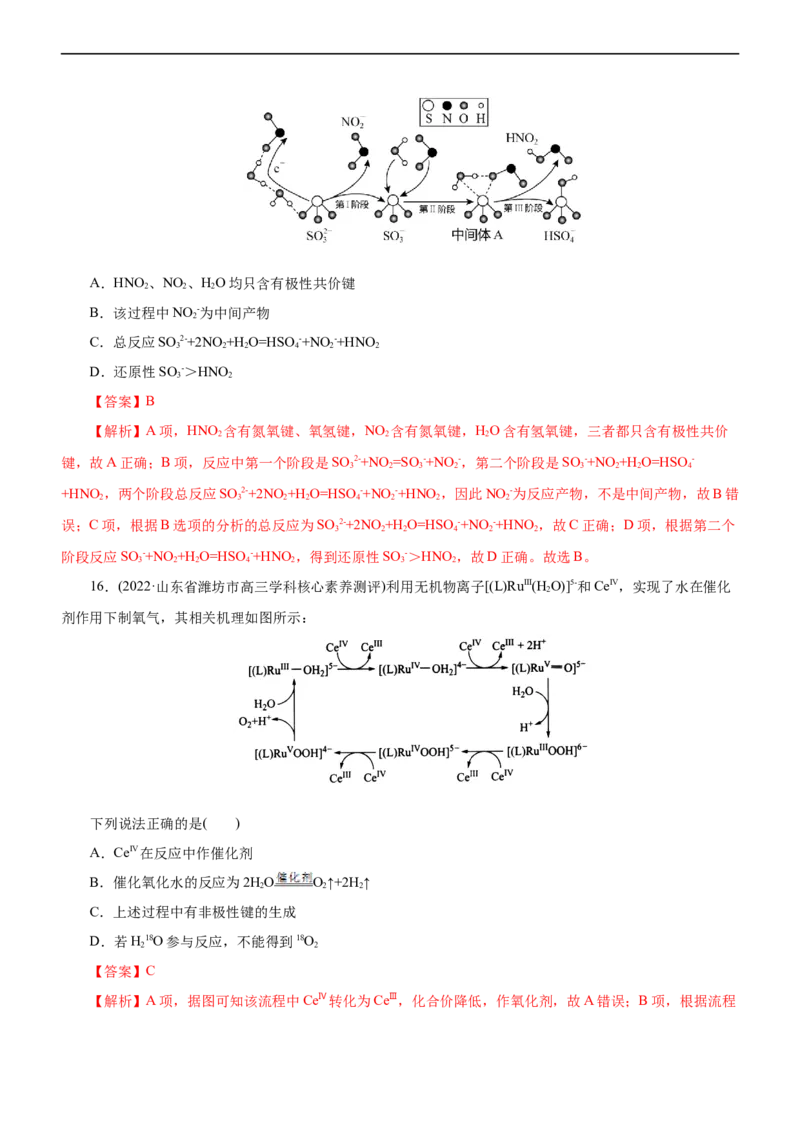
16.(2022·山东省潍坊市高三学科核心素养测评)利用无机物离子[(L)RuIII(H O)]5-和CeIV,实现了水在催化
2
剂作用下制氧气,其相关机理如图所示:
下列说法正确的是( )
A.CeIV在反应中作催化剂
B.催化氧化水的反应为2HO O↑+2H ↑
2 2 2
C.上述过程中有非极性键的生成
D.若H18O参与反应,不能得到18O
2 2
【答案】C
【解析】A项,据图可知该流程中CeⅣ转化为CeⅢ,化合价降低,作氧化剂,故A错误;B项,根据流程可知该反应中HO和[CeⅣ(NO )]2-为反应物,最终产物为[CeⅢ(NO )]3-、O 和H+,总反应为
2 3 6 3 6 2
2HO+4[CeⅣ(NO )]2- O↑+4[CeⅢ(NO )]3-+4H+,故B错误;C项,上述过程中生成O,有非极性键的生成,
2 3 6 2 3 6 2
故C正确;D项,据图可知[(L)RuⅤ=O]5-与HO反应生成[(L)RuⅢOOH]6-和H+,根据元素守恒可知若H18O参与
2 2
反应,则[(L)RuⅢOOH]6-中存在18O,故D错误。
17.(2022·湖南省邵阳市一模)酸性环境中,纳米Fe/Ni去除NO -过程中的含氮微粒变化如图所示,溶液中
3
铁以Fe2+形式存在。下列有关说法不正确的是( )
A.反应ⅱ的离子方程式为:NO -+3Fe+8H+=NH++3Fe2++2H O
2 4 2
B.增大单位体积水体中纳米Fe/Ni的投入量,可提高NO -的去除效果
3
C.假设反应过程都能彻底进行,反应ⅰ、ⅱ消耗的铁的物质的量之比为3:1
D.a mol NO -完全转化为NH +至少需要4a mol的铁
3 4
【答案】C
【解析】A项,据图可知反应ii中NO -被Fe还原为NH +,根据电子守恒、元素守恒可得离子方程式为
2 4
NO -+3Fe+8H+=NH++3Fe2++2H O,A正确;B项,增大单位体积水体中纳米Fe/Ni的投入量,即增大其浓度,
2 4 2
同时也增大反应物间的接触面积,可提高NO -的去除效果,B正确;C项,反应i中NO -中被Fe还原为
3 3
NO -,Fe被氧化为Fe2+,根据电子守恒可知1mol NO -氧化1molFe,同时生成1mol NO -,根据A选项可知,
2 3 2
1mol NO -可以氧化3molFe,所以反应ⅰ、ⅱ消耗的铁的物质的量之比为1:3,C错误;D项,根据C选项分析
2
可知,将a mol NO -完全转化为NH +至少需要amol+3amol=4a mol的铁,D正确;故选C。
3 4
18.(2022·辽宁·大连市第一中学高三期中)科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,
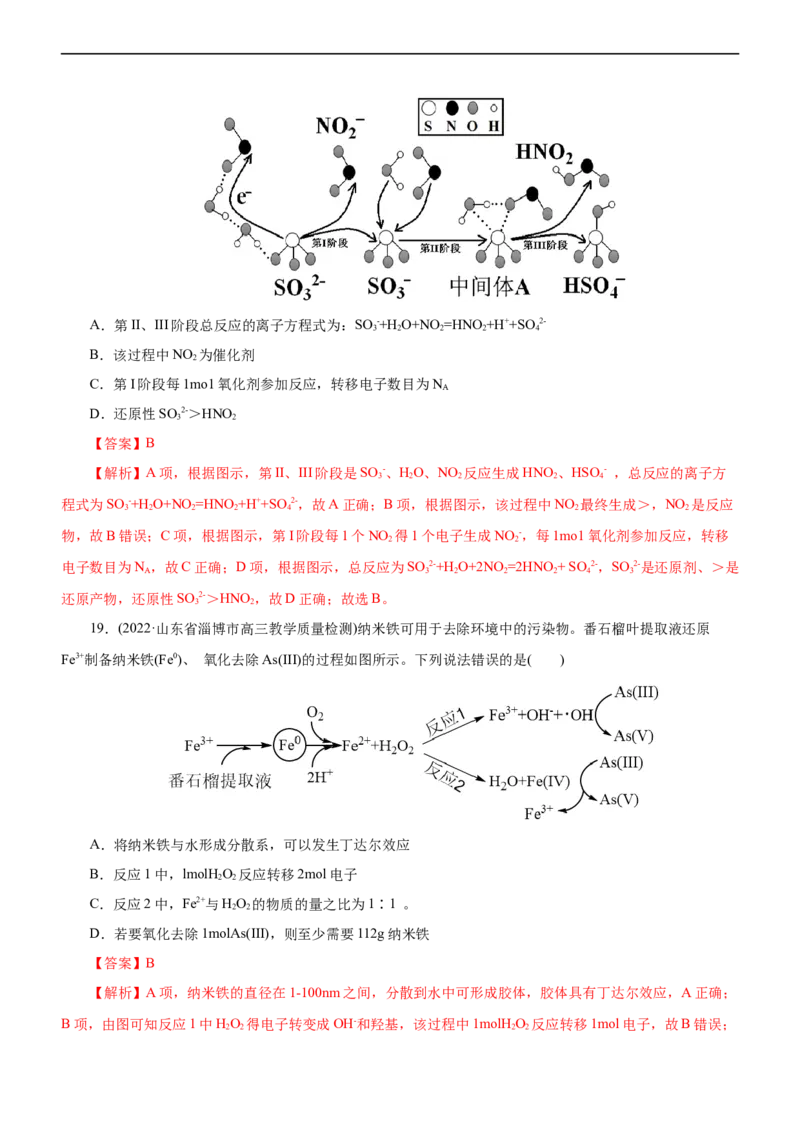
其主要过程示意如下。下列说法错误的是( )A.第II、III阶段总反应的离子方程式为:SO -+H O+NO =HNO +H++SO2-
3 2 2 2 4
B.该过程中NO 为催化剂
2
C.第I阶段每1mo1氧化剂参加反应,转移电子数目为N
A
D.还原性SO 2->HNO
3 2
【答案】B
【解析】A项,根据图示,第II、III阶段是SO -、HO、NO 反应生成HNO、HSO - ,总反应的离子方
3 2 2 2 4
程式为SO -+H O+NO =HNO +H++SO2-,故A正确;B项,根据图示,该过程中NO 最终生成>,NO 是反应
3 2 2 2 4 2 2
物,故B错误;C项,根据图示,第I阶段每1个NO 得1个电子生成NO -,每1mo1氧化剂参加反应,转移
2 2
电子数目为N ,故C正确;D项,根据图示,总反应为SO 2-+H O+2NO =2HNO + SO 2-,SO 2-是还原剂、>是
A 3 2 2 2 4 3
还原产物,还原性SO 2->HNO,故D正确;故选B。
3 2
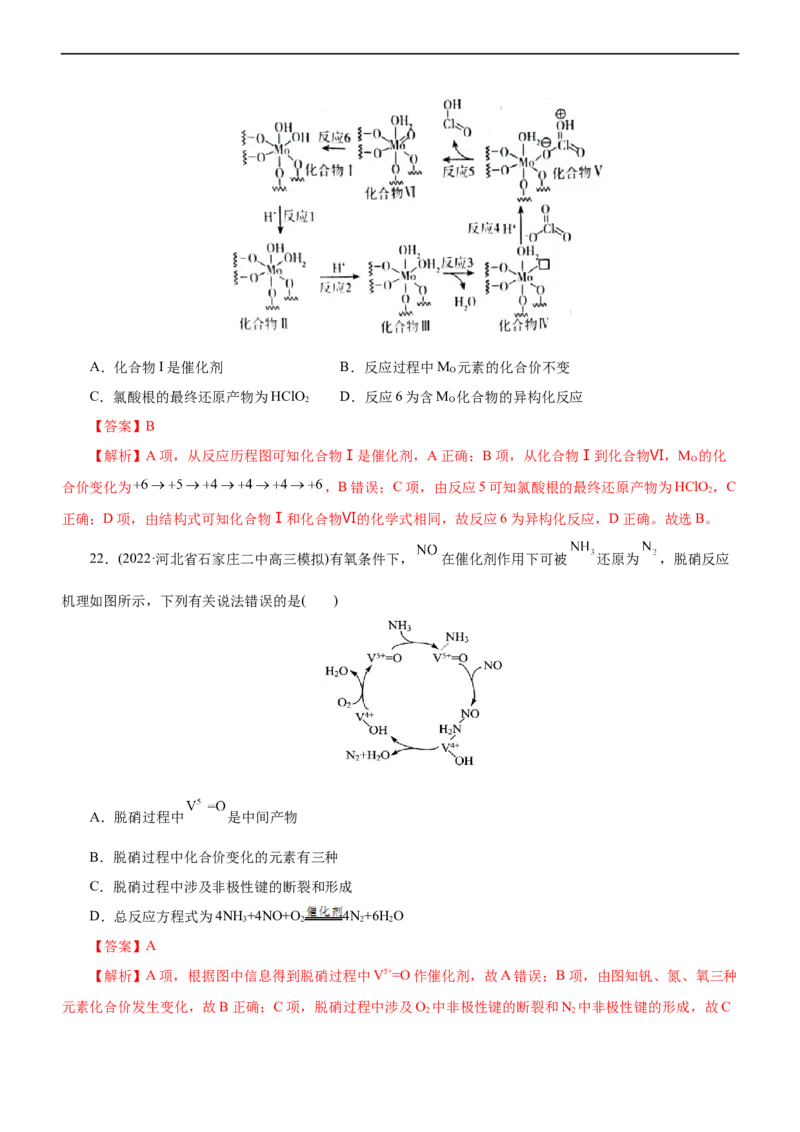
19.(2022·山东省淄博市高三教学质量检测)纳米铁可用于去除环境中的污染物。番石榴叶提取液还原
Fe3+制备纳米铁(Fe0)、 氧化去除As(III)的过程如图所示。下列说法错误的是( )
A.将纳米铁与水形成分散系,可以发生丁达尔效应
B.反应1中,lmolHO 反应转移2mol电子
2 2
C.反应2中,Fe2+与HO 的物质的量之比为1∶1 。
2 2
D.若要氧化去除1molAs(III),则至少需要112g纳米铁
【答案】B
【解析】A项,纳米铁的直径在1-100nm之间,分散到水中可形成胶体,胶体具有丁达尔效应,A正确;
B项,由图可知反应1中HO 得电子转变成OH-和羟基,该过程中1molH O 反应转移1mol电子,故B错误;
2 2 2 2C项,由图中信息可知反应2为亚铁离子与HO 反应生成Fe和水,1mol Fe2+得2mol电子,1molH O 反应生成
2 2 2 2
水失去2mol电子,两者物质的量之比为1:1,故C正确;D项,要氧化去除1molAs(III)转化成As(V),转移
2mol电子,则消耗Fe2+转化成Fe3+,转移2mol电子消耗2mol Fe2+,结合图示可知,则至少需要2mol纳米铁即
112g,故D正确;故选B。
20.(2022·安徽省芜湖一中高三诊断模拟考试)硼氢化钠(NaBH )在工业生产中应用广泛。它在催化剂作用
4
下与水反应获取氢气的微观过程如图所示。下列说法不正确的是( )
A.水在此过程中做氧化剂
B.若将NaBH 中的H用D代替,反应后生成的气体为D
4 2
C.催化剂可以加快反应速率,其用量多少可影响反应速率
D.NaBH 与水反应的离子方程式为BH-+4HO=B(OH) -+4H↑
4 4 2 4 2
【答案】B
【解析】根据NaBH 在催化剂作用下与水反应获取氢气的微观过程图可知,BH-和HO生成B(OH) -和
4 4 2 4
H,离子反应方程式为:BH-+4H O= B(OH) -+4H ↑。A项,HO变成H,水中氢元素的化合价降低,是氧化
2 4 2 4 2 2 2
剂,A正确;B项,若用D代替NaBH 中H,由图示知,BH-首先吸附在催化剂表面释放出D,第二步项,第
4 4 2
三步中产生HD,最后一步中产生H,故生成的氢气有H、HD、D,B错误;C项,使用催化剂可以改变化
2 2 2
学反应速率,所以通过控制催化剂的用量和表面积,可以控制氢气的产生速率,一定范围内,催化剂的用量多
少也会影响反应速率,C正确;D项,反应的离子方程式为:BH-+4H O= B(OH) -+4H ↑,D正确;故选B。
4 2 4 2
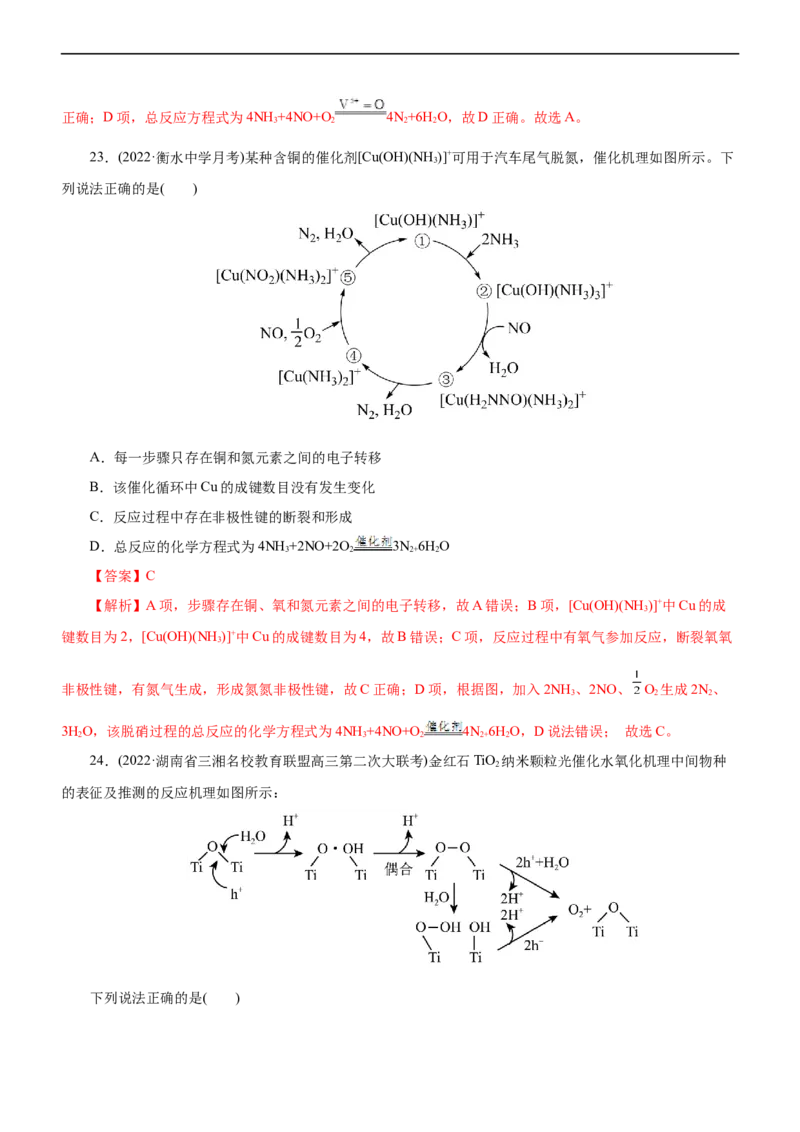
21.(2022·安徽省百校联盟高三联考)饮用水氯消毒和废水电化学处理的副反应均会产生污染环境的氯酸盐,
一种含M 催化剂可用于高盐条件下快速清洁地还原氯酸盐,其反应过程如图所示,下列说法错误的是( )
OA.化合物I是催化剂 B.反应过程中M 元素的化合价不变
O
C.氯酸根的最终还原产物为HClO D.反应6为含M 化合物的异构化反应
2 O
【答案】B
【解析】A项,从反应历程图可知化合物Ⅰ是催化剂,A正确;B项,从化合物Ⅰ到化合物Ⅵ,M 的化
O
合价变化为 ,B错误;C项,由反应5可知氯酸根的最终还原产物为HClO,C
2
正确;D项,由结构式可知化合物Ⅰ和化合物Ⅵ的化学式相同,故反应6为异构化反应,D正确。故选B。
22.(2022·河北省石家庄二中高三模拟)有氧条件下, 在催化剂作用下可被 还原为 ,脱硝反应
机理如图所示,下列有关说法错误的是( )
A.脱硝过程中 是中间产物
B.脱硝过程中化合价变化的元素有三种
C.脱硝过程中涉及非极性键的断裂和形成
D.总反应方程式为4NH +4NO+O 4N+6H O
3 2 2 2
【答案】A
【解析】A项,根据图中信息得到脱硝过程中V5+=O作催化剂,故A错误;B项,由图知钒、氮、氧三种
元素化合价发生变化,故B正确;C项,脱硝过程中涉及O 中非极性键的断裂和N 中非极性键的形成,故C
2 2正确;D项,总反应方程式为4NH +4NO+O 4N+6H O,故D正确。故选A。
3 2 2 2
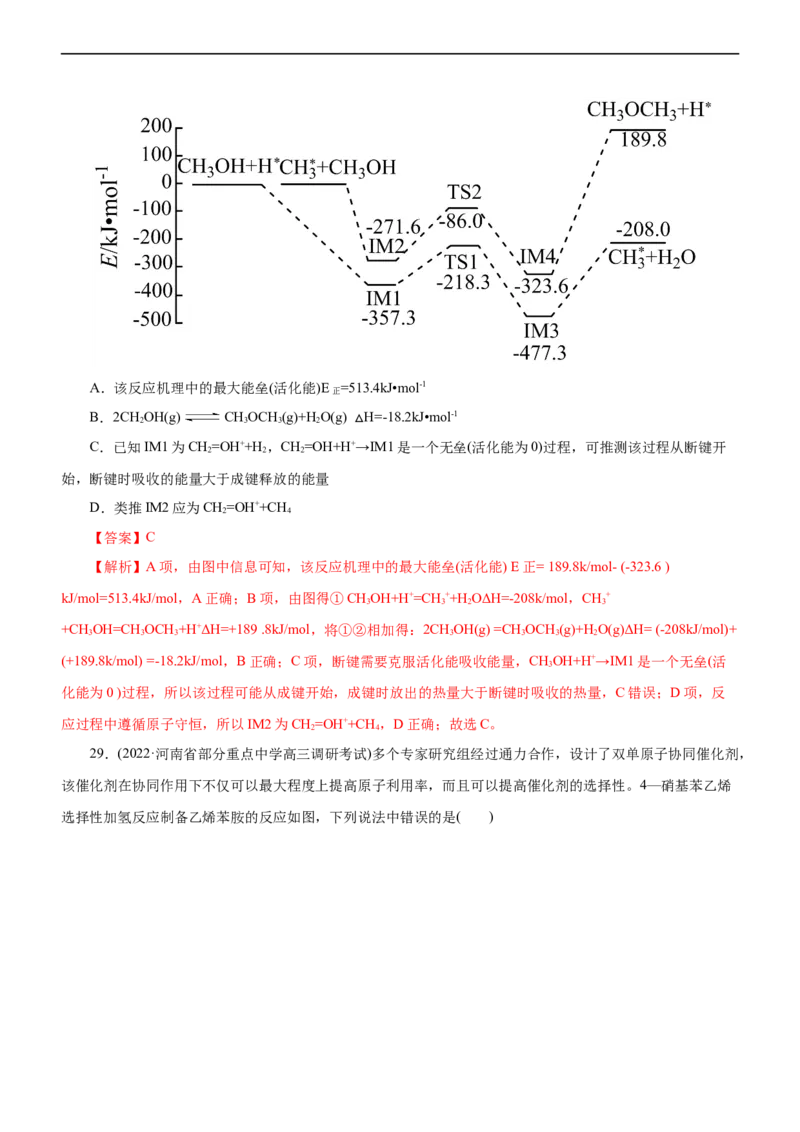
23.(2022·衡水中学月考)某种含铜的催化剂[Cu(OH)(NH )]+可用于汽车尾气脱氮,催化机理如图所示。下
3
列说法正确的是( )
A.每一步骤只存在铜和氮元素之间的电子转移
B.该催化循环中Cu的成键数目没有发生变化
C.反应过程中存在非极性键的断裂和形成
D.总反应的化学方程式为4NH +2NO+2O 3N 6HO
3 2 2+ 2
【答案】C
【解析】A项,步骤存在铜、氧和氮元素之间的电子转移,故A错误;B项,[Cu(OH)(NH )]+中Cu的成
3
键数目为2,[Cu(OH)(NH )]+中Cu的成键数目为4,故B错误;C项,反应过程中有氧气参加反应,断裂氧氧
3
非极性键,有氮气生成,形成氮氮非极性键,故C正确;D项,根据图,加入2NH 、2NO、 O 生成2N、
3 2 2
3HO,该脱硝过程的总反应的化学方程式为4NH +4NO+O 4N 6HO,D说法错误; 故选C。
2 3 2 2+ 2
24.(2022·湖南省三湘名校教育联盟高三第二次大联考)金红石TiO 纳米颗粒光催化水氧化机理中间物种
2
的表征及推测的反应机理如图所示:
下列说法正确的是( )A.光激发条件下TiO 纳米颗粒作催化剂未参与水氧化的反应
2
B.TiO 纳米颗粒光催化水氧化反应的方程式为2HO 2H+O
2 2 2 2
C.在反应过程中存在分解反应:Ti O+H O=TiOOH+TiOH
2 2 2
D.TiO 纳米颗粒光催化水氧化的溶液酸性减小
2
【答案】C
【解析】A项,TiO 纳米颗粒作催化剂参与了水氧化的反应,只是反应后又生成了TiO,反应前后TiO
2 2 2
的质量和化学性质不变,A错误;B项,从机理图中并没有看到水分解生成氢气,B错误;C项,机理图中存
在 ,.即反应Ti O+H O=TiOOH+TiOH,C正确;D项,从机理图中可看出TiO 纳米颗粒光催
2 2 2 2
化水氧化的过程中生成H+,导致溶液酸性增强,D错误;故选C。
25.(2022·安徽省皖江名校高三第四次联考)一种利用太阳能将甲烷重整制氢原理的示意图如下:
下可有关说法正确的是( )
A.第I步反应中,CH 是氧化剂
4
B.第II步发生的反应为:NiO+2FeO+H O=NiO·Fe O+H ↑
2 2 3 2
C.理论上反应中转移6mol电子时,可重整生成67.2LH
2
D.NiO·Fe O 是整个反应中可以循环利用的中间产物
2 3
【答案】B
【解析】A项,第I步反应为NiFe O+CH =NiO+2FeO+CO(g)+2H ,CH 被氧化,是还原剂,A错误;B
2 4 4 2 4
项,根据流程判断,第I步发生的反应为NiO + 2FeO + H O =NiO·Fe O + H , B正确;C项,总反应为
2 2 3 2CH+H O=CO+3H,理论上反应中转移6mol电时,可重整生成标准状况下67.2LH ,但未说明标准状况,C
4 2 2 2
错误; D项,NiO·Fe O 是整个反应的催化剂,不是循环利用的物质的中间产物,D错误。故选B。
2 3
26.(2022·山东省菏泽市高三期末)为实现“碳中和”,CO 的再利用非常关键,据文献报道CO 与H 可
2 2 2
在 催化下生成CH,其反应机理如下图。下列说法正确的是( )
4
A.过程中只涉及极性键的断开与形成
B.反应过程中,既有氧化还原反应,又有非氧化还原反应
C.图中涉及碳的价态没有发生变化
D.总反应为CO+4H CH+2H O
2 2 4 2
【答案】BD
【解析】A项,反应中还有氢气参与,因此还有非极性键的断开与形成,故A正确;B项,氧化镁和二氧
化碳反应是非氧化还原反应,氢气参与的反应是氧化还原反应,因此反应过程中,既有氧化还原反应,又有非
氧化还原反应,故B正确;C项,甲烷中碳元素为-4价,二氧化碳中碳元素为+4价,从MgOCO 开始连续得
2
氢,碳元素的化合价降低,故C错误;D项,整个过程是CO 与H 在催化剂条件下生成CH,同时有水生成,
2 2 4
反应方程式表示为:CO+4H CH+2H O,故D正确。故选BD。
2 2 4 2
27.(2022·湖南省衡阳市八中高三模拟)中国科学家研究在Pd/SVG催化剂上H 还原NO生成N 和NH 的
2 2 3
路径,各基元反应及活化能E(kJ·mol﹣1)如图所示,下列说法正确的是( )
aA.生成NH 的各基元反应中,N元素均被还原
3
B.在Pd/SVG催化剂上,NO更容易被H 还原为N
2 2
C.决定NO生成NH 速率的基元反应为NH NO → NHNOH
3 2
D.生成NH 的总反应方程式为2NO+5H 2NH +2H O
3 2 3 2
【答案】AD
【解析】A项,NO生成NH 的各基元反应中,N元素化合价由+2价逐渐降低为-3价,N元素均被还原,
3
故A正确;B项,在Pd/SVG催化剂上,NH NO → NHNOH、NHNOH → N +H O基元反应的活化能大,所以
2 2 2
NO不易被H 还原为N,故B错误;C项,NO生成NH 的各基元反应中,基元反应为NH O → NHOH的活
2 2 3 2 2
化能最大,决定NO生成NH 速率的基元反应为NH O → NHOH,故C错误;D项,NO被氢气还原为NH ,
3 2 2 3
根据得失电子守恒,总反应方程式为2NO+5H 2NH +2H O,故D正确;故选AD。
2 3 2
28.(2022·辽宁省铁岭市六校高三联考)我国某科研团队通过计算机模拟技术提出在12—磷钨酸(固体强酸)
催化作用下甲醇气相脱水合成二甲醚的反应机理:CHOH+H+→IM1(中间体1)→TS1(过渡态1)→IM3(中间体
3
3)→CH++H O,CH++CH OH→IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CHOCH +H+。反应过程和相
3 2 3 3 3 3
对能量E(kJ•mol-1)如图所示。下列说法错误的是( )A.该反应机理中的最大能垒(活化能)E =513.4kJ•mol-1
正
B.2CHOH(g) CHOCH (g)+HO(g) H=-18.2kJ•mol-1
2 3 3 2
C.已知IM1为CH
2
=OH++H
2
,CH
2
=OH+H+△→IM1是一个无垒(活化能为0)过程,可推测该过程从断键开
始,断键时吸收的能量大于成键释放的能量
D.类推IM2应为CH=OH++CH
2 4
【答案】C
【解析】A项,由图中信息可知,该反应机理中的最大能垒(活化能) E正= 189.8k/mol- (-323.6 )
kJ/mol=513.4kJ/mol,A正确;B项,由图得①CHOH+H+=CH ++H OΔH=-208k/mol,CH+
3 3 2 3
+CH OH=CH OCH +H+ΔH=+189 .8kJ/mol,将①②相加得:2CHOH(g) =CHOCH (g)+HO(g)ΔH= (-208kJ/mol)+
3 3 3 3 3 3 2
(+189.8k/mol) =-18.2kJ/mol,B正确;C项,断键需要克服活化能吸收能量,CHOH+H+→IM1是一个无垒(活
3
化能为0 )过程,所以该过程可能从成键开始,成键时放出的热量大于断键时吸收的热量,C错误;D项,反
应过程中遵循原子守恒,所以IM2为CH=OH++CH ,D正确;故选C。
2 4
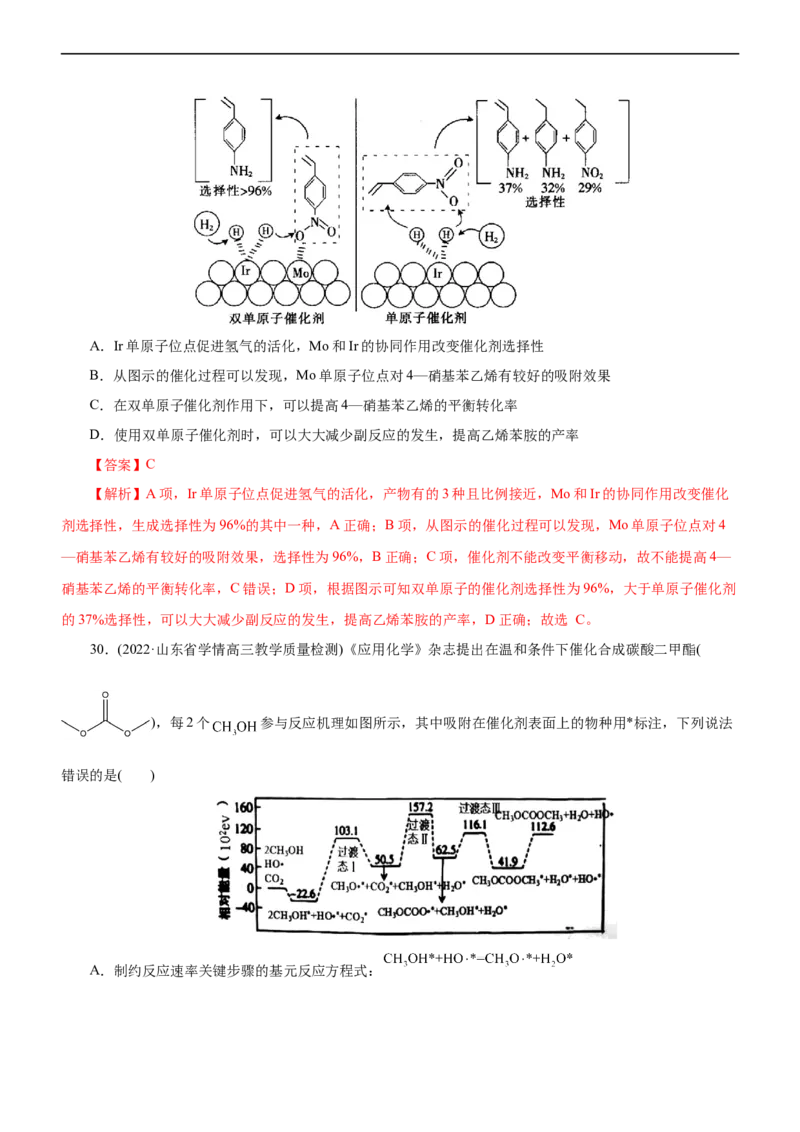
29.(2022·河南省部分重点中学高三调研考试)多个专家研究组经过通力合作,设计了双单原子协同催化剂,
该催化剂在协同作用下不仅可以最大程度上提高原子利用率,而且可以提高催化剂的选择性。4—硝基苯乙烯
选择性加氢反应制备乙烯苯胺的反应如图,下列说法中错误的是( )A.Ir单原子位点促进氢气的活化,Mo和Ir的协同作用改变催化剂选择性
B.从图示的催化过程可以发现,Mo单原子位点对4—硝基苯乙烯有较好的吸附效果
C.在双单原子催化剂作用下,可以提高4—硝基苯乙烯的平衡转化率
D.使用双单原子催化剂时,可以大大减少副反应的发生,提高乙烯苯胺的产率
【答案】C
【解析】A项,Ir单原子位点促进氢气的活化,产物有的3种且比例接近,Mo和Ir的协同作用改变催化
剂选择性,生成选择性为96%的其中一种,A正确;B项,从图示的催化过程可以发现,Mo单原子位点对4
—硝基苯乙烯有较好的吸附效果,选择性为96%,B正确;C项,催化剂不能改变平衡移动,故不能提高4—
硝基苯乙烯的平衡转化率,C错误;D项,根据图示可知双单原子的催化剂选择性为96%,大于单原子催化剂
的37%选择性,可以大大减少副反应的发生,提高乙烯苯胺的产率,D正确;故选 C。
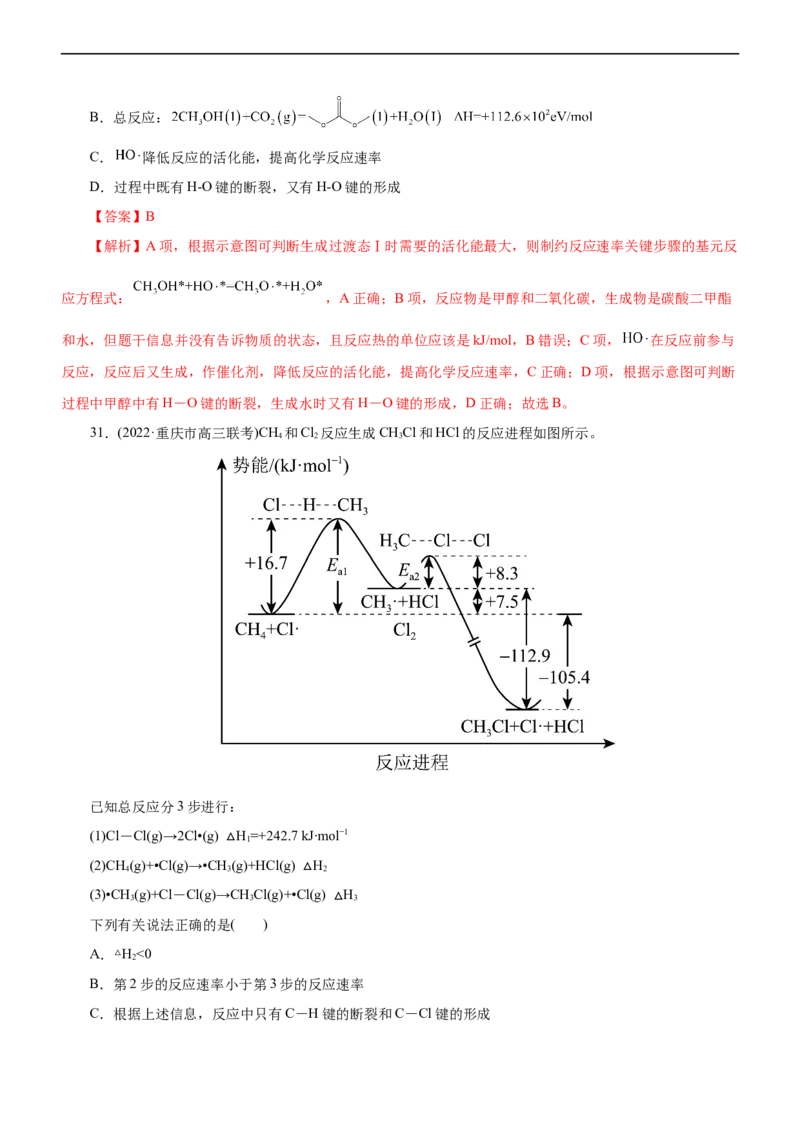
30.(2022·山东省学情高三教学质量检测)《应用化学》杂志提出在温和条件下催化合成碳酸二甲酯(
),每2个 参与反应机理如图所示,其中吸附在催化剂表面上的物种用*标注,下列说法
错误的是( )
A.制约反应速率关键步骤的基元反应方程式:B.总反应:
C. 降低反应的活化能,提高化学反应速率
D.过程中既有H-O键的断裂,又有H-O键的形成
【答案】B
【解析】A项,根据示意图可判断生成过渡态Ⅰ时需要的活化能最大,则制约反应速率关键步骤的基元反
应方程式: ,A正确;B项,反应物是甲醇和二氧化碳,生成物是碳酸二甲酯
和水,但题干信息并没有告诉物质的状态,且反应热的单位应该是kJ/mol,B错误;C项, 在反应前参与
反应,反应后又生成,作催化剂,降低反应的活化能,提高化学反应速率,C正确;D项,根据示意图可判断
过程中甲醇中有H-O键的断裂,生成水时又有H-O键的形成,D正确;故选B。
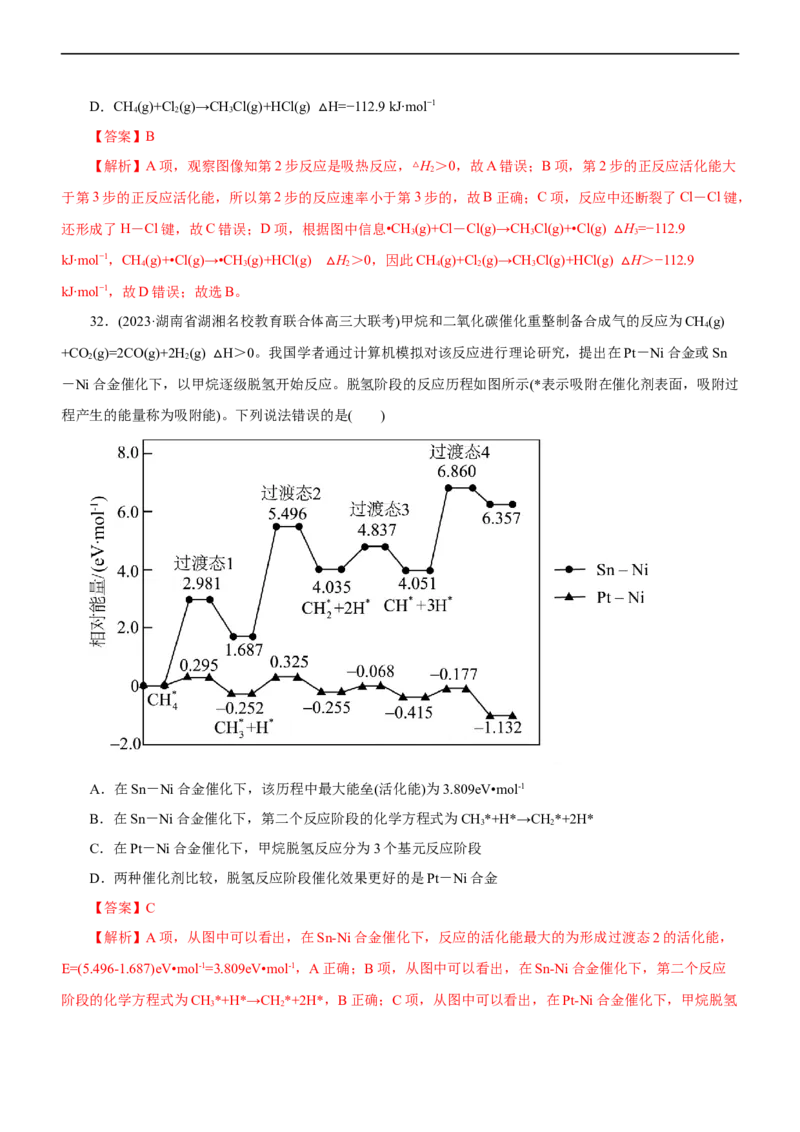
31.(2022·重庆市高三联考)CH 和Cl 反应生成CHCl和HCl的反应进程如图所示。
4 2 3
已知总反应分3步进行:
(1)Cl-Cl(g)→2Cl•(g) H=+242.7 kJ∙mol−1
1
(2)CH
4
(g)+•Cl(g)→•CH△3 (g)+HCl(g) H
2
(3)•CH
3
(g)+Cl-Cl(g)→CH
3
Cl(g)+•C△l(g) H
3
下列有关说法正确的是( ) △
A.△H<0
2
B.第2步的反应速率小于第3步的反应速率
C.根据上述信息,反应中只有C-H键的断裂和C-Cl键的形成D.CH(g)+Cl (g)→CH Cl(g)+HCl(g) H=−112.9 kJ∙mol−1
4 2 3
【答案】B △
【解析】A项,观察图像知第2步反应是吸热反应,△H>0,故A错误;B项,第2步的正反应活化能大
2
于第3步的正反应活化能,所以第2步的反应速率小于第3步的,故B正确;C项,反应中还断裂了Cl-Cl键,
还形成了H-Cl键,故C错误;D项,根据图中信息•CH(g)+Cl-Cl(g)→CH Cl(g)+•Cl(g) H=−112.9
3 3 3
kJ∙mol−1,CH(g)+•Cl(g)→•CH (g)+HCl(g) H>0,因此CH(g)+Cl (g)→CH Cl(g)+HCl(g) △ H>−112.9
4 3 2 4 2 3
kJ∙mol−1,故D错误;故选B。 △ △
32.(2023·湖南省湖湘名校教育联合体高三大联考)甲烷和二氧化碳催化重整制备合成气的反应为CH(g)
4
+CO (g)=2CO(g)+2H(g) H>0。我国学者通过计算机模拟对该反应进行理论研究,提出在Pt-Ni合金或Sn
2 2
-Ni合金催化下,以甲烷△逐级脱氢开始反应。脱氢阶段的反应历程如图所示(*表示吸附在催化剂表面,吸附过
程产生的能量称为吸附能)。下列说法错误的是( )
A.在Sn-Ni合金催化下,该历程中最大能垒(活化能)为3.809eV•mol-1
B.在Sn-Ni合金催化下,第二个反应阶段的化学方程式为CH*+H*→CH*+2H*
3 2
C.在Pt-Ni合金催化下,甲烷脱氢反应分为3个基元反应阶段
D.两种催化剂比较,脱氢反应阶段催化效果更好的是Pt-Ni合金
【答案】C
【解析】A项,从图中可以看出,在Sn-Ni合金催化下,反应的活化能最大的为形成过渡态2的活化能,
E=(5.496-1.687)eV•mol-1=3.809eV•mol-1,A正确;B项,从图中可以看出,在Sn-Ni合金催化下,第二个反应
阶段的化学方程式为CH*+H*→CH*+2H*,B正确;C项,从图中可以看出,在Pt-Ni合金催化下,甲烷脱氢
3 2反应分为4个基元反应阶段,C错误;D项,选用催化剂Pt-Ni合金时,脱氢反应的活化能低,脱氢反应阶段
催化效果更好,D正确;故选C。
33.(2023·河南省三门峡市高三阶段性考试)氮氧化物(NO )是硝酸和肼等工业的主要污染物。一种以沸石
x
笼作为载体对氮氧化物进行催化还原的原理如图1所示,反应物A在沸石笼内转化为B、C、D等中间体的过
程如图2所示。下列说法正确的是( )
A.A在沸石笼内转化为B、C、D等中间体的过程都是吸热反应
B.过程Ⅱ中,脱除1molNO转移6mol电子
C.脱除NO的总反应中,氧化剂和还原剂的物质的量之比为4:5
D.由A到B的变化过程可表示为2[Cu(NH )] + +O →[(NH )Cu-O-O-Cu(NH )]2+
3 2 2 3 2 3 2
【答案】D
【解析】A项,反应过程中,若反应物能量高于生成物能量,则反应放热,由图2可判断A、B、C、D相
对能量的高低,因此A在沸石笼内转化为B、C、D等中间体的过程都是放热反应,故A项错误;B项,过程
Ⅱ中发生反应的方程式为[Cu(NH )]2++NO=[Cu(NH )]++N +H O+NH +,反应中化合价升高的是[Cu(NH )]2+中
3 4 3 2 2 2 4 3 4
的N元素,化合价降低的是[Cu(NH )]2+中的Cu元素和NO中的N元素,可以判断脱除1mol NO转移3mol电
3 4
子,故B项错误;C项,根据图1可知,脱除NO的反应物为NO、NH 、O,生成物为N 和HO,所以总反
3 2 2 2
应的方程式为4NO+4NH +O 4N+6H O,氧化剂为NO和O,还原剂为NH ,氧化剂和还原剂的物质的
3 2 2 2 2 3
量之比为5:4,故C项错误;D项,根据图1可知,沸石笼的反应物为[Cu(NH )]+和O,根据图2可知B为
3 2 2
[(NH )Cu-O-O-Cu(NH )]2+,所以A到B的变化过程可表示为2[Cu(NH )] + +O →[(NH )Cu-O-O-Cu(NH )]2+,
3 2 3 2 3 2 2 3 2 3 2
故D项正确。故选D。
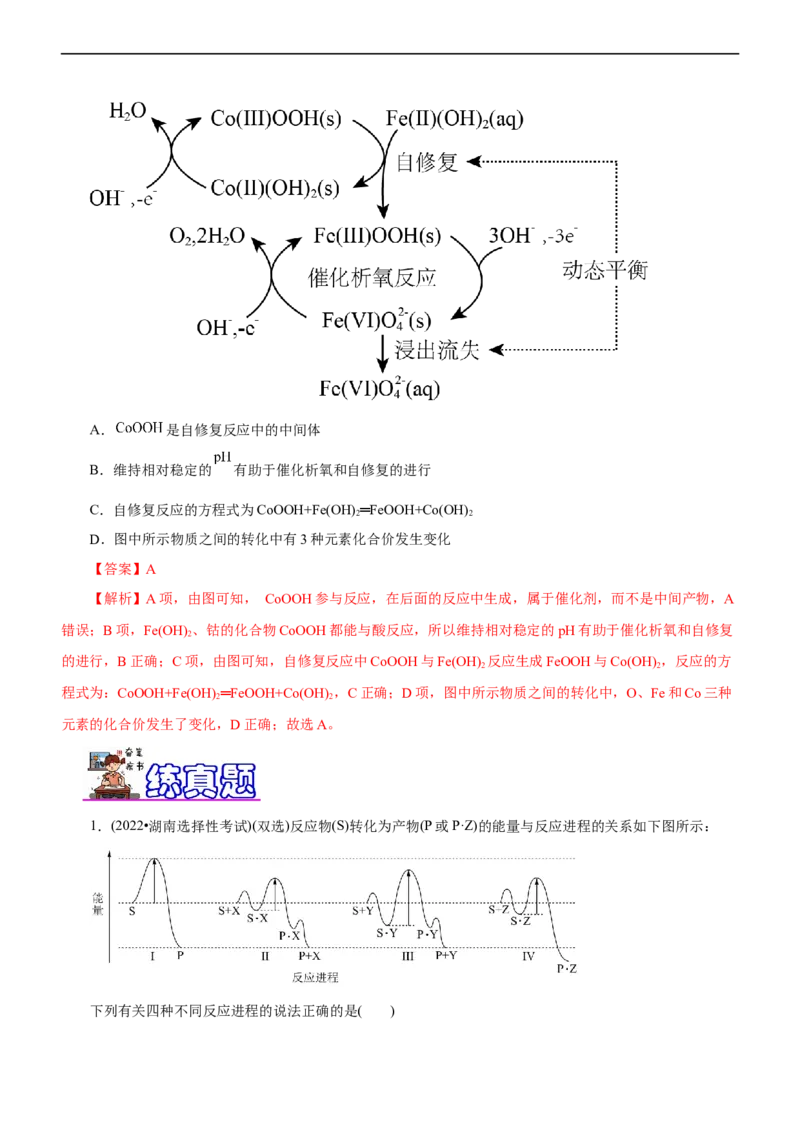
34.(2023·山东省济南市高三期中)钴(Co)使某析氧反应催化剂中流失Fe的自修复机理如图。下列说法错
误的是( )A. 是自修复反应中的中间体
B.维持相对稳定的 有助于催化析氧和自修复的进行
C.自修复反应的方程式为CoOOH+Fe(OH) ═FeOOH+Co(OH)
2 2
D.图中所示物质之间的转化中有3种元素化合价发生变化
【答案】A
【解析】A项,由图可知, CoOOH参与反应,在后面的反应中生成,属于催化剂,而不是中间产物,A
错误;B项,Fe(OH) 、钴的化合物CoOOH都能与酸反应,所以维持相对稳定的pH有助于催化析氧和自修复
2
的进行,B正确;C项,由图可知,自修复反应中CoOOH与Fe(OH) 反应生成FeOOH与Co(OH) ,反应的方
2 2
程式为:CoOOH+Fe(OH) ═FeOOH+Co(OH) ,C正确;D项,图中所示物质之间的转化中,O、Fe和Co三种
2 2
元素的化合价发生了变化,D正确;故选A。
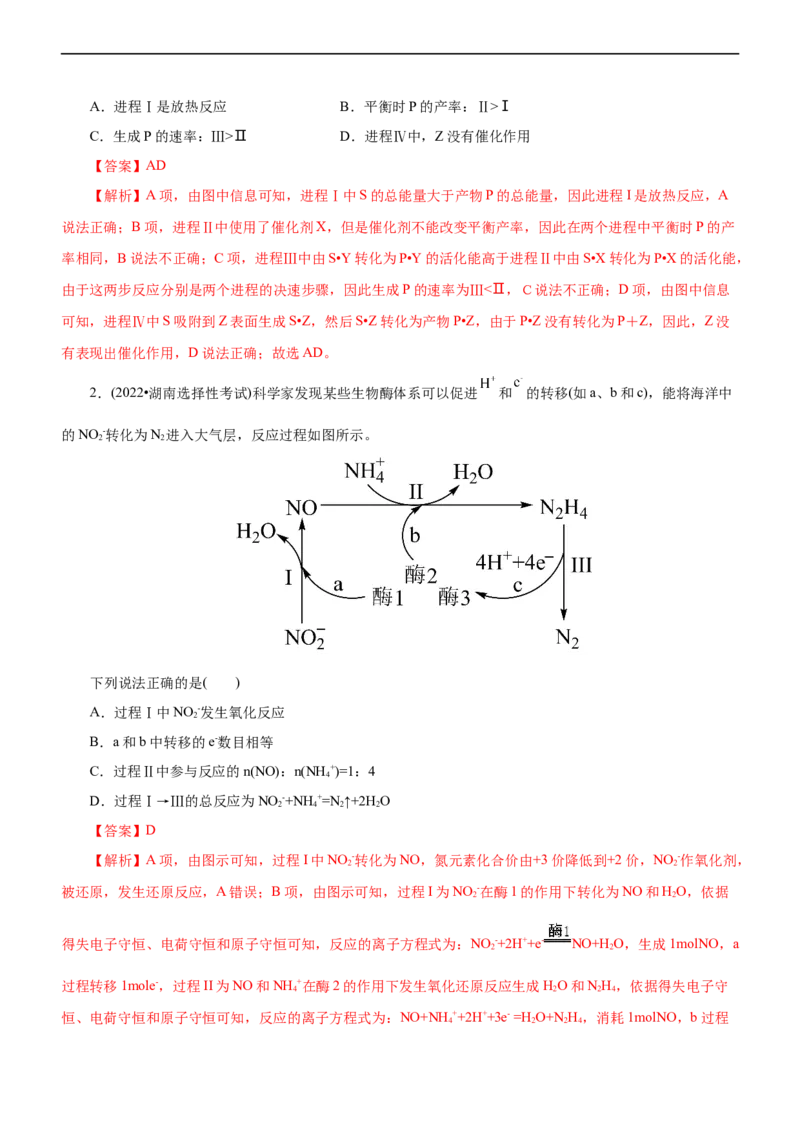
1.(2022•湖南选择性考试)(双选)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是( )A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A项,由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A
说法正确;B项,进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产
率相同,B说法不正确;C项,进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,
由于这两步反应分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;D项,由图中信息
可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为P+Z,因此,Z没
有表现出催化作用,D说法正确;故选AD。
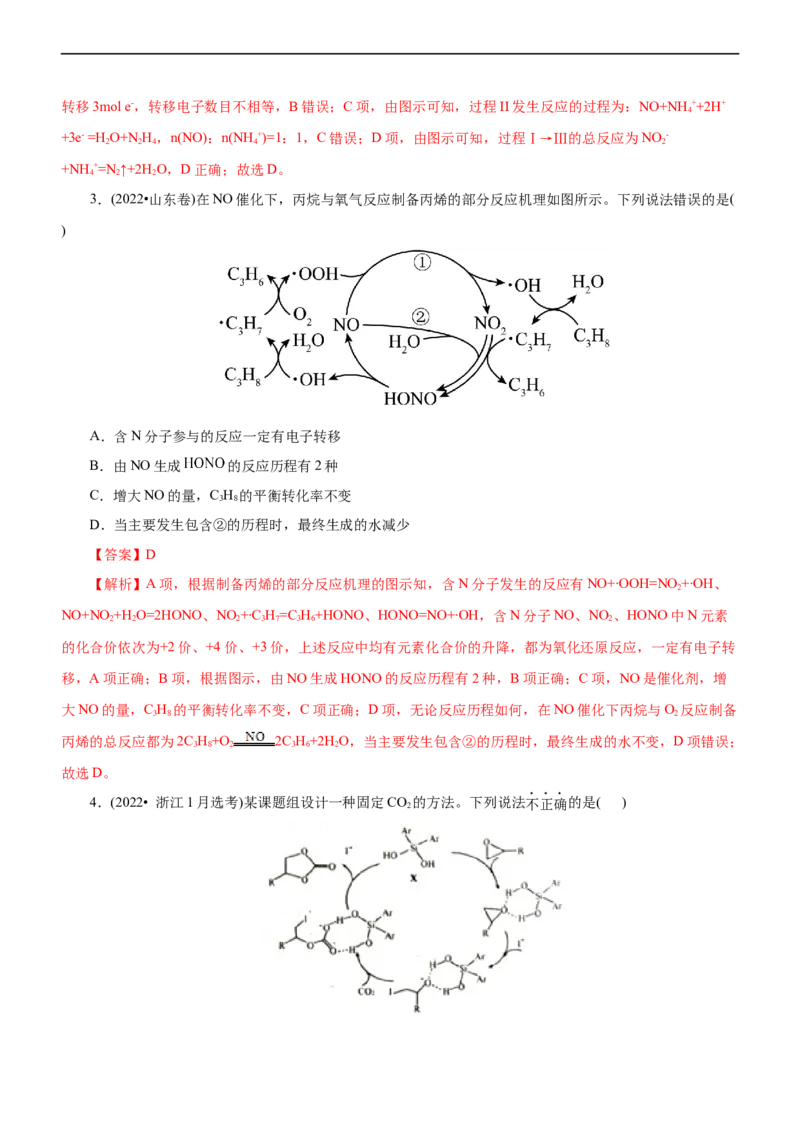
2.(2022•湖南选择性考试)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中
的NO -转化为N 进入大气层,反应过程如图所示。
2 2
下列说法正确的是( )
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO):n(NH +)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O
2 4 2 2
【答案】D
【解析】A项,由图示可知,过程I中NO -转化为NO,氮元素化合价由+3价降低到+2价,NO -作氧化剂,
2 2
被还原,发生还原反应,A错误;B项,由图示可知,过程I为NO -在酶1的作用下转化为NO和HO,依据
2 2
得失电子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO -+2H++e- NO+H O,生成1molNO,a
2 2
过程转移1mole-,过程II为NO和NH +在酶2的作用下发生氧化还原反应生成HO和NH,依据得失电子守
4 2 2 4
恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO+NH ++2H++3e- =H O+NH,消耗1molNO,b过程
4 2 2 4转移3mol e-,转移电子数目不相等,B错误;C项,由图示可知,过程II发生反应的过程为:NO+NH ++2H+
4
+3e- =H O+NH,n(NO):n(NH +)=1:1,C错误;D项,由图示可知,过程Ⅰ→Ⅲ的总反应为NO -
2 2 4 4 2
+NH+=N ↑+2H O,D正确;故选D。
4 2 2
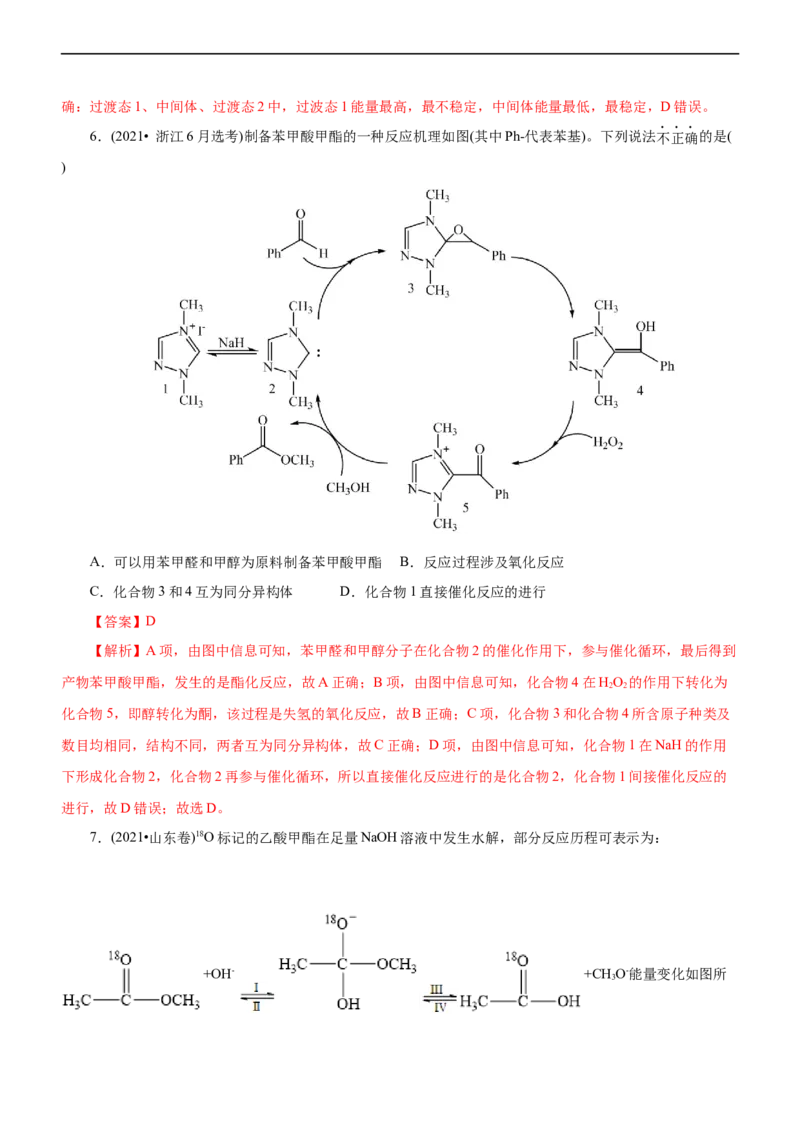
3.(2022•山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是(
)
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A项,根据制备丙烯的部分反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO+∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中N元素
2 2 2 3 7 3 6 2
的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有电子转
移,A项正确;B项,根据图示,由NO生成HONO的反应历程有2种,B项正确;C项,NO是催化剂,增
大NO的量,C H 的平衡转化率不变,C项正确;D项,无论反应历程如何,在NO催化下丙烷与O 反应制备
3 8 2
丙烯的总反应都为2C H+O 2C H+2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误;
3 8 2 3 6 2
故选D。
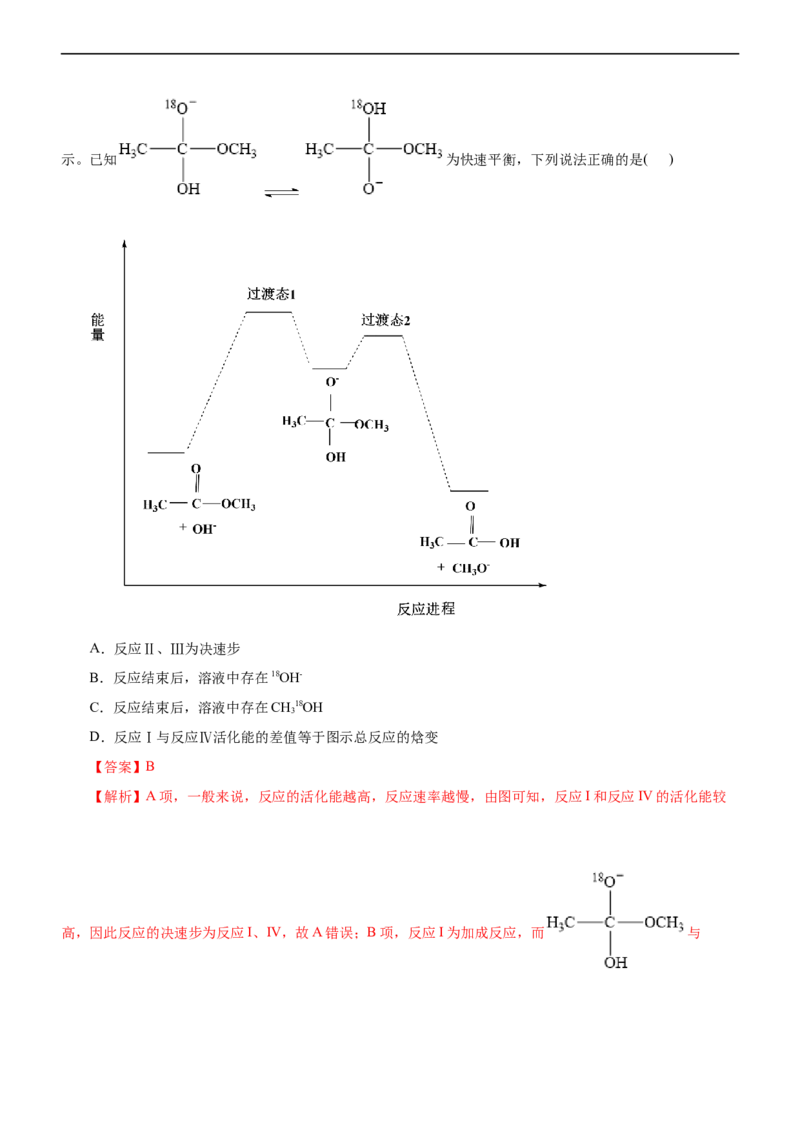
4.(2022• 浙江1月选考)某课题组设计一种固定CO 的方法。下列说法不正确的是( )
2A.反应原料中的原子100%转化为产物
B.该过程在化合物X和I-催化下完成
C.该过程仅涉及加成反应
D.若原料用 ,则产物为
【答案】C
【解析】A项,通过图示可知,二氧化碳和 反应生成 ,没有其它物质生成,反应原料
中的原子100%转化为产物,A正确;B项,通过图示可知,X和I-在反应过程中是该反应的催化剂,B正确;
C项,在该循环过程的最后一步中形成五元环的时候反应类型为取代反应,C错误;D项,通过分析该反应流
程可知,通过该历程可以把三元环转化为五元环,故若原料用 ,则产物为 ,D正确;故
选C。
5.(2021·山东临沂费县高三适应性考试)氯代叔丁烷[(CH )C—Cl]的水解反应进程与能量的关系如图所示。
3 3
下列说法正确的是( )
A.氯代叔丁烷水解的正反应活化能大于逆反应活化能
B.化学键发生异裂时,可以产生正、负离子
C.HO分子亲核进攻碳正离子时吸收能量
2
D.过渡态1、中间体和过渡态2中,过渡态1最稳定
【答案】BC
【解析】
由图像可知,反应物总能量高于生成物总能量,即正反应为放热反应,则正反应活化能小于逆反应活化能,
A错误;图中过渡态1发生化学键异裂生成了中间体碳正高子和氯离子,即化学键发生异裂时,产生了正、负
离子,B正确:图中HO分子亲核进攻碳正离子后生成了能显更高的过波态2,即本过程需要吸收能量,C正
2确:过渡态1、中间体、过渡态2中,过波态1能量最高,最不稳定,中间体能量最低,最稳定,D错误。
6.(2021• 浙江6月选考)制备苯甲酸甲酯的一种反应机理如图(其中Ph-代表苯基)。下列说法不正确的是(
)
A.可以用苯甲醛和甲醇为原料制备苯甲酸甲酯 B.反应过程涉及氧化反应
C.化合物3和4互为同分异构体 D.化合物1直接催化反应的进行
【答案】D
【解析】A项,由图中信息可知,苯甲醛和甲醇分子在化合物2的催化作用下,参与催化循环,最后得到
产物苯甲酸甲酯,发生的是酯化反应,故A正确;B项,由图中信息可知,化合物4在HO 的作用下转化为
2 2
化合物5,即醇转化为酮,该过程是失氢的氧化反应,故B正确;C项,化合物3和化合物4所含原子种类及
数目均相同,结构不同,两者互为同分异构体,故C正确;D项,由图中信息可知,化合物1在NaH的作用
下形成化合物2,化合物2再参与催化循环,所以直接催化反应进行的是化合物2,化合物1间接催化反应的
进行,故D错误;故选D。
7.(2021•山东卷)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如图所
3示。已知 为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【解析】A项,一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较
高,因此反应的决速步为反应I、IV,故A错误;B项,反应I为加成反应,而 与为快速平衡,反应II的成键和断键方式为 或
,后者能生成18OH-,因此反应结束后,溶液中存在18OH-,故B正确;C项,反应III
的成键和断键方式为 或 ,因此反应结束后溶液中不会存在
CH18H,故C错误;D项,该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因此
3
和CHO-的总能量与 和OH-的总能量之差等于图示总反应的焓变,
3
故D错误;故选B。
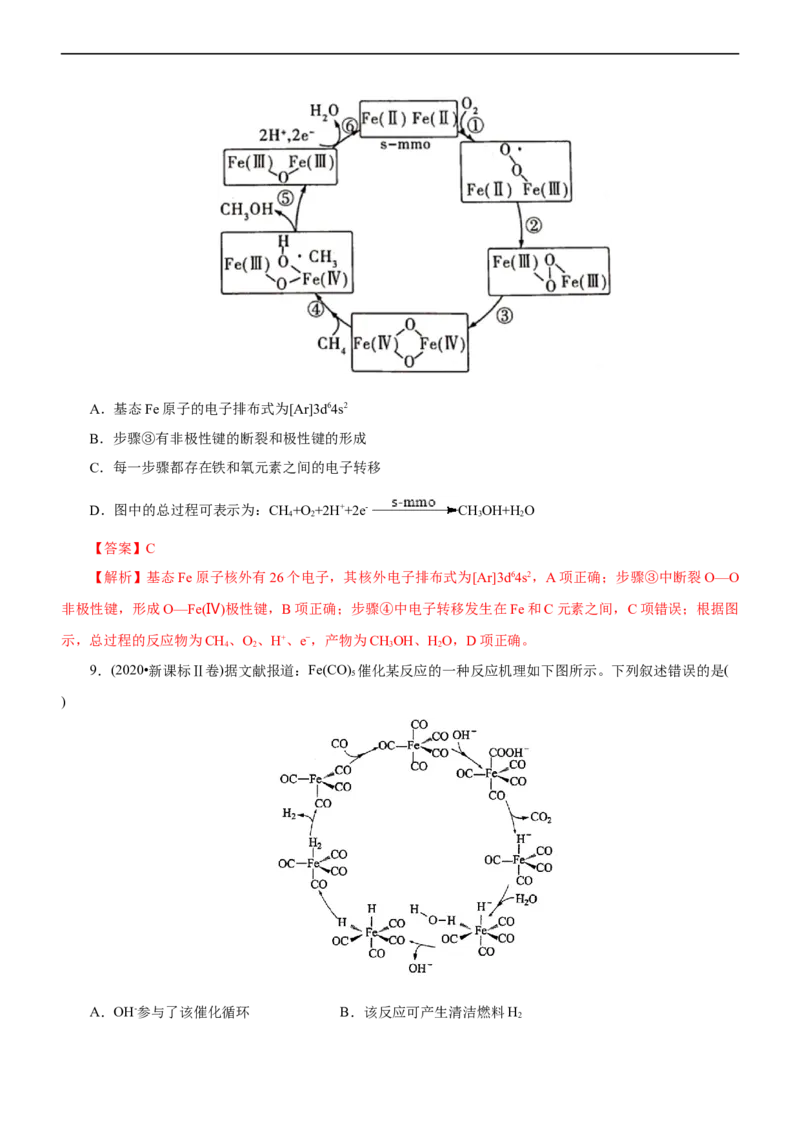
8.(2021•湖北选择性考试)甲烷单加氧酶(s-mmo)含有双核铁活性中心,是O 氧化CH 生成CHOH的催化
2 4 3
剂,反应过程如图所示。下列叙述错误的是( )A.基态Fe原子的电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
【答案】C
【解析】基态Fe原子核外有26个电子,其核外电子排布式为[Ar]3d64s2,A项正确;步骤③中断裂O—O
非极性键,形成O—Fe(Ⅳ)极性键,B项正确;步骤④中电子转移发生在Fe和C元素之间,C项错误;根据图
示,总过程的反应物为CH、O、H、e,产物为CHOH、HO,D项正确。
4 2 3 2
9.(2020•新课标Ⅱ卷)据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述错误的是(
5
)
A.OH-参与了该催化循环 B.该反应可产生清洁燃料H
2C.该反应可消耗温室气体CO D.该催化循环中Fe的成键数目发生变化
2
【答案】C
【解析】题干中明确指出,铁配合物Fe(CO) 充当催化剂的作用。机理图中,凡是出现在历程中,进去的
5
箭头表示反应物,出来的箭头表示生成物,既有进去又有出来的箭头表示为催化剂或反应条件,其余可以看成
为中间物种。由题干中提供的反应机理图可知,铁配合物Fe(CO) 在整个反应历程中成键数目,配体种类等均
5
发生了变化;并且也可以观察出,反应过程中所需的反应物除CO外还需要HO,最终产物是CO 和H,同时
2 2 2
参与反应的还有OH-,故OH-也可以看成是另一个催化剂或反应条件。A项,从反应机理图中可知,OH-有进
入的箭头也有出去的箭头,说明OH-参与了该催化循环,故A项正确;B项,从反应机理图中可知,该反应的
反应物为CO和HO,产物为H 和CO,Fe(CO) 作为整个反应的催化剂,而OH-仅仅在个别步骤中辅助催化
2 2 2 5
剂完成反应,说明该反应方程式为CO+HO CO+H ,故有清洁燃料H 生成,故 B项正确;C项,由
2 2 2 2
B项分析可知,该反应不是消耗温室气体CO,反而是生成了温室气体CO,故 C项不正确;D项,从反应机
2 2
理图中可知,Fe的成键数目和成键微粒在该循环过程中均发生了变化,故 D项正确;故选C。