文档内容
专题 10 化学反应速率与平衡
1.下列关于化学反应速率及化学平衡的说法,正确的是( )
A.升高温度能增大单位体积内活化分子数目,加快反应速率
B.增大反应物浓度,可增大活化分子的百分数,因而反应速率加快
C.化学反应条件改变,已处于化学平衡的可逆反应一定发生平衡移动
D.催化剂可以提高化学反应的选择性,进而提高反应物的平衡转化率
【答案】A
【解析】A项,升高温度,可增大活化分子百分数,则单位体积内活化分子数增多,反应速率加快,
故A正确;B项, 增大反应物浓度,增大了单位体积的活化分子数,没有改变活化分子百分数,故B错
误;C项,若同等程度改变反应速率,满足正逆反应速率相等,则平衡不移动,故C错误;D项,使用催
化剂能加快反应速率但不能提高反应物的平衡转化率,故D错误;故选A。
2.某工业生产中发生反应:2A(g)+B(g) 2M(g) ΔH>0。下列有关该工业生产的说法不正确的
是( )
A.工业上合成M时,一定采用高压条件,因为高压有利于M的生成
B.若物质B价廉易得,工业上一般采用加入过量的B以提高A的转化率
C.工业上一般采用较高温度合成M,因温度越高,反应物的转化率越高
D.工业生产中常采用催化剂,因为生产中使用催化剂可提高M的日产量
【答案】A
【解析】A项,高压对设备的要求较高,则合成M时选择合适的压强即可,A错误;B项,增大一种
反应物浓度,可促进另一种反应物的转化,由于物质B价廉易得,工业上一般采用加入过量的B的方法以
提高A的转化率,B正确;C项,焓变为正反应的反应热,由题意可知该反应的正反应为吸热反应,升高
温度化学平衡正向移动,使反应物的转化率增大,则工业上一般采用较高温度合成M,C正确;D项,催
化剂可同等程度的加快反应速率,因而可提高M的日产量,但对化学平衡移动无影响,D正确。故选A。
3.氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。氯气-氯水体系中存在以下平衡
关系:
Cl(g) Cl(aq) ①
2 2
Cl(aq)+ HO HClO + HCl ②
2 2
下列表述正确的是( )A.反应②的平衡常数K=
B.氯水中加入硫酸调节pH, pH越低消毒能力越强
C.氯处理饮用水时,在夏季的杀菌效果比在冬季好
D.氯水中加入四氯化碳进行萃取,反应②逆向移动,反应①正向移动
【答案】D
【解析】A项,HCl是强电解质,在溶液中无HCl分子,故反应②的离子方程式为Cl(aq)+ HO
2 2
HClO + H++Cl-,故反应②的平衡常数K= ,A错误;B项,根据反应②的离
子方程式Cl(aq)+ HO HClO + H++Cl-,可知氯水中加入硫酸调节pH, pH越低即H+浓度越大,反
2 2
应②平衡逆向移动,HClO浓度减小,故消毒能力减弱,B错误;C项,氯处理饮用水时,在夏季气温比冬
季高,故过程①平衡逆向移动即Cl 的溶解性减小,故夏季的杀菌效果比在冬季弱,C错误;D项,由于
2
Cl 为非极性分子,四氯化碳也是非极性分子,HO为极性分子,根据“相似相溶”原理,可知Cl 在四氯
2 2 2
化碳的溶解度比在水中大得多,氯水中加入四氯化碳进行萃取,反应②逆向移动,反应①正向移动,D正
确;故选D。
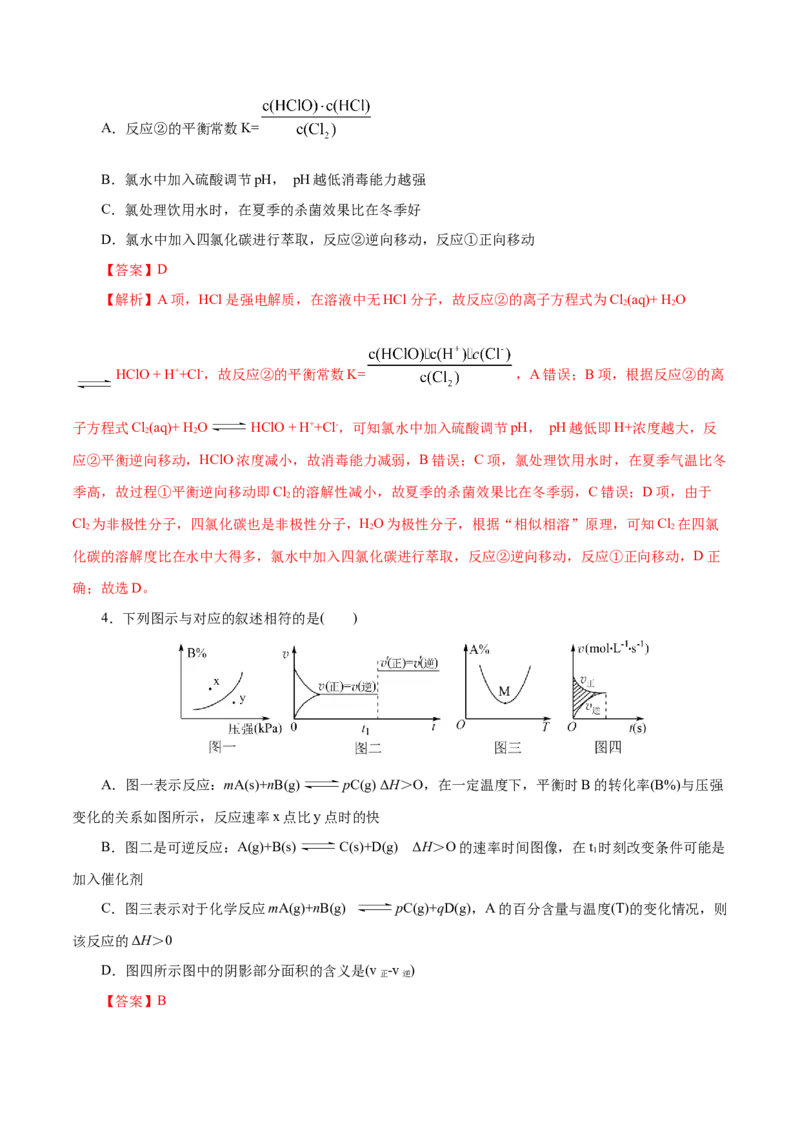
4.下列图示与对应的叙述相符的是( )
A.图一表示反应:mA(s)+nB(g) pC(g) ΔH>O,在一定温度下,平衡时B的转化率(B%)与压强
变化的关系如图所示,反应速率x点比y点时的快
B.图二是可逆反应:A(g)+B(s) C(s)+D(g) ΔH>O的速率时间图像,在t 时刻改变条件可能是
1
加入催化剂
C.图三表示对于化学反应mA(g)+nB(g) pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则
该反应的ΔH>0
D.图四所示图中的阴影部分面积的含义是(v -v )
正 逆
【答案】B【解析】A项,由图一可看出,x点的压强比y点小,所以反应速率x点比y点时的慢,A不正确;B
项,由图二可知,在t 时刻正、逆反应速率都增大且增大的程度相同,所以改变的条件可能是加入催化剂,
1
B正确;C项,由图三可知,在M点之前,反应未达平衡,在M点之后,随着温度的不断升高,A的百分
含量不断增大,则平衡逆向移动,所以该反应的ΔH<0,C不正确;D项,图四表示速率-时间关系曲线,
图中的阴影部分面积的含义是(v -v )t,D不正确;故选B。
正 逆
5.反应NH HS(s) NH (g)+HS(g)在某温度下达到平衡,下列各种情況下,不会使平衡发生移
4 3 2
动的是( )
A.温度、容积不变时,通入SO 气体 B.将NH HS固体全部移走
2 4
C.保持温度和容器体积不变,充入氮气 D.保持温度和压强不变,充入氮气
【答案】C
【解析】A项,通入SO 气体与HS(g)反应生成S,生成物浓度减小,平衡正向移动,故A不选;B
2 2
项,将NH HS固体全部移走,可看成起始加入生成物,平衡逆向移动,故B不选;C项,保持温度和容器
4
体积不变,充入氮气,反应体系中各物质的浓度不变,平衡不移动,故C选;D项,保持温度和压强不变,
充入氮气,体积增大,相等于减小压强,平衡正向移动,故D不选;故选C。
6.硫酸是当今世界上重要的化工产品之一,广泛应用于工业上的各个方面。目前工业上主要采用接
触法制备硫酸,接触室中发生如下反应:2SO (g)+ O (g) 2SO (g)。下列关于该反应的说法中不正
2 2 3
确的是( )
A.升高温度能加快反应速率 B.增大接触室内炉气的压强能加快反应速率
C.添加合适的催化剂可加快反应速率 D.增大O 的浓度能使SO 完全转化
2 2
【答案】D
【解析】A项,温度升高,分子运动速率加快,会加大反应速率,故A正确;B项,增大接触室内炉
气的压强,相当于增大反应物浓度,会加快反应速率,故B正确;C项,添加催化剂,降低反应所需活化
能,能加快反应速率,故C正确;D项,2SO + O 2SO ,可逆反应,反应有限度,反应物不能完
2 2 3
全转化为生成物,故D不正确;故选D。
7.一定条件下,0.3molN(g)与0.3molH(g)在体积为1L的密闭容器中发生反应:N(g)+3H(g)
2 2 2 2
2NH (g),下列示意图合理的是( )
3
A. B.C. D.
【答案】C
【解析】A项,因为为可逆反应,消耗H 物质的量应小于0.3mol,则消耗N 物质的量小于0.1mol,
2 2
则平衡时N 物质的量大于0.2mol,图象不符合,A不符合;B项,反应速率之比等于化学方程式计量数之
2
比,2υ(N ) =υ(NH ) ,此时反应达到平衡状态,υ(N ) =υ(NH ) 时,反应没有达到平衡状态,B不符合;
2 正 3 逆 2 正 3 逆
C项,设转化N 物质的量为x,随反应进行N、H、NH 物质的量依次为(0.3-x)mol、(0.3-3x)mol、
2 2 2 3
2xmol,N 的体积分数为 ×100%=50%,随反应进行N 的体积分数分数不变化恒为50%,
2 2
NH 的体积分数逐渐增大,但小于50%,图象符合,C符合;D项,H 消耗0.1mol,生成NH 物质的量为
3 2 3
mol,图象中反应的定量关系不符合反应比,D不符合;故选C。
8.某密闭容器中,按物质的量之比1:1充入X、Y两种气体,发生反应X(g)+Y(g) 3Z(g) H
>0,达到平衡后,下列有关说法正确的是( ) △
A.继续通入少量物质的量之比为1:1的X、Y气体,保持容器容积不变,达到新平衡时,Z的体积分
数增大
B.其他条件不变,升高温度,正逆反应速率都增大,平衡时Z的体积分数比原平衡的体积分数大,
平衡常数增大
C.其他条件不变,将容积压缩至原来的一半,平衡逆向移动,平衡时X的体积分数比原平衡的体积
分数大,平衡常数减小
D.保持容器容积不变,增加Z的量,平衡逆向移动,平衡时Z的浓度比原平衡的小,体积分数比原
平衡的体积分数小
【答案】B
【解析】A项,此反应的正反应为气体分子数增大的反应,继续通入少量物质的量之比为1:1的X、Y
气体,保持容器容积不变,相当于加压,平衡逆向移动,达到新平衡时,Z的体积分数减小,故A错误;
B项,由题意可知该反应为吸热反应,所以当其他条件不变,升高温度,正逆反应速率都增大,平衡时Z
的体积分数比原平衡的体积分数大,平衡常数增大,故B正确;C项,平衡常数只与温度有关,所以当他
条件不变,将容积压缩至原来的一半,平衡逆向移动,平衡时X的体积分数比原平衡的体积分数大,但平衡常数不变,故C错误;D项,保持容器容积不变,增加Z的量,相当于加压,平衡逆向移动,平衡时Z
的浓度比原平衡的大,体积分数比原平衡的体积分数小,故D错误。故选B。
9.在水溶液中,CrO2-呈黄色,Cr O2-呈橙色,重铬酸钾(K Cr O)在水溶液中存在以下平衡:Cr O2-
4 2 7 2 2 7 2 7
+H O 2CrO2-+2H+,下列说法正确的是( )
2 4
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙色
B.该反应是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液
大
D.向体系中加入少量水,平衡逆向移动
【答案】C
【解析】A项,向该溶液中加入过量浓NaOH溶液后,消耗氢离子,氢离子浓度减小,平衡正向移动,
溶液呈黄色,A错误;B项,反应前后元素的化合价均不发生变化,该反应不是氧化还原反应,B错误;C
项,向该溶液中滴加适量的浓硫酸,氢离子浓度增大,平衡向逆反应方向移动,由于只能是减弱这种改变,
所以再次达到平衡后,氢离子浓度比原溶液大,C正确;D项,向体系中加入少量水,相当于稀释,平衡
正向移动,D错误;故选C。
10.硫酰氯(SO Cl)是一种重要的磺化试剂,其可利用SO (g)+ Cl (g) SOCl (g) ∆H<0制备。
2 2 2 2 2
1000C时,该反应的压强平衡常数 ,在恒温恒容的容器中发生反应,下列说法正确的
是( )
A.已知硫酰氯结构式为 ,硫酰氯每个原子均达到8电子稳定结构
B.容器内气体的平均摩尔质量不变时,反应达到平衡
C.温度升高,平衡逆向移动,反应的压强平衡常数增大
D.上述制备硫酰氯的反应,在高温下自发
【答案】B
【解析】A项,已知硫酰氯结构式为 ,硫原子的最外层电子全部参与成键,所以硫原子已达
12个电子,A错误;B项,因为反应体系中反应物和生成物都是气体,正向气体体积减小的反应,所以只
不达到平衡状态,气体的总物质的量都在变化,则气体的平均摩尔质量也在变化,当容器内气体的平均摩尔质量不变时,反应达到平衡,B正确;C项,该反应正向为放热反应,温度升高,平衡逆向移动,反应
的压强平衡常数减小,C错误;D项,该反应为气体体积减小的反应,△S<0,又因为△H<0,在低温
时易自发进行,D错误;故选B。
11.侯氏制碱法以氯化钠、二氧化碳、氨和水为原料,发生反应
NaCl+NH +CO +H O=NaHCO ↓+NHCl。将析出的固体灼烧获取纯碱,向析出固体后的母液中加入食盐可
3 2 2 3 4
获得副产品氯化铵,通过以下两步反应可实现NH Cl分解产物的分离:
4
NH Cl(s)+MgO(s) NH (g)+Mg(OH)Cl(s) ΔH=+61.34kJ·mol-1
4 3
Mg(OH)Cl(s) HCl(g)+MgO(s) ΔH=+97.50kJ·mol-1
下列说法不正确的是( )
A.反应NH Cl(s)=NH (g)+HCl(g)的ΔH=+158.84kJ·mol-1
4 3
B.两步反应的ΔS均大于0
C.MgO是NH Cl分解反应的催化剂
4
D.5.35gNHCl理论上可获得标准状况下的HCl约2.24L
4
【答案】C
【解析】A项,由盖斯定律,两式相加可得:NH Cl(s)=NH (g)+HCl(g) ΔH=+158.84kJ·mol-1,A正确;
4 3
B项,气体混乱度越大,S越大,则两步反应的ΔS均大于0,B正确;C项,MgO参与了NH Cl分解,不
4
是催化剂,C错误;D项,5.35gNHCl的物质的量 ,由反应NH Cl(s)=NH (g)
4 4 3
+HCl(g),可生成0.1molHCl,标准状况下体积为V=nV =2.24L,D正确;故选C。
m
12.二氧化碳催化加氢制甲醇的反应为3H(g)+CO(g) HO(g)+CHOH(g) ∆H<0。下列说法正
2 2 3
确的是( )
A.增大压强,平衡正向进行,该反应的平衡常数K增大
B.升高温度可使该反应的正反应速率增大,逆反应速率减小
C.温度越低越有利于该反应的进行,从而提高甲醇的生产效率
D.使用高效催化剂,可降低反应的活化能,增大活化分子百分数
【答案】D
【解析】A项,该反应的正反应是气体分子数减小的反应,因此增大压强,平衡向正向进行,但平衡
常数K不变,平衡常数K只与温度有关,A项错误;B项,升高温度可使该反应的正、逆反应速率均增大,
B项错误;C项,反应的正反应是放热反应,在一定范围内,降低温度有理于平衡向正向移动,能提高甲醇的生产效率,温度过低不利于反应的进行,C项错误;D项,使用高效催化剂,可降低反应的活化能,
增大活化分子百分数,增加反应速率,D项正确;故选D。
13.人体内的血红蛋白(Hb)可与O 结合形成HbO ,Hb(aq)也可以与CO结合,人体发生CO中毒的原
2 2
理为:HbO (aq)+CO(g) HbCO(aq)+O (g) ΔH<0.下列说法不正确的是( )
2 2
A.海拔较高的地区由于气压较低,所以血红蛋白较难与O 结合,容易产生缺氧现象
2
B.已知CO中毒为熵减过程,则理论上冬天比夏天可能更容易发生CO中毒现象
C.把CO中毒的人转到高压氧仓中有助于缓解症状
D.此反应的平衡常数K=
【答案】D
【解析】A项,根据方程式Hb (aq)+O(g) HbO (aq)可知正反应是一个气体体积减小的方向,
2 2
减小压强,平衡逆向移动,A正确;B项,根据HbO (aq)+CO(g) HbCO(aq)+O(g) ΔH<0,ΔS<
2 2
0可知反应低温自发,B正确;C项,增加氧气的浓度可以使平衡逆向移动,C正确;D项,根据反应方程
式可知,该反应的平衡常数K= ,D错误;故选D。
14.一定温度的密闭容器中,反应A(g)+B(g) 2C(g) ΔH>0达平衡。则下列有关说法不正确的
是( )
A.相同时间内,存在消耗关系:
B.其他条件不变,增大压强或添加催化剂,c (A)、c (B)不变
C.反应正向的活化能一定大于逆向的活化能
D.同一温度下,平衡浓度与平衡压强存在关系:Kc =Kp
【答案】B
【解析】A项,因化学反应的速率比等于方程式计量数之比,相同时间内,存在消耗关系:
,故A正确;B项, 反应A(g)+B(g) 2C(g)是反应前后气体的体积不变的反应,其他
条件不变,增大压强或添加催化剂,平衡不移动,但改变压强后c (A)、c (B)可能发生改变,故B错误;
C项, 反应正向的活化能一定大于逆向的活化能,反应是吸热反应,故C正确;D项, Kc被称为平衡常数,它是用平衡浓度来量度的,Kc= ,对于气相反应,我们还可以用平衡分压Kp,来表示对于
气相反应A(g)+B(g) 2C(g) 而言Kp= ,通过克拉伯龙方程PV=nRT,我们可以导出Kp与
K的关系Kp=Kc(RT) n (Δn=2-1-1=0),同一温度下,平衡浓度与平衡压强存在关系:Kc =Kp,故D正确;
△
故选B。
15.830℃,在某容器中充入物质的量之比为1∶1的CO和水蒸气,发生反应:CO(g)+HO(g)
2
CO(g)+H(g),10 min后到达平衡,已知该温度下反应平衡常数是1.0,下列叙述正确的是( )
2 2
A.水蒸气的平衡转化率为50%
B.温度高于830℃时K<1.0,则该反应的
C.反应至5min时,CO 的物质的量分数小于12.5%
2
D.向平衡后的体系中充入一定量的H,重新达到平衡后K>1.0
2
【答案】A
【解析】设CO(g)、HO(g)的物质的量都为1mol,根据反应可列三段式:
2
则K= =1.0,x=0.5。A项,水蒸气的平衡转化率为 ×100%=50%,故A正确;B项,温度
高于830℃时K<1.0,说明升高温度,平衡逆向移动,则正反应为放热反应,该反应的△H<0,故B错误;
C项,平衡时CO 的物质的量分数为 ×100%=25%,随着反应的进行,正反应速率逐渐减小,则前
2
5min速率大于5-10min的速率,可知反应至5min时,CO 的物质的量分数大于12.5%,故C错误;D项,
2
平衡常数只与温度有关,向平衡后的体系中充入一定量的H,如温度不变,则平衡常数不变,故D错误;
2
故选A。
16.830℃,在某容器中充入物质的量之比为1∶1的CO和水蒸气,发生反应:CO(g)+HO(g)
2CO(g)+H(g),10 min后到达平衡,已知该温度下反应平衡常数是1.0,下列叙述正确的是( )
2 2
A.水蒸气的平衡转化率为50%
B.温度高于830℃时K<1.0,则该反应的
C.反应至5min时,CO 的物质的量分数小于12.5%
2
D.向平衡后的体系中充入一定量的H,重新达到平衡后K>1.0
2
【答案】A
【解析】设CO(g)、HO(g)的物质的量都为1mol,根据反应可列三段式:
2
则K= =1.0,x=0.5。A项,水蒸气的平衡转化率为 ×100%=50%,故A正确;B项,温度
高于830℃时K<1.0,说明升高温度,平衡逆向移动,则正反应为放热反应,该反应的△H<0,故B错误;
C项,平衡时CO 的物质的量分数为 ×100%=25%,随着反应的进行,正反应速率逐渐减小,则前
2
5min速率大于5-10min的速率,可知反应至5min时,CO 的物质的量分数大于12.5%,故C错误;D项,
2
平衡常数只与温度有关,向平衡后的体系中充入一定量的H,如温度不变,则平衡常数不变,故D错误;
2
故选A。
17.对利用甲烷消除NO 污染进行研究,CH+2NO N+CO +2H O。在2L密闭容器中,控制不
2 4 2 2 2 2
同温度,分别加入0.50molCH 和1.2nolNO ,测得n(CH)随时间变化的有关实验数据见表。
4 2 4
时间/min
组别 温度 0 10 20 40 50
n/mol
① T n(CH) 0.50 0.35 0.25 0.10 0.10
1 4
② T n(CH) 0.50 0.30 0.18 … 0.15
2 4
下列说法不正确的是( )
A.组别①中,0~10min内,CO 的生成速率为0.0075mol·L-1·min-1
2
B.0~20min内,NO 的降解速率①>②
2C.40min时,表格中T 对应的数据为0.15
2
D.由实验数据可知实验控制的温度T①,相同的时间内N⋅ O⋅降解速率:
4 2
②>①,故B不正确;C项,40min时组别①中甲烷的物质的量不再改变,说明反应达到平衡,组别②反应
速率比组别①更快,所以40min时组别②也已经达到平衡,所以表格中T 对应的数据为0.15,故C正确;
2
D项,开始时CH 的物质的量相同,10min后,T 温度时甲烷物质的量更小,说明反应速率快,温度越高
4 2
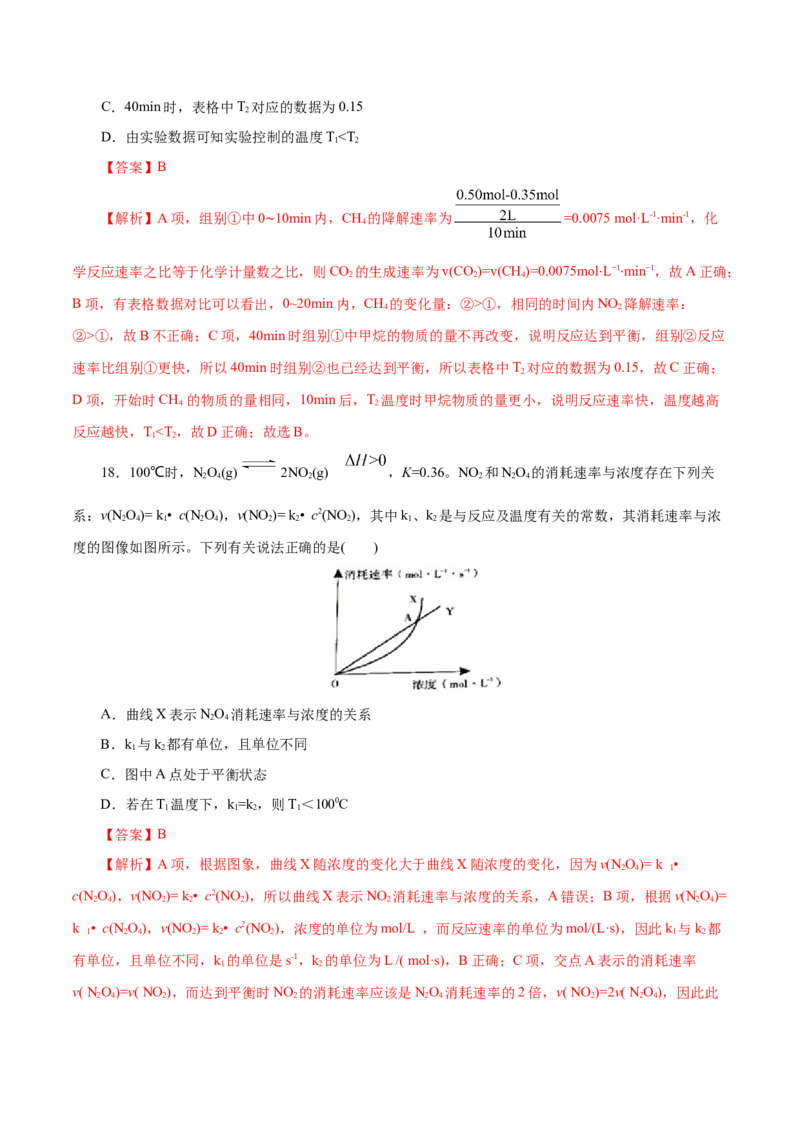
反应越快,Tv(正),B错误;C项,由
题干信息可知,则:
故化学平衡为 ,C正确;D项,该反应前后气体系数之和相等,当其他条件不变时,再充入0.2molZ,重新达到平衡,与原平衡为等效平衡,则平衡时X的体积分数不变,D错误;故
选C。
20.某反应 的速率方程为 ,其半衰期(当剩余反
应物恰好是起始的一半时所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示:
c(A)/( mol·L-1) c(B)/( mol·L-1) v/(10-3mol·L-1·min-1)
0.25 0.050 1.4
0.50 0.050 2.8
1.00 0.050 5.6
0.50 0.100 2.8
下列说法正确的是( )
A.速率方程中的 、
B.该反应的速率常数k=2.8×10-3min-1
C.增大反应物浓度,k增大导致反应的瞬时速率加快
D.在过量的B存在时,反应掉87.5%的A所需的时间是375min
【答案】D
【解析】A项,将第一组数据和第二组数据代入 可得 ,则
m=1,将第二组数据和第四组数据代入 可得 ,则n=0,A错误;
B项,由A选项的分析可知,m=1,n=0,则 ,代入第一组数据可得,k=5.6×10-3min-1,B错
误;C项,增大反应物的浓度,增大了速率,并没有改变瞬时速率常数k(只受温度影响),C错误;D项,
存在过量的B时,反应掉87.5%的A可以看作经历3个半衰期,即50%+25%+12.5%,因此所需的时间为,D正确;故选D。
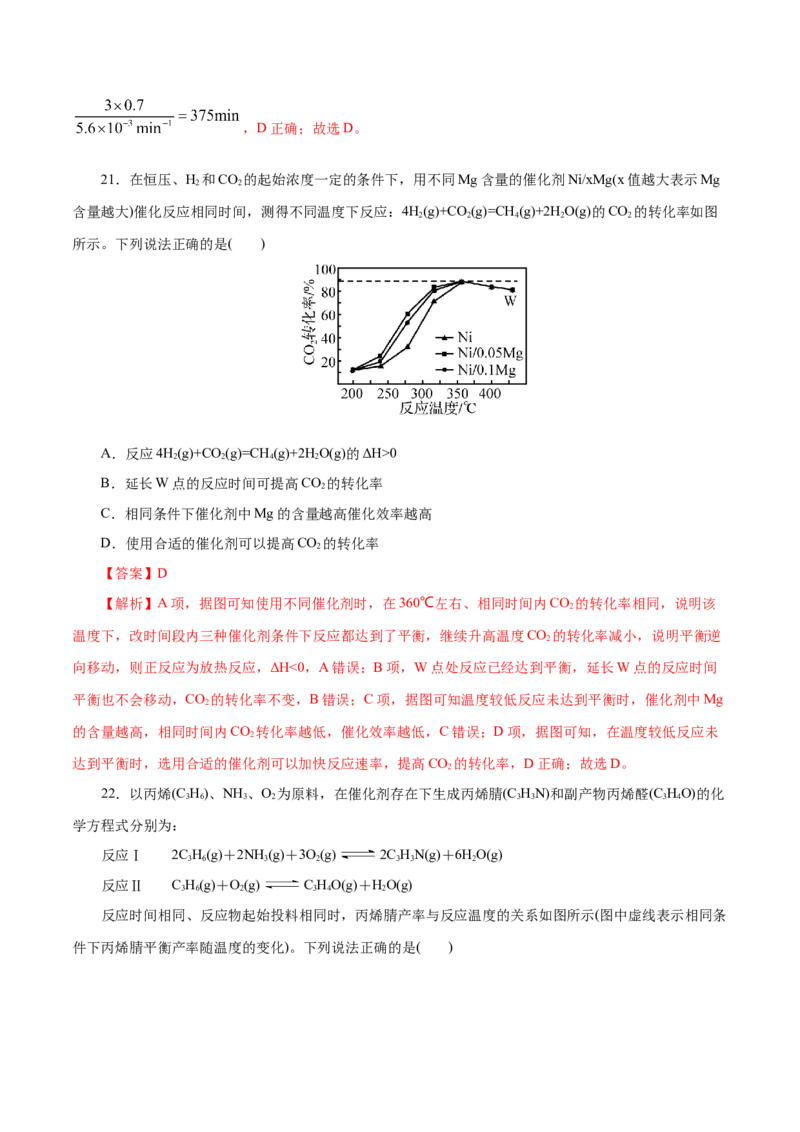
21.在恒压、H 和CO 的起始浓度一定的条件下,用不同Mg含量的催化剂Ni/xMg(x值越大表示Mg
2 2
含量越大)催化反应相同时间,测得不同温度下反应:4H(g)+CO (g)=CH (g)+2HO(g)的CO 的转化率如图
2 2 4 2 2
所示。下列说法正确的是( )
A.反应4H(g)+CO (g)=CH (g)+2HO(g)的ΔH>0
2 2 4 2
B.延长W点的反应时间可提高CO 的转化率
2
C.相同条件下催化剂中Mg的含量越高催化效率越高
D.使用合适的催化剂可以提高CO 的转化率
2
【答案】D
【解析】A项,据图可知使用不同催化剂时,在360℃左右、相同时间内CO 的转化率相同,说明该
2
温度下,改时间段内三种催化剂条件下反应都达到了平衡,继续升高温度CO 的转化率减小,说明平衡逆
2
向移动,则正反应为放热反应,ΔH<0,A错误;B项,W点处反应已经达到平衡,延长W点的反应时间
平衡也不会移动,CO 的转化率不变,B错误;C项,据图可知温度较低反应未达到平衡时,催化剂中Mg
2
的含量越高,相同时间内CO 转化率越低,催化效率越低,C错误;D项,据图可知,在温度较低反应未
2
达到平衡时,选用合适的催化剂可以加快反应速率,提高CO 的转化率,D正确;故选D。
2
22.以丙烯(C H)、NH 、O 为原料,在催化剂存在下生成丙烯腈(C HN)和副产物丙烯醛(C HO)的化
3 6 3 2 3 3 3 4
学方程式分别为:
反应Ⅰ 2C H(g)+2NH (g)+3O(g) 2C HN(g)+6HO(g)
3 6 3 2 3 3 2
反应Ⅱ C H(g)+O(g) C HO(g)+HO(g)
3 6 2 3 4 2
反应时间相同、反应物起始投料相同时,丙烯腈产率与反应温度的关系如图所示(图中虚线表示相同条
件下丙烯腈平衡产率随温度的变化)。下列说法正确的是( )A.其他条件不变,增大压强有利于提高丙烯腈平衡产率
B.图中X点所示条件下,延长反应时间或使用更高效催化剂均能提高丙烯腈产率
C.图中Y点丙烯腈产率高于X点的原因是温度升高导致反应I建立的平衡向正反应方向移动
D.图中X点丙烯腈产率与Z点相等(T <T),则一定有Z点的正反应速率大于X点的正反应速率
1 2
【答案】B
【解析】A项,反应Ⅰ中正反应体积增大,反应Ⅱ中反应前后体积不变,因此其他条件不变,增大压
强不有利于提高丙烯腈平衡产率,A错误;B项,根据图像可知图中X点所示条件下反应没有达到平衡状
态,又因为存在副反应,因此延长反应时间或使用更高效催化剂均能提高丙烯腈产率,B正确;C项,根
据图像可知图中X点、Y点所示条件下反应均没有达到平衡状态,Z点反应达到平衡状态,升高温度平衡
逆向进行,因此图中Y点丙烯腈产率高于X点的原因不是因为温度升高导致反应I建立的平衡向正反应方
向移动,C错误;D项,由于温度会影响催化剂的活性,因此Z点的正反应速率不一定大于X点的正反应
速率,D错误;故选B。
23.将1molM和2molN置于体积为2L的恒容密闭容器中,发生反应:M(s)+2N(g) P(g)+Q(g)
H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
△
A.升高温度、及时分离出产物均有利于提高反应物的平衡转化率
B.若X、Y两点的平衡常数分别为K 、K ,则K K ,B错误;C项,该反应前后气体计量数之和不变,则反应前后气体物质的量不变,恒温恒容时气体
1 2
压强始终不变,所以不能根据压强判断平衡状态,C错误;D项,温度为T 时,该反应前后气体计量数之
1
和不变,则反应前后气体物质的量不变,由图知P的平衡浓度为 , 列三段式得:
所以N的平衡转化率 =80%,D正确;故选D。
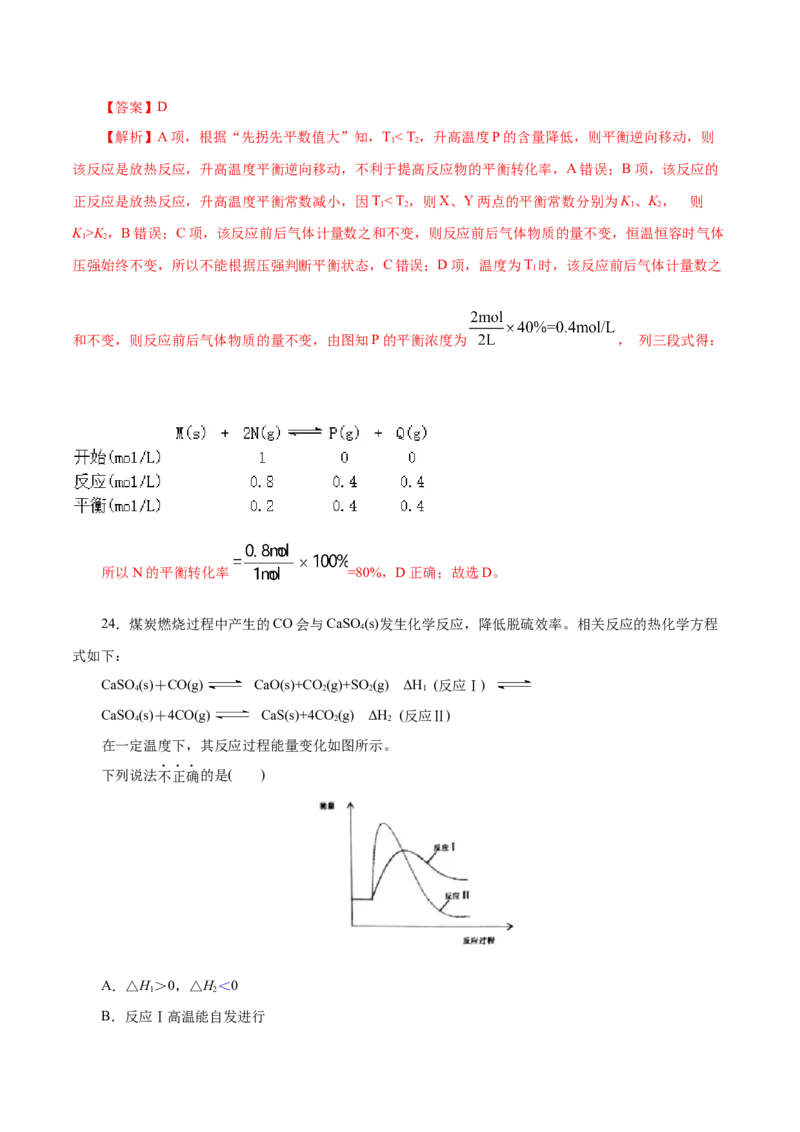
24.煤炭燃烧过程中产生的CO会与CaSO(s)发生化学反应,降低脱硫效率。相关反应的热化学方程
4
式如下:
CaSO(s)+CO(g) CaO(s)+CO (g)+SO(g) ΔH (反应Ⅰ)
4 2 2 1
CaSO(s)+4CO(g) CaS(s)+4CO (g) ΔH (反应Ⅱ)
4 2 2
在一定温度下,其反应过程能量变化如图所示。
下列说法不正确的是( )
A.△H>0,△H<0
1 2
B.反应Ⅰ高温能自发进行C.反应Ⅰ的速率(v)大于反应Ⅱ的速率(v)
1 2
D.在恒温恒容下,二氧化硫浓度一直增大直至达到平衡
【答案】D
【解析】A项,由图可知,反应Ⅰ为吸热反应,反应Ⅱ为放热反应,所以△H>0,△H<0,故A正
1 2
确;B项,由图可知,CaSO(s)+CO(g) CaO(s)+CO (g)+SO(g) ΔH >0,该反应为气体体积增大
4 2 2 1
的反应,△S>0,由△G= H-T S可知,高温能自发进行,故B正确;C项,由图可知,反应Ⅰ的活化能
较低,所以反应速率(v)大△于反应△Ⅱ的速率(v),故C正确;D项,反应Ⅰ和反应Ⅱ同时进行,而且反应速
1 2
率(v)大于反应Ⅱ的速率(v),刚开始生成的二氧化硫速率快,随着反应的进行,生成的二氧化碳越来越多,
1 2
促使反应Ⅰ逆向移动,导致二氧化硫的量降低,直至达到平衡,所以二氧化硫浓度先增大后减小,最后不
变,故D错误;故选D。
25.25℃时,将20mL3x mol·L-1NaAsO、20mL3x mol·L-1I 和20mL NaOH溶液混合,发生反应:
3 3 2
AsO3−(aq)+I(aq)+ 2OH−(aq)= AsO3−(aq)+2I(aq)+HO(l)。溶液中c(AsO3−)与反应时间(t)的关系如图所示。
3 2 4 - 2 4
下列说法正确的是
A.0~ t min用HO表示的平均反应速率为
1 2
B.当2v (AsO3−)=v (I-)时,反应达到平衡状态
正 3 逆
C.a点的逆反应速率小于b点的正反应速率
D.平衡时溶液的pH=13,则该反应的平衡常数
【答案】C
【解析】A项,一般不用纯固体、纯液体表示反应速率,不能用HO表示该反应的平均反应速率,故
2
A错误;B项,依据反应速率之比等于化学计量数之比,当2v (AsO3−)=v (I-)时,正逆反应速率相等,反
正 3 逆
应达到平衡状态,故B错误;C项,由图可知,a到b的过程中,反应一直正向进行,正反应速率一直减
小,逆反应速率一直增大,直到增大到与正反应速率相等,反应达到平衡状态,在反应达到平衡前,逆反应速率均小于正反应速率,a点和b点均未达到平衡状态,且a到b反应逐渐趋于平衡,a点的逆反应速率
小于b点的正反应速率,故C正确;D项,根据题意,溶液混合后起始时,c(AsO3−)= c(I-)= x mol·L-1,由
3
图可知, 平衡时c(AsO3−)=y mol·L-1,c(I)= 2y mol·L-1,c(AsO3−)= c(I)=(x- y) mol·L-1,平衡时溶液的
4 2 3 2
pH=13,则c(OH-)=0.1mol·L-1,反应的平衡常数 ,故D错误;故选
C。
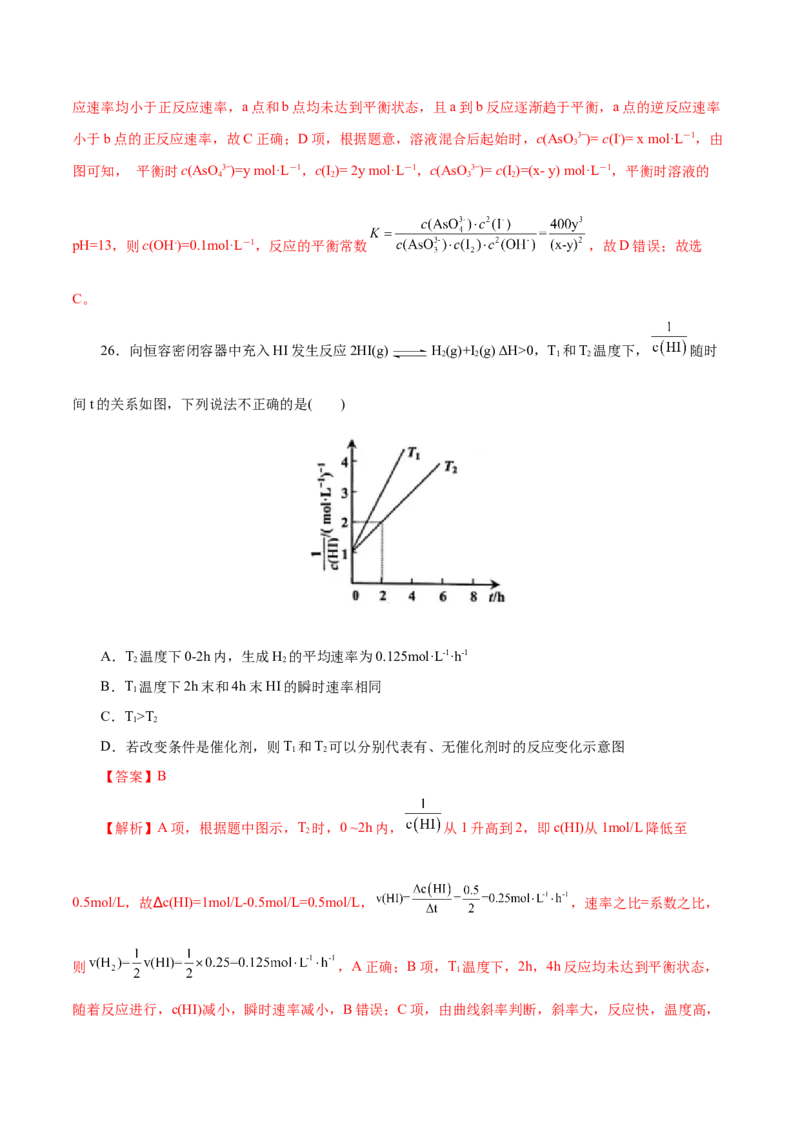
26.向恒容密闭容器中充入HI发生反应2HI(g) H(g)+I (g) ΔH>0,T 和T 温度下, 随时
2 2 1 2
间t的关系如图,下列说法不正确的是( )
A.T 温度下0-2h内,生成H 的平均速率为0.125mol·L-1·h-1
2 2
B.T 温度下2h末和4h末HI的瞬时速率相同
1
C.T>T
1 2
D.若改变条件是催化剂,则T 和T 可以分别代表有、无催化剂时的反应变化示意图
1 2
【答案】B
【解析】A项,根据题中图示,T 时,0 ~2h内, 从1升高到2,即c(HI)从1mol/L降低至
2
0.5mol/L,故∆c(HI)=1mol/L-0.5mol/L=0.5mol/L, ,速率之比=系数之比,
则 ,A正确;B项,T 温度下,2h,4h反应均未达到平衡状态,
1
随着反应进行,c(HI)减小,瞬时速率减小,B错误;C项,由曲线斜率判断,斜率大,反应快,温度高,故T>T,C正确;D项,T 曲线斜率大,说明反应速率快,表示有催化剂,T 没有催化剂,D正确;故选
1 2 1 2
B。
27.2SO (g)+O(g) 2SO (g)是工业制备硫酸的重要反应,恒温恒容条件下c(SO )随时间的变化
2 2 3 3
如图中曲线Ⅰ所示。下列说法正确的是( )
A.t~tmin,v(SO ) = mol·L-1·min-1
1 2 3 正
B.曲线Ⅱ对应的条件改变可能是增大了压强
C.工业上采用高温高压的反应条件以提高SO 的转化率
2
D.相同条件下,t 时再充入与起始投料等量的反应物,达到平衡后,SO 转化率增大
3 2
【答案】D
【解析】A项,由图中曲线Ⅰ,t~tmin内,三氧化硫的浓度变化量为(c—c),反应速率v(SO ) =
1 2 1 2 3 正
mol·L-1·min-1,故A错误;B项,若曲线Ⅱ对应的条件改变是增大了压强,则平衡正向移动,即曲线
Ⅱ条件下反应达到平衡时,三氧化硫的浓度应大于曲线Ⅰ,与题给图示不符,故B错误;C项,该反应是
放热反应,升高温度,平衡向逆反应方向移动,二氧化硫的转化率减小,故C错误;D项,相同条件下,
t 时再充入与起始投料等量的反应物相当于增大混合气体的压强,该反应是气体体积减小的反应,增大压
3
强,平衡向正反应方向移动,二氧化硫的转化率增大,故D正确;故选D。
28.在催化剂作用下,向刚性容器中按物质的量比1︰1充入甲醇和异丁烯(用R表示),分别在T 和T
1 2
两个温度下发生反应生成有机物W:CHOH(g)+R(g) W(g) ΔH。异丁烯的转化率随时间的变化关系如
3
图所示。下列说法正确的是( ) ⇌A.T>T,ΔH>0
1 2
B.v =v >v
M正 B正 A逆
C.维持T 不变,再向容器中充入1 mol W,新平衡时W的百分含量减小
2
D.T 时,容器内起始总压为p kPa,则用分压表示的该反应的平衡常数K= kPa-1
1 0 p
【答案】D
【解析】A项,“先拐先平数值大”,T 先拐,所以T>T,由T 到T,温度升高,异丁烯的转化率
1 1 2 2 1
降低,即平衡逆向移动,逆向为吸热反应,则ΔH<0,A项不符合题意;B项,温度相同时,M点和B点
异丁烯的转化率相同,即异丁烯的浓度相同,有 ,但是M点对应的温度T 偏高,所以
1
vM(正)>vB(逆),B项不符合题意;C项,其他条件不变,再冲入1molW,使R的转化率提高,而W自身
的转化率降低,此时W的百分含量会相应升高,C项不符合题意;D项,假设甲醇和异丁烯的初始物质的
量都是1mol,T 时异丁烯的转化率为80%,则消耗的异丁烯为0.8mol,列出三段式:
1
平衡时总物质的量为0.2+0.2+0.8=1.2mol,因为是刚性容器,所以容器体积不变,则压强改变,初始
压强为p,平衡时压强为 ,则 ,
0
, kPa-1,D项符合题意;故选D。
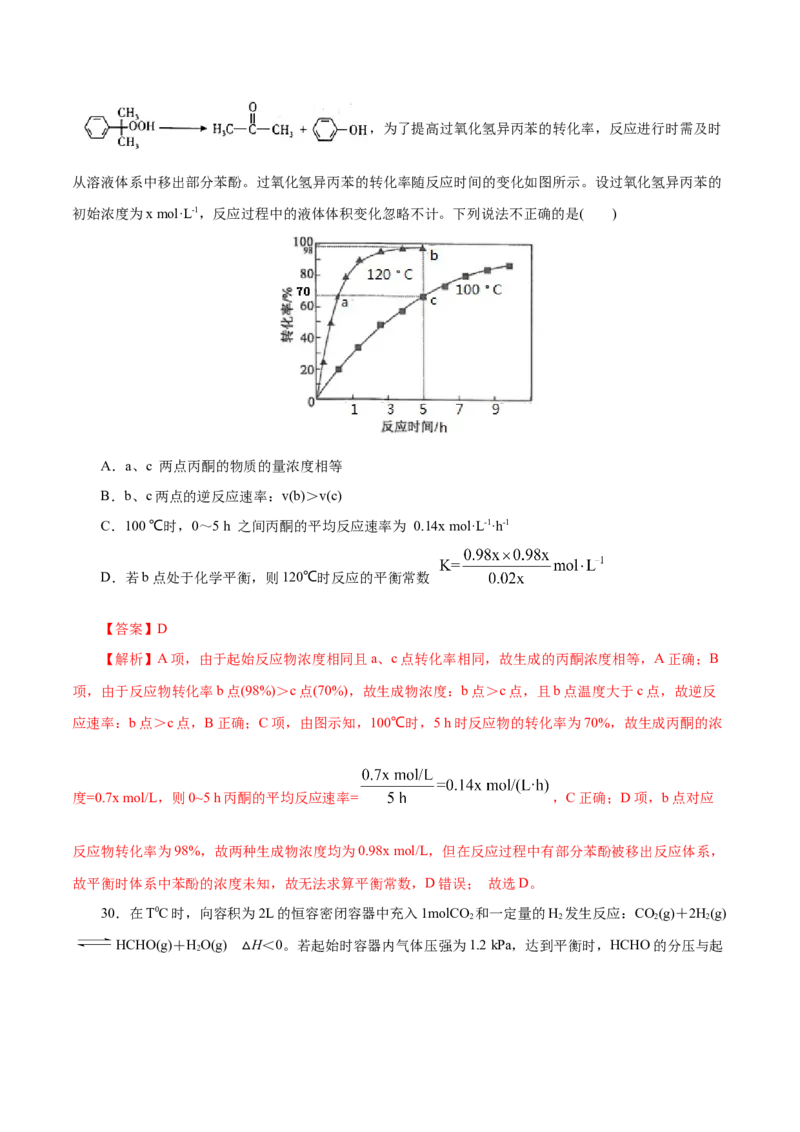
29.丙酮是重要的有机合成原料,可以由过氧化氢异丙苯合成。其反应为:,为了提高过氧化氢异丙苯的转化率,反应进行时需及时
从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的
初始浓度为x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法不正确的是( )
A.a、c 两点丙酮的物质的量浓度相等
B.b、c两点的逆反应速率:v(b)>v(c)
C.100 ℃时,0~5 h 之间丙酮的平均反应速率为 0.14x mol·L-1·h-1
D.若b点处于化学平衡,则120℃时反应的平衡常数
【答案】D
【解析】A项,由于起始反应物浓度相同且a、c点转化率相同,故生成的丙酮浓度相等,A正确;B
项,由于反应物转化率b点(98%)>c点(70%),故生成物浓度:b点>c点,且b点温度大于c点,故逆反
应速率:b点>c点,B正确;C项,由图示知,100℃时,5 h时反应物的转化率为70%,故生成丙酮的浓
度=0.7x mol/L,则0~5 h丙酮的平均反应速率= ,C正确;D项,b点对应
反应物转化率为98%,故两种生成物浓度均为0.98x mol/L,但在反应过程中有部分苯酚被移出反应体系,
故平衡时体系中苯酚的浓度未知,故无法求算平衡常数,D错误; 故选D。
30.在T0C时,向容积为2L的恒容密闭容器中充入1molCO 和一定量的H 发生反应:CO(g)+2H(g)
2 2 2 2
HCHO(g)+HO(g) H<0。若起始时容器内气体压强为1.2kPa,达到平衡时,HCHO的分压与起
2
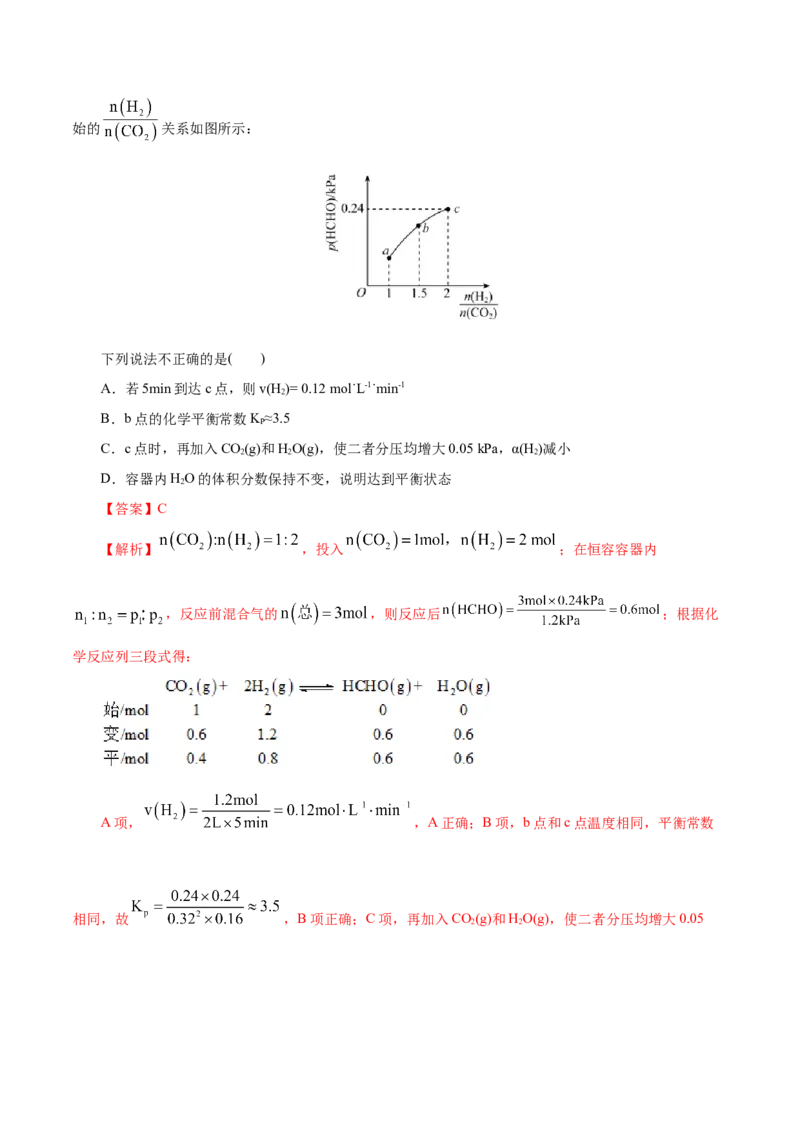
△始的 关系如图所示:
下列说法不正确的是( )
A.若5min到达c点,则v(H )= 0.12 mol˙L-1˙min-1
2
B.b点的化学平衡常数K ≈3.5
P
C.c点时,再加入CO(g)和HO(g),使二者分压均增大0.05kPa,α(H )减小
2 2 2
D.容器内HO的体积分数保持不变,说明达到平衡状态
2
【答案】C
【解析】 ,投入 ;在恒容容器内
,反应前混合气的 ,则反应后 ;根据化
学反应列三段式得:
A项, ,A正确;B项,b点和c点温度相同,平衡常数
相同,故 ,B项正确;C项,再加入CO(g)和HO(g),使二者分压均增大0.05
2 2kPa,则 ,化学平衡向右移动,故H 的转化率增大,C项错误;D项,在2L容器
2
内HO的体积分数保持不变,各物质的浓度保持不变,反应达到平衡状态,D项正确;故选C。
2