文档内容
专题 10 大题突破——化学工艺流程
目录
01 模拟基础练
【题型一】工艺流程中的操作判断及操作步骤书写
【题型二】工艺流程中的条件控制及原因分析
【题型三】产物或反应物推断、陌生方程式的书写
【题型四】数据的分析与处理
02 重难创新练
03 真题实战练
题型一 工艺流程中的操作判断及操作步骤书写
1.(2025·山西省学业水平考试适应性测试,节选)以黄铁矿或硫黄为原料生产硫酸,同时将产出的炉
渣进行资源化利用的一种工艺流程如图所示:
(1)在反应前,需要粉碎黄铁矿,其目的是 。
2.[真题改编](2021·河北,14(4))向含NH Cl的滤液中加入NaCl粉末,存在NaCl(s)+
4
NH Cl(aq)→NaCl(aq)+NH Cl(s)过程。为使NH Cl沉淀充分析出并分离,根据NaCl和NH Cl溶解度曲线,
4 4 4 4
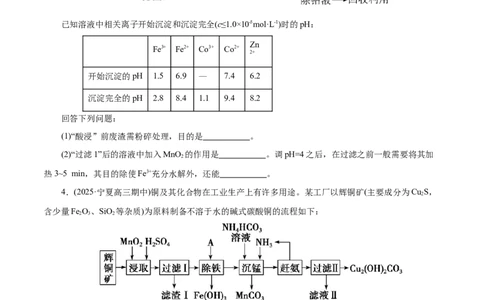
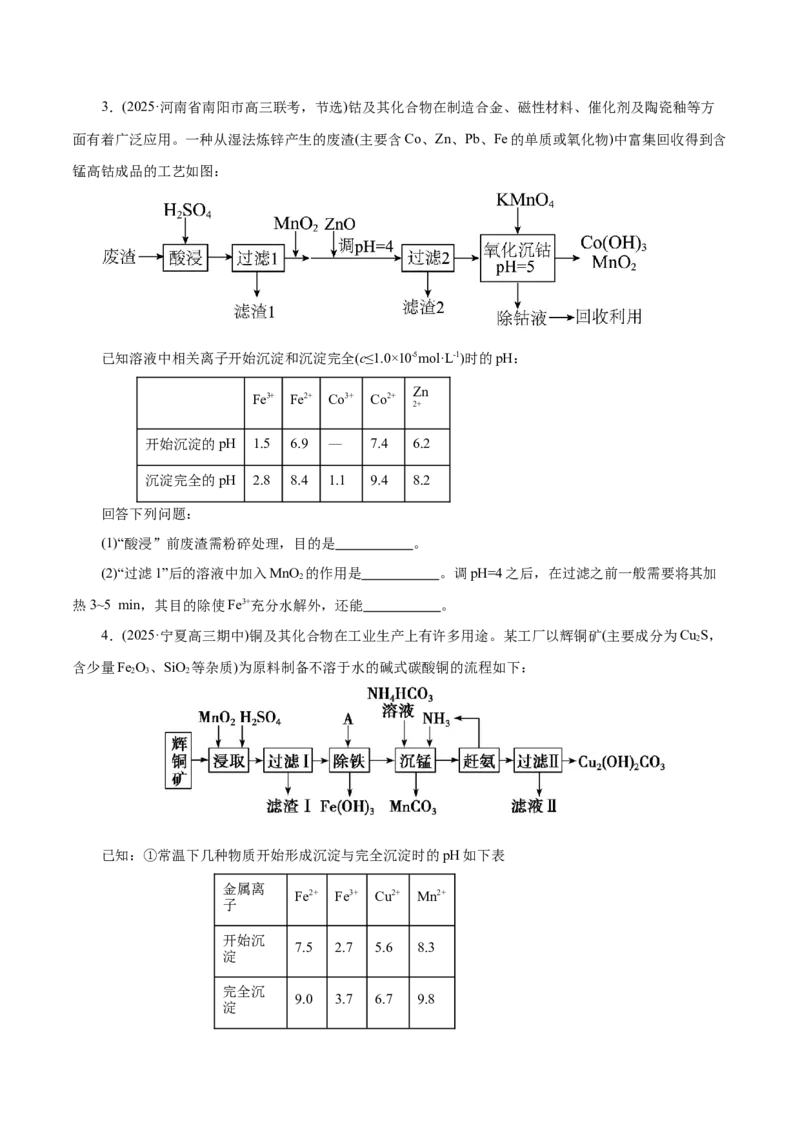
需采用的操作__________、__________、洗涤、干燥。3.(2025·河南省南阳市高三联考,节选)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方
面有着广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含
锰高钴成品的工艺如图:
已知溶液中相关离子开始沉淀和沉淀完全(c≤1.0×10-5mol·L-1)时的pH:
Zn
Fe3+ Fe2+ Co3+ Co2+
2+
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是 。
(2)“过滤1”后的溶液中加入MnO 的作用是 。调pH=4之后,在过滤之前一般需要将其加
2
热3~5 min,其目的除使Fe3+充分水解外,还能 。
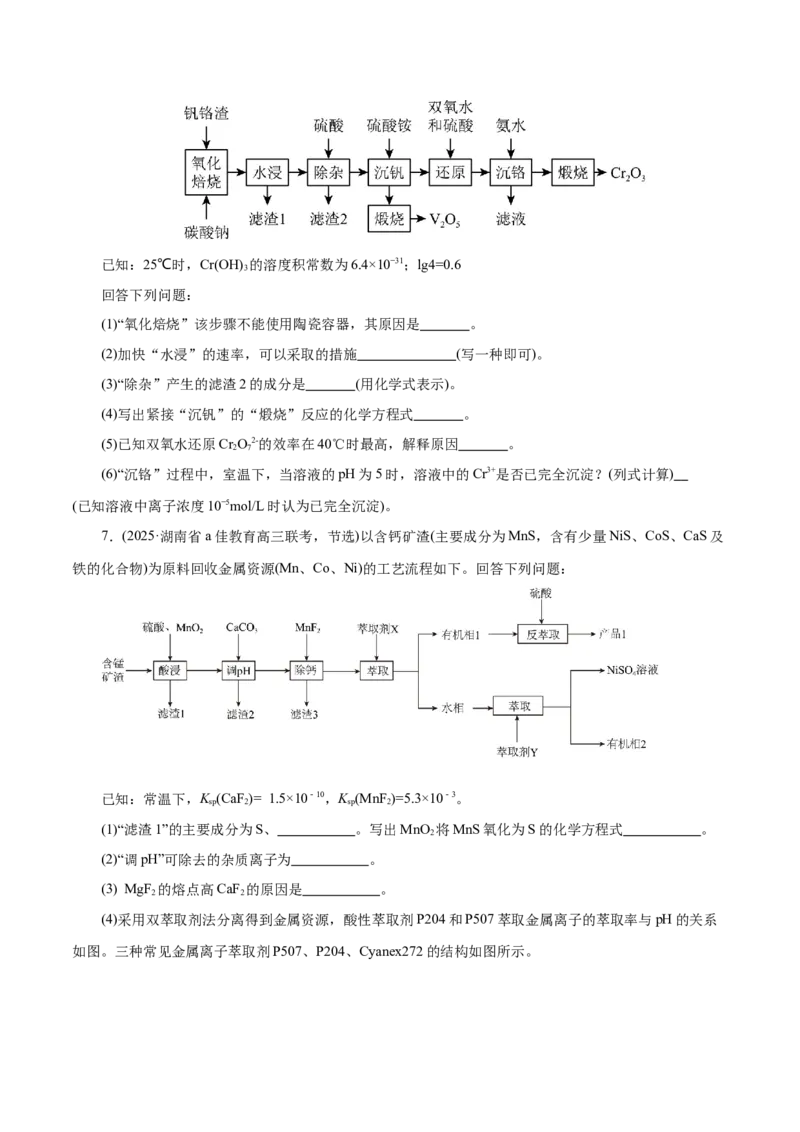
4.(2025·宁夏高三期中)铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu S,
2
含少量Fe O、SiO 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
2 3 2
已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离
Fe2+ Fe3+ Cu2+ Mn2+
子
开始沉
7.5 2.7 5.6 8.3
淀
完全沉
9.0 3.7 6.7 9.8
淀(1)为提高“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有 (任写一种)。
(2)辉铜矿中亚铜离子的价电子排布式为 。
(3)滤渣I中的主要成分是MnO 、S、SiO,请写出“浸取”反应中生成S的离子反应方程式:
2 2
。
(4)常温下“除铁”时加入的试剂A可以是 ,pH的调节范围为 。
(5)过滤II得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是 。
题型二 工艺流程中的条件控制及原因分析
5.(2025·四川省德阳市高三联考,节选)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形
式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:①最高价铬酸根在酸性介质中以Cr O2-存在,在碱性介质中以CrO2-存在。
2 7 4
②相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Fe3+ Al3+ Mg2+
开始沉淀的pH 1.5 3.4 9.0
沉淀完全的pH 2.8 4.7 10.9
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是 。
(4)“除硅磷”步骤中,使硅以MgSiO 的形式沉淀,该步需要控制溶液的pH≈9以上,pH>9时,会导
3
致 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO +或
2 5 2 5 2
VO3+,在碱性条件下,溶解为VO -或VO 3-,上述性质说明VO 具有 (填标号)。
3 4 2 5
A.酸性 B.碱性 C.两性
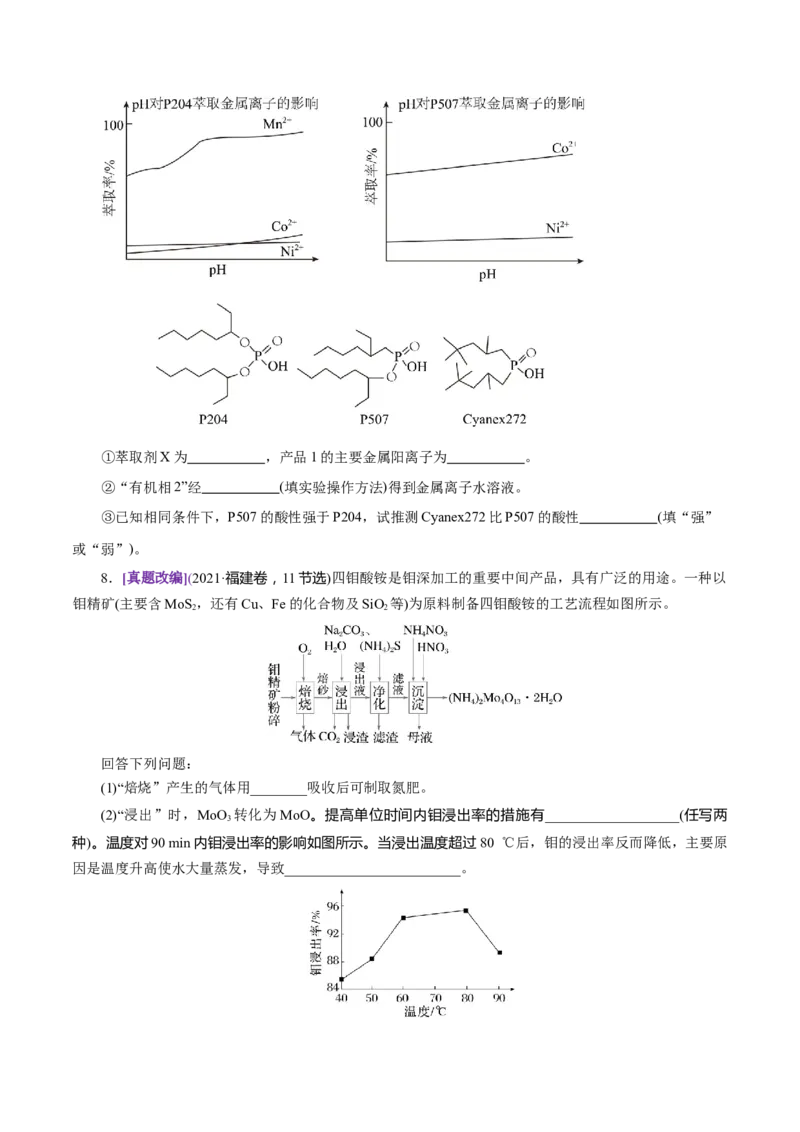
6.(2025·湖南省衡阳市高三联考)为解决钒、铬资源的利用问题,利用钒铬渣(含有VO、Cr O、及
2 3 2 3
SiO、Fe O、FeO等)提取钒铬的工艺流程:
2 2 3已知:25℃时,Cr(OH) 的溶度积常数为6.4×10−31;lg4=0.6
3
回答下列问题:
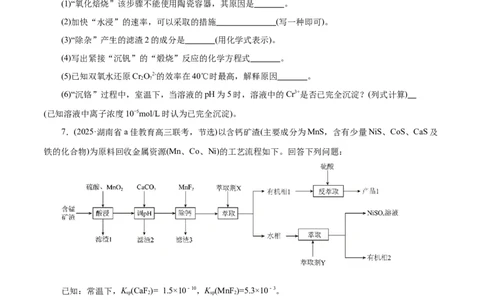
(1)“氧化焙烧”该步骤不能使用陶瓷容器,其原因是 。
(2)加快“水浸”的速率,可以采取的措施 (写一种即可)。
(3)“除杂”产生的滤渣2的成分是 (用化学式表示)。
(4)写出紧接“沉钒”的“煅烧”反应的化学方程式 。
(5)已知双氧水还原Cr O2-的效率在40℃时最高,解释原因 。
2 7
(6)“沉铬”过程中,室温下,当溶液的pH为5时,溶液中的Cr3+是否已完全沉淀?(列式计算)
(已知溶液中离子浓度10−5mol/L时认为已完全沉淀)。
7.(2025·湖南省a佳教育高三联考,节选)以含钙矿渣(主要成分为MnS,含有少量NiS、CoS、CaS及
铁的化合物)为原料回收金属资源(Mn、Co、Ni)的工艺流程如下。回答下列问题:
已知:常温下,K (CaF )= 1.5×10-10,K (MnF )=5.3×10-3。
sp 2 sp 2
(1)“滤渣1”的主要成分为S、 。写出MnO 将MnS氧化为S的化学方程式 。
2
(2)“调pH”可除去的杂质离子为 。
(3) MgF 的熔点高CaF 的原因是 。
2 2
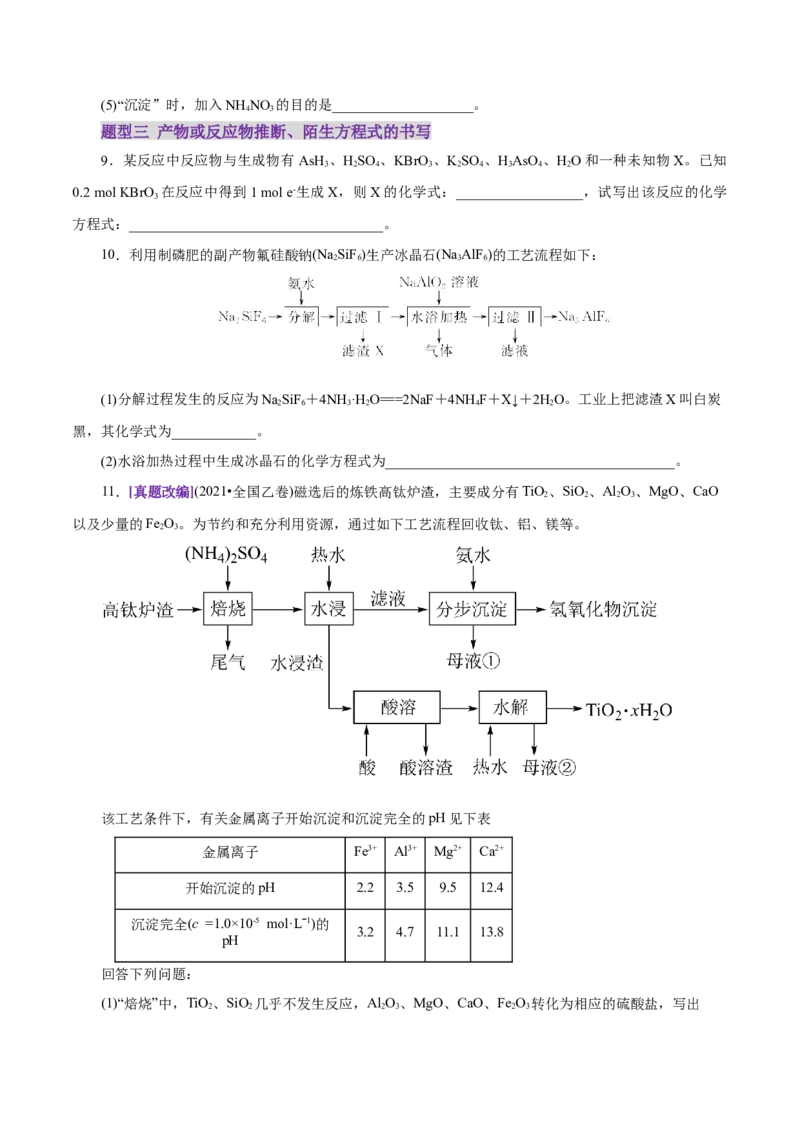
(4)采用双萃取剂法分离得到金属资源,酸性萃取剂P204和P507萃取金属离子的萃取率与pH的关系
如图。三种常见金属离子萃取剂P507、P204、Cyanex272的结构如图所示。①萃取剂X为 ,产品1的主要金属阳离子为 。
②“有机相2”经 (填实验操作方法)得到金属离子水溶液。
③已知相同条件下,P507的酸性强于P204,试推测Cyanex272比P507的酸性 (填“强”
或“弱”)。
8.[真题改编](2021·福建卷,11节选)四钼酸铵是钼深加工的重要中间产品,具有广泛的用途。一种以
钼精矿(主要含MoS ,还有Cu、Fe的化合物及SiO 等)为原料制备四钼酸铵的工艺流程如图所示。
2 2
回答下列问题:
(1)“焙烧”产生的气体用________吸收后可制取氮肥。
(2)“浸出”时,MoO 转化为MoO。提高单位时间内钼浸出率的措施有___________________(任写两
3
种)。温度对90 min内钼浸出率的影响如图所示。当浸出温度超过80 ℃后,钼的浸出率反而降低,主要原
因是温度升高使水大量蒸发,导致_________________________。(5)“沉淀”时,加入NH NO 的目的是____________________。
4 3
题型三 产物或反应物推断、陌生方程式的书写
9.某反应中反应物与生成物有AsH 、HSO 、KBrO 、KSO 、HAsO 、HO和一种未知物X。已知
3 2 4 3 2 4 3 4 2
0.2 mol KBrO 在反应中得到1 mol e-生成X,则X的化学式:__________________,试写出该反应的化学
3
方程式:____________________________________。
10.利用制磷肥的副产物氟硅酸钠(Na SiF)生产冰晶石(Na AlF)的工艺流程如下:
2 6 3 6
(1)分解过程发生的反应为NaSiF+4NH ·H O===2NaF+4NH F+X↓+2HO。工业上把滤渣X叫白炭
2 6 3 2 4 2
黑,其化学式为____________。
(2)水浴加热过程中生成冰晶石的化学方程式为_________________________________________。
11.[真题改编](2021•全国乙卷)磁选后的炼铁高钛炉渣,主要成分有TiO、SiO、Al O、MgO、CaO
2 2 2 3
以及少量的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c =1.0×10-5 mol·Lˉ1)的
3.2 4.7 11.1 13.8
pH
回答下列问题:
(1)“焙烧”中,TiO、SiO 几乎不发生反应,Al O、MgO、CaO、Fe O 转化为相应的硫酸盐,写出
2 2 2 3 2 3Al O 转化为NH Al(SO) 的化学方程式_______。
2 3 4 4 2
(2)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。
(3)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO·x H O沉淀,该反应的离子方程式是
2 2
_______。
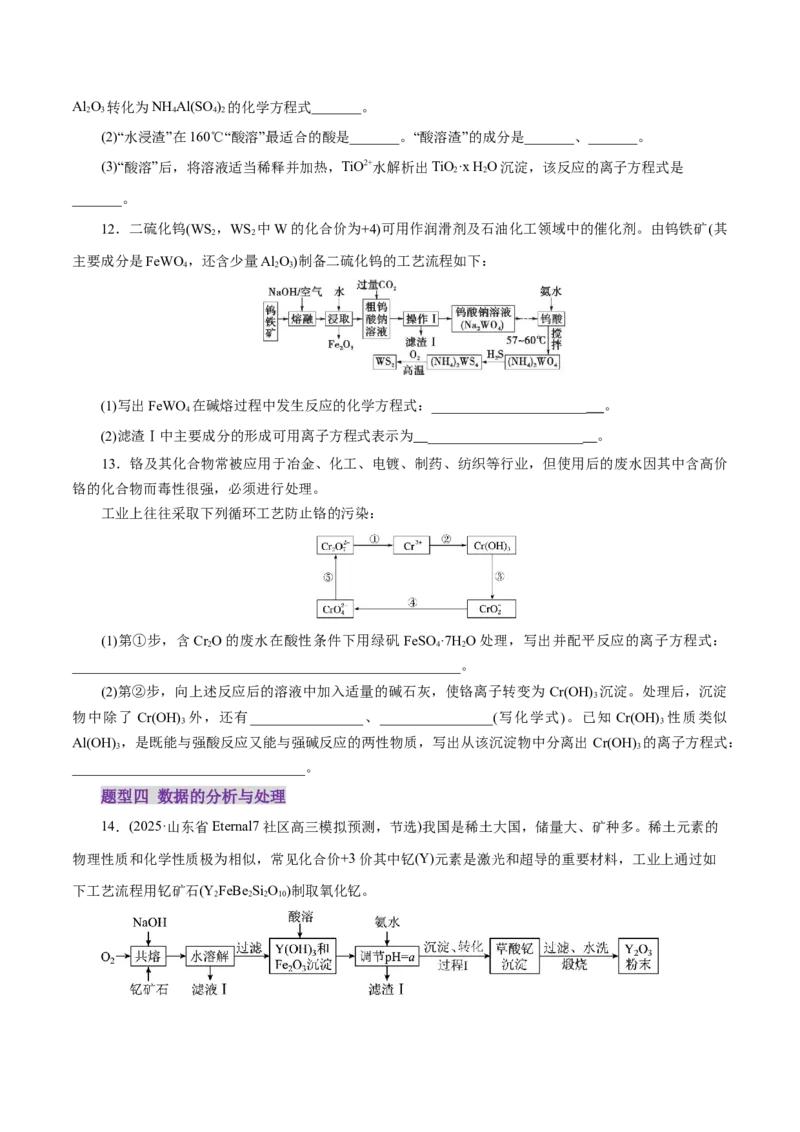
12.二硫化钨(WS ,WS 中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由钨铁矿(其
2 2
主要成分是FeWO,还含少量Al O)制备二硫化钨的工艺流程如下:
4 2 3
(1)写出FeWO 在碱熔过程中发生反应的化学方程式:______________________ 。
4
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为 ______________________ 。
13.铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价
铬的化合物而毒性很强,必须进行处理。
工业上往往采取下列循环工艺防止铬的污染:
(1)第①步,含Cr O的废水在酸性条件下用绿矾FeSO ·7H O处理,写出并配平反应的离子方程式:
2 4 2
_______________________________________________________。
(2)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为 Cr(OH) 沉淀。处理后,沉淀
3
物中除了 Cr(OH) 外,还有________________、________________(写化学式)。已知 Cr(OH) 性质类似
3 3
Al(OH) ,是既能与强酸反应又能与强碱反应的两性物质,写出从该沉淀物中分离出 Cr(OH) 的离子方程式:
3 3
_________________________________。
题型四 数据的分析与处理
14.(2025·山东省Eternal7社区高三模拟预测,节选)我国是稀土大国,储量大、矿种多。稀土元素的
物理性质和化学性质极为相似,常见化合价+3价其中钇(Y)元素是激光和超导的重要材料,工业上通过如
下工艺流程用钇矿石(Y FeBe Si O )制取氧化钇。
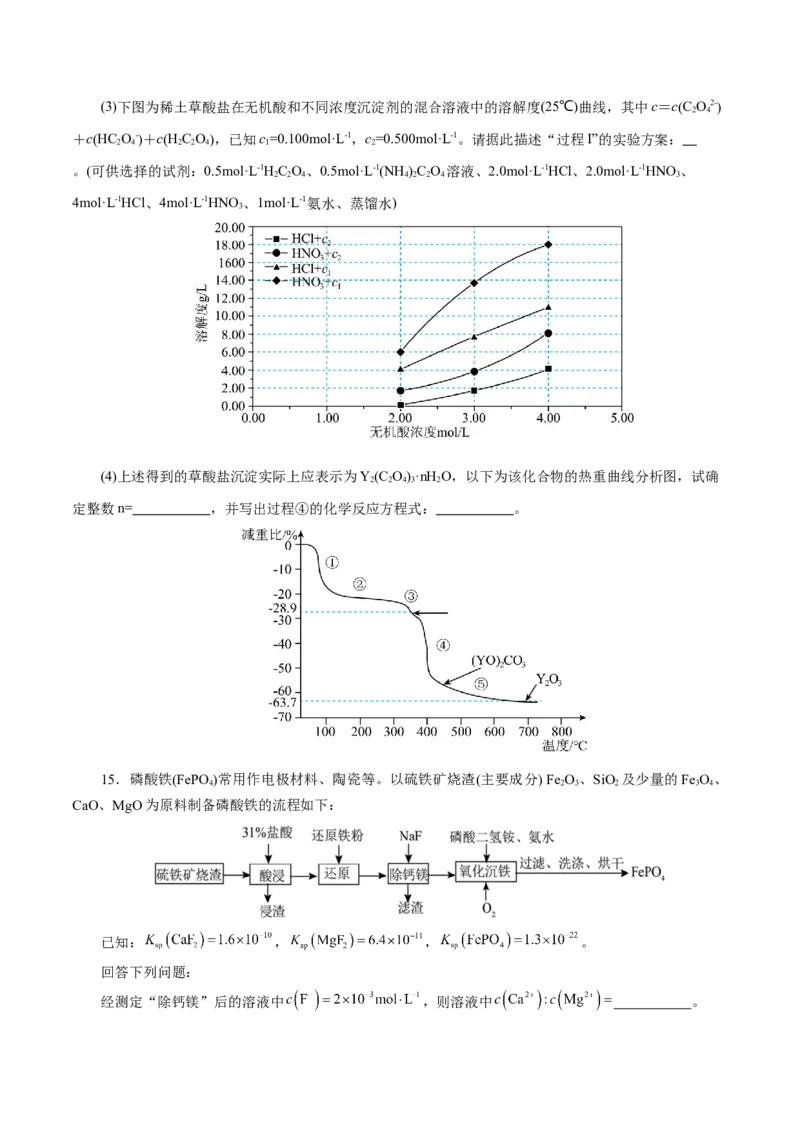
2 2 2 10(3)下图为稀土草酸盐在无机酸和不同浓度沉淀剂的混合溶液中的溶解度(25℃)曲线,其中c=cC O2-
2 4
+cHC O-+cHC O,已知c=0.100mol·L-1,c=0.500mol·L-1。请据此描述“过程I”的实验方案:
2 4 2 2 4 1 2
。(可供选择的试剂:0.5mol·L-1HC O、0.5mol·L-1(NH )C O 溶液、2.0mol·L-1HCl、2.0mol·L-1HNO、
2 2 4 4 2 2 4 3
4mol·L-1HCl、4mol·L-1HNO、1mol·L-1氨水、蒸馏水)
3
(4)上述得到的草酸盐沉淀实际上应表示为Y(C O)·nH O,以下为该化合物的热重曲线分析图,试确
2 2 4 3 2
定整数n= ,并写出过程④的化学反应方程式: 。
15.磷酸铁(FePO )常用作电极材料、陶瓷等。以硫铁矿烧渣(主要成分) Fe O 、SiO 及少量的Fe O 、
4 2 3 2 3 4
CaO、MgO为原料制备磷酸铁的流程如下:
已知: , , 。
回答下列问题:
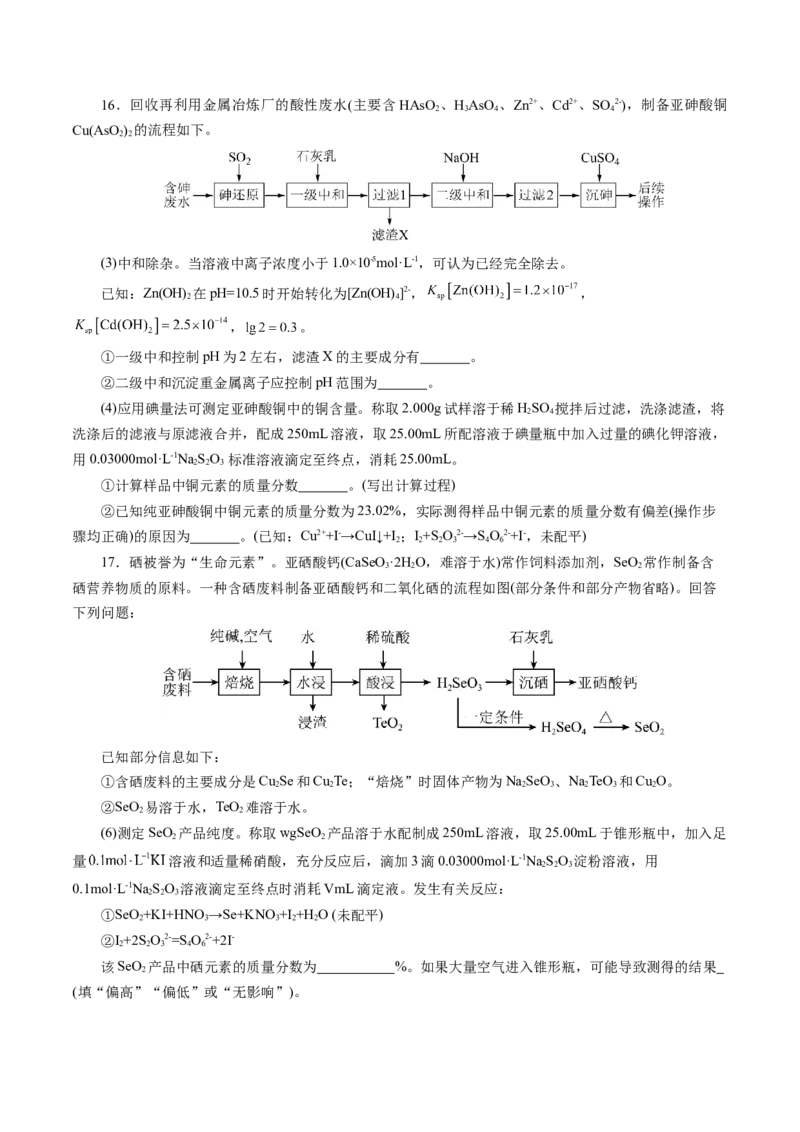
经测定“除钙镁”后的溶液中 ,则溶液中 。16.回收再利用金属冶炼厂的酸性废水(主要含HAsO 、HAsO 、Zn2+、Cd2+、SO 2-),制备亚砷酸铜
2 3 4 4
Cu(AsO ) 的流程如下。
2 2
(3)中和除杂。当溶液中离子浓度小于1.0×10-5mol·L-1,可认为已经完全除去。
已知:Zn(OH) 在pH=10.5时开始转化为[Zn(OH) ]2-, ,
2 4
, 。
①一级中和控制pH为2左右,滤渣X的主要成分有 。
②二级中和沉淀重金属离子应控制pH范围为 。
(4)应用碘量法可测定亚砷酸铜中的铜含量。称取2.000g试样溶于稀HSO 搅拌后过滤,洗涤滤渣,将
2 4
洗涤后的滤液与原滤液合并,配成250mL溶液,取25.00mL所配溶液于碘量瓶中加入过量的碘化钾溶液,
用0.03000mol·L-1NaSO 标准溶液滴定至终点,消耗25.00mL。
2 2 3
①计算样品中铜元素的质量分数 。(写出计算过程)
②已知纯亚砷酸铜中铜元素的质量分数为23.02%,实际测得样品中铜元素的质量分数有偏差(操作步
骤均正确)的原因为 。(已知:Cu2++I-→CuI↓+I ;I+S O2-→SO2-+I-,未配平)
2 2 2 3 4 6
17.硒被誉为“生命元素”。亚硒酸钙(CaSeO·2H O,难溶于水)常作饲料添加剂,SeO 常作制备含
3 2 2
硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答
下列问题:
已知部分信息如下:
①含硒废料的主要成分是Cu Se和Cu Te;“焙烧”时固体产物为NaSeO、NaTeO 和Cu O。
2 2 2 3 2 3 2
②SeO 易溶于水,TeO 难溶于水。
2 2
(6)测定SeO 产品纯度。称取wgSeO 产品溶于水配制成250mL溶液,取25.00mL于锥形瓶中,加入足
2 2
量 溶液和适量稀硝酸,充分反应后,滴加3滴0.03000mol·L-1NaSO 淀粉溶液,用
2 2 3
0.1mol·L-1NaSO 溶液滴定至终点时消耗VmL滴定液。发生有关反应:
2 2 3
①SeO+KI+HNO →Se+KNO +I +H O (未配平)
2 3 3 2 2
②I+2S O2-=S O2-+2I-
2 2 3 4 6
该SeO 产品中硒元素的质量分数为 %。如果大量空气进入锥形瓶,可能导致测得的结果
2
(填“偏高”“偏低”或“无影响”)。1.(2025·福建省部分学校高三半期联考)氮化钛(Ti N)常作仿金饰品,乳酸亚铁[Fe(C HO)]常作补铁
3 4 3 5 3 2
制剂。以钛铁矿(主要含FeTiO,还含少量Al O、SiO)为原料制备氮化钛和乳酸亚铁的工艺如图。回答下
3 2 3 2
列问题:
部分物质的熔点、沸点数据如表所示:
MgCl
物质 TiCl Mg Ti
4
2
熔点/℃ -25 648.8 714 1667
沸点/℃ 136.4 1090 1412 3287
(1) FeTiO 中Ti的化合价为 价。
3
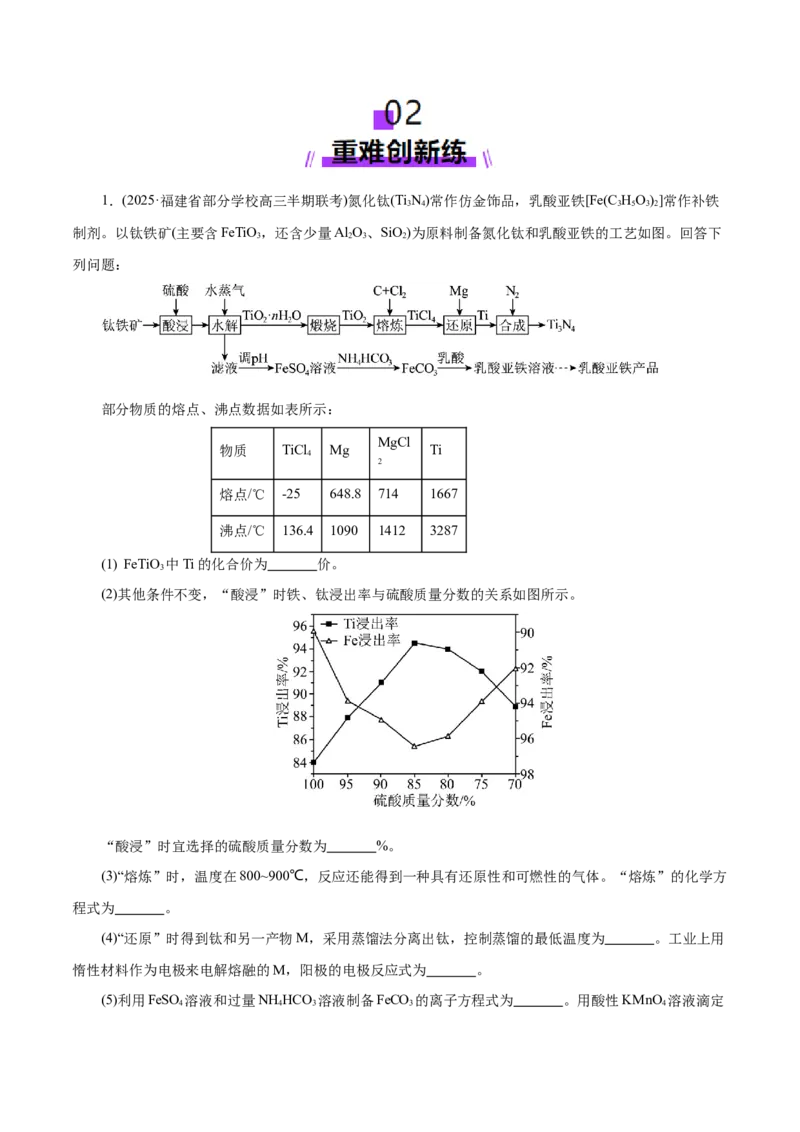
(2)其他条件不变,“酸浸”时铁、钛浸出率与硫酸质量分数的关系如图所示。
“酸浸”时宜选择的硫酸质量分数为 %。
(3)“熔炼”时,温度在800~900℃,反应还能得到一种具有还原性和可燃性的气体。“熔炼”的化学方
程式为 。
(4)“还原”时得到钛和另一产物M,采用蒸馏法分离出钛,控制蒸馏的最低温度为 。工业上用
惰性材料作为电极来电解熔融的M,阳极的电极反应式为 。
(5)利用FeSO 溶液和过量NH HCO 溶液制备FeCO 的离子方程式为 。用酸性KMnO 溶液滴定
4 4 3 3 4法测定乳酸亚铁产品的纯度,所有操作均正确,但经多次实验结果发现,测得值高于实际值,其原因是
。已知滴定反应为Fe2++MnO -+H+→Fe3++Mn2++H O(未配平)。
4 2
(6)某工厂用10t该钛铁矿通过该工艺流程最终制得乳酸亚铁11840.4kg,已知在该流程中铁的损耗率为
8%。
①乳酸亚铁中含有的化学键为 。
②该钛铁矿中钛的含量为 %。
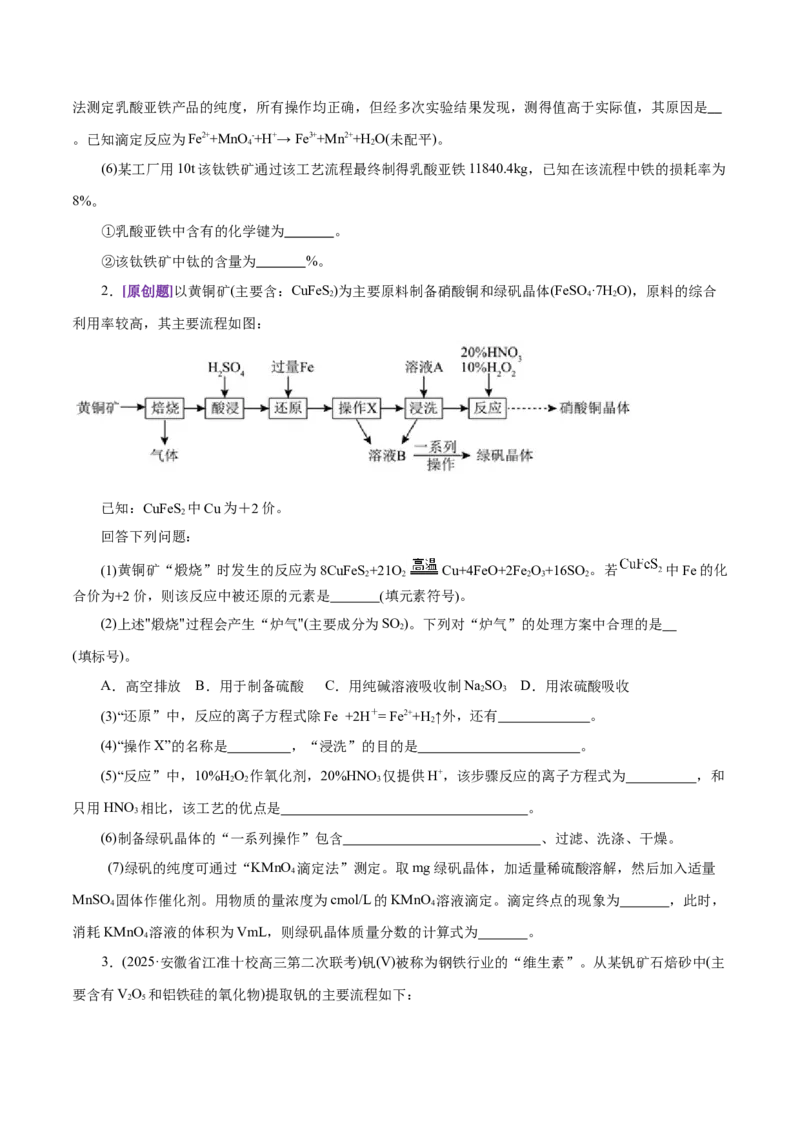
2.[原创题]以黄铜矿(主要含:CuFeS)为主要原料制备硝酸铜和绿矾晶体(FeSO ·7H O),原料的综合
2 4 2
利用率较高,其主要流程如图:
已知:CuFeS 中Cu为+2价。
2
回答下列问题:
(1)黄铜矿“煅烧”时发生的反应为8CuFeS+21O Cu+4FeO+2Fe O+16SO 。若 中Fe的化
2 2 2 3 2
合价为+2价,则该反应中被还原的元素是 (填元素符号)。
(2)上述"煅烧"过程会产生“炉气"(主要成分为SO )。下列对“炉气”的处理方案中合理的是
2
(填标号)。
A.高空排放 B.用于制备硫酸 C.用纯碱溶液吸收制NaSO D.用浓硫酸吸收
2 3
(3)“还原”中,反应的离子方程式除Fe +2H+= Fe2++H ↑外,还有 。
2
(4)“操作X”的名称是 ,“浸洗”的目的是 。
(5)“反应”中,10%H O 作氧化剂,20%HNO 仅提供H+,该步骤反应的离子方程式为 ,和
2 2 3
只用HNO 相比,该工艺的优点是 。
3
(6)制备绿矾晶体的“一系列操作”包含 、过滤、洗涤、干燥。
(7)绿矾的纯度可通过“KMnO 滴定法”测定。取mg绿矾晶体,加适量稀硫酸溶解,然后加入适量
4
MnSO 固体作催化剂。用物质的量浓度为cmol/L的KMnO 溶液滴定。滴定终点的现象为 ,此时,
4 4
消耗KMnO 溶液的体积为VmL,则绿矾晶体质量分数的计算式为 。
4
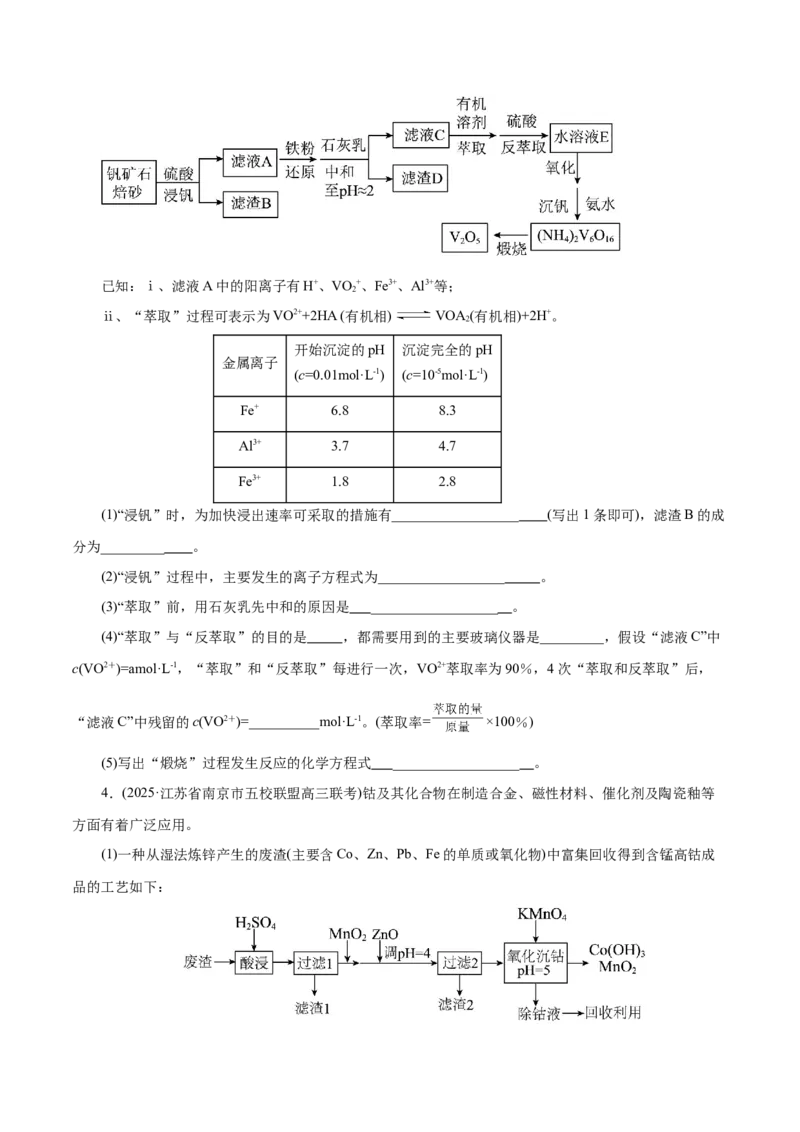
3.(2025·安徽省江准十校高三第二次联考)钒(V)被称为钢铁行业的“维生素”。从某钒矿石焙砂中(主
要含有VO 和铝铁硅的氧化物)提取钒的主要流程如下:
2 5已知:ⅰ、滤液A中的阳离子有H+、VO +、Fe3+、Al3+等;
2
ⅱ、“萃取”过程可表示为VO2++2HA (有机相) VOA(有机相)+2H+。
2
开始沉淀的pH 沉淀完全的pH
金属离子
(c=0.01mol·L-1) (c=10-5mol·L-1)
Fe+ 6.8 8.3
Al3+ 3.7 4.7
Fe3+ 1.8 2.8
(1)“浸钒”时,为加快浸出速率可采取的措施有__________________ (写出1条即可),滤渣B的成
分为_________ 。
(2)“浸钒”过程中,主要发生的离子方程式为__________________ 。
(3)“萃取”前,用石灰乳先中和的原因是 __________________ 。
(4)“萃取”与“反萃取”的目的是 ,都需要用到的主要玻璃仪器是_________,假设“滤液C”中
c(VO2+)=amol·L-1,“萃取”和“反萃取”每进行一次,VO2+萃取率为90%,4次“萃取和反萃取”后,
“滤液C”中残留的c(VO2+)=__________mol·L-1。(萃取率= ×100%)
(5)写出“煅烧”过程发生反应的化学方程式 __________________ 。
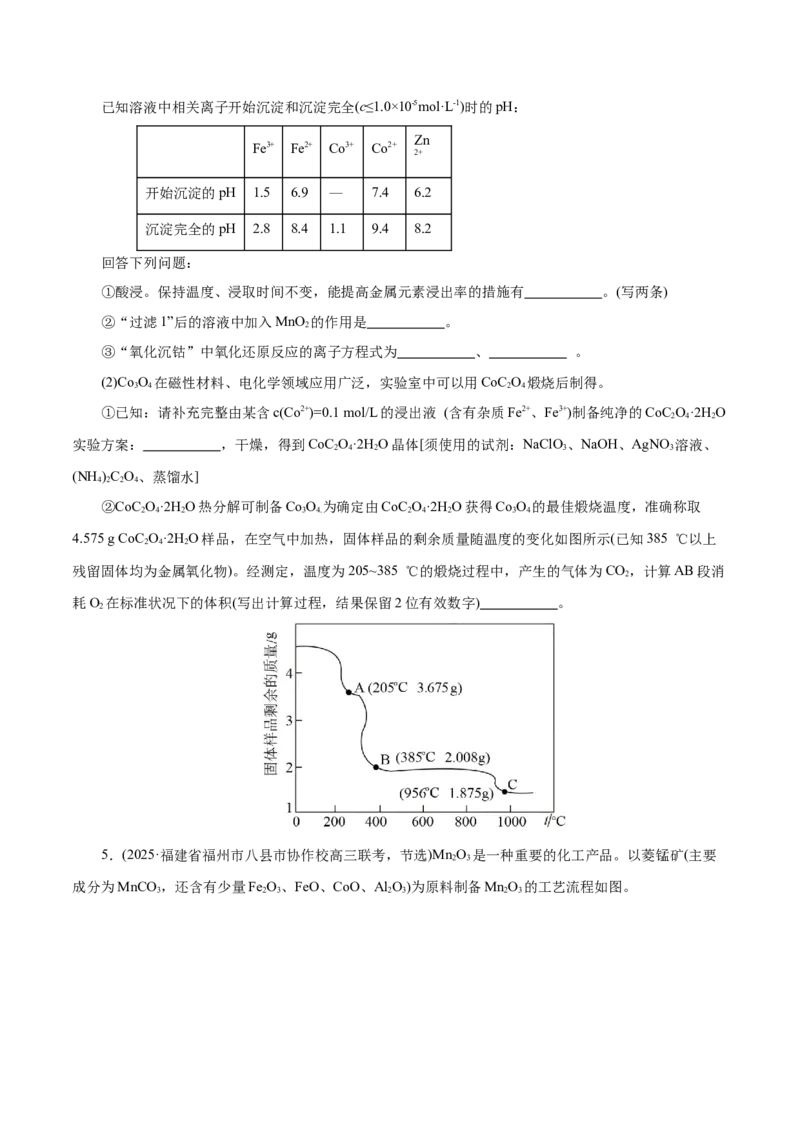
4.(2025·江苏省南京市五校联盟高三联考)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等
方面有着广泛应用。
(1)一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成
品的工艺如下:已知溶液中相关离子开始沉淀和沉淀完全(c≤1.0×10-5mol·L-1)时的pH:
Zn
Fe3+ Fe2+ Co3+ Co2+
2+
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
①酸浸。保持温度、浸取时间不变,能提高金属元素浸出率的措施有 。(写两条)
②“过滤1”后的溶液中加入MnO 的作用是 。
2
③“氧化沉钴”中氧化还原反应的离子方程式为 、 。
(2)Co O 在磁性材料、电化学领域应用广泛,实验室中可以用CoC O 煅烧后制得。
3 4 2 4
①已知:请补充完整由某含c(Co2+)=0.1 mol/L的浸出液 (含有杂质Fe2+、Fe3+)制备纯净的CoC O·2H O
2 4 2
实验方案: ,干燥,得到CoC O·2H O晶体[须使用的试剂:NaClO、NaOH、AgNO 溶液、
2 4 2 3 3
(NH )C O、蒸馏水]
4 2 2 4
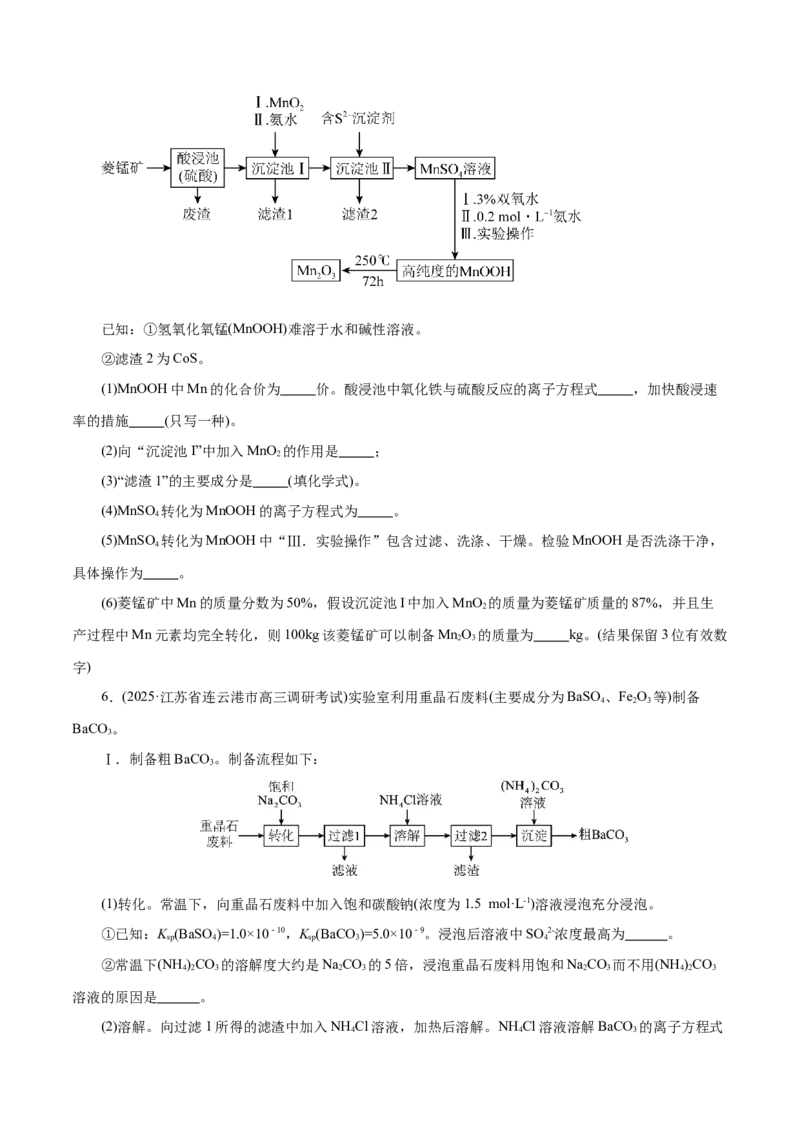
②CoC O·2H O热分解可制备Co O 为确定由CoC O·2H O获得Co O 的最佳煅烧温度,准确称取
2 4 2 3 4. 2 4 2 3 4
4.575 g CoC O·2H O样品,在空气中加热,固体样品的剩余质量随温度的变化如图所示(已知385 ℃以上
2 4 2
残留固体均为金属氧化物)。经测定,温度为205~385 ℃的煅烧过程中,产生的气体为CO,计算AB段消
2
耗O 在标准状况下的体积(写出计算过程,结果保留2位有效数字) 。
2
5.(2025·福建省福州市八县市协作校高三联考,节选)Mn O 是一种重要的化工产品。以菱锰矿(主要
2 3
成分为MnCO ,还含有少量Fe O、FeO、CoO、Al O)为原料制备MnO 的工艺流程如图。
3 2 3 2 3 2 3已知:①氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
②滤渣2为CoS。
(1)MnOOH中Mn的化合价为 价。酸浸池中氧化铁与硫酸反应的离子方程式 ,加快酸浸速
率的措施 (只写一种)。
(2)向“沉淀池I”中加入MnO 的作用是 ;
2
(3)“滤渣1”的主要成分是 (填化学式)。
(4)MnSO 转化为MnOOH的离子方程式为 。
4
(5)MnSO 转化为MnOOH中“Ⅲ.实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,
4
具体操作为 。
(6)菱锰矿中Mn的质量分数为50%,假设沉淀池I中加入MnO 的质量为菱锰矿质量的87%,并且生
2
产过程中Mn元素均完全转化,则100kg该菱锰矿可以制备MnO 的质量为 kg。(结果保留3位有效数
2 3
字)
6.(2025·江苏省连云港市高三调研考试)实验室利用重晶石废料(主要成分为BaSO、Fe O 等)制备
4 2 3
BaCO 。
3
Ⅰ.制备粗BaCO 。制备流程如下:
3
(1)转化。常温下,向重晶石废料中加入饱和碳酸钠(浓度为1.5 mol·L-1)溶液浸泡充分浸泡。
①已知:K (BaSO)=1.0×10-10,K (BaCO)=5.0×10-9。浸泡后溶液中SO 2-浓度最高为 。
sp 4 sp 3 4
②常温下(NH )CO 的溶解度大约是NaCO 的5倍,浸泡重晶石废料用饱和NaCO 而不用(NH )CO
4 2 3 2 3 2 3 4 2 3
溶液的原因是 。
(2)溶解。向过滤1所得的滤渣中加入NH Cl溶液,加热后溶解。NH Cl溶液溶解BaCO 的离子方程式
4 4 3为 。
Ⅱ.测定粗BaCO 样品中铁元素的含量。
3
取5.0000g的粗BaCO 样品,用20% HSO 充分溶解,再加入足量溶液充分反应,然后加蒸馏水配制
3 2 4
成100mL溶液。准确量取20.00mL配制的溶液于锥形瓶中,调节溶液pH=6,用
0.0150mol·L-1EDTA(NaHY)溶液滴定至终点(滴定反应为Fe2++H Y2-=FeY2-+2H+),平行滴定3次,平均消耗
2 2 2
EDTA溶液20.00mL。
(3)测定过程中,加入足量NaSO 溶液的目的是 。
2 2 3
(4)计算粗BaCO 样品中铁元素的质量分数 (写出计算过程)。
3
(5)若稀释后滤液用酸性KCr O 滴定,测得的数值明显高于上述方法测定的数值,原因是 。
2 2 7
Ⅲ.制备。
(6)粗BaCO 中含有杂质Fe(OH) 。补充完整由粗BaCO 制取高纯度BaCO 的实验方案:取一定量粗
3 3 3 3
BaCO 固体, ,用蒸馏水充分洗涤沉淀,干燥,得到高纯度BaCO 。[已知:pH=3.2时Fe(OH) 沉淀
3 3 3
完全。实验中必须使用的试剂:稀HCl、NaCO 溶液]
2 3
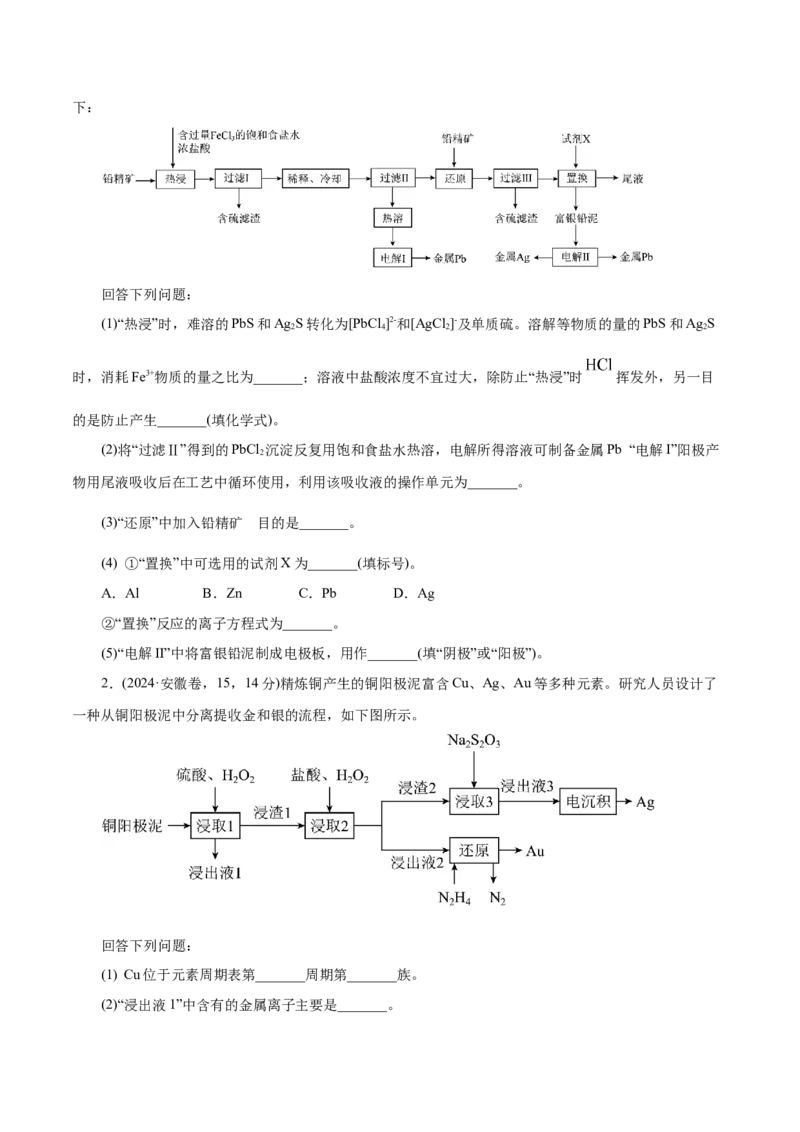
7.(2025·浙江省嘉兴市高三基础测试)精炼铜产生的铜阳极泥含Cu、Ag、Au多种单质。某研究小组设
计从Cu、Ag、Au的混合物中分离提收金和银的流程,如下图所示:
已知:电沉积时生成Ag的电极反应为:[Ag(S O)]3-+ e-=Ag↓+2SO2-。
2 3 2 2 3
回答下列问题:
(1)“浸出液1”中含有的阳离子主要是 。
(2)“浸取2”步骤中,单质Au转化为HAuCl ,其反应的化学方程式为 。
4
(3)下列说法正确的是_______。
A.两次“浸取”所加的酸均可为硫酸或盐酸
B.“浸取3”步骤中,“浸渣2”中的AgCl转化为[Ag(S O)]3-
2 3 2
C.在“浸取2”步骤中,加入适量 可提高混合物中Au的收率
D.上述流程中的HO、NH、NaSO 均为还原剂
2 2 2 4 2 2 3
(4)Na SO 可被I 氧化为NaSO,从物质结构的角度分析NaSO 中阴离子的结构应为下图中的
2 2 3 2 2 4 6 2 4 6(填“甲”或“乙”)。
(5)设计实验验证Cu、Ag、Au混合物中含有Ag 。
8.(2025·浙江部分高中高三开学考试)矿物资源的综合利用有多种方法,硅镀钇矿(Y FeBeSi O )是一
2 2 2 10
种含钇族稀土元素和氧化铍为主的主要矿物,该矿石中含稀土元素约35%,含氧化铍约5%,如图是利用
硅铍钇矿生产氧化铍与稀土产品的转化过程:
已知:过程I中未有电子转移,且物质X由多种氧化物混合而成。请回答:
(1)写出物质X中的所有氧化物 (填化学式);步骤III中,加入NH Cl的作用是 。步骤II
4
中存在氧化还原过程,设计实验验证含铍溶液中的阳离子(除 以外) 。
(2)已知:铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似。下列说法不正确的
是_______。
A.Be(OH) 是两性氢氧化物,能与强酸、强碱反应
2
B.Al Cl 沸点低于相似结构的BeCl
2 6 2 4
C.为得到无水BeCl,可通过Cl与BeCl·6H O混合并加热制得
2 2 2
D. 的第一电离能大于B的第一电离能的主要原因是电子排布为半充满,较为稳定
(3)某化学科研工作者对复盐沉淀进行精密分析,最终确认其化学式为Y(SO )·Na SO ·2H O。
2 4 3 2 4 2
①向复盐沉淀中加入NaOH溶液生成Y(OH) ,写出该反应的化学方程式 。
3
②检验氢氧化钇是否洗涤干净的操作方法为 。
1.(2024·山东卷,18,12分)以铅精矿(含PbS,AgS等)为主要原料提取金属Pb和Ag的工艺流程如
2下:
回答下列问题:
(1)“热浸”时,难溶的PbS和AgS转化为[PbCl]2-和[AgCl]-及单质硫。溶解等物质的量的PbS和AgS
2 4 2 2
时,消耗Fe3+物质的量之比为_______;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,另一目
的是防止产生_______(填化学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属Pb “电解I”阳极产
2
物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为_______。
的
(3)“还原”中加入铅精矿 目的是_______。
(4) ①“置换”中可选用的试剂X为_______(填标号)。
A.Al B.Zn C.Pb D.Ag
②“置换”反应的离子方程式为_______。
(5)“电解II”中将富银铅泥制成电极板,用作_______(填“阴极”或“阳极”)。
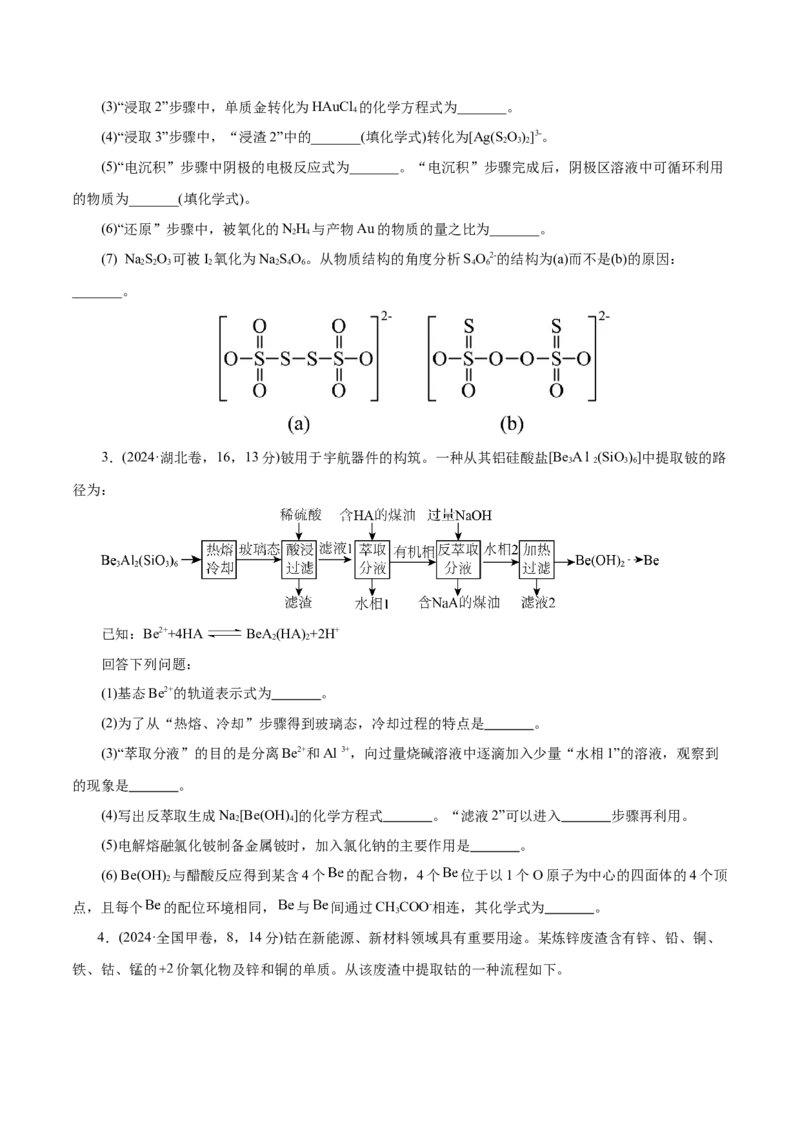
2.(2024·安徽卷,15,14分)精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了
一种从铜阳极泥中分离提收金和银的流程,如下图所示。
回答下列问题:
(1) Cu位于元素周期表第_______周期第_______族。
(2)“浸出液1”中含有的金属离子主要是_______。(3)“浸取2”步骤中,单质金转化为HAuCl 的化学方程式为_______。
4
(4)“浸取3”步骤中,“浸渣2”中的_______(填化学式)转化为[Ag(S O)]3-。
2 3 2
(5)“电沉积”步骤中阴极的电极反应式为_______。“电沉积”步骤完成后,阴极区溶液中可循环利用
的物质为_______(填化学式)。
(6)“还原”步骤中,被氧化的NH 与产物Au的物质的量之比为_______。
2 4
(7) Na SO 可被I 氧化为NaSO。从物质结构的角度分析SO2-的结构为(a)而不是(b)的原因:
2 2 3 2 2 4 6 4 6
_______。
3.(2024·湖北卷,16,13分)铍用于宇航器件的构筑。一种从其铝硅酸盐[Be A l (SiO)]中提取铍的路
3 2 3 6
径为:
已知:Be2++4HA BeA(HA) +2H+
2 2
回答下列问题:
(1)基态Be2+的轨道表示式为 。
(2)为了从“热熔、冷却”步骤得到玻璃态,冷却过程的特点是 。
(3)“萃取分液”的目的是分离Be2+和Al 3+,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到
的现象是 。
(4)写出反萃取生成Na[Be(OH) ]的化学方程式 。“滤液2”可以进入 步骤再利用。
2 4
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是 。
(6) Be(OH) 与醋酸反应得到某含4个 的配合物,4个 位于以1个O原子为中心的四面体的4个顶
2
点,且每个 的配位环境相同, 与 间通过CHCOO-相连,其化学式为 。
3
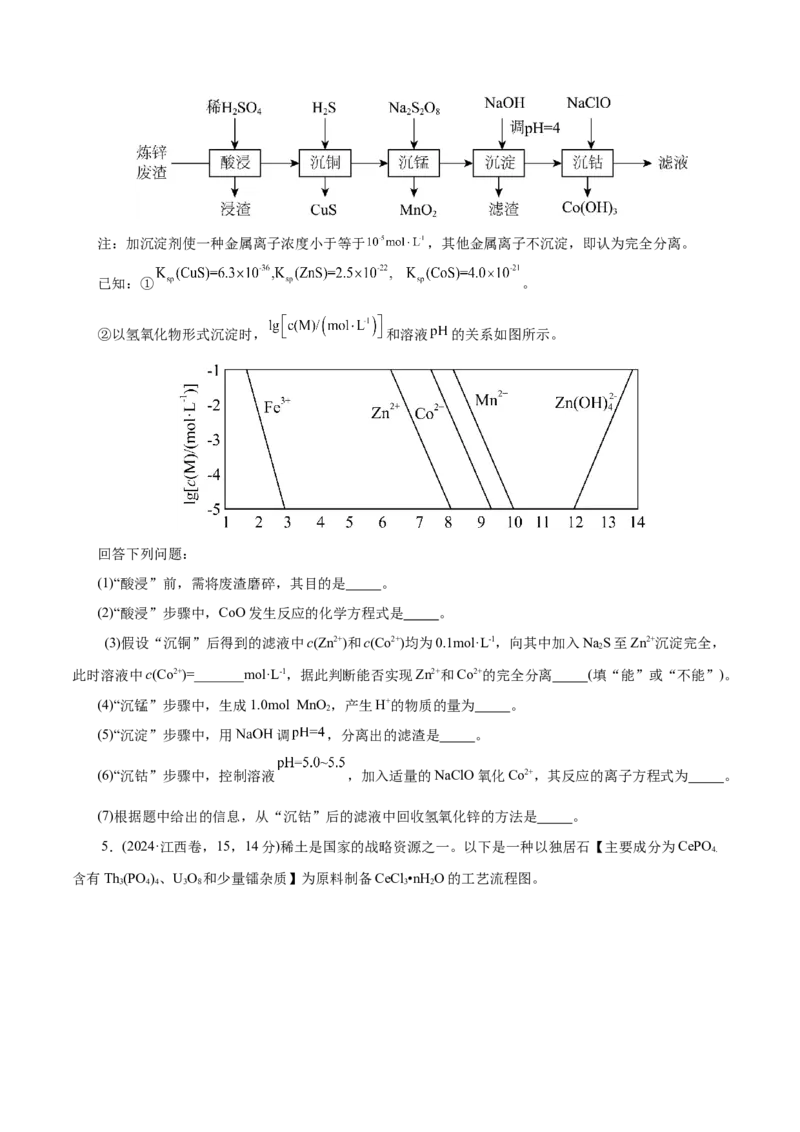
4.(2024·全国甲卷,8,14分)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、
铁、钴、锰的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。注:加沉淀剂使一种金属离子浓度小于等于 ,其他金属离子不沉淀,即认为完全分离。
已知:① 。
②以氢氧化物形式沉淀时, 和溶液 的关系如图所示。
回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是 。
(2)“酸浸”步骤中,CoO发生反应的化学方程式是 。
(3)假设“沉铜”后得到的滤液中c(Zn2+)和c(Co2+)均为0.1mol·L-1,向其中加入NaS至Zn2+沉淀完全,
2
此时溶液中c(Co2+)=_______mol·L-1,据此判断能否实现Zn2+和Co2+的完全分离 (填“能”或“不能”)。
(4)“沉锰”步骤中,生成1.0mol MnO ,产生H+的物质的量为 。
2
(5)“沉淀”步骤中,用 调 ,分离出的滤渣是 。
(6)“沉钴”步骤中,控制溶液 ,加入适量的NaClO氧化Co2+,其反应的离子方程式为 。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是 。
5.(2024·江西卷,15,14分)稀土是国家的战略资源之一。以下是一种以独居石【主要成分为CePO
4.
含有Th(PO )、UO 和少量镭杂质】为原料制备CeCl •nH O的工艺流程图。
3 4 4 3 8 3 2已知:ⅰ.K [Th(OH) ]=4.0×10﹣45,K [Ce(OH) ]=1.6×10﹣20,K [Ce(OH) ]=2.0×10﹣48
sp 4 sp 3 sp 4
ⅱ.镭为第ⅡA族元素
回答下列问题:
(1)关于独居石的热分解,以下说法正确的是 _______(填标号)。
a.降低压强,分解速率增大 b.降低温度,分解速率降低
c.反应时间越长,分解速率越大 d.提高搅拌速度,分解速率降低
(2)NaUO 中铀元素的化合价为 _______,热分解阶段UO 生成NaUO 的化学反应方程式为
2 2 7 3 8 2 2 7
_______。
(3)浓缩结晶后,得到的晶体产物化学式为 _______,滤液可用于 _______阶段循环利用,避免产生大
量的高碱度废水。
(4)溶解阶段,将溶液pH先调到1.5~2.0,反应后再回调至4.5。
①盐酸溶解Ce(OH) 的离子方程式为 _______。
4
②当溶液pH=4.5时,c(Th4+)=_______mol/L,此时完全转化为氢氧化钍沉淀。
(5)以BaSO 为载体形成共沉淀,目的是去除杂质 _______。
4