文档内容
专题 11 水溶液中离子反应
1.(2023·安徽省皖优联盟高三第二次阶段测试)下列有关NaHCO 的说法中错误的是( )
3
A.NaHCO 溶液中:c(OH―)>c(H+)
3
B.NaHCO 溶液中:n(Na+)= n(CO 2-)+ n(HCO -)+ n(H CO)
3 3 3 2 3
C.苏打是NaHCO 的俗称,可用于食品加工
3
D.加热滴加有酚酞的NaHCO 溶液时,溶液颜色会加深
3
2.(2023·上海·卢湾高级中学高三期中)Na CO 溶液中存在水解平衡:CO2-+H O OH-+HCO-。下列
2 3 3 2 3
说法错误的是( )
A.通入CO,溶液pH减小 B.加入NaOH固体, 减小
2
C.加水稀释,溶液中所有离子的浓度都减小 D.升高温度,平衡常数增大
3.(2023·广东省百校高三联考)苯甲酸钠(PhCOONa)是一种常用食品防腐剂。已知25℃,PhCOOH的
K=1.0×10-4.2。下列有关PhCOONa溶液说法不正确的是( )
a
A.PhCOONa溶液呈碱性
B.0.1mol/L PhCOONa溶液中: c(PhCOO-)<0.1mol/L
C. 25℃,pH=7的PhCOONa和PhCOOH的混合溶液中:c(PhCOOH)>c(PhCOO-) = c(Na+)
D.PhCOONa溶液加水稀释时,溶液中c(PhCOO-)减小
4.(2023·浙江省宁波市高三选考模拟考试)下列说法正确的是( )
A.25℃时,将pH=5的醋酸溶液与pH=5的盐酸等体积混合,混合后溶液pH>5
B.25℃时,等浓度的盐酸与醋酸分别稀释相同倍数,稀释后溶液pH:盐酸<醋酸
C.25℃时,等体积、等pH的盐酸与醋酸分别用等浓度的NaOH溶液中和,盐酸消耗NaOH溶液多
D.25℃时,pH=3的一元酸HA溶液与pH=11的一元碱MOH溶液等体积混合后溶液呈酸性,则HA是强
酸
5.已知某温度下CHCOOH和NH ·H O 的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CHCOOH溶
3 3 2 3
液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.c(NH)/c(NH ·H O)先增大再减小
3 2
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
6.某研究小组为测定食用白醋中醋酸的含量进行了如下操作,正确的是( )
A.用碱式滴定管量取一定体积的待测白醋放入锥形瓶中
B.称取4.0 g NaOH放到100 mL容量瓶中,加水至刻度线,配成1.00 mol/L NaOH标准溶液
C.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时
为滴定终点
D.滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量
7.把Ca(OH) 放入蒸馏水中,一段时间后达到平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。下列说法
2 2
正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入NaCO 溶液,其中固体质量增加
2 3
D.向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
8.已知Ag CrO 是砖红色沉淀,下列滴定反应中,指示剂使用不正确的是( )
2 4
A.用标准FeCl 溶液滴定KI溶液,选择KSCN溶液
3
B.用I 溶液滴定NaSO 溶液,淀粉作指示剂
2 2 3
C.用AgNO 溶液滴定NaCl溶液,NaCrO 作指示剂
3 2 4
D.用HO 溶液滴定KI溶液,淀粉作指示剂
2 2
9.室温下,向20.00 mL 0.1000 mol·L−1盐酸中滴加0.1000 mol·L−1 NaOH溶液,溶液的pH随NaOH溶液
体积的变化如图,已知lg3=0.5。下列说法不正确的是( )
A.选择变色范围在pH突变范围内的指示剂,可减小实验误差
B.用移液管量取20.00 mL 0.1000 mol·L−1盐酸时,移液管水洗后需用待取液润洗
C.NaOH标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定NaOH溶液
的浓度,标定时采用甲基橙为指示剂
D.V(NaOH)=10.00 mL 时,pH约为1.510.(2023·浙江省七彩阳光新高考研究联盟高三返校联考)已知HX、HY均为一元酸,室温下用
NaOH溶液分别滴定20.00mL等物质的量浓度的HX、HY溶液时的滴定曲线如下。下列有关说
法正确的是( )
A.a=20
B.HX可能为强酸,HY一定是弱酸
C.若E为滴定终点,则室温下K(HY)<1.0×10-6
a
D.图中B、D两点对应的溶液中存在c(Y-)=c(X+)
11.(2022·江苏省泰州市高三联考)室温下,通过下列实验探究NaHS溶液的性质。
实验 实验操作和现象
1 向0.1mol•L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红
2 向0.1mol•L-1NaHS溶液中加入等体积0.1mol•L-1NaOH溶液充分混合
3 向0.1mol•L-1NaHS溶液中通入过氯气,无淡黄色沉淀产生
4 向0.1mol•L-1NaHS溶液中滴加过CuCl 溶液,产生黑色沉淀
2
下列有关说法正确的是( )
A.0.1mol/LNaHS溶液中:c(HS-)>c(S2-)>c(H S)
2
B.实验2所得溶液中:c(Na+)-c(S2-)-c(HS-)-c(HS)=0.05mol•L-1
2
C.实验3证明HS-不能被氧化
D.实验4反应静置后的上层清液中有c(Cu2+)•c(S2-)c(CHCOOH)
3
14.根据下表提供的数据,判断下列离子方程式或化学方程式正确的是( )
化学式 电离常数
HClO K=3×10-8
HCO K =4×10-7 K =6×10-11
2 3 a1 a2
A.向NaCO 溶液中滴加少量氯水:CO+2Cl+HO===2Cl-+2HClO+CO↑
2 3 2 2 2
B.向NaHCO 溶液中滴加少量氯水:2HCO+Cl===Cl-+ClO-+2CO↑+HO
3 2 2 2
C.向NaClO溶液中通入少量CO:CO+NaClO+HO===NaHCO+HClO
2 2 2 3
D.向NaClO溶液中通入过量CO:CO+2NaClO+HO===Na CO+2HclO
2 2 2 2 3
15.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+ +
2NH ·HO Ag(NH)+ + 2H O。下列分析不正确的是( )
3 2 3 2 2
A.浊液中存在沉淀溶解平衡:AgCl (s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+能力比Cl-强
3
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
16.常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol·L-1氨水,溶液中水电离的氢离子浓度随加入氨
水的体积变化如图。下列分析正确的是( )A.V=40
B.c点所示溶液中:c(H+)-c(OH-)=2c(NH ·H O)
3 2
C.NH ·H O的电离常数K=10-4
3 2
D.d点所示溶液中:c(NH)=2c(SO)
1.(2023·江苏省高三第二次大联考)室温下,通过下列实验探究有关AgNO 的性质[已知:
3
]。
实验1:向 0.1mol·L-1的AgNO 溶液中滴加 0.1mol·L-1的NaCl溶液,产生白色沉淀,过滤,
3
实验2:向实验1所得滤液中滴加 0.1mol·L-1 溶液,产生淡黄色沉淀,过滤。
实验3:向实验2所得滤液中逐滴滴加氨水,产生沉淀先变多后变少,直至消失。
下列说法正确的是( )
A.实验1过滤后滤液中c(Ag+)=10-4.9mol·L-1
B.通过实验1和实验2可得出
C.实验2所得滤液中c(Ag+)+c(H+)=c(Cl-)+c(Br-)+ c(OH-)
D.实验3滴加氨水过程中,c(Ag+)一直减小
2.下表是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是( )
化学式 CHCOOH HCO AgCl Ag CrO
3 2 3 2 4
K =4.1×10-7 K =1.8×
a1 sp
K 或K K=1.8×10-5 K =2.0×10-12
a sp a sp
K =5.6×10-11 10-10
a2
A.常温下,相同浓度①CHCOONH ②NH HCO ③(NH )CO 溶液中,c(NH)由大到小的顺序是:①
3 4 4 3 4 2 3
>②>③
B.AgCl易溶于氨水难溶于水,所以AgCl 在氨水中的K 大于水中的K
sp sp
C.向饱和氯水中滴加NaOH 溶液至溶液刚好为中性时,c(Na+)=2c(ClO-)+c(HClO)
D.向浓度均为1×10-3 mol·L-1的KCl和KCrO 混合液中滴加1×10-3 mol·L-1的AgNO 溶液,CrO先形
2 4 3
成沉淀3.(2022·江苏省高邮市高三学情调研试题)已知:①AgCl为难溶于水和酸的白色固体,Ag S为难溶于水
2
和酸的黑色固体。
②室温下,K (AgCl)=2.0×10-10,K (Ag S)=2.0×10-48。
sp sp 2
向AgCl的悬浊液中加入一定量的NaS溶液并振荡,白色固体向黑色固体转化。下列说法正确的是( )
2
A.NaS溶液中存在:c(OH-)=c(H+)+c(HS-)+2c(S2-)
2
B.向AgCl悬浊液加入足量氨水,溶液变澄清。反应的离子方程式为:AgCl+4NH•H O=[Ag(NH)]++Cl-
3 2 3 4
+4H O
2
C.反应2AgCl+S2- Ag S+2Cl-正向进行,需满足 <2×1028
2
D.将转化后的体系静置,上层清液中离子存在关系:c(Ag+)= 且c(Ag+)>
4.(2022·河南省名校联盟高三联考)天门冬氨酸( ,记为HY)是一种天然氨基酸,水溶液显
2
酸性,溶液中存在HY H++HY-,HY- H++Y2-,与足量NaOH反应生成NaY ,与盐酸反应生成
2 2
YH Cl。下列说法正确的是( )
3
A.常温下,0.05 mol·L-1的HY溶液的pH=1
2
B.pH=2.97的HY溶液稀释100倍,所得溶液pH=4.97
2
C.YH Cl水溶液中:c(H+)+c(YH-)= c(OH-)+ c(Cl-)+c(HY-)
3 3
D.NaY溶液中:c(OH-)=c(H+)+c(HY-)+ 2c(HY)+3c(YH -)
2 2 3
5.(2022·河南省实验中学高三期中)一种测定水样中溴离子浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00mL,加入几滴NH Fe(SO ) 溶液。
4 4 2
②加入V mL c mol∙L−1AgNO 溶液(过量),充分摇匀。
1 1 3
③用c mol∙L−1KSCN标准溶液进行滴定,至终点时消耗标准溶液VmL 。
2 2
已知:K (AgBr)=7.7×10−13,Ag++SCN-= AgSCN(白色)↓,K (AgSCN)=1×10−12,下列说法不正确的是
sp sp
( )
A.滴定终点时,溶液变为红色
B.该水样中溴离子浓度为:c(Br-)= mol∙L−1
C.AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该实验需要严格控制水样的pH,若pH过高则测定结果将偏高6.(2023·浙江省强基联盟高三上学期10月统测)25℃时,按下表配制两份溶液。
一元弱酸溶液 加入的NaOH溶液 混合后所得溶液
溶液ⅠpH=5.0
溶液ⅡpH=4.0
下列说法不正确的是( )
A.溶液Ⅰ中:c(A-)>c(Na+)>c(H+)>c(OH-)
B.混合Ⅰ和Ⅱ:c(Na+)=c(A-)+c(HA)= c(B-)+c(HB)
C.Ⅰ和Ⅱ的pH相差1.0,说明
D.将等体积、等 的NaA、NaB溶液稀释相同倍数,pH变化更大的是NaA溶液
7.(2022·江苏省南通市海门区高三第二次诊断测试)室温下: 、 、
、 实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下:
实验 实验操作和现象
1 测定0.10mol•L-1NaHCO 溶液的pH约为8
3
测定0.10mol•L-1HCN与0.05mol•L-1NaOH溶液等体积混合,测得混合溶液的
2
pH>7
3 向NaClO溶液中通入少量的CO,测得pH降低
2
4 向0.01mol•L-1NaCO 溶液中加入等体积0.02mol•L-1CaCl 溶液,产生白色沉淀
2 3 2
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)+c(H+)= c(OH-)+c(CO 2-)+c(HCO-)
3 3
B.由实验2可得
C.实验3反应的离子方程式:CO+H O+2 = CO2-+2HClO
2 2 3
D.实验4所得上层清液中的
8.(2023·江苏省南通市高三期中)室温下: , , ,。实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下:
实验 实验操作和现象
1 测定0.10mol•L-1 NaHCO 溶液的pH约为8
3
2 测定0.10mol•L-1HCN与0.05mol•L-1NaOH溶液等体积混合,测得混合溶液的pH>7
3 向NaClO溶液中通入少量的CO,测得pH降低
2
4 向0.01mol•L-1 Na CO 溶液中加入等体积0.03mol•L-1 CaCl 溶液,产生白色沉淀
2 3 2
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)>c(H CO)>c(HCO -)>c(CO2-)>c(H+)
2 3 3 3
B.由实验2可得
C.实验3反应的离子方程式:CO+H O+2ClO-=CO 2-+2HClO
2 2 3
D.实验4所得上层清液中的c(CO2-)=1.0×10-6.55mol·L-1
3
9.常温下,有关物质的溶度积如下
物质 CaCO MgCO Ca(OH) Mg(OH) Fe(OH)
3 3 2 2 3
K 4.96×10-9 6.82×10-6 4.68×10-6 5.61×10-12 2.64×10-39
sp
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl 杂质,选用NaOH溶液比NaCO 溶液效果好
2 2 3
B.常温下,除去NaCl溶液中的CaCl 杂质,选用NaOH溶液比NaCO 溶液效果好
2 2 3
C. 向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg 2+)∶c(Fe3+)
=2 .125×1021
D.将适量的Ca(OH) 固体溶于100mL水中,刚好达到饱和[c(Ca2+)=1.054×10-2mol/L],若保持温度不变,
2
向其中加入100mL 0.012mol/L的NaOH,则该溶液变为不饱和溶液。
10.已知:pAg=-lg c(Ag+),K (AgCl)=1.56×10-10。如图是向10 mL AgNO 溶液中逐渐加入 0.1
sp 3
mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图像(实线)。根据图像所得下
列结论正确的是[提示:K (AgCl)>K (AgI)]( )
sp spA.原AgNO 溶液的物质的量浓度为0.1 mol·L-1
3
B.图中x点的坐标为(100,6)
C.图中x点表示溶液中Ag+恰好完全沉淀
D.把0.1 mol·L-1的NaCl换成0.1 mol·L-1 NaI则图像在终点后变为虚线部分
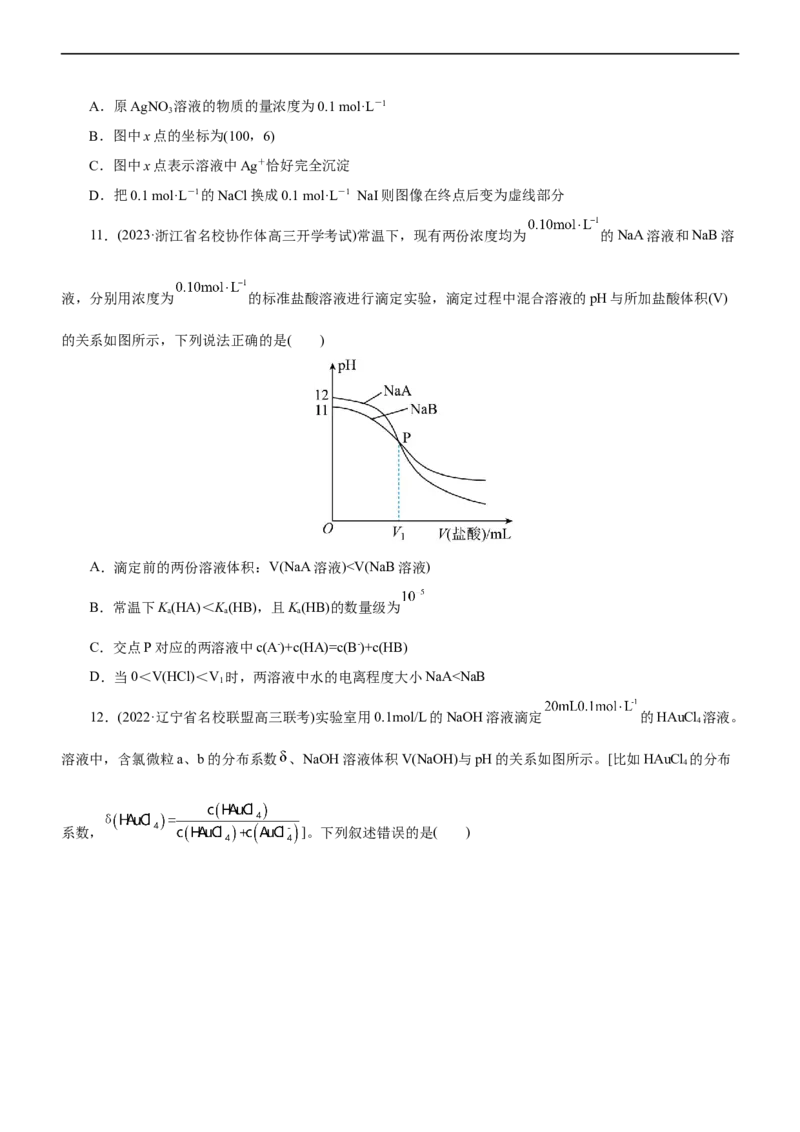
11.(2023·浙江省名校协作体高三开学考试)常温下,现有两份浓度均为 的NaA溶液和NaB溶
液,分别用浓度为 的标准盐酸溶液进行滴定实验,滴定过程中混合溶液的pH与所加盐酸体积(V)
的关系如图所示,下列说法正确的是( )
A.滴定前的两份溶液体积:V(NaA溶液)c(HA-)>c(H A)
2
14.(2022·安徽省百校联盟高三联考)马来酸又称顺丁烯二酸,可简写为HX,主要用于制造不饱和聚酯树
2
脂、染色助剂和油脂防腐剂等。常温下,将 溶液滴加到 等浓度的HX溶液中,测得混合溶液的
2与 或 浓度变化关系如图所示。下列叙述错误的是( )
A.N代表 与 的变化曲线
B.a点时,加入NaOH溶液的体积为5mL
C.NaHX溶液中:c(Na+)>c(HX-)>c(X2-)>c(HX)
2
D.当pH=7时,加入NaOH溶液的体积大于
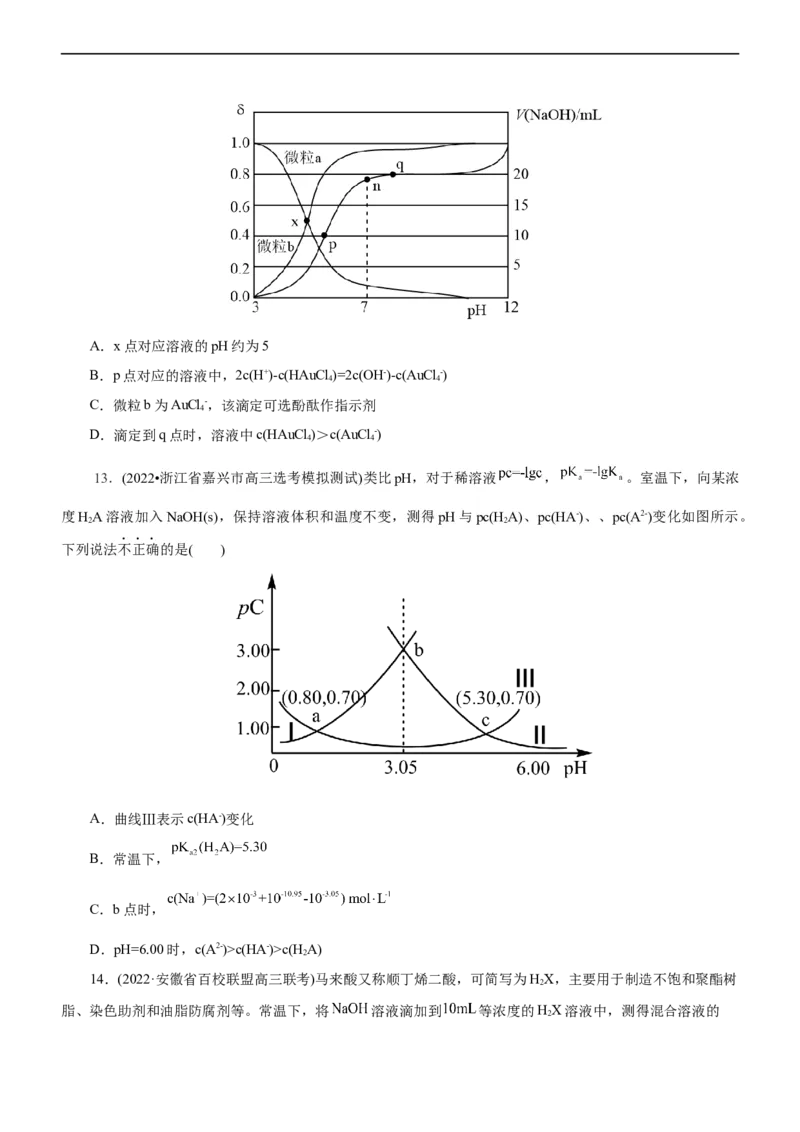
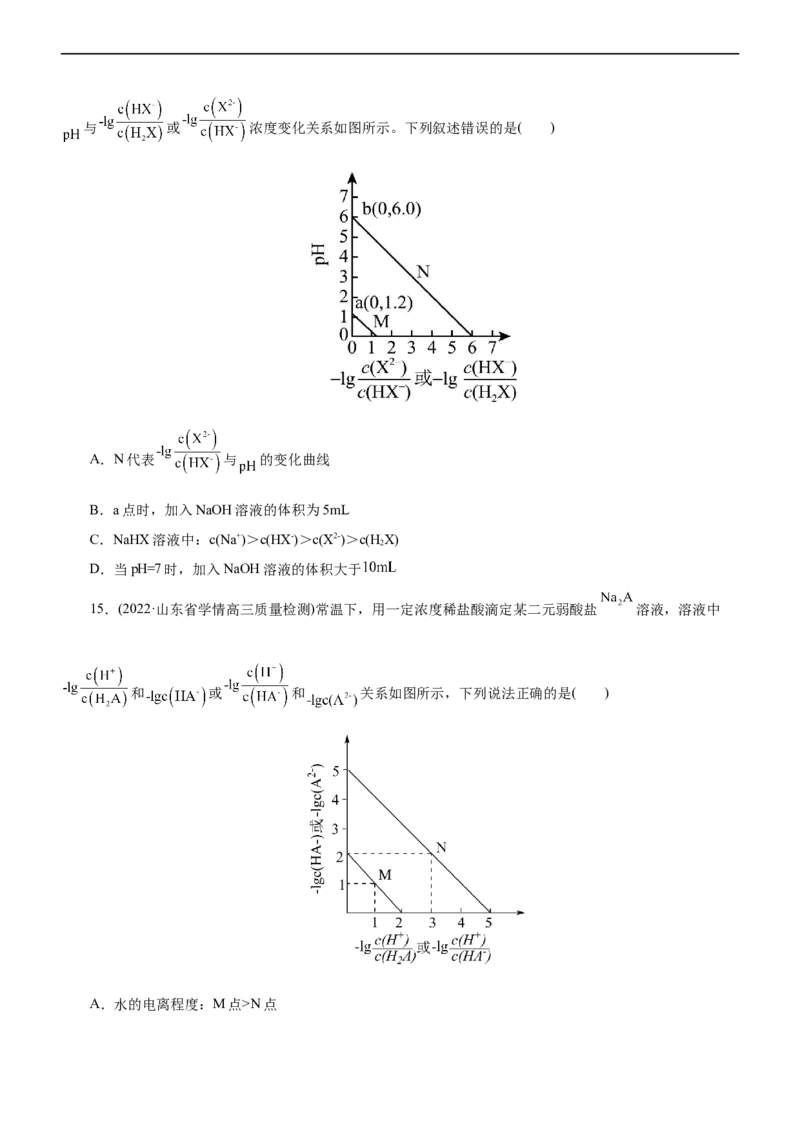
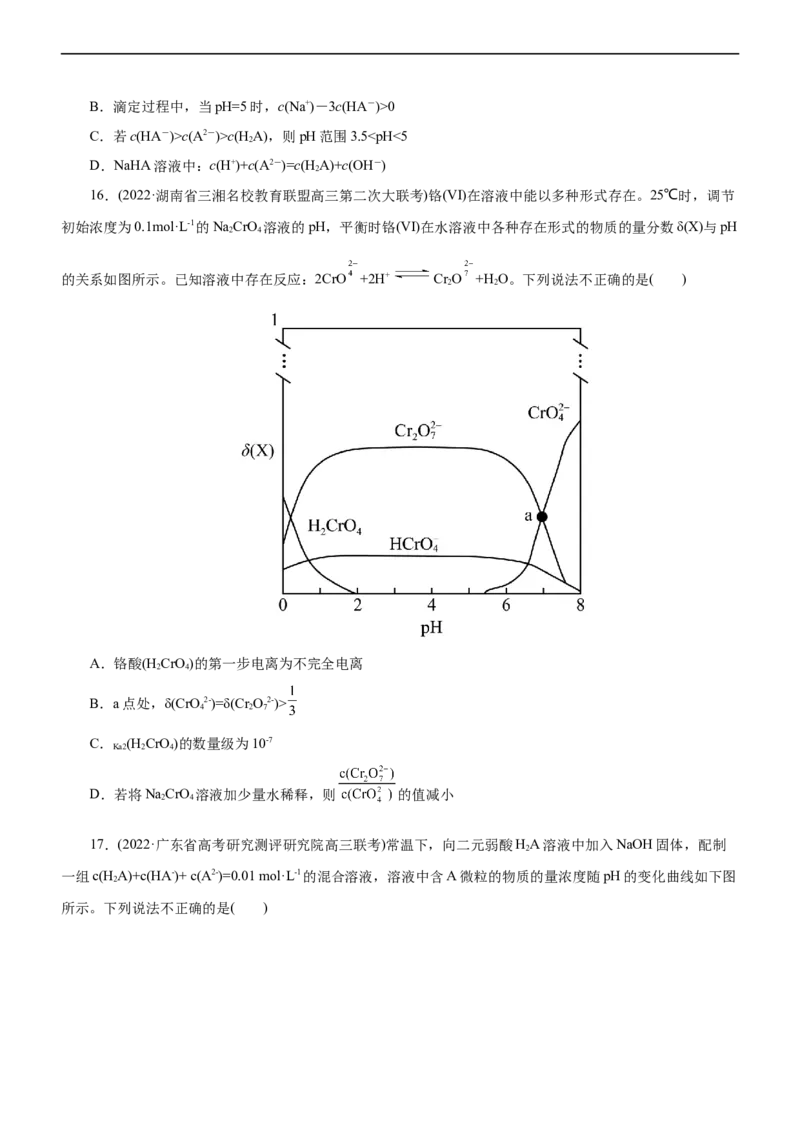
15.(2022·山东省学情高三质量检测)常温下,用一定浓度稀盐酸滴定某二元弱酸盐 溶液,溶液中
和 或 和 关系如图所示,下列说法正确的是( )
A.水的电离程度:M点>N点B.滴定过程中,当pH=5时,c(Na+)-3c(HA-)>0
C.若c(HA-)>c(A2-)>c(H A),则pH范围3.5
4 2 7
C. (H CrO)的数量级为10-7
Ka2 2 4
D.若将NaCrO 溶液加少量水稀释,则 的值减小
2 4
17.(2022·广东省高考研究测评研究院高三联考)常温下,向二元弱酸HA溶液中加入NaOH固体,配制
2
一组c(HA)+c(HA-)+ c(A2-)=0.01 mol·L-1的混合溶液,溶液中含A微粒的物质的量浓度随pH的变化曲线如下图
2
所示。下列说法不正确的是( )A.K =10 K
a1 a2
B.M点溶液中, c(Na+)=0.01 mol·L-1
C.M点溶液中由水电离出的c(H+)小于N点溶液中由水电离出的c(H+)
D.NaHA溶液中,c(HA) 小于c(A2-)
2
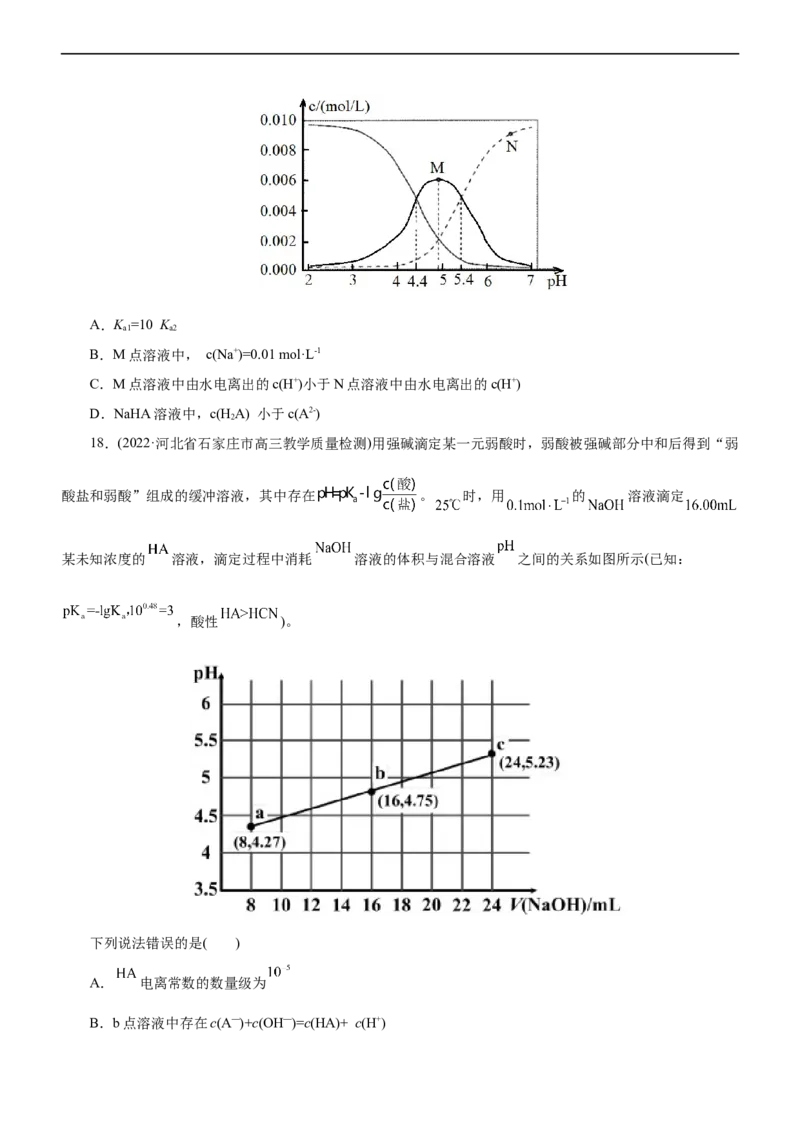
18.(2022·河北省石家庄市高三教学质量检测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱
酸盐和弱酸”组成的缓冲溶液,其中存在 。 时,用 的 溶液滴定
某未知浓度的 溶液,滴定过程中消耗 溶液的体积与混合溶液 之间的关系如图所示(已知:
,酸性 )。
下列说法错误的是( )
A. 电离常数的数量级为
B.b点溶液中存在c(A—)+c(OH—)=c(HA)+ c(H+)C.c点溶液中离子浓度的大小关系为c(A—)>c(HA) >c(H+)>c(OH—)
D.若将 改为等体积等浓度的 ,则 随 溶液体积的变化曲线竖直上移
19.(2022·广东省“六校联盟“高三第三次联考)高氯酸用途广泛,可用于电镀工业,也用于生产烟花和炸
药,还可作化学分析试剂。在某温度时,将xmol/L氨水滴入10mL1.0mol/L高氯酸中,溶液pH和温度随加入
氨水体积变化曲线如图所示。下列有关说法正确的是( )
A.a~b点温度逐渐升高是反应放热和NH ·H O电离放热共同的结果
3 2
B.b点时氨水和高氯酸恰好完全反应
C.d点:c(NH +)+c(H+)>c(ClO -)+c(OH-)
4 4
D.c点:c(NH +)+c(NH·H O)= c(ClO-)
4 3 2 4
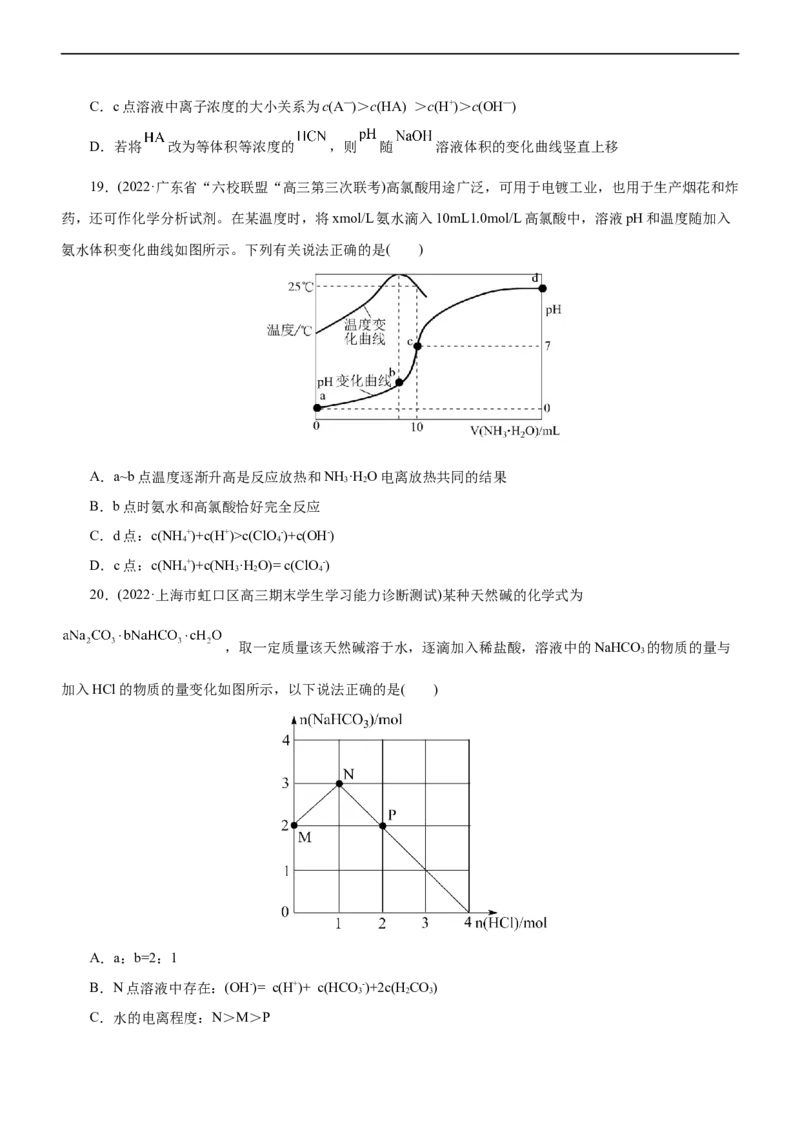
20.(2022·上海市虹口区高三期末学生学习能力诊断测试)某种天然碱的化学式为
,取一定质量该天然碱溶于水,逐滴加入稀盐酸,溶液中的NaHCO 的物质的量与
3
加入HCl的物质的量变化如图所示,以下说法正确的是( )
A.a:b=2:1
B.N点溶液中存在:(OH-)= c(H+)+ c(HCO -)+2c(HCO)
3 2 3
C.水的电离程度:N>M>PD.取天然碱溶液加入盐酸,离子方程式可能是:3HCO -+2CO 2-+7H+=5CO ↑+5H O
3 3 2 2
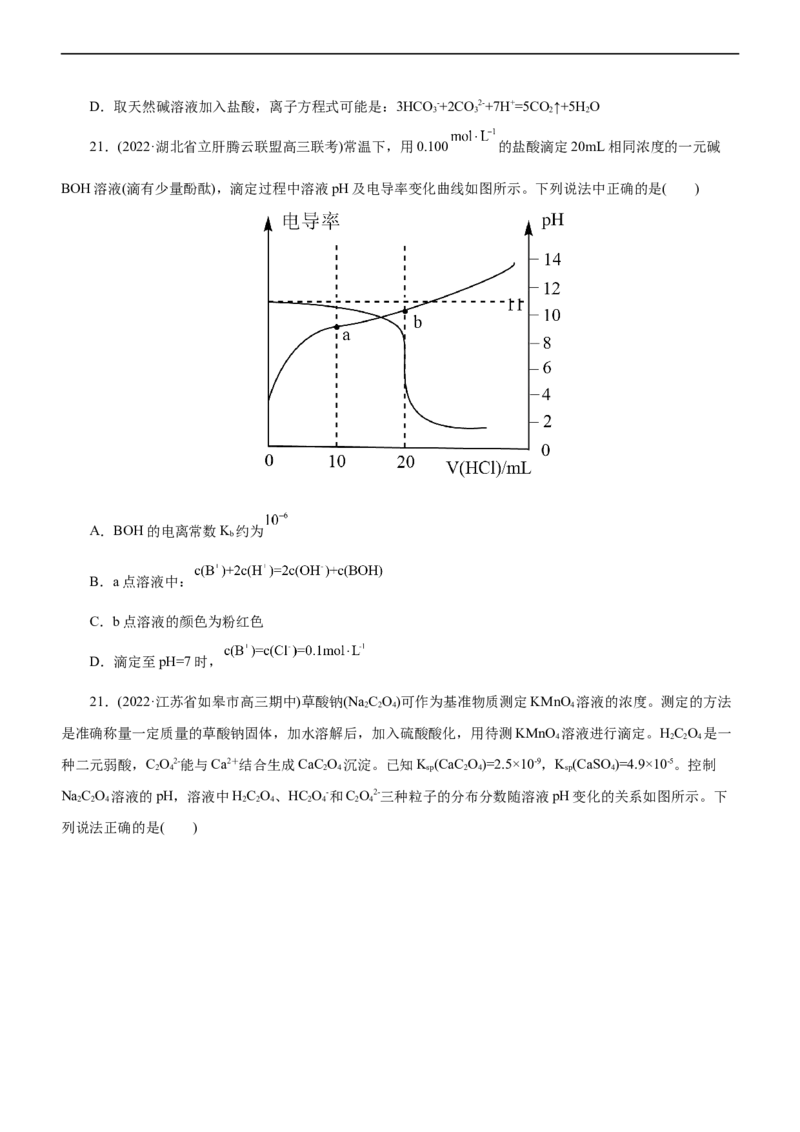
21.(2022·湖北省立肝腾云联盟高三联考)常温下,用0.100 的盐酸滴定20mL相同浓度的一元碱
BOH溶液(滴有少量酚酞),滴定过程中溶液pH及电导率变化曲线如图所示。下列说法中正确的是( )
A.BOH的电离常数K 约为
b
B.a点溶液中:
C.b点溶液的颜色为粉红色
D.滴定至pH=7时,
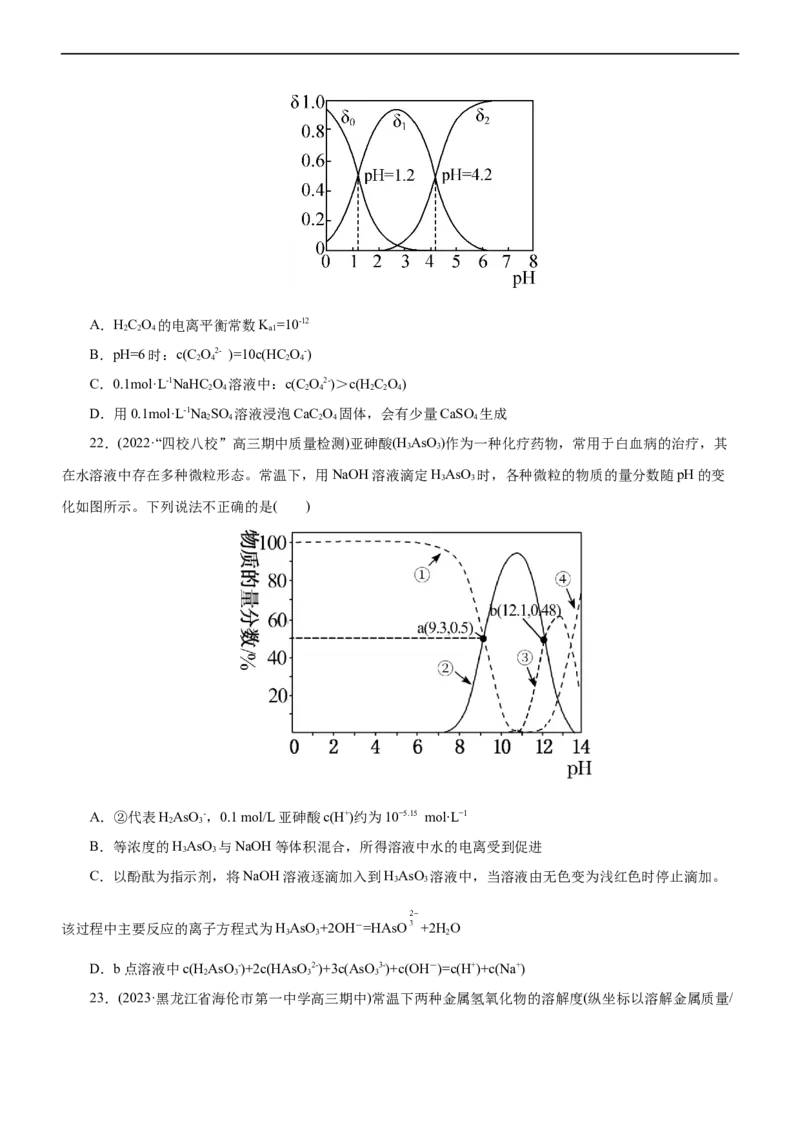
21.(2022·江苏省如皋市高三期中)草酸钠(Na C O)可作为基准物质测定KMnO 溶液的浓度。测定的方法
2 2 4 4
是准确称量一定质量的草酸钠固体,加水溶解后,加入硫酸酸化,用待测KMnO 溶液进行滴定。HC O 是一
4 2 2 4
种二元弱酸,C O2-能与Ca2+结合生成CaC O 沉淀。已知K (CaC O)=2.5×10-9,K (CaSO)=4.9×10-5。控制
2 4 2 4 sp 2 4 sp 4
NaC O 溶液的pH,溶液中HC O、HC O-和C O2-三种粒子的分布分数随溶液pH变化的关系如图所示。下
2 2 4 2 2 4 2 4 2 4
列说法正确的是( )A.HC O 的电离平衡常数K =10-12
2 2 4 a1
B.pH=6时:c(C O2- )=10c(HC O-)
2 4 2 4
C.0.1mol·L-1NaHC O 溶液中:c(C O2-)>c(HC O)
2 4 2 4 2 2 4
D.用0.1mol·L-1NaSO 溶液浸泡CaC O 固体,会有少量CaSO 生成
2 4 2 4 4
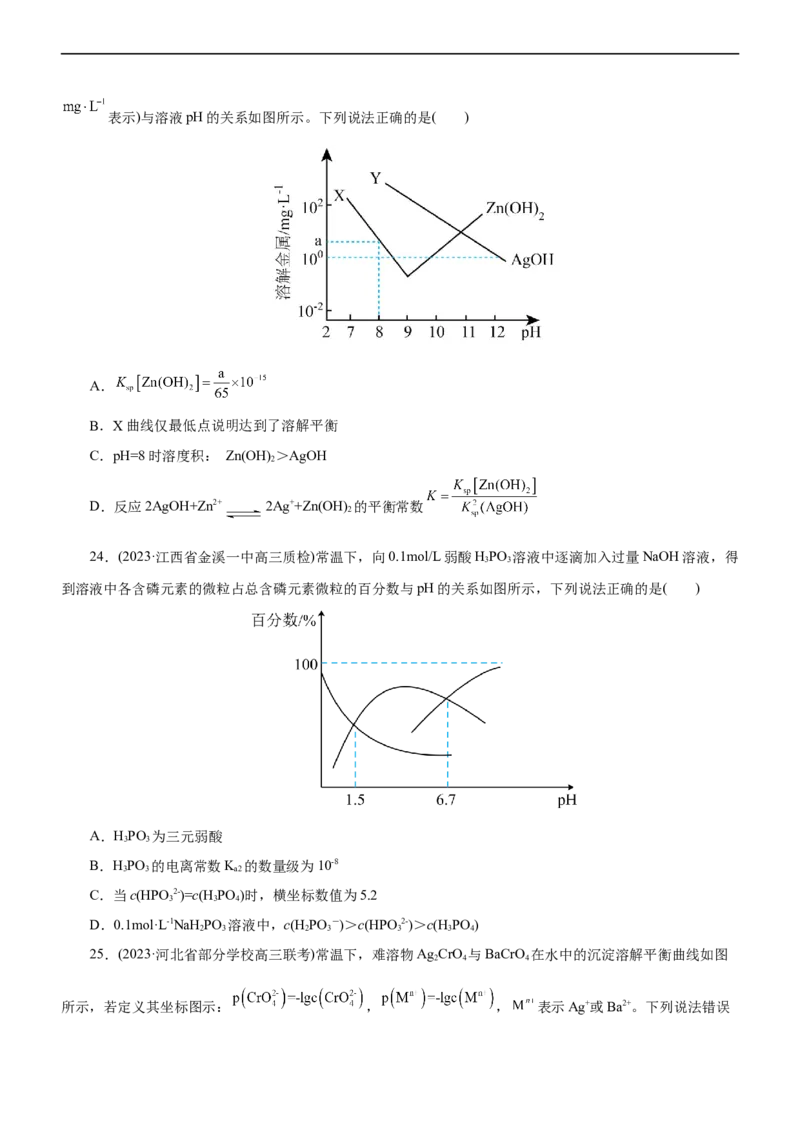
22.(2022·“四校八校”高三期中质量检测)亚砷酸(H AsO )作为一种化疗药物,常用于白血病的治疗,其
3 3
在水溶液中存在多种微粒形态。常温下,用NaOH溶液滴定HAsO 时,各种微粒的物质的量分数随pH的变
3 3
化如图所示。下列说法不正确的是( )
A.②代表HAsO -,0.1 mol/L亚砷酸c(H+)约为10−5.15 mol∙L−1
2 3
B.等浓度的HAsO 与NaOH等体积混合,所得溶液中水的电离受到促进
3 3
C.以酚酞为指示剂,将NaOH溶液逐滴加入到HAsO 溶液中,当溶液由无色变为浅红色时停止滴加。
3 3
该过程中主要反应的离子方程式为HAsO +2OH-=HAsO +2H O
3 3 2
D.b点溶液中c(HAsO -)+2c(HAsO 2-)+3c(AsO 3-)+c(OH-)=c(H+)+c(Na+)
2 3 3 3
23.(2023·黑龙江省海伦市第一中学高三期中)常温下两种金属氢氧化物的溶解度(纵坐标以溶解金属质量/表示)与溶液pH的关系如图所示。下列说法正确的是( )
A.
B.X曲线仅最低点说明达到了溶解平衡
C.pH=8时溶度积: Zn(OH) >AgOH
2
D.反应2AgOH+Zn2+ 2Ag++Zn(OH) 的平衡常数
2
24.(2023·江西省金溪一中高三质检)常温下,向0.1mol/L弱酸HPO 溶液中逐滴加入过量NaOH溶液,得
3 3
到溶液中各含磷元素的微粒占总含磷元素微粒的百分数与pH的关系如图所示,下列说法正确的是( )
A.HPO 为三元弱酸
3 3
B.HPO 的电离常数K 的数量级为10-8
3 3 a2
C.当c(HPO 2-)=c(H PO )时,横坐标数值为5.2
3 3 4
D.0.1mol·L-1NaH PO 溶液中,c(H PO -)>c(HPO 2-)>c(H PO )
2 3 2 3 3 3 4
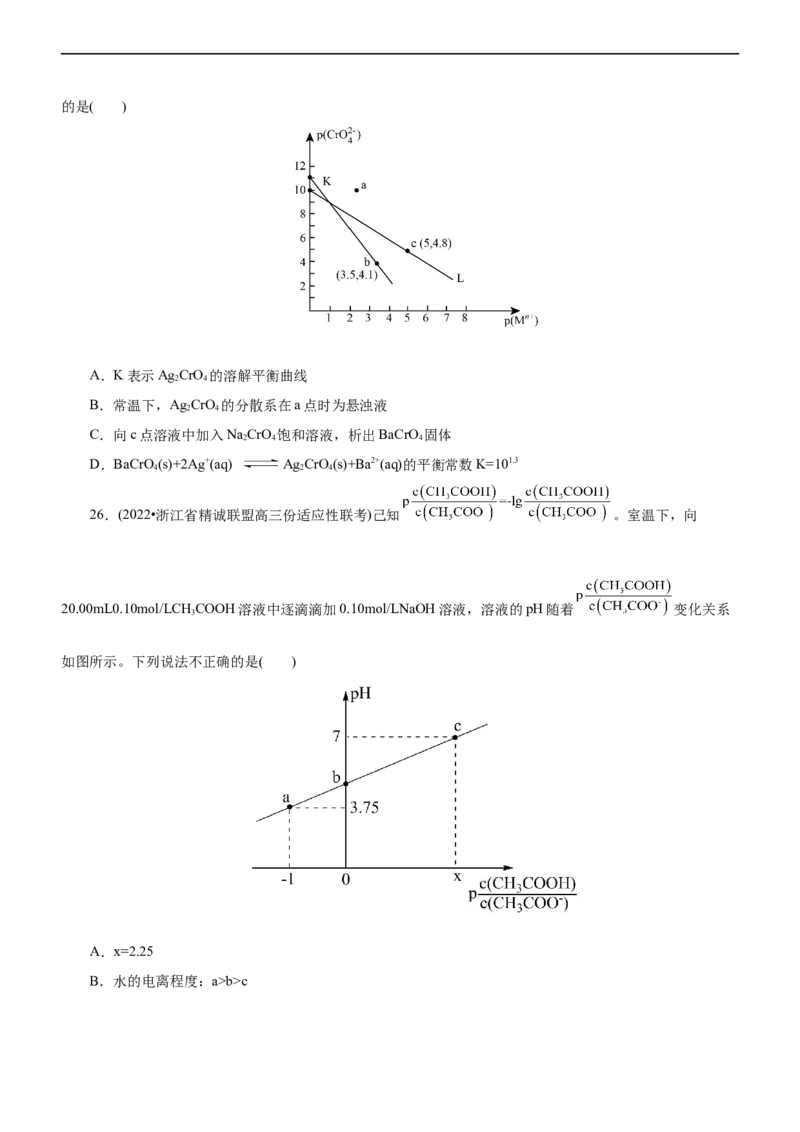
25.(2023·河北省部分学校高三联考)常温下,难溶物Ag CrO 与BaCrO 在水中的沉淀溶解平衡曲线如图
2 4 4
所示,若定义其坐标图示: , , 表示Ag+或Ba2+。下列说法错误的是( )
A.K表示Ag CrO 的溶解平衡曲线
2 4
B.常温下,Ag CrO 的分散系在a点时为悬浊液
2 4
C.向c点溶液中加入NaCrO 饱和溶液,析出BaCrO 固体
2 4 4
D.BaCrO(s)+2Ag+(aq) Ag CrO(s)+Ba2+(aq)的平衡常数K=101.3
4 2 4
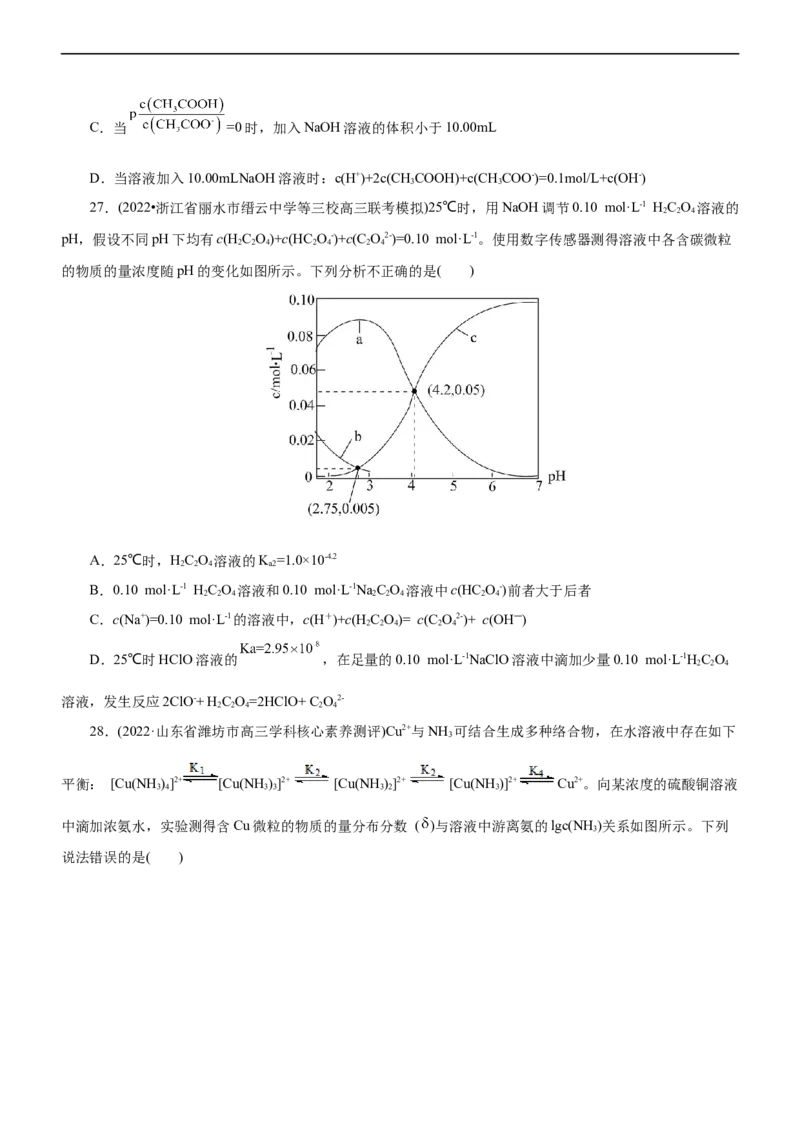
26.(2022•浙江省精诚联盟高三份适应性联考)己知 。室温下,向
20.00mL0.10mol/LCH COOH溶液中逐滴滴加0.10mol/LNaOH溶液,溶液的pH随着 变化关系
3
如图所示。下列说法不正确的是( )
A.x=2.25
B.水的电离程度:a>b>cC.当 =0时,加入NaOH溶液的体积小于10.00mL
D.当溶液加入10.00mLNaOH溶液时:c(H+)+2c(CH COOH)+c(CH COO-)=0.1mol/L+c(OH-)
3 3
27.(2022•浙江省丽水市缙云中学等三校高三联考模拟)25℃时,用NaOH调节0.10 mol·L-1 HC O 溶液的
2 2 4
pH,假设不同pH下均有c(HC O)+c(HC O-)+c(C O2-)=0.10 mol·L-1。使用数字传感器测得溶液中各含碳微粒
2 2 4 2 4 2 4
的物质的量浓度随pH的变化如图所示。下列分析不正确的是( )
A.25℃时,HC O 溶液的K =1.0×10-4.2
2 2 4 a2
B.0.10 mol·L-1 HC O 溶液和0.10 mol·L-1NaC O 溶液中c(HC O-)前者大于后者
2 2 4 2 2 4 2 4
C.c(Na+)=0.10 mol·L-1的溶液中,c(H+)+c(HC O)= c(C O2-)+ c(OH―)
2 2 4 2 4
D.25℃时HClO溶液的 ,在足量的0.10 mol·L-1NaClO溶液中滴加少量0.10 mol·L-1HC O
2 2 4
溶液,发生反应2ClO-+ H C O=2HClO+ C O2-
2 2 4 2 4
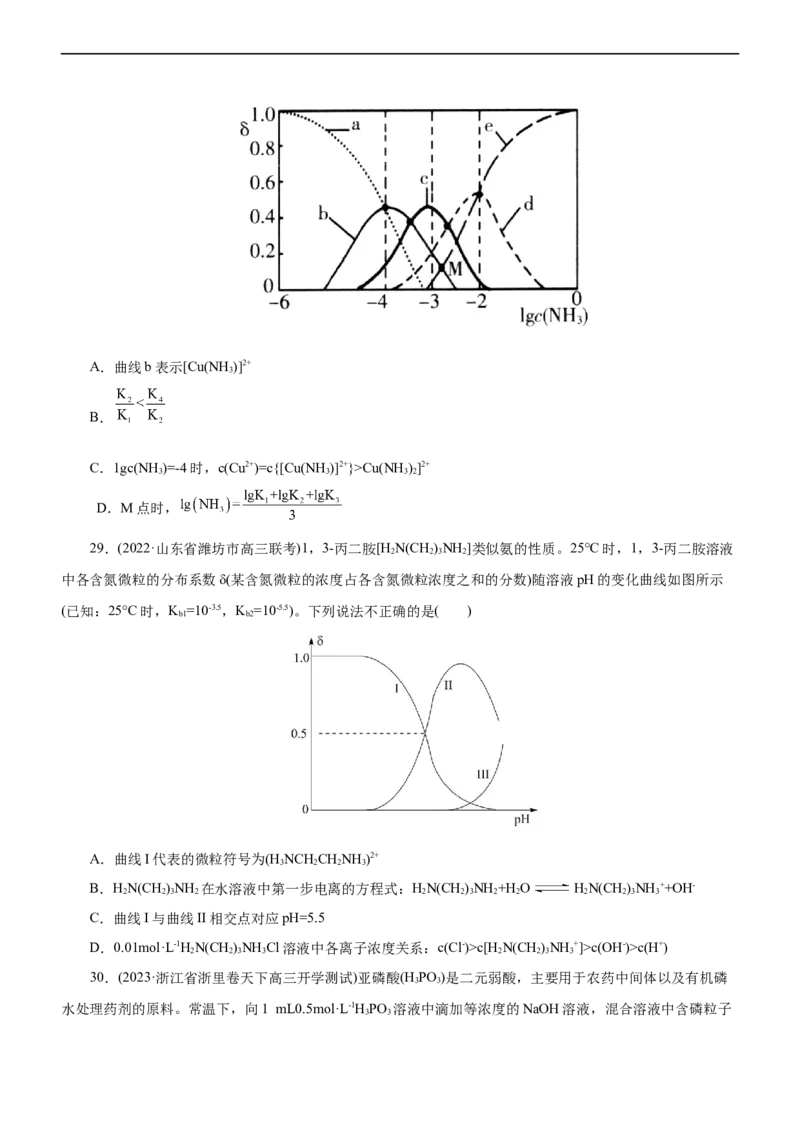
28.(2022·山东省潍坊市高三学科核心素养测评)Cu2+与NH 可结合生成多种络合物,在水溶液中存在如下
3
平衡: [Cu(NH )]2+ [Cu(NH )]2+ [Cu(NH )]2+ [Cu(NH )]2+ Cu2+。向某浓度的硫酸铜溶液
3 4 3 3 3 2 3
中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数 ( )与溶液中游离氨的lgc(NH)关系如图所示。下列
3
说法错误的是( )A.曲线b表示[Cu(NH )]2+
3
B.
C.1gc(NH )=-4时,c(Cu2+)=c{[Cu(NH )]2+}>Cu(NH )]2+
3 3 3 2
D.M点时,
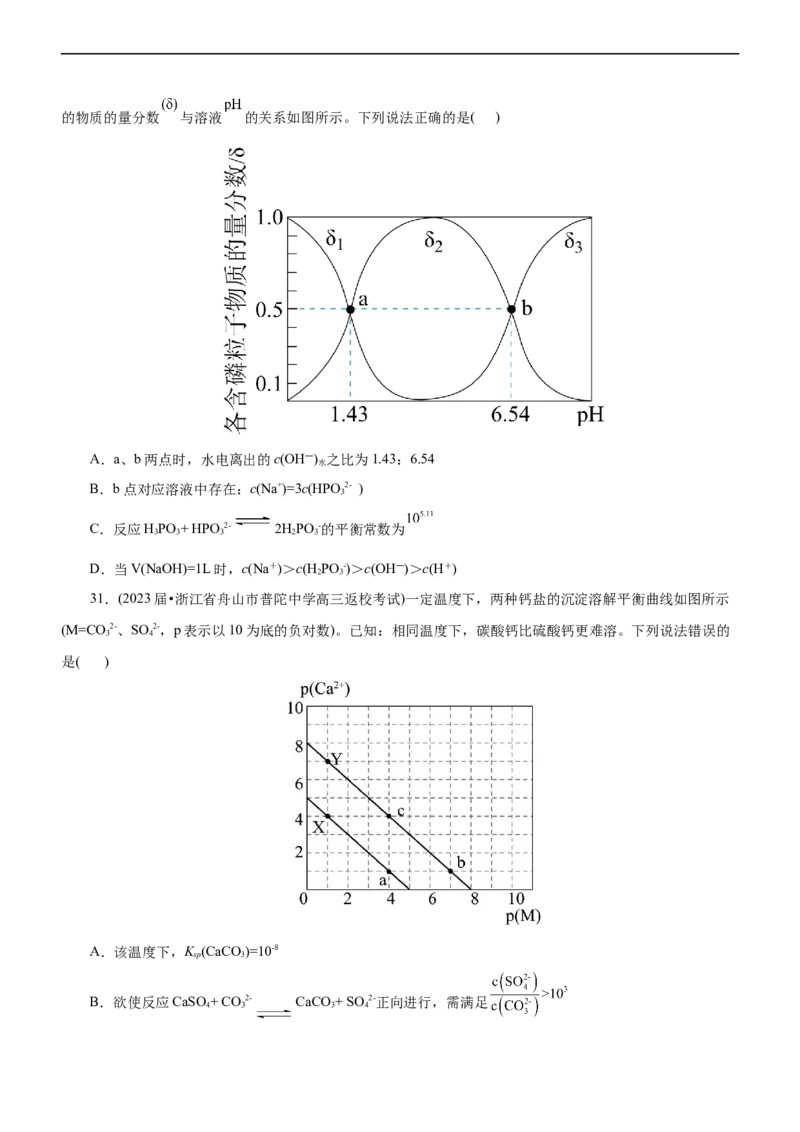
29.(2022·山东省潍坊市高三联考)1,3-丙二胺[H N(CH )NH ]类似氨的性质。25°C时,1,3-丙二胺溶液
2 2 3 2
中各含氮微粒的分布系数δ(某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pH的变化曲线如图所示
(已知:25°C时,K =10-3.5,K =10-5.5)。下列说法不正确的是( )
b1 b2
A.曲线I代表的微粒符号为(H NCH CHNH )2+
3 2 2 3
B.HN(CH )NH 在水溶液中第一步电离的方程式:HN(CH )NH +H O HN(CH )NH ++OH-
2 2 3 2 2 2 3 2 2 2 2 3 3
C.曲线I与曲线II相交点对应pH=5.5
D.0.01mol·L-1HN(CH )NH Cl溶液中各离子浓度关系:c(Cl-)>c[H N(CH )NH +]>c(OH-)>c(H+)
2 2 3 3 2 2 3 3
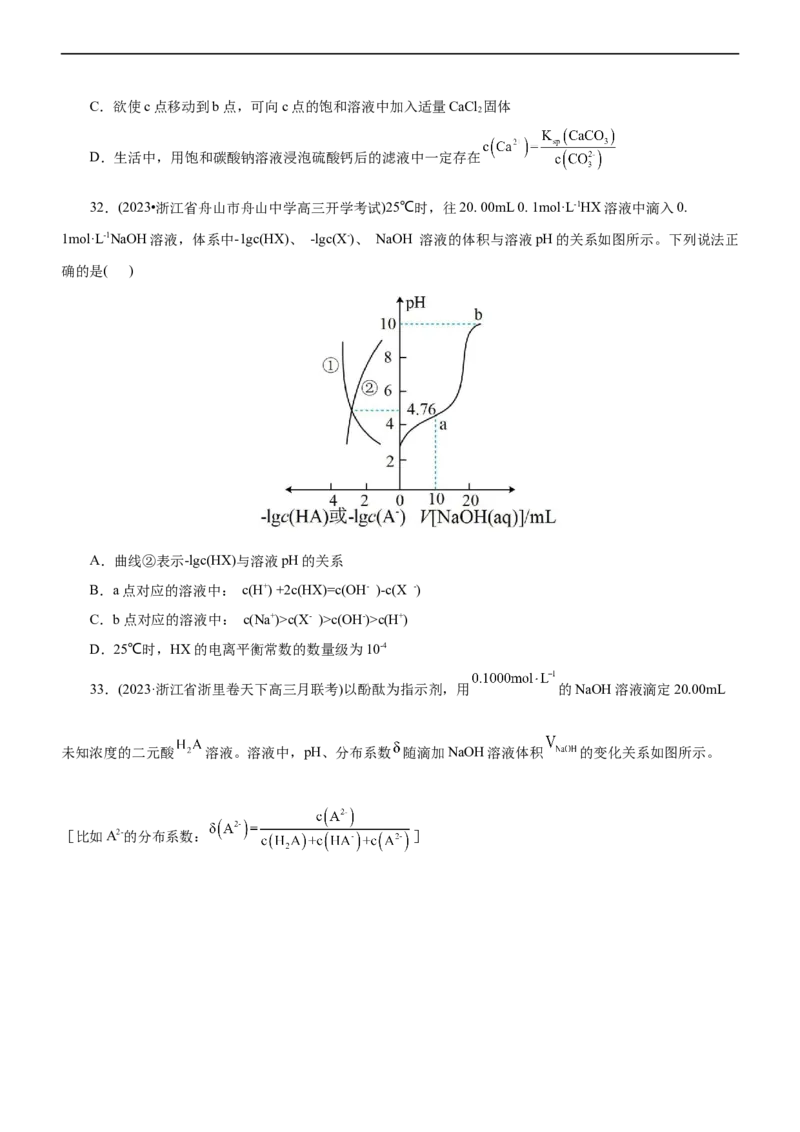
30.(2023·浙江省浙里卷天下高三开学测试)亚磷酸(HPO )是二元弱酸,主要用于农药中间体以及有机磷
3 3
水处理药剂的原料。常温下,向1 mL0.5mol·L-1HPO 溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子
3 3的物质的量分数 与溶液 的关系如图所示。下列说法正确的是( )
A.a、b两点时,水电离出的c(OH―) 之比为1.43:6.54
水
B.b点对应溶液中存在:c(Na+)=3c(HPO 2- )
3
C.反应HPO + HPO 2- 2HPO -的平衡常数为
3 3 3 2 3
D.当V(NaOH)=1L时,c(Na+)>c(H PO -)>c(OH―)>c(H+)
2 3
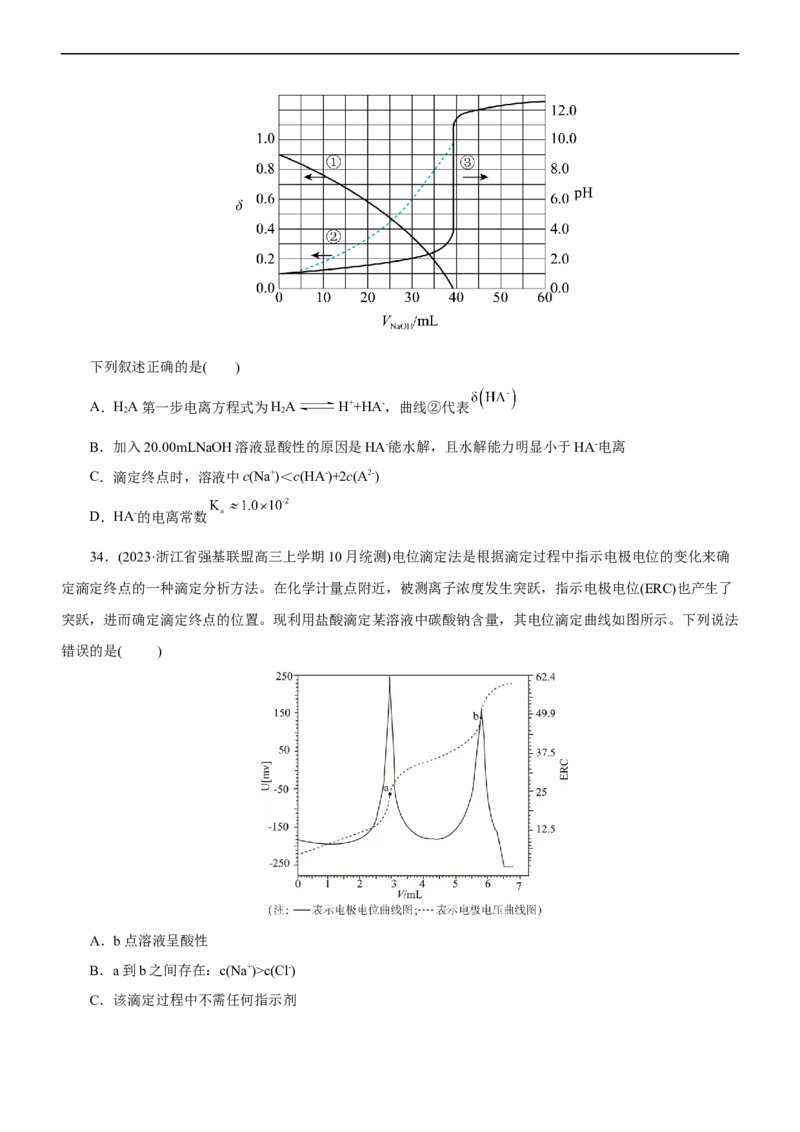
31.(2023届•浙江省舟山市普陀中学高三返校考试)一定温度下,两种钙盐的沉淀溶解平衡曲线如图所示
(M=CO2-、SO 2-,p表示以10为底的负对数)。已知:相同温度下,碳酸钙比硫酸钙更难溶。下列说法错误的
3 4
是( )
A.该温度下,K (CaCO)=10-8
sp 3
B.欲使反应CaSO+ CO2- CaCO + SO 2-正向进行,需满足
4 3 3 4C.欲使c点移动到b点,可向c点的饱和溶液中加入适量CaCl 固体
2
D.生活中,用饱和碳酸钠溶液浸泡硫酸钙后的滤液中一定存在
32.(2023•浙江省舟山市舟山中学高三开学考试)25℃时,往20. 00mL 0. 1mol·L-1HX溶液中滴入0.
1mol·L-1NaOH溶液,体系中-1gc(HX)、 -lgc(X-)、 NaOH 溶液的体积与溶液pH的关系如图所示。下列说法正
确的是( )
A.曲线②表示-lgc(HX)与溶液pH的关系
B.a点对应的溶液中: c(H+) +2c(HX)=c(OH- )-c(X -)
C.b点对应的溶液中: c(Na+)>c(X- )>c(OH-)>c(H+)
D.25℃时,HX的电离平衡常数的数量级为10-4
33.(2023·浙江省浙里卷天下高三月联考)以酚酞为指示剂,用 的NaOH溶液滴定20.00mL
未知浓度的二元酸 溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积 的变化关系如图所示。
[比如A2-的分布系数: ]下列叙述正确的是( )
A.HA第一步电离方程式为HA H++HA-,曲线②代表
2 2
B.加入20.00mLNaOH溶液显酸性的原因是HA-能水解,且水解能力明显小于HA-电离
C.滴定终点时,溶液中c(Na+)<c(HA-)+2c(A2-)
D.HA-的电离常数
34.(2023·浙江省强基联盟高三上学期10月统测)电位滴定法是根据滴定过程中指示电极电位的变化来确
定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了
突跃,进而确定滴定终点的位置。现利用盐酸滴定某溶液中碳酸钠含量,其电位滴定曲线如图所示。下列说法
错误的是( )
A.b点溶液呈酸性
B.a到b之间存在:c(Na+)>c(Cl-)
C.该滴定过程中不需任何指示剂D.a点溶液中存在: c(Na+)=c(HCO-)+c(CO 2-)+c(H CO)
3 3 2 3
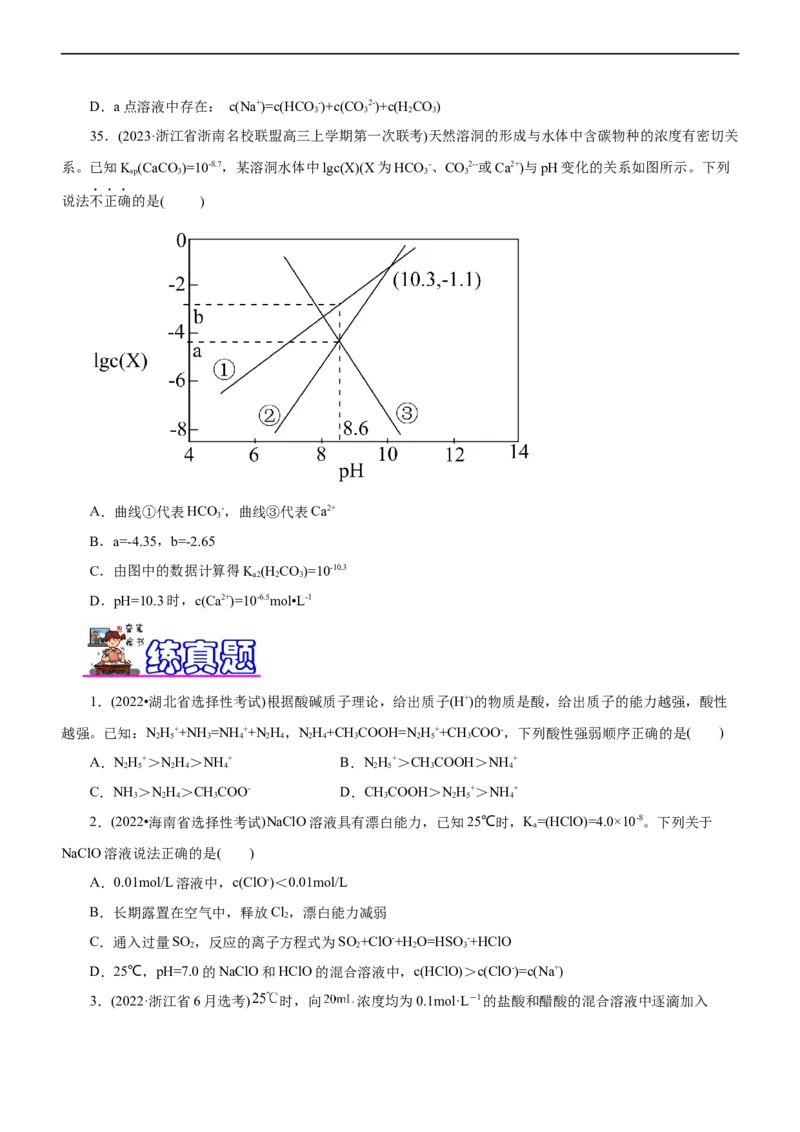
35.(2023·浙江省浙南名校联盟高三上学期第一次联考)天然溶洞的形成与水体中含碳物种的浓度有密切关
系。已知K (CaCO)=10-8.7,某溶洞水体中lgc(X)(X为HCO -、CO2--或Ca2+)与pH变化的关系如图所示。下列
sp 3 3 3
说法不正确的是( )
A.曲线①代表HCO -,曲线③代表Ca2+
3
B.a=-4.35,b=-2.65
C.由图中的数据计算得K (H CO)=10-10.3
a2 2 3
D.pH=10.3时,c(Ca2+)=10-6.5mol•L-1
1.(2022•湖北省选择性考试)根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸性
越强。已知:NH++NH=NH++N H,NH+CH COOH=N H++CH COO-,下列酸性强弱顺序正确的是( )
2 5 3 4 2 4 2 4 3 2 5 3
A.NH+>NH>NH + B.NH+>CHCOOH>NH +
2 5 2 4 4 2 5 3 4
C.NH >NH>CHCOO- D.CHCOOH>NH+>NH +
3 2 4 3 3 2 5 4
2.(2022•海南省选择性考试)NaClO溶液具有漂白能力,已知25℃时,K=(HClO)=4.0×10-8。下列关于
a
NaClO溶液说法正确的是( )
A.0.01mol/L溶液中,c(ClO-)<0.01mol/L
B.长期露置在空气中,释放Cl,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO-+H O=HSO -+HClO
2 2 2 3
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO-)=c(Na+)
3.(2022·浙江省6月选考) 时,向 浓度均为0.1mol·L-1的盐酸和醋酸的混合溶液中逐滴加入0.1mol·L-1的NaOH溶液(醋酸的K=1.8×10-5;用0.1mol·L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定终点
a
的 突跃范围4.3~9.7)。下列说法不正确的是( )
A.恰好中和时,溶液呈碱性
B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H O
2
C.滴定过程中,c(Cl-)=c(CH COO-)+c(CH COOH)
3 3
D. 时,c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH)
3 3
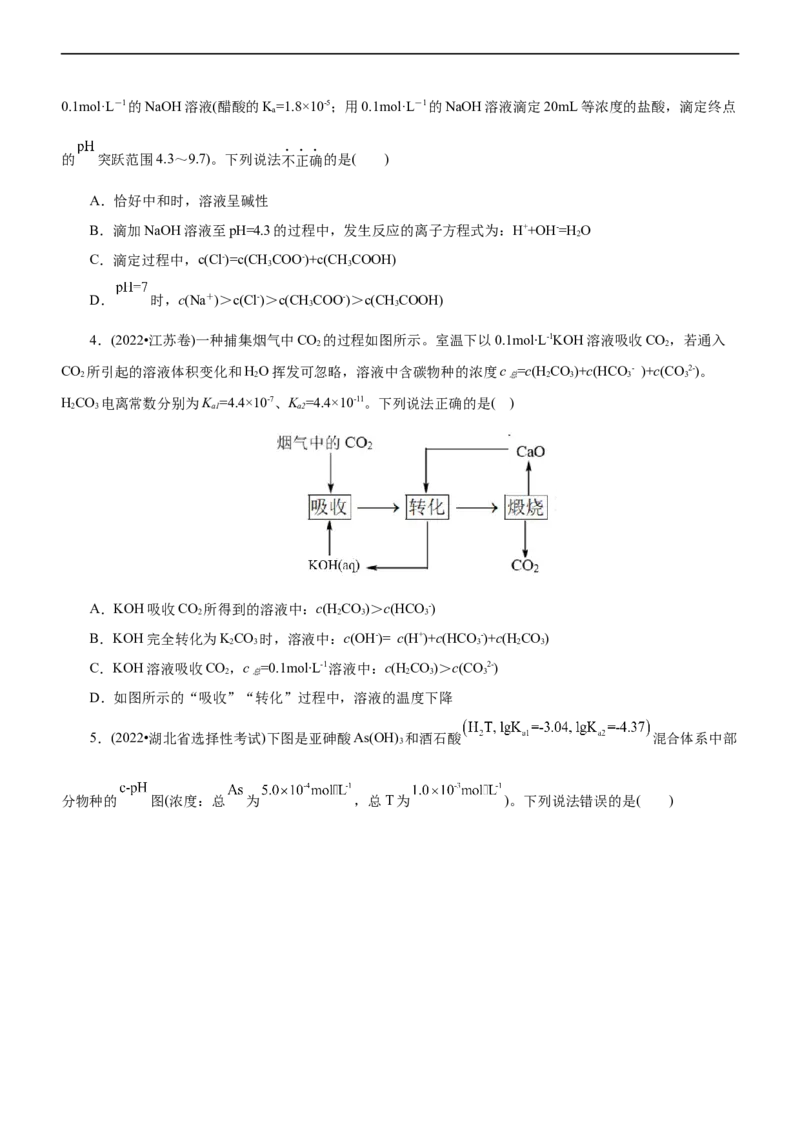
4.(2022•江苏卷)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通入
2 2
CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c(HCO - )+c(CO2-)。
2 2 总 2 3 3 3
HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是( )
2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c(HCO -)
2 2 3 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c(HCO -)+c(H CO)
2 3 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c(CO2-)
2 总 2 3 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
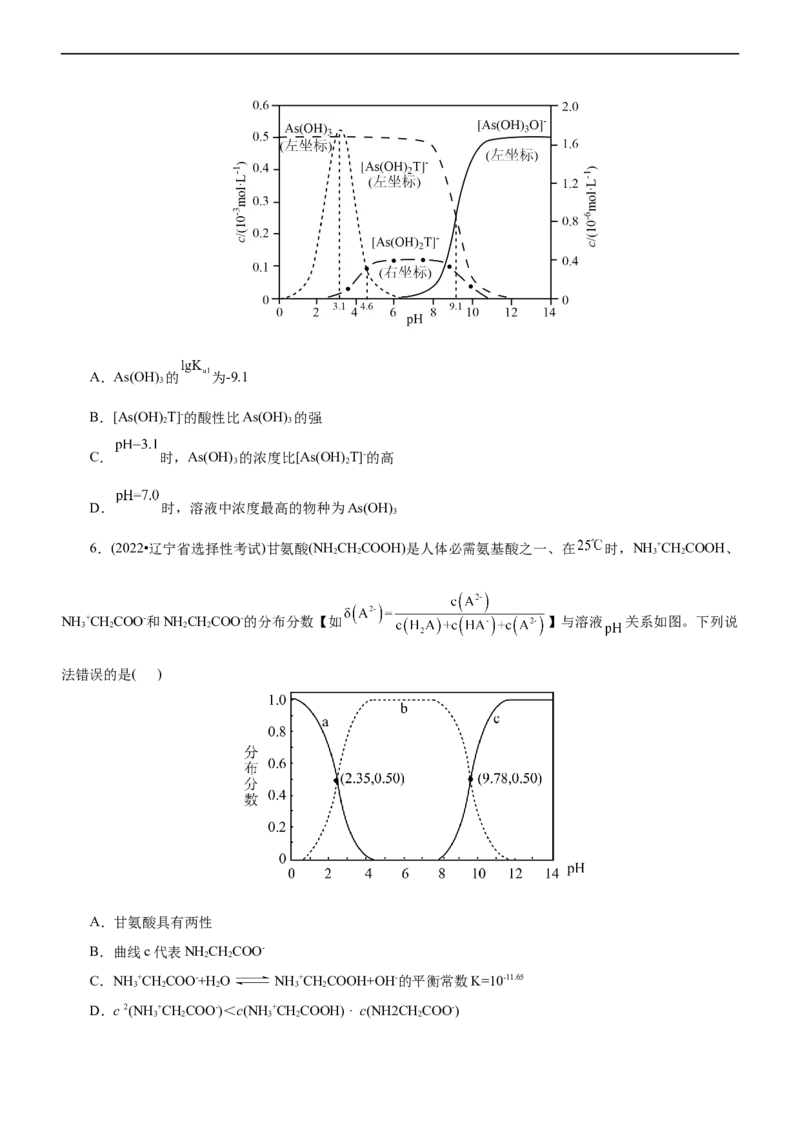
5.(2022•湖北省选择性考试)下图是亚砷酸As(OH) 和酒石酸 混合体系中部
3
分物种的 图(浓度:总 为 ,总T为 )。下列说法错误的是( )A.As(OH) 的 为-9.1
3
B.[As(OH) T]-的酸性比As(OH) 的强
2 3
C. 时,As(OH) 的浓度比[As(OH) T]-的高
3 2
D. 时,溶液中浓度最高的物种为As(OH)
3
6.(2022•辽宁省选择性考试)甘氨酸(NH CHCOOH)是人体必需氨基酸之一、在 时,NH +CHCOOH、
2 2 3 2
NH +CHCOO-和NH CHCOO-的分布分数【如 】与溶液 关系如图。下列说
3 2 2 2
法错误的是( )
A.甘氨酸具有两性
B.曲线c代表NH CHCOO-
2 2
C.NH +CHCOO-+H O NH +CHCOOH+OH-的平衡常数K=10-11.65
3 2 2 3 2
D.c 2(NH +CHCOO-)<c(NH +CHCOOH) · c(NH2CHCOO-)
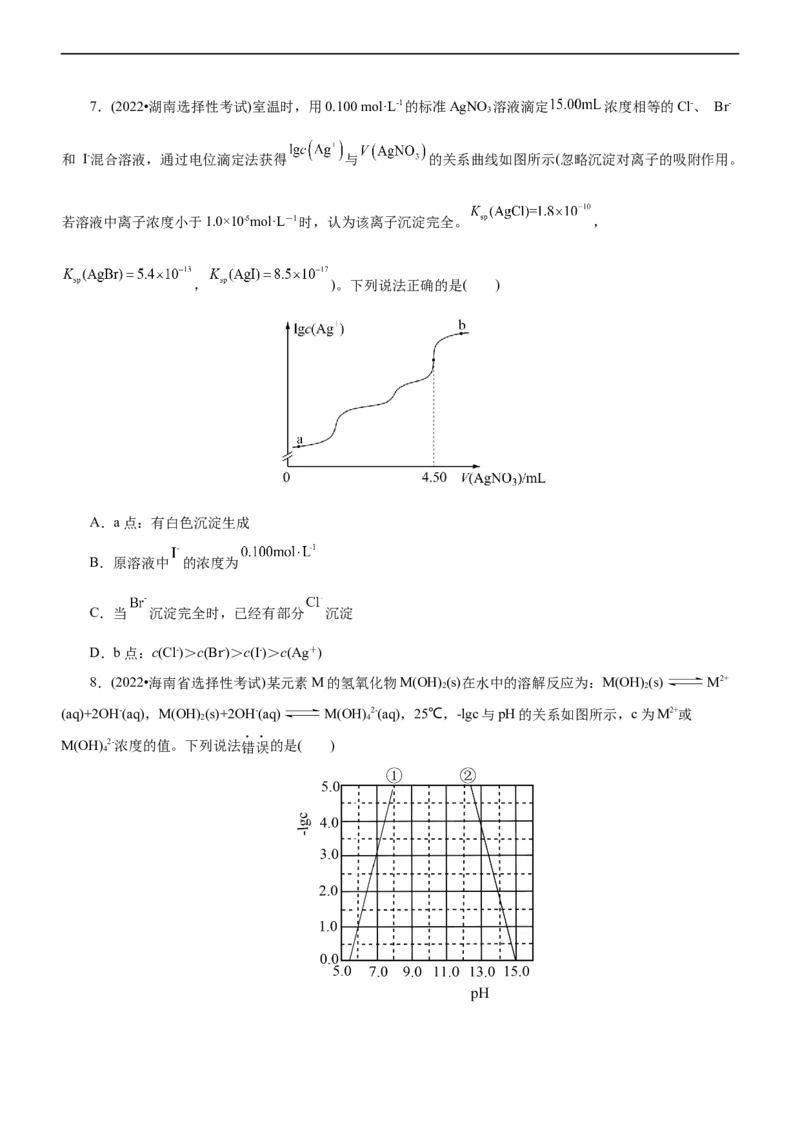
3 2 3 2 27.(2022•湖南选择性考试)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定 浓度相等的Cl-、 Br-
3
和 I-混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。
若溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子沉淀完全。 ,
, )。下列说法正确的是( )
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
8.(2022•海南省选择性考试)某元素M的氢氧化物M(OH) (s)在水中的溶解反应为:M(OH) (s) M2+
2 2
(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) 2-(aq),25℃,-lgc与pH的关系如图所示,c为M2+或
2 4
M(OH) 2-浓度的值。下列说法错误的是( )
4A.曲线①代表-lg c(M2+)与pH的关系
B.M(OH) 的K 约为1×10-10
2 sp
C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以M(OH) (s)存在
2
D.向c[M(OH) 2-]=0.1mol/L的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在
4
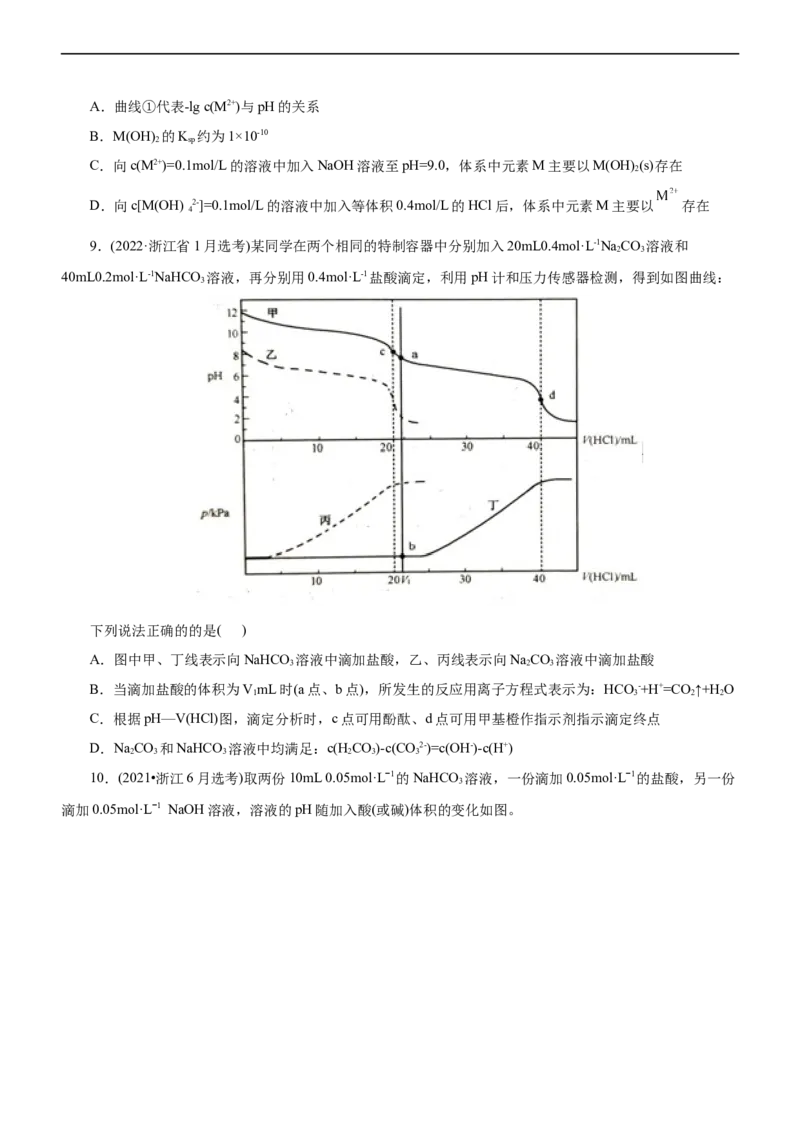
9.(2022·浙江省1月选考)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
3
下列说法正确的的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -+H+=CO ↑+H O
1 3 2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
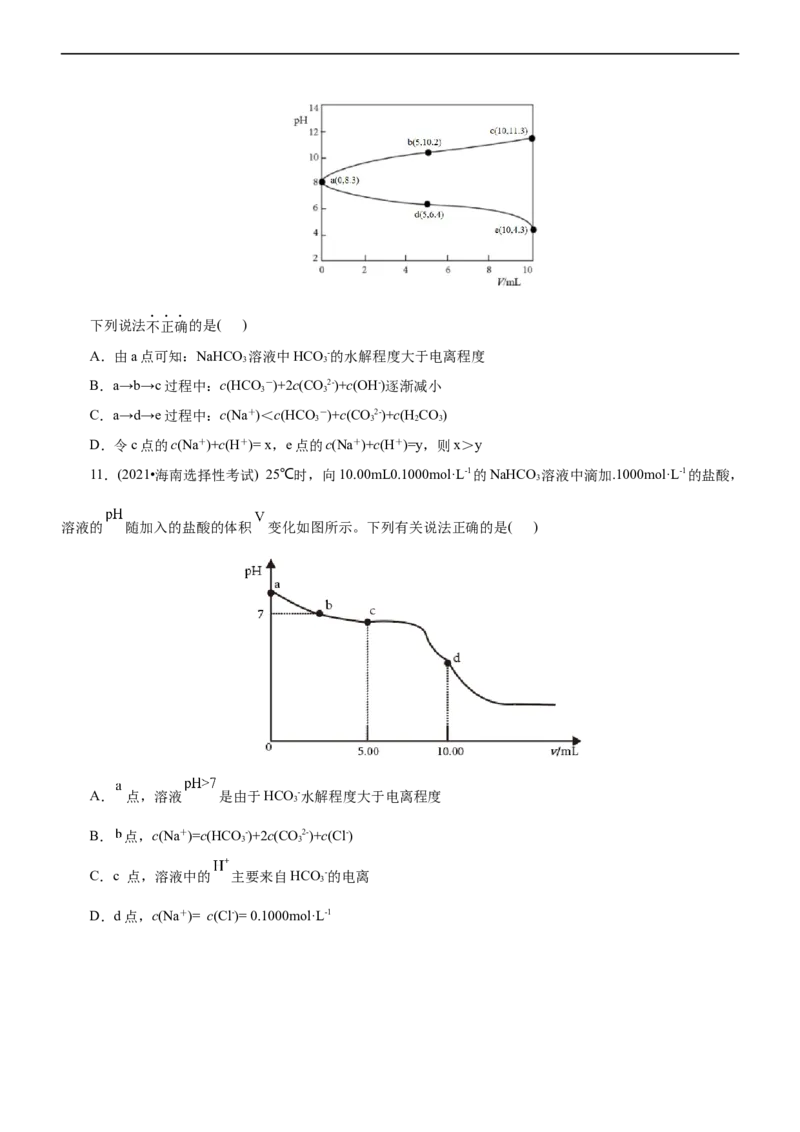
10.(2021•浙江6月选考)取两份10mL 0.05mol·Lˉ1的NaHCO 溶液,一份滴加0.05mol·Lˉ1的盐酸,另一份
3
滴加0.05mol·Lˉ1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B.a→b→c过程中:c(HCO -)+2c(CO2-)+c(OH-)逐渐减小
3 3
C.a→d→e过程中:c(Na+)<c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
D.令c点的c(Na+)+c(H+)= x,e点的c(Na+)+c(H+)=y,则x>y
11.(2021•海南选择性考试) 25℃时,向10.00mL0.1000mol·L-1的NaHCO 溶液中滴加.1000mol·L-1的盐酸,
3
溶液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是( )
A. 点,溶液 是由于HCO -水解程度大于电离程度
3
B. 点,c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-)
3 3
C.c 点,溶液中的 主要来自HCO -的电离
3
D.d点,c(Na+)= c(Cl-)= 0.1000mol·L-1