文档内容
专题 17 氮及其化合物
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 氮及其化合物的结构、性质及应用
考点二 氮及其化合物制备的工艺流程
考点三 氮及其化合物的有关计算
考点一 氮及其化合物的结构、性质及应用
1.(2023·江苏盐城·盐城中学校考二模)下列有关物质的性质与用途的对应关系正确的是
A.N 性质不活泼,可作为粮食保护气 B.NH 具有还原性,可用作制冷剂
2 3
C.NH 的熔沸点较低,可用作火箭推进剂 D.NH Cl受热易分解,可用作铁的除锈剂
2 4 4
【答案】A
【解析】A.氮气含有氮氮三键,化学性质稳定,一般不与物质发生反应,可用作保护气,A正确;B.液
氨汽化吸收大量的热,具有制冷作用,可用作制冷剂,与其还原性无关,B不正确;C.NH 在空气中燃
2 4
烧或与过氧化氢HO 反应时,能生成大量气体(N 和水蒸气),因此可用作火箭燃料,与其熔沸点较低
2 2 2
无关,C不正确;D.因为NH Cl在水中电离出的 , 水解使溶液显酸性,因此可作为铁的除锈剂,
4
与其受热易分解无关,D不正确。答案选A。
2.(2023秋·云南昆明·高三昆明市官渡区第二中学校考开学考试)用以下三种途径来制取等质量的硝酸铜。
①铜与稀硝酸反应;②铜与浓硝酸反应;③铜先与氧气反应生成氧化铜,氧化铜再跟硝酸反应。以下叙述
不正确的是
A.三种途径所消耗铜的质量相等
B.三种途径所消耗硝酸的物质的量是①>②>③
C.途径③的制备方法最符合“绿色化学”理念
D.途径①中被氧化的铜与被还原的硝酸的物质的量之比是3:2
【答案】B
【解析】三种方法制取硝酸铜的有关反应原理用方程式表示分别为:
①铜与稀硝酸反应:3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO;②铜与浓硝酸反应:
3 3 2 2
Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O;③铜先与氧气反应生成氧化铜,氧化铜再跟硝酸反应:2Cu+O
3 3 2 2 2 2
2CuO,CuO+2HNO = Cu(NO );A. 根据Cu元素守恒,铜元素都反应生成了硝酸铜,所以制取等量
3 3 2
的硝酸铜消耗铜的质量相等,A正确;B. 假设反应制取3 mol Cu(NO ),三种方法消耗的硝酸的物质的量
3 2
分别是8 mol、14 mol、6 mol,可见三种途径所消耗硝酸的物质的量大小关系为:②>①>③,B错误;C.
途径③的制备方法中硝酸中的N元素全部转化为硝酸铜,原子利用率最高,且没有污染环境的气体NO、
NO 等的产生,最符合“绿色化学”理念,C正确;D. 途径①中3 mol Cu作还原剂,被氧化;而参加反应
2
1
原创精品资源学科网独家享有版权,侵权必究!的硝酸,8 mol HNO 中只有2 mol被还原,所以被氧化的铜与被还原的硝酸的物质的量之比是3:2,D正
3
确;故合理选项是B。
3.(2023春·青海西宁·高三统考开学考试)氮是各种生物体生命活动中不可缺少的重要元素。自然界中的
氮循环为生物体提供了氮元素。下列有关氮元素说法不正确的是
A.铵态氮肥被植物吸收的过程属于氮的固定
B.雷雨发庄稼的起因是打雷时空气中 与 化合成NO
C.城市空气中的氮氧化物主要来源是燃油汽车产生的尾气
D.工业利用 和 合成 ,其中 的来源是空气
【答案】A
【解析】A.氮的固定是将游离态的氮,即氮单质,转化为化合态的过程,而铵态氮肥中氮元素本就以化
合态形式存在,不属于氮的固定,A项错误;B.氮气和氧气可以在放电的条件下生成一氧化氮,一氧化
氮与空气中氧气化合成二氧化氮,二氧化氮溶于雨水下落,最终以氮肥的形式被庄稼吸收,故称雷雨发庄
稼,B项正确;C.燃油汽车发动机内,空气中氮气与氧气在放电或高温条件下发生反应生成NO,C项正
确;D.工业制取气体需要考虑原料成本,空气中含有大量氮气且容易分离出来,故工业利用N 和H 合成
2 2
NH , 的来源是空气,D项正确;故选:A。
3
4.(2023·河北秦皇岛·昌黎一中校考模拟预测)液氨可以微弱的电离产生 和 ,NH 中的一个H原
3
子若被-NH 取代可形成NH(联氨),若被-OH取代可形成NH OH (羟胺)。NH 经过一定的转化可以形成
2 2 4 2 3
N、NO、NO 、NO(无色)、HNO 等。下列有关NH 、NH OH、 、 的说法正确的是
2 2 2 4 3 3 2
A.NH 的键角比 中的大 B.NH OH难溶于水
3 2
C. 的空间构型为直线形 D.含 的溶液都具有强氧化性
【答案】A
【解析】A.NH 、 的N原子都采用sp3杂化,NH 的N原子上有1对孤电子对,而 的N原子上有
3 3
2对孤电子对,孤电子对对成键电子对的排斥作用大于成键电子对之间的排斥作用,导致NH 的键角比
3
中的大,A正确;B.-OH是亲水基,NH OH与水分子之间容易形成氢键,增加了分子之间的吸引作
2
用,因此NH OH易溶于水,B错误;C. 中的中心N原子的价层电子对数是2+ =3,N原子
2
上含有1对孤电子对,因此 的空间构型是V形,C错误;D.在酸性溶液中,含 的溶液H+、
起HNO 的作用,表现强氧化性,而当溶液显中性或碱性时不具有强氧化性,D错误;故合理选项是A。
3
5.(2023·湖南衡阳·衡阳市八中校考三模)自然界中氮循环过程如图所示,下列说法错误的是A.反硝化过程中,含氮物质被还原
B.氨氧化过程中,NO 与NH 理论物质的量之比为1:1
C. 属于氮的固定,N 发生还原反应
2
D.土壤中Fe2+离子有利于除去水体中的铵态氮
【答案】D
【解析】A.反硝化过程中氮元素化合价降低,做氧化剂被还原,A正确;B. 中N元素为+3价,
中N元素为-3价,二者反应产物为N,化合价为0价,根据转移电子守恒可知,反应过程中二者的理
2
论物质的量之比为1:1,B正确;C.氮的固定是指游离态氮元素转化为化合态的氮元素,氮气转化为铵根,
氮元素化合价降低,做氧化剂被还原,C正确;D.由转化图可知,亚铁离子能与水体中的硝酸根反应,
可以除去水体中的硝态氮,D错误;故选D。
6.(2023·江苏南通·校考模拟预测)含氮物质可发生如下反应:①
②
③
下列说法正确的是
A.常温下,NO与 混合能立即看到红棕色气体,说明该反应已达平衡
B.反应②的
C.反应③消耗 ,理论上会生成标准状况下约
D.利用反应①、②、③可以同时处理 含量较高的废气和含 的废水
【答案】C
【解析】A.常温下,NO与 混合能立即看到红棕色气体,说明该反应生成了二氧化氮气体,但是不确
定是否平衡,故A错误;B.反应②为气体分子数减小的反应,为熵减反应,故B错误;C.由方程式可
知,反应③消耗 ,理论上会生成1mol氮气,在标准状况下约 ,故C正确;D.反应中
涉及氢氧化钠和氯化铵两种物质,两者会反应生成氨气和氯化钠,故不能利用反应①、②、③可以同时处
理 含量较高的废气和含 的废水,故D错误。故选C。
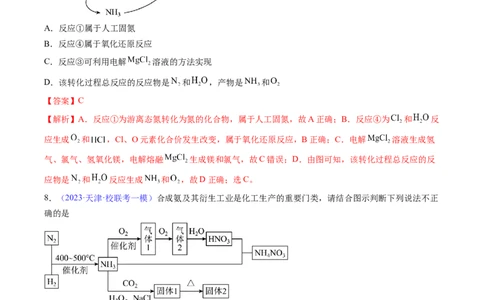
7.(2023秋·河南郑州·高三河南省实验中学校考开学考试)氨广泛应用于化工、化肥、制药等领域,一种新型制备氨的方法如图。下列说法错误的是
A.反应①属于人工固氮
B.反应④属于氧化还原反应
C.反应③可利用电解 溶液的方法实现
D.该转化过程总反应的反应物是 和 ,产物是 和
【答案】C
【解析】A.反应①为游离态氮转化为氮的化合物,属于人工固氮,故A正确;B.反应④为 和 反
应生成 和 ,Cl、O元素化合价发生改变,属于氧化还原反应,B正确;C.电解 溶液生成氢
气、氯气、氢氧化镁,电解熔融 生成镁和氯气,故C错误;D.由图可知,该转化过程总反应的反
应物是 和 反应生成 和 ,故D正确;选C。
8.(2023·天津·校联考一模)合成氨及其衍生工业是化工生产的重要门类,请结合图示判断下列说法不正
确的是
A.合成氨采用400~500℃是为了提高原料转化率和反应速率
B.湿润的淀粉KI试纸不可以鉴别气体2和溴蒸气
C.生成固体1的化学方程式为NaCl+NH +CO +H O=NaHCO ↓+NHCl
3 2 2 3 4
D.1L气体1、2的混合气与1 L NH 在一定条件下转化为对环境无害的物质,混合气中二者的体积比为
3
1∶1
【答案】A
【分析】由图可知:NH 在催化剂条件下与氧气反应生成气体1为NO气体,NO被氧化生成气体2为NO
3 2
气体,NO 气体与水反应生成硝酸,NH 与CO、HO、NaCl反应生成固体1为NaHCO ,NaHCO 受热分
2 3 2 2 3 3解生成固体2为NaCO,据此答题。
2 3
【解析】A.合成氨反应为放热反应,温度越低,反应越向着正向移动,原料的转化率越高,所以
400~500℃不利于提高原料的转化率,故A错误;B.由分析可知:气体2为NO 气体,NO 气体和溴蒸气
2 2
都有较强的氧化性,都能使淀粉碘化钾试纸变蓝,故B正确;C.固体1为碳酸氢钠,氯化钠、二氧化碳、
水和氨气可以生成碳酸氢钠固体,故方程式为:NaCl+NH +CO +H O=NaHCO ↓+NHCl,故C正确;D.
3 2 2 3 4
由分析可知:气体1为NO,气体2为NO ,1LNO、NO 的混合气与1LNH 在一定条件下转化为对环境无
2 2 3
害的物质,反应方程式为: ,NO、NO 的体积比等于化学计量数之比,为
2
1:1,故D正确;故选A。
考点二 氮及其化合物制备的工艺流程
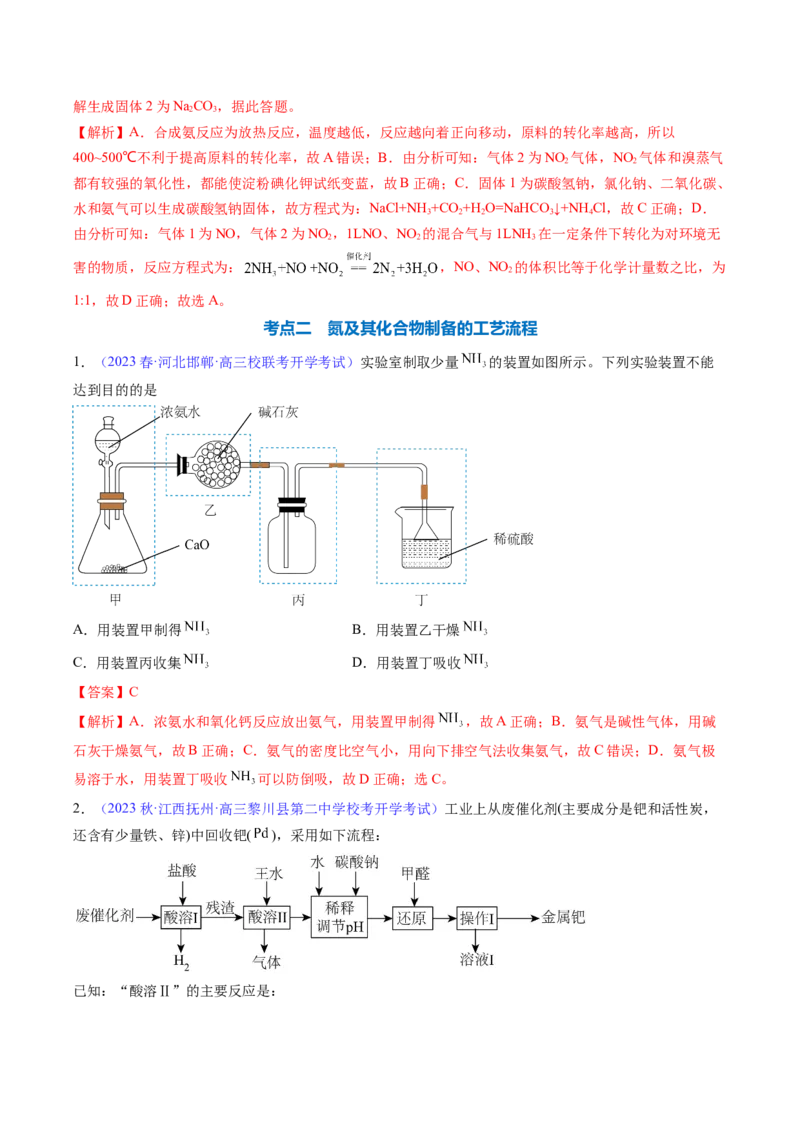
1.(2023春·河北邯郸·高三校联考开学考试)实验室制取少量 的装置如图所示。下列实验装置不能
达到目的的是
A.用装置甲制得 B.用装置乙干燥
C.用装置丙收集 D.用装置丁吸收
【答案】C
【解析】A.浓氨水和氧化钙反应放出氨气,用装置甲制得 ,故A正确;B.氨气是碱性气体,用碱
石灰干燥氨气,故B正确;C.氨气的密度比空气小,用向下排空气法收集氨气,故C错误;D.氨气极
易溶于水,用装置丁吸收 可以防倒吸,故D正确;选C。
2.(2023秋·江西抚州·高三黎川县第二中学校考开学考试)工业上从废催化剂(主要成分是钯和活性炭,
还含有少量铁、锌)中回收钯( ),采用如下流程:
已知:“酸溶Ⅱ”的主要反应是:.
下列说法错误的是
A.“酸溶Ⅰ”的目的是除去铁、锌等杂质
B.为加快酸溶速率,“酸溶Ⅱ”需要高温条件
C.调节 使溶液显碱性可以减少甲醛的损耗
D.溶液Ⅰ可能含有
【答案】B
【分析】废催化剂中主要成分是钯和活性炭,还含有少量铁和锌,先加入稀盐酸,铁和锌与稀盐酸反应生
成ZnCl、FeCl 和氢气,钯不与盐酸反应,过滤得到含有钯的固体,滤渣中加入王水,发生信息中的反应
2 2
生成NO和HPdCl ,HPdCl 的溶液中加水和碳酸钠稀释并调节pH至碱性,再加入甲醛将HPdCl 还原为
2 4 2 4 2 4
钯单质,甲醛被氧化为甲酸盐,最后经过过滤得到金属钯。
【解析】A.废催化剂中的少量铁、锌能与盐酸反应生成可溶性盐,酸溶Ⅰ的目的是除去铁、锌等杂质,
A正确;B.王水含有加热易分解和挥发的硝酸,且盐酸也易挥发,因此酸溶Ⅱ的温度不宜过高,B错误;
C.硝酸根离子在酸性条件下具有强氧化性,会氧化甲醛,碱性环境可以减少甲醛的损耗,C正确;D.甲
醛被氧化生成甲酸,在碱溶液中生成甲酸盐,D正确;故答案选B。
3.(2023·河北张家口·统考一模)氮化硅可用作耐高温、耐腐蚀材料。由石英(含少量铁、铜氧化物)和空
气制备氮化硅的一种工艺流程如图所示。
下列说法错误的是
A.“高温转化I”硅元素参与的反应中氧化剂与还原剂物质的量之比为1:2
B.“净化”可将空气依次通过NaOH溶液、热还原铁粉、浓HSO
2 4
C.“洗涤”时酸洗可选用稀硝酸
D.SiO 中的Si-O键能高于Si N 中Si-N键能
2 3 4
【答案】B
【解析】A.“高温转化I”二氧化硅与足量碳反应的化学方程式为 ,则氧化剂与
还原剂的物质的量之比为1:2,故A正确;B.“净化”需依次除去空气中的二氧化碳、水蒸气、氧气,
则可将空气依次通过NaOH溶液、浓 、热还原铁粉,故B错误;C.稀硝酸可溶解铁、铜,而不能
溶解耐腐蚀的氮化硅,故C正确;D. 和 均为共价晶体,成键原子半径越小,键长越短、键能
越大,O原子半径小于N原子,所以SiO 中的Si-O键能高于Si N 中Si-N键能,故D正确;选B。
2 3 4
4.(2023·全国·模拟预测)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的流程如图:下列说法错误的是
A.“氨分离器”中主要应用了氨气易液化的性质
B.工业上可用铁槽车储运浓硝酸
C.流程中的转化涉及复分解反应
D.为提高氮的利用率,尾气可循环进入“合成塔”
【答案】C
【分析】N、H 在合成塔中制取NH ,将生成的NH 液化分离后,N、H 循环使用;在氧化炉内,NH 催
2 2 3 3 2 2 3
化氧化为NO等,在吸收塔内,NO、O、HO反应生成硝酸。
2 2
【解析】A.N、H 在合成塔中制取NH ,“氨分离器”中,将生成的NH 液化分离后,N、H 循环使用,
2 2 3 3 2 2
所以主要应用了氨气易液化的性质,A正确;B.常温下,浓硝酸能使铁钝化,从而阻止铁与浓硝酸的继
续反应,所以工业上可用铁槽车储运浓硝酸,B正确;C.流程中的转化,涉及的反应有:N、H 合成氨
2 2
反应,NH 催化氧化生成NO的反应,NO、O、HO化合生成HNO 的反应,没有涉及复分解反应,C错
3 2 2 3
误;D.因为尾气中含有大量的N、H,依图中信息,为提高氮的利用率,尾气可循环进入“合成塔”,
2 2
D正确;故选C。
5.(2023·北京西城·北京四中校考模拟预测)某小组探究NH 的催化氧化,实验装置图如图。③中气体颜
3
色无明显变化,④中收集到红棕色气体,一段时间后,④中产生白烟。
下列分析不正确的是
A.若②中只加入NH Cl不可以实现上述现象
4
B.③、④中现象说明③中的反应是4NH +5O 4NO+6H O
3 2 2
C.④中白烟的主要成分是NH Cl
4
D.一段时间后,⑤中溶液可能变蓝
【答案】C
【分析】①中高锰酸钾受热制备氧气,装置②中氯化铵与强氧化钙共热反应制备氨气,装置③中氨气在催
化剂作用下与氧气发生催化氧化反应生成一氧化氮,装置④中反应生成的NO与过量的O 反应生成红棕色
2
气体NO ,NO 与水蒸气反应生成硝酸,硝酸与氨气反应生成硝酸铵,会有白烟产生,装置⑤中氮的氧化
2 2
物与氧气溶于水反应生成硝酸,硝酸与铜反应生成淡蓝色的硝酸铜溶液,据此回答。【解析】A.氯化铵受热分解生成氨气和氯化氢,两者在试管口又会化合生成氯化铵,A正确;B.由分析
可知,③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟说明③中氨气在催化剂作
用下与氧气发生催化氧化生成一氧化氮,反应方程式为:4NH +5O 4NO+6H O,B正确;C.由分
3 2 2
析可知,④中白烟的主要成分是硝酸铵,C错误;D.装置⑤中氮的氧化物与氧气溶于水反应生成硝酸,
硝酸与铜反应生成淡蓝色的硝酸铜溶液,D正确;故选C。
6.(2023·广东·模拟预测)绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含
废水和工业废气(主要含N、CO、SO 、NO、CO,不考虑其他成分),设计了如图流程:
2 2 2
下列说法不正确的是
A.固体1中主要含有CaCO 、CaSO、Ca(OH)
3 3 2
B.X可以是空气,但不能过量
C.捕获剂所捕获的气体主要是CO、N
2
D.处理含 废水时,发生的反应为: + =N ↑+2H O
2 2
【答案】C
【分析】工业废气(主要含N、CO、SO 、NO、CO不考虑其他成分)通过过量的石灰乳,二氧化碳和二氧
2 2 2
化硫被吸收,生成碳酸钙和亚硫酸钙,气体1是不能被过量石灰水吸收的N、NO、CO,气体1通入气体
2
X,用氢氧化钠溶液处理后到的NaNO ,X可为空气,但不能过量,否则得到硝酸钠,亚硝酸钠和铵根离
2
子的溶液反应生成无污染的气体,应为氮气,气体2有氮气和一氧化碳,捕获剂所捕获的气体主要是一氧
化碳,据此解答。
【解析】A.工业废气中CO、SO 可被石灰水吸收,生成CaCO 、CaSO,因氢氧化钙过量,则固体1为主
2 2 3 3
要含有Ca(OH) 、CaCO 、CaSO,故A正确;B.由分析可知,气体1是不能被过量石灰水吸收的N、
2 3 3 2
NO、CO,气体1通入气体X,用氢氧化钠溶液处理后得到NaNO ,X可为空气,但不能过量,否则得到
2
硝酸钠,故B正确;C.根据分析可知,气体2含有CO、N,经捕获剂得到氮气和CO,所捕获的气体主
2
要是CO,防止污染空气,故C错误;D.根据图示可知,氢氧化钠溶液处理后到的NaNO 与含有 的
2
溶液反应生成无污染气体,应生成氮气,发生反应的离子方程式为: + =N ↑+2H O,故D正确;
2 2
故答案为C。
7.(2023·辽宁沈阳·统考一模)明代《徐光启手迹》记载了制备王水的方法,其主要流程如图所示(水蒸
气等部分产物已省略),下列说法中正确的是A.X不能使酸性 溶液褪色 B.操作1的名称为蒸馏
C.流程中涉及的均为非氧化还原反应 D.步骤ⅱ能在铁容器中进行
【答案】B
【解析】A.由题意,Fe元素化合价升高,故部分硫元素化合价降低,X的化学式应为SO ,SO 具有还原
2 2
性能使酸性 溶液褪色,故A错误;B.操作1后得到硝酸,该过程中制取硝酸是利用了硝酸易挥发
的性质,则操作1的名称为蒸馏,故B正确;C.步骤i中煅烧绿矾生成SO 过程中,S、Fe的化合价发生
2
变化,属于氧化还原反应,故C错误;D.王水是浓硝酸和浓盐酸按体积比=1:3的混合物,会腐蚀铁容器,
步骤ⅱ不能在铁容器中进行,故D错误;故选B。
8.(2023·重庆万州·重庆市万州第二高级中学校考二模)汽车尾气中的氮氧化合物(NO )与大气中的
x
NH 发生如下作用,形成一种雾霾。
3
NO NO HNO 烟(一种雾霾)
x 2 5 3
有关该雾霾的叙述错误的是
A.该雾霾中含硝酸铵固体 B.反应②是非氧化还原反应
C.NH 是形成该雾霾的催化剂 D.NH 可能来自过度施用氮肥
3 3
【答案】C
【分析】由于工业生产中使用矿物作为燃料,大量向空气中排放污染物,加上汽车尾气的大量排放,以及
冬季取暖也向空气中排放粉尘,致使大量微小尘粒、烟粒或盐粒等颗粒悬浮在大气中,形成雾霾。
【解析】A.硝酸与氨气反应生成硝酸铵固体,故A正确;B.反应②是五氧化二氮与水反应生成硝酸,
反应中元素没有化合价变化,属于非氧化还原反应,故B正确;C.硝酸与氨气反应生成硝酸铵固体,氨
气是反应物,不是催化剂,故C错误;D.铵盐不稳定易分解产生氨气,则NH 可能来自过度施用氮肥,
3
故D正确;故选C。
考点三 氮及其化合物的有关计算
1.(2023·河南安阳·安阳一中校考模拟预测)下列四组混合气体中各组分的体积比为 ;
; ; 。将分别盛满上述各种气体的容积相等的四支
试管倒置于盛有水的水槽中,最后试管内液面由低到高的顺序为
A. B. C. D.
【答案】A
【解析】 发生反应: ,试管中 、 的体积比为 ,剩余 ,最终液
体充满试管容积的 ; 发生反应: ,试管中NO、 的体积比为 ,剩余NO,最终液体充满试管容积的 ; 易溶于水, 不易溶于水,试管中 、 的体积比为 ,
全部剩余,最终液体充满试管容积的 ; 发生反应: ,试管中 、
NO、 的体积比为 ,恰好完全反应,无气体剩余,最终液体充满试管。综上所述,最后试管内液面
由低到高的顺序为 ,选项A正确;答案选A。
2.(2023秋·湖南长沙·高三长沙市明德中学校考开学考试)某稀硫酸和稀硝酸的混合溶液 ,平均
分成两份。向其中一份中逐渐加入铜粉,最多能溶解 。向另一份中逐渐加入铁粉,产生气体的量随铁
粉质量增加的变化如图所示 已知硝酸只被还原为NO气体 。下列分析或结果错误的是
A.原混合酸中 的物质的量为
B.OA段产生的是NO,AB段发生的反应为 ,BC段产生氢气
C.第二份溶液中最终溶质为
D. 浓度为
【答案】A
【分析】由图象可知,由于铁过量,OA段发生反应为: ,AB段发生反
应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H ↑。
2
A、OA段发生反应为: ,硝酸全部起氧化剂作用,根据铁的物质的量结
合离子方程式计算;B、铁先与硝酸反应生成一氧化氮与铁离子,之后铁与铁离子反应生产亚铁离子,最
后是铁和硫酸反应;C、铁先与硝酸反应,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应,铁
单质全部转化为亚铁离子,硝酸全部起氧化剂作用,没有显酸性的硝酸;D、根据铁和硫酸的反应中铁的
质量来确定所需硫酸的量,进而确定硫酸的浓度。
【解析】A、根据题图可知,OA段发生的反应为: ,硝酸全部起氧化剂
作用,所以每份混合酸中 ,所以原混合酸中 的物质的量为 ,
A符合题意;B、OA段发生的反应为: ,产生NO,AB段发生的反应为
,BC段发生的反应为 ,产生氢气,B不符合题意;C、第二份溶液
中硝酸全部被还原,因为溶液中有 ,并且Fe全部转化为 ,所以最终溶液中溶质为 ,C不符合题意;D、反应最终消耗 ,其物质的量为 ,所有的铁都以硫酸亚铁的形式
存在于溶液中,根据 守恒可知,每份溶液中含硫酸 ,所以硫酸的浓度是 ,
D不符合题意;故答案为:A。
3.(2023秋·宁夏吴忠·高三吴忠中学校考开学考试)向27.2gCu和Cu O的混合物中加入某浓度的稀硝酸
2
0.5 L,固体物质完全反应,生成NO和Cu(NO )。在所得溶液中加入1.0 mol/L的NaOH溶液1.0 L,此时
3 2
溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g,下列说法不正确的是
A.Cu与Cu O的物质的量之比为1:2
2
B.硝酸的物质的量浓度为2.4 mol/L
C.产生的NO在标准状况下的体积为4.48 L
D.Cu、Cu O与硝酸反应后剩余HNO 的物质的量为0.2 mol
2 3
【答案】A
【分析】在所得溶液中加入1.0 mol/L的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀
质量为39.2g,则生成的Cu(OH) 质量为39.2g,n[Cu(OH) ]= =0.4mol,Cu2+消耗NaOH的物质的量
2 2
为0.8mol,则剩余HNO 的物质的量为1.0 mol/L×1.0 L-0.8mol=0.2mol。
3
27.2gCu和Cu O的混合物中,n(Cu) = 0.4mol,m(Cu) = 0.4mol×64g/mol=25.6g,m(O)= 27.2g-25.6g=1.6g,
2 总 总
n(O)= =0.1mol。
【解析】A.n(O)= 0.1mol,则 n(Cu O)=0.1mol,n(Cu)=0.4mol-0.2mol=0.2mol,所以Cu与Cu O的物质的
2 2
量之比为0.2:0.1=2:1,A不正确;B.n(Cu O)=0.1mol,n(Cu)=0.2mol,则表现出酸性的硝酸为0.8mol,表
2
现出氧化性的硝酸为 =0.2mol,剩余硝酸0.2mol,硝酸的物质的量浓度为 =2.4
mol/L,B正确;C.表现出氧化性的硝酸为0.2mol,则产生的NO为0.2mol,在标准状况下的体积为
0.2mol×22.4L/mol=4.48 L,C正确;D.由分析知,Cu、Cu O与硝酸反应后剩余HNO 的物质的量为0.2
2 3
mol,D正确;故选A。
4.(2023·校联考二模)有一稀硫酸和稀硝酸的混合酸,其中HSO 和HNO 的物质的量浓度分别是1
2 4 3
mol/L和0.5 mol/L,取10 mL此混合酸,向其中加入过量的铁粉,反应结束后产生标准状况下的气体的体
积是(设反应中HNO 被还原成NO)
3
A.0.168 L B.0.112 L C.0.672 L D.0.224 L
【答案】A
【解析】10 mL混合酸中含有:n(H+) = 0.01 L × 2 × 1 mol/L + 0.01 L × 0.5 mol/L = 0.025 mol,n(NO ) = 0.01
L × 0.5 mol/L = 0.005 mol,由于铁过量,先后发生的反应为:3 Fe + 2 NO + 8 H+ = 3 Fe2+ + 2 NO↑ + 4
HO,Fe + 2 H+ = Fe2+ + H ↑,则:
2 2,反应后剩余
n(H+)=0.025mol-0.02mol=0.005mol,则: 0.005mol H+~0.0025H↑,所以:n(NO)
2
+n(H )=0.005mol+0.0025mol=0.0075mol, V(NO)+V(H )=0.0075mol×22.4L/mol=0.168L;答案选A。
2 2